PASSAGGI DI STATO - Home - people.unica.it
Transcript of PASSAGGI DI STATO - Home - people.unica.it

LLSS
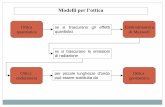
solidificazione
fusione ebollizione
condensazione
sublimazione
brinamento
VV
CaloreCaloreCaloreCalore
PASSAGGI DI STATOPASSAGGI DI STATOPASSAGGI DI STATOPASSAGGI DI STATOPASSAGGI DI STATOPASSAGGI DI STATOPASSAGGI DI STATOPASSAGGI DI STATO
Scrittura in formule:Scrittura in formule:Scrittura in formule:Scrittura in formule:
- HHHH2222O (s) O (s) O (s) O (s) →→→→ HHHH2222O (l) fusioneO (l) fusioneO (l) fusioneO (l) fusione- HHHH2222O (l) O (l) O (l) O (l) →→→→ HHHH2222O (g) evaporazioneO (g) evaporazioneO (g) evaporazioneO (g) evaporazione- HHHH2222O (s) O (s) O (s) O (s) →→→→ HHHH2222O (g) sublimazioneO (g) sublimazioneO (g) sublimazioneO (g) sublimazione

CaloreCaloreCaloreCaloreCaloreCaloreCaloreCalore nelle transizioni di fasenelle transizioni di fasenelle transizioni di fasenelle transizioni di fasenelle transizioni di fasenelle transizioni di fasenelle transizioni di fasenelle transizioni di fase
Una qualsiasi transizione di fase implica liberazione o assorbimento di energia sottoforma di calore.
In particolare è richiesto calore per:
- far fondere un solido (fusione)- far evaporare un liquido (evaporazione)- far evaporare un solido (sublimazione)
Ovvero questi processi fisici sono endotermici (∆H>0).
Al contrario i processi inversi sono esotermici (∆H<0) e producono la stessa quantità di calore.

CaloreCaloreCaloreCaloreCaloreCaloreCaloreCalore specificospecificospecificospecificospecificospecificospecificospecifico
Riscaldando una sostanza - sia essa solida, liquida o gassosa - il calore fornito provoca un aumento della temperatura.
La grandezza che collega il calore fornito e l’innalzamento della temperatura è il calore specifico C.
Esso rappresenta la quantità di calore necessaria per innalzare di un grado la temperatura di un grammo di sostanza.
L’unità di misura è: J/(g K)
Poiché il calore può essere scambiato a volume o pressione costante si distingue
cV = calore specifico a volume costantecP = calore specifico a pressione costante
( )ifP TTmcQ −=

P=1 P=1 P=1 P=1 atmatmatmatm
Calore fornito al sistema
S L00°°CC
L VL V100100°°CC
fusionefusione ebollizioneebollizione
HH22OO
TTTT
SOLIDO LIQUIDO VAPORE
∆Hfus ∆Hev

Durante la transizione di fase il calore fornito serve per separare le molecole e la temperatura rimane costante fino a che tutta la sostanza non è passata alla fase successiva.Il calore scambiato è relativo alle modificazioni delle forze intermolecolari.
Il calore fornito o ceduto durante il passaggio di fase si chiama calore latente molare.
Per esempio per l’evaporazione si parla di calore latente molare di evaporazione e si indica con
CaloreCaloreCaloreCaloreCaloreCaloreCaloreCalore latentelatentelatentelatentelatentelatentelatentelatente
∆Hev
Tem
pera
tura
(°C
)
tempo di riscaldamento (min)
Te (100°C a P=1 atm)
acqua
acqua + vapore
vapore

Tem
pera
tura
(°C
)
tempo di riscaldamento (min)
Tf (0°C a P=1 atm)
ghiaccio
ghiaccio + acqua
acqua
ghiaccio ghiaccio + acqua acqua

Esempio: stabilire la quantità di calore necessaria per portare 1 kg di acqua liquida da 25°C fino a 130°C.
1) Innalzamento di temperatura del liquido da 25 a100°C (calore sensibile):
kJCCCkg
kJkgTTmcQ OliqpH 5.313)25100(18.41)( 121 2
====°°°°−−−−°°°°°°°°
⋅⋅⋅⋅====−−−−====
2) Passaggio alla fase vapore a T=100°C costante (calore latente):
kJkgkJ
kgHmQ ev 2400240012 ====⋅⋅⋅⋅====∆∆∆∆====
3) Innalzamento di temperatura del vapore da 100 a130°C (calore sensibile):
kJCCCkg
kJkgTTmcQ OvappH 2.61)100130(04.21)( 123 2
====°°°°−−−−°°°°°°°°
⋅⋅⋅⋅====−−−−====
T (
°C)
Q kJ
acqua
acqua + vapore
vapo
re
25
100
130
Q1 Q2 Q3
Q = Q1+Q2+Q3=2774.7 kJ

TensioneTensioneTensioneTensioneTensioneTensioneTensioneTensione di vaporedi vaporedi vaporedi vaporedi vaporedi vaporedi vaporedi vapore
I liquidi ed alcuni solidi (quelli molecolari) subiscono un processo continuo di evaporazioneevaporazioneevaporazioneevaporazioneevaporazioneevaporazioneevaporazioneevaporazione.
Le molecola sono trattenute nel corpo del liquido da una forza netta di attrazione verso l’interno. Le molecole con maggiore energia cinetica possono però sfuggire dalla superfice.
Le particelle in superficie devono vincere forze di attrazione di minore entità rispetto a quelle presenti all’interno del liquido
Forze di coesione

Le molecole possono sia sfuggire dalla Le molecole possono sia sfuggire dalla Le molecole possono sia sfuggire dalla Le molecole possono sia sfuggire dalla superficesuperficesuperficesuperficedel liquido verso il vapore che del liquido verso il vapore che del liquido verso il vapore che del liquido verso il vapore che ricondensarericondensarericondensarericondensare dal dal dal dal vapore verso lavapore verso lavapore verso lavapore verso la superficesuperficesuperficesuperfice del liquido.del liquido.del liquido.del liquido.
Parte delle molecole del liquido –quelle con energia cinetica maggiore- tenderanno a sfuggire dalla superficie del liquido per cui nello spazio sovrastante il liquido si forma del vapore.
La pressione parziale del vapore sovrastante il liquido aumenta progressivamente e con essa aumenta il numero di molecole presenti in fase vapore La probabilità che molecole del vapore collidano con la superficie del liquido e ricondensino in fase liquida aumenta quando cresce il numero di particelle in fase vapore.

Quando la velocitQuando la velocitQuando la velocitQuando la velocitàààà di condensazione diventa uguale alla velocitdi condensazione diventa uguale alla velocitdi condensazione diventa uguale alla velocitdi condensazione diventa uguale alla velocitàààà di di di di evaporazione si raggiunge uno stato di equilibrio dinamico. evaporazione si raggiunge uno stato di equilibrio dinamico. evaporazione si raggiunge uno stato di equilibrio dinamico. evaporazione si raggiunge uno stato di equilibrio dinamico.
liquido vapore
La pressione parziale esercitata dal vapore in condizioni di equilibrio con il suo liquido è chiamata tensione di vaporetensione di vaporetensione di vaporetensione di vapore.
La tensione di vapore di una sostanza dipende dalla temperatura.La tensione di vapore di una sostanza dipende dalla temperatura.La tensione di vapore di una sostanza dipende dalla temperatura.La tensione di vapore di una sostanza dipende dalla temperatura.
Al crescere della temperatura aumenta l’energia cinetica molecolare e quindi la tendenza delle molecole a sfuggire dal liquido. La tensione di vapore aumenta all’aumentare della temperatura.

dGdG = = dQdQ -- PdVPdV + + PdVPdV + + VdPVdP –– TdSTdS -- SdTSdT
dGdG = = dQdQ -- VdPVdP –– TdSTdS -- SdTSdT
dGdG = = VdpVdp -- SdTSdT
Passaggi di fase Passaggi di fase Passaggi di fase Passaggi di fase Passaggi di fase Passaggi di fase Passaggi di fase Passaggi di fase
G=HG=H--TSTS
H=E+PVH=E+PVG=E+PVG=E+PV--TSTS
E=QE=Q--WWPrimo principioPrimo principio
G=QG=Q--W+PVW+PV--TSTS
G=QG=Q--W+PVW+PV--TSTS
� �
dQdQ==TdSTdSSecondo principioSecondo principio
� �

dGdG = = VdPVdP -- SdTSdT
Il passaggio di fase è un equilibrio, quindi per il generico passaggiodalla fase 1 alla 2 si ha:
Gf1=Gf2 � dGf1=dGf2
Vf1dP – Sf1dT = Vf2dP – Sf2dT
Riordinando i termini:
dP(Vf1 – Vf2) = dT(Sf1– Sf2)
VT
H
dTdP
T
HS
essendo
VS
VV
SS
dTdP
passaggio
passaggio
ff
ff
∆∆∆∆∆∆∆∆
====
∆∆∆∆====∆∆∆∆
∆∆∆∆∆∆∆∆====
−−−−−−−−
====21
12

VT
H
dTdP passaggio
∆∆∆∆∆∆∆∆
====
Per passaggio di fase liquido - vapore si avrà quindi:
)( liqvap
ev
VVTH
dTdP
−−−−∆∆∆∆====
Il volume delle fasi condensate (liquido e solido) è trascurabile rispettoal volume del vapore.
Per l’acqua per esempio:
SOLIDA V=20 cm3
Volume molare LIQUIDA V=18 cm3
T=25°C P=1 atm VAPORE V=22.41 dm3
vap
ev
TVH
dTdP ∆∆∆∆====

Per una mole di vapore possiamo sostituite Vvap utilizzando l’equazionedi stato dei gas perfetti:
vap
ev
TVH
dTdP ∆∆∆∆====
PRT
Vvap ====
2
2
variabili le separando
RTdTH
PdP
RTHP
dTdP
ev
ev
∆∆∆∆====
∆∆∆∆====
Integrando tra P1, T1 e P2, T2 si ha:
−−−−
∆∆∆∆−−−−====
∆∆∆∆==== ∫∫∫∫∫∫∫∫
212
1
2
11ln
2
1
2
1
TTRH
PP
RTdTH
PdP
ev
T
T
evP
P

−−−−
∆∆∆∆−−−−====
212
1 11ln
TTRH
PP ev
Equazione di Equazione di Equazione di Equazione di Equazione di Equazione di Equazione di Equazione di ClausiusClausiusClausiusClausiusClausiusClausiusClausiusClausius--------ClapeyronClapeyronClapeyronClapeyronClapeyronClapeyronClapeyronClapeyron
Indica come varia la pressione di vapore con la temperatura.

Quindi per il passaggio da una fase condensata al vapore si ha:
SOLIDO��VAPORE
LIQUIDO ��VAPORE CRTH
P ev ++++∆∆∆∆−−−−====ln
CRTH
P subl ++++∆∆∆∆−−−−====ln
Per il passaggio da solido – liquido, le variazioni di pressione rispetto alla temperatura sono date da:
SOLIDO��LIQUIDO
VT
H
dTdP fus
∆∆∆∆∆∆∆∆
====

Pv
P esterna
Pv
In un sistema chiuso, la pressionedi vapore è funzione esponenzialedella temperatura assoluta
In un sistema aperto, quando la pressione di vapore uguagliaquella esterna si ha ebollizione del liquido

LLLLLLLL’’’’’’’’ebollizioneebollizioneebollizioneebollizioneebollizioneebollizioneebollizioneebollizioneL’acqua bolle a 100°C perché, a tale temperatura, la tensione di vapore dell’acqua diventa pari a 1 atmosfera.
In questa situazione la pressione del vapore consente la formazione di bole di vapore all’interno del liquido che così comincia a bollire
Pressione atmosferica Pressione esercitata dalle molecole di vapore che urtano contro le pareti della bolla
Pressione dell’atmosfera verso l’interno

DIAGRAMMI DI FASEDIAGRAMMI DI FASEDIAGRAMMI DI FASEDIAGRAMMI DI FASEDIAGRAMMI DI FASEDIAGRAMMI DI FASEDIAGRAMMI DI FASEDIAGRAMMI DI FASE
SS
LL
VVP
T
O
a b
cc
4.58 mmHg
0.01°C
E’ un grafico pressione-temperatura in cui ogni punto del grafico rappresenta uno stato (fase o equilibrio di fase) in cui può trovarsi una sostanza. Esso fornisce le condizioni di temperatura e pressione alle quali una sostanza esiste come solido, liquido o gas, o come due o tre di queste fasi in equilibrio tra loro.
Curva a: FUSIONE ↔ SOLIDIFICAZIONE
VT
H
dTdP fus
∆∆∆∆∆∆∆∆
====
Curva b: EVAPORAZIONE ↔ CONDENSAZIONE
CRTH
P ev ++++∆∆∆∆−−−−====ln
CRTH
P subl ++++∆∆∆∆−−−−====ln
Curva c: SUBLIMAZIONE ↔ BRINAMENTO
Punto O: E’ il punto triplo, a cui corrispondo le condizioni di temperatura e pressione per cui coesistono le tre fasi in equilibrio

DIAGRAMMA DI FASE DELLDIAGRAMMA DI FASE DELLDIAGRAMMA DI FASE DELLDIAGRAMMA DI FASE DELLDIAGRAMMA DI FASE DELLDIAGRAMMA DI FASE DELLDIAGRAMMA DI FASE DELLDIAGRAMMA DI FASE DELL’’’’’’’’ACQUAACQUAACQUAACQUAACQUAACQUAACQUAACQUA
SS
LL
VVP
T
O
a b
cc
4.58 mmHg
0.01°C
La curva a rappresenta l’effetto della pressione sul punto di fusione della sostanza: essendo questo molto poco influenzato dalla pressione, la curva è quasi verticale. La sua pendenza è:
VT
H
dTdP fus
∆∆∆∆∆∆∆∆
====
Per l’acqua:∆V = Vliq – Vsol è negativo poiché il volume molare del ghiaccio è maggiore di quello del liquido. Quindi la retta di equilibrio solido – liquido ha pendenza negativa.

Il punto triplo della anidride carbonica si trova ad una pressione pari a 5.2 atm. Quindi a pressione atmosferica la CO2 solida sublima senza prima fondere (ghiaccio secco).
DIAGRAMMA DI FASE CODIAGRAMMA DI FASE CODIAGRAMMA DI FASE CODIAGRAMMA DI FASE CODIAGRAMMA DI FASE CODIAGRAMMA DI FASE CODIAGRAMMA DI FASE CODIAGRAMMA DI FASE CO22222222
Se il liquido è meno denso del solido (come accade in quasi tutti i casi) il punto di fusione aumenta al crescere della pressione (il solido fonde più facilmente a pressioni minori) e la curva solido-liquido ha pendenza positiva.

SS
LL
VV
0°C 100°C
P=1atmP=1atm
P<1atmP<1atmP
T
A
O
B
C
a b
a’ b’
ccP<4,58 mmHgP<4,58 mmHg
4.58 mmHg
0.01°C

SS
LL
VVP
T
O
a b
cc1
2
3
Punto 1 - BIVARIANTE: posso far variare in modo indipendente P e T senza alterare il sistema.
Punto 2 - MONOVARIANTE posso far variare in modo indipendente solo P o T senza alterare il sistema.Punto 3 – ZEROVARIANTE

Se si ripete la procedura con vapore acqueo a temperatura maggiore si ottiene una curva analoga alla recedente.
L’intervallo di volume tra il punto di vapore saturo e quello di liquido saturo è più piccolo.
Partendo dal punto A si ha il vapore.
Riducendo il volume in condizioni isoterme il vapore inizia a condensare (B-C).
Se si continua a comprimere il liquido, non si osserva una apprezzabile variazione di volume.
P (bar)
VAPORE
BC
LIQ
UID
O
Miscela isoterma di liquido e vapore
B’C’
V (dm3)
1
1 V (dm3)
1
1
T
DiagrammiDiagrammiDiagrammiDiagrammiDiagrammiDiagrammiDiagrammiDiagrammi PPPPPPPP--------V per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza pura

P (bar)
VAPORE
BC
Se si aumenta T, si raggiunge una temperatura critica (a cui corrisponde una isoterma critica) in cui la transizione di fase avviene per ben definiti volume, pressione e temperatura (punto critico).
LIQ
UID
O
Miscela isoterma di liquido e vapore
B’
C’ B”
C” B’’’
C”’
B’’’’C”’’Isoterma critica
punto critico
Tc
V (dm3)
1
1
DiagrammiDiagrammiDiagrammiDiagrammiDiagrammiDiagrammiDiagrammiDiagrammi PPPPPPPP--------V per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza puraV per una sostanza pura

T(°C)
V(m3)
P(bar)
punto triplo
T(°C)P(bar)
V(m3)
P(bar)
liquido
gas
solido
vapore