UNIVERSITA’ DEGLI STUDI DI PISASia nella gravidanza normale che nel GDM, la secrezione insulinica...
Transcript of UNIVERSITA’ DEGLI STUDI DI PISASia nella gravidanza normale che nel GDM, la secrezione insulinica...

UNIVERSITA’ DEGLI STUDI DI PISA
Facoltà di Medicina e Chirurgia
Scuola di Specializzazione in Endocrinologia e Malattie del Ricambio
ad Indirizzo Malattie del Ricambio e Diabetologia
Direttore: Prof. Stefano Del Prato
Tesi di Specializzazione
Espressione genica del tessuto adiposo
nella gravidanza fisiologica
Relatore: Candidata:
Chiar.mo Prof. Stefano Del Prato Dr.ssa Veronica Resi
Anno Accademico
2010/2011

1
Sommario
Indice............................................................................................................................. 1
Riassunto ....................................................................................................................... 3
Introduzione ................................................................................................................. 5
Fisiologia del Metabolismo in Gravidanza ....................................................................... 6
Metabolismo Glucidico .........................................................................................................6
Insulino Resistenza ............................................................................................................7
Significato Adattivo dell’Insulino Resistenza……………………………………………………………8
Secrezione Insulinica…………………………………………………………………………………..……..8
Ormoni associati alle variazioni di secrezione ed azione insulinica .................................. 12
Prima Fase di Gravidanza............................................................................................... 15
Fase Finale di Gravidanza .............................................................................................. 17
Impatto Sulla Concentrazione dei Nutrienti Materni ...................................................... 19
Metabolismo Lipidico .................................................................................................... 20
Metabolismo Proteico ................................................................................................... 22
La Composizione Materna Riflette i Cambiamenti Omeostatici ....................................... 24
Funzione Endocrina e Metabolica del Tessuto Adiposo .................................................. 25
Rimodellamento del Tessuto Adiposo ................................................................... 27
Lo Scopo dello Studio .................................................................................................... 28
Soggetti e Metodi .......................................................................................................... 29
Caratteristiche Metaboliche e Antropometriche ............................................................ 30
Analisi Biochimica ......................................................................................................... 31
Analisi del Tessuto Adiposo ........................................................................................... 32
Caratteristiche delle Cellule Adipocitarie ......................................................................... 32
Immunoistochimica ................................................................................................... 32
Espressione Proteica .......................................................................................... 33
Analisi Statistica ............................................................................................................ 34
Risultati ........................................................................................................................ 35
Cambiamenti Fenotipici e Metabolici Longitudinali ....................................................... 35
Caratteristiche Molecolari del Tessuto Adiposo ..................................................... 38

2
Discussione ................................................................................................................... 49
Espansione e Rimodellamento del Tessuto Adiposo…………………………………………………50
Espansione e Rimodellamento del Tessuto Adiposo……………………………………..52
Infiammazione…………………………………………………………………………………..…54
Conclusioni ................................................................................................................... 56
Bibliografia ................................................................................................................... 57
Ringraziamenti .............................................................................................................. 76

3
Riassunto
I cambiamenti endocrino-metabolici del tessuto adiposo sono fondamentali per gli
adattamenti dell’omeostasi energetica a cui va incontro l’intero organismo durante
tutta la gravidanza. Al fine di approfondire la conoscenza circa i meccanismi
molecolari che supportano il rimodellamento tissutale, abbiamo caratterizzato i
cambiamenti longitudinali del genoma del tessuto adiposo nella gravidanza
fisiologica. 11 donne sane normopeso sono state reclutate prima della gravidanza e
seguite longitudinalmente nel primo periodo (8^-12^ settimana) e nell’ultimo
periodo (36^-38^ settimana) di gravidanza. Sono state eseguite biopsie del tessuto
adiposo sottocutaneo in regione gluteale ad ogni punto dello studio. Il trascrittoma
adiposo è stato esaminato mediante l’analisi del DNA genoma con microarray.
L’espressione dei geni correlati al sistema immunitario e ai componenti della
matrice extra-cellulare è stata validata utilizzando l’analisi RT-PCR. La massa
adiposa, la dimensione e il numero degli adipociti incrementavano
significativamente nell’ultimo periodo di gravidanza rispetto ai valori prima della
gravidanza (p<0.001), mentre non si osservavano modifiche nel primo periodo di
gestazione. Il trascrittoma adiposo si modifica in gravidanza, con un 10-15% di geni
differentemente espressi rispetto al periodo pre-gravidanza. L’analisi funzionale
genica per gruppi ha rivelato che i cambiamenti molecolari nel primo periodo di
gravidanza interessano la risposta immunitaria, l’angiogenesi, il rimodellamento
della matrice e la sintesi lipidica. L’incrementata espressione dei marker macrofagici
(CD68, CD14 e il recettore del mannosio-6 fosfato) enfatizzano il reclutamento del
sistema immunitario sia nel primo che nell’ultimo periodo di gestazione. In
particolare, è attivata la via di segnale di TLR4-NFkB in relazione ai geni delle
adipochine infiammatorie e delle chemochine. Il precoce reclutamento della rete
molecolare del sistema immunitario e del metabolismo lipidico precede la comparsa
dei cambiamenti fisiologici relativi alla gravidanza del tessuto adiposo materno. Il
pattern bifasico suggerisce che l’infiammazione fisiologica è uno step precoce che

4
precede lo sviluppo dell’insulino-resistenza presente nell’ultimo periodo di
gravidanza.

5
Introduzione
La gravidanza umana è uno stato caratterizzato da numerose modifiche dell’
adiposità materna, gli adattamenti del metabolismo lipidico materno si modificano
per tutta la durata della gravidanza. Possiamo distinguere nella gravidanza
fisiologica, due momenti differenti, sia per quanto riguarda l’omeostasi metabolica
sia per quanto riguarda il rimodellamento del tessuto adiposo: il primo periodo di
gestazione e l’ultimo. Le due fasi metaboliche sono associate con adattamenti della
funzione delle cellule adipocitarie e con il rimodellamento dei tessuti, con
conseguente prevalenza di percorsi lipogenici nel primo periodo e percorsi lipolitici
nell’ultimo. L'accumulo di tessuto adiposo è il risultato di un equilibrio tra la sintesi
dei lipidi e la loro ripartizione. Conosciamo bene dalla letteratura che l’obesità
materna e il diabete gestazionale alterano gli aggiustamenti metabolici materni e
influenzano lo sviluppo placentare, embrionico e la crescita fetale. Sappiamo bene
che l’obesità materna pre-gravidica e il successivo sviluppo di diabete gestazionale
sono in continua espansione in tutto il mondo. Numerosi studi ci hanno permesso di
comprendere i meccanismi ormonali e le modifiche dell’omeostasi materna che
sottendono i cambiamenti a cui va incontro l’organismo materno nel corso della
gravidanza. Per meglio conoscere e trattare la gravidanza complicata da eccessivo
incremento ponderale o obesità è necessario comprendere i meccanismi
molecolari, ancora non noti, responsabili delle modifiche fenotipiche nel corso di
una gravidanza fisiologica. Comprendere i meccanismi molecolari ed endocrino-
metabolici nel corso della gravidanza fisiologica rappresenta il punto di partenza
imprescindibile per la comprensione, la gestione, il trattamento e il miglioramento
dell’outcome materno-fetale nella gravidanza patologica.

6
Fisiologia del Metabolismo in Gravidanza
La gravidanza è caratterizzata da un complesso rimaneggiamento endocrino-
metabolico finalizzato a garantire il necessario apporto di nutrienti al feto e
preparare adeguatamente l’organismo materno al parto e alla lattazione (1). Le
principali modifiche metaboliche che si osservano in gravidanza si possono
riassumere in una riduzione della sensibilità insulinica, un aumento della risposta -
cellulare, un modesto aumento delle glicemie, soprattutto post-prandiali, ed una
alterazione dei livelli circolanti di acidi grassi liberi, dei trigliceridi, del colesterolo e
dei fosfolipidi.
Metabolismo Glucidico
La condizione di insulino-resistenza che si instaura con il progredire della
gravidanza, più evidente a livello del tessuto muscolare e adiposo (2), è una
condizione fisiologica finalizzata alla crescita fetale. La minore utilizzazione del
glucosio insulino-mediata da parte dell’organismo materno, determina, infatti, una
maggiore utilizzazione dei substrati lipidici a fini energetici, e contemporaneamente
garantisce al feto un maggior apporto di carboidrati. Inoltre, la modesta ma più
prolungata iperglicemia postprandiale, che si sviluppa per effetto della minore
sensibilità insulinica, favorisce il flusso di nutrienti dalla madre al feto (3). Le basi
molecolari dell’insulino-resistenza periferica che si sviluppa in gravidanza,
interessano prevalentemente le tappe post-recettoriali con alterazioni
dell’attivazione del recettore insulinico e del trasporto e del metabolismo del
glucosio (4). Nella gravidanza normale la glicemia basale rimane pressoché costante
fino al terzo trimestre. Le variazioni della secrezione e dell’azione insulinica
dipendono dalle alterazioni endocrine che accompagnano la gravidanza.

7
Insulino-Resistenza
Nelle fasi iniziali della gravidanza la sensibilità insulinica sembra essere normale se
non addirittura aumentata (5). E’ con il suo progredire che si instaura una
condizione di insulino-resistenza, più spiccata a livello del tessuto muscolare che
adiposo. La riduzione della sensibilità insulinica è evento comune ed indipendente
dalla condizione di partenza. Catalano e coll. (6, 7)(Fig.1) utilizzando la tecnica del
clamp euglicemico-iperinsulinemico hanno stimato, nel terzo trimestre di
gestazione, una riduzione della sensibilità insulinica del 47% nelle donne obese e del
56% in quelle normopeso. Secondo altri studi, con il progredire della gravidanza, si
registra una riduzione della sensibilità insulinica fino al 60-80% (8)
Fig.1 The longitudinal changes in insulin sensitivity in normal glucose tolerant women as
estimated by the hyperinsulinemic euglycemic clamp. Early pregnancy 12-14 weeks and late
pregnancy 34-36 weeks; longitudinale changes over time, p=0.0001.(6)

8
La minore sensibilità insulinica che si instaura in gravidanza, sembra essere un
evento fisiologico che favorisce l’utilizzo di substrati di pronto impiego (carboidrati)
da parte del feto. La minore utilizzazione insulino-mediata di glucosio determina
infatti un prevalente impiego, ai fini energetici, di substrati lipidici (acidi grassi liberi)
da parte dei tessuti materni, risparmiando i carboidrati per il feto. La modesta ma
più prolungata iperglicemia post-prandiale che si sviluppa per effetto della minore
sensibilità insulinica favorisce il flusso di nutrienti dalla madre al feto (9, 10).
I determinanti cellulari dell’insulino-resistenza in gravidanza non sono noti. I
principali passaggi coinvolti nell’up-take insulino-dipendente di glucosio possono
essere compromessi nelle donne gravide. La riduzione della sensibilità insulinica
diventa ancor più evidente nelle donne con diabete gestazionale, sia magre che
obese. L’insulino-resistenza periferica che si instaura in corso di gravidanza è molto
simile a quella osservabile in soggetti con diabete Tipo 2. Come in quel caso, il
difetto di azione insulinica sembra coinvolgere più le tappe post-recettoriali con
alterazioni dell’attivazione del recettore insulinico e del trasporto e metabolismo
del glucosio nei tessuti insulino-sensibili. Lo studio del legame insulinico al proprio
recettore di membrana non ha dimostrato alterazioni significative sia nella
gravidanza normale che nel GDM (11, 12). Rispetto allo stato pregravidico, è stata
dimostrata invece una ridotta funzione (30-40%) dell’attività tirosino-chinasica del
recettore insulinico del muscolo scheletrico di donne obese, sia nella gravidanza
normale che in quella con GDM (13, 14).
Una riduzione dell’attività del substrato del recettore insulinico (IRS) è stata pure
segnalata. L’espressione di IRS-1 si riduce in animali da esperimento in gravidanza
(15) e la stessa osservazione è stata confermata a livello del muscolo scheletrico di
donne nelle ultime settimane di gravidanza, sia normo-tolleranti che con GDM (14).
La fosforilazione tirosinica di IRS-1 indotta dall’insulina risulta ridotta, rispetto allo
stato pregravidico, del 28% nella gravidanza normale e del 41% in quella con GDM.
Da segnalare, infine, che nelle fasi finali della gravidanza e in maggior misura in

9
quella complicata da GDM, si assiste ad una riduzione delle concentrazioni cellulari
del trasportatore insulino-dipendente del glucosio GLUT4 (16, 17).
E’ possibile che, oltre a variazioni intrinseche della funzione delle proteine della
cascata del segnale insulinico, altri fattori possano contribuire alla sua modulazione.
Recentemente è stato ipotizzato, sulla base di esperienze condotte in vitro (18), un
ruolo per le glicoproteine di differenziazione cellulare plasmatica come la PC-1 che
sono maggiormente espresse nel muscolo scheletrico di donne normo-tolleranti e
con GDM (13). La riduzione della sensibilità insulinica è risultata correlata ai livelli
del fattore di necrosi tumorale (TNF-). L’aumento di questa citochina, prodotta
dall’adipocita, è associato con un aumento della massa grassa materna (19).
Sebbene l’ormone lattogeno placentare (hPL) sia stato spesso citato come la causa
della ridotta sensibilità insulinica (20), a causa della sua produzione placentare e del
suo incremento con il progredire della gravidanza, più recentemente il ruolo delle
citochine infiammatorie e l’incremento dei livelli di acidi grassi liberi (FFA) è stato
correlato con i cambiamenti longitudinali nella sensibilità-insulinica nelle donne non
gravide (21) cosi come nelle donne in gravidanza (22). Il meccanismo cellulare
dell’insulino-resistenza in gravidanza è pertanto multifattoriale e coinvolge diverse
tappe della generazione e propagazione intracellulare del segnale insulinico .

10
Significato Adattivo dell’Insulino-Resistenza
I vantaggi adattivi dell’insulino-resistenza, dell’iperinsulinemia e della lieve
iperglicemia post-prandiale possono essere doppi. Primo, come suggerito da
Freinkel e coll. (23) , la modesta iperglicemia postprandiale serve ad aumentare la
durata del periodo in cui i livelli glicemici materni sono superiori ai livelli basali dopo
il pasto, aumentando quindi il flusso di nutrienti dalla madre al feto e favorendo
l’anabolismo fetale. Secondo, nella misura in cui l’insulino-resistenza nel muscolo
scheletrico è più spiccata rispetto a quella nel tessuto adiposo (24), la prima può
favorire il dirottamento di nutrienti ingeriti verso il tessuto adiposo, promuovendo
quindi anche l’anabolismo materno e l’immagazzinamento di energia durante
l’assunzione di cibo.
Secrezione Insulinica
Sia nella gravidanza normale che nel GDM, la secrezione insulinica aumenta
progressivamente dal primo trimestre fino a raggiungere la massima entità nel terzo
e tornare ai valori normali dopo il parto (25,26). La risposta insulinica dopo carico
orale di glucosio si associa ad un aumento del 120% della prima fase di secrezione
insulinica alla 12^-14^ settimana gestazionale. La seconda fase non sembra invece
essere particolarmente interessata, almeno nelle prime settimane di gravidanza. La
risposta insulinica ad un test di tolleranza al glucosio per via endovenosa (IVGTT)
(27) è aumentata rispetto ai valori precedenti (28) e successivi la gravidanza. I livelli
plasmatici a digiuno di proinsulina e dei suoi precursori sono aumentati nel corso
della gravidanza e ritornano ai valori normali nel post-partum. L’aumento della
proinsulina in gravidanza è certamente espressione di un blocco maturativo nel
processo di secrezione dell’insulina, secondario ad uno stress secretorio (29). Infatti
per soddisfare l’aumentata richiesta di insulina che si sviluppa in corso di
gravidanza, le isole di Langerhans vanno incontro a importanti cambiamenti

11
strutturali e funzionali caratterizzati da ipertrofia e iperplasia -cellulare (30)
(Tab.1).
Tab 1. Effetti della gravidanza sul metabolismo glucidico
Metabolismo glucidico
Glicemia
↓ Glicemia a digiuno ↑ Glicemie post prandiali
Secrezione insulinica
Dopo stimolo glucidico
1° fase
2° fase
↑ Gravidanza normale - ↑ Diabete gestazionale ↑↑ Gravidanza normale - ↑ Diabete gestazionale ↑↑ Gravidanza normale - ↑ Diabete gestazionale ↑ Gravidanza normale - ↑ Diabete gestazionale
Insulino-resistenza
Sede
Meccanismi cellulari
↑ Gravidanza normale - ↑↑ Diabete gestazionale Tessuto muscolare ↓ Attività tirosino-chinasica ↑ PC 1 ↑ IRS ↑ TNF alfa ↓ Glut 4

12
Ormoni associati alle variazioni di secrezione ed azione insulinica
Per quanto il meccanismo specifico delle variazioni di secrezione ed azione
insulinica rimanga incerto, è probabile che un contributo sostanziale sia fornito
dalle alterazioni endocrine che accompagnano la gravidanza. I cambiamenti della
funzione -cellulare avvengono in parallelo con lo sviluppo dell’unità feto-
placentare e la produzione locale di ormoni quali la somatotropina corionica umana
(HCS), il progesterone, il cortisolo, e la prolattina (Tab.2). Questi ormoni sono in
grado di indurre insulino-resistenza sia in vitro che in vivo. Nell’animale da
esperimento, inoltre, è stato ampiamente dimostrato come essi possano
influenzare la funzione delle -cellule e/o la sensibilità dei tessuti periferici
all’insulina.
Estrogeni e progesterone aumentano durante le fasi precoci della gravidanza e sono
implicati nelle alterazioni glicometaboliche materne. Sperimentalmente è stato
dimostrato che gli estrogeni aumentano la concentrazione ed il legame insulinico
(31), mentre il progesterone comporta una diminuzione della tolleranza glucidica
attraverso la diminuzione del trasporto del glucosio e del legame dell’insulina al suo
recettore. Inoltre il progesterone inibisce la soppressione insulinica della neo-
glucogenesi epatica (32). La concentrazione plasmatica di cortisolo aumenta in
gravidanza di circa il doppio rispetto allo stato non gravidico. Recenti osservazioni
hanno dimostrato che l’eccesso di glucocorticoidi induce insulino-resistenza a
livello post-recettoriale con una diminuita fosforilazione del recettore insulinico ed
una minore contenuto di IRS-1 (33). L’ormone lattogeno placentare svolge azioni
simili a quelle dell’ormone della crescita (GH) e, insieme al GH di origine placentare,
stimola la produzione di IGFs, modula il metabolismo intermedio e favorisce la
disponibilità di glucosio ed aminoacidi per il feto (34,35). Per la sua analogia con il
GH, l’hPL è stato a lungo considerato uno dei principali fattori responsabili
dell’insulino-resistenza tipica della gravidanza (31) e dell’aumento della glicemia.

13
Nella gravidanza complicata da diabete gestazionale, le alterazioni riscontrate a
carico dell’espressione dei geni della famiglia ormone della crescita/somatotropine
corioniche sarebbero responsabili dell’alterato rapporto nella produzione dei due
ormoni a favore dell’ormone della crescita (36). Dati recenti depongono per un
possibile effetto plastico sulla massa beta-cellulare esercitato dall’azione dei
lattogeni placentari (hPL, GH, PRL) (37). Studi in vivo ed in vitro hanno evidenziato
che l’hPL induce nelle isole di Langerhans gli stessi cambiamenti osservabili in
gravidanza. Questi cambiamenti sono rappresentati da un aumento della secrezione
glucosio stimolata dell’insulina e riduzione della soglia di stimolo glucidico (38,39),
un aumento della sintesi d’insulina (40), un aumento dell’utilizzo e dell’ossidazione
del glucosio (41, 42), ipertrofia ed iperplasia cellulare (43) ed un aumento del cAMP
intracellulare (44).La prolattina aumenta di 5-10 volte durante la gravidanza, ma il
suo ruolo nello sviluppo delle alterazioni metaboliche in gravidanza non è ancora
ben definito (45). La leptina, un prodotto del gene ob, è un ormone polipeptidico di
167 aminoacidi scoperto nel 1994 (46). E’ secreta dal tessuto adiposo ed agisce a
livello ipotalamico attraverso l’inibizione del fattore stimolante l’appetito
(neuropeptide Y) e l’aumento della termogenesi (47). Le concentrazioni di leptina
aumentano significativamente nel corso della gravidanza, raggiungendo un picco nel
secondo trimestre e restando elevate fino all’espletamento del parto. Le azioni
proprie della leptina sono difficilmente conciliabili con le finalità della gravidanza ed
è stato ipotizzato che la gravidanza possa rappresentare uno stato di leptino-
resistenza (48, 49). I livelli plasmatici circolanti di leptina correlano con l’insulinemia
e la massa adiposa materna e, come tali, possono essere considerati un indicatore
di insulino-resistenza ed obesità (50). Sul versante fetale, gli alti livelli di leptina
nella vena ombelicale suggeriscono che la placenta possa essere una delle maggiori
sedi di produzione di leptina fetale. Le sue concentrazioni sono correlate con il peso
alla nascita e con gli altri indici antropometrici fetali (51, 52). Gli studi disponibili
indicano che la leptina svolge un ruolo nella crescita fetale e può interferire con il
metabolismo glucidico materno, anche se i meccanismi di queste azioni non sono
ancora ben definiti.

14
Tab.2 Effetti degli ormoni della gravidanza sul metabolismo glucidico
ORMONI
AZIONE
ESTROGENI
↑ Concentrazione insulinica ↑ Legame insulina-recettore
PROGESTERONE
↓ Trasporto del glucosio ↓ Legame insulinico al recettore ↓ Soppressione insulinica della neoglucogenesi
CORTISOLO
↑ Insulino-resistenza per: _ ↓ Fosforilazione recettore insulinico _ ↓ IRS-1
LATTOGENI PLACENTARI
(hPL, GH, PRL)
↓ Sensibilità insulinica ↑ Sintesi insulinica ↓ Soglia di stimolo glucidico ↑ Secrezione insulinica ↑ Utilizzazione del glucosio ↑ cAMP intracellulare
↑ Proliferazione delle β-cellule ↑ Massa delle β-cellule
LEPTINA
↑ Insulino-resistenza (?)

15
Prima Fase di Gravidanza
Durante la prima fase di gravidanza, la tolleranza glucidica è normale o leggermente
aumentata e la sensibilità periferica (muscolo scheletrico) all’insulina e la
produzione epatica basale di glucosio sono normali (5-7). Con la tecnica del clamp
euglicemico-iperinsulinemico e mediante la tecnica dell’ IVGTT (Intravenous-
Glucose-Tolerance Test) è stato osservato che l’effetto di abbassamento della
glicemia indotto dalla somministrazione esogena di insulina, è più elevato del
normale nel primo trimestre di gravidanza rispetto al secondo e al terzo. Anche la
risposta insulinica al carico orale di glucosio è maggiore nel primo trimestre rispetto
a prima della gravidanza. Queste osservazioni sono consistenti con un 120% di
incremento alla 12^-14^ settimana di gestazione nella prima fase di secrezione
insulinica, riferendosi al cambiamento della concentrazione insulinica relativo
all’elevazione della concentrazione del glucosio da 0 a 5 minuti dopo la
somministrazione endovenosa di glucosio.
La seconda fase di secrezione insulinica, che si riferisce al tasso di rilascio insulinico
relativo all’aumento di concentrazione di glucosio da 5 a 60 minuti dopo la
somministrazione endovenosa di glucosio, non differisce significativamente nella
prima fase di gravidanza rispetto allo stato pregravidico. La causa dell’incrementata
sensibilità insulinica non è sicura perché la sensibilità insulinica periferica e la
produzione epatica di glucosio non differiscono rispetto ai valori pregravidici. Nel
primo trimestre inoltre, la glicemia basale e le concentrazioni insuliniche non
differiscono significativamente dai valori della non gravidanza (7).
La produzione epatica di glucosio, stimata utilizzando [6,6H2]glucosio non differisce
alla 12^-14^ settimana di gestazione rispetto allo stato pregravidico. Dopo un
iniziale decremento dei livelli di triacilglicerolo, acidi grassi liberi, colesterolo,
lipoproteine e fosfolipidi nelle prime 8 settimane di gestazione, si osserva un
incremento stazionario nella prima fase di gravidanza. Il colesterolo è utilizzato dalla
placenta per la sintesi degli steroidi e degli acidi grassi liberi e per la formazione

16
delle membrane. I cambiamenti nelle concentrazioni totali di colesterolo riflettono i
cambiamenti nelle varie frazioni lipoproteiche. Il colesterolo HDL incrementa a
partire dalla 12^settimana di gestazione in risposta agli estrogeni e rimane elevato
per tutta la gravidanza. Il colesterolo totale, il colesterolo LDL e le VLDL
diminuiscono nelle prime 8 settimane di gestazione per poi incrementare fino a
termine di gravidanza. I cambiamenti del metabolismo lipidico nel primo stadio di
gravidanza promuovono l’immagazzinamento del grasso materno. Nel primo
trimestre, l’incremento di estrogeni, progesterone e insulina favorisce l’accumulo
dei lipidi e inibisce la lipolisi.
L’attività di LPL (Lipoprotein-Lipasi) nel tessuto adiposo dalla regione femorale, ma
non dalla regione addominale, è elevata durante 8^-11^ settimana di gestazione.
Questo assetto metabolico sotto l’influenza di cortisolo, estrogeni e progesterone
favorisce la lipogenesi e l’accumulo di grasso (5).

17
Fase Finale di Gravidanza
Studi longitudinali sulla tolleranza glucidica in gravidanza mostrano un progressivo
incremento nella risposta insulinica indotta dai nutrienti a discapito di un minimo
peggioramento della tolleranza glucidica, consistente con una progressiva insulino-
resistenza (5-7).
La tecnica del clamp euglicemico-iperinsulinemico e l’IVGTT indicano che l’azione
insulinica nel periodo tardivo di gravidanza risulta di circa 50-70% più bassa rispetto
alle donne non gravide con normale tolleranza glucidica. Si osserva inoltre un
progressivo incremento delle concentrazioni insuliniche basali e postprandiali con
l’avanzare della gravidanza (8). La prima e la seconda fase di secrezione insulinica
sono dai 3- a 3.5- volte maggiori nell’ultimo trimestre di gravidanza (7).
Sebbene i meccanismi non siano ancora noti, le alterazioni dell’assetto metabolico
e ormonale materno sembrano responsabili della ridotta sensibilità insulinica. I
cambiamenti della risposta β-cellulare avvengono in parallelo con la crescita
dell’unità feto-placentare e la sua elaborazione del milieu ormonale. La prevalente
insulino-resistenza produce dei cambiamenti notevoli nelle concentrazioni
postprandiali dei nutrienti (es. glucosio, VLDL, aminoacidi).
L’insulino-resistenza serve ad indirizzare i nutrienti al feto. A partire dal terzo
trimestre la produzione epatica di glucosio incrementa del 16-30% per incontrare i
bisogni feto-placentari. Inoltre i cambiamenti epatici e il metabolismo adiposo
alterano le concentrazioni dei lipidi circolanti. Nella seconda metà di gravidanza, per
esempio, la clearance delle VLDL è alterata a causa della ridotta attività della LPL
nel tessuto adiposo e nel fegato e del suo aumento nella placenta. Nel terzo
trimestre di gravidanza l’ormone corionico umano promuove la lipolisi e la
mobilizzazione del tessuto adiposo. L’incremento degli acidi grassi liberi e del
glicerolo nel plasma sono correlati alla mobilizzazione nel tessuto adiposo.

18
Questo cambiamento da uno stato anabolico ad uno stato catabolico promuove
l’utilizzo dei lipidi come fonte di energia materna mentre preserva il glucosio e gli
aminoacidi per il feto. Con il digiuno prolungato (24h) si osserva una rapida
diversione del metabolismo materno verso l’ossidazione dei lipidi con l’elaborazione
dei chetoni. L’incrementata lipolisi e la chetogenesi permettono alle donne di
utilizzare i lipidi immagazzinati per sopperire ai bisogni energetici e minimizzare il
catabolismo proteico.

19
Impatto sulla concentrazione dei nutrienti materni
L’effetto integrato degli adattamenti metabolici materni descritti in precedenza si
riflette nell’andamento dei livelli circolanti di glucosio, di insulina e di trigliceridi, di
FFA e di aminoacidi durante la gravidanza. La gravidanza non si associa soltanto ad
alterazioni del metabolismo glucidico ma anche ad alterate concentrazioni di lipidi e
aminoacidi in circolo, come dimostrato da Phelps e coll. (53) (Fig.2)
Fig.2 Adapted from Phelps RL, Am J Obstet Gynecol 1981; 140:730–736). Profiles of plasma
glucose, insulin, free fatty acids (FFA), triglycerides, and two representative amino acids in
eight nonpregnant women (open symbols) and eight pregnant women with normal glucose
tolerance studied during the third trimester (closed symbols).
L’andamento delle concentrazioni di glucosio, di insulina e degli acidi grassi liberi
costituisce un’esagerazione delle normali oscillazioni tra l’anabolismo dello stato
alimentato e il catabolismo dello stato di digiuno osservabili in donne non gravide.

20
Metabolismo Lipidico
Le concentrazioni di trigliceridi nelle donne gravide aumentano di 1,5-2 volte nel
terzo trimestre rispetto alle donne non gravide. L’ipertrigliceridemia degli stadi
tardivi della gravidanza sembra derivare dalla combinazione di tre fattori (54): 1)
aumento degli FFA circolanti ed iperinsulinemia, che favoriscono la produzione di
trigliceridi da parte del fegato; 2) aumento dell’assunzione di cibo, cui consegue
un’aumentata produzione di cibo, cui consegue un’aumentata produzione di
chilomicroni da parte dell’intestino; 3) ridotta attività della lipoprotein-lipasi nel
tessuto adiposo, che determina una ridotta clearance dei trigliceridi dal circolo (55).
Il primo fattore è responsabile di buona parte dell’incremento dei trigliceridi a
digiuno osservabile nelle fasi tardive di gravidanza, mentre tutti e tre i fattori
probabilmente contribuiscono all’ipertrigliceridemia nello stato alimentato.
Sebbene esista un’ampia letteratura sui cambiamenti del metabolismo glucidico
durante la gestazione, i dati sulle alterazioni del metabolismo lipidico sono minimi
(56). Darmady e Postle (57) hanno misurato il colesterolo e i trigliceridi prima,
durante e dopo la gravidanza in 34 donne normali. Sia il colesterolo che il
triacilglicerolo diminuivano approssimativamente alla 7^settimana di gestazione e
progressivamente incrementavano fino alla fine. Il triacilglicerolo diminuiva nel
post-partum. Il decremento era più rapido nelle donne che allattavano al seno
rispetto alle altre. L’incremento degli acidi grassi liberi nell’ultimo periodo di
gestazione è stato ipotizzato essere correlato alla diminuzione della materna
insulino sensibilità presente nell’ultimo periodo di gestazione. Gli acidi grassi liberi
sono stati associati con un’eccessiva crescita fetale in particolare del tessuto
adiposo. Esiste una significativa differenza nella concentrazione artero-venosa degli
acidi grassi liberi alla nascita quanta ce n’è con la concentrazione arterovenosa di
glucosio. Knopp e coll. (58) hanno riportato che il peso alla nascita era direttamente
correlato con la concentrazione di triacilglicerolo e di acidi grassi liberi, i quali
direttamente attraversano la placenta nell’ultimo periodo di gestazione. Kleigman e
coll. (59) hanno riportato che i bambini di donne obese non soltanto avevano un

21
peso alla nascita incrementato ma anche un aumento degli acidi grassi liberi
rispetto ai neonati di madri normopeso. Studi effettuati utilizzando la metodica del
clamp euglicemico-iperinsulinemico in donne normo tolleranti (60) e in donne con
diabete gestazionale (61) hanno mostrato che esiste una ridotta capacità
dell’insulina di sopprimere gli acidi grassi liberi con il progredire della gravidanza. La
capacità di soppressione dell’insulina nelle donne con diabete gestazionale era
inferiore rispetto alle normotolleranti (61). Questi studi dimostrano che la
sensibilità insulinica ai nutrienti diminuisce in tutte le donne con l’avanzare della
gravidanza. Questo decremento della sensibilità insulinica è ulteriormente
accentuato dalla presenza di uno stato pregravidico di già ridotta insulino sensibilità
che si rende manifesto nel corso di gravidanza con lo sviluppo del diabete
gestazionale (56).

22
Metabolismo Proteico
Insieme al glucosio, che rappresenta la fonte primaria di energia per i tessuti
fetoplacentari, l’accumulo proteico è essenziale per la crescita fetale. Si stima che ci
sia un incremento di circa 500 gr nell’accumulo di proteine a partire dalla
30^settimana. Basata su una review di molti studi, Duggleby e Jackson (62) hanno
stimato che durante il primo trimestre di gravidanza la sintesi proteica è simile a
quella di donne non gravide, mentre aumenta di circa il 15% durante il secondo
trimestre e addirittura arriva al 25% di incremento nel terzo trimestre. Inoltre
esistono marcate differenze interindividuali in ogni periodo della gravidanza che
presentano una forte relazione con la crescita fetale. Gli aminoacidi possono essere
utilizzati anche per l’accumulo di proteine o ossidati come fonte di energia. In
generale nel primo periodo di gravidanza esiste un modesto cambiamento verso
l’ossidazione degli aminoacidi mentre nel terzo trimestre di gravidanza gli
aminoacidi vengono accumulati per la sintesi proteica. Studi preliminari di Catalano
e coll. (63) hanno riportato che in tutte le donne in gravidanza, la diminuzione della
sensibilità insulinica si manifesta mediante una ridotta soppressione del turnover
della leucina durante un’infusione di insulina nell’ultimo periodo di gravidanza.
Inoltre esiste un’evidenza di un incremento del turnover della leucina basale nelle
donne con diabete gestazionale rispetto al gruppo di controllo. Se questo
decremento nella sensibilità insulinica aminoacidica sia correlato alla sintesi epatica
proteica o ad un incrementato esaurimento non è ancora noto. Le concentrazioni di
aminoacidi circolanti sono ridotte nelle donne gravide rispetto alle non gravide.
L’andamento dei livelli di aminoacidi circolanti nel terzo trimestre rivela un
abbassamento delle concentrazioni postprandiali e a digiuno. I meccanismi che
possono contribuire all’ipoaminoacidemia postprandiale della gravidanza
comprendono un accelerato up-take materno di aminoacidi in risposta
all’iperinsulinemia postprandiale, alterazioni del volume di distribuzione degli
aminoacidi come risultato della ritenzione di liquidi in gravidanza, e un aumentato

23
utilizzo di aminoacidi da parte del feto durante le fasi tardive della gestazione (64).I
meccanismi alla base dell’ipoaminoacidemia in gravidanza non sono stati chiariti.

24
La composizione corporea materna riflette i cambiamenti omeostatici
La gravidanza è uno stato caratterizzato da modifiche dell’adiposità materna che
conducono ad un incremento del tessuto adiposo durante la prima fase di
gravidanza e seguito da un decremento della massa grassa nella fase tardiva di
gravidanza. (65) Queste due fasi metaboliche si associano agli adattamenti
funzionali delle cellule adipocitarie, risultando in una predominanza della via
lipogenica e lipolitica rispettivamente. La rete anabolica che caratterizza la prima
fase della gravidanza sembra essere guidata dall’insulina, comunque i meccanismi
che legano la relazione tra insulino-sensibilità e accumulo di tessuto adiposo rimane
ancora sconosciuta. L’accumulo di grasso è una delle caratteristiche più comuni
della gravidanza, si presenta sia nelle donne che negli animali. L’incremento dei
depositi di grasso avviene nel primo e secondo trimestre di gravidanza mentre
declina o addirittura si arresta nell’ultimo trimestre (66). L’accumulo di grasso
corporeo durante la prima fase si associa sia all’iperfagia che all’aumentata
lipogenesi. L’iperfagia incrementa con il progredire della gravidanza. Questo
progressivo incremento della disponibilità di substrati esogeni contribuisce
attivamente all’accumulo materno di depositi di grasso. L’incremento della sintesi
degli acidi grassi è stato scoperto in ratti gravidi quando studiati in vivo e questa
aumentata sintesi lipidica sembra contribuire attivamente all’accumulo di grasso
durante la gravidanza. Cosi come l’incremento dell’azione della LPL nel tessuto
adiposo possa contribuire all’accumulo di grasso nel primo trimestre della
gestazione, (67) la sua riduzione nel terzo trimestre contribuisce ad incrementare la
mobilizzazione del tessuto adiposo. La transizione da uno stato anabolico ad uno
catabolico nel metabolismo del tessuto adiposo materno coincide con la fase di
massima crescita fetale (65), quando cioè la madre ha bisogno di incrementare
progressivamente i supplementi per il feto. Durante il corso della gravidanza
avvengono modifiche estensive della composizione corporea materna. La massa

25
adiposa totale e il volume di sangue circolante incrementano significativamente
mentre la massa magra cambia di poco (68, 69). Il ruolo dinamico del tessuto
adiposo negli adattamenti metabolici materni in gravidanza è sottolineato dai
cambiamenti longitudinali nella massa del tessuto adiposo. C’è un range variabile
individuale nell’accumulo del tessuto adiposo che può raggiungere tra i 2 ai 10 Kg
per donna, sulla base dell’etnia, della razza e dei fattori nutrizionali e metabolici
(70,71). Nelle donne magre, l’incremento totale della massa grassa rappresenta
circa il 30% dell’incremento ponderale gestazionale (72), sebbene le donne con
obesità pre-gravidica solitamente acquistano meno peso rispetto alle donne magre
(73). Precedenti studi hanno mostrato che gravidanze non complicate con
appropriato incremento ponderale l’accumulo di grasso si manifesta durante il
secondo trimestre e rimane costante fino a termine di gravidanza (72,75). I
meccanismi sottostanti il rimaneggiamento precoce del tessuto adiposo devono
ancora essere definiti sia nella gravidanza normale che nelle gravidanze
metabolicamente compromesse.
Funzione Endocrina e Metabolica del Tessuto Adiposo
I cambiamenti della composizione corporea durante la gravidanza sono
principalmente guidati dagli adattamenti dell’omeostasi metabolica materna. Lo
scopo finale dei cambiamenti indotti dalla gravidanza è quello di incontrare la
richiesta energetica elevata dello sviluppo fetale. Il glucosio, la principale fonte di
energia usata dai tessuti fetali, deve essere reso disponibile per il trasferimento
transplacentare mentre i tessuti materni possono dipendere da altri substrati
energetici come i lipidi (75). Gli adattamenti del metabolismo lipidico seguono un
pattern bifasico ormai noto. La prima metà della gravidanza è focalizzata
sull’immagazzinamento dell’energia materna come trigliceridi del tessuto adiposo
mentre nell’ultimo periodo di gestazione i lipidi immagazzinati vengono mobilizzati
per essere utilizzati dai tessuti periferici e per preparare la lattazione (76). Questi

26
adattamenti sequenziali sono facilitati dalle modifiche nella secrezione e nell’azione
insulinica che avvengono durante il corso della gravidanza. Nel primo trimestre
l’incremento della sensibilità insulinica facilita l’anabolismo cellulare attraverso
l’attivazione della lipogenesi. Successivamente, l’insulino-resistenza si sviluppa
progressivamente fino a culminare nel terzo trimestre (77) e permettendo al
tessuto adiposo di mobilizzare i lipidi immagazzinati prima e al muscolo scheletrico
di utilizzare meno glucosio. Questi cambiamenti nell’omeostasi metabolica materna
si combinano per determinare un incremento dei livelli circolanti di insulina e
trigliceridi nell’ultimo periodo di gestazione (78). In aggiunta alle alterazioni nella
capacità di immagazzinare energia, anche la funzione endocrina del tessuto adiposo
evolve durante la gravidanza. La sintesi e la concentrazione plasmatica della leptina
e dell’adiponectina, le due principali adipochine, presentano cambiamenti
longitudinali paralleli a quelli dell’insulino sensibilità. Mentre le concentrazioni di
leptina incrementano durante il primo trimestre precocemente, si osserva una
diminuzione nell’adiponectina plasmatica durante il terzo trimestre (79,80). Le
modifiche longitudinali delle adipochine nella gravidanza fisiologica sono
ulteriormente accentuate nel contesto di una gravidanza complicata da obesità e
diabete (81,82).

27
Rimodellamento del Tessuto Adiposo
Il tessuto adiposo bianco presenta una notevole flessibilità caratterizzata da
un’importante e reversibile capacità di espansione durante la vita adulta.
Il rimodellamento della massa del tessuto adiposo richiede l’interazione di
meccanismi cellulari al fine di supportare l’incremento della misura e/o del numero
degli adipociti che lo compongono. Il turn over delle cellule del tessuto adiposo è
altamente sensibile alle variazioni dell’assetto metabolico e ormonale che
avvengono nel corso della vita, come per esempio lo sviluppo, l’invecchiamento, la
dieta o i disordini metabolici che si verificano durante la durata della vita (83-85).
Negli individui obesi, l’allargamento del tessuto adiposo richiede un attivo turn over
degli adipociti in presenza di uno stato di infiammazione cronica stimolata
dall’accumulo di macrofagi nel compartimento stromale vascolare (86,87). Come
già precedentemente mostrato in altri studi, l’infiltrazione macrofagica e
l’incrementata morte cellulare degli adipociti contribuiscono all’infiammazione nelle
donne in gravidanza con obesità pre-gravidica (88,89).

28
Lo scopo dello studio
La comprensione dei fattori e dei meccanismi che guidano il rimodellamento del
tessuto adiposo e delle modifiche endocrine in condizioni fisiologiche merita
ulteriori studi.
Lo scopo dello studio è stato quello di caratterizzare i meccanismi responsabili
dell’incremento della massa del tessuto adiposo durante una normale gravidanza.
Abbiamo condotto un’analisi longitudinale che iniziava prima e proseguiva
attraverso tutta la gravidanza, al fine di caratterizzare i tratti morfologici e
molecolari del tessuto adiposo in donne non obese. Abbiamo mostrato che i
cambiamenti molecolari che supportano il rimodellamento del tessuto adiposo
gluteale precedono i cambiamenti fenotipici nell’incremento del tessuto adiposo e
nel metabolismo lipidico che culminano nell’ultimo periodo di gestazione.

29
Soggetti e Metodi
Questo studio longitudinale è stato condotto presso il Dipartimento di Ginecologia e
Ostetricia (Ob/Gyn) del MetroHealth Medical Center, Case Western University di
Cleveland (Ohio).
Undici donne primipare sono state reclutate prima della gravidanza (P) e seguite
longitudinalmente sia nel primo trimestre di gravidanza (8-12 settimane di
gestazione) (early) (E) che nel terzo trimestre di gravidanza (36-38 settimane di
gestazione) (late) (L). Il protocollo di studio è stato approvato da Institutional
Review Board and Clinical Research Unit (CRU) Scientific Review Committee. Le
pazienti volontarie hanno firmato il Consenso Informato in accordo con le linee
guida per la protezione e privacy dei pazienti del MetroHealth Medical Center,
Cleveland, Ohio.

30
Caratteristiche Metaboliche e Antropometriche
La composizione corporea è stata valutata utilizzando l’idro-densitometria come
descritto da Catalano e coll. (90,91) nei punti dello studio P (pre-gravidanza) e E (I^
trimestre). Al punto L (III^ trimestre) il grasso corporeo è stato valutato aggiustando
per la densità della massa magra a causa dell'incremento dell’acqua corporea
totale nell’ultimo periodo di gestazione. Inoltre sono state eseguite misurazioni per
la plicometria cutanea.
Ad ogni punto dello studio le donne sono state sottoposte a clamp euglicemico-
iperinsulinemico (6). La produzione endogena di glucosio (principalmente epatica) è
stata stimata dopo un digiuno notturno di 11 ore utilizzando un’infusione costante
di glucosio marcato, [6,6-2H2] glucosio. Il turnover basale del glucosio è stato
stimato in accordo con l’equazione dello steady-state di Steele (92). La sensibilità
insulinica è stata stimata come il tasso di infusione di glucosio necessario per
mantenere l’euglicemia durante il clamp più ogni residua produzione endogena di
glucosio durante l’infusione di insulina. Il clamp euglicemico-iperinsulinemico a 2
ore è stato eseguito dopo la stima della produzione endogena epatica di glucosio
come descritto da De Fronzo e coll (93) per stimare la sensibilità insulinica
periferica. La produzione endogena di glucosio residua durante l’infusione di
insulina è stata stimata mantenendo costante l’infusione di glucosio marcato e
aggiungendo l’isotopo addizionale al 20% dell’infusione di glucosio come descritta
da Tserng e Kalhan (94). L’indice di sensibilità insulinica (ISI) è stato misurato
dividendo la sensibilità insulinica per la media di concentrazione insulinica raggiunta
durante il clamp.

31
Analisi Biochimica
Il plasma è stato separato mediante centrifugazione e congelato a -20°C fino
all’analisi. La glicemia è stata misurata mediante il metodo della glucosio ossidasi
(YSI, Yellow Springs,OH). L’insulina plasmatica è stata misurata utilizzando il kit
radio-immunologico per l’insulina umana (Linco Research, St.Charles, MO). Il limite
di sensibilità per il dosaggio dell’Insulina è di 0.2 µU/ml con un coefficiente di
variabilità (CV) del 4.4-6.8%. La leptina e l’adiponectina sono state misurate
utilizzando il kit ELISA (R&D Systems, Minneapolis, MN) con CV di 3.0-6.2% e 6.2-
8.4% rispettivamente. L’Interleukina-6 e l’Interleukina-8 sono state dosate mediante
la tecnica ELISA (QuantiGlo; R&D Systems, Minneapolis, MN) con CV di 5.3-7.8% e
2.6-3.4% rispettivamente. Tutti i campioni di plasma sono stati analizzati in
duplicato.

32
Analisi del Tessuto Adiposo
Caratteristiche delle Cellule Adipocitarie
Le biopsie del tessuto adiposo (800-1200 mg) sono state ottenute per ogni donna
mediante liposuzione dei depositi di tessuto adiposo sottocutaneo nella regione
gluteale. I prelievi bioptici sono stati effettuati per ogni punto dello studio: Prima
della Gravidanza (P), nel I^Trimestre (E) e nel III^ Trimestre di Gravidanza (L). Un
frammento di tessuto è stato fissato immediatamente per l’immunoistochimica, un
frammento è stato stoccato nel nitrogeno liquido per l’elaborazione del RNA e il
rimanente tessuto è stato processato per la digestione con collagenase. Dopo la
digestione con 1 mg/ml di collagenase (Worthington Biochemical, Lakewood, NJ), e
aver mantenuto il tessuto per 45’ a 37°C, la mistura è stata filtrata attraverso una
rete di garza di 100 µm. L’infranatante è stato rimosso e lo strato fluttuante degli
adipociti è stato portato a 10 ml per il conteggio e la misurazione delle dimensioni. Il
diametro degli adipociti è stato determinato utilizzando un W.F obiettivo 10x con
un righello (microcopio Olympus BH-2,Hiroshima,Japan). E’ stata eseguita una
media dei numeri da 10 campi e la cellularità è stata definita come il numero degli
adipociti per grammi di tessuto adiposo digerito (95).
Immunoistochimica
Le sezioni di tessuto adiposo erano state fissate in formalina al 10% e incluse in
paraffina. Le sezioni di 5 µm sono state colorate utilizzando l’ematossilina Gill II e
l’eosina (Sigma Aldrich). Le immagini digitalizzate sono state ottenute utilizzando
una Nikon E600 microscopio equipaggiata con una camera DXM200.

33
L’Espressione Proteica
I lisati degli adipociti sono stati preparati utilizzando il metodo di estrazione con
Trizol (Invitrogen, Carlsbad, CA). L’espressione genica è stata analizzata mediante
l’analisi del genoma con microarray utilizzando il metodo Affymetrix U133 e la
piattaforma come descritto (96). La selezione dei trascritti significativamente
modificati è stata eseguita mediante un sistema di filtri multi-step .
Tra i geni che sono stati evidenziati come “presenti” ovvero espressi, in accordo
con l’algoritmo MAS 5.0, noi abbiamo selezionato i geni che avevano una differenza
di almeno 4.5 volte la deviazione standard. L’intensità di ibridazione dei geni
significativamente modificati è stata esaminata mediante l’analisi gerarchica dei
gruppi con il software Gene-Spring GX (Agilent Technologies, Inc, Sanata Clara,CA) e
del software Treeview (free). I geni che soddisfacevano questi criteri sono stati
selezionati sulla base di un fold change >1.52 e <-1.52 che fosse coerente in almeno
due confronti. I geni relativi al metabolismo energetico sono stati identificati

34
secondo la funzione delle proteine putative codificate prese da un pubblico
database (IPA, Ingenuity System, Redwood,CA). I cambiamenti nell’espressione
genica sono stati validati dalla real-time PCR (Roche thermocycler, RocheApplied
Science, Indianapolis, IN) con LightCycler FAstStart DNA Sybr Green 1 master mix e
primer da Integrated DNA Technoologies (Coralville,IA). I primer per le specifiche
sequenze target sono state disegnate sulle regione 3’ codificante dei geni.
Analisi Statistica
Tutti i valori sono presentati come medie +/- SEM. Le differenze tra le variabili
dipendenti sono state esaminate con l’analisi della varianza a una via o a due vie
(ANOVA). Le differenze significative medie tra i tre punti dello studio sono state
identificate con il test posthoc di Fisher’s PLSD. I dati sono stati analizzati usando il
sistema statistico StatView II (Abacus Concepts, Berkeley, CA). La significatività
statistica è stata valutata per valori di p<0.05.

35
RISULTATI
Cambiamenti Fenotipici e Metabolici Longitudinali
Le misurazioni longitudinali sono state eseguite prima della gravidanza (Pre) e poi
nel primo periodo (8^-12^ settimana di gestazione) (Early) e nell’ultimo periodo
(36^-38^ settimana) (Late).
Tab.3 Caratteristiche antropometriche e metaboliche dei soggetti in esame. Esiste
una significativa differenza statistica tra P-Pregnancy e Late Pregnancy: * p=0.0001;
^ p=0.01. Esiste una differenza significativa tra Pre-pregnancy e Early-Pregnancy
^P=0.01
Le donne in esame erano tutte normopeso e con una normale tolleranza glucidica
prima della gravidanza. Presentavano tutte un sovrapponibile incremento
ponderale nel corso di gravidanza.
Pre Pregnancy
Early Pregnancy
Late Pregnancy
Weight, (Kg) 62.8 ± 13.08 64.9 ± 13.1 77.3 ± 14.5*
BMI, (Kg/m2) 22.7 ± 4.4 23.2 ± 4.2 27.7 ± 4.7*
Body fat, (%) 25.6 ± 8.2 26.3 ± 7.3 27.1 ± 6.6
LBM, (Kg) 45.9 ± 5.2 47.05 ± 5.6 55.5 ± 6.5*
Cholesterol (mg/dl) 151 ± 22.6 162.5 ± 32.7 242.09 ± 35.9*
FFA basal (mmol/ml) 0.66 ± 0.22 0.52 ± 0.19^ 0.51 ± 0.11^
Fasting Insulin (uU/ml) 12.1 ± 3.8 9.9 ± 3.2 15.4± 6.3
ISI (mg.min-1.Kg-1) 9.80 ± 2.5 9.25 ± 1.9 6.2 ± 1.9 *
Leptin Basal (ng/ml) 12.2 ± 9.08 20.7 ± 15.5^ 25.3 ± 16.1*

36
Sia la concentrazione del colesterolo e dei trigliceridi erano incrementate
nell’ultimo periodo di gravidanza mentre gli acidi grassi liberi (FFA) erano diminuiti
rispetto al periodo prima della gravidanza. L’insulino-sensibilità risultava
significativamente ridotta nell’ultimo trimestre di gravidanza rispetto sia al primo
trimestre che al periodo prima della gravidanza. Le concentrazioni di leptina
aumentavano significativamente nel primo trimestre e rimanevano elevate fino
all’ultimo trimestre.
Le misurazioni della composizione corporea mostravano che la massa grassa
corporea totale incrementava nell’ultimo periodo di gravidanza (p<0.0001) (Fig.3A).
Fig.3A Cambiamenti morfologici nel tessuto adiposo in gravidanza. Massa adiposa
totale (fat mass), dimensione degli adipociti (adipocyte size) e numero degli adipociti
(cellularity) prima e durante la gravidanza fisiologica. Pre-P: prima della gravidanza.
Early-E: 8^-12ˆsettimana di gestazione. Late-L: 32^-36^ settimana di gestazione.
Significatività statistica:* p<0.0001 vs pre-gravidanza. I risultati sono mostrati come
medie ± SD di 11 donne
*

37
Correlatamente, abbiamo osservato un incremento nel numero degli adipociti e
nelle loro dimensioni nell’ultimo periodo di gravidanza rispetto a prima della
gravidanza mentre questi cambiamenti non si sono osservati nel primo periodo
(p<0.001) (Fig.3B).
Fig.3B Sezioni di Immunoistochimica del tessuto adiposo sottocutaneo gluteale.
Ingrandimento iniziale X20. Pre-P: prima della gravidanza. Early-E: 8^-12ˆsettimana
di gestazione. Late-L: 32^-36^ settimana di gestazione

38
Caratteristiche Molecolari del Tessuto Adiposo
Utilizzando l’analisi microarray dell’intero genoma abbiamo analizzato n=22.277
geni e abbiamo osservato che il trascrittoma del tessuto adiposo, che comprendeva
12897±417 geni, rimaneva quantitativamente stabile durante la gravidanza con
13510±197 geni espressi durante la prima fase di gravidanza e 13097±298 geni
espressi durante l’ultimo periodo di gravidanza. L’Analisi dei Componenti Principali
(PCA) ha rivelato una sovrapposizione di grandi dimensioni nel pattern di
espressione tra il periodo prima della gravidanza (P), il primo trimestre (E) e l’ultimo
periodo (L) (Fig.4A).
Fig.4A Grafico tridimensionale a dispersione dell’analisi dei componenti principali
(PCA) del trascrittoma del tessuto adiposo. Le biopsie del tessuto adiposo gluteale
sono ottenute longitudinalmente Pre-gravidanza (P), nel primo trimestre (E) e nel
terzo trimestre (L). L’analisi dei dati completi (n=22.277 geni) mostrava una larga
sovrapposizione dei profili del trascrittoma prima e durante la gravidanza.

39
I geni differentemente espressi nel primo trimestre (n=1286) e nel terzo trimestre
(n=1111) di gravidanza rappresentano il 10-15% del transcrittoma del tessuto
adiposo rispettivamente. Il confronto dell’espressione genica globale, utilizzando
l’analisi delle componenti principali, ha inoltre rivelato un distinto pattern di
espressione genica tra il primo periodo di gravidanza e l’ultimo periodo (Fig.4B).
Fig.4B L’analisi dei geni significativamente modificati nel primo (n=1286 geni) e
nell’ultimo trimestre di gravidanza (n=1111 geni) rispetto a prima della gravidanza
mostravano un distinto pattern di espressione per ogni stadio della gravidanza. Ogni
punto rappresenta un set dati del microarray.

40
Ulteriori analisi sono state effettuate sui geni significativamente modificati, basate
sulla loro funzione biologica indicando che il 65% dei cambiamenti associati alla
gravidanza erano correlati al metabolismo lipidico (26%) e al rimodellamento
tissutale (39%) (Fig.5).
Fig.5. I cambiamenti trascrizionali nel tessuto adiposo durante la gravidanza.
L’analisi funzionale dei geni basate sulle annotazioni biologiche della loro sequenza
DNA., la cui espressione è modificata durante la gravidanza rispetto a prima della
gravidanza.

41

42
[GSE37215 approvato -NCBI tracking system #16555203]
Tab.4 I geni significativamente modificati nel tessuto adiposo nella prima fase di
gestazione sono espressi in “fold change” rispetto al periodo pre-gravidanza.

43

44
Tab.5 I geni significativamente modificati nel tessuto adiposo nell’ultima fase di
gestazione sono espressi in “fold change” rispetto al periodo pre-gravidanza.

45
I geni coinvolti nel rimodellamento tissutale sono stati poi ulteriormente separati in
tre categorie funzionali principali: i mediatori della risposta immunitaria, i
componenti della matrice extra-cellulare e i fattori angiogenici (Fig.6).
Fig.6 L’analisi per cluster ha identificato 3 principali gruppi funzionali di geni up-
regolati in gravidanza rispetto a prima della gravidanza. I geni implicati nel
metabolismo, nel rimodellamento cellulare-angiogenesi e nell’attivazione
immunitaria.

46
I cambiamenti significativi nei geni che regolano le vie per la risposta infiammatoria
e per le vie del metabolismo energetico sono stati osservati nel primo periodo di
gravidanza rispetto a prima della gravidanza.
La risposta del sistema immunitario innato attivata attraverso la via di segnale del
TLR4-NFkB conduce ad un rapido incremento nell’espressione genica e proteica di
TLR4 così come di TNF-alpha,IL-6, e delle piccole chemochine della famiglia CXCL
(Fig.7 A,B).
Fig.7A Cambiamenti trascrizionali relativi alla gravidanza nel tessuto adiposo-TLR4
network. Geni implicati nella via di segnale del TLR4 selezionati dalla lista in Tab.4.
I valori di mRNA dal tessuto adiposo sono stati misurati con l’analisi quantitativa
Real Time PCR nel primo periodo di gravidanza (E). I valori di controllo (Ct) sono stati
normalizzati per actina e espressi come fold change vs prima della gravidanza.
Significatività statistica: *p<0.05; prima della gravidanza: barre grigie, primo
trimestre (E): barre blu, con n=6 determinazioni indipendenti.

47
Fig.7B Analisi longitudinale immuno-enizimatica della proteina TLR4 contenuta nel
tessuto adiposo prima della gravidanza (P), nel primo trimestre (E) e nell’ultimo
periodo di gestazione (L).
Riguardo i geni implicati nella via metabolica, quelli coinvolti nel facilitare
l’accumulo dei lipidi attraverso la differenziazione adipocitaria e la lipogenesi erano
i più attivati nel primo trimestre di gravidanza (Fig. 8 A,B).
Fig.8 Cambiamenti trascrizionali correlati alla gravidanza nelle vie metaboliche del
tessuto adiposo. Geni coinvolti nella via metabolica selezionati da Tab.5. I valori di
mRNA dal tessuto adiposo sono stati misurati con l’analisi quantitativa Real Time

48
PCR nel primo periodo di gravidanza (E). I valori di controllo (Ct) sono stati
normalizzati per actina e espressi come fold change vs prima della gravidanza.
Significatività statistica: *p<0.05; prima della gravidanza: barre bianche; primo
trimestre (E): barre blu, con n=6 determinazioni indipendenti.
L’elevata espressione genica dei fattori di trascrizione appartenenti alle famiglie di
FOXO,PPARƴ,CREB e SERB era indicativa per una differenziazione adipocitaria.
L’incremento del recettore per VLDL e LDL related-protein 1, fatty acid synthase
(FAS), acetyl CoA caroboxylase (ACC) e stearoyl-CoA desaturase (SCD) che
catalizzano l’up-take degli acidi grassi liberi, la sintesi e l’allungamento delle loro
catene erano segni evidenti di una attiva lipogenesi. I componenti della matrice
extra-cellulare con proprietà strutturali (elastina, collagene) e proprietà di adesione
cellulare (laminina, fibronectina) erano fortemente espressi nel primo periodo di
gravidanza e includevano l’elevata espressione delle metalloproteasi (MMPs) per
incrementare la plasticità tissutale attraverso il rilascio di insulin-like growth factor
1 (IGF-1). L’attivazione concomitante di diversi fattori angiogenici (VEGF,TGF-beta,
ANG, FGFR2) suggeriva che il processo di neovascolarizzazione era associato con il
rimodellamento di matrice.

49
Discussione
Il nostro studio dimostra un’espansione del tessuto adiposo durante la gravidanza
che combina l’incremento del numero delle cellule (iperplasia) con l’incremento
della loro dimensione (ipertrofia).
Questo è in accordo con i dati mostrati per i depositi di grasso nella parte inferiore
del corpo nelle donne in gravidanza (97,98) ma differisce dai meccanismi descritti
nell’obesità dove l’ipertrofia si manifesta prima dell’iperplasia. La crescita
iperplastica appare geneticamente regolata mentre l’ipertrofia è più regolamentata
dalla nutrizione (99). Comunque sia, la crescita è anche dipendente da ogni
deposito e dal gene che definisce i precursori della proliferazione degli adipociti
(100). Il depot sottocutaneo della regione gluteale in gravidanza si espande in
maniera preferenziale rispetto al viscerale (73), è accessibile alla biopsia e più
incline ai cambiamenti infiammatori del deposito viscerale mesenterico o omentale
(101). Comunque, ulteriori studi effettuati sul tessuto viscerale permetterebbero di
comprendere il disegno globale dell’intero tessuto adiposo.

50
Espansione e Rimodellamento del Tessuto Adiposo
I nostri dati rivelano che gli adattamenti del tessuto adiposo in una gravidanza
fisiologica si sviluppano in maniera temporale con un insieme di cambiamenti
molecolari che precedono l’espansione antropometrica della massa adiposa.
L’espansione del tessuto adiposo è un processo complesso che si basa su di un
cross-talk molecolare tra differenti tipi cellulari della frazione stromale-vascolare
intorno agli adipociti (102,103). In accordo con questo concetto, il nostro studio
suggerisce che l’espansione del tessuto adiposo indotta dalla gravidanza coinvolge
una combinazione di vie di segnale condivise dai pre-adipociti, dalle cellule
immunitarie e endoteliali. La flessibilità della matrice cellulare che circonda gli
adipociti gioca un ruolo centrale nella regolazione dell’espandibilità del tessuto. Il
rimodellamento delle componenti della matrice extra-cellulare è accelerato in
numerose malattie metaboliche ed è associato con i cambiamenti del milieu
ormonale (86,102). L’incremento delle metalloproteinasi, fibronectina e laminina
accelerano la differenziazione pre-adipocitaria nel tessuto adiposo ipertrofico degli
individui obesi (104,105). Dall’altro lato l’angiogenesi, necessaria per i
rimodellamento del tessuto adiposo, può essere facilitato dalle metalloproteinasi e
dalle collagenasi (106). VEGF-A e il suo principale partner funzionale,
l’angiopoietina, sono essenziali per iniziare il programma di angiogenesi (107,108).
Quindi, l’incremento combinato dei fattori di crescita (IGF2, FGFR2) e dei fattori
angiogenici (VEGF, TGF-β) è in linea con il contributo dei meccanismi angiogenici al
complessivo rimodellamento del tessuto adiposo nel primo periodo della gestazione
(109). Il microambiente che circonda gli adipociti può anche essere modellato dalla
produzione di adipochine che esercitano sia un effetto paracrino che una funzione
endocrina propriamente detta. TNF-α e IL-6 mostrano un’incrementata espressione
sia nel primo trimestre di gravidanza che nell’ultimo periodo e possono quindi
regolare l’espressione di altri geni che contribuiscano all’azione negativa
dell’insulina (110). L’incrementata espressione di LepR è in accordo con il ruolo di
stimolazione della leptina sull’angiogenesi mentre la mancata regolazione del gene

51
della leptina è coerente con l’aumento dei livelli plasmatici di leptina in gravidanza,
essendone la placenta il principale produttore (111).

52
Biologia degli Adipociti
Il 29% di incremento della massa grassa misurata nell’ultimo periodo di gravidanza è
stata associata con un attivo rimodellamento del tessuto adiposo. L’attivazione
dell’ormone endoteliale lipoprotein-lipasi (LPL) nell’ultimo periodo di gravidanza,
suggerisce un’accelerata idrolisi dei trigliceridi circolanti in acidi grassi liberi (FFA),
rendendoli disponibili per l’up-take cellulare. I nostri risultati supportano l’elegante
studio di Herrera e coll. che ha dimostrato il ruolo cruciale di LPL nell’incrementare
l’immagazzinamento dei lipidi nel tessuto adiposo dei ratti in gravidanza (65).
L’elevata espressione di molti altri geni che direttamente influenzano la lipogenesi e
la differenziazione adipocitaria sta ad indicare che queste vie sono reclutate nel
primo periodo della gravidanza al fine di incrementare l’immagazzinamento lipidico
sia negli adipociti maturi che in quelli di nuova sintesi (Fig.9)
Fig.9 Diagramma della via metabolica molecolare identificata con l’analisi gene
ontology dei geni differentemente regolati nel primo trimestre di gravidanza.
Il fattore di trascrizione forkhead FOXO, isoforma 1, uno dei principali regolatori
dell’omeostasi energetica del tessuto adiposo, è un dei geni indotti nel primo
periodo di gravidanza. L’attivazione di FOXO1 potrebbe contribuire alla regolazione
delle dimensioni degli adipociti in risposta all’eccessivo introito calorico (112,113).

53
Così come FOXO1 è un ligando diretto di PPARƴ, cosi esso può contribuire alla
regolazione delle dimensioni degli adipociti e delle vie adipogeniche (114,115). I
geni sensibili ai nutrienti come cEBP-α, SREBP1 e PPARƴ, che rappresentano i
regolatori obbligatori della prima e ultima fase del programma di differenziazione
adipocitaria (116-118), sono inoltre attivati nella prima fase di gestazione. Nel suo
complesso, i cambiamenti nei meccanismi metabolici indicano che il maggior
accumulo adipocitario e l’incrementata differenziazione di nuovi adipociti, iniziano
ad uno stadio precoce della gravidanza per permettere l’ampliamento della massa
adiposa totale. Queste scoperte enfatizzano il concetto che i meccanismi
molecolari del processo adipogenico iniziano ben prima della comparsa dei classici
marker fenotipici. I nostri dati suggeriscono inoltre una somiglianza tra i meccanismi
della fisiologica espansione del tessuto adiposo in gravidanza e la patologica
espansione nell’obesità. Un esempio è il precoce incremento della proteina
secreted frizzled-related protein 1 (SFRP1), un modulatore endogeno della via di
Wnt/β-catenin che raggiunge il picco nei pazienti con una moderata obesità e
gradualmente si riduce nei soggetti con obesità morbigena (119).

54
Infiammazione
I segni della presenza di un’infiammazione molecolare sono presenti nel tessuto
adiposo a partire dalle prime fasi di gravidanza fino a termine. La gravidanza è
inoltre in sé e per sé una condizione infiammatoria, probabilmente iniziata per
consentire l’immunotolleranza verso il feto da parte della madre (120). I gruppi
funzionali di geni correlati alla regolazione immunitaria rappresentano circa il 30%
di tutti i geni significativamente modificati in gravidanza se comparati allo stato
pregravidico. L’espressione genica incrementata dei marker macrofagici CD14,
CD68, HLA-DR, HLA-DQ e del recettore del mannosio sono in accordo con un
recente report circa i cambiamenti infiammatori nel tessuto adiposo nei topi
nell’ultimo periodo di gravidanza (121). Il Toll-like receptor 4 (TLR4) così come
l’mRNA dei modulatori a valle della via di segnale del TLR4 erano significativamente
incrementati nelle prime fasi di gravidanza. TLR4 appartiene ad una famiglia di
recettori di membrana reclutati nella prima risposta del sistema immunitario innato
attraverso il legame della porzione Lipid A del lipopolisaccaride (LPS) rilasciato dai
batteri Gram negativi (122). (Fig.10)
Fig.10 Diagramma della via molecolare relativa all’attivazione di TLR4 identificata
con l’analisi gene ontology.

55
I fattori ambientali che possono innescare il reclutamento della via del sistema
immunitario innato nella prima fase di gravidanza non sono conosciuti. L’attivazione
del segnale di trasduzione di TLR4 è stata proposta come il link molecolare tra
obesità indotta dalla dieta e l’incrementata insulino-resistenza (122,123). I
cambiamenti nutrizionali come l’iperfagia materna o la disfagia che avvengono nel
primo periodo della gravidanza sono i candidati potenziali che potrebbero
impattare i recettori del tessuto adiposo e la loro stessa funzione (124). Sempre su
questa linea, i cambiamenti dei microbioti sono stati documentati in relazione
all’incremento del peso gestazionale e potrebbero avere un impatto sulla via di
segnale del TLR4 in gravidanza (125). Il riconoscimento dei batteri da parte del
recettore SAA, CD36, può avviare il processo infiammatorio in risposta
all’approvvigionamento di grasso (126,127). Le proteine della fase acuta
appartenenti alla famiglia delle SAA, sono marker di un basso grado di
infiammazione e di obesità e promuovono il rimodellamento endoteliale in parte
attraverso la mediazione della via di segnale del TLR4 (128-130).

56
Conclusioni
Mentre una considerevole letteratura ha definito l’infiammazione come una
componente obbligatoria del rimodellamento del tessuto adiposo nell’obesità e in
altre patologie questo report è la prima indicazione del reclutamento della via
infiammatoria nella gravidanza umana fisiologica.
Il precoce incremento del tessuto adiposo e la risposta immunitaria precedono la
comparsa dei cambiamenti fenotipici materni della composizione corporea e
dell’azione insulinica. Il pattern bifasico rivela come l’infiammazione fisiologica
rappresenti uno step precoce verso lo sviluppo della fisiologica insulino-resistenza
che raggiunge l’apice durante l’ultimo periodo della gravidanza. (Fig.11)
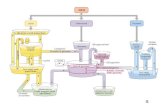
Fig.11 L’attivazione dei pattern trascrizionali suggerisce che la rete molecolare da differenti
tipi cellulari adiacenti contribuisce al rimodellamento del tessuto adiposo durante la
gravidanza. I componenti della matrice extra-cellulare e i fattori angiogenici sono necessari
alla crescita vascolare e adipocitaria. I geni lipogenici e i fattori di trascrizione sono richiesti
per la differenziazione cellulare e l’immagazzinamento dei lipidi. I macrofagi infiltrati tra le
cellule stromali producono citochine pro-infiammatorie, IL-6, IL-8 e TNF che possono sia
incrementare la neovascolarizzazione che facilitare lo sviluppo di insulino-resistenza.

57
Bibliografia
1) Di Cianni G, Miccoli R, Volpe L, Del Prato S. Intermediate metabolism in
normal pregnancy and in gestational diabetes. Diabetes Metab Res Rev
2003; 19: 259-270
2) Leturque A, Ferre P, Burnol AF. Glucose utilization tares and insulin
sensitivity in vivo in tissues of virgin and pregnant rats. Diabetes 1986;
35:172-177
3) Buchanan Ta. Metabolic changes during normal and diabetic pregnancy. In
Diabetes Mellitus in Pregnancy, Reece EA, Coustan DR (eds). Curchill
Livingstone: New York, 1995; 59-77
4) Shao J, Catalano PM, Yamashita H. Decreased insulin receptor tyrosine
kinase activity and plasma cell membrane glycoprotein-1 overexpression in
skeletal muscle from obese women with GDM: evidence for increase
serine/threonine phosphorylation in pregnancy and GDM. Diabetes
2000;49:603-610
5) Butte NF.: Carbohydrate and lipid metabolism in pregnancy: Normal
compared with gestational diabetes mellitus. Am J Clin Nutr 71, (suppl.1):
12656S, 2000.
6) Catalano PM, Tyzbir ED, Roman NM, Amini SB, Sims EA. Longitudinal
changes in insulin release and insulin resistance in non obese pregnant
women. Am J Obstet Gynecol 165: 1667-1672, 1991.

58
7) Catalano PM., Huston L., Amin SB., Kalhan SC.: Longitudinal change in
glucose metabolism during pregnancy in obese women with normal glucose
tolerance and gestational diabetes mellitus. Am J Obstet Gynecol 180 , 903,
1995.
8) Buchanan TA., Metzger BE., Freinkel N.: Insulin sensitivity and B-cell
responsiveness to glucose during late pregnancy in lean and moderately
obese women with normal glucose tolerance or mild gestational diabetes.
Am J Obstet Gynecol 162: 1008,1990.
9) Bartha J., Delgado R., Martinez-Del-Fresno P., Fernandez Barrios M.,
Berthencourt I., Corral L.M.: Insulin-Sensitivity Index and Carbohydrate and
Lipid Metabolism in Gestational Diabetes.J.Reprod Med 45, 185, 2000.
10) Kühl C.: Etiology and Pathogenesis of Gestational Diabetes. Diabetes Care,
vol 21 (Suppl 2): B19, 1998.
11) Andersen O., Kühl C.: Adipocyte insulin receptor binding and lipogenesis at
term in normal pregnancy. Eur J Clin Invest. 18: 575, 1988.
12) Damm P., Handber A., Kühl C., et al.: Insulin receptor binding and tyrosine
kinase activity in skeletal muscle from normal pregnant women and women
with gestational diabetes. Obstet Gynecol 82, 251,1993.
13) Shao J., Catalano PM., Yamashita H., Ruyte I., Smith S., Youngren J.,
Friedman JE.: Decreased insulin receptor tyrosine kinase activity and
overexepression of PC-1 in skeletal muscle from obese women with

59
gestational diabetes mellitus(GDM): evidence for increased serine:threonine
phosphorylation in pregnancy and GDM. Diabetes 49 (4): 603, 2000.
14) Friedman JE., Ishizuka T., Shao J., Huston L., Higman T., Catalano P.: Impaired
tyrosine glucose transport and insulin receptor tyrosine phosphorylation in
skeletal muscle from obese women with gestational diabetes. Diabetes 48
(9): 1807, 1999.
15) Saad MJA., Maeda L., Brenelli SL., et al.: Defect in insulin signal transduction
in liver and muscle of pregnant rats. Diabetologia 40: 179. 1997.
16) Okuno S., Akazawa S., Yasuhi I. et al.: Decreased expression of GLUT4
glucose transporter protein in adipose tissue during pregnancy. Horm Metab
Res, 27,231, 1996.
17) Ishizuka T., Klepcyk P., Liu S. et al.: Effects of overexpression of human
GLUT4 gene on maternal diabetes and fetal growth in spontaneous
gestational diabetic C57BL6/J Lepr/(db/+) mice. Diabetes 48: 1061, 1999.
18) Goldfine ID., Maddux BA., Youngreen JF.: Membrane glycoprotein PC-1 and
insulin resistance. J Biochem 182: 177,1998.
19) Catalano P., Highman T., Hustone L., Friedman J.: Relationship between
reproductive hormones/TNF-alpha and longitudinal changes in insulin
sensitivity during gestation. Diabetes 45(suppl 2):175,1996.
20) Ryan Ea e Enns L. Role of gestational hormones in the induction of insulin
resistance. JCEM 67:341-347, 1988

60
21) Hotamisligil GS, Murray K, Baron AD. Tumor necrosis factor alpha inhibits
signaling from the insulin receptor PNAS 91: 4854-4858, 1994
22) Xiang AH, Peters RK, Trigo E Multipl metabolic defects during late pregnancy
in women at high risk for type 2 diabetes. Diabetes 48:848-854, 1999
23) Freinkel N, Metzeger BE, Nitzan M: Facilitaed anabolism in late pregnancy:
some novel maternal compensation for accelerated starvation. VIII congress
IDF, Amsterdam 1974
24) LeTurque A, Ferre P, Burnol A. Glucose utilization rates and insulin sensitivity
in vivo in tissues of virgin and pregnant rats. Diabetes 35:172,1986
25) Silvan E., Chen X., Homko CJ., Reece EA., Boden G.: Longitudinal study of
carbohydrate metabolism in healthy obese pregnant women. Diabetes Care.
20, 1470, 1997.
26) Catalano PM., Tyzbir ED., Wolfe RR., Calles J., Roman NM., Amini SB., Sims
EAH: Carbohydrate metabolism during pregnancy in control subject and
women with gestational diabetes. Am J Physiol 264: E60, 1993.
27) Bergman RN., Ider YZ., Bowden CR., Cobelli C.: Quantitative estimation of
insulin sensitivity. Am J Phisiol 236: E667,1979
28) Bowes SB., Hennesy TR., Umpleby AM., Benn JJ., Jackckson NC, Boroujerdi
MA. Sonksen PH, Lowy C: measurement of glucose metabolism and insulin
secretion during normal pregnancy and pregnancy complicated by
gestational diabetes. Diabetologia 39, 976, 1996.

61
29) Swinn RA., Wareham NJ., Gregory R.: Excessive secretion of insulin precursor
characterizes and predict gestational diabetes. Diabetes 44:911,1995.
30) Van Assche FA., Aerts L., De Prins F.: A morphologic study of the endocrine
pancreas in human pregnancy. Br J Obstet Gynaecol 85, 818, 1978.
31) Ryan EA., Enns L.: Role of gestational hormons in the induction of insulin
resistance. J Clin Endocrinol Metab 67: 341, 1988.
32) Nelson T., Shuman G., Grainger D., Diamond MP..: Progesterone
administration induced impairment of insulin suppression of hepatic glucose
production. Fertil Steril 62: 491, 1994.
33) Giorgino F., Almahfouz A., Goodyear LJ., Smith RJ.: Glucocorticoid regulation
of insulin receptor IRS-1 tyrosine phosphorylation in rat skeletal muscle in
vivo. J Clin Invest. 91: 2020, 1993
34) Kawai M, Kishi K.: Adaptation of pancreatic B-cells during the last third of
pregnancy: regulation of B-cell function and proliferation by lactogenic
hormones in rats. Eur J Endocrinol 141: 419-425, 1999.
35) Handwerger S, Freemark M.: The roles of placental growth and placental
lactogen in the regulation of human fetal growth and development. J Pediatr
Endocrinol Metab 13: 343-356, 2000.
36) Hu L, Lytras A, Bock ME, Yuen CK et al.: Detection of placental growth
hormone variant and chorionic somatomammotropin-L RNA expression in
normal and diabetic pregnancy by reverse transcriptase-polymerase chain
reaction. Mol Cell Endocrinol: 157: 121-143, 1999.

62
37) Sorenson RL , Breje TC. Adaptation of islet of Langerhans to pregnancy: beta-
cell growth, enhanced insulin secretion and the role of lactogenic hormones.
Horm Metab Res: 29 (6) : 301-7, 1997.
38) Sorenson RL, Scharp DW, Lacy PE,Ogreen L, Talamantes F, Robertson M,
Friesen HG, Effect of Homologous placental lactogens prolactins, and
growth hormones on islet B-cell division and insulin secretion in rat, mouse,
and human islets: implication for placental lactogen regulation of islet
function during pregnancy. Endocrinology 132 (2): 879-87, 1993.
39) Sorenson RL, BreLje TC, Roth C. Effects of steroid and latogenic hormones on
islets of Langerhans: a new hypothesis for the role of pregnancy steroids in
the adaptation of islets to pregnancy. Endocrinology 133 : 2227-34, 1993.
40) Markoff E, Battie GM, Hayek A, Lewis SL. Effect of prolactin and glycosylated
prolactin on (pro)insulin synthesis and insulin release from cultured rat
pancreatic islets. Pancreas 5:99-103, 1990.
41) Weinhaus AJ, Stout LE, Sorenson RL. Glucokinase, hexokinase, glucose
transporter 2 and glucose metabolism in islets during pregnancy and
prolactin treated islets in vitro: mechanisms for long term up-regulation of
islets. Endocrinology 137:1640-1649, 1996.
42) Brelje TC, Allaire P, Hegre OD, Sorenson RL. Effect of prolactin versus growth
hormone on islets function and the importance of using homologous
mammosomatotropic hormones. Endocrinology 125:1459-1466, 1992.

63
43) Vasavada RC, Garcia-Ocaña A, Zawalich WS, Sorenson RL, Dann P, Syed M,
Ogren L, Talamantes F, Stewart AF. Targeted expression of placental
lactogen in the beta cells of transgenic mice results in beta cell proliferation,
islet mass augmentation, and hypoglycemia. J Biol Chem 275:15399-15406,
2000.
44) Weinhaus AJ, Bhagroo NV, Brelje TC, Sorenson RL. Role of camp in
upregulation of insulin secretion during the adaptation of islets of
Langerhans to pregnancy. Diabetes 47:1426-1435, 1998.
45) Yamashita H., Shao J., Friedman JE.: Physiologic and Molecular Alterations in
Carbohydrate Metabolism During Pregnancy and Gestational Diabetes
Mellitus. Clin Obstet and Gynecol 43: 87, 2000.
46) Zhang Y., Proenaca R., Maffei M., Barone M., Leopold L., Friedman JM.
Positional cloning of mouse gene and its human homologue. Nature 372:
425, 1994.
47) Campfield LA., Smith FJ., Guiser Y., Devos R., Burn P.: Recombination mouse
OB protein: Evidence for a peripheral signal linking adiposity and central
neural networks. Science 269: 546, 1994.
48) Masuzaki H., Ogawa Y., Sagawa N.et al.: Nonadipose tissue production of
leptin: leptin as a novel placental-derived hormone in humans. Nat Med. 3:
1029, 1997.
49) Higman TJ., Friedman JE., Huston LP., Wong WW., Catalano PM.:
Longitudinal change in maternal serum leptin concentrations body

64
composition and resting metabolic rate in pregnancy. Am J Obstet Gynecol
178:1010, 1999.
50) Virkammäki A., Ueki K., Kahn CR.: Protein interaction in insulin signaling and
the molecular mechanisms of insulin resistance. J Clin Invest., 103: 931,
1999.
51) Maffei M., Volpe L., Di Cianni G., Bertacca A., Ferdeghini M., Murru S. et al.:
Plasma leptin levels in newborns from normal and diabetic mothers. Horm
Metab Res 30: 575, 1998.
52) Yura S., Sagawa N., Mise H., Masuzaki H., Ogawa Y., Nakao K.: A positive
umbilical venous-arterial difference of leptin level and its rapid decline after
birth. Am J Obstet Gynecol. 178: 926, 1999.
53) Phelps RL, Metzger BE, Freinkel N: Diurnal profiles of glucose, insulin, free
fatty acids, triglycerides, cholesterol, and individual aminoacids in late
normal pregnancy. AJOG 140: 730,1981
54) Herrera E,Gomez D, Lasuncion MA:Lipid metabolism in pregnancy. Biol
Neonate 51: 70.1987
55) Topping DL, The iimediated effect of insulin and fructose on the metabolism
of the perfused liver. Biochem J, 126:295,1972
56) Catalano PM, Kirwan JP, Hauguel-de Mouzon : Gestational Diabetes and
Insulin Resistance: role in short- and Long Term Implications for mother and
fetus. Metabolism, J.Nutr 133: 1674S-1683S, 2003
57) Darmady JM e Postle AD. Lipid metabolism in pregnancy. BJOG. 89:211-215

65
58) Knopp RH, Bergelin RO, Wahl PW. Relationship of infant birth size to
maternal lipoproteins, apoproteins, fuels, hormones, clinical chemestries,
and body wight at 36 week gestation. Diabetes 34 (Suppl 2) 104:601-607,
1985
59) Kliegman R, Gross T, Morton S, Dunnington R. Intrauterine growth and post
natal fasting metabolism in infants of obese mothers. J.Pediatr.104: 601-
607, 1984
60) Sivan E, Homko C, Chen X, Reece EA, Boden G. Effect of insulin on fat
metabolism during and after normal pregnancy. Diabetes 48: 834-838,1999
61) Catalano PM, Niezielski SE, Shao J, Presley L, Friedman JE. Down regulation
of IRS-1 and PPRgamma in obese women with gestational diabetes:
relationship of free fatty acids during pregnancy. AL Perinatol. 282:E522-
E533
62) Duggleby SC, Jackson AA. Protein amminoacid and nitrogen metabolism
during pregnancy: how might the mother meet the needs of her fetus? Curr
Opin.Clin.Nutr. Metab.Care 14: 561-569,2002
63) Catalano P, Drago N, Highman T. Huston L. Longitudinal changes in
aminoacid insulin sensitivity during pregnancy. JSGI.abstract, 1996
64) Kalhan SC, Assel BG: protein metabolism in pregnancy: principles of
perinatal-neonatal metabolism. Springer verlag, new York,1991
65) Ramos MP, Crespo-Solans MD, del Campo S, Cacho J, Herrera E. Fat
accumulation in the rat during early pregnancy is modulated by enhanced

66
insulin responsiveness. Am J Physiol Endocrinol Metab 285: E318-E328,
2003.
66) Herrera E. Lipid metabolism in pregnancy and its consequences in the fetus
and the newborn. Endocrine, vol 19, no1. 43-45, 2002
67) Palacin M, Lasuncion M, Asuncion M, Herrera E. Circulating metabolite
utilization by perluterine adipose tissue in situ in pregnant rat. Metabolism
40,534-539,1991
68) Hytten FE. Water storage in pregnancy. Midwife Health Visit 3: 60-62, 1967.
69) Larciprete G, Valensise H, Vasapollo B, Altomare F, Sorge R, Casalino B, De
Lorenzo A, Arduini D. Body composition during normal pregnancy: reference
ranges. Acta Diabetol 40: S225-S232, 2003.
70) King JC, Butte NF, Bronstein MN, Kopp LE, Lindquist SA. Energy metabolism
during pregnancy: influence of maternal energy status. Am J Clin Nutr 59:
439S-445S, 1994.
71) Poppitt SD, Prentice AM, Goldberg GR, Whitehead RG. Energy-sparing
strategies to protect human fetal growth. Am J Obstet Gynecol 171: 118-
125, 1994.
72) Kopp-Hoolihan LE, van Loan MD. Fat mass deposition during pregnancy
using a four component model. J Appl Physiol 87: 196-202, 1992.
73) Ehrenberg HM, Huston-Presley L, Catalano PM. The influence of obesity and
gestational diabetes mellitus on accretion and the distribution of adipose
tissue in pregnancy. Am J Obstet Gynecol 189: 944-948, 2003.

67
74) Villar J, Cogswell M, Kestler E, Castillo P, Menendez R, Repke JT. Effect of fat
and fatfree mass deposition during pregnancy on birth weight. Am J Obstet
Gynecol 167: 1344-1352, 1992.
75) Battaglia FC, Meschia G. Principal substrates of fetal metabolism. Physiol Rev
58:499-527, 1978.
76) Herrera E. Metabolic adaptations in pregnancy and their implications for the
availability of substrates to the fetus. Eur J Clin Nutr 54 Suppl 1: S47-S51,
2000.
77) Ryan EA, O'Sullivan MJ, Skyler JS. Insulin action during pregnancy. Studies
with the euglycemic clamp technique. Diabetes 34: 380-389, 1985.
78) Knopp RH, Warth MR, Carrol CJ. Lipid metabolism in pregnancy. I. Changes in
lipoprotein triglyceride and cholesterol in normal pregnancy and the effects
of diabetes mellitus. J Reprod Med 10: 95-101, 1973.
79) Catalano PM, Hoegh M, Minium J, Huston-Presley L, Bernard S, Kalhan S,
Hauguel De Mouzon S. Adiponectin in human pregnancy: implications for
regulation of glucose and lipid metabolism. Diabetologia 49: 1677-1685,
2006.
80) Highman TJ, Friedman JE, Huston LP, Wong WW, Catalano PM. Longitudinal
changes in maternal serum leptin concentrations, body composition, and
resting metabolic rate in pregnancy. Am J Obstet Gynecol 178: 1010-1015,
1998.

68
81) Hauguel-de Mouzon S, Lepercq J, Catalano P. The known and unknown of
leptin in pregnancy. Am J Obstet Gynecol 194: 1537-1545, 2006.
82) Catalano PM, Presley L, Minium J, Hauguel-de Mouzon S. Fetuses of obese
mothers develop insulin resistance in utero. Diabetes Care 32: 1076-1080,
2009.
83) Lee MJ, Wu Y, Fried SK. Adipose tissue remodeling in pathophysiology of
obesity. Curr Opin Clin Nutr Metab Care 13: 371-376, 2010.
84) Van Harmelen V, Skurk T, Röhrig K, Lee YM, Halbleib M, Aprath-Husmann I,
Hauner H. Effect of BMI and age on adipose tissue cellularity and
differentiation capacity in women. Int J Obes Relat Metab Disord 27: 889-
895, 2003.
85) Doyle SL, Donohoe CL, Lysaght J, Reynolds JV. Visceral obesity, metabolic
syndrome, insulin resistance and cancer. Proc Nutr Soc 3: 1-9, 2011.
86) Cinti S, Mitchell G, Barbatelli G, Murano I, Ceresi E, Faloia E, Wang S, Fortier
M, Greenberg AS, Obin MS. Adipocyte death defines macrophage
localization and function in adipose tissue of obese mice and humans. J Lipid
Res 46: 2347-2355, 2005.
87) Xu H, Barnes GT, Yang Q, Tan G, Yang D, Chou CJ, Sole J, Nichols A, Ross JS,
Tartaglia LA, Chen H. Chronic inflammation in fat plays a crucial role in the
development of obesity related insulin resistance. J Clin Invest 112: 1821-
1830, 2003.

69
88) Basu S, Haghiac M, Surace P, Challier JC, Guerre-Millo M, Singh K, Waters T,
Minium J, Presley L, Catalano PM, Hauguel-de Mouzon S. Pregravid obesity
associates with increased maternal endotoxemia and metabolic
inflammation. Obesity 19: 476-482,2011.
89) Vora N, Johnson KL, Basu S, Presley L, Minium J, Catalano PM, Bianchi DW,
Hauguel-de Mouzon S. Increased circulating cell free DNA in plasma of obese
pregnant women. Am J Obstet Gynecol 201: S252, 2009.
90) Catalano PM, Wong WW, Drago NM, Amini SB. Estimating body composition
in late gestation: a new hydration constant for body density and total body
water. Am J Physiol 268: E153-E158, 1995.
91) Huston Presley L, Wong WW, Roman NM, Amini SB, Catalano PM.
Anthropometric estimation of maternal body composition in late gestation.
Obstet Gynecol 96: 33-37, 2000
92) Steele R. Influences of glucose loading and of injected insulin on hepatic
glucose output. Ann NY Acad Sci 82: 420-430, 1959
93) De Fronzo RA, Tobin D and Andres R. Glucose clamp technique: a method for
quantifying insulin secretion and resistance. AJPEMGP 237: E2147-223, 1979
94) Tserng KY and Kalhan SC. Calculation of substrate turnover rate in stable
isotope tracer studie. AJPEM 245: E308-E311,1983
95) Salans LB, Horton ES, Sims EA. Experimental obesity in man: cellular
character of the adipose tissue. J Clin Invest. 50:1005-1011, 1971.

70
96) Radaelli T, Lepercq J, Varastehpour A, Basu S, Catalano PM, Hauguel-De
Mouzon S. Differential regulation of genes for fetoplacental lipid pathways
in pregnancy with gestational and type 1 diabetes mellitus. Am J Obstet
Gynecol 201: 209.e1-209.e10, 2009.
97) Drolet R, Richard C, Sniderman AD, Mailloux J, Fortier M, Huot C, Rhéaume
C, Tchernof A. Hypertrophy and hyperplasia of abdominal adipose tissues in
women. Int J Obes 32:283-291. 2008
98) Tchoukalova YD, Koutsari C, Karpyak MV, Votruba SB, Wendland E, Jensen
MD. Subcutaneous adipocyte size and body fat distribution. Am J Clin Nutr.
87:56-63, 2008.
99) Jo J, Gavrilova O, Pack S, Jou W, Mullen S, Sumner AE, Cushman SW, Periwal
V. Hypertrophy and/or Hyperplasia: Dynamics of Adipose Tissue Growth.
PLoS Comput Biol. 5: 2009.
100) Yamamoto Y, Gesta S, Lee KY, Tran TT, Saadatirad P, Kahn CR.Adipose depots
possess unique developmental gene signatures. Obesity (Silver Spring).;18:
872-878, 2010.
101) Evans J, Goedecke JH, Söderström I, Burén J, Alvehus M, Blomquist C,
Jonsson F, Hayes PM, Adams K, Dave JA, Levitt NS, Lambert EV, Olsson T.
Depot- and ethnic specific differences in the relationship between adipose
tissue inflammation and insulin sensitivity. Clin Endocrinol (Oxf). 74:51-59.
2011.

71
102) Sun K, Kusminski CM, Scherer PE. Adipose tissue remodeling and obesity. J
Clin Invest 121: 2094-2101, 2011.
103) Sethi JK, Vidal-Puig AJ. Thematic review series: adipocyte biology. Adipose
tissue function and plasticity orchestrate nutritional adaptation. J Lipid Res
48: 1253-1262, 2007.
104) Spencer M, Unal R, Zhu B, Rasouli N, McGehee RE Jr, Peterson CA, Kern PA.
Adipose Tissue Extracellular Matrix and Vascular Abnormalities in Obesity
and Insulin Resistance. J Clin Endocrino Metab Oct 12. epub ahead of print,
2011.
105) Keophiphath M, Achard V, Henegar C, Rouault C, Clément K, Lacasa D.
Macrophage secreted factors promote a profibrotic phenotype in human
preadipocytes. Mol Endocrinol 23: 11-24, 2009.
106) Chavey C, Mari B, Monthouel MN, Bonnafous S, Anglard P, Van Obberghen
E, Tartare, Deckert S. Matrix metalloproteinases are differentially expressed
in adipose tissue during obesity and modulate adipocyte differentiation. J
Biol Chem 278: 11888-11896, 2003.
107) Papetti M, Herman IM. Mechanisms of normal and tumor-derived
angiogenesis. Am J Physiol Cell Physiol. 2002 May;282(5):C947-70.
108) Zhang QX, Magovern CJ, Mack CA, BudenbendeKT, Ko W, Rosengart TK.
Vascular endothelial growth factor is the major angiogenic factor
inomentum: mechanism of the omentum-mediated angiogenesis. J Surg Res
67: 147–154, 1997.

72
109) Tam J, Duda DG, Perentes JY, Quadri RS, FukumuraD, Jain RK. Blockade of
VEGFR2 and not VEGFR1 can limit diet-induced fat tissue expansion:role of
local versus bone marrow-derived endothelial cells. PLoS One 4: e4974,
2009.
110) Kirwan JP, Hauguel-De Mouzon S, Lepercq J, Challier JC, Huston-Presley L,
Friedman JE, Kalhan SC, Catalano PM. TNF-alpha is a predictor of insulin
resistance in human pregnancy. Diabetes 51: 2207-2213, 2002.
111) Lepercq J, Cauzac M, Lahlou N, Timsit J, Girard J, Auwerx J, Hauguel-de
Mouzon S. Overexpression of placental leptin in diabetic pregnancy: a critical
role for insulin. Diabetes 47: 847-850, 1998.
112) Nakae J, Kitamura T, Kitamura Y, Biggs WH 3rd, Arden KC, Accili D. The
forkhead transcription factor Foxo1 regulates adipocyte differentiation. Dev
Cell 4: 119-129, 2003.
113) Nakae J, Cao Y, Oki M, Orba Y, Sawa H, Kiyonari H, Iskandar K, Suga K,
Lombes M, Hayashi Y. Forkhead transcription factor FoxO1 in adipose tissue
regulates energy storage and expenditure. Diabetes 57: 563-576, 2008.
114) Dowell P, Otto TC, Adi S, Lane MD. Convergence of peroxisome proliferator-
activated receptor gamma and Foxo1 signaling pathways. J Biol Chem 278:
45485-45491, 2003.
115) Vidal-Puig A, Jimenez-Linan M, Lowell BB, Hamann A, Hu E, Spiegelman B,
Flier JS, Moller DE. Regulation of PPAR gene expression by nutrition and
obesity in rodents. J Clin Invest 97: 2553-2561, 1996.

73
116) Girard J, Ferré P, Foufelle F. Mechanisms by which carbohydrates regulate
expression of genes for glycolytic and lipogenic enzymes. Annu Rev Nutr 17:
325-352, 1997.
117) Boizard M, Le Liepvre X, Lemarchand P, Foufelle F, Ferré P, Dugail I. Obesity-
related overexpression of fatty-acid synthase gene in adipose tissue involves
sterol regulatory element-binding protein transcription factors. J Biol Chem
273: 29164-29171, 1998.
118) Wu Z, Rosen ED, Brun R, Hauser S, Adelmant G, Troy AE, McKeon C,
Darlington GJ, Spiegelman BM. Cross-regulation of C/EBP alpha and PPAR
gamma controls the transcriptional pathway of adipogenesis and insulin
sensitivity. Mol Cell 3: 151-158, 1999.
119) Lagathu C, Christodoulides C, Tan CY, Virtue S, Laudes M, Campbell M,
Ishikawa K, Ortega F, Tinahones FJ, Fernández-Real JM, Orešic M, Sethi JK,
Vidal-Puig A. Secreted frizzled-related protein 1 regulates adipose tissue
expansion and is dysregulated in severe obesity. Int J Obes (Lond) 34: 1695-
1705, 2010.
120) Challis JR, Lockwood CJ, Myatt L, Norman JE, Strauss JD, Petraglia F.
Inflammation and pregnancy. Reprod Sci 2009; 16:206-15
121) Zhang L, Sugiyama T, Murabayashi N, Umekawa T, Ma N, Kamimoto Y,
Ogawa Y, Sagawa N. The inflammatory changes of adipose tissue in late
pregnant mice. J Mol Endocrinol 47: 157-65, 2011.

74
122) Shi H, Kokoeva MV, Inouye K, Tzameli I, Yin H, Flier J. TLR4 links innate
immunity and fatty acid-induced insulin resistance. J Clin Invest 116: 3015–
3025, 2006.
123) Tsukumo DML, Carvalho-Filho MA, Carvalheira JBC, Prada PO, Hirabara SM,
Schenka AA, Araújo EP, Vassallo J, Curi R, Velloso LA, Saad JAS. Loss-of-
function mutation in Toll-like receptor 4 prevents diet-induced obesity and
insulin resistance. Diabetes 56: 1986–1998, 2007.
124) Björntorp P. Growth hormone, insulin-like growth factor-I and lipid
metabolism: interactions with sex steroids. Horm Res 46: 188-191, 1996.
125) Collado MC, Isolauri E, Laitinen K, Salminen S. Distinct composition of gut
microbiota during pregnancy in overweight and normal-weight women. Am J
Clin Nutr 88: 894-899, 2008.
126) Baranova IN, Bocharov AV, Vishnyakova TG, Kurlander R, Chen Z, Fu D, Arias
IM, Csako G, Patterson AP, Eggerman TL. CD36 is a novel serum amyloid A
(SAA) receptor mediating SAA binding and SAA-induced signaling in human
and rodent cells. J Biol Chem 285: 8492-506, 2010.
127) Yang RZ, Lee MJ, Hu H, Pollin TI, Ryan AS, Nicklas BJ, Snitker S, Horenstein
RB, Hull K, Goldberg NH, Goldberg AP, Shuldiner AR, Fried SK, Gong DW.
Acute-phase serum amyloid A: an inflammatory adipokine and potential link
between obesity and its metabolicomplications. PLoS Med 3: e287, 2006.
128) Poitou C, Coussieu C, Rouault C, Coupaye M, Cancello R, Bedel JF, Gouillon
M, Bouillot JL, Oppert JM, Basdevant A, Clément K. Serum amyloid A: a

75
marker of adiposity-induced low-grade inflammation but not of metabolic
status. Obesity (Silver Spring) 14: 309-318, 2006.
129) Mortensen OH, Nielsen AR, Erikstrup C, Plomgaard P, Fischer CP, Krogh-
Madsen R, Lindegaard B, Petersen AM, Taudorf S, Pedersen BK. Calprotectin-
-a novel marker of obesity. PLoS One 4: e7419, 2009.
130) Averill MM, Kerkhoff C, Bornfeldt KE. S100A8 and S100A9 in cardiovascular
biology and disease. Arterioscler Thromb Vasc Biol Nov 17, 2011 [Epub
ahead of print].

Ringraziamenti
Seduta alla mia scrivania e occupata nelle ultime correzioni della tesi, ancora non mi rendo
conto di esser giunta al termine di questo cammino. Guardandomi alle spalle vedo quante
cose nella mia vita sono cambiate. Questo mio percorso è iniziato molti anni fa. Non sempre
è stato tutto semplice ma, sicuramente, l’esperienza universitaria è stata e rimarrà unica.
Il mio primo grazie va al Prof. Stefano Del Prato, per avermi incitata in questi anni a
migliorare gli aspetti della professione medica, per avermi dato le basi per affrontare sfide
coraggiose e per aver riso spesso alle mie battute.
Voglio esprimere la mia più profonda gratitudine al mio mentore, il Dr. Graziano Di Cianni,
per la sua guida, comprensione, pazienza e incoraggiamento nei passati anni. Il suo
illimitato sostegno è stata la maggior forza trainante durante il mio percorso di medico e la
mia formazione come persona.
Il mio più affettuoso e generoso grazie va alla Dr.ssa Laura Volpe, per il suo continuo e
instancabile appoggio, la straordinaria professionalità e il suo entusiasmo contagioso. Mi ha
ispirata nel corso di questi lunghi anni a diventare un medico e una persona migliore.
Grazie di cuore alla Dr.ssa Rosa Giannarelli. Non mi è mai mancato il suo affetto e la sua
comprensione. Non dimenticherò mai i suoi insegnamenti, né le colazioni che mi ha pagato
dopo ogni turno di notte.
Un grazie sincero alla Dr.ssa Bertolotto. In questi ultimi anni abbiamo condiviso difficoltà e
soddisfazioni. La ringrazio per quello che è stato e per quello che sarà.
Voglio ringraziare di cuore la Dr. Sylvie Hauguel de-Mouzon. Mi ha incoraggiata a sviluppare
un pensiero indipendente e competenze scientifiche che mi hanno preparata ad affrontare
sfide future. Senza di lei questo lavoro non sarebbe stato realizzato. Voglio ringraziare il Dr.
Patrick Michael Catalano. La grandezza di un uomo risiede nella sua capacità di essere
umile. Ha messo a mia disposizione la sua conoscenza e la sua professionalità nell’intento
unico di insegnare.
Grazie, mille volte, ai miei strutturati: Dr.Aragona, per aver condiviso con me sorrisi, musica
e citazioni; Dr.Campi per i momenti esilaranti e folli; Dr.ssa Ciccarone, per gli incontri-
scontri costruttivi per entrambe; Dr.Coppelli, per aver condiviso con me l’affetto per la
Giannina e le ore di guardia; Dr.ssa Dardano, per tu sai cosa; Prof. Marchetti, per il
confronto con una realtà diversa e le sue opportunità; Dr. Miccoli, per lo sguardo severo e
attento durante i miei passi in tutti questi anni; Dr.Penno, per le risate, i momenti di svago e
le buone parole sempre spese per me; Dr.Piaggesi, per il confronto spigoloso e la crescita
professionale; Dr.ssa Rizzo, per lo sguardo benevolo ma sempre un po’critico, come quello
di una mamma. E al Prof. Benzi, per i primi insegnamenti e gli abbracci affettuosi.
Un enorme grazie alla Dr.ssa Cristina Bianchi. Collega prima, capa poi, amica sempre.

Grazie di cuore al Personale Infermieristico e Para-Infermieristico della nostra U.O. per gli
insegnamenti, le ramanzine, le ore trascorse insieme. Grazie per esservi presi cura non solo
della specializzanda ma anche di Veronica. Non lo dimenticherò mai.
Grazie ai Podologi, ai Biologi, ai Ricercatori per l’aiuto tecnico e gli insegnamenti preziosi.
Siete stati tutti degli ottimi maestri.
Grazie a quelle due persone che mantengono il nostro Dipartimento unito e funzionale, e
con le quali è sempre un piacere fare due chiacchere: Lia e Giulia.
Il ringraziamento più sentito va ai colleghi specializzandi e agli amici di sempre. Avete
trasformato la Scuola di Specializzazione in un percorso di vita. Grazie ad Alessia e Chiara,
nel passato come nel presente. Grazie a Francesca Panki, sempre presente. Grazie ad
Alessandra e Ilaria, angeli custodi e a Cristina L,non solo disquisizioni scientifiche. Grazie ad
Anna e Francesca Palu’, le grandi del gruppo. Grazie a Nicolò e Marco, inimitabili. Grazie ad
Andrea. Grazie a Isabella e Dario, piccoli già grandi. Grazie a Elisabetta S e Rossella, non solo
medicina direi. Grazie a Emilia, una piccola me con un cuore più grande del mio. Grazie a
Marianna e Elisabetta I, poco tempo insieme ma spero buono. Grazie alle nuove
generazioni Monia e Mario. E Grazie a Miriam, la vita può separarci, il bene poi continuerà.
Grazie ai colleghi medici che ho incontrato in questo percorso. Ho imparato che la
conoscenza condivisa acquista più valore. Ho imparato che il confronto leale e aperto
accresce tutti. Ho imparato che diventare un buon medico richiede tempo e sacrifici.
Un grazie pieno di affetto va a Savvina. Splendida compagna di viaggio. Maestra di gioia e
allegria.
E ovviamente il mio grazie va a tutti i pazienti che ho incontrato. Alcuni di loro mi hanno
insegnato a fare il medico, altri hanno cambiato la mia visione della malattia.
Il mio pensiero va, infine, al mio babbo, alla mia mamma e a David senza i quali non sarei
mai potuta giungere a questo punto. Grazie, per il sostegno a volte tacito e a volte esplicito,
indispensabile per superare i numerosi ostacoli incontrati in questo cammino. Siete sempre
stati la fonte di coraggio per affrontare ogni difficoltà.
Grazie a Marco. Hai ridato un significato nuovo alla parola futuro.
Un grazie a tutti coloro che, quaggiù sulla terra o lassù in cielo, instancabilmente illuminano
il mio cammino.
Considero il mio percorso ancora un work in progress, ma tutto quello che di buono ho
fatto e tutto quello che ho imparato, lo devo al micro-mondo dell’U.O. di Diabetologia di
Pisa.
Ho ricevuto più di quel che ho dato, da tutti quanti, ed è tanta la gratitudine che le parole
ormai non bastano più a descriverla.
Grazie a Eleonora e Margherita. Mi raccontate del mio passato. Siete nel mio presente. V’immagino nel mio futuro.