REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI derivati... · Un cloruro acilico Una...
Transcript of REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI derivati... · Un cloruro acilico Una...

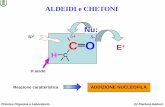
REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ALDEIDI E CHETONI
L’azoto nucleofilo dell’amminaattacca il carbonio elettrofilo delchetone
Come potremmo rendere questareazione più “facile”?
Emiamminale

La velocità della reazione però non continua ad aumentare con il decresceredel pH. Perchè?
Ci chiediamo ora che cosa succede all’emiamminale che si è formato…

Altri reagenti possono dare reazioni simili?
Immina; è il prodotto finale della reazione

Idrazina
Idrazone
Ma anche:
Idrossilammina
Ossima

Immine, idrazoni ed ossime possono essere idrolizzate
Per rigenerare il composto carbonilico di partenza
Un idrazone (X=NH2)
Che cosa può spostare l’equilibrioverso l’idrolisi?

Una immina può essere ridotta ad ammina con un riducente come un idruro.Idruri che si possono usare sono il NaBH4 o il LiAlH4
Una immina può essere ridotta ad ammina con un riducente come un idruro.Idruri che si possono usare sono il NaBH4 o il LiAlH4
La formazione di legami imminici gioca un ruolo importante nella stabilizzazione di proteine……

La catena laterale di unalisina viene ossidata
Si forma un’aldeide
Reticolazione

Che cosa succede se invece di far reagire con un aldeide o un chetone un’ ammina primaria usiamo una secondaria?
EmiamminaleEmiamminale
Enammina

Questa formula limite di una enammina da conto del carettere basico o
nucleofilo dell’atomo di carbonio in a
Enammina si protona a ione imminio
Enammina funge da nucleofilo e attacca un alogenuro alchilico

Quest’ultima reazione costituisce un ottimo metodo per alchilarein alfa un chetone in condizioni molto blande
Come vedremo in seguito l’alchilazione diretta in alfa di un chetone non è una reazione così semplice

REAZIONI DI ADDIZIONE-ELIMINAZIONE DI ACIDI CARBOSSILICI E LORO DERIVATI
Acido benzoico benzammide
NOMENCLATURA
Acido benzoico benzammide
esanammide 2-etilesanammide N-etilesanammide
Un estere fenilbutanoato isopropilbenzoatometlciclopentancarbossilato

Un gruppo acilico è quello che resta di un acido carbossilico o di un suo derivato quando si toglie la parte che contiene l’eteroatomo
Gruppo benzoilico o benzolile
pentanoile
formile acetile

Un nucleofilo si addiziona al carbonio carbonilico di un derivato di un acido carbossilico (come nel caso di aldeidi e chetoni) per dare un intermedio tetraedrico che però può eliminare il gruppo legato all’eteroatomo
Questa reazione è tanto più veloce tanto migliore è X-come gruppo uscentecome gruppo uscente
La situazione è molto diversa rispetto a quella che si verifica con aldeidi e chetoni

Il quadro della reattività
Un cloruro acilico Una anidride Un tioestere Un estere Una ammide
Reattività decrescente rispetto all’addizione nucleofila
Basicità crescente
Reattività decrescente rispetto all’eliminazione del gruppo uscente
Basicità crescente (con concomitante diminuzione crescente delle proprietà di gruppo uscente)

Come mai mancano gli acidi carbossilici?
In un acido carbossilico il sito elettrofilo principale è il protone che quindi reagirà per primo

In presenza di catalisi acida però…..
In un acido carbossilico neutro il protone è il sito elettrofilo principale mentre in un acido carbossilico proronato il sito elettrofilo è il carbonio carbonilicocarbonilico
Questo è un metodo semplice per sintetizzare esteri

Un lattone è un estere ciclico
Un ββββ lattone un γγγγ lattone un δδδδ lattone
La formazione di un lattone dal corrispondete idrossiacido avviene molto facilmente in presenza di tracce di acido

I cloruri degli acidi sono molto importanti perchè permettono disintetizzare molto facilmente tutti i derivati (perchè Cl- è un ottimo gruppo uscente!)
I cloruri degli acidi si ottengono per reazione con cloruro di tionile

A partire dai cloruri si ottengono facilmente sia esteri che ammidi
Ammide 1° ammide 2° ammide 3°

Le anidridi si Le anidridi si ottengono per disidratazione da due molecole di ottengono per disidratazione da due molecole di acidoacido(la reazione è particolarmente facile per ottenere anidridi cicliche)(la reazione è particolarmente facile per ottenere anidridi cicliche)
o per reazione di un anione o per reazione di un anione carbossilatocarbossilato con il cloruro di un acidocon il cloruro di un acido
Acido maleico anidride maleica acido ftalico andidride ftalica
o per reazione di un anione o per reazione di un anione carbossilatocarbossilato con il cloruro di un acidocon il cloruro di un acido
Intermedio tetraedricoIntermedio tetraedrico

Da una anidride si possono ottenere sia esteri che ammidiDa una anidride si possono ottenere sia esteri che ammidi
Intermedio tetraedricoIntermedio tetraedrico
Acido acetico pentilacetato (un estere)Acido acetico pentilacetato (un estere)
Provate ora a sintetizzare un’ammide a partire da una anidride….

Ovviamente un estere può reagire con un altro alcol per dare una reazione di transesterificazione in presenza di un acido
Per questa ragione non è mai una buonaidea conservare un estere in un solventealcolico

Sulla base di quanto abbiamo visto fino ad ora siete in grado di anticipare se Sulla base di quanto abbiamo visto fino ad ora siete in grado di anticipare se un’ammide può essere sintetizzata a partire da un estere?un’ammide può essere sintetizzata a partire da un estere?
Non servono due equivalenti di Non servono due equivalenti di ammina perché non si libera un acidoammina perché non si libera un acido
Sulla base di quanto visto nella tabella dellereattività come si comporterà un tioestere?I tioesteri sono quasi tanto reattivi quanto le anidridi e i cloruri degli acidi e sono usati in ambitobiochimico come un “equivalenti sintetici” di un cloruro di un acido

Effetti di risonanzaEffetti di risonanzaEffetti induttiviEffetti induttivi
La presenza di due gruppi La presenza di due gruppi elettronegativi rende l’atomo di elettronegativi rende l’atomo di carbonio altamente carbonio altamente elettrofilicoelettrofilico
Minore contributo Minore contributo all’ibrido di risonanzaall’ibrido di risonanza
TioesteriTioesteri in sistemi biologiciin sistemi biologici
Piruvato acetil coenzima A il tioestere di un acido grasso(n è di solito 15)
Molti passaggi Molti passaggi
Coenzima A

Biosintesi dei Biosintesi dei fosfolipidi (ffosfolipidi (formazione ormazione di esteri in sistemi di esteri in sistemi biologici)biologici)
DiidrossiacetoneDiidrossiacetonefosfatofosfato TioestereTioestere ((CoACoA--SHSH) )
Sito attivo dell’enzima Sito attivo dell’enzima diidrossiacetonediidrossiacetone fosfato fosfato
aciltransferasiaciltransferasi
fosfatofosfato TioestereTioestere ((CoACoA--SHSH) ) di un acido grassodi un acido grasso
Intermedio tetraedricoIntermedio tetraedrico
Formazione dell’estereFormazione dell’estere

Triacil glicerolo (un grasso)
Diacil glicerolo fosfato
Molti passaggi
Molti passaggi
ESERCIZIOESERCIZIO
In laboratorio i tioesteri si preparano per reazione di un acilcloruro e tioli. Sulla base
delle vostre conoscenze riguardo la formazione degli esteri proponete un meccanismo
ragionevole per la sintesi del propiltioacetato a partire dall’acetil cloruro e l’1-
propantiolo

La conversione dei derivati degli acidi carbossilici in acidi carbossilici: idrolisiLa conversione dei derivati degli acidi carbossilici in acidi carbossilici: idrolisi(ambiente basico)(ambiente basico)
Dopo l’idrolisi basica bisogna trattarecon acido per ottenere l’acidocarbossilico dal carbossilato
Questa reazione si chiama “saponificazione” perchè è un modo per convertire gliesteri degli acidi grassi in carbossilati degli acidi a catena lunga (saponi)

Idrolisi di ammidi in ambiente basico(è (è una reazione molto più lenta di quella di un estere!)
Questa specie è una base forte e Questa specie è una base forte e quindi un cattivo gruppo uscentequindi un cattivo gruppo uscente
L’idrolisi basica di cloruri e anidridi è invece una reazione molto veloce (perché?)

L’idrolisi dei L’idrolisi dei derivati derivati degli degli acidi carbossilici acidi carbossilici può essere condotta anche può essere condotta anche in in ambiente acidoambiente acido
Il processo è esattamente Il processo è esattamente l’opposto della sintesi acido l’opposto della sintesi acido catalizzata degli esteri.catalizzata degli esteri.
Per spostare l’equilibrio a destra Per spostare l’equilibrio a destra si effettua la reazione in si effettua la reazione in
presenza di acquapresenza di acqua

L’idrolisi L’idrolisi di ammidi in ambiente di ammidi in ambiente acido è più veloce della reazione in acido è più veloce della reazione in ambiente basico. Perché?ambiente basico. Perché?
Il carbonio carbonilico non è un buonelettrofilo perchè la formula di risonanzapiù importante non ha una carica positivasu quell’atomo
La protonazione lo trasforma in unaspecie più elettrofila

Come catalizza un enzima l’idrolisi di un legame ammidico (di una proteina)?
Acido asparticoAcido aspartico
istidinaistidina serinaserina
EnzimaEnzima
Il trucco è la stabilizzazione dello statodi transizione mediantelegami ad H
Vi sono vari gruppifunzionali nel sitocatalitico dell’enzima
L’enzima Chimotripsina (una proteasi serinica) è un esempio specifico
Questo è il suo Questo è il suo substratosubstrato
legami ad H
Legame scissile

Prima si forma il complesso Enzima-Substrato
Successivamente l’OH di una serina funge da nucleofilo
Per arrivare all’intermedio tetraedrico

Un gruppo protonato (un imidazolo) funge daacido e trasferisce un protone all’N peptidicotrasformandolo in un buon gruppo uscente;Il prodotto che si ottiene è un estere dellaserina (non è ancora il prodotto di idrolisi)
Nuovo peptide Nuovo peptide NN--terminaleterminale

Intermedio tetraedrico
La vera idrolisi avviene in questa serie di passaggi;Questa volta a reagire è un estere! E’ una reazionepiù facile dell’idrolisi di una ammide.

Ancora una volta è un imidazolo protonatoa facilitare l’uscita del gruppo uscente

Come si sintetizza un peptide in laboratorio?
= dicicloesilcarbodiimmide
= dicicloesilurea
Nella sintesi posso usareun ammino acido senzaprecauzioni?1. Un ammino acido
possiede sia un gruppocarbossilico che unaammina;
2. Bisogna “proteggerli” a turno;
3. Bisogna “liberarli” quando si vuole farlireagire