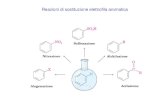
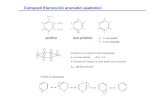
Proprietà dei SOSTITUENTI legati ad ANELLI ETEROCICLICI La reattività dei SOSTITUENTI può essere...
-
Upload
ennio-pippi -
Category
Documents
-
view
228 -
download
1
Transcript of Proprietà dei SOSTITUENTI legati ad ANELLI ETEROCICLICI La reattività dei SOSTITUENTI può essere...

Proprietà dei SOSTITUENTI
legati ad ANELLI ETEROCICLICI
La reattività dei SOSTITUENTI può essere notevolmente influenzata dalla NATURA
dell’eterociclo e dalla POSIZIONE nell’anello

Z N
N
N N
O
S N
R
> > >> >≥
Influenza degli anelli eterociclici sulla reattività dei sostituenti

Sostituenti
ALOGENI: vengono sostituiti più facilmente dai nucleofili
-NH2: i sali di diazonio sono meno stabili (tranne che per gli N-
ossidi)
-CH3: più “attivo” (CH2- viene stabilizzato). Utile nelle applicazioni
sintetiche
-CH=CH2: l’addizione di Michael è più favorita

Anelli benzenici fusi:
-reazioni con elettrofili
N
S
N
O
minore
maggioreminore
maggiore
(più aromatico è l’anello, maggiore è la probabilità che l’elettrofilo vada in α)

Anelli benzenici fusi:
-reazione di ossidazione
N COOH
COOH
N
COOH
COOH

Anelli benzenici fusi:-effetto della sostituzione sull’anello benzenico
N
NO2
N
NO2
N
OMe
N
HO

Alchil gruppi (reattività simile al toluene):
-l’ossidazione con KMnO4, CrO3 dà i corrispondenti acidi carbossilici o chetoni
-bromurazione radicalica con N-bromosuccinimmide:
N
O
H3C
H3C
ClN
O
H3C
BrH2C
Cl
NBS
N
O
R
R
H3CN
O
R
R
BrH2C
NBS

Ammino gruppi:
-attacco da parte di elettrofili:
ad N eteroaromatico: H+, Met+, RX (facile e reversibile)ad NH2: RCOCl, HNO2, RNO, NO2
+
ad β-C: Cl +, NO2+, SO3 (difficile e
irreversibile)
Reazioni in competizio
ne
N NH2
E+
E+
E+

Ammino gruppi: competizione fra l’azoto esociclico e quello endociclico nelle reazioni di metilazione e ossidazione
N NMe
Me
RCO3H
N NMe
MeO
MeI
N NMe
MeMe
I-
N
N
Me
Me
RCO3HN
N
Me
Me
O
MeI
N
N
Me
Me
Me
I-
N
N
Me Me
RCO3HN
N
Me Me
O
MeI
N
Me
I-
N
Me Me
imped. sterico

N Y HO
Me
Y H
Z Y H
Reattività in catena laterale di sostituenti adiacenti all’azoto piridinico (vedi gruppi adiacenti al carbonile): perdita di un protone
-OH: sono acidi (confronta con gli acidi carbossilici)-NH2: sono meno basici (confronta con le ammidi)-alchili: sono “attivi” (confronta con gli alchil chetoni)

Tautomeria:
N YH NH
Y
-OH: esiste per circa il 99% nella forma piridone (confronta con gli ac. carboss.)-NH2: esiste per circa lo 0.1% nella forma piridoimmina (confronta con le ammidi)-SH: esiste per circa il 99.9% nella forma piridotione (confronta con gli ac. tiocarboss.)
O
Me
YH HO
Me
Y

Decarbossilazione:
N CH2
O
H
O
NH
CH2
Carbossimetile: decarboss. a 50° C (confronta con β-chetoacidi)
O
Me
CH2
CH2
H
O
HO
Me
CH2
NH
O H
O
NH
Me
O HO
O
Me
HO
Carbossile: decarboss. a 200° C (confronta con α-chetoacidi)

Reazione di Michael:
N CH
CH2
Nu-
N CH2
H2C Nu
N CHH2C OH N C
HCH2
Nu-
H
Vinil/Etinil-Py: subiscono R. di Michael (confronta con chetoni αβ-insaturi)
β-idrossietil Py: subiscono reaz. opposta alla R. di Michael
(confronta con β-idrossi chetoni)