Agli studenti del corso di Laurea in C.T.F. (anno accademico … · 2017-03-13 · transmembrana...
Transcript of Agli studenti del corso di Laurea in C.T.F. (anno accademico … · 2017-03-13 · transmembrana...

Agli studenti del corso di Laurea in C.T.F. (anno accademico 2016-17)
Questo file riguarda argomenti selezionati delle lezioni del corso di Farmacologia
Generale e Farmacoterapia I.
Si raccomanda agli studenti (come più volte sottolineato durante le lezioni) di usare
questo materiale solo come aiuto/guida alla preparazione del relativo esame di
Farmacologia Generale e Farmacoterapia I.
Si rammenta, infatti, che l’USO dei TESTI di Farmacologia consigliati (ad esclusiva
scelta dello studente) è indispensabile per una corretta, utile e più facile
preparazione della materia.
Si precisa che il programma completo per la preparazione dell’esame è sempre
reperibile presso la segreteria della Sezione di Farmacologia.
Gli studenti sono tenuti a svolgere tutti gli argomenti indicati nel programma
anche se non compresi nel materiale didattico utilizzato a lezione.
Infine, si mettono in guardia gli studenti dall’uso di fotocopie di materiale didattico
(presunte stampe delle lezioni contenute nel cd) ABUSIVAMENTE vendute presso le
copisterie.
Le figure utilizzate nelle lezioni sono quelle dei libri di testo consigliati o sono immagini copyright-free da siti web specializzati

FARMACOLOGIA GENERALE
Farmacodinamica Studio del meccanismo d’azione dei farmaci a livello molecolare, cellulare e di tessuto
•Bersagli cellulari dell’azione dei farmaci •Interazione farmaco-recettore •Attività intrinseca di un farmaco •Meccanismi di trasduzione del segnale
Farmacocinetica Studio delle variazioni cinetiche del farmaco nell’organismo. Influenza la farmacodinamica, l’azione terapeutica e la tossicità
•Assorbimento •Distribuzione •Metabolismo •Eliminazione
Meccanismi generali che regolano l’attività biologica di qualsiasi xenobiotico !

Meccanismo d’azione dei farmaci Il meccanismo d’azione dei farmaci può essere considerato ai seguenti quattro livelli diversi :
Sistemi corporei Componenti tissutali Costituenti cellulari Molecole
Meccanismo definizione componenti della risposta Sistema Effetto sulla funzione Sistemi integrati, compresi i sistemi del sistema collegati (es. sistema nervoso, cardivas.) Tessuto Effetto sulla funzione Elettrogenesi, contrazione, secrezione, del tessuto attività metabolica, proliferazione... Cellula Trasduzione Le sostenze biochimiche legate al bersaglio del farmaco (es. canale ionico, enzima,...) Molecola Interazione con il Il bersaglio del farmaco (es. recettore, canale bersaglio molecolare ionico, enzima, molecola di trasporto) del farmaco

Ad esempio, il propranololo Farmaco utile, tra l’altro, nella cura dell’angina pectoris, una condizione risultante da ischemia relativa (cioè, flusso coronarico insufficiente) in una porzione del cuore.
Sistema : Prop riduce la risposta normale del cuore a incrementi dell’attività del sistema nervoso simpatico (aumento del ritmo e della forza di contrazione cardica)
Tessuto : Prop riduce la forza contrattile cardiaca e il ritmo cardiaco (inotrop e
cronotropo negativo) in conseguenza del blocco delle azioni dei neurotransmettitori rilasciati dal sistema nervoso simpatico cardiaco.
Cellulare : Prop previene l’innalzamento dell’adenosin monofosfato ciclico (cAMP) intracellulare, della fosforilazione delle proteine, della mobilitazione del calcio e del metabolismo ossidativo indotto dall’attività del sistema nervoso simpatico.
Molecolare : Prop agisce per antagonismo competitivo, reversibile, del legame
dell’adrenalina e noradrenalina agli adrenorecettori b1.

RECETTORI FISIOLOGICI PER I FARMACI
Le cellule, vicine o distanti tra loro, comunicano attraverso molecole (MEDIATORI o NEUROTRASMETTITORI, ORMONI, AUTACOIDI) che si legano a macromolecole nella cellula ricevente (RECETTORI)
1. RECETTORI DI MEMBRANA
2. RECETTORI INTRACELLULARI

I diversi recettori mediano funzioni cellulari per mediatori di diversa natura
e con tempi differenti

RECETTORI FISIOLOGICI: Sensori nel
sistema di comunicazioni chimiche
che coordinano le funzioni dei gruppi
cellulari dell’organismo.
Legano in modo specifico e con
elevata affinità i mediatori endogeni,
subendo trasformazioni
conformazionali da cui scaturiscono
gli effetti biologici
MOLTE FAMIGLIE
In ciascun tipo di recettore fisiologico
possiamo distinguere 2 domini:
1. Dominio di legame con il ligando
2. Dominio per l’effettore
Azioni:
Diretta sul bersaglio cellulare (proteina
effettrice)
Mediata da molecole “intermediarie”
(trasduttori)

Trasducono il segnale portato da mediatori idrofilici (neurotrasmettitori classici e peptidici, fattori di crescita, citochine, ecc)
Trasducono il segnale generando modificazioni biofisiche e biochimiche della cellula
RECETTORI DI MEMBRANA

Sono divisi in 4 famiglie:
RECETTORI – CANALE
RECETTORI ACCOPPIATI ALLE PROTEINE G
RECETTORI DOTATI DI ATTIVITA’ TIROSIN CHINASICA
INTRINSECA
RECETTORI DOTATI DI ATTIVITA’ GUANILATO
CICLASICA INTRINSECA
RECETTORI DI MEMBRANA

CANALI IONICI
•Canali ionici operati dal voltaggio
•Canali operati da ligandi Recettori canale Canali operati da 2ndi messaggeri, proteine G, prodotti metabolici
•Canali operati da stimoli sensoriali Canali meccanosensibili
Canali attivati da fotoni o agenti chimici odoranti e gustativi (spesso
mediante 2ndi messaggeri)

Sono dei complessi macroproteici transmembranari che formano un canale ionico (aperto dal legame con il neurotrasmettitore o con farmaci agonisti)
La loro attivazione determina dei rapidi cambiamenti delle concentrazioni ioniche intracellulari e del potenziale elettrico transmembranario
1° classe RECETTORI DELLA SUPERFAMIGLIA DEI RECETTORI NICOTINICI (recettore nicotinico muscolare e neuronale, recettore GABAa, recettore della glicina e recettore 5HT3 serotonina
2° classe RECETTORI IONOTROPI PER IL GLUTAMMATO (recettori NMDA, AMPA e Kainato)
3° classe RECETTORI APERTI DA NUCLEOTIDI CICLICI (recettori cAMP e cGMP)
4° classe RECETTORI IONOTROPI DELL’ATP (P2X)
RECETTORI CANALE

RECETTORI CANALE
Oligomeri formati da 3, 4 o 5 subunità che si organizzano a formare un poro
canale per cationi o per anioni (GABAa e glicina) La loro apertura può determinare
depolarizzazione o iperpolarizzazione
La 1° classe è
composta da pentameri
ed ogni subunità è
formata da 4 segmenti
transmembrana.
Il segmento M2 di ogni
subunità forma la parete
del poro idrofilo.
Nella 2° classe i recettori sono
tetrameri in cui il segmento M2 è
sostituito da un segmento P. L’apertura
del canale avviene
quando il ligando si lega a ciascuna
subunità
Le anse citoplasmatiche tra
M3 ed M4 siti di consenso per
fosforilazione da PKA e PKC
che controllano cinetica e
desensitizzazione

QuickTime™ and a TIFF (Uncompressed) decompressor are needed to see this picture.
Topologia dei canali “Cys-Loop”
Cys
Cys
Modified from Ashcroft, Ion Channels and Disease,
Academic Press (2000)
Keramidas et al., Prog. Biophys. Mol. Biol.
86: 161 (2004)

1a classe Recettore nicotinico
RECETTORI CANALE
Il legame di due molecole di Ach
determina l’apertura del canale
cationico (entra Na+ ed esce
K+)e la depolarizzazione di
membrana
•Elevata espressione nella placca
neuromuscolare : 50 milioni •Pentamero: a2bgd o e (nel muscolo adulto) con omologia dal 40 ad 80% •Elevata affinità a-bungarotossina, che ne ha permesso identificazione, purificazione e isolamento. •Recettore nicotinico neuronale, gangliare e SNC : pentameri formati solo da subunità a e b, con diversa stechiometria
Le isoforme di subunità a influenzano la selettività ionica: ad esempio a1 sodio; a7 calcio

Recettore nicotinico
Subunità a: identico sito di legame per Ach; le altre subunità influenzano la farmacologia

b
a
ACh
g (or e)
d ACh
Pentamero di subunità
proteiche con due siti di
legame per acetilcolina
che, quando legata altera
la conformazione del
recettore e causa
l’apertura del poro canale.
Il poro permette l’ingresso
di ioni Na+ che entrano in
cellula secondo gradiete
elettrochimico
Recettore nicotinico

nAChR: registrazione da singolo canale
Ashcroft, Ion Channels and Disease. Academic Press (2000) Clementi – Fumagalli IV edizione

Filtro di selettività
Acidic Residues
Gate Region
Modified from Keramidas et al., Prog. Biophys. Mol. Biol. 86: 161 (2004)

Modello di gating di nAChR: rotazione di eliche M2
Polar Ser or Thr (Selectivity Filter) Hydrophobic Leu (Gate)
OPEN CLOSED
Modified from Zigmond et al. (Eds.) Fundamental Neuroscience, Sinauer (1999)

RECETTORI CANALE GABA A
2a 2b 1g Sito di legame su subunità b all’interfaccia con la a



Filtro di selettività
Basic Residues
Gate Region
Modified from Keramidas et al., Prog. Biophys. Mol. Biol. 86: 161 (2004)

I recettori-canale presentano anche siti di regolazione della loro funzione che sono importanti bersagli dell’azione dei farmaci

Benzodiazepine e Barbiturici aumentano le correnti
GABAA attraverso meccanismi differenti
Open Time
Probability
of Opening
Twyman et al (1989) Ann. Neurol. 25: 213-220 (1989)

2° CLASSE Recettori ionotropi per il glutammato: NMDA, AMPA*, kainato
Coinvolti in diversi aspetti (fisiologici e patologici) della neurotrasmissione eccitatoria
Glicina: co-agonista
Poliamine: modulatori positivi
PCP (fenciclidina ed altri
anestetici dissociativi): antagonisti
Mg2+ : bloccante del canale
*alfa-Amino-3-Idrossi-5-Metil-4-isoxazolone propionato

3° CLASSE Recettori-canale aperti da nucleotidi ciclici
Eterotetrameri. Ciacuna subunità è formata da 6 segmenti transmembrana con struttura simile a quella dei canali cationici voltaggio dipendenti. Siti di legame cAMP o cGMP intracellulari. Implicati nella trasduzione di stimoli olfattivi o visivi

Omotrimeri di 7 differenti subunità (P2X1-7) formati da due segmenti transmembrana. Poro selettivo ai cationi (calcio +/- sodio)
4° CLASSE Recettori ionotropi per ATP

RECETTORI ACCOPPIATI ALLE PROTEINE G
Unica catena polipeptidica che attraversa sette volte la membrana tre loops extracellulari e tre intra. Diversi sistemi effettori: Enzimi Canali ionici Proteine di trasporto
Recettori di membrana che trasducono il segnale di moltissimi mediatori e sono il bersaglio di numerosi farmaci agonisti ed antagonisti
GPCR: G protein coupled receptors

RECETTORI ACCOPPIATI ALLE PROTEINE G
Premio Nobel 2012
Robert J. Lefkowitz
Howard Hughes Medical Institute and Duke University Medical Center, Durham, NC, USA
and
Brian K. Kobilka
Stanford University School of Medicine, Stanford, CA, USA
"for studies of G-protein–coupled receptors"
The studies by Lefkowitz and Kobilka are crucial for understanding how G-protein–coupled
receptors function. Furthermore, in 2011, Kobilka achieved another break-through; he and his
research team captured an image of the β-adrenergic receptor at the exact moment that it is
activated by a hormone and sends a signal into the cell. This image is a molecular
masterpiece – the result of decades of research.

RECETTORI ACCOPPIATI ALLE PROTEINE G
Modello schematico di disposizione spaziale dei recettori accoppiati
a proteine G e diverse strategie di interazione con ligandi (Clementi – Fumagalli IV edizione)

Le proteine G sono una famiglia di molecole proteiche, chiamate così per la loro interazione con i nucleotidi guaninici GTP e GDP
Ogni proteina G è formata da 3 subunità (a, b e g)
20 isoforme di subunità a
6 isoforme di subunità b
12 isoforme di subunità g
N.B. la diversa composizione regola la selettività di accoppiamento tra proteine G e recettori
GTP e GDP si legano alla subunità a, che ha attività GTPasica intrinseca
(GTP -> GDP)
b e g sono
-associate a formare il complesso bg
-idrofobiche
-ancorate alla superficie citoplasmatica della membrana
RECETTORI ACCOPPIATI ALLE PROTEINE G

Le proteine G sono coinvolte nella trasduzione del segnale all’interno della cellula in seguito all’attivazione recettoriale
Ciclo del meccanismo di trasduzione: Legame agonista con recettore e cambio di conformazione Aumento affinità per proteina G (3° loop citoplasmatico e COOH terminale) Distacco GDP e legame del GTP Distacco a-GTP da bg
Azione su effettori (enzimi, canali ionici) Azione GTPasica determina idrolisi del GTP in GDP e formazione del eterotrimero

RECETTORI ACCOPPIATI ALLE PROTEINE G
La subunità a possiede attività GTPasica intrinseca: spegnimento del segnale

RECETTORI ACCOPPIATI ALLE PROTEINE G
Trasduzione del segnale delle proteine G (Clementi – Fumagalli IV edizione)

LE PROTEINE G
GS (as) Noradrenalina (b), dopamina (D1-D5), adenilatociclasi ( AMPc) 5-HT,glucagone, etc. canali del calcio (attivati)
Gi1,Gi2,Gi3 Noradrenalina (a2), Ach (M2, M4), adenilatociclasi ( AMPc) 5-HT, oppioidi, dopamina (D2) apertura canali K+ (GIRK (ai) e molti altri frequenza cardiaca)
Gq ACh (M3), 5-HT, noradrenalina (a) fosfolipasi C ( IP3, DAG, (aq) Vasopressina (V1), etc calcio citoplasmatico)
Go neuromodulatori e neurotrasmettitori canali al calcio (inibiti) (ao) (meno caratterizzati)
Gt fotoni (rodospina), odoranti GMPc (fototrasduzione)
Recettori per: Effettori
Generalmente classificate sulla base del tipo di subunità a e del sistema effettore modulato
Effettori di subunità bg: canali al potassio (GIRK, PLC, cascate enzimatiche)

I RECETTORI ACCOPPIATI A PROTEINE Gs e Gi HANNO EFFETTI OPPOSTI SULL’ADENILATO CICLASI
L’AMP ciclico modula l’attività della proteina chinasi A e quindi la fosforilazione (su residui di serina e tronina) di vari bersagli cellulari. I livelli di cAMP vengono poi successivamente ridotti dagli enzimi fosfodiesterasi (bersagli dell’azione di farmaci ad esempio metil-xantine)
(Clementi – Fumagalli IV edizione)

Diversi effetti cellulari mediati da PKA-AMPc dipendente in diversi tessuti
Aumento attività canale del calcio voltaggio dipendente: aumento contrazione cardiaca
Azione su enzimi metabolici: aumento disponibilità di glucosio
Fosforilazione ed inibizione MLCK (chinasi catena leggera della miosina):
Rilassamento muscolatura liscia

L’aumento di AMPc modula la trascrizione genica
La PKA attivata entra nel nucleo e fosforila dei fattori di Trascrizione quali CREB (cAMP Response Element Binding protein). Il CREB fosforilato forma un complesso con CBP (CREB Binding Protein) e lega il DNA sui siti di riconoscimento per CREB stimolando la trascrizione genica
Molecular Biology of the Cell, 2002

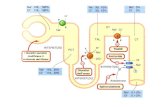
GPCR legati a proteine Gq Attivazione di Fosfolipasi C
La fosfolipasi Cb (PLCb) catalizza l’idrolisi di PIP2 Formazione di 2 secondi messaggeri
IP3 e DAG
**
**

Il calcio può essere considerato il 3° messaggero
Il legame alla calmodulina stimola la Chinasi Ca++/calmodulina dipendente che
è implicata in cascate fosforilative che modulano diverse funzioni cellulari

Effetti a lungo termine:
Trascrizione genica attivata da proteina
kinasi C
Two Independent Pathways
Molecular Biology of the Cell, 2002
MAPKinasi: Chinasi attivata da mitogeni NF-kB: Fattore Nucleare-kB
DAG e calcio attivano proteine kinasi C calcio e fosfolipidi dipendenti (serina treonina kinasi). Le PKC fosforilano e modulano la funzione di diverse proteine cellulari, quali enzimi, canali ionici etc.

Ciclo del fosfoinositolo


Sistema di amplificazione del segnale



Proteine G monomeriche
•Piccole proteine intracellulari (20-40 kD) in grado di legare ed idrolizzare il GTP
•Attività indipendente dall’attivazione dei classici GPCR ma spesso dovuta all’attivazione di altri tipi recettoriali (ad es. Recettori-kinasi)
•Lo scambio GDP-GTP (attivazione) è regolato da interazione con specifiche proteine, quali ad esempio SOS
•Le proteine G monomeriche attivate interagiscono con sistemi effettori intracellulari
Ras: Attivazione della cascata MAP chinasi ERK-1 e 2
Rap-1: inibitore di Ras e attivazione MAP chinasi ERK-1 e 2 Ras indipendente
Rac: Controllo risposta a stress cellulare (apoptosi da MAP kinasi JNK)
Rab: Trasporto e esocitosi vescicole
Rho: Assemblaggio del citoscheletro
ARF: Assemblaggio apparato Golgi
EF-2: Regolazione sintesi proteica nei ribosomi
Ran: Scambio di RNA e proteine tra nucleo e citoplasma

RECETTORI AD ATTIVITA’ ENZIMATICA
Recettori con attività tirosin-chinasica intrinseca Enzimi regolati da ligandi endogeni Recettori per ormoni peptidici (insulina) e per fattori di crescita (IGF; VEGF; PDGF). Regolano attività metaboliche nonchè crescita, differenziazione sviluppo
Dominio extracellulare: responsabile del
legame al ligando endogeno
Dominio intracellulare: attività catalitica
uniti da una corta sequenza transmembrana
Attivazione recettoriale determina l’attivazione dell’attività enzimatica ed il trasferimento di gruppi fosfato su residui di tirosina
Diverse sottofamiglie (almeno15) classificate sulla base del grado di omologia dei dominii extracellulari
Patologie dovute ad alterazione nei recettori e/o nei sistemi di trasduzione

RECETTORI CON ATTIVITA’ TIROSIN-CHINASICA RECETTORI AD ATTIVITA’ ENZIMATICA
Dominio extracellulare: maggiore variabilità rappresenta il sito di riconoscimento per il ligando. Altamente glicosilato possiede numerosi residui di cisteina Dominio transmembrana: circa 25 AA idrofobici funge da connettore. Oltre al Ruolo strutturale può anche modulare l’attività chinasica Dominio iuxtamembrana: circa 50 AA ed ha funzioni regolatorie Dominio catalitico: responsabile di attività chinasica circa 250 AA conservati Coda C terminale: lunghezza e funzioni variabili. Nel recettore attivato lega i trasduttori intracellulari
Legame del ligando determina dimerizzazione del recettore. Stabilizzazione dello stato attivo della chinasi e trans-autofosforilazione del recettore sui residui di tirosina all’interno e all’esterno del dominio catalitico (zona iuxtamembrana e coda C-terminale)
Clementi – Fumagalli IV edizione

RECETTORI AD ATTIVITA’ ENZIMATICA
Recettore dell’ Insulina è sempre un dimero: due subunità a (135 kD) due subunità b (95kD) legate tra loro da ponti disolfuro
La trans-autofosforilazione sui residui di tirosina porta alla formazione di siti di ancoraggio riconosciuti dai trasduttori citoplasmatici del segnale contenenti specifici domini.
I trasduttori sono proteine che si possono ancorare ad alta affinità al recettore fosforilato perchè posseggono specifiche sequenze (SH2 e/o PTB) che riconoscono le tirosine fosforilate.
Alcune delle proteine SH2 hanno attività enzimatica (PLCg), altre sono proteine modulatorie prive di attività enzimatica (Grb2, Shc)
Nel caso del recettore per l’insulina, il recettore fosforilato viene riconosciuto e legato da IRS (insulin-receptor substrate)

RECETTORI AD ATTIVITA’ ENZIMATICA

Effetti cellulari di fattori di crescita

Organi bersaglio: Fegato, Muscolo scheletrico, Cellule adipose. Gli effetti metabolici prevedono la stimolazione delle vie che utilizzano il glucosio (aumento glicolisi, glicogenesi, sintesi di glicerolo), la sintesi di trigliceridi ed acidi grassi e la sintesi proteica. Gluconeogenesi, glicogenolisi e lipolisi sono inibite
Effetti cellulari dell’insulina

RECETTORI AD ATTIVITA’ ENZIMATICA
Approcci farmacologici: Intensa ricerca in considerazione del coinvolgimento di alcuni di questi recettori in disturbi metabolici e in processi tumorali
Inibitori interazione ligando-recettore Anticorpi monoclonali contro epitopi extracellulari dei recettori per fattori di crescita Herceptin : anticorpo recettore EGF Avastin : anticorpo recettore VEGF (inibitore di angiogenesi) Inibitori attività catalitica tirosin-chinasica • Composti naturali (quercetina, genisteina) mimano il composto intermedio che si forma tra ATP ed il residuo di tirosina durante la reazione chinasica (molto tossici) • Composti di sintesi (gefitinib per EGRF; PTK787 per VEGFR; etc) Inibitori della farnesil-transferasi: enzima che catalizza la farnesilazione di Ras

RECETTORI AD ATTIVITA’ ENZIMATICA
Clementi – Fumagalli IV edizione

1. Recettori chinasici che agiscono fosforilando i residui di serina e treonina:
Recettore per TGF-b
2. Recettori con altre attività enzimatiche
Dominio intracellulare è una guanilciclasi che sintetizza GMP ciclico che
agisce come 2° messaggero
Recettore per il peptide natriuretico atriale
RECETTORI AD ATTIVITA’ ENZIMATICA
3. Recettori chinasici senza dominio catalitico
intracellulare: legano o attivano chinasi di
membrana o citoplasmatiche.
• Recettori per citochine
• Recettori per peptidi neurotrofici
• Recettori per antigeni a subunità multipla sui
linfociti T e B

RUOLO CENTRALE DELLE CHINASI NELLE VIE DI TRASDUZIONE DEL SEGNALE

RECETTORI INTRACELLULARI
Trasducono il segnale portato da ormoni e da altri mediatori lipofilici
Interagiscono con il genoma, modificando l’espressione genica e quindi la composizione proteica della cellula, senza cascate di eventi ionici o metabolici
Distribuzione eterogenea:
Estrogeni, progesterone, ormone tiroideo, vitamina D, acido retinoico: recettore nucleare
Mineralcorticoidi, glucocorticoidi: recettori citoplasmatici che entrano nel nucleo quando sono attivati
La condizione necessaria è che il ligando superi la membrana cellulare grazie alla sua lipofilia. Il legame tra ormone e recettore permette il legame al DNA e quindi l’attivazione o la repressione della trascrizione genica

RECETTORI INTRACELLULARI
Il recettore per i gluococorticoidi è il prototipo di recettore intracellulare
L’ormone entra in cellula, lega il recettore e rimuove il legame di proteine inibitorie (heat shock proteins) Il complesso recettore-ormone dimerizza migra nel nucleo e lega il DNA ad una sequenza (glucocorticoid response elements GRE) a monte di promotori di specifici geni di cui regolano l’attività in senso positivo o negativo

RECETTORI INTRACELLULARI
I recettori intracellulari sono costituiti da una catena polipeptidica che contiene due domini: Dominio di dimerizzazione e legame all’ormone: porzione COOH terminale Dominio di legame al DNA: formato da circa 70 AA, caratterizzato dalla presenza di numerose cisteine che legano lo Zn2+ mediante un legame di coordinazione “zinc-binding finger”: caratteristico di proteine che legano il DNA

RECETTORI INTRACELLULARI
Recettori per glucocorticoidi Distribuiti nella maggior parte dei tessuti Due isoforme: forma a: 777 AA legante i glucocorticoidi forma b: 742 AA che non lega i glucocorticoidi ma compete per il legame al DNA RG non occupato è complessato a più proteine HSP quali HSP90, HSP70 e HSP56. I RG attivano la trans-attivazione di diversi geni ed aumentano l’espressione di varie proteine: Annessina 1 (o lipocortina): inibitore di fosfolipasi A2 Ikb: fattore inibitorio di NF-kB, fattore di trascrizione di geni pro-infiammatori Sul DNA sono anche presenti sequenze negative nGR. In questo caso il legame di GR impedisce la trascrizione. Queste interazioni reprimono l’espressione di citochine, COX, NOS, PLA2.

Difetti genetici possono compromettere la funzione dei recettori intracellulari
• Riduzione del numero di recettori • Ridotta capacità di legare l’ormone • Ridotta capacità di dimerizzare • Ridotta affinità per il DNA

RECETTORI NUCLEARI
PPAR: Peroxisome-Proliferator-Activated Receptor
3 isoforme codificate da geni differenti
PPARa : Fegato, muscolo, rene e cuore (stimola la beta-ossidazione degli acidi grassi)
vasi e macrofagi
PPARg : Intestino, vasi macrofagi, tessuto adiposo (stimola la differenziazione degli adipociti)
PPARb/d: meno noto
Dominio A/B ; Dominio C (legame al DNA)
Regione D centrale (variabile), Dominio E (legame ligando)

RECETTORI NUCLEARI
Dopo stimolazione da ligando, il PPAR si lega con RXR (recettore per i retinoidi) e
dimerizza.
Il complesso PPAR-RXR riconosce uno specifico sito di legame sul DNA (PPRE: sequenza
AGGTCA).
Segue variazione conformazionale del DNA con stimolazione/inibizione trascrizione geni
bersaglio


Inhibition of trascription of
pro-inflammatory genes

MODULAZIONE DELLA RISPOSTE RECETTORIALI
DESENSIBILIZZAZIONE
DESENSITIZZAZIONE
riduzione della capacità di un recettore di trasdurre il segnale, anche se legato all’agonista (riduzione affinità o dell’efficienza del sistema di trasduzione
DOWN – REGULATION
Riduzione del numero di recettori
Fenomeno in base al quale l’esposizione persistente ad un agonista porta a riduzione dell’effetto biologico atteso: responsabile del fenomeno di tolleranza
Il fenomeno opposto (aumento di sensibilità ad un agonista) prende il nome di “ipersensibilità” e può essere dovuto asd un aumento di espressione dei recettori (up-regulation). Si osserva spesso dopo trattamenti prolungati con antagonisti

La desensitizzazione può essere omologa o eterologa e coinvolge processi di fosforilazione del recettore. Il fenomeno è stato ampiamente caratterizzato per o recettori accoppiati a proteine G