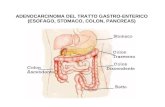
TUMORE DELL APPARATO GASTRO-ENTERICO COLON-RETTO Michele Reni Dipartimento Oncologico Ospedale S....
-
Upload
rosalba-tosi -
Category
Documents
-
view
221 -
download
6
Transcript of TUMORE DELL APPARATO GASTRO-ENTERICO COLON-RETTO Michele Reni Dipartimento Oncologico Ospedale S....

TUMORE DELL’
APPARATO GASTRO-ENTERICO
COLON-RETTO
Michele Reni
Dipartimento Oncologico
Ospedale S. Raffaele - Milano

EPIDEMIOLOGIA

EPIDEMIOLOGIA

CANCRO DEL COLON-RETTO
dimensioni del problemaNuovi casi/anno
783.000 nel mondo150.000 in Europa35.000-40.000 in Italia
Morti/anno437.000 nel mondo95.000 in Europa18.000 in Italia

Eziologia del CRC:fattori ambientali
Increased Incidence Decreased Incidence
High-calorie diet Antioxidant vitamin consumption
High red meat consumption Consumption of fresh fruit and vegetables
Overcooked red meat consumption Use of nonsteroidal antiinflammatory drugs
High saturated fat consumption High-calcium diet
Cigarette smoking; Excess alcohol consumption
Sedentary lifestyle
Obesity
Note: Coffee or tea consumption has no effect on incidence.

Fattori di rischio ambientali• Rischio 4 volte > nei Paesi avanzati rispetto ai meno
evoluti• Sesso: un soggetto maschile ha una probabilità di
ammalare del 4,5% rispetto al 3,2% di uno di sesso femminile.
• Stili di vita: condizionano lo sviluppo del cancro in tempi diversi (sovrappeso e obesità, dieta ipercalorica, scarsa attività fisica, massa corporea, dieta)
• Consumo di elevate quantità di grassi ed una assunzione ridotta di fibre vegetali, alto consumo di carni rosse e grassi animali.
• Ridotto consumo di folati associato ad alto consumo di alcol e al fumo di sigaretta incrementano il rischio di adenomi

POLIPI COLORETTALI ED ALTRI FATTORI DI RISCHIO
Il rischio di evoluzione verso la forma cancerosa dipende:
* istotipo villoso (T 75%, T-V 20%, V 5%)
* dimensioni del polipo (diametro > 1 cm: 3% a 5 anni,
8% a 10 anni, 25% a 20 anni)
* numero di polipi (rischio maggiore per i polipi
multipli)
* grado di displasia

POLIPOSI FAMILIARE
• Numerose formazioni polipoidi
• Il tratto fenotipico si manifesta fra i 10-15 anni
• I familiari di I grado hanno un elevato rischio
(circa 50%) di contrarre la malattia e vanno
sottoposti a controlli endoscopici dall’età di 12-
16 anni. Posta la diagnosi il trattamento di scelta
è chirurgico.
• Se non trattata la FAP evolve verso lo sviluppo di
un cancro nel 100%

HNPCCLa diagnosi di HNPCC va sospettata in base
ai criteri di Amsterdam :* almeno tre parenti con carcinoma del
colon-retto documentato istologicamente* almeno due generazioni successive affette* in uno degli individui affetti,diagnosi
posta prima dei 50 anni di età• Si associano criteri minori come: * prevalente localizzazione del tumore nel
colon destro * frequente associazione di carcinomi
dell’endometrio, dello stomaco, dell’apparato urogenitale e dell’ovaio (S. Lynch II)

Metodiche di screening nella popolazione a rischio generico (adulti
con età >50 anni)Test American American
Cancer Society College of Gastroenterology
Hemoccult Ogni anno associato In alternativa alla colonscopia:
a sigmoidoscopia ogni 5 anni hemoccult ogni anno associato a sigmoidoscopia ogni 5 anni
Sigmoidoscopia Ogni 5 anni associata In alternativa alla colonscopia:
a hemoccult ogni anno sigmoidoscopia ogni 5 anni
con hemoccult ogni anno
TEST SANGUE OCCULTO RIDUCE IL RISCHIO DEL 15-20%

Cancro del colon
L’80% dei casi viene operato radicalmente con chirurgia di elezione (circa 24.000/anno)
Circa il 50% di questi morira’ per recidiva di malattia (circa 12.000/anno)
La chemioterapia adiuvante ogni anno evita in Italia la morte di almeno 3000 pazienti con cancro del colon

Diagnosi: sintomi• Symptoms associated with colorectal
cancer include – lower gastrointestinal bleeding
– change in bowel habits
– abdominal pain
– weight loss
– change in appetite
– weakness
– obstructive symptoms

Diagnosi: esame obiettivo
• palpable mass• bright blood through the rectum (usually left-
sided colon cancers or rectal cancer)• melena (right-sided colon cancers) • lesser degrees of bleeding (positive result on
stool test for occult blood)• Adenopathy• Hepatomegaly• Jaundice• pulmonary signs • Obstruction (usually in the sigmoid or left colon)

Complicazioni all’esordio
• Acute gastrointestinal bleeding
• Acute obstruction
• Perforation
• Metastasis with impairment of distant
organ function

Diagnosi: esami di laboratorio
• Iron-deficiency anemia
• Electrolyte derangements
• Liver function abnormalities
• CEA may be elevated and is most helpful
in postoperative monitoring if the level is
reduced to normal as a result of surgery

Esami di valutazione
• Complete history
• Family history
• Physical examination
• Laboratory tests
• Colonscopy
• Total-body CT scan

Stadiazione: TNM
• T1 tumors invade into but not through the
submucosa.
• T2 tumors invade into but not through the
muscularis propria
• T3 tumors invade through the muscularis propria
into the subserosa or into nonperitonealized
pericolic or perirectal tissue
• T4 tumors invade other named organs or structures
(T4a) or perforate the visceral peritoneum (T4b)

Stadiazione: TNM
• N0 all nodes examined are negative
• N1 includes tumors with metastasis in one to
three regional lymph nodes
• N2 indicates metastasis in four or more regional
lymph nodes. Metastatic nodules or foci found in
the pericolic, perirectal, or adjacent mesentery
without evidence of residual lymph node tissue
are regarded as being equivalent to a regional
node metastasis and are counted accordingly

Vie di diffusione
Estensione transmurale attraverso la muscolare propria nei tessuti molli pericolici o perirettali con invasione delle strutture contigue
tumori del retto: estensione in strutture pelviche (es. vagina o vescica)
Tumori del colon: si estendono alla superficie peritoneale, perforano la sierosa e determinano carcinosi peritoneale con metastasi omentali e ovariche
Altre vie di diffusione sono per via linfatica ai linfonodi locoregionali; per via ematogena principalmemente al fegato

TNM Classification of Colorectal Cancer according to AJCC-UICC
Stage T N M
0 Tis N0 M0
I T1 N0 M0
T2 N0 M0
IIA T3 N0 M0
IIB T4 N0 M0
IIIA T1–T2 N1 M0
IIIB T3–T4 N1 M0
IIIC Any T N2 M0
IV Any T Any N M1

DISEASE STAGE AT DIAGNOSIS
Stage II: 20–30%Stage II: 20–30%
Stage I: 15%Stage I: 15%
Stage III: 30–40%Stage III: 30–40%
Stage IV: 20–25%Stage IV: 20–25%
Stage II: 37%Stage II: 37%
Stage I: 17%Stage I: 17%
Not staged: 8%Not staged: 8%
Stage IV: 15%Stage IV: 15%
Stage III: 23%Stage III: 23%
USAUSA
ItalyItaly

SOPRAVVIVENZA
• TNM stadio Sopravvivenza 5 aa
• I A, B1 85-95%
• II B2 60-80%
• III C1, C2 30-60%
• IV D <10%

PRINCIPI TERAPEUTICI• Gli obiettivi terapeutici includono - Guarigione - Prolungamento della sopravvivenza - Palliazione dei sintomi - Miglioramento o preservazione della qualità di vita - Ritardo della progressione della malattia
e sintomi associati - Risposta obiettiva

Elementi per la gestione corrente della terapia del carcinoma
colorettale1. Persona (paziente)
• clinica (organi vitali, capacità personali, psiche, comorbidità) • famiglia (cultura, circostanze, altro)
2. Tumore• clinica• patologia
3. Sanitari• dottori
chirurgo (laparotomia vs laparoscopia)oncologoradioterapistaradiologo interventista
• infermieri• farmacisti
4. Organizzazione e ricerca & sviluppo farmaceutici • sistemi sanitari (nazionale vs regionale vs privato)• disponibilità dei farmaci


• Chemioterapia sistemica• Chemioterapia locoregionale• Resezione epatica o re-resezione• Tecniche ablative• Approcci misti chirurgia + terapia adiuvante chemioterapia neoadiuvante+chirurgia RF + chemioterapia
OPZIONI TERAPEUTICHE

Chemioterapici attivi• 5-Fluorouracile
• Antagonisti delle pirimidine: Capecitabina
• Farmaci che interferiscono con il catabolismo del 5FU :UFT
• Inibitori della TS: ratiltrexed
• Inibitori della Topoisomerasi: irinotecan
• Agenti alchilanti: oxaliplatino

Caratteristiche e meccanismo di azione dei nuovi farmaci
* Capecitabina: fluoropirimidina carbamato per uso orale in grado di mimare l’infusione continua di 5FU.
* UFT: combinazione di tegafur e uracile in rapporto molare 1:4 Attraverso un’inibizione della DPD aumenta i livelli intracellulari di 5FU.
* Raltitrexed: inibitore diretto e specifico della TS
* Irinotecan: inibitore della topoisomerasi I. Attivo in G2
* Oxaliplatino: agente alchilante, forma addotti intra e interfilamento. Gli addotti non sono riconosciuti dal complesso MMR. Induce maggior espressione di topoisomerasi I

OXALIPLATINO: I linea trattamento
De Gramont et al 2000
FOLFOXLVFU2
210210
50,722.3
9.06.2
16.214,7
Goldberg et al 2004
FOLFOXIFLIROX
267264264
453135
8.76.96.5
19.515
17.4
Grothey et al 2002
FUFOXBolus FU/LV
118124
48.322.6
7.95.3
20.416.1
Tournigand et al 2004
FOLFOX /FOLFIRI
FOLFIRI/FOLFOX
111
111
FOLFOX 54%FOLFIRI 4%FOLFIRI 56%FOLFOX 15%
10.9
14.2
20.6
21.5
STUDIO N pz RR% mPFS mOS

IRINOTECAN:I linea trattamento
STUDIO N pz RR% m PFS mOS
Saltz et al N Engl J Med 2000IFLBolus FU/LVIrinotecan
231226226
392118
7.04.34.2
14.812.612.0
Douillard et alLancet 2000FOLFIRIFU/LV
198187
34.821,9
6.74.4
17.414.1
Koehne et al 2003
FOLFIRIFU/LV
214216
54.231.5
8.56.4
20.116.9

FOLFOX E FOLFIRI vs.
FU+AF
0
10
20
30
40
50
60
0123456789
FU+AF FOLFIRI FOLFOX
ORR PFS
% me
si

STUDIO N9741 Bolus IFL FOLFOX OXA/CPT11 (N=264) (N=267) (N=264)
mOS 14.8 19.6* 17.4*
mTTP 6.9 8.7* 6.5
RR 31 45* 34(%)
*p:<0.05
Goldberg R. J Clin Oncol 22:23-30,2004

STUDIO NCCTG N9741
• incremento del TTP in pazienti trattati con FOLFOX rispetto a quelli trattati con IFL o con IROX
• FOLFOX: trattamento standard

CHEMIOTERAPIA MALATTIA AVANZATA
CONCLUSIONI• pz trattati in I linea con un regime di combinazione
hanno un aumento di S mediana di 3.5 mesi per cui la combinazione deve essere la terapia di I linea
• FOLFOX4 è superiore a IFL
• FOLFIRI=FOLFOX, entrambi considerati I linea
• l’impiego di FU/LV + Oxa o IRI durante la malattia aumenta la sopravvivenza mediana

NUOVE TERAPIE BIOLOGICHE
• inibitori angiogenesi
• inibitori EGFR
• inibitori COX-2
• inibitori metallo proteinasi membrana
• vaccini

BEVACIZUMAB
Avastin
anticorpo monoclonale umanizzato anti
VEGF prodotto mediante tecnica del DNA
ricombinante in cellule ovariche di criceto
cinese

BEVACIZUMAB
IFL/bevacizumab 402 44.8 10.6 20.3
IFL 411 34.8 6.2 15.6
Hurwitz et al N Engl J Med 2004;350:2335-2342
FU/LV/bevacizumab(high dose)
33 24 7.2 16.1
FU/LV/bevacizumab(low dose)
35 40 9.0 21.5
FU/LV 36 17 5.2 13.8
Kabbinavar et al J Clin Oncol 2003
n.pz RR mPFS mOS

Hurwitz H et al, N Engl J Med 350:2335-2342, 2004


Pro
bab
ilit
y
1.0
0.8
0.6
0.4
0.2
0
Overall survival (months)0 3 6 9 12 15 18 21 24 27 30 33 36
AliveDead MedianTotalA: FOLFOX4 + bevacizumab 289 246 43 12.9B: FOLFOX4 290 257 33 10.8C: Bevacizumab 243 216 27 10.2
HR=0.76
A vs B: p=0.0018
B vs C: p=0.95
HR = hazard ratio
10.2 12.9
10.8
BevacizumabMetastatic colorectal cancer, 2nd
line

CETUXIMAB
Erbitux
anticorpo monoclonale umanizzato anti EGFR


dal 1993 al 2005
6
9,511,5 12,1
14,5
20
24
2,5 3,45
6 6,2
8,7
0
4
8
12
16
20
24
28
Solosupporto
FU bolus FU-FA bolus FU-FA ic FU-FA bolus& ic
FU-FA conIrinotecan oOxaliplatin
Anticorpi &CT
Sopravvivenza (OS)
Sopravvivenza senzaprogressione (PFS)
Mesi
Carcinoma Colorettale MetastaticoEvoluzione della Terapia Medica

TUMORE DELL’
APPARATO GASTRO-ENTERICO
NON COLON-RETTO
STOMACO

CARCINOMA GASTRICO
1a causa di morte per tumore nel XX
secolo (ora 2a dopo il polmone)
875000 nuovi casi per anno
incidenza in calo in molti paesi (abitudini
alimentari) per i tumori sotto la
giunzione esofago-gastrica, in aumento
per quelli sopra

CARCINOMA GASTRICO
Incidenza diversa in funzione delle aree
geografiche
Elevata in Europa occidentale, Giappone,
Sud America (30-85/100000)
Bassa in USA, Israele, Kuwait (4-
8/100000)

CARCINOMA GASTRICO
Incidenza aumenta con l’età
Incidenza diversa in funzione di razza
(afro-americani:bianchi=2:1;
cardias:contrario)
Incidenza diversa in funzione del sesso
(uomini : donne = 2:1)

EZIOLOGIA FATTORI AMBIENTALI
importanza primaria (immigrati
Giapponesi di 1° e 2° generazione e
Polacchi): esposizione durante
l’infanzia e fattori culturali
ABITUDINI ALIMENTARI: sale
gastrite cronica atrofica; nitrati
metaplasia intestinale

FATTORI ACQUISITI
1.Nutrizionali elevato consumo di sale
elevato consumo di nitrati
basso consumo vit A e C
processi conservazione
(cibi affumicati, sotto
sale, assenza refrigerazione)
consumo di acqua di
pozzo
elevato body mass index
elevato consumo calorico

FATTORI ACQUISITI2.Occupazionali gomma
carboneesposizione a radiazioni
3.Abitudini voluttuarie fumo di sigaretta (OR:
2.4)4.Sanitario Helicobacter Pylori (5% a
10y)Epstein-Barrchirurgia x ulcera
gastricareflusso gastro-esofageo
(x2)

FATTORI GENETICI
Anamnesi familiare
Gruppo sanguigno A
Anemia perniciosa
Sindrome di Li-Fraumeni (p53)
Carcinoma del colon non poliposi
ereditario

FATTORI GENETICI
componente familiare ereditaria: 8-
10%
OR di cancro gastrico:
1.7 se parente di 1° grado affetto (madre >
padre)
2.6 se gemello affetto
8.5 se più di un parente di 1° grado affetto

Variante intestinale
tendenza a formare ghiandole
origina da lesioni precancerose
(atrofia gastrica; metaplasia intestinale)
più frequente negli uomini
più frequente negli anziani
prevalente in aree geografiche di endemia
EZIOLOGIA AMBIENTALE ?

Variante diffusa
tendenza a infiltrazione sottomucosa
diffusa metastatizzazione precoce
non origina da lesioni precancerose
più comune in aree a bassa incidenza
più frequente nella donna e nel giovane
associata a familiarità (gruppo A),
EZIOLOGIA GENETICA ?

MODALITÀ DI DIFFUSIONE
Infiltrazione della sierosa gastrica (60-90%):
rischio di invasione delle strutture adiacenti e
di disseminazione a peritoneo, omento, milza,
surrene, diaframma, fegato, pancreas, colon
Metastasi linfatiche (50%), peritoneali e a
distanza
Penetrazione ed estensione attraverso la
parete interessamento sempre più esteso
dell’organo fino a raggiungere esofago e
duodeno

loco-regionale 27-69%
peritoneale 17-42%
distante 13-44%
PATTERN DI RECIDIVA

Sintomi vaghi e aspecifici ritardata
diagnosi
CALO PONDERALE:
frequente (80%), precoce e suggestivo
Calo ponderale > 10% negli ultimi 6 mesi
= fattore prognostico sfavorevoleSAZIETÀ PRECOCE infrequente e
indicativa di tumore diffusamente
infiltrante con perdita di distensibilità
della parete gastrica
SINTOMATOLOGIA

DISFAGIA: localizzazioni cardiali
VOMITO: infiltrazione pilorica
SANGUINAMENTO: ematemesi 10-15%
ASCITE: sintomo tardivo
ITTERO: sintomo tardivo
OCCLUSIONE: da infiltrazione peritoneale
o del colon trasverso

Marcatori:
CEA elevato in 1/3 dei casi. Bassa
sensibilità. Correlato con lo stadio
Endoscopia:
esame di prima scelta
Ecoendoscopia utile per identificare
l’early gastric cancer di tipo diffuso.
Fornisce informazioni su T ed N con
accuratezza del 90% e 75%
rispettivamente (>TC)

TC:
utile per identificare la presenza di
disseminazione ai linfonodi perigastrici,
al fegato o al polmone
PET: mancano dati affidabili che ne
dimostrino l’utilità nel cancro gastrico
glucose transporter-1, importante
trasportatore di FDG nella cellula
tumorale è raramente presente in
sottotipi comuni di cancro gastrico come
l’adenoca con cellule ad anello con
castone e l’adenoca mucinoso (2.0% e
6.3%)
I tumori in cui è presente o che sono
avidi di FDG sono associati a peggior
prognosi

Laparoscopia
consente l’ispezione diretta del
peritoneo e delle superfici viscerali e il
riscontro di micrometastasi non visibili
alla TC (13-37% negli anni ‘90)
Conseguentemente permette di
risparmiare una laparotomia inutile in
pazienti con malattia metastatica

STADIAZIONE - T

NX Regional lymph node(s) cannot be
assessed
N0 No regional lymph node metastasis
N1 Metastasis in 1–6 regional lymph nodes
N2 Metastasis in 7–15 regional lymph
nodes
N3 Metastases in > 15 regional lymph
nodes
STADIAZIONE - N

Sopravvivenza a 5 anni cresciuta dal
15.4% (1973) al 21.8% (1997)
Prognosi peggiore per i tumori del
cardias e giunzione gastro-esofagea
rispetto a quelli del corpo
PROGNOSI

STADIO - T
A: TisB: T1C: T2D: T3T4 not shown

stadio II-III
chirurgia: necessaria ma insufficiente
60% recidiva e morte entro 5 anni dalla
diagnosi
chemio + radio postoperatoria
chemio neoadiuvante

stadio II-III

stadio IV
best supportive care
monochemioterapia
chemioterapia di combinazione

TUMORE DELL’
APPARATO GASTRO-ENTERICO
NON COLON-RETTO
VIE BILIARI

ANATOMIA

EPIDEMIOLOGIA
- colangiocarcinoma -
tumore raro
incidenza e mortalità in aumento
colangiocarcinoma 2-3000 nuovi casi/anno
(USA)
Picco di incidenza nell’8° decade di vita
La maggior parte dei pazienti ha > 65
anni
Leggermente più frequente nell’uomo

EPIDEMIOLOGIA
-colangiocarcinoma –
colangiocarcinoma ilare 67%
colangiocarcinoma distale 27%
colangiocarcinoma intraepatico 6%

FATTORI DI RISCHIOinfiammazione cronicacolangite sclerosante primaria (x160;
multifocale; età <)
cisti coledocicaparassitosi (87/105; opisthorchis viverrini, clonorchis
sinensis)
batteriemia portale cronica/flebite (rischio
10%)
fumo di sigarettaesposizione a: radionuclidi, radon,
nitrosamine, diossina, asbesto AIDS

ISTOLOGIA
sclerosante reazione desmoplastica
ispessimento diffuso dei dotti
difficile da trattare
nodulare massa intraepatica
papillare raro, basso grado, massa
polipoide a crescita endoluminale,
invasione minima, assenza di reazione
desmoplastica, prognosi
favorevole

ittero non accompagnato da dolore 70-
90% prurito 66%
dolore addominale, calo ponderale 30-
50%
febbre colangitica 20%
sintomi più precoci nei colangiocarcinomi
ilari e distali rispetto a quelli intraepatici
SEGNI & SINTOMI

elevazione indici di stasi
modesto aumento indici di sintesi
CEA poco utile
CA19.9sensibilità e specificità > 85%,
diagnosi
differenziale: colangite, colelitiasi
LABORATORIO

ECOGRAFIA: 1° esame x pz itterico o con
indici di stasi elevati x escludere
colelitiasi
TC: documenta ispessimento del dotto e
dilatazione a monte
ERCP: utile x localizzare e caratterizzare la
lesione
COLANGIORM: se disponible è il test di
elezione
ESAMI STRUMENTALI

BIOPSIA
BRUSHING dei DOTTI BILIARI
AGOASPIRATO sotto guida TC
si tratta di tumori ipocellulari difficili da
diagnosticare: sensibilità 62%
diagnosi differenziale con epatoca:
facile
con M+ : difficile

Approccio multidisciplinare: chirurgo,
oncologo, gastroenterologo, radiologo
interventista, patologo, radioterapista
indicazioni di resecabilità non
chiaramente definite (32-90%)
Sopravvivenza mediana 15-59 mesi
5 anni 13-50%
PRINCIPI di TERAPIA

TUMORE DELL’
APPARATO GASTRO-ENTERICO
NON COLON-RETTO
COLECISTI

vicinanza con
vena porta, arteria epatica, dotto
biliare
segmenti epatici IVb e V
dotto biliare comune
parete sottile
lamina propria stretta
singolo strato muscolare

EPIDEMIOLOGIA
- ca colecisti -
1.2 casi per 105 anno in USA
incidenza variabile per regione e razza (Cile, Bolivia, Europa centrale, Israele, Indiani
americani, Americani di origine Messicana; Spagna,
India, neri americani)
principale causa di morte x cancro per le
cilene

FATTORI DI RISCHIO infiammazione cronica (colelitiasi !)
75-98% di pz con ca colecisti hanno colelitiasi
0.3-3% pz con colelitiasi sviluppano cancro
colecisti a porcellana associata con ca colecisti nel 10-25% dei casi
età avanzata
sesso femminile
anomalia giunzione pancreatico-biliare

MODALITÀ DI DIFFUSIONE
infiltrando attraverso il sottile strato
muscolare ha precoce accesso ai linfatici
e vasi con precoce disseminazione
linfatica ed ematogena
Le M+ ematogene, attraverso il sistema
venoso portale, raggiungono il IV e V
segmento epatico
La sede più comune di M+ extra-
addominali è il polmone

sintomi di colecistite cronica o colica
biliare
perdita di peso
dolore persistente ipocondrio destro
ittero
anoressia
SEGNI & SINTOMI

La chirurgia radicale offre le migliori
possibilità di guarigione
È necessaria un’accurata valutazione pre-
operatoria dei pazienti che devono subire una
colecistectomia per sintomi di colecistite o
altre lesioni sospette
La resezione epatica en bloc e la resezione
linfonodale senza interruzione del piano di
resezione sottosieroso colecistico è la terapia
di elezione
PRINCIPI di TERAPIA


5y OS
T1N0 100%
T2N0 extended cholecystectomy
70-90%
simple cholecystectomy 20-40%
T3N1 extended cholecystectomy
45-60%
RISULTATI della CHIRURGIA