SezioneD Polimeri e materiali - staticmy.zanichelli.it · per omopolimero e copolimero. 4. Qual è...
Transcript of SezioneD Polimeri e materiali - staticmy.zanichelli.it · per omopolimero e copolimero. 4. Qual è...

Sezione
DAPolimerie materiali

D130
Le materie plastiche hanno cambiato il nostro modo di vivereI materiali polimerici sono una delle innovazioni tecnologiche che ha contri-buito maggiormente allo sviluppo dell’industria e al miglioramento della quali-tà della vita. Dal secondo dopoguerra a oggi, infatti, la produzione delle materieplastiche è passata da 1,5 milioni di tonnellate annue a oltre 250 milioni di ton-nellate, con un tasso medio annuo di crescita pari a circa l’8,5% (figura 1). Soloin Europa si contano circa 60 000 aziende e 1,45 milioni di persone occupate nelsettore, per un fatturato medio annuo totale di 300 miliardi di euro.
Il grande successo delle plastiche risiede nella loro versatilità e nel loro costo;infatti, a seconda del polimero scelto si possono ottenere materiali che concilia-no diverse caratteristiche come la leggerezza, la resistenza, l’isolamento, l’elasti-cità, l’inerzia chimica e la lavorabilità. La maggior parte dei polimeri è impiegatanel settore degli imballaggi e del packaging, ma questi composti sono utilizzatiin tantissimi altri settori come l’edilizia, l’arredamento, l’agricoltura, l’elettroni-ca e i trasporti. Dalle bottiglie alle pellicole, dagli elettrodomestici alle tubazio-ni, dalle automobili alle vernici (figura 2), i polimeri possono essere prodotti informe diverse e a un prezzo accessibile grazie alle tecnologie di trasformazioneche permettono di mantenere i costi di lavorazione relativamente contenuti e piùcompetitivi rispetto a materiali come il legno, il vetro e i metalli.
1Macromolecolee polimeri
I polimeri
19601950 1970 1980 1990 2000 2010 2020
300
250
200
150
100
50
0
Anno
Mil
ion
i di t
on
ne
lla
te(M
t)
1950 1976 1989 2002 2010 2011 201220091,7 47 99 204 270 280 288250
0,35 19,8 27,4 56,1 57 58 5755
Produzionemondiale di plastica
Produzione europea di plastica
3 Figura 1La produzione di plastica nelmondo dal 1950 al 2012, inmilioni di tonnellate (Mt).Fonte: Plastic Europe (PEMRG)/Consultic.
Dagli anni Cinquanta del secolo scorso la produzionemondiale di plastica è passata da 1,5 milioni ditonnellate annue a oltre 250 milioni di tonnellate.
D4Capitolo

D131
capitolo D4 I polimeri
I polimeri sono costituiti dalla ripetizione di monomeriI polimeri, o macromolecole, sono molecole a elevata massa molecolare costituitedalla ripetizione di molecole più semplici dette monomeri, legate tra loro da lega-mi di tipo covalente.
A seconda della loro origine, i polimeri possono essere naturali o sintetici:
• i polimeri naturali (figura 3) sono macromolecole di origine biologica (chiama-te anche biomolecole o macromolecole biologiche) e rappresentano i costituenti fon-damentali degli organismi viventi. Appartengono a questa classe i carboidraticome cellulosa, amido e glicogeno, le proteine e gli acidi nucleici (DNA, RNA);
• i polimeri sintetici (figura 4 a pagina seguente) sono prodotti attraverso re-azioni chimiche di sintesi, tipicamente a partire da monomeri ottenuti dallalavorazione del petrolio. Polimeri come polietilene, Teflon®, cellophane®, ple-xiglas®, nylon, fibre acriliche e poliuretano sono materie plastiche utilizzatein tantissimi beni di consumo, come contenitori, pellicole per imballaggi, bot-tiglie, vernici, materiali per l’edilizia e fibre tessili.
Attualmente, solo il 4% del petrolio estratto è destinato alla produzione di poli-meri sintetici. I monomeri sono ottenuti dalla lavorazione del petrolio e succes-sivamente trasformati in polimeri attraverso i processi di polimerizzazione. In
AGRICOLTURA
3,3%
ELETTRONICA
5,8%
INDUSTRIA
AUTOMOBILISTICA
8,9%
EDILIZIA
19,7%
IMBALLAGGI
E PACKAGING
39,9%
ALTRI
22,4%
7 Figura 2La domanda di materialiplastici in Europa neiprincipali settori dimercato (2015).
Le paroleUn monomero (dal greco mónos =«uno solo» e méros = «parte») è l’unitàmolecolare che si ripete nelle molecolepolimeriche.
A B C
7 Figura 3(A) La seta è una fibra proteica di origineanimale; (B) ogni fibra è formata da duefili costituiti dalla proteina fibroina (checostituisce circa l’80% in peso) avvolte in unaseconda proteina chiamata sericina (20%circa). (C) La fibra di cotone si ricava dallapeluria che ricopre i semi di una pianta dellaspecie Gossypium ed è costituita quasi per il100% da cellulosa.
Fibre di setaosservate almicroscopioelettronico ascansione.
A colpo d’occhio
SINTETICI
POLIETILENE,TEFLON®,PLEXIGAS®,NYLON,CELLOPHANE®,FIBRE ACRILICHE,POLIURETANO
NATURALI
POLIMERI
CARBOIDRATI,PROTEINE,ACIDI NUCLEICI

D132
particolare, gli idrocarburi presenti nel petrolio sono trasformati in monomeriattraverso il cracking, un insieme di reazioni chimiche realizzate nelle raffine-rie. Tra questi il più importante è il cracking catalitico (detto FCC, Fluid Catalytic
Cracking), un processo che sfrutta dei catalizzatori acidi per produrre alcheni, iprincipali building blocks («blocchi da costruzione») dell’industria dei polimeri.
I monomeri formano catene: omopolimeri e copolimeriI polimeri si rappresentano attraverso l’unità ripetente, che corrisponde al grup-po di atomi che si ripete n volte lungo la catena polimerica e costituisce l’unitàstrutturale fondamentale di una macromolecola (figura 5). Il numero di unitàripetenti (n) determina il grado di polimerizzazione del polimero.
Ti ricordi?Un alchene, detto anche olefina, è unidrocarburo che contiene un doppiolegame carbonio-carbonio.
3 Figura 4Alcuni esempi dipolimeri sintetici.
CuriositàPer semplificare la denominazionechimica dei polimeri, le aziende chebrevettano questi materiali assegnanoai loro prodotti dei nomi commerciali,come Teflon®, Kevlar®, Nomex®,plexiglas®, Lycra®. Anche se si trattadi marchi registrati, alcuni di questinomi sono diventati negli anni partedel linguaggio comune. Un esempio è ilnylon, un polimero prodotto da DuPont(in origine marchio registrato Nylon®)a partire dagli anni Quaranta delNovecento, che oggi denomina non piùun singolo polimero ma una famiglia dipoliammidi.
3 Figura 5L’unità ripetente di unpolimero è uguale almonomero (o al gruppodi monomeri) che hasubìto la reazione dipolimerizzazione.
3 Figura 6Gli omopolimeri sono formatida monomeri di un unico tipo;i copolimeri sono costituiti damonomeri diversi.
CopolimeroOmopolimero
Monomeri
Polimero
Unitàripetente
Polimerizzazione
Polietilene
PET (polietilene tereftalato) ABS (acrilonitrile-butadiene-stirene)
Vernici e resine
Fibre acriliche Polipropilene
I polimeri si denominano aggiungendo il prefisso poli- al nome dei monomeridi partenza che costituiscono l’unità ripetente: il polietilene (PE), il polivinilclo-ruro (PVC), il polistirene (PS) sono formati rispettivamente dalla ripetizione diunità monomeriche di etilene, cloruro di vinile e stirene.
Le catene polimeriche possono essere formate da uno o più tipi di monomero(figura 6):
• un polimero costituito da un solo tipo di monomero è un omopolimero;• un polimero costituito da monomeri diversi è un copolimero.
Nylon

--
D133
capitolo D4 I polimeri
Al contrario, la reazione di polimerizzazione dello stirene e del butadiene portaalla formazione di un copolimero, la gomma stirene-butadiene chiamata gommaSBR (da Styrene Butadiene Rubber).
Per esempio, la reazione di polimerizzazione dell’etilene porta alla formazione diun omopolimero, il polietilene:
Ti ricordi?Un diene è un idrocarburo che contienedue doppi legami; nei dieni coniugati,come l’1,3-butadiene, i doppi legami sialternano con legami semplici.
Le catene polimeriche hanno massa molecolare variabileLe reazioni di polimerizzazione portano alla formazione di catene polimerichecon lunghezza variabile. A seconda del grado di polimerizzazione e del processodi sintesi, si possono ottenere polimeri con pesi molecolari differenti (figura 7);per questo motivo quando si parla di peso molecolare di un polimero ci si riferisce auna media statistica dei pesi molecolari delle diverse catene macromolecolari.
7 Figura 7La polimerizzazione porta allaformazione di macromolecolecon diversa massa molecolare.
−−−⟶
etilene
-(CH2-CH
2)
n-n CH
2=CH
2
polietilene
−−−⟶
−−−⟶
1,3-butadiene + stirene
m CH2=CH-CH=CH
2+ n CH=CH
2
MonomeroMonomero
copolimero stirene-butadiene
(CH2-CH=CH-CH
2)
m(CH-CH
2)
n
Unitˆ ripetente
-- --- --
Polimerizzazione
Monomero
Catena polimerica
Se riportiamo in un grafico il numero di catene presenti e i rispettivi pesi moleco-lari, otterremo una curva che rappresenta la distribuzione statistica della massamolecolare di un polimero (figura 8).
7 Figura 8Distribuzione statisticadella massa molecolare diun polimero.
Massa molecolare della catena polimerica
Num
ero
di c
aten
e po
limer
iche
Se si raggruppa in un grafico ilnumero di catene che hanno ugualemassa in funzione della massamolecolare stessa, si ottiene unadistribuzione di pesi molecolari chepresenta la tipica forma a gaussiana.

D134
Dalla massa molecolare media si ottengono informazionisull’eterogeneità di un polimeroLa massa molecolare media si definisce nei seguenti modi:
• la massa molecolare media numerale (Mn) rappresenta la media matematica
d =M
w
Mn
della massa molecolare delle catene; si ottiene dividendo la sommatoria dellemasse molecolari per il numero delle catene presenti:
• la massa molecolare media ponderale (Mw) rappresenta invece la media pon-derale della massa molecolare delle catene. Questa grandezza attribuisce unamaggiore importanza alle catene più lunghe e per questo è influenzata dallapresenza di catene con masse molecolari elevate.
Il rapporto tra massa molecolare media ponderale e massa molecolare media nu-merale di un polimero rappresenta l’indice di dispersità (d) o di polidispersità.Questo valore fornisce un’indicazione del grado di eterogeneità di un polimero,cioè della distribuzione dei pesi molecolari delle catene presenti:
• in un polimero monodisperso l’indice di polidispersità è uguale a 1; questipolimeri sono costituiti da catene con masse molecolari omogenee;
• in un polimero polidisperso l’indice di polidispersità è maggiore di 1; questipolimeri sono costituiti da catene con masse molecolari eterogenee.
L’indice di polidispersità dipende dal processo di polimerizzazione utilizzato perla sintesi del polimero e rappresenta un parametro fondamentale da cui dipen-dono varie proprietà dei materiali. Per esempio, la resistenza meccanica di unmateriale plastico è influenzata dalla lunghezza delle catene, cioè è direttamentecollegata alla massa molecolare media del campione.
Facciamoil punto
1. A che cosa si deve il successodei polimeri nel mercatomondiale?
2. In base alla loro origine, comesi classificano i polimeri?
3. Spiega che cosa si intendeper omopolimero ecopolimero.
4. Qual è la differenza tra unitàripetente e monomero?
5. Come sono definite la massamolecolare media numeralee la massa molecolare mediaponderale di un polimero?
I primi materiali plasticiLo studio dei polimeri sintetici è una brancadella chimica che ha avuto uno sviluppoimprovviso a cavallo di un secolo circa,vediamo qui le principali scoperte e gliscienziati che ne sono stati i protagonisti.
Nel 1839, l’inventore statunitenseCharles Goodyear scopre che l’aggiuntadi zolfo alla gomma naturale, seguita dariscaldamento, la rende più elastica eresistente ai solventi: è nata la gomma
vulcanizzata (figura). Una trentina di annidopo, John H. Hyatt brevetta la prima pallada biliardo in finto avorio: il nuovo materialesi chiama celluloide. Questa sarà utilizzatafino agli anni Cinquanta del Novecento perfabbricare le pellicole cinematografiche;anche se il polimero, a base di nitrato dicellulosa, risulta altamente infiammabile.
Nel 1907, il chimico statunitense diorigine belga Leo H. Baekeland inventa la
1 - Storia della scienza
bachelite, la prima plastica termoindurenteottenuta in laboratorio. Si tratta di unaresina fenolo-formaldeide, un materialeresistente alle alte temperature e isolante.Negli anni successivi, vengono brevettatiuna serie di altri materiali plastici:• il polivinilcloruro (PVC, 1912);• il polistirene (PS, 1930);• il polietilene (PE, 1935);• il polimetilmetacrilato (PMMA, 1939).
Tra il 1939 e il 1941, due chimicistatunitensi, Roy Plunkett e Wallace HumeCarothers scoprono rispettivamente ilpolitetrafluoroetilene (PTFE), chiamatoanche Teflon®, e la prima poliammide (PA)che viene chiamata Nylon®.
Nel 1954, l’italiano Giulio Natta e iltedesco Karl Ziegler riescono per la primavolta a sintetizzare il polipropilene isotattico
(PP); nel 1963 condivideranno il premioNobel per la Chimica ottenuto grazie alle“loro scoperte nel campo della chimica edella tecnologia dei polimeri”.
1 FiguraLa gomma vulcanizzata si usa nellafabbricazione degli pneumatici.

D135
capitolo D4 I polimeri
I polimeri di addizione si formanoper successive addizioni del monomeroDal punto di vista cinetico, i polimeri possono essere prodotti attraverso duemeccanismi:
• polimerizzazione di addizione o a catena (polimeri di addizione);• polimerizzazione di condensazione o a stadi (polimeri di condensazione).
Un polimero si forma per addizione o per condensazione a seconda delle caratte-ristiche chimiche dei monomeri di partenza, cioè segue la reattività dei gruppifunzionali presenti nei reagenti.
Nella polimerizzazione per addizione il polimero si forma per addizioni suc-cessive del monomero. Il meccanismo di polimerizzazione per addizione è dettoanche polimerizzazione a catena perché ogni passaggio dipende da quello prece-dente; in altre parole, l’accrescimento della catena procede con un’unità mono-merica alla volta. I monomeri che seguono questo meccanismo sono soprattuttomolecole caratterizzate dalla presenza di doppi legami carbonio-carbonio (C=C),cioè alcheni (tabella 1).
2I polimeridi addizione
Monomero Formula Polimero ImpieghiEtilene CH2=CH2 Polietilene Giocattoli e contenitori in plastica,
rivestimenti per cavi.
Stirene CH=CH2 Polistirene Componenti di elettrodomestici,materiale per isolamento e perimballaggi (polistirolo espanso).
Metacrilato di metileC=C
CH3H
H C=O
OCH3
Polimetacrilato dimetile (plexiglas®)
Vetri sintetici.
Cloruro di vinile CH2=CHCl Polivinilcloruro (PVC) Tubi per l’edilizia, profili per infissi,pellicole e imballaggi.
Tetrafluoroetilene CF2=CF2 Politetrafluoroetilene(Teflon®)
Rivestimenti di organi meccanicie utensili da cucina, lubrificanti eisolanti elettrici.
5 Tabella 1Alcuni polimeri ottenuti perpolimerizzazione per addizione.
A colpo d’occhio
DI CONDENSAZIONE
POLIMERIZZAZIONE
PER ADDIZIONE
RADICALICA
ANIONICA
CATIONICA

D136
La polimerizzazione per addizione cationica è un meccanismo di reazione acatena che coinvolge cationi; la specie attiva che prende parte alla reazione è uncarbocatione. A livello industriale, la polimerizzazione cationica è utilizzata perla sintesi del poliisobutilene, un’importante gomma sintetica. I monomeri chepolimerizzano per via cationica sono molecole in grado di comportarsi da dona-tori di elettroni nella fase di propagazione, cioè sono nucleofili; inoltre contengo-no doppi legami carbonio-carbonio (C=C), come gli alcheni, i dieni, i compostivinilici (aromatici e ammine) e gli eteri.
Nella fase di inizio (figura 10A) si genera il carbocatione utilizzando iniziatoridi tipo acido, come acidi protonici (HCl) e acidi di Lewis (AlCl3). Nella fase di pro-pagazione il carbocatione reagisce con il monomero per dare un nuovo carboca-tione, che propaga la reazione con addizioni successive di monomero (figura 10B).
Ti ricordi?Un carbocatione è uno ione con caricapositiva sull’atomo di carbonio; unreagente come un carbocatione, che«cerca» elettroni per raggiungere laconfigurazione elettronica stabile diottetto, si definisce elettrofilo.
La polimerizzazione per addizione avviene in tre fasiLa polimerizzazione per addizione o a catena avviene in tre fasi successive:
• nella fase di inizio si forma la specie attiva, cioè la specie chimica che avviail processo di polimerizzazione;
• nella fase di propagazione la specie attiva reagisce con i monomeri che, at-traverso un meccanismo di addizioni successive, portano alla formazione diuna catena;
• nella fase di terminazione si arresta l’accrescimento della macromolecolamediante reazioni chimiche che bloccano il centro attivo della catena e, diconseguenza, impediscono al monomero di addizionarsi.
A seconda della specie attiva responsabile della propagazione della catena, esisto-no tre tipi di polimerizzazione per addizione:
• polimerizzazione radicalica, in cui la specie attiva è un radicale;• polimerizzazione cationica, in cui la specie attiva è un catione;• polimerizzazione anionica, in cui la specie attiva è un anione.
La polimerizzazione per addizione radicalica è un meccanismo di reazione acatena che coinvolge radicali liberi. A causa della presenza di un elettrone spaia-to, i radicali sono fortemente reattivi per cui tendono a reagire facilmente conaltre specie chimiche per raggiungere una configurazione elettronica stabile. Laconseguenza di questo comportamento è che le reazioni radicaliche sono moltoveloci e seguono un meccanismo a catena.
Come si vede nella tabella 1, i monomeri che polimerizzano per via radicalicasono caratterizzati dalla presenza di un doppio legame carbonio-carbonio (C=C).Per avviare la polimerizzazione è necessario che tra i monomeri sia presente laspecie attiva, cioè i radicali liberi; per questo si utilizza un iniziatore radicalico,un composto che produce radicali nell’ambiente di reazione e dà inizio alla poli-merizzazione.
Gli iniziatori radicalici sono composti instabili che possiedono un legame de-bole e subiscono facilmente una scissione omolitica, per effetto del calore o dellaluce (radiazione UV), generando radicali liberi.
A seconda del meccanismo che provoca la scissione omolitica, esistono diversitipi di iniziatori:
• gli iniziatori termici sviluppano radicali quando sono sottoposti a calore; i piùutilizzati sono perossidi e idroperossidi organici, caratterizzati dalla presenzadel legame —O—O— (figura 9);
• gli iniziatori redox sviluppano radicali a seguito di reazioni di ossidoriduzione;• gli iniziatori fotochimici generano radicali in presenza di radiazioni ultraviolette.
−−−⟶- C- O- O- C-
=
O
=
Ocalore
- C- O$ + $O- C-
=
O
=
O3 Figura 9Scissione omolitica del perossidodi benzoile, un iniziatoreradicalico di tipo termico.
Ti ricordi?Un radicale è una specie chimicacaratterizzata dalla presenza di unelettrone spaiato che può derivaredalla scissione omolitica di un legamecovalente.

D137
capitolo D4 I polimeri
Ti ricordi?Un carbanione è uno ione con caricanegativa sull’atomo di carbonio; unreagente come un carbanione, che«cerca» un protone o un altro centropositivo, si definisce nucleofilo.
La polimerizzazione per addizione anionica è un meccanismo di reazione a cate-na che coinvolge anioni; la specie attiva che prende parte alla reazione è un carba-nione. I monomeri polimerizzabili per via anionica sono molecole che contengonodoppi legami carbonio-carbonio (C=C), strutture cicliche con ossigeno (ossido dietilene) e alcuni composti carbonilici (formaldeide). Le principali applicazioni in-dustriali riguardano la produzione del polibutadiene e del poliisoprene.Nella fase di inizio il carbanione è generato utilizzando come iniziatori dei fortielettrondonatori, in particolare metalli alcalini (Na, K) o composti litio-organici(R-Li) come il butil-litio. Questi, cedendo facilmente elettroni al monomero, pro-ducono un carbonio con carica negativa. Nella fase di propagazione, per addizio-ni successive dei carbanioni sul doppio legame carbonio-carbonio del monome-ro, si forma la catena polimerica (figura 11).
1 Figura 10(A) Fase di inizio della polimerizzazionecationica. (B) Fase di propagazione dellapolimerizzazione cationica.
⟶⟶C=CH3
CH3
CH3
+
H2C=CCH3
CH3
CH3-C-CH2-C
CH3
CH3
CH3
CH3
+
CH3-C---CH2-C---CH2-C
CH3
CH3
CH3
CH3
CH3
CH3
+
n
poliisobutilene
⟶ ⟶CH3-CH2-CH2-CH2-C-CÐ Li+ +$$
HC=C
H
HH
H
H
H
H
CH3-CH2-CH2-CH2-C-C-C-C-Li+
H
H
H
H
H
H
--C-C--
H
H
H
Hn
H
H
7 Figura 11La polimerizzazione anionicadell’etilene con butil-litio comeiniziatore.
⟶C=CH2
CH3
CH3
H+
C=CH3
CH3
CH3
isobutilene carbocatione
+
Iniziatore acido
La polimerizzazione radicalica dell’etilene
Nello stadio di inizio della polimerizzazione radicalica dell’etilene,l’iniziatore radicalico genera la prima specie radicalica:
2 - Per saperne di più
Il radicale R−O, molto reattivo, si addiziona al doppio legameC=C dell’etilene, con la formazione del radicale del carbonio, cherappresenta la specie attiva:
In questo modo la catena polimerica aumenta progressivamente lesue dimensioni:
−−⟶ R-O$+$O-RR-O-O-R D
−−⟶$
RO-CH2-CH2RO$ + CH2=CH2
−−⟶ RO-CH2-CH2-CH2-CH2RO-CH2-CH2 + CH2=CH2
$ $
−−⟶ RO-(CH2-CH2)n+m
RO-(CH2)n-CH2$+$CH2-(CH2)
m-OR -OR
Nello stadio di terminazione la propagazione si conclude quandodue radicali del carbonio reagiscono tra loro formando un legamecovalente. Scomparendo la specie attiva (il radicale), si fermal’addizione dei monomeri alla catena e si ottiene una macromolecolacon un numero variabile di unità ripetenti:
Il polimero che si ottiene presenta agli estremi della catena i gruppidi atomi provenienti dall’iniziatore radicalico. Gli atomi derivantidall’iniziatore rappresentano una porzione molto piccola rispettoal polimero e, per questo, non vanno ad alterare le caratteristichecomplessive del materiale.
Nello stadio di propagazione il radicale al carbonio reagisce conuna molecola di etilene, generando un nuovo radicale al carbonio.Attraverso questo meccanismo le molecole di monomero sisommano una all’altra generando di volta in volta un radicale.
Le polimerizzazioni a catena sono regolate da parametri come la temperatura, lapressione, la concentrazione dei reagenti e la concentrazione del catalizzatore (inquesto caso l’iniziatore). In particolare, le polimerizzazioni cationiche e anioni-che sono molto sensibili alle condizioni di reazione e alla presenza di impurez-ze, per questo motivo la loro riproducibilità è alquanto complessa. Ma attraversoun’opportuna regolazione di questi fattori è possibile modulare il grado di poli-merizzazione del polimero finale e ottimizzare il processo di sintesi.
Facciamoil punto
1. Descrivi le fasi checaratterizzano lapolimerizzazione peraddizione.
2. In che cosa si differenziano lepolimerizzazioni radicaliche,anioniche e cationiche?
3. Fai alcuni esempi di polimeriottenuti per addizione.
4. Qual è la differenza trainiziatore e specie attiva?
A B

D138
I polimeri di condensazione si formano a stadiPer ottenere polimeri di condensazione è necessario che i monomeri coinvoltisiano almeno bifunzionali e che la reazione sia accompagnata dall’eliminazionedi molecole con massa molecolare ridotta, tipicamente acqua. In questo modo sipossono ottenere sia omopolimeri sia copolimeri, a seconda che la reazione av-venga tra monomeri uguali o diversi:
• quando la reazione di condensazione coinvolge gruppi funzionali presenti su
monomeri differenti si ottiene un copolimero;• quando la reazione di condensazione avviene tra gruppi funzionali presenti
sullo stesso monomero si ottiene un omopolimero.
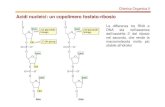
L’acido polilattico, o poli(acido lattico) – PLA, è un esempio di omopolimero dicondensazione; esso infatti si ottiene dalla polimerizzazione dell’acido lattico,un monomero che presenta gruppi funzionali differenti nella medesima unitàmonomerica, in particolare un gruppo ossidrilico e un gruppo carbossilico.
Di seguito è riportata la reazione di condensazione tra due monomeri di acidolattico:
3I polimeridi condensazione
−−⟶-H
2O
CH3-CH-COOH + CH
3-CH-COOH
OH OH
CH3-CH-CO-O-CH-COOH
OH CH3
Il gruppo carbossilico di un monomero di acido lattico reagisce per condensazio-ne con il gruppo ossidrilico di un altro monomero di acido lattico, formando unestere. Reazioni di condensazione successive generano il PLA, un poliestere.
Il PET (polietilentereftalato), invece, è un esempio di copolimero di conden-sazione, perché è un poliestere che si ottiene dalla reazione tra due monomeridiversi, in particolare da un acido dicarbossilico e da un diolo, come vedremo piùavanti.
La polimerizzazione di condensazione viene anche detta a stadi perché, a dif-ferenza dei polimeri di addizione, i monomeri non si addizionano uno alla volta,ma diverse catene in accrescimento si legano tra loro a formare una macromole-cola più grande.
Per permettere la formazione della catena polimerica, i monomeri che poli-merizzano per condensazione devono possedere almeno due gruppi funzionali;la bifunzionalità dei monomeri infatti è un requisito fondamentale perché con-sente alla polimerizzazione di proseguire agli estremi della catena e di allungareil polimero in entrambe le direzioni.
A differenza della polimerizzazione per addizione in cui la specie attiva èun radicale, un carbocatione oppure un carbanione, nella condensazione sono igruppi funzionali che reagendo tra loro permettono l’allungamento del polime-ro. I monomeri che possono seguire questo meccanismo sono principalmente idioli (alcoli con due gruppi –OH), gli acidi dicarbossilici (acidi con due gruppi–COOH) e le diammine (ammine con due gruppi –NH2).
Il nome del polimero di condensazione è costituito dal prefisso poli- e dalnome del gruppo funzionale risultante dalla reazione tra i monomeri (per esem-pio poliesteri o poliammidi). Come per i polimeri di addizione, però, accanto allanomenclatura tradizionale sono utilizzati anche sigle (come PET) e nomi com-merciali come per esempio nel caso del Kevlar®.
Gruppocarbossilico
Legame estereo
Gruppoossidrilico

D139
capitolo D4 I polimeri
La reattività dei gruppi funzionali nella polimerizzazione a stadiLe reazioni tra monomeri seguono la reattività tipica dei gruppi funzionali e pos-sono essere suddivise in due grandi gruppi: le reazioni che coinvolgono il gruppocarbossilico e le reazioni di sostituzione elettrofila seguite da una reazione dicondensazione.
Nel primo caso, un acido dicarbossilico può reagire con una diammina for-mando una poliammide, come il nylon, un copolimero di condensazione.
−−
⟶
H-N-(CH2)
6-N-H HO-C-(CH
2)
4-C-OH H-N-(CH
2)
6-N-H
H
=
OH
=
O H
$N-(CH2)
6-N$
H H
+H2O
$C-(CH2)
4-C$
=
O
=
O
+H2O
$N-(CH2)
6-N$
H H
-N-(CH2)
6-N-----
H H
-C-(CH2)
4-C-----
=
O
=
O
-N-(CH2)
6-N-
H H
+H2O +H
2O
H
nylon 6,6
acido dicarbossilicodiammina
In alternativa l’acido dicarbossilico può reagire con un diolo per formare un po-liestere, come il PET; anche questo è un copolimero di condensazione perché siottiene da due monomeri differenti:
Ti ricordi?In una reazione di condensazione duemolecole si combinano rimuovendoun’altra piccola molecola che in genereè acqua o alcol.
Nelle reazioni di sostituzione elettrofila seguite da una reazione di condensazio-ne, i composti aromatici ricchi di elettroni π possono reagire con gli elettrofili inmodo tale che un atomo di idrogeno dell’anello viene sostituito dall’elettrofilo. Aquesto punto, se le molecole del composto aromatico sostituito reagiscono tra diloro per condensazione, si può formare un polimero. Queste reazioni permettonoper esempio la sintesi delle resine fenoliche, una famiglia di polimeri ottenutaper reazione tra fenolo e formaldeide (la reazione può interessare le posizioni siaorto sia para):
Ti ricordi?In una reazione di sostituzioneelettrofila aromatica l’anellobenzenico, ricco in elettroni di tipoπ, viene attaccato da un reagenteelettrofilo.
−−−⟶
fenolo
OH
H+ C=O
H
OHcatalizzatore
basicoCH
2OH
+
OH
CH2OH
formaldeide orto para
–H2O –H2O
n HOCH2CH
2OH
diolo
-- COOH +
acido dicarbossilico
--CO-- -- COOCH2CH
2O-- + n H
2O
polietilentereftalato (PET)n
n HOOC-- −−⟶
−−⟶
n H2O
–H2O

OH
D140
La prima materia plastica sintetica è stata proprio una resina fenolica, la bacheli-te (figura 12), che deve il suo nome a Leo Baekeland, il chimico che l'ha sintetiz-zata per la prima volta nel 1907.
Poliammidi e poliesteri sono tra i polimeri di uso più comunePoliammidi e poliesteri sono le principali famiglie di polimeri ottenute per con-densazione. Nella tabella 2 sono riportati alcuni esempi.
Il polietilentereftalato (PET) è un poliestere che si ottiene dalla reazione traun diacido aromatico, l’acido tereftalico, e un diolo, il glicole etilenico (reazionedi esterificazione):
−−−⟶
OH
n
CH2OH polimerizzazione
-H2O
OH
-CH2---
OH
-CH2--
resina fenolo-formaldeide
n
1 Figura 12In passato i telefoni erano fatti di bachelite,la prima materia plastica sintetica a esserestata prodotta all’inizio del Novecento.
HOOC C- OH+H -O-CH2-CH
2-OH
O
=
acido tereftalico glicole etilenicoH2O
HOOC COO-CH2-CH
2-OH
Gruppo estereo
Poiché entrambi i monomeri sono bifunzionali, in seguito alla reazione tra ilgruppo carbossilico e il gruppo ossidrilico si forma un dimero che ha alle estre-mità ancora un gruppo acido –COOH e un gruppo alcolico –OH. In questo modola catena si allunga da entrambe le estremità e si forma il polimero:
HOOC C O-CH2-CH
2-OOC
O
=
O
=
C O-CH2-CH
2-OH
n
Gruppi funzionali Monomeri Polimero (unità ripetente)diolo + acido dicarbossilico → poliestere
glicole etilenico + acido tereftalico
O
HO-CH2-CH2-OH + HO-C- -C-OH
O
O
-- C- -C-O-CH2-CH2-O--
Opolietilentereftalato (PET)
n
diammina + acido dicarbossilico→ poliammide
esametilendiammina + acido adipico
H2N-(CH2)6-NH2 + HOOC-(CH2)4-COOHO
--N-(CH2)6-N-C-(CH2)4-C--
nylon 6,6
n
H H O
p-fenilendiammina + acido tereftalico
O
H2N- HO-C-
O
-NH2 + -C-OH
-- NH- -NH-C-
O
Kevlar®
n
-C--
O
5 Tabella 2Esempi di polimeri ottenutiper condensazione.

D141
capitolo D4 I polimeri
Il PET è utilizzato principalmente per la produzione di contenitori per alimenti,in particolare bottiglie per l’acqua (figura 13).
I nylon sono una famiglia di poliammidi alifatiche che si ottengono dalla re-azione tra un acido dicarbossilico e una diammina. A seconda del numero degliatomi di carbonio delle catene alchiliche del diacido e della diammina si possonoottenere diversi tipi di nylon. Uno dei nylon più diffusi nell’industria si ottienea partire da acido adipico ed esametilendiammina: poiché il primo monomeroè un diacido con 6 atomi di carbonio, mentre il secondo è una diammina con 6atomi di carbonio, il nylon ottenuto è chiamato nylon 6,6:
——C-CH2-CH
2-CH
2-CH
2-C-NH-CH
2-CH
2-CH
2-CH
2-CH
2-CH
2-NH—— + 2n H
2O
O
=
O
=
n
n HO-C-CH2-CH
2-CH
2-CH
2-C-OH + n H
2N-CH
2-CH
2-CH
2-CH
2-CH
2-CH
2-NH
2
O
=
O
=
acido adipico esametilendiammina
nylon 6,6
I nylon sono polimeri molto versatili perché conciliano leggerezza e resistenza.Infatti, possono essere utilizzati per la produzione di materiali delicati come lefibre tessili o per materiali più resistenti come funi e guarnizioni.
Il Kevlar® è una fibra sintetica creata nel 1965, ottenuta per copolimerizzazio-ne di una diammina aromatica con acido tereftalico:
7 Figura 13Il PET è un polimero utilizzatoper produrre contenitori diliquidi e alimenti.
−−−−−⟶–2n HCl
H2N
+
NH2
=
O
=
O
Cl
ClC
n
NH
N
H OH
nH
C
=
O
C=
O
C
La caratteristica principale del Kevlar® è la grande resistenza meccanica alla tra-zione: a parità di peso, è cinque volte più resistente dell’acciaio. Il Kevlar® possie-de inoltre una grande resistenza al calore e alla fiamma. Per le sue caratteristicheè usato come fibra di rinforzo per la costruzione di giubbotti antiproiettile edelmetti, di attrezzature per gli sport estremi e per componenti di aeroplani, im-barcazioni e vetture da competizione.
Un copolimero è formato da diversi monomeriLa possibilità di utilizzare monomeri diversi permette di ottenere una grandevarietà di materiali. Quando un polimero è formato da monomeri diversi vienedetto copolimero.
A seconda di come sono legate tra loro le unità monomeriche nella catena, sipossono avere quattro tipi di copolimeri (figura 14 a pagina seguente):
• copolimero random, costituito da monomeri distribuiti con una sequenza ca-suale;
• copolimero alternato, costituito da una sequenza di monomeri che si alterna-no nella catena;
• copolimero a blocchi, costituito dall’alternarsi di blocchi ciascuno compostoda un solo tipo di monomero;
• copolimero aggraffato, caratterizzato da una catena principale di un omopo-limero a cui sono legate catene di un omopolimero diverso.
A colpo d’occhio
OMOPOLIMERI
POLIMERI
COPOLIMERI
RANDOM
ALTERNATI
AGGRAFFATI
A BLOCCHI
Guarda il video nell’ebookLa sintesi dei polimeriIl nylon in provetta

D142
Come abbiamo visto, anche i copolimeri si possono ottenere per addizione o percondensazione, a seconda delle caratteristiche delle unità monomeriche.
Le proprietà fisiche di un copolimero dipendono dalla natura dei monomeri edalla loro distribuzione nella catena polimerica: per questo, attraverso la copoli-merizzazione si possono ottenere materiali con proprietà intermedie rispetto a dueomopolimeri. Un esempio sono i copolimeri stirene-butadiene, prodotti a partiredagli anni Trenta del secolo scorso con il nome commerciale di Buna S®. Attual-mente conosciuto come gomma SBR (Styrene Butadiene Rubber), questo copolimeroconcilia la flessibilità tipica del polibutadiene alla tenacità tipica del polistirene.Infatti, mentre la gomma polibutadienica ha bassa tenacità e scarsa durezza, l’ag-giunta del polistirene conferisce al polimero una maggiore resistenza meccanica,pur mantenendo buone proprietà elastiche. La gomma SBR prodotta a livello indu-striale è costituita da circa il 75% di butadiene e dal 25% di stirene ed è utilizzataper la produzione di pneumatici, tubi, guarnizioni, suole da scarpe (figura 15).
Un altro copolimero di interesse industriale costituito da stirene e butadie-ne, ma con proprietà differenti, è il polistirene ad alto impatto chiamato ancheHIPS (High Impact PoliStyrene). Si tratta di un copolimero aggraffato caratterizzatoda una catena principale di polistirene sulla quale sono innestate catene di poli-butadiene (figura 16). Questo copolimero presenta una maggiore tenacità e unamaggiore resilienza rispetto all’omopolimero di polistirene, cioè risulta menofragile ed è in grado di sopportare urti maggiori senza rompersi.
3 Figura 14I diversi tipi di copolimeri.
A blocchi
Alternato
Aggraffato
Random
1 Figura 15La gomma SBR viene utilizzata per fabbricarela suola delle scarpe in virtù della suaresistenza meccanica e plasticità.
-CH2-CH-CH2-CH--- CH-CH-CH2-CH-CH2-CH-
CH2
CH2
CH2
CH2
HC
HCCH2
CH2
HC
HCCH2
CH2
CH2
HC
HC
CH2
HC
HC
Catena principaledi polistirene
Innesto di catenedi polibutadiene
3 Figura 16Stuttura del polistirenead alto impatto (HIPS).
Facciamoil punto
1. Descrivi come avvienela polimerizzazione dicondensazione.
2. Quali polimeri sipossono ottenere perpolimerizzazione dicondensazione?
3. Spiega quali sono le diversetipologie di copolimeri.

D143
capitolo D4 I polimeri
Le proprietà dei polimeri dipendono dalla disposizionee dalle interazioni tra le macromolecoleLe proprietà dei polimeri sono strettamente collegate alla disposizione dellemacromolecole nello spazio e alle loro interazioni. I fattori che determinano lastruttura microscopica della macromolecola si riflettono nelle caratteristiche ma-
croscopiche del materiale.
• La natura dei monomeri: polimeri costituiti da monomeri alifatici sono piùflessibili di polimeri costituiti da anelli aromatici che, al contrario, conferi-scono rigidità al polimero finale.
• La presenza di gruppi funzionali: monomeri con più gruppi funzionali pos-sono dare luogo a reazioni di reticolazione tra catene oppure possono svilup-pare interazioni come i legami a idrogeno.
• Il grado di polimerizzazione: a seconda del numero di unità ripetenti cam-biano le interazioni tra catene e di conseguenza le proprietà del polimero.
• La regolarità delle catene: se sono presenti isomerie geometriche (cis, trans) ocentri chirali nell’unità ripetente i polimeri possono essere stereoregolari e leloro caratteristiche varieranno a seconda della regolarità spaziale.
• Il processo di polimerizzazione: la sintesi chimica e la lavorazione del poli-mero permettono di modulare le proprietà del materiale finale.
L’organizzazione spaziale delle macromolecoleQuando viene prodotto un polimero, il processo di polimerizzazione porta allaformazione di molte catene.
Le proprietà del polimero non dipendono soltanto dalla struttura chimicadi ogni singola catena, ma anche dalla disposizione nello spazio delle macromo-lecole: queste caratteristiche insieme definiscono la struttura supramolecolareche rappresenta l’organizzazione tridimensionale del polimero.
Per esempio, nelle poliammidi come il nylon si instaurano legami a idrogenotra gli atomi di ossigeno del gruppo carbonilico presente in una catena e gli atomidi idrogeno del gruppo amminico di un’altra catena (figura 17). Sebbene i legamia idrogeno siano interazioni deboli (se paragonati ai legami covalenti), essi sonopresenti in un numero elevato e consentono alle catene di disporsi in modo ordi-nato: questo genera complessivamente un ordine tridimensionale.
4Le proprietàdei polimeri
O
=-
N
=
O
H
-
HN
O
=
-
NH
O
=
=
N
-
H
O
=
O
N
-
H
-
HN
O
=
N
-
H
=
O
=
N
-
H
O
=
O
N
-
H
=
N
-
H
O
=
O
N
-
H
=
N
-
H
O
-
NH
-
NH
-
NH
=
O
=
O
...
...
...
...
...
...
...
...
...
...
7 Figura 17Legami a idrogeno trale catene di nylon 6,6.
I polimeri possono essere amorfi o cristalliniQuando le catene di un polimero hanno una disposizione regolare nello spazio,il polimero si dice cristallino. Al contrario, quando le catene sono disposte inmodo irregolare il polimero si dice amorfo. In generale i polimeri non sono maicompletamente cristallini, ma è sempre presente un numero di catene dispostein modo disordinato. Quando nel polimero coesistono parti amorfe e parti cri-stalline, i polimeri vengono detti semicristallini (figura 18 a pagina seguente).

D144
La cristallinità influenza direttamente le proprietà meccaniche dei materiali:i polimeri cristallini sono più resistenti e più tenaci, mentre i polimeri amorfisono più flessibili. Polimeri con gruppi funzionali come i poliesteri, le poliammi-di e i poliacrilati sono materiali semicristallini, mentre polimeri alifatici come ilpolietilene sono principalmente amorfi (figura 19).
La temperatura di transizione vetrosa determinail passaggio da uno stato all’altroPer capire a quali temperature si può usare un materiale polimerico occorre co-noscere la sua temperatura di transizione vetrosa (tg). La transizione vetrosa èun fenomeno che si verifica nei polimeri amorfi e semicristallini e consiste nellatrasformazione del materiale da uno stato rigido a uno stato gommoso.
A temperature inferiori rispetto alla tg, le catene hanno una mobilità ridottae il polimero si presenta rigido e vetroso; per temperature superiori alla tempe-ratura di transizione vetrosa, invece, le catene acquistano mobilità e il polimeroassume gradualmente uno stato gommoso, senza tuttavia raggiungere la fusione(figura 20). Il valore della tg è influenzato dalle caratteristiche molecolari del po-limero, come la presenza di sostituenti e di gruppi funzionali in grado di creareinterazioni intermolecolari. Oltre alla temperatura di transizione vetrosa, i poli-meri che presentano porzioni cristalline possiedono anche una temperatura difusione (tf) al di sopra della quale avviene il passaggio allo stato fuso.
La temperatura di fusione e la temperatura di transizione vetrosa sono para-metri molto importanti per le applicazioni dei polimeri in campo industrialeperché permettono di definire l’intervallo di temperatura permesso per l’utilizzodi un materiale. Per esempio il polistirene si usa per la produzione dei bicchieridi plastica perché ha una tg di circa 100 °C (tabella 3): questo significa che questomateriale si presenta allo stato vetroso al di sotto dei 100 °C, un intervallo di tem-peratura idoneo per il consumo delle bevande.
3 Figura 18Nei polimeri le catene possonoallinearsi formando zone cristalline,oppure possono disporsi in mododisordinato generando zone amorfe.
1 Figura 19Le proprietà dei polimeri e la lorostruttura microscopica.
1 Figura 20La temperatura di fusione e la temperaturadi transizione vetrosa sono due parametriimportanti per scegliere il polimero adatto aun determinato utilizzo.
Amorfo Cristallino Semicristallino
I polimeri non sonomai completamentecristallini,coesistono partiamorfe e particristalline.
Amorfo Cristallino
Ordine
Disordine
amorfo
vetrosorigido
viscosogommoso
Tem
pera
tura
cristallino
temperaturadi fusione (tf)
polimeriamorfisolo tg
polimerisemicristallinitg e tf
liquido
temperaturadi transizionevetrosa (tg)
solido
REGOLARESTRUTTURASUPRAMOLECOLARE
STRUTTURACHIMICA
NATURA DEIMONOMERI
REGOLARITÀDELLE CATENE
PRESENZADI GRUPPIFUNZIONALI
GRADO DIPOLIMERIZZAZIONE
IRREGOLARE
POLIMEROAMORFO
FORMAZIONEDELLE CATENE
ORGANIZZAZIONEDELLE CATENE
PROCESSO DIPOLIMERIZZAZIONE
COESISTENZA ZONE AMORFE E CRISTALLINE:POLIMERO SEMICRISTALLINO
POLIMEROCRISTALLINO
PROPRIETÀ DEI POLIMERI (CARATTERISTICHE MACROSCOPICHE)
STRUTTURA MICROSCOPICA

D145
capitolo D4 I polimeri
Materiali Temperatura di transizionevetrosa (°C)
Temperaturadi fusione (°C)
Polietilene (bassa densità) ‒110 115Politetrafluoroetilene ‒97 327Polietilene (alta densità) ‒90 137Polipropilene ‒18 175Nylon 6,6 57 265Poliestere (PET) 69 265Cloruro di polivinile 87 212Polistirene 100 240Policarbonato 150 265
7 Tabella 3Temperature di transizione vetrosae di fusione di alcuni polimeri.
1 Figura 21Le diverse conformazioni delle catenegenerano un gomitolo disordinato.
Le caratteristiche dei polimeri:conformazione, configurazione e stereoregolaritàPer studiare l’organizzazione spaziale di un polimero bisogna tenere in conside-razione tre princìpi caratteristici delle molecole organiche: la conformazione, laconfigurazione e la stereoregolarità. Le conformazioni sono le possibili dispo-sizioni nello spazio di una molecola dovute alla libera rotazione intorno ai legamisingoli carbonio-carbonio. Se un polimero è costituito da catene alifatiche e si tro-va in soluzione o allo stato fuso, i legami singoli carbonio-carbonio hanno liberarotazione e possono dare un numero molto elevato di conformazioni. Questo puògenerare un «gomitolo disordinato» di catene detto random coil (figura 21).
Mentre una molecola può assumere diverse conformazioni grazie alla liberarotazione sui legami singoli, la configurazione può cambiare soltanto se si veri-fica la rottura di alcuni legami e la successiva formazione di nuovi. La configu-razione infatti rappresenta l’orientazione nello spazio degli atomi e dei gruppiatomici di una molecola che non può essere modificata per rotazione sui legamisingoli. L’isomeria ha un effetto importante sui polimeri, poiché a seconda del-la configurazione si possono avere macromolecole con proprietà molto diverse.Quando nell’unità strutturale della macromolecole sono presenti atomi di car-bonio con isomeria spaziale (isomeria geometrica di tipo cis-trans o centri chiraliresponsabili di isomeria ottica), la distribuzione di questi centri lungo la catenadetermina la stereoregolarità del polimero.
Consideriamo l’esempio del poliisoprene, ottenuto dalla polimerizzazionedell’isoprene (figura 22A).
L’isoprene è un monomero caratterizzato dalla presenza di due doppi legamicarbonio-carbonio (C=C). A seconda di come si dispone il monomero nella fasedi addizione, si possono avere il poliisoprene 1,4-cis chiamato comunementegomma naturale o caucciù, oppure il poliisoprene 1,4-trans chiamato guttaperca(figura 22B - C). Entrambi sono polimeri di origine vegetale prodotti rispettiva-mente da Hevea brasiliensis e dalle piante della famiglia delle Sapotacee. La diversaconfigurazione è responsabile delle proprietà dei due polimeri: mentre il caucciùha ottime proprietà elastiche, la guttaperca è un polimero rigido e poco elastico.
C
CH3
H2C
isoprene
C
H
CH2
5 Figura 22(A) Struttura dell’isoprene.L’isomeria cis-trans delpoliisoprene genera duepolimeri diversi: il caucciù(B) e la guttaperca (C).
RR
CH3
poliisoprene 1,4-trans (guttaperca)
CH3CH3 CH3
R
poliisoprene 1,4-cis (caucciù)
CH3 CH3
CH3 CH3
R
BA
C
Il caucciù ogomma naturale siestrae sotto formadi lattice dall’alberodella gomma(Hevea brasiliensis).
La guttaperca si usa in odontoiatria perchiudere i canali dopo la devitalizzazionedella polpa, la parte più interna deldente; questo polimero si ricava da
alcune piante del genere Palaquium.

D146
La stereoregolarità influenza le proprietà dei polimeriOltre all’isomeria geometrica di tipo cis-trans, un polimero può presentare isome-ria ottica. Se sono presenti atomi di carbonio legati a quattro sostituenti diversi,la stereoregolarità è determinata dalla configurazione dei centri stereogenici edalla loro distribuzione lungo la macromolecola.
Uno dei più importanti polimeri stereoregolari è il polipropilene, ottenutodalla polimerizzazione del propilene (figura 23A). A seconda di come avvienel’addizione nel processo di polimerizzazione si può ottenere polipropilene condiversa stereoregolarità. I monomeri di propilene sono planari, ma i due lati dellamolecola non sono equivalenti: per questo l’addizione da un lato o dall’altro gene-ra centri chirali con configurazioni diverse (figura 23B).
Quando l’orientazione dei centri stereogenici è la stessa lungo la catena polime-rica, il polimero è detto isotattico. Nel caso del polipropilene, i gruppi metile sitrovano sempre dalla stessa parte (figura 24A). Quando invece l’orientazione deicentri stereogenici varia lungo la catena in modo alternato, il polimero è dettosindiotattico. In questo caso, i gruppi metile del polipropilene si alternano daparti opposte (figura 24B). Quando, infine, l’orientazione dei centri stereogenicivaria lungo la macromolecola in modo casuale, il polimero è detto atattico. Inquesto caso i gruppi metile del polipropilene sono disposti da una parte all’altradella catena senza un ordine preciso (figura 24C).
La stereoregolarità influenza in modo significativo le proprietà dei polimeri.Grazie alla regolarità nell’orientazioni dei gruppi metile il polipropilene isotatti-co è un materiale con ottime proprietà meccaniche, al contrario del polipropile-ne atattico che presenta prestazioni meccaniche peggiori.
Le paroleUn centro stereogenico o stereocentroè rappresentato da un atomo dicarbonio legato a quattro sostituentitutti diversi tra loro.
⟶C=C
propilene
CH3
HH
H--C-C---
H
H
H
CH3n
polipropilene
A B3 Figura 23(A) Struttura tridimensionale di una molecoladi propilene. (B) Il polipropilene è un polimerocon un centro stereogenico nella sua unitàripetente.
-C-C-C-C-C-C-C-C-
CH3 CH3 CH3 CH3
-C-C-C-C-C-C-C-C-
CH3
CH3
CH3
CH3
-C-C-C-C-C-C-C-C-
CH3 CH3
CH3
CH3
3 Figura 24Il polipropilene isotattico (A),sindiotattico (B), atattico (C).
Polipropilene isotattico Polipropilene sindiotattico Polipropilene atatticoA B C
⟶
CH3CH
2-Al
Cl
ClCH
2
Cl
H3C
Cl Cl
=
C
C
H CH3
H H
CH3CH
2-Al
ClCH
2
Cl
H3C
TiCl Cl
C
C-H
H
CH3
H
---
----
Cl
Ti
3 Figura 25I catalizzatori Ziegler-Nattapermettono di ottenere ilpolipropilene isotattico.
Centrostereogenico
La polimerizzazione stereoregolare sfrutta catalizzatori Ziegler-NattaIntorno alla metà degli anni Cinquanta del secolo scorso, l’italiano Giulio Nattariuscì a sintetizzare il polipropilene isotattico utilizzando i catalizzatori messia punto dal chimico tedesco Karl Ziegler. Per la loro scoperta i due chimici ot-tennero il premio Nobel per la Chimica nel 1963. La polimerizzazione stereore-golare, detta anche polimerizzazione Ziegler-Natta, utilizza catalizzatori a basedi titanio e di derivati organometallici dell’alluminio [TiCl3 e Al(CH2CH3)2Cl]. Imonomeri di propilene interagiscono con il catalizzatore, coordinandosi sempredallo stesso lato: per questo le molecole si addizionano con la stessa orientazione,rendendo la polimerizzazione stereoselettiva (figura 25).
Nel corso degli anni è stata sviluppata un’ampia gamma di catalizzatori per lasintesi del polipropilene, variando i metalli coinvolti e i sistemi organometallici.Questo ha consentito di controllare la stereoselettività delle polimerizzazioni edi migliorare l’efficienza dei processi industriali.
Leggi l’approfondimento nell’ebookStoria della scienzaUn chimico del Nobel: Giulio Natta

D147
capitolo D4 I polimeri
Le proprietà fisiche dei polimeri:comportamento termico e proprietà meccanicheI polimeri possono differenziarsi tra loro per il comportamento termico e perle proprietà meccaniche. All’aumentare della temperatura alcuni possono de-formarsi diventando modellabili, altri invece rispondono in maniera contrariaindurendosi. Nella grande varietà dei polimeri naturali e sintetici rientrano ma-teriali che sono più rigidi e difficili da deformare, mentre altri sono più elastici epossono modificare facilmente le loro dimensioni. A seconda di queste caratteri-stiche, i polimeri possono essere suddivisi in tre gruppi (figura 26).
• Elastomeri o gomme: questi polimeri sono dotati di proprietà elastiche, cioèpossono subire un allungamento quando sono sottoposti a una tensione, recu-perando successivamente la dimensione originaria, una volta cessata l’azionedella forza.
• Plastomeri: sono polimeri dotati di plasticità, cioè sono modellabili. Questipolimeri rammolliscono per effetto del riscaldamento, diventando viscosi efluidi; una volta impartita loro una forma, possono solidificare per raffredda-mento. Variando la temperatura, il ciclo può essere ripetuto più volte.
• Resine sintetiche: sono un tipo di materie plastiche la cui lavorabilità cambia aseconda della temperatura; nelle resine termoplastiche l’aumento della tempera-tura porta alla fusione del polimero, mentre in quelle termoindurenti la tempera-tura innesca la reticolazione tra le catene, provocando l’indurimento irreversibiledel materiale. Le resine termoindurenti sono polimeri rigidi e poco deformabili.
Un’importante proprietà meccanica è la resistenza a trazione, un parametro checonsente di valutare la rigidità di un materiale. Questa viene rappresentata gra-ficamente attraverso la curva sforzo-deformazione, che descrive come varia l’allun-gamento di un campione all’aumentare della forza applicata (figura 27).
7 Figura 26Classificazione dei polimeri inbase al comportamento termicoe alle proprietà meccaniche.
7 Figura 27La resistenza a trazione sirappresenta attraverso la curvasforzo-deformazione.Allungamento
Resine
Plastomeri
Elastomeri
Forz
a
Snervamento
CRISTALLINI AMORFI
NON RETICOLATI
TERMOPLASTICI
ELASTOMERIO GOMME
RESINETERMOINDURENTI
RETICOLATI
SCARSAMENTE
POLIMERI
ALTAMENTE

D148
Gli elastomeri e le resine sono polimeri caratterizzati da catene reticolate, cioèlegate tra loro da legami covalenti. Quando i punti di reticolazione sono presentiin numero ridotto, il polimero può deformarsi facilmente e riesce a recuperare lapropria forma quando il carico applicato viene rimosso. Al contrario, quando lecatene sono fortemente reticolate, il materiale si presenta rigido ed è difficilmen-te deformabile. Nei plastomeri, invece, non sono presenti punti di reticolazione ele catene sono legate tra loro soltanto da interazioni intermolecolari.
Biopolimeri e biodegradabilitàI polimeri sono destinati alla produzione di tantissimi manufatti. A seconda delloro utilizzo, possono subire modificazioni nel loro aspetto e nella loro composi-zione per effetto di agenti fisici, chimici o ambientali. I processi di degradazioneche coinvolgono i polimeri sono quattro:
• degradazione termica: il calore può provocare la rottura di legami nella cate-na polimerica che può portare alla formazione di oligomeri e alterare i gruppifunzionali presenti;
• degradazione meccanica: fenomeni di usura, urti e sforzi meccanici possonomodificare l’aspetto del materiale e comprometterne le prestazioni;
• degradazione ossidativa: i polimeri possono subire reazioni di ossidazione adopera dell’ossigeno dell’aria, causando un peggioramento delle proprietà mec-caniche e delle caratteristiche estetiche (per esempio, l’ingiallimento);
• degradazione fotochimica: le radiazioni ultraviolette possono innescare rea-zioni radicaliche che vanno a modificare le catene polimeriche.
Attualmente la maggior parte dei polimeri vengono prodotti da risorse non rin-novabili come il petrolio ed è quindi importante tenere in considerazione il lorociclo di vita e il loro destino nell’ambiente. Un polimero deteriorato può esseresmaltito come rifiuto oppure riciclato. I polimeri ottenuti dalla polimerizza-zione di alcheni, detti anche poliolefine, sono macromolecole molto stabili perla presenza di un numero elevato di legami singoli carbonio-carbonio. A causadella particolare stabilità di questi legami, queste macromolecole necessitano dilunghi periodi di tempo per essere degradati, motivo per cui occorrono soluzionisostenibili per ridurre l’impatto legato al loro accumulo nell’ambiente.
Per far fronte all’esigenza di avere materiali polimerici ecocompatibili, negliultimi anni sono stati immessi sul mercato polimeri biodegradabili.
Un polimero si dice biodegradabile quando può essere decomposto in modonaturale dai decompositori presenti nell’ambiente (microrganismi come funghie batteri). Questi microrganismi, attraverso processi enzimatici, riducono le mo-lecole organiche complesse in costituenti più semplici come diossido di carbonio,metano, acqua e altri composti organici e inorganici che non hanno effetti dan-nosi sull’ambiente. Secondo gli standard UNI e ISO un polimero è biodegradabilese può essere degradato per il 90% del suo peso nell’arco di sei mesi.
Sono biodegradabili polimeri di origine naturale come la cellulosa, l’amido, leproteine. In presenza di acqua e di specifici enzimi, infatti, i legami glicosidici epeptidici possono essere spezzati mediante la reazione di idrolisi, permettendo cosìdi ripristinare i monomeri di partenza.
Negli ultimi anni sono stati immessisul mercato prodotti diversi polimeribiodegradabili come il Mater-Bi® e l’acido polilattico (PLA), utilizzati soprattut-to nel settore degli imballaggi e nel biomedicale. Oltre ad essere biodegradabili,questi polimeri sono anche biopolimeri perché si ottengono da fonti alternativeal petrolio, cioè da fonti rinnovabili come il mais e il granoturco.
È importante sottolineare che «biopolimero» non è sinonimo di «biodegra-dabile». Esistono infatti biopolimeri che non sono biodegradabili, mentre alcontrario esistono polimeri ottenuti da fonti fossili che sono biodegradabili. Peresempio, il Mater-Bi® è un biopolimero a base di amido di mais, un polisaccarideche contiene circa l’80% di amilopectina e il 20% di amilosio. Oltre all’amido,nel Mater-Bi® sono presenti anche alcuni polimeri di sintesi che permettono di
Ti ricordi?La reazione di idrolisi è il processochimico inverso alla reazione dicondensazione.

D149
capitolo D4 I polimeri
migliorare le proprietà meccaniche del materiale e di incrementarne la biodegra-dabilità, in particolare il policaprolattone (PCL) e polibutilentereftalato (PBT).Questi ultimi, nonostante derivino da fonti fossili, sono completamente biode-gradabili e consentono di migliorare le prestazioni del Mater-Bi®. Questo biopoli-mero è utilizzato per la produzione di sacchetti per la raccolta dell’umido lattico(figura 28) e nel settore agricolo per la produzione dei teli per la pacciamatura.
7 Figura 28I sacchetti compostabili sonorealizzati in Mater-Bi®, unpolimero biodegradabile.
7 Figura 29L’acido lattico (A) è unmonomero bifunzionaleda cui si ottiene l’acidopolilattico (B), utilizzato perprodurre suture chirurgichebioassorbibili.
Facciamoil punto
1. Che cosa si intende conpolimero amorfo e polimerocristallino?
2. Quali sono le differenze trapolipropilene isotattico,sindiotattico e atattico?
3. In base alle proprietàmeccaniche come vengonoclassificati i polimeri?
4. A quali tipi di degradazionepossono andare incontro imateriali polimerici?
5. Quali requisiti deve avere unpolimero per essere definitobiodegradabile?
OH
H3C OH
O
*
Gruppo ossidrilico
Gruppocarbossilico
Centrostereogenico
L’acido polilattico o PLA è un biopolimero ottenuto dalla polimerizzazione dell’a-cido lattico (figura 29) che si produce a partire dalla fermentazione di biomasse,in particolare dalla lavorazione dell’amido di mais, da barbabietola e canna dazucchero e da derivati della tapioca. L’acido lattico è un monomero asimmetricobifunzionale perché è costituito da un gruppo ossidrilico e un gruppo carbossi-lico, e presenta inoltre un centro stereogenico. La polimerizzazione avviene percondensazione tra il gruppo ossidrilico e il gruppo carbossilico e porta alla for-mazione di un poliidrossoestere. Il PLA è un omopolimero impiegato principal-mente per la produzione di imballaggi alimentari; grazie alla sua biocompatibili-tà, è utilizzato anche nel settore biomedicale, per il rilascio controllato di farmacie per le suture bioassorbibili.
A B

D150
SINTESIDI FINE CAPITOLO
Tipi di polimeriUn polimero è una molecola a elevatamassa molecolare (macromolecola)costituita dalla ripetizione di molecolepiù semplici dette monomeri, legate traloro da legami di tipo covalente. Le catenepolimeriche possono essere formate daun solo tipo di monomero (omopolimeri) omonomeri diversi (copolimeri).
A seconda di come sono legate traloro le unità monomeriche nella catena,si possono avere quattro tipi di copolimeri:random, alternato, a blocchi, aggraffato.
I polimeri si rappresentano attraversol’unità ripetente, che corrisponde algruppo di atomi che si ripete n voltelungo la catena polimerica e costituiscel’unità strutturale fondamentale diuna macromolecola. Il numero diunità ripetenti (n) determina il grado dipolimerizzazione del polimero.
Classificazione dei polimeriI polimeri naturali sono macromolecoledi origine biologica (o biomolecole) e sono icostituenti fondamentali degli organismiviventi. Appartengono a questa classei carboidrati come cellulosa, amido eglicogeno, le proteine e gli acidi nucleici(DNA, RNA).
I polimeri sintetici sono prodottiattraverso reazioni chimiche di sintesi,tipicamente a partire da monomeriottenuti dalla lavorazione del petrolio.Polimeri come polietilene, Teflon®,cellophane®, plexiglas®, nylon, fibreacriliche e poliuretano sono materieplastiche utilizzate in tantissimi beni diconsumo, come contenitori, pellicole perimballaggi, bottiglie, vernici, materialiper l’edilizia e fibre tessili.
Come si ottengonoi polimeri sinteticiI polimeri possono essere prodottiattraverso due meccanismi:• polimerizzazione di addizione o a
catena (polimeri di addizione);• polimerizzazione di condensazione o a
stadi (polimeri di condensazione).
Un polimero si forma per addizioneo per condensazione a seconda dellecaratteristiche chimiche dei monomeridi partenza, cioè segue la reattività deigruppi funzionali presenti nei reagenti.
La polimerizzazione per addizionee per condensazioneNella polimerizzazione per addizioneil polimero si forma per addizionisuccessive del monomero. Il meccanismodi polimerizzazione per addizione è dettoanche polimerizzazione a catena perché ognipassaggio dipende da quello precedente.I monomeri che seguono questomeccanismo sono soprattutto alcheni.
Per ottenere polimeri dicondensazione è necessario che imonomeri coinvolti siano almenobifunzionali e che la reazione siaaccompagnata dall’eliminazione dimolecole con massa molecolare ridotta,in genere acqua. La polimerizzazione dicondensazione viene anche detta a stadiperché diverse catene in accrescimentosi legano tra loro a formare unamacromolecola più grande.
Le proprietà dei polimeriLe proprietà del polimero non dipendonosoltanto dalla struttura chimica di ognisingola catena, ma anche dalla disposizionenello spazio delle macromolecole: questecaratteristiche definiscono la strutturasupramolecolare ovvero l’organizzazionetridimensionale del polimero. Quandole catene di un polimero hanno unadisposizione regolare nello spazio, ilpolimero si dice cristallino. Al contrario,quando le catene sono disposte in modoirregolare il polimero si dice amorfo.Quando nel polimero coesistono partiamorfe e parti cristalline, viene dettosemicristallino.
Le caratteristiche di un polimeroPer studiare l’organizzazione spaziale di unpolimero bisogna tenere in considerazionela conformazione, la configurazione e lastereoregolarità. Con conformazionisi intendono le possibili disposizioninello spazio di una molecola dovute allalibera rotazione intorno ai legami singolicarbonio-carbonio. La configurazionerappresenta l’orientazione nello spaziodegli atomi e dei gruppi atomici di unamolecola che non può essere modificata perrotazione sui legami singoli. Quando nellamacromolecola ci sono atomi di carboniocon isomeria spaziale (isomeria geometricadi tipo cis-trans o centri stereogeniciresponsabili di isomeria ottica), ladistribuzione di questi centri determina lastereoregolarità del polimero.
La stereoregolaritàLa stereoregolarità influenza in modosignificativo le proprietà dei polimeri.Quando l’orientazione dei centristereogenici è la stessa lungo la catenapolimerica, il polimero è detto isotattico.Quando invece l’orientazione dei centristereogenici varia lungo la catena inmodo alternato, il polimero è dettosindiotattico. Infine, se l’orientazionedei centri stereogenici varia lungo lamacromolecola in modo casuale, ilpolimero è detto atattico.
La polimerizzazione stereoregolare,detta anche polimerizzazione Ziegler-Natta, utilizza catalizzatori a base dititanio e di derivati organometallicidell’alluminio.
Proprietà fisichee degradazione di un polimeroI polimeri possono differenziarsi traloro per il comportamento termico e perle proprietà meccaniche. All’aumentaredella temperatura alcuni possonodeformarsi diventando modellabili,altri invece rispondono in manieracontraria indurendosi. A seconda diqueste caratteristiche, i polimeri possonoessere suddivisi in tre gruppi: elastomerio gomme, elastomeri, resine sintetiche(termoplastiche o termoindurenti).
A seconda del loro utilizzo, i polimeripossono subire modificazioni nel loroaspetto e nella loro composizioneper effetto di agenti fisici, chimici oambientali. I processi di degradazionesono: degradazione termica, degradazionemeccanica, degradazione ossidativa,degradazione fotochimica.
I polimeri biodegradabiliUn polimero deteriorato può esseresmaltito come rifiuto oppure riciclato. Perfar fronte all’esigenza di avere materialipolimerici ecocompatibili, negli ultimianni sono stati immessi sul mercatopolimeri biodegradabili che possonoessere decomposti in modo naturale daimicrorganismi presenti nell’ambiente.

D151
capitolo D4 I polimericapitolo D4 I polimeri
VERIFICALE TUE CONOSCENZE
Lezione 1
Macromolecole e polimeri1. Quale tra i seguenti è un
omopolimero?
A Teflon®.B Nylon.C PET.D HIPS.
2. Quale tra i seguenti è uncopolimero?
A Plexiglas®.B Cellulosa.C PP.D HIPS.
3. Un esempio di polimero sintetico è
A l’RNA.B il nylon.C una proteina.D la cellulosa.
Lezione 2
I polimeri di addizione4. Riporta accanto alla sigla il nome
del polimero corrispondente:
PVC: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
PE: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
PS: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
PP: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
PMMA: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
5. Quale polimero è ottenutoindustrialmente perpolimerizzazione di addizionecationica?
A Polistirene.B Nylon.C Poliisobutilene.D Polipropilene.
6. Quale fra le seguenti classi dicomposti può polimerizzare con unmeccanismo di addizione?
A Composti carbonilici.B Alcani.C Idrocarburi aromatici.D Alcheni.
7. La polimerizzazione di addizione
A avviene tra monomeri bifunzionali.B è tipica degli alcheni.C è accompagnata dall’eliminazione di
acqua.D è un processo a stadi.
8. La poliaddizione anionica prevedela formazione come intermedio direazione di
A un carboanione.B una specie radicalica.C un carbocatione.D un carbonio pentalegante.
9. La poliaddizione cationica prevedela formazione come intermedio direazione di
A un carboanione.B una specie radicalica.C un carbocatione.D un carbonio pentalegante.
10. Quale delle molecole riportate diseguito darà luogo facilmente a unareazione di poliaddizione?
A CH3—CH2—OHB CH3—CH3
C CF2CF2
D CH3—CH2—O—CH3
11. Gli idroperossidi organici sonoiniziatori di quale tipo?
A Termici.B Redox.C Fotochimici.D Cationici.
Lezione 3
I polimeri di condensazione12. Riporta accanto alla sigla il nome
del polimero corrispondente:
PET: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
PLA: . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
13. Quale polimero si ottiene perpolimerizzazione di condensazione?
A Polistirene (PS).B Polietilentereftalato (PET).C Polivinilcloruro (PVC).D Polietilene (PE).
14. Il nylon è una poliammide chesi ottiene mediante reazione dipolimerizzazione
A radicalica.B di condensazione.C cationica.D anionica.
15. Il PET è un poliestereche si ottiene dalla reazionedi polimerizzazione tra
A un diolo e un diacido.B un diacido e una diammina.C un diolo e una diammina.D un alcol e un acido carbossilico.
16. La gomma SBR è
A un copolimero alternato.B composto da butadiene e stirene.C un polimero di condensazione.D una resina termoindurente.
17. Le resine fenoliche si ottengonodalla policondensazionedel fenolo con
A acido maleico.B formaldeide.C urea.D fosgene.
Lezione 4
Le proprietà dei polimeri18. La guttaperca corrisponde al
A poliisoprene 1,4-cis.B poliisoprene 1,4-trans.C polibutadiene 1,4-cis.D polibutadiene 1,4-trans.
19. Il grado di polimerizzazione di unpolimero rappresenta il numero n di
A monomeri.B unità ripetenti.C catene polimeriche.D omopolimeri.
20. Quali dei seguenti polimeri èbiodegradabile?
A Polietilene.B Polipropilene.C Cellulosa.D Teflon®.
21. Un polimero, che durante ilriscaldamento si trasforma in unmateriale duro e infusibile, è unpolimero
A vulcanizzato.B termoindurente.C termoplastico.D lineare.
ONLINE

D152
28. Per ciascuna delle seguenti unitàripetenti:
1) H
-
--C-C--
-
H
--
H H( (
n
2)
--CH2-CH--
-
n
3)
--N -
n
N-C
H
-
H
=
O
- ---==
O
- -
4)
n
=
O=O
O
O
a) scrivi il nome del polimerorappresentato;
b) identifica il/i monomero/i dipartenza;
c) scrivi se è un omopolimero o uncopolimero;
d) indica se viene ottenuto attraversopolimerizzazione di addizione o dicondensazione.
29. L’1,3-butadiene è un diene coniugatoutilizzato come monomero per laproduzione del polibutadiene:
a) scrivi la formula dell’unità ripetentedel polibutadiene;
b) confronta il monomero e l’unitàripetente indicando l’ibridazione delcarbonio e la geometria;
c) spiega il meccanismo dipolimerizzazione;
d) indica quali isomeri si possonoottenere.
30. Rappresenta la formula razionaledi un omopolimero costituito da tremonomeri di:
a) propilene;b) stirene.
22. Scegli e motivale affermazioni false.
A Un polimero è atattico se nonpresenta sostituenti che sporgonodalla catena polimerica.
B Il polipropilene isotattico è in genereamorfo e colloso.
C Le catene di polimeri stereoregolari(isotattici e sindiotattici) sono adattea formare materiali densi e compatti.
D La conformazione di un polimero chesi forma spontaneamente è quellaatattica.
23. Con riferimento al Kevlar®, unafibra costituita dal polimero che hala formula seguente:
31. La bachelite è un polimero dicondensazione ottenuto mediantela reazione tra il fenolo e laformaldeide. Sapendo che il gruppometilenico –CH
2 è in posizione
orto e/o para rispetto all’ossidrilefenolico, rappresenta la formuladel polimero costituito da seimonomeri.
VERSO L'UNIVERSITÀ
Preparati ai test di ammissionesul sito Unitutor.
32. Quale delle seguenti classi dicomposti non ha strutturapolimerica?
A Polisaccaridi.B Polieni.C Poliesteri.D Proteine.E Acidi ribonucleici.[dal test di ammissione a Veterinaria, 2010-11]
TEST YOUR ENGLISH
Choose the correct answer.
33. The monomer unit of PVC is
A ethylene.B propene.C vinyl chloride.D styrene.
34. The isobutylene unit is common inmany synthetic polymers.Isobutylene is
A CH3—CHCH—CH3
B CH2CH-CH2—CH3
C (CH3)2CCH—CH3
D CH2C(CH3)2
35. Terital is an example of a
A polyamide.B polyacrylate.C polyester.D polyurethane.
36. Which of the following is athermosetting polymer?
A Polypropylene.B Teflon®.C Polyethylene.D Bakelite.
VERIFICALE TUE ABILITÀ
H
HNC
O
O
CN
n
a) scrivi la formula dei monomeri da cuideriva;
b) specifica il tipo di reazione dipolimerizzazione.
24. Considera il polimero aventeformula –[CH(CH
3)CH
2]
n– e
specifica:
a) da quale monomero deriva;b) di che tipo di polimerizzazione si
tratta;c) il nome del polimero.
25. Mostra il meccanismo dellapoliaddizione cationica delpropilene relativamente all’unionedi due unità monomeriche.
26. La cristallinità di un polimero
A peggiora le proprietà meccaniche.B aumenta con la temperatura.C è favorita dai legami a idrogeno.D è favorita da bassi gradi di
polimerizzazione.
27. L’1,1- dicloroetene e il cloruro divinile formano un copolimeroalternato. Rappresenta la formuladi una catena costituita da quattromonomeri.

D153
capitolo D4 I polimeri
VERSO L'ESAME:LE TUE COMPETENZE
IPOTIZZA E ARGOMENTA37. Dacron® e Kevlar® sono due fibre sintetiche utilizzate per
le vele delle navi. Il Dacron® è un poliestere ottenuto daglicole etilenico e dimetiltereftalato; il Kevlar® è una fibraaramidica ottenuta da 1,4-fenilendiammina e cloruro ditereftaloile.
1)
n
=
O
-O O
=O
2)
n
OH N
-
H
-
H
-
N
=
=
OH
O
a) Scrivi le formule di struttura dei monomeri di partenzae individua i gruppi funzionali presenti.
b) Riporta il meccanismo di polimerizzazione che permettedi produrre ciascun polimero.
c) Quale tra i due polimeri si presenterà tendenzialmentepiù cristallino? Quale ha prestazioni meccaniche migliori?
d) Se al posto della 1,4-fenilendiammina si utilizzassela 1,2-fenilendiammina si otterrebbe un polimerocon le stesse proprietà?
IPOTIZZA38. Il PLA o acido polilattico, polimero di condensazione
dell’acido lattico, è un materiale plastico che possiedesia un gruppo funzionale carbossilico sia un gruppofunzionale ossidrilico.a) Quale pensi possa essere il gruppo funzionale risultante
dal processo di condensazione?b) L’acido lattico è una molecola chirale: quale processo
si potrebbe usare per produrre selettivamente un soloenantiomero di tale molecola, da usare come materiaprima?
IPOTIZZA E ARGOMENTA39. Il poliidrossibutirrato (PHB) è un biopolimero scoperto
per la prima volta nel 1925 dal microbiologo franceseMaurice Lemoigne. Viene prodotto dal microrganismoBacillus megaterium come macromolecola di riserva sottoforma di granuli.
n
HOH
==
__
O
OCH3
a) Quali gruppi funzionali sono presenti nell’unità ripetente?b) Attraverso quale meccanismo di polimerizzazione si può
produrre?c) Il polimero presenta centri chirali? È stereoregolare?d) Può essere biodegradabile? Motiva la risposta ipotizzando
il meccanismo.
CLASSIFICA40. Assegna il nome dei polimeri rappresentati e la relativa
stereoregolarità:a)
CH3
-C
H
H
-
C
H
H
-C
H
H
-
C
H
H
-
C
H
H
-
C
H
CH3
-
C
H
CH3
-
C
H
H
-
C
CH3
H
-
C
CH3
b)CH
3
-
C
H
H
-
C
H
H
-
C
H
H
-
C
H
H
-
C
H
H
-C
H
CH3
-
C
H
CH3
-C
H
CH3
-
C
H
CH3
-
C
H
c)CH
3
-
C
H
H
-
C
H
H
-
C
H
H
-
C
H
H
-
C
H
H
-
C
H
CH3
-
C
H
H
-
C
CH3
H
-
C
CH3
CH3
-
C
H
capitolo D4 I polimeri
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .