Presentazione standard di PowerPoint · pag. 95/2 Il metabolismo degli amminoacidi. La principale...
Transcript of Presentazione standard di PowerPoint · pag. 95/2 Il metabolismo degli amminoacidi. La principale...
In base al valore biologico (ovvero al contenuto di AAE) si distinguono:
- p. ad alto valore biologico contengono tutti gli AAE (es. carne, pesce, uova,
latte e formaggi)
- p. a medio valore biologico uno o più AAE non sono presenti in quantità
significativa ai fini nutrizionali (es. nei legumi scarseggiano gli AA solforati)
- p. a basso valore biologico manca uno o più AAE (es. nei cereali manca l’AA
lisina)
Complementarietà delle proteine: p. a medio valore
biologico + p. a basso valore biologico (nello stesso
pasto) = pool completo di AAE (equivalenza nutrizionale
con p. ad alto valore biologico).
La classificazione delle proteine
La denaturazione è una qualsiasi modificazione della conformazione spaziale della
proteina, ma senza che questa comporti la rottura dei legami peptidici.
Generalmente la denaturazione è un processo irreversibile che comporta:
- perdita della struttura nativa della proteina
- perdita delle proprietà fisico-chimiche e biologiche
Può essere causata da:
- agenti fisici, ad es. calore, agitazione meccanica
- agenti chimici, ad es. acidi, basi, alcol
La denaturazione proteica
Sono proteine in grado di catalizzare una reazione
biologica (in pratica accelerano la velocità della
reazione).
Sono così costituti:
apoenzima + coenzima = oloenzima
(parte proteica) (parte non proteica)
Gli enzimi sono molto specifici per la reazione catalizzata e per i substrati
coinvolti.
Gli enzimi
L’attività degli enzimi dipende:
- dalla temperatura
- dal pH
- dalla concentrazione dei substrati
Secondo la nomenclatura convenzionale il nome degli enzimi è costituito dal
nome del substrato (o del processo chimico catalizzato) e dal suffisso -asi
(es. saccarasi è il nome dell’enzima attivo sul saccarosio).
Digestione delle proteine
La digestione delle proteine inizia
nello stomaco per azione dellapepsina (proteasi gastrica), attivata asua volta dall'acido cloridrico. Siformano così i polipeptidi (cateneformate da più aminoacidi)
gli enzimi contenuti nel succo
enterico (peptidasi), liberano i singoliaminoacidi, che assorbiti dai villiintestinali giungono al fegatoattraverso la vena porta.
I polipeptidi insieme alle proteine
denaturate passano nel duodenodove gli enzimi pancreatici (proteasi)li demoliscono a catene di aminoacidiancora più piccole.
gli enzimi digestivi determinano l’idrolisi delle proteine
Pepsina
Proteasi
Peptidasi
peptidi
proteina
amminoacidi
Grazie ai villi intestinali, gli AA liberati durante la digestione vengono assorbiti
a livello del tenue, e tramite la vena porta giungono al fegato per essere
metabolizzati.
pag. 94 La digestione delle proteine
Gli AA vengono utilizzati nell’organismo primariamente per la sintesi di proteine.
Gli AA, in base al loro destino metabolico, possono essere distinti in:
- glucogenetici se possono essere trasformati in glucosio
- chetogenetici se possono dare corpi chetonici
pag. 95/1 Il metabolismo degli amminoacidi
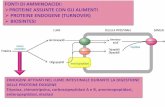
»Eliminazione dell’azoto
Il gruppo –NH2 dell’AA viene convertito in ammoniaca (NH3) che è una
sostanza tossica viene rapidamente trasformata in urea eliminata
attraverso le urine.
La trasformazione di ammoniaca in urea avviene
tramite una serie di reazioni nota come ciclo
dell’urea (localizzato nelle cellule del fegato).
pag. 95/2 Il metabolismo degli amminoacidi
La principale funzione delle proteine è di tipo plastico (o strutturale), ma
assolvono anche un ruolo regolatore (ad es. enzimi e alcuni ormoni).
Le proteine in eccesso vengono utilizzate per produrre energia o per la sintesi di
altre molecole.
pag. 96 Le funzioni delle proteine
1 g di proteine = 4 kcal = 17 kJ
Per un adulto sano la quantità di proteine consigliata è di 1 g/kg di peso
corporeo al giorno (circa il 10-15% dell’apporto energetico totale).
Il fabbisogno proteico varia in funzione:
- dell’età
- della massa corporea
- delle condizioni fisiologiche
- dell’apporto energetico della dieta e della qualità delle proteine ingerite
Eccesso proteico obesità e surplus di lavoro per i reni.
Carenza proteica deperimento generale e nelle gravi insufficienze un grave
stato patologico noto con il nome di kwashiorkor.
pag. 97 Il fabbisogno proteico