Presentazione di PowerPoint - Università degli Studi di …€¦ · PPT file · Web...
Transcript of Presentazione di PowerPoint - Università degli Studi di …€¦ · PPT file · Web...

Idrocarburi alifatici aciclici saturi: AlcaniGli alcani, caratterizzati da legami semplici C-C (saturazione), presentano desinenza –ano. I loro nomi, ricavati unendo radice+desinenza, saranno pertanto metano, etano, propano,butano pentano etc.
metano CH4
etano CH3-CH3
Propano CH3-CH2-CH3
butano CH3-CH2-CH2-CH3
Pentano CH3-CH2-CH2-CH2-CH3

I residui che si formano togliendo un idrogeno, conservano la stessa radice, ma cambiano la desinenza da –ano in –ile e saranno pertanto metile, etile, propile, butile, pentile etc.
alchile R- (generico)metile CH3-
metilene -CH2-
etile CH3-CH2-
propile CH3-CH2-CH2-
butile CH3-CH2-CH2-CH2-
pentile CH3-CH2-CH2-CH2-CH2-

1 2 3 4 5 6 7CH3 – CH – CH2 – CH – CH2 – CH2 – CH3 | | CH3 CH2 - CH3
4-etil-2-metileptano
I nomi dei residui si usano quando si presentano catene ramificate. L’alcano prende il nome dalla catena lineare più lunga, preceduto dai nomi dei residui che costituiscono le catene laterali (a loro volta preceduti dal numero d’ordine dell’atomo di carbonio della catena principale al quale il residuo è legato)
2-metilbutano CH3 – CH – CH2 – CH3
| CH3
La catena principale deve essere numerata in modo da dare il numero più basso possibile alle catene laterali. I residui vanno elencati in ordine alfabetico

Gli alcheni sono gli idrocarburi caratterizzati dalla presenza di un doppio legame carbonio-carbonio e quindi non saturi. Gli alcheni prendono il loro nome dai corrispondenti alcani di pari numero di atomi di carbonio: è sufficiente sostituire la desinenza –ano con –ene:
Il primo termine della serie è l'etene, o etilene: CH2=CH2
I termini successivi di questa famiglia di idrocarburi sono:Propene, o propilene: CH2=CH–CH3
Butene, o butilene: CH2=CH–CH2–CH3

Per l’etenile ed il 2-propenile è ancora in uso la vecchia nomenclatura: vinile e allile spesso usata nella nomenclatura di alcuni alcheni-derivati (vedi ad esempio l'alcol vinilico ed i relativi polimeri):
I residui che si formano togliendo un idrogeno agli alcheni, conservano la stessa radice, ma cambiano la desinenza da –ene in –enile e saranno pertanto:
etenile CH2=CH- vinile 1-propenile CH3-CH=CH- allile2-propenile CH2=CH-CH2-ecc.

Con il butene "inizia" il fenomeno dell'isomeria negli alcheni.L’isomeria è un fenomeno caratteristico dei composti organici. Si definiscono isomeri i composti chimici che presentano identica formula
grezza (e quindi medesima massa molecolare), ma diverse caratteristiche
chimiche e/o fisiche.

Isomeria costituzionale (o di struttura) - i composti differiscono per l’ordine con cui sono legati i loro atomi e presentano pertanto diversa
formula di struttura e può essere ricondotta a tre diverse cause 1 - Isomeria di catena
n-butano Isobutano (2-metilpropano)
CH3 – CH2 – CH2 – CH3 CH3 – CH – CH3|
CH3
1-propanolo
CH3 – CH2 – CH2 |
OH
2-propanolo
CH3 – CH – CH3|
OH
2 - Isomeria di posizione (del gruppo funzionale o del doppio legame)
1-butene CH2 = CH – CH2 – CH3
2-butene
CH3 – CH = CH – CH3

3 - Isomeria di gruppo funzionale – (Diverso tipo di gruppo funzionale) Etanolo CH3 – CH2 | OH
Etere dimetilico CH3 – O – CH3
Isomeridi
catena
Isomeridi
posizione
Isomeridi
gruppo funzionaleDiversa
concatenazione degli atomi di carbonio
Diversa posizione del medesimo gruppo funzionale
Diverso gruppo funzionale
Riassumendo

L'isomeria conformazionale deriva dalla possibilità di rotazione attorno al legame semplice carbonio-carbonio, ed alle diverse disposizioni spaziali che gli atomi o i raggruppamenti atomici possono assumere come conseguenza di tale rotazione.
L'isomeria configurazionale è una forma di isomeria spaziale in cui gli isomeri possono essere trasformati l’uno nell’altro solo rompendo legami chimici e scambiando di posizione i gruppi legati ad un atomo di carbonio.
StereoisomeriaLa stereoisomeria descrive gli isomeri che, pur mantenendo inalterati i legami tra gli atomi, differiscono per la loro disposizione nello spazio tridimensionale e presentano pertanto diversa formula spaziale.
In relazione alla modalità con cui gli stereoisomeri possono idealmente essere convertiti l’uno nell’altro si può distinguere

Trans-2-butene Cis-2-butene
Nell’isomero cis i due gruppi metilici si trovano dallo stesso lato rispetto al doppio legame, mentre nell’isomero trans si trovano su lati opposti.
Isomeria geometrica (o cis-trans)
L’isomeria geometrica è una forma di isomeria configurazionale che deriva dalla presenza nella molecola di un elemento di rigidità (doppio legame) che impedisce alla molecola di ruotare liberamente e attorno ad un legame Carbonio-Carbonio.

La forma definita isobutene non è un isomero geometrico. Infatti, l'isomeria geometrica non può esistere se uno dei due atomi impegnati nel doppio legame è legato a due gruppi uguali. (in realtà
andrebbe definito 2-metil propene):

Gruppi Funzionali Contenenti Legami Multipli Carbonio-Carbonio
Gruppo Funzionale Nome Esempio Nome IUPAC Nome
Comune
Alchene H2C=CH2 Etene Etilene
Alchino HCCH Etino Acetilene
Arene C6H6 Benzene

Gruppi Funzionali Contenenti un Atomo Elettronegativo Legato al Carbonio con un Legame Singolo
Gruppo Funzionale Nome Esempio Nome IUPAC Nome Comune
Alogenuro H3C-I Iodometano Ioduro di metile
Alcol CH3CH2OH Etanolo Alcol Etilico
Etere CH3CH2OCH2CH3 Dietil etere Etere
Ammina H3C-NH2 Amminometano Metilammina
Nitro Composto H3C-NO2 Nitrometano
Tiolo H3C-SH Metantiolo Metil mercaptano
Solfuro H3C-S-CH3 Dimetil solfuro

Gruppi Funzionali Contenenti un Eteroatomo Legato al Carbonio con Legami Multipli
Gruppo Funzionale Nome Esempio Nome
IUPAC Nome Comune
Nitrile
H3C-CN
Etanonitrile
Acetonitrile
Aldeide H3CCHO Etanale Aldeide acetica
Chetone H3CCOCH3 Propanone Acetone
Acido carbossilico
H3CCO2HAcido
Etanoico Acido acetico
Estere H3CCO2CH2CH3 Etil etanoato Acetato di etile
Cloruro acilico
H3CCOCl Etanoil cloruro Cloruro di acetile
Ammide H3CCON(CH3)2
N,N-Dimetiletana
mmide
N,N-Dimetilacetammi
de
Anidride acilica
(H3CCO)2OAnidride Etanoica Anidride acetica

DIVERSI MODI DI RAPPRESENTAZIONE DEI COMPOSTI CHIMICI:GLI ISOMERI DI FORMULA C4H10O
Struttura di Kekulé Struttura Condensata Struttura lineare

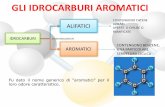
Classificazione Schematica degli Idrocarburi

Nomenclatura degli Alcani Lineari
Nome Formula Molecolare
Formula di Struttura Isomeri Nome Formula
MolecolareFormula di Struttura Isomeri
metano CH4 CH4 1 esano C6H14 CH3(CH2)4CH3 5
etano C2H6 CH3CH3 1 eptano C7H16 CH3(CH2)5CH3 9
propano C3H8 CH3CH2CH3 1 ottano C8H18 CH3(CH2)6CH3 18
butano C4H10 CH3CH2CH2CH3 2 nonano C9H20 CH3(CH2)7CH3 35
pentano C5H12 CH3(CH2)3CH3 3 decano C10H22 CH3(CH2)8CH3 75
i. Le formule e le strutture di questi alcani aumentano uniformemente di un CH2 . ii. Una variazione uniforme di questo genere in una serie di composti è chiamata omologa. iii. Tutte queste formule soddisfano la regola CnH2n+2 . Questo è anche il più alto possible rapporto H/C per idrocarburi. iv. Poichè il rapporto H/C in questi composti è il massimo, li chiameremo saturi (con idrogeno).

Orbitali Atomici Del Carbonio ed Orbitali Ibridi sp3
C:1s2 2s2 2p2

GLI ISOMERI DI STRUTTURA DELL'ESANO

Regole IUPAC per la Nomenclatura degli Alcani Ramificati
Trovare e nominare la più lunga catena di atomi di carbonio.
Identificare e nominare i gruppi alchilici attaccati a questa catena.
Numerare la catena partendo dall'atomo di carbonio terminale più vicino al gruppo sostituente.
Designare la posizione di ogni gruppo alchilico sostituente con l'appropriato numero e nome.
Assemblare il nome, elencando i gruppi in ordine alfabetico. I prefissi di, tri, tetra, etc., usati per designare più di un gruppo dello stesso tipo, non sono considerati ai fini dell'elencazione in ordine alfabetico.
Se sono presenti due o più catene di eguale lunghezza, si scieglie quella con il maggior numero di sostituenti.


I NOMI IUPAC DEGLI ISOMERI DELL'ESANO
B 2-metilpentano C 3-metilpentano
D 2,2-dimetilbutano E 2,3-dimetilbutano

Conformazioni Limite nell' Etano
Nome del Conformero
Struttura a Cunei Struttura a Cavalletto Proiezione di Newman
Repulsioni nell'Etano

Energia Potenziale dell’Etano in Funzione dell’Angolo Diedro