PCR - REAZIONE a CATENA della POLIMERASI E IL mezzo per produrre in vitro grandi quantità di una...
-
Upload
thorello-viviani -
Category
Documents
-
view
219 -
download
3
Transcript of PCR - REAZIONE a CATENA della POLIMERASI E IL mezzo per produrre in vitro grandi quantità di una...

PCR - REAZIONE a CATENA della POLIMERASI
E’ “IL” mezzo per produrre in vitro grandi quantità di una specifica sequenza di DNA, partendo da DNA estremamente complesso.
Primer a RNA
Nuovo filamento
DNA polimerasi
DNA stampo
Nuovo filamento
Primers a RNA
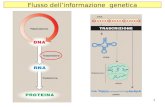
Il principio a cui si ispira la PCR è la replicazione del DNA:
REPLICAZIONE
5’3’
5’ 3’DNA stampo
PCR
1
1 x 109
PCR
DNA
3’
Primer oligonucleotidic
o
5’3’
DNA polimerasi termostabile Nuovo filamento
5’
5’3’5’3’

Le FASI della PCR
Allungamento(~ 70°C)
Denaturazione(~ 95°C)
Annealing(~ 60°C)
DENATURAZIONE:
Il DNA viene denaturato mediante riscaldamento in provetta a ~ 92-95°C
ANNEALING:La miscela viene raffreddata fino a raggiungere la temperatura che garantisce la specifica ibridazione dei primers alle regioni dello stampo ad essi complementari
ALLUNGAMENTO:La temperatura della miscela viene portata a 68-72°C consentendo alla DNA polimerasi termostabile di sintetizzare il filamento complementare allo stampo a partire dall’innesco oligonucleotidico

5’3’
primer 1
5’ 3’
3’ 5’
primer 2
i filamenti vengono separati ed i primers si
appaiano
i primers si estendono
3’ 5’
complementarietà al primer 1
5’ 3’
complementarietà al primer 2
i filamenti vengono separati ed i primers si
appaiano5’3’
3’5’
i primers si estendono
3’5’
5’3’
filamenti di lunghezza omogenea
filamenti di lunghezza variabile
5’
3’3’5’
regione di interesse
3’5’
complementarietà al primer 1
complementarietà al primer 2
i filamenti vengono separati ed i primers si
appaiano
i primers si estendono
3’5’
5’3’
3’5’
5’3’
I°step
II°step
III°step
Frammenti desiderati (quelli di lunghezza variabile non sono
mostrati)
E così via
PCR

I primi 4 cicli della PCR in dettaglio
DNA stampo
Frammento desiderato
1° ciclo
2° ciclo3° ciclo 4° ciclo
35° ciclo
Amplificazione esponenziale
21 = 2 22 = 4 23 = 8 24 = 16 235
Numero di copie di DNA contenenti il
frammento desiderato
Numero di copie di DNA della corretta
lunghezza contenenti il frammento desiderato
0 0 2 8

PROGETTAZIONE dei PRIMERS
Caratteristiche di un buon primer:
Una sequenza di 16 bp sarà statisticamente presente solo una volta ogni 416 bp (~ 4 miliardi di basi) corrispondenti circa alla grandezza del genoma umano.
Lunghezza: 16 bp o più
La Tm dipende dalla lunghezza e dalla sequenza del primers
Tm = 4(G+C)+2(A+T)°C
~ 2-5°C al di sotto della più bassa Tm dei due primers usatiT annealing
Tm primer 1 Tm primer 2~
Se la Ta dei due primers è molto diversa si possono verificare amplificazioni asimmetriche o a singolo filamento.
Assenza di sequenze ripetute invertite che possano far ripiegare il primers su se stesso o di sequenze complementari fra i primers che causano l’amplificazione di dimeri dei primers

PROGETTAZIONE “COMPUTERIZZATA” dei PRIMERS
rev
rev
for
3314
842
425
GTGTGCGTACAGCGCAAC
GGGTGGGACCTGGGCGCCCCCGCCGTGAGCGCCTACTGCTCCACCTGGGACGCCGGCAAGCCGTACTCG
1859 1876
5’- -3’Primer REVPrimability of Match = 71%Stability of Match = 44%
Primer REVPrimability of Match = 100%Stability of Match = 81%
2264 2281
CATGCATGATGCTCAAATGCCGCATTGTTGCGCTGTACGCACACATGTATGAATGCATGGCACGGATCAA
GTTGCGCTGTACGCACAC
-5’3’-
GGACACGTATGCCACAGCCC
TGCTAAATTTTCCAGCTAGGTAGCAGGACACGTATGCCACAGCCCTTAAAAGCATATCTGCACATGTCTT
1442 1461
5’- -3’Primer FORPrimability of Match = 100%Stability of Match = 82%

...PROGETTAZIONE “COMPUTERIZZATA” dei PRIMERS
CTTTTGGCATAGACCACATGCCA5’ TGTTACAAGTGTGGATGGATGCC5’
GGCCAGTGAATTCAGCTCACGCCCCAAATATGCAGCTTCCAGTCCAGTTTCATCCGGCGCGCTGAAGATTTTTTAGAGCATGCTCTATTATGCAGCGTCCGTTGGAATGCTCTTTTTAACTCCGCGCGCGCTAAACTTGCGATTTTTTGGGCGCGGCGCTGATATTGGGCGTCTGTTGAAGATGCTCTTAAGTGGCCACAAGGGAGATGGGTCGGGCTAAGGTTTCATATCTTACAATATAAAGTTGAAGACGATTTGTGGCACCCAGGGGCGGGAGACGCATGCATGCAGCTGCATGATTGCACCAAGATCCGAAGAGTGGTTTATGGTTTGAGCTTAATTACTGCATGCATGCAACTTTTTGGTACAACTTTTGGCATAGACCACATGCCATCCCACCTCCCATGCTTTTCATTTTTACTTGTAAATTTGGATCTATTATATCTTTTGAATCAAAAGTTCAATTTATATTTCGTTTGCGTATTCTTGTCCCTTGTGTCGAGAGCTTTGAAACAAGCCCACTTTTGAATACGTTTTGACAAATTCTAAAAACTTAAGTGAGTTTCAACTGCTAAAACTTGATAGAATGAATGAAAAATTTAGCAAGTTTCAAAGACTAAAACTGAAACCCTAAGCCCTTAGCCCTAGATCCTAAGCCCTAAGCCGGAAGTCCTAAACCGTATGCCCCTAACA
Tm = 58.6 Tm = 56.1
Tm = 83.6
? Clear Open file Calculate Minimum stem size:Minimum 3’ overlap:
4
2
Optimal annealing temperature is 56.7. 3’ end of oligo 1 pairs to positions 5 to 10 of itself.

COMPONENTI di una REAZIONE di PCR
Stampo DNA a doppio filamento
Deossiribonucleotidi trifosfati Miscela equimolare di dATP, dTTP, dGTP, dCTP
PrimersOligonucleotidi complementari a regioni dei filamenti opposti che fiancheggiano la sequenza DNA bersaglio
Tampone contenente cloruro di magnesio
Lo ione Mg2+ è essenziale per il funzionamento dell’enzima
EnzimaTradizionalmente viene usata la Taq polimerasi, enzima termostabile estratto dal batterio termofilo Thermus aquaticus
dNTPMg2+

I FATTORI CRITICI della PCR…nella miscela di reazione
Non utilizzare quantità eccessive di stampo, primers e/o dNTP al fine di evitare amplificazioni non specifiche.
Dosare accuratamente la [Mg2+] in funzione della quantità di stampo, primers e dNTP utilizzata
Mg2+ è indispensabile al funzionamento della Taq polimerasi, ma è chelato da stampo, primers e dNTP. Se in eccesso causa una perdita di fedeltà da parte dell’enzima.
Selezionare l’enzima più idoneo alle proprie necessità
Emivita alla temperatura di denaturazioneProcessività Capacità di correzione degli errori
Taq,Pfu...

I FATTORI CRITICI della PCR…nella programmazione
94°C1’
72°C1’
Emivita Taq polimerasi: 30 min a 95°C~30 cicli di denaturazione di 1 min
TDEN › 95°C o N. cicli › 30 Diminuire il tempo di denaturazione/ciclo
TEMPERATURA e TEMPO di DENATURAZIONE
91-97°C a seconda della complessità dello stampo
Quindi, se:
60°C30’’
TEMPERATURA e TEMPO di ANNEALING
TANN troppo bassa amplificazione aspecifica
TANN troppo alta amplificazione con bassa resa
TANN ~ TMELTING
o primers lunghi Allungare il
tempo di annealing
TEMPERATURA e TEMPO di ALLUNGAMENTO
TEMPERATURA: 68-72°C a seconda dell’enzima
TEMPO: 1min / Kb di amplificato
ALLUNGAMENTO FINALE di 7-10 min per completare la sintesi degli eventuali prodotti parziali
NUMERO di CICLI
Dipende da [stampo]iniziale
3x105 molecole iniziali
25-30 cicli
50 molecole iniziali
40-45 cicli
N.B. Dopo 30-35 cicli:
- l’attività dell’enzima si
riduce- primers e dNTP si
esauriscono

STRATEGIE per AUMENTARE la SPECIFICITA’
TOUCHDOWN PCR
Den. 30 sec 94°C
Ann. 30 sec Tm(+5°C) -1°C/ciclo
All. 1 min/Kb 72°C
10 cicli
Den. 30 sec 94°C
Ann. 30 sec Tm(-5°C)
All. 1 min/Kb 72°C
20cicli
Den. iniziale
3-5 min 94°C 1 ciclo
All.finale 7 min 72°C
1 ciclo
Manteni-mento
4°C
Den. 30 sec 94°C
Ann. 30 sec Tm(-5°C)
All. 1 min/Kb 72°C
30cicli
Den. iniziale
3-5 min 94°C 1 ciclo
All.
finale 7 min 72°C1
ciclo
Manteni-mento 4°C
PCR CLASSICA

...STRATEGIE per AUMENTARE la SPECIFICITA’
HOT START NESTED PRIMER PCR
La PCR “hot start” previene la formazione di questi prodotti non specifici in quanto un componente chiave della miscela di reazione (enzima o MgCl2) viene aggiunto dopo lo step di denaturazione iniziale.
Durante l’allestimento della reazione di PCR o durante il riscaldamento iniziale del campione si possono verificare situazioni di appaiamento non specifico fra primers e stampo.
Fra 40 e 50°C la Taq polimerasi ha un’efficiente attività polimerasica e può estendere i primers non correttamente appaiati.
Perché realizzare una PCR “hot start”?
NOVITA’: Enzimi “Hot start”
Gocce di cera
Procedura:
L’amplificazione è realizzata con un set di primers
Il prodotto è riamplificato con un set di primers interni ai precedenti
I prodotti non specifici amplificati nella Ia PCR non saranno amplificati nella IIa
5’3’
3’5’
5’ 3’
3’ 5’
Ia PCR
IIa PCR
5’3’
3’5’
5’
3’5’
3’
pr. nestedpr. nested

TT
r
CLONAGGIO dei PRODOTTI di PCR
La Taq e altre polimerasi hanno un’attività trasferasi-terminale che conduce all’aggiunta di un singolo nucleotide all’estremità 3’ dei prodotti di PCR.
In presenza dei 4 dNTPs è preferenzialmente aggiunto dA.
5’ A-3’
5’3’-A
I prodotti di PCR possono quindi essere agevolmente clonati in plasmidi aperti che contengono un deossitimidin nucleoside (dT) alle estremità 5’.
Siti di clonaggio multiplo

APPLICAZIONI della PCR
Produzione di sonde oligonucleotidichePCR
Clonaggio e manipolazione dei geniPCRPC
R
Tipizzazione dei geni e del DNA:
-caratterizzazione di ricombinanti batterici
-diagnosi cliniche
-analisi di campioni biologici in medicina legale
PCRPC
R
PCRPC
R
Mutagenesi casuale o sito-specificaPCR
PCRPC
R

CLONAGGIO e MANIPOLAZIONE di GENI
STRATEGIA
Presentano varie opzioni a certe posizioni della sequenza rendendo possibile l’annealing e l’amplificazione di sequenze omologhe da organismi differenti
Primers degenerati
R = A, G H = A, C, TY = C, T B = C, G, TW = A,T V = A, C, GM = A,C D = A, G, TK = G, T N o I= A, C, G, TS = C, G
Sequenza genica nota
Caso 1: Caso 2:
Sequenza genica omologa notao
sequenza proteica nota
Si amplifica il gene desiderato direttamente dal DNA genomico o
dall’’RNA
Si disegna un primer specifico Si disegna un primer degenerato
N.B.I primers possono essere disegnati in maniera tale da contenere al 5’ la sequenza di specifici siti di restrizione che possono essere sfruttati per l’inserimento dei prodotti di PCR nei vettori di clonaggio.
5’-TCGAATTCNCCYAAYTGNCC-3’ EcoRI

Sintesi primo filamento cDNA
AAAAA-3’7-mG
Aggiunta coda omopolimera al primo filamento cDNA
Trasferasi terminale+ dATP
Trascrittasi inversa+ GSP1
GSP1
5’3’-AAAAAAAAA
Sintesi secondo filamento cDNA
AAAAA-3’7-mGmRNA
GSP1
5’3’-AAAAAAAAA GSP1
TTTTTP
GSP1
complementarietà al primerGSP1
complementarietà al primerP(dT)
TTTTP
TTTTTP GSP1’
I° gruppo di amplificazioni
5’
5’3’
3’
5’AAAAAP’ GSP1
3’
TTTTTP GSP1’
5’ 3’
II° gruppo di amplificazioni
TTTTTP GSP1’
5’ 3’
GSP2
5’AAAAAP’ GSP1
3’
TTTTTP
5’AAAAAP’3’ GSP2
TTTTTP5’ 3’GSP2’
Prodotto PCR finale
5’ - RACE Rapid Amplification Complementary Ends

3’ - RACE Rapid Amplification Complementary Ends
Sintesi primo filamento cDNA
AAAAAAAA-3’7-mG
Trascrittasi inversa+ P(dT)
AAAAAAAA-3’7-mGmRNA
TTTTTP
Sintesi secondo filamento cDNA
GSP1
GSP1 complementarie
tà al primerP(dT)
I° gruppo di amplificazioni
TTTTT P 5’3’
complementarietà al primerGSP1
5’ GSP1
AAAAA P’ 3’
TTTTT PGSP1’
5’3’
TTTTT PGSP1’
5’3’GSP2
5’ GSP1
AAAAA P’ 3’
TTTTT P
GSP2
5’ AAAAA P’ 3’
5’3’ GSP2’
TTTTT P
II° gruppo di amplificazioni
Prodotto PCR finale

MUTAGENESI CASUALE
In che modo delle mutazioni nel gene influenzano la funzione del prodotto??
ER OR PRONE PCRR
PREMESSA:
La frequenza di errore delle DNA polimerasi è ~allo 0,001 ‰ (una base ogni 106 nucleotidi)
grazie ad un’attività corretrice 3’ 5’ che rimuove i nucleotidi male incorporati.
E’ possibile indurre l’aumento di errori nella PCR utilizzando:
Taq polimerasi prive di attività correttriceBasse temperature di annealing che diminuiscono la fedeltàIneguali concentrazioni dei dNTPElevate concentrazioni di MgCl2Alto numero di cicli (60-80)Amplificazioni successive del prodotto di PCR

primer con differenza di un solo nucleotide
sequenza bersaglio
nucleotide originale
nucleotide cambiato
LEGENDA
DNA lineare amplificato
DNA plasmidico circolare con
incisure e nucleotide cambiato
3
4
2
1
PCR PCR
Filamento 1
Filamento 2 Filamento 3
Filamento 4
Filamento 1
Filamento 3 Filamento 2
Filamento 4
Denaturazione, rinaturazione
Trasformazione di E. coli
MUTAGENESI SITO-SPECIFICA

Amplificazione sequenza bersaglio
+quantificazione dell’espressione genica
identificazione del prodotto di amplificazione specifico rispetto a prodotti aspecifici
analisi simultanea di due campioni nella stessa reazione
individuazione di mutazioni puntiformi
… on-line e in tempo reale!
REAL-TIME PCR

LigthCycler SYSTEM
Caratteristiche:
Come mezzo di trasmissione della temperatura dalla resistenza ai campioni viene utilizzata l’aria che, essendo virtualmente senza massa, rende questo processo molto veloce.
Le reazioni vengono preparate in capillari di vetro borosilicato che, avendo un alto rapporto superficie:volume, assicurano una rapida equilibrazione fra l’aria ed i componenti della reazione.
Una reazione di PCR di 30-40 cilci può essere completata in 20-30 min.
Rapide variazioni di temperatura durante i cicli termici
Monitoraggio on-line e simultaneo dell’amplificazione dei vari campioni mediante sistemi di rilevamento della fluorescenza
Roche

...LigthCycler SYSTEM
resistenza
capillari(max 32)
camera termica
filtriLED
ventilatore
canali di rilevamento fluorimetrico
L’unità ottica è dotata di un LED come sorgente di luce e di tre canali di rilevamento che misurano la luce emessa a tre differenti lunghezze d’onda:
530nm 640nm 710nm
I valori di fluorescenza rilevati vengono visualizzati sullo schermo del computer consentendo il monitoraggio on-line della reazione di PCR.
L’intensità del segnale prodotto dal fluoroforo è proporzionale alla quantità del prodotto di PCR.
Numero di cicli
Flu
ore
scen
za
L’aumento dell’intensità del segnale inizia a cicli differenti a seconda della concentrazione iniziale del DNA bersaglio.

SYBR Green
E’ un colorante fluorescente che si lega solo al DNA a doppio filamento ed emette la fluorescenza solamente in queste condizioni.
DENATURAZIONENon viene rilevata fluorescenza
L’intensità della fluorescenza comincia ad aumentare
ANNEALING
ALLUNGAMENTO
L’intensità della fluorescenza continua ad aumentare e diventa massima al termine della fase di
allungamento
L’AUMENTO DELLA FLUORESCENZA E’ REGISTRATO A 530nm
SYBR Green
Primer Luce emessa
Polimerasi

SONDE di IBRIDAZIONE
Due sonde oligonucleotidiche sequenza-specifiche, marcate con coloranti diversi, ibridizzano con la sequenza bersaglio sul
filamento di DNA amplificato in un arrangiamento testa-coda che consente
l’emissione della fluorescenza.
DENATURAZIONENon viene rilevata fluorescenza:
il colorante donatore è eccitato dalla sorgente ed emette energia in grado di eccitare
l’accettore solo se la distanza fra i due è pari a 1-5 nucleotidi
Colorante donatore
Colorante accettore
ANNEALINGViene registrata la massima fluorescenza
L’AUMENTO DELLA FLUORESCENZA E’ REGISTRATO A 640nm
Oligo 1Fluoresceina Oligo 2
LC Red 640
Prodotto di amplificazione
EccitazioneEmissione
Trasferimento
1-5 nucleotidi

ANALISI della CURVA di MELTING
Consente di identificare il prodotto di amplificazione specifico rispetto a prodotti aspecifici.
Al termine della PCR la temperatura viene lentamente aumentata inducendo un decremento della fluorescenza.La temperatura in corrispondenza della quale si ha un repentino decremento della fluorescenza corrisponde alla Tm del prodotto.
Curva di fluorescenza
0 10 20 30 40 50
3.0
2.5
2.0
1.5
1.0
0.5
0
0 copie
10 copie
104 copie
Flu
ore
scen
za
Cicli di amplificazione
65 70 75 80 85 90 95
104 copie10 copie 0 copie
Temperatura (°C)
Flu
ore
scen
za
100
80
60
40
20
0
Curva di melting
Derivata negativa della curva di melting
65 70 75 80 85 90 95
Temperatura (°C)
-dF/
dT
TM
104 copie10 copie 0 copie
100
80
60
40
20
0
prodotti non
specifici

QUANTIFICAZIONE del PRODOTTO di PCR
Identificando il primo ciclo della PCR in corrispondenza del quale inizia l’amplificazione esponenziale del prodotto è possibile quantificare la concentrazione iniziale del DNA bersaglio.
104 copie105106
Numero cicli
Flu
ore
scen
za
Curva di fluorescenza di campioni a concentrazione nota
Estrapolazione della curva standard
N.
cic
liLog concentrazione
104 copie105106
linea di base
La linea di base identifica il ciclo in corrispondenza del quale inizia l’aumento esponenziale della fluorescenza per ciascun campione.
Riportando in grafico il valore di intersezione con la linea di base in funzione del Log della concentrazione iniziale di ciascun campione si ottiene la curva standard da cui si può estrapolare il valore della concentrazione di campioni a titolo ignoto.

MULTIPLEX PCR
Fluorecseina LC Red 640 Fluorecseina LC Red 705
Consente l’analisi simultanea di due campioni nella stessa reazione
Due coppie di Sonde di Ibridazione, ciascuna specifica per un prodotto di amplificazione, vengono marcate con un diverso colorante accettore che emette la fluorescenza a differenti lunghezze d’onda.
STRATEGIA:
Il segnale emesso viene letto simultaneamente attraverso due
canali di rilevamento fluorimetrico.
Canale 3 705 nm
Canale 2640 nm
Eccitazione
Trasferimento
Emissione

ANALISI di MUTAZIONI PUNTIFORMI
Sfrutta differenze nella Tm di Sonde di Ibridazione perfettamente legate al DNA bersaglio o il cui legame è destabilizzato dalla presenza di basi non appaiate.
gene mutato
La Sonda 1 si ibridizza alla parte della sequenza bersaglio
mutata
La Sonda 2 si ibridizza alla parte della sequenza bersaglio non
mutata
gene selvatico
Sonda 1marcata con Fluoresceina
Sonda 2marcata con LC Red 640
Al termine della PCR si analizza la curva di melting: se è presente una mutazione, la Tm dell’ibrido sarà più bassa che in assenza di mutazione.
Temperatura50 55 60 65 70 75 80
omozigote wildtypeomozigote mutanteeterozigote
3.0
2.5
2.0
1.5
Flu
ore
scen
za
50 55 60 65 70 75 80 Temperatura
0.25
0.20
0.15
0.10
0.05
0.00
-0.05
-dF/
dT

L’ETICHETTATURA nei REGOLAMENTI C.E.E.
Disciplina la vendita di prodotti contenenti OGM destinati al consumo umano ed introduce la nozione di sostanziale equivalenza : due alimenti sono considerati sostanzialmente equivalenti quando non presentano alcuna differenza dal punto di vista nutrizionale, organolettico e della sicurezza.
Rende inoltre obbligatoria l’etichettatura degli alimenti transgenici che non siano sostanzialmente equivalenti ai prodotti convenzionali.
REGOLAMENTO 258/97 sui Novel Food
REGOLAMENTI COMUNITARI 49 E 50/2000
Prevedono l’obbligo di etichettatura per tutti gli alimenti che contengano ingredienti (49/2000), additivi e aromi (50/2000) derivanti da organismi geneticamente modificati. L’obbligo non vale se il prodotto risulti accidentalmente contaminato da derivati di organismi geneticamente modificati in una percentuale non superiore all’1%.

DIAGNOSTICA degli OGM negli ALIMENTI
TEST sulle PROTEINE
Rilevazione immunologica della
proteina codificata dal transgene (ELISA)
- Quali- / quantitativo
- Rapido
- Test da campo
Richiede materie prime non lavorateL’espressione delle proteine è spesso tessuto-specifica e sviluppo-dipendente
-
-
TEST sul DNARicerca del transgene e di sequenze ad esso correlate
(Real-time PCR)
- Quali- / quantitativo
- Rapido
- Sensibile (limite = 0.0001%)
- Degradazione del DNA
- Presenza di inibitori della polimerasi
Possibili contaminazioni con DNA estraneo
Non tutti i derivati alimentari contengono DNA (es. olio di semi di mais)
-
-

Analisi qualitativa (screening)
I° STEP
Rivela la presenza/assenza dell’OGM nel campione
Si ricerca la presenza di sequenze regolatrici comuni alla maggior parte degli OGM
risultatopositivo
Si identifica il transgene presente, verificando se è uno di quelli autorizzati in
commercio
risultatonegativo
L’analisi si arresta
Nessun transgene autorizzato
Alimento illegale
Transgene autorizzato
II° STEP
Analisi quantitativa
Se i singoli ingredienti superano la percentuale dell’1% scatta l’obbligo di riportarne la presenza in etichetta
ITER per il RILEVAMENTO di OGM negli alimenti mediante TEST sul DNA

GENI BERSAGLIO nell’analisi qualitativa degli alimenti
Individuazione del transgene
Elementi caratteristici dei costrutti ricombinanti
Promotore CaMV 35S
Transgene tNOSGene
marcatore
Promotore CaMV 35S
tNOS
Gene marcator
ePCR QUALITATIVA
Amplificazione di una delle seguenti sequenze:
Amplificazione di geni sicuramente presenti nel campione (es. lectina della soia, zeina del mais)
PCR QUANTITATIVA
(è disponibile una banca dati che contiene tutte le sequenze di DNA depositate nei brevetti a livello mondiale)

2 ESEMPI di QUANTIFICAZIONE...
La soia Roundup Ready (Monsanto) è stata modoficata geneticamente per resistere alla somministrazione del glifosato, un diserbante ad ampio spettro.
Soia Roundup Ready
Per quantificare mais e soia transgenici negli alimenti sono state opportunamente disegnate combinazioni di Sonde di Ibridazione che riconoscono tanto il transgene quanto un gene endogeno, rendendo possibile quantificare simultaneamente sia il contenuto di mais/soia GM che di mais/soia totale nel campione in analisi.
Sonda 1 specifica per il transgene cryIA(b), codificante per la tossina
Sonda 2 specifica per il gene endogeno codificante per l’enzima invertasi
Sonda 1 specifica per il transgene CP4-EPSPS
Sonda 2 specifica per il gene endogeno codificante per la lectina
Mais Bt
di un gene che codifica per una tossina insetticida
Il mais-BT è stato reso resistente alla piralide mediante l’inserimento
derivata dal batterio Bacillus turingiensis la cui ingestione provoca la morte delle larve paralizzandone l’intestino.