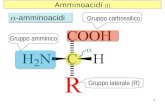
Amminoacidi (1) Gruppo carbossilico Gruppo amminico Gruppo laterale (R) -amminoacidi 1.
1 ESERCITAZIONE di CHIMICA 23 gennaio, 2013 STEREOISOMERIA CARBOIDRATI AMMINOACIDI.
-
Upload
pina-vinci -
Category
Documents
-
view
222 -
download
2
Transcript of 1 ESERCITAZIONE di CHIMICA 23 gennaio, 2013 STEREOISOMERIA CARBOIDRATI AMMINOACIDI.

1
ESERCITAZIONE di CHIMICA23 gennaio, 2013
STEREOISOMERIA
CARBOIDRATI
AMMINOACIDI

2
STEREOISOMERIA

3
Carbonio asimmetrico (“chirale”): carbonio legato a quattro sostituenti diversi!
La presenza di un atomo di carbonio asimmetrico determina l’isomeria ottica (“stereoisomeria”)
I due stereoisomeri sono immagini speculari
I due stereoisomeri hanno le stesse proprietà chimiche e fisiche, tranne la rotazione del piano della luce polarizzata (l’angolo di rotazione è identico, ma di segno opposto!)

4

MOLECOLE SPECULARI
NON SONOSOVRAPPONIBILI!
MOLECOLE DIFFERENTI!
5

MOLECOLENON
SPECULARI
SONOSOVRAPPONIBILI!
MOLECOLE UGUALI!
6

Una precisazione sul carbonio asimmetrico!
C CH2 CH3
CH2
Cl
CH2
OH
CH2NH2 C CH2 CH3
CH2
Cl
CH2
OH
CH2NH2 *
Simmetricoo
asimmetrico?Asimmetrico!
7

8
CH
CH2OH
CO H
OH
L (-) gliceraldeide
C HHO
CH2OH
CO H
D (+) gliceraldeide
Come distinguere i due stereoisomeri?
specchio
**

9
2009-2010
Quale tra le seguenti molecole ha attività ottica?
C
CH3
H3C Cl
Br
C
CH3
Cl
Br
H C
CH3
ClBr
CH3
C
CH3
Cl
Br
Br

10
CARBOIDRATI
SACCARIDI
GLUCIDI

11
CH
CH2OH
CO H
OH
D (+) gliceraldeide D (?) glucidi
CH
CH2OH
CO H
OH

C
C
C
O
H
H
H
H
OH
OH
OH
CH2OH
C
*
**
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
HO *
**
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
HO
*
**
C
C
C
O
H
H
H
H
OH
CH2OH
C
HO
HO *
**
aldo-pentosi (5 atomi di C): 8 isomeri!
D (-) ribosio
D (-) arabinosio
D (+) xilosio
D (-) lixsosio
12

13
Scrivere le formule di Fischer di: D-ribosio e L-ribosio
C
C
C
O
H
H
H
H
OH
OH
OH
CH2OH
C
*
**
C
C
C
O
H
H
H
H
CH2OH
C
HO
HO
HO
*
**
C
C
C
O
H
H
H
H
OH
OH
CH2OH
CHO
*
**
D (-) ribosio L (+) ribosio L (+) lixsosio

14
aldo-esosi (6 atomi di C): 16 isomeri!
D (+) allosio
D (+) atrosio
D (+) glucosio
D (-) gulosio
C
C
C
O
H
H
H
H
OH
OH
OH
CH2OH
C
CH OH
*
*
*
*
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
CH OH
HO *
*
*
*
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
CH OH
HO
*
*
*
*
C
C
C
O
H
H
H
H
OH
OH
OH
CH2OH
C
C HHO
*
*
*
*

15
aldo-esosi (6 atomi di C): 16 isomeri!
D (+) mannosio
D (+) idosio
D (+) galattosio
D (-) talosio
C
C
C
O
H
H
H
H
OH
CH2OH
C
CH OH
HO
HO *
*
*
*
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
C H
HO
HO
*
*
*
*
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
C H
HO
HO
*
*
*
*
C
C
C
O
H
H
H
H
OH
CH2OH
C
C HHO
HO
HO *
**
*

16
Scrivere le formule di Fischer di: D-glucosio e L-glucosio
D (+) glucosio L (-) glucosio L (-) idosio
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
HO
CH OH
*
*
*
* **
*
C
C
C
O
H
H
H
H
OH
CH2OH
C
HO
C HHO
HO *
C
C
C
O
H
H
H
H
OH
CH2OH
C
HO
CH OH
HO
*
**
*

17
CARBOIDRATI 2010-2011
Quale tra le seguenti molecole è un D-cheto-pentoso?
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
HO
C
CH
H OH
CH2OH
C
CH2OH
O
OH
C
C
C
O
H
H
H
H
OH
CH2OH
C
HO
HO
C
C H
H
CH2OH
C
CH2OH
O
HO
HO

18
CARBOIDRATI 2009-2010
I monosaccaridi della serie D sono caratterizzati dall’avere un atomo di
carbonio con la stessa configurazione di quello della D-gliceraldeide.
Negli aldo-esosi tale carbonio è il carbonio:
6 5 3 2
C
C
C
O
H
H
H
H
OH
OH
CH2OH
C
CH OH
HO

19
AMMINOACIDI

20
C HHO
CH2OH
CO H
C H
CO OH
H2N
R
L (-) gliceraldeide L (?) amminoacido
ossidazione
sostituzione
derivato
* *

catena laterale Rapolarepolareacidabasica
21
C H
CO OH
H2N
R
L (?) amminoacido
*

22
C H
CO OH
H2N
R
Amminoacido e pH: gruppi da considerare!
1 gruppo alfa carbossilico
2 gruppo alfa amminico
3 catena laterale
*

23
AMMINOACIDI 2010-2011
Disegnare la curva di titolazione dell’amminoacidoaspartato (pka1 = 2,1; pka2 = 3,9; pka3 = 9,9) ed indicare
la carica elettrica ai vari pH
Disegnare la curva di titolazione dell’amminoacidoarginina (pka1 = 2,2; pka2 = 9,0; pka3 = 12,5) ed indicare
la carica elettrica ai vari pH

24
EQUAZIONE DI HENDERSON-HASSELBACH
HA + H2O H3O+ + A- (equilibrio!)
[ HA ] - log [ H3O+ ] = - log ka - log -------- [ A- ]
[ acido ] pH = pka - log ------------ [ base ]

25
EQUAZIONE DI HENDERSON-HASSELBACH
[ acido ] pH = pka - log ------------ [ base ]
Il rapporto tra le concentrazioni di acido e base coniugata determina il pH
Imponendo dall’esterno il pH, il rapporto tra le concentrazioni di acido e base coniugata cambia!

26
0
2
4
6
8
10
12
14
0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1,0 1,1
moli NaOH
pH
acido acetico 1 mol / L titolato con NaOH
pka = 4,76HAc > Ac- HAc < Ac-
HAc = Ac-
[ HAc ]pH = pka - log ---------- [ Ac- ]

amminoacido pka1 αCOOH pka2 αNH3+ pka3 laterale
glicina 2,3 9,6
(+) alanina 2,3 9,7
(-) serina 2,2 9,2
(-) treonina 2,6 10,4
(-) tirosina 2,2 9,1 10,1 fenolo
(-) triptofano 2,4 9,4
(+) aspartato 2,1 9,8 3,9 carbossile
(-) glutammato 2,2 9,7 4,3 carbossile
(-) istidina 1,8 9,2 6,0 imidazolo
(+) lisina 2,2 9,0 10,5 ammina
(+) arginina 2,2 9,0 12,5 guanina
27

0
2
4
6
8
10
12
14
0,0 0,5 1,0 1,5 2,0 2,5
glicina 1 mol / L titolata con NaOH
C
COOH
H
H
+NH3 C H
H
COO-
NH2C H
H
COO-
NH3+
pka1 = 2,3
pka2 = 9,6pH
moli NaOH
pI = 5,95
28

29
AMMINOACIDI 2010-2011
Il punto isoelettrico dell’amminoacido alanina ha un valore di circa:
9,52,34,56,0

0
2
4
6
8
10
12
14
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5
L (+) acido aspartico 1 mol / L titolato con NaOH
C
COOH
H+NH3
CH2 COOH
C H+NH3
CH2
COO-
COO-
C H+NH3
CH2
COO-
COOH
C HNH2
CH2
COO-
COO-
pka1 = 2,1
pka2 = 3,9
pka3 = 9,8
pI = 3,0
moli NaOH
pH
30

31
AMMINOACIDI 2010-2011
Il punto isoelettrico dell’amminoacido bi-carbossilico acido glutammico ha un valore di circa:
9,53,04,57,0

0
2
4
6
8
10
12
14
0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5
L (+) arginina 1 mol / L titolata con NaOH
pH
moli NaOH
pka1 = 2,2pka2 = 9,0
pka3 = 12,5pI = 10,75
C
COOH
HNH3
CH2......NH2
+
+
C HNH3
CH2......NH2
+
+
COO -
C HNH2
CH2......NH2
+
COO -
C HNH2
CH2......NH
COO -
32

33
AMMINOACIDI 2010-2011
Il punto isoelettrico dell’amminoacido bi-amminico lisina ha un valore di circa:
9,53,54,57,0

amminoacido pka COOH pka NH3+ pka laterale pI
glicina 2,3 9,6 6,0
alanina 2,3 9,7 6,0
serina 2,2 9,2 5,7
treonina 2,6 10,4 6,5
tirosina 2,2 9,1 10,1 fenolo 5,7
triptofano 2,4 9,4 5,9
aspartato 2,1 9,8 3,9 carbossile
3,0
glutammato 2,2 9,7 4,3 carbossile
3,2
istidina 1,8 9,2 6,0 imidazolo 7,6
lisina 2,2 9,0 10,5 ammina 9,8
arginina 2,2 9,0 12,5 guanina 10,834

amminoacido carico negativamente
cariche negative = cariche positive
amminoacido carico positivamente
La carica netta di un amminoacido cambia con il pH
pH
pI
35

36
AMMINOACIDI 2010-2011
In una elettroforesi in un tampone a pH = 6,gli alfa-L-amminoacidi bi-carbossilici si muoveranno:
verso il catodo (-)verso l’anodo (+)
non si muoverannodipende dal voltaggio
pI = circa 3 pH > pI carica negativa!

37
AMMINOACIDI 2010-2011
In una elettroforesi in un tampone a pH = 6,gli alfa-L-amminoacidi bi-amminici lisina e arginina si
muoveranno:
verso il catodo (-)verso l’anodo (+)
non si muoverannodipende dal voltaggio
pI = circa 10 pH < pI carica positiva!

38
AMMINOACIDI 2009-2010
Il pka dell’alfa carbossile di un amminoacido ha unvalore di circa:
1,0-1,52,0-2,23,0-4,54,5-5,5

39
AMMINOACIDI 2009-2010
L’amminoacido glicina (pka1 = 2,3; pka2 = 9,8) potrà essere usato per fare tamponi a pH:
tra 6 e 7tra 5 e 6tra 2 e 3tra 7 e 8

40
AMMINOACIDI 2009-2010
Il pka dell’alfa ammino-gruppo di un amminoacido haun valore di circa:
10-119,0-9,53,0-4,54,5-5,5

41
AMMINOACIDI 2009-2010
La catena laterale dell’amminoacido istidina può assumere:
una carica positivauna carica negativa
nessuna caricadue cariche positive

42
AMMINOACIDI 2009-2010
La catena laterale dell’amminoacido acido glutammico può assumere:
una carica positivauna carica negativa
nessuna caricadue cariche negative

43
AMMINOACIDI 2009-2010
Quale è la forma predominante dell’amminoacidoalanina a pH = 6?
C HNH3+
COO -
CH3
C H
COO -
CH3
NH2 C H
CH3
NH2
COOH
C HNH3+
CH3
COOH

44
AMMINOACIDI 2010-2011
Quale è la forma predominante dell’amminoacidoserina a pH = 12?
C HNH3+
COO -
CH2 OH
C H
COO -
CH2 OH
NH2 C H
CH2
NH2
COOH
O -
C HNH3+
CH2 OH
COOH

Struttura degli amminoacidi a pH fisiologico pH = 7,2-7,4
C HNH3+
COO -
R
C HNH3+
COO -
R -
C HNH3+
COO -
R +
neutro acidoaspartato
glutammato
basicolisina
arginina
45

proteina carica negativamente
cariche negative
=
cariche positive
acido asparticoacido glutammico
istidinalisina
arginina
proteina carica positivamente
La carica netta di una proteina cambia con il pH
pH
pI
46

47
Punto isoelettrico delle proteine
Proteina Punto isoelettrico, pI
pepsina minore di 1,0
ovoalbumina 4,6
albumina sierica 4,9
ureasi 5,0
emoglobina 6,8
mioglobina 7,0
citocromo c 10,7
lisozima 11,0

48
FINE !