Modellazione farmacocinetica del trasporto di farmaci al cervello: … · 2017-10-31 ·...
Transcript of Modellazione farmacocinetica del trasporto di farmaci al cervello: … · 2017-10-31 ·...

Modellazione farmacocineticadel trasportodifarmaci al cervello: ruolo della barrieraematoencefalicaTesidilaureaspecialisticaScuoladiIngegneriaIndustrialeedell’InformazioneCorsodilaureamagistraleiningegneriachimicaRelatore:prof.DavideMancaCorrelatore:ing.AdrianaSavocaStudenti:StefanoCampa,matricola753982 FrancescoPigazzini,matricola852943AnnoAccademico:2016/17

ii

iii
IndicedeicontenutiIndice delle figure vii
Indice delle tabelle xiii
Acronimi xvii
Simboli xvii
Estratto xix
1 INTRODUZIONE ................................................................................................ 1
1.1 INTRODUZIONE ALLA FARMACOCINETICA E OBBIETTIVO DELLA TESI ............................................. 11.2 ANATOMIA DEL CERVELLO ............................................................................................................. 4
1.2.1 Cerebro .................................................................................................................................. 51.2.2 Cervelletto ............................................................................................................................. 61.2.3 Tronco cerebrale ................................................................................................................... 71.2.4 Diencefalo .............................................................................................................................. 8
1.3 PROTEZIONE E VASCOLARIZZAZIONE DEL CERVELLO ...................................................................... 91.3.1 Le meningi ............................................................................................................................. 91.3.2 Liquido cerebrospinale ........................................................................................................ 101.3.3 Barriera ematoencefalica .................................................................................................... 15
1.4 TRASPORTO DEI FARMACI AL CERVELLO ....................................................................................... 161.4.1 Sistema di trasporto in ingresso sangue-cervello attraverso la BEE .................................. 181.4.2 Sistema di trasporto in uscita cervello-sangue attraverso la BEE ...................................... 191.4.3 Sistemi di trasporto in ingresso e in uscita attraverso la BCS ............................................ 20
1.5 ANALGESIA E ANESTESIA .............................................................................................................. 211.5.1 Morfina ................................................................................................................................ 221.5.2 ADME della morfina ........................................................................................................... 231.5.3 Meccanismo d’azione della morfina ................................................................................... 24
2 MODELLO FARMACOCINETICO DELLA MORFINA NEI RATTI ...................................... 27
2.1 STATO DELL’ARTE ........................................................................................................................ 272.2 MODELLO TRICOMPARTIMENTALE ................................................................................................ 302.3 MODELLO PBPK ........................................................................................................................... 412.4 RISULTATI E CONVALIDA MODELLO TRICOMPARTIMENTALE PER INFUSIONE VIA BOLO DI BASSE
DOSI 472.5 RISULTATI E CONVALIDA MODELLO TRICOMPARTIMENTALE PER INFUSIONE VIA BOLO DI MEDIE
DOSI 492.6 RISULTATI MODELLO TRICOMPARTIMENTALE PER INFUSIONE VIA BOLO DI ALTE DOSI: BOURASSET
ET AL. (2006) .............................................................................................................................................. 502.7 RISULTATI MODELLO TRICOMPARTIMENTALE PER INFUSIONE CONTINUA: KISSIN ET AL. (1991) .. 512.8 RISULTATI E CONVALIDA MODELLO PBPK PER INFUSIONE VIA BOLO DI BASSE DOSI ..................... 52

iv
2.9 RISULTATI E CONVALIDA MODELLO PBPK PER INFUSIONE VIA BOLO DI MEDIE DOSI .................... 532.10 RISULTATI MODELLO PBPK PER INFUSIONE VIA BOLO DI ALTE DOSI: BOURASSET ET AL. (2006) .. 542.11 RISULTATI MODELLO TRICOMPARTIMENTALE PER INFUSIONE CONTINUA: KISSIN ET AL. (1991) .. 542.12 ANALISI E CONFRONTO DEI RISULTATI DEI DUE MODELLI ............................................................. 55
2.12.1 Analisi dei risultati ottenuti dal modello tricompartimentale ............................................. 602.12.2 Analisi dei risultati ottenuti dal modello PBPK .................................................................. 622.12.3 Confronto dei risultati ottenuti dai due modelli .................................................................. 63
3 MODELLO FARMACOCINETICO DELLA MORFINA NEGLI UOMINI ............................. 66
3.1 METABOLIZZAZIONE DELLA MORFINA .......................................................................................... 663.1.1 M3G e M6G ......................................................................................................................... 663.1.2 Farmacologia di M3G e M6G ............................................................................................. 68
3.2 COSTRUZIONE DEL MODELLO A QUATTRO COMPARTIMENTI E DEL MODELLO PBPK .................... 693.2.1 Modello a quattro compartimenti ........................................................................................ 703.2.2 Modello PBPK ..................................................................................................................... 78
3.3 RISULTATI DEL MODELLO A QUATTRO COMPARTIMENTI ............................................................... 863.3.1 Caso-studio 1: Stuart Harris et al. (2000) .......................................................................... 863.3.2 Caso-studio 2: Lötsch et al. (2002) ..................................................................................... 863.3.3 Caso-studio 3: Osborne et al. (1990) .................................................................................. 873.3.4 Caso-studio 4: Stansky et al. (1978) .................................................................................... 88
3.4 RISULTATI DEL MODELLO PBPK ................................................................................................... 883.4.1 Caso-studio 1: Stuart Harris et al. (2000) .......................................................................... 893.4.2 Caso-studio 2: Lötsch et al. (2002) ..................................................................................... 893.4.3 Caso-studio 3: Osborne et al. (1990) .................................................................................. 893.4.4 Caso-studio 4: Stansky et al. (1978) .................................................................................... 90
3.5 DISCUSSIONE E CONFRONTO DEI RISULTATI .................................................................................. 903.5.1 Osservazioni sul modello a quattro compartimenti ............................................................. 933.5.2 Osservazioni sul modello PBPK .......................................................................................... 943.5.3 Confronto tra i due modelli ................................................................................................. 95
3.6 OSSERVAZIONI SULL’OTTIMIZZAZIONE ......................................................................................... 963.6.1 Confronto dei risultati del modello a quattro compartimenti per lo studio di Stuart Harris
et al. (2000) .......................................................................................................................................... 973.6.2 Confronto dei risultati del modello a quattro compartimenti per lo studio Lötsch et al.
(2002) 983.6.3 Confronto dei risultati del modello a quattro compartimenti per lo studio di Osborne et al.
(1990) 983.6.4 Confronto dei risultati del modello a quattro compartimenti per lo studio Stansky et al.
(1978) 993.6.5 Confronto dei risultati del modello PBPK per lo studio di Stuart Harris et al. (2000) .... 100

v
3.6.6 Confronto dei risultati del modello PBPK per lo studio di Lötsch et al. (2002) ............... 1003.6.7 Confronto dei risultati del modello PBPK per lo studio di Osborne et al. (1990) ............ 1013.6.8 Confronto dei risultati del modello PBPK per lo studio di Stansky et al. (1978) ............. 1023.6.9 Discussione dei risultati .................................................................................................... 102
4 ANALISI DI SENSITIVITÀ PARAMETRICA ............................................................................ 106
4.1 METODI DI ANALISI DI SENSITIVITÀ ............................................................................................ 1064.1.1 Analisi di sensitività locale ................................................................................................ 1064.1.2 Analisi di sensitività globale ............................................................................................. 107
4.2 COSTRUZIONE DELLA MATRICE DI SENSITIVITÀ .......................................................................... 1074.2.1 Normalizzazione della matrice di sensitività ..................................................................... 108
4.3 RISULTATI DELL’ANALISI DI SENSITIVITÀ ................................................................................... 1094.3.1 Analisi di sensitività del modello tricompartimentale dei ratti ......................................... 1104.3.2 Analisi di sensitività del modello PBPK dei ratti .............................................................. 1114.3.3 Analisi di sensitività del modello a quattro compartimenti umano ................................... 1134.3.4 Analisi di sensitività del modello PBPK umano ................................................................ 114
4.4 COMMENTO DEI RISULTATI ......................................................................................................... 1174.4.1 Modello tricompartimentale per i ratti .............................................................................. 1174.4.2 Modello PBPK per i ratti .................................................................................................. 1184.4.3 Modello a quattro compartimenti per gli umani ............................................................... 1204.4.4 Modello PBPK per gli umani ............................................................................................ 120
4.5 CONCLUSIONI .............................................................................................................................. 122
5 CONCLUSIONI E SVILUPPI FUTURI ........................................................................................ 124
Bibliografia 129

vi

vii
IndicedellefigureFigura1.1Ilmercatoglobalenel1998perfarmaciperilSistemanervosocentrale(SNC)e
farmaci per Disturbi cardiovascolari (DCV) (a) è diagrammato insieme al numero di
individuinegliUSAcondisturbialSNCoDCV(b).Questidatisonoutilizzatipercalcolare
ilrapportoannuodidollarispesiperpaziente(c),chemostraunrapportoperidisturbi
cardiovascolari6voltepiùaltocheperidisturbialSNC.Questorapportoèstatocalcolato
sulmercatodegliUSA,cherappresentacircail30%delmercatoglobaledeifarmaci.Si
trattadiunarappresentazioneapprossimativa,attaafarrifletteresullagrandedisparità
tralamisuradeimercatideiduetipidifarmaci.ImmaginetrattadaPardridge,(2002)...3
Figura1.2Sezionesagittaledelcervello,vistamediana.Inbassoasinistra,ossianellaparte
posteriore,sitrovailcervelletto,nellapartecentralevièiltroncocerebraleesopradi
essoildiencefalo.Ilcerebroricopretuttelealtreporzionidicervello,immaginetrattada
NielseneTortora(2013)....................................................................................................5
Figura1.3Vistadall’altodel cerebro. Si possono facilmentedistinguere i dueemisferi
cerebrali e la fessura longitudinale che li separa. Immagine tratta da Educational
TechnologyClearinghouse–UniversityofSouthFlorida...................................................6
Figura 1.4 Sezione sagittale del cervello, vista mediana. In basso a destra si può
distinguereilcervelletto.ImmaginetrattadaMyers(2006).............................................7
Figura 1.5 Sezione sagittale e visione mediana del cervello e del midollo spinale. Si
possonodistinguerelediversepartichecompongonoiltroncocerebrale,immaginetratta
daNielseneTortora(2013)...............................................................................................8
Figura 1.6 Visionemediana della sezione sagittale del diencefalo, immagine tratta da
McKinleyetal.(2015)........................................................................................................9
Figura1.7Visioneanterioredellasezionefrontaledelcranio,sipossonodistinguereivari
stratidellemeningi.ImmaginetrattadaNielseneTortora(2013)..................................10
Figura1.8Visioneanterioredelcervello.Sonoevidenziatiiquattroventricolieleaperture
chepermettonogliscambifraessi.ImmaginetrattadaNielseneTortora(2013).........12
Figura 1.9Dettaglio di una sezione frontale di unplesso coroideo. La freccia indica la
direzione della filtrazione dal sangue al liquor, immagine tratta da Nielsen e Tortora
(2013)...............................................................................................................................13

viii
Figura1.10Riassuntodellaformazione,circolazioneeassorbimentodelliquor.Immagine
trattadaNielseneTortora(2013)...................................................................................14
Figura1.11Vistaposterioredei senivenosiedelleprincipaliveneche fuoriesconodal
cervello.ImmaginetrattadaDepartmentofMedicineandHaematology,CalicutMedical
College..............................................................................................................................14
Figura1.12Vistadalbasso(sullasinistra)evisionelaterale(sulladestra)dellacircolazione
delsanguearteriosonelcervello.ImmaginetrattadaNiekroetal.(2008).....................15
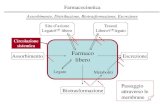
Figura1.13Rappresentazionedelletrebarriereprincipalitrasangueecervello:(a)BEE;
(b)BCS;(c)barrieraaracnoidea,immaginetrattadaAbbottetal.(2009)......................17
Figura 1.14Meccanismi di trasporto in entrata e uscita dalla BEE. Immagine tratta da
OhtsukieTerasaki(2007).................................................................................................19
Figura 1.15 Struttura chimica della morfina. A destra gli atomi di ossigeno sono
rappresentati inrosso,inazzurroquellidi idrogeno,ingrigioquellidicarbonioeinblu
l’unicoatomodiazoto.ImmaginetrattadaDrugBank...................................................23
Figura1.16IlfarmacoApuòinteragireconilrecettorealcontrariodelfarmacoB,aseguito
dell’interazione tra i due si ha l’effetto farmacologico. Immagine tratta da Pharmacy
Magazine..........................................................................................................................24
Figura1.17Asinistraeadestravienemostratoilmeccanismocompetitivodovesoloun
recettore può interagire con il sito accettore, al centro entrambi i ligandi possono
interagireconlostessorecettorequindisihaunmeccanismononcompetitivo.Immagine
trattadaMembraneReceptors........................................................................................25
Figura 2.1 Schema del modello tricompartimentale per i ratti. Le frecce indicano la
direzionedei flussi tra i compartimenti. Il significatodeiparametri indicati suciascuna
frecciaverràspiegatopiùneldettaglioneiprossimiparagrafi........................................31
Figura 2.2 Schema rappresentativo dei supporti permeabili transwells adottati per
misuraresperimentalmenteilflussodifarmacoattraversolamembranaendotelialeCACO
2.......................................................................................................................................38
Figura2.3SchemadelmodelloPBPK.Lefrecceindicanoladirezionedeiflussidifarmaco
traicompartimenti..........................................................................................................42

ix
Figura2.4Rappresentazionedelmodellotricompartimentaleperinfusioneendovenosa
di 0.44 mgmorfina/kgratto tramite bolo nei ratti. I rombi in rosso indicano le misure
sperimentali di Plomp et al. (1981), la linea blu è il risultato delmodello. A sinistra è
rappresentato il profilo di concentrazione di morfina nel compartimento centrale, a
destrailprofilodiconcentrazionedimorfinanelcompartimentocervello....................48
Figura2.5Rappresentazionedelmodellotricompartimentaleperinfusioneendovenosa
di 2.5 mgmorfina/kgratto tramite bolo nei ratti. I rombi in rosso indicano le misure
sperimentalidiDahlstrometal.(1975),lalineabluèilrisultatodelmodello.Asinistraè
rappresentato il profilo di concentrazione di morfina nel compartimento centrale, a
destrailprofilodiconcentrazionedimorfinanelcompartimentocervello....................50
Figura2.6Rappresentazionedelmodellotricompartimentaleperinfusioneendovenosa
di 10 mgmorfina/kgratto tramite bolo nei ratti. I rombi in rosso indicano le misure
sperimentalidiBourassetetal.(2006),lalineabluèilrisultatodelmodello.Asinistraè
rappresentato il profilo di concentrazione di morfina nel compartimento centrale, a
destrailprofilodiconcentrazionedimorfinanelcompartimentocervello....................51
Figura2.7Rappresentazionedelmodellotricompartimentaleperinfusioneendovenosa
continuadi4mgmorfina/kgratto/hneiratti.Irombiinrossoindicanolemisuresperimentali
diKissinetal.(1991),lalineabluèilrisultatodelmodello.Asinistraèrappresentatoil
profilodi concentrazionedimorfinanel compartimento centrale, adestra il profilodi
concentrazionedimorfinanelcompartimentocervello..................................................52
Figura 2.8 Rappresentazione del modello PBPK per infusione endovenosa di 0.44
mgmorfina/kgrattotramiteboloneiratti.Irombiinrossoindicanolemisuresperimentalidi
Plomp etal. (1981), la lineabluè il risultatodelmodello.Asinistraè rappresentato il
profilodi concentrazionedimorfinanel compartimento centrale, adestra il profilodi
concentrazionedimorfinanelcompartimentocervello..................................................53
Figura 2.9 Rappresentazione del modello PBPK per infusione endovenosa di 2.5
mgmorfina/kgrattotramiteboloneiratti.Irombiinrossoindicanolemisuresperimentalidi
Dahlstrometal.(1975),lalineabluèilrisultatodelmodello.Asinistraèrappresentatoil
profilodi concentrazionedimorfinanel compartimento centrale, adestra il profilodi
concentrazionedimorfinanelcompartimentocervello..................................................54

x
Figura2.10Rappresentazionedelmodellotricompartimentaleperinfusioneendovenosa
di 10 mgmorfina/kgratto tramite bolo nei ratti. I rombi in rosso indicano le misure
sperimentalidiBourassetetal.(2006),lalineabluèilrisultatodelmodello.Asinistraè
rappresentato il profilo di concentrazione di morfina nel compartimento centrale, a
destrailprofilodiconcentrazionedimorfinanelcompartimentocervello....................54
Figura2.11Rappresentazionedelmodellotricompartimentaleperinfusioneendovenosa
continuadi4mgmorfina/kgratto/hneiratti.Irombiinrossoindicanolemisuresperimentali
diKissinetal.(1991),lalineabluèilrisultatodelmodello.Asinistraèrappresentatoil
profilodi concentrazionedimorfinanel compartimento centrale, adestra il profilodi
concentrazionedimorfinanelcompartimentocervello..................................................55
Figura3.1Illustrazionedeiduemetabolitiprincipalidellamorfina.................................67
Figura3.2Strutturachimicadell’acidoglucuronico.........................................................67
Figura 3.3 Schematizzazione del modello a quattro compartimenti: il compartimento
centrale,ilcompartimentodegliorganipocoperfusidasangue,ilcompartimentocervello
edinfineilcompartimentometabolismo.........................................................................70
Figura 3.4 È rappresentata una schematizzazione degli otto compartimenti che
compongono ilmodelloPBPK: ilcompartimentoplasma, ilcompartimentodegliorgani
poco perfusi da sangue, il compartimento degli organi molto perfusi da sangue, il
compartimento vascolarizzazione del cervello, il compartimento tessuti del cervello, il
compartimento del sistema circolatorio gastrointestinale, il compartimento fegato ed
infineilcompartimentometabolismo..............................................................................79
Figura3.5AsinistrasonoriportatiirisultatidellamorfinaedestraquellidelM6G,inrosso
sonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.....86
Figura3.6AsinistrasonoriportatiirisultatidellamorfinaedestraquellidelM6G,inrosso
sonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.....87
Figura3.7AsinistrasonoriportatiirisultatidellamorfinaedestraquellidelM6G,inrosso
sonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.....88
Figura3.8Inrossosonorappresentatiidatisperimentali,lalineablu,invece,rappresenta
ilmodello..........................................................................................................................88

xi
Figura3.9AsinistrasonoriportatiirisultatidellamorfinaedestraquellidelM6G,inrosso
sonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.....89
Figura3.10Asinistrasonoriportati i risultatidellamorfinaedestraquellidelM6G, in
rossosonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.
..........................................................................................................................................89
Figura3.11Asinistrasonoriportati i risultatidellamorfinaedestraquellidelM6G, in
rossosonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.
..........................................................................................................................................90
Figura 3.12 In rosso sono rappresentati i dati sperimentali, la linea blu, invece,
rappresentailmodello.....................................................................................................90
Figura3.13Risultatidelmodellotricompartimentaleottenuticon la funzioneobiettivo
logaritmica (colonna sinistra); risultati con la funzione obiettivo standard (colonna
destra)..............................................................................................................................97
Figura3.14Risultatidelmodellotricompartimentaleottenuticon la funzioneobiettivo
logaritmica (colonna sinistra); risultati con la funzione obiettivo standard (colonna
destra)..............................................................................................................................98
Figura3.15Risultatidelmodellotricompartimentaleottenuticon la funzioneobiettivo
logaritmica (colonna sinistra); risultati con la funzione obiettivo standard (colonna
destra)..............................................................................................................................99
Figura3.16Risultatidelmodellotricompartimentaleottenuticon la funzioneobiettivo
logaritmica (colonna sinistra); risultati con la funzione obiettivo standard (colonna
destra)..............................................................................................................................99
Figura 3.17 Risultati del modello PBPK ottenuti con la funzione obiettivo logaritmica
(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra)..........100
Figura 3.18 Risultati del modello PBPK ottenuti con la funzione obiettivo logaritmica
(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra)..........101
Figura 3.19 Risultati del modello PBPK ottenuti con la funzione obiettivo logaritmica
(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra)..........102
Figura 3.20 Risultati del modello PBPK ottenuti con la funzione obiettivo logaritmica
(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra)..........102

xii
Figura 4.1 I parametri perturbati sono sei: k10, k12, k21, Pact, Pdiff e PactiveIN. Per ogni
compartimentocisonotredifferentibarrecolorate,cherappresentanoidiversi istanti
temporali:ilblurappresenta5min,ilverde60mineilgiallo200min.ANorddiciascuna
immagineèriportato ilparametrocheèstatoperturbato,sull’asseysihannoidiversi
compartimentiesull’assexilvaloredell’indicedisensitività........................................111
Figura4.2Iparametriperturbatisonododici:k12,k21,k13k31,jlp,jpl,effH,effK,CLlil,Pact,Pdiff
ePActiveIN.Perognicompartimentocisonotredifferentibarrecolorate,cherappresentano
idiversiistantitemporali:ilblurappresenta5min,ilverde60mineilgiallo200min.A
Norddiciascunaimmagineèriportatoilparametrocheèstatoperturbato,sull’asseysi
hannoidiversicompartimentiesull’assexilvaloredell’indicedisensitività...............113
Figura4.3Iparametriperturbatisonootto:k10,k12,k21,k40,kcin,Pact,PdiffePActiveIN.Perogni
compartimentocisonotredifferentibarrecolorate,cherappresentanoidiversi istanti
temporali:ilblurappresenta5min,ilverde60mineilgiallo200min.ANorddiciascuna
immagineèriportato ilparametrocheèstatoperturbato,sull’asseysihannoidiversi
compartimentiesull’assexilvaloredell’indicedisensitività........................................114
Figura4.4Iparametriperturbatisonoquattordici:k12,k21,k13k31,jlp,jpl,effH,effK,CLlil,Pact,
Pdiff,PActiveIN,kcinek40.Perognicompartimentocisonotredifferentibarrecolorate,che
rappresentanoidiversiistantitemporali:ilblurappresenta5min,ilverde60mineilgiallo
200min.ANorddiciascunaimmagineèriportatoilparametrocheèstatoperturbato,
sull’asseysihannoidiversicompartimentiesull’assexilvaloredell’indicedisensitività.
........................................................................................................................................117
Figura4.5Dettagliodeigraficiottenutidallaperturbazionedik12,k21eCLlil,sievidenzia
che gli indici di sensitività sono fino a quatto ordini di grandezza più piccoli di quelli
ottenutidaglialtriparametri..........................................................................................119
Figura4.6Sonoriportatiindettaglioivaloridegliindicidisensitivitàottenutiperturbando
ilparametroCLlil,sipuònotarechesonodiversiordinidigrandezza inferioririspettoa
quellideglialtriparametri..............................................................................................121

xiii
IndicedelletabelleTabella1.1Elencodelleprincipalisostanzechepossonoononpossonoattraversare la
barrieraematoencefalica.................................................................................................16
Tabella1.2PrincipalitrasportatoriesistemiditrasportoattraversolaBEE.Localizzazione
sullamembrana:latoluminale(L)eabluminale(A)dellecelluleendotelialideicapillari.
Direzione:dalsanguealcervello(In)edalcervelloalsangue(Ef).NDnondeterminato.
TabellatrattadaOhtsukieTerasaki,2007.......................................................................20
Tabella1.3TrasportatoriattraversolaBCS.Localizzazione:latoapicale(BB)elatobasale
(BL)dellecelluleepitelialideiplessicoroidei.Direzione:dalsanguealFCS(In)edalFCSal
sangue(Ef).NDnondeterminato.TabellatrattaDrugdeliverytothebrain,AAPS2014.
..........................................................................................................................................21
Tabella2.1Frazionemassivaedensitàdiorganietessutineiratti.................................32
Tabella2.2Parametrichecompaiononelmodellotricompartimentaledeiratti............33
Tabella 2.3 valori di primo tentativo assegnati a ciascun parametro del modello
tricompartimentale..........................................................................................................39
Tabella2.4Valorideiparametridelmodellotricompartimentaleottimizzatiperciascuna
tipologiadisomministrazionedellamorfina....................................................................40
Tabella2.5ParametridelmodelloPBPKindividualizzati,assegnatieincogniti...............45
Tabella2.6ValorideiparametridelmodelloPBPKottimizzatiperciascuna tipologiadi
somministrazionedellamorfina.......................................................................................47
Tabella 2.7 Casi studio utilizzati per la convalida del modello tricompartimentale per
infusioneendovenosaviabolodibassedosidimorfina..................................................49
Tabella 2.8Caso studioutilizzatoper la convalidadelmodello tricompartimentaleper
infusioneendovenosaviabolodimediedosidimorfina.................................................50
Tabella2.9Valorimassimiteoricichepossonoessereraggiuntidallamorfinaall’interno
delplasma.*=Valorecalcolatosu8ore,laduratadell’infusionenell’esperimentodiKissin
etal.(1991)......................................................................................................................56
Tabella2.10Valorimassimidiconcentrazionedimorfinamisuratisperimentalmentenei
rattiattraversoilprelievodicampionidiplasma.............................................................57

xiv
Tabella2.11Valorimassimidiconcentrazionedimorfinamisuratisperimentalmentenei
rattiattraversoilprelievodicampionidiplasma.............................................................57
Tabella2.12Valorimassimidiconcentrazionedimorfinamisuratisperimentalmentenei
rattiattraversoilprelievodicampionidiplasma.............................................................58
Tabella2.13Valorimassimidiconcentrazionedimorfinamisuratisperimentalmentenei
rattiattraversoilprelievodicampionidiplasma.............................................................59
Tabella2.14AUCpercentualipericasistudiodelmodellotricompartimentaleperbasse
dosidimorfinasomministrataendovenaviaboloneiratti.............................................60
Tabella2.15AUCpercentualipericasistudiodelmodellotricompartimentalepermedie
dosidimorfinasomministrataendovenaviaboloneiratti.............................................61
Tabella2.16AUCpercentualiper icasistudiodelmodellotricompartimentaleperalte
dosidimorfinasomministrataendovenaviaboloneiratti.............................................61
Tabella 2.17 AUC percentuali per i casi studio del modello tricompartimentale per
infusionecontinuadimorfinasomministrataendovenaneiratti...................................61
Tabella2.18AUCpercentualipericasistudiodelmodelloPBPKperbassedosidimorfina
somministrataendovenaviaboloneiratti......................................................................62
Tabella2.19AUCpercentualipericasistudiodelmodelloPBPKpermediedosidimorfina
somministrataendovenaviaboloneiratti......................................................................62
Tabella2.20AUCpercentualipericasistudiodelmodelloPBPKperaltedosidimorfina
somministrataendovenaviaboloneiratti......................................................................63
Tabella2.21AUCpercentualipericasistudiodelmodelloPBPKperinfusionecontinuadi
morfinasomministrataendovenaneiratti......................................................................63
Tabella2.22ConfrontoAUCpercentualiottenutenelcompartimentocentraledalmodello
tricompartimentaleenelcompartimentoplasmadalmodelloPBPK..............................63
Tabella2.23ConfrontoAUCpercentualiottenutenelcompartimentocervellodalmodello
tricompartimentaleenelcompartimentobrainvasculaturedalmodelloPBPK.............64
Tabella 3.1 Sono riportati i parametri che compaiono nel modello a quattro
compartimentiumano,essipossonoesseredistintitra:individualizzati,assegnatiegradi
dilibertà...........................................................................................................................72

xv
Tabella3.2Frazionemassivaedensitàdeidifferentiorganietessuti(Brownetal.,1997).
..........................................................................................................................................75
Tabella 3.3 Da sinistra: limite inferiore dell’ottimizzazione vincolata, valore di primo
tentativo,limitesuperioredell’ottimizzazioneevalorefinaleottenuto.........................77
Tabella 3.4 Sono riportati i parametri che compaiono nel modello PBPK umano, essi
possonoesseredistintitra:individualizzati,assegnatiegradidilibertà.........................81
Tabella 3.5 Da sinistra: limite inferiore dell’ottimizzazione vincolata, valore di primo
tentativo,limitesuperioredell’ottimizzazioneevalorefinaleottenuto.........................85
Tabella3.6Vengonoriportati ivalorideipicchimassimineiquattrostudiconsideratie
l’istanteincuisonostatimisurati....................................................................................91
Tabella3.7Valorimassimiteoricidellamorfinanelplasmachepossonoessereraggiunti
inciascunodeidiversistudiconsiderati...........................................................................91
Tabella3.8VengonoriportatiivalorideipicchimassimidiM6Gnelplasmaneitrestudi
consideratiel’istanteincuisonostatimisurati...............................................................92
Tabella3.9Vengono riportati i picchidelle concentrazionidimorfinaedelmetabolita
M6Gnelplasmaprevistidalmodelloaquattrocompartimenti......................................93
Tabella3.10Vengonoriportati ipicchidelleconcentrazionidimorfinaedelmetabolita
M6GnelplasmaprevistidalmodelloPBPK.....................................................................94
Tabella 3.11 Sono riportati i valori dell’indice di performance delmodello PBPK e del
modelloaquattrocompartimentiperlamorfina............................................................95
Tabella 3.12 Sono riportati i valori dell’indice di performance delmodello PBPK e del
modelloaquattrocompartimentiperilmetabolitaM6G...............................................95
Tabella3.13Indicediperformancedelmodelloaquattrocompartimentiperlamorfina
ottenutiutilizzandoilmetododiottimizzazionelogaritmicoequellostandard...........103
Tabella3.14Indicediperformancedelmodelloaquattrocompartimentiperilmetabolita
M6Gottenutiutilizzandoilmetododiottimizzazionelogaritmicoequellostandard...103
Tabella3.15Sonoriportati ivaloridell’indicediperformancedelmodelloPBPK per la
morfinaottenutiutilizzando ilmetododiottimizzazione logaritmicoequellostandard.
........................................................................................................................................104

xvi
Tabella3.16-Sono riportati i valoridell’indicediperformancedelmodelloPBPKper il
metabolitaM6G ottenuti utilizzando il metodo di ottimizzazione logaritmico e quello
standard.........................................................................................................................104
Tabella5.1Principaliproprietàfisiologichedeineonatichedifferisconodagliadulti,che
influenzanolafarmacocinetica.(Stephensonetal.,2005)............................................127

xvii
AcronimiADME Absorption,Distribution,Metabolism,andExcretion AUC AreaUnderCurve
ATP AdenosineTriphosphate
BCS BarrieraCerebro-Spinale
BEE BarrieraEmatoencefalica
BM BodyMass
CO CardiacOutput
DCV DisturbiCardiovascolari
FCS FluidoCerebrospinale
GIA GlobalIndustryAnalysts
GICS Gastro-IntestinalCirculatorySystem ND Nondeterminato
P-gp P-glicoproteina
PBPK Physiologicallybasedpharmacokineticmodeling
SNC SistemaNervosoCentrale
SimboliA Abluminale -
C Concentrazione [ng/mL]
CL Clearance [mL/min]
Eff Efficienza -
IR InfusionRate [ng/min]
L Luminale -
P Permeabilità [cm/s]
ρ Densità [g/mL]
V Volume [cm3omL]

xviii

xix
EstrattoIlcervelloèl’organopiùcomplessodegliesseriumani,eadogginonsonoancoramolti
gli studi che cercano di spiegare in maniera dettagliata i fenomeni di scambio che
avvengonotrailsangueeilsuddettoorgano.Allostessotempo,negliultimiannilaricerca
ha fattonotevolipassi inavantinellaproduzionedi farmaci, ingradodi raggiungere il
Sistema Nervoso Centrale oltrepassando la Barriera Ematoencefalica, per la cura di
disturbi e malattie cerebrali o per il trattamento del dolore. La difficoltà della
individuazioneesintesiditaliprincipiattividerivadalcomplessosistemadiprotezione
delcervelloneiconfrontidellesostanzeestranee.Aciòsiaggiungonol’impossibilitàdi
condurre esperimenti direttamente sull’uomo, in quanto estremamente invasivi, e la
necessitàdicontrollarechelaconcentrazionedeifarmacinelcervellocadaall’internodel
cosiddetto indice terapeutico. In questo contesto risultano di grande aiuto i modelli
farmacocinetici,ingradodisimulareilprofilodiconcentrazionediunfarmacoall’interno
delcervelloaseguitodellasomministrazione.
Loscopodiquestolavoroècostruireunmodellofarmacocineticoperlasomministrazione
di morfina per via endovenosa, partendo da dati sperimentali raccolti sui ratti, che
permettadiprevedernelaconcentrazionenelcervelloanchedell’uomo.Dopounostudio
approfonditosull’anatomiadelcervello,elaspiegazionedeimeccanismidiscambiotra
sangueecervello,sièoptatoinizialmenteperlaimplementazionenumericadiunmodello
farmacocineticopiùsempliceatrecompartimenti,inaccordoconimodellipiùdiffusiin
letteratura che includono il compartimento cervello. Successivamente si è voluto
proporre un modello più complesso, a sette compartimenti (PBPK), tra cui un
compartimentoperilfegatoeunoperilsistemacircolatoriogastro-intestinale,avendo
cosìlapossibilitàdianalizzarepiùneldettaglioladistribuzionedellamorfinanelcorpo.Si
è scelto di trascurare i compartimenti stomaco e intestino, in quanto, essendo la
somministrazione endovenosa, la concentrazione della morfina in tali organi è
trascurabile. A seguire, data la possibilità di sfruttare per gli esseri umani la stessa
strutturacompartimentale/matematica/parametricadeimodellipropostiperiratti,siè
andati ad analizzare la farmacocinetica della morfina negli uomini. A causa della
mancanzadidatisperimentaliperlaconcentrazionedifarmacinelcervellodegliuomini,

xx
è stato d’obbligo rinunciare ad un’analisi farmacocinetica del cervello umano. È stato
effettuato,invece,unostudiosulmetabolismodellamorfinanell’uomo,implementando
entrambi imodelli,siaquelloatrecompartimentichequelloasette,con l’aggiuntadi
un’equazione in grado di descrivere la cinetica di metabolizzazione della morfina.
Pertantonelcasodell’uomosiavrannounmodelloaquattrocompartimentieunoaotto
compartimenti.
Un’analisidisensitivitàparametricaèstataeffettuataal finedivalutare lastabilitàdei
gradi di libertà dei modelli. Sia per lo studio sui ratti che per lo studio sugli umani,
entrambi i modelli proposti si sono rivelati soddisfacenti dal punto di vista
dell’accuratezza.Questolavoroponedunquelebasipercontinuareadapprofondirela
modellazione farmacocinetica del cervello e, grazie alla presenza di parametri
individualizzati su ciascun paziente, contribuisce allo sviluppo di una cura sempre più
personalizzata.

Introduzione
1
1 Introduzione
1.1 Introduzioneallafarmacocineticaeobbiettivodellatesi
IlterminefarmacocineticafuintrodottoperlaprimavoltadaF.H.Dostnel1953nelsuo
Der Blütspiegel-Kinetic der Konzentrationsablaüfe in der Frieslaufflüssigjeit (Dost,
1953).Neltempovariedefinizionisonostatedateaquestaparola.Letteralmente,tale
termineindical’applicazionedellacineticaalpharmacon,farmacoingreco.Lacinetica,
dalgrecokinesis,movimento,èquellabrancadellascienzachestudiacomecambiano
una o più variabili nel tempo. Lo scopo della farmacocinetica è quello di osservare il
comportamento nel tempo della concentrazione di farmaci emetaboliti all’interno di
organietessutidegliesseriviventi,riconducibileallefasidiassorbimento,distribuzione,
metabolizzazioneedeliminazione(ADME),ecostruireunmodellomatematicoingrado
di riprodurre in maniera affidabile questi dati. Per raggiungere questo obbiettivo, si
descrive l’intero sistemadi organi e tessuti del corpoattraversouna seriedi relazioni
matematiche che esprimono il “cammino” del farmaco tenendo conto degli aspetti
fisiologiciefarmacologici(Wagner,1981).Ilfinedelmodellofarmacocineticoèquellodi
poter prevedere la concentrazione del farmaco all’interno dei tessuti dell’individuo
considerato.L’utilizzodellafarmacocineticaperlacuradelpazienteprevedecomefinalità
ultime:
§ L’individualizzazionedelladoseperciascunpaziente,equindilapossibilitàdiuna
curapersonalizzata;
§ L’utilizzo di parametri farmacocinetici come variabili per testare nuovi agenti
chemioterapici;
§ Losviluppodiunmetodononinvasivopervalutarelaconcentrazionedifarmaco
nelpaziente;
§ La determinazione di eventuali interazioni tra farmaci diversi, in modo da
prevederleedevitarle;
§ Lapossibilitàdieffettuareunoscalingpassandodairisultatiottenutidastudisugli
animaliarisultativalidipergliumaniattraversoopportunicoefficienti;

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
2
§ L’identificazione dimetodi per accelerare lo smaltimento di farmaci in caso di
sovradosaggio.
L’origine di questa materia può essere identificata molto tempo prima che la parola
“farmacocinetica” cominciasse ad essere utilizzata. Già nel 1847, l’inglese Buchanan,
mentrestudiaval’anestesiaeffettuataconetere,capìchiaramentecheilquantitativodi
anesteticinel cervellodipendessedalla concentrazionearteriosa,a suavoltacorrelata
all’intensitàdellamiscelainalata(Buchanan,1847).Daallora,ilcrescenteinteresseperla
materia ha portato a fare della modellazione farmacocinetica quello che oggi è una
componente chiave per lo sviluppo della medicina personalizzata al fine valutare
complessi scenari clinici, in grado di simulare, attraverso l’utilizzo di informazioni
fisiologiche e dati fisico-chimici, vari stati fisiologici e risposte farmacocinetiche
(Hartmanshennetal.,2016).
Daunpuntodivistaprettamenteeconomico,inaccordoconlostudiodiPardridge(2002),
venti anni fa si stimava che ilmercato dei farmaci che agiscono sul SistemaNervoso
Centrale(CNS)sarebbedovutocresceredel500%peresserequantomenocomparabilea
quello dei farmaci cardiovascolari. Sempre nel suo studio Pardridge attesta che
nonostanteilnumerodipazientiaffettidadisturbicardiovascolarifosseinferioreaquello
dipazientiaffettidadisturbialSistemaNervosoCentrale,laspesapro-capiteannuaper
pazienti affetti damalattie cardiovascolari era di $480 contro i $75per chi affettoda
malattiedelsistemanervoso(Fig.1.1).

Introduzione
3
Figura1.1Ilmercatoglobalenel1998perfarmaciperilSistemanervosocentrale(SNC)efarmaciperDisturbicardiovascolari(DCV)(a)èdiagrammatoinsiemealnumerodiindividuinegliUSAcondisturbialSNCoDCV(b).Questidatisonoutilizzatipercalcolareilrapportoannuodidollarispesiperpaziente(c),chemostraunrapportoperidisturbicardiovascolari6voltepiùaltocheperidisturbialSNC.QuestorapportoèstatocalcolatosulmercatodegliUSA,cherappresentacircail30%delmercatoglobaledeifarmaci.Sitrattadiunarappresentazioneapprossimativa,attaafarrifletteresullagrandedisparitàtralamisuradeimercatideiduetipidifarmaci.ImmaginetrattadaPardridge,(2002).
La causa di questa disparità, secondo Pardridge (2003), va ricercata nella difficoltà di
azionediquestatipologiadifarmaci(SNC),enellorobassoindiceterapeutico.Ifarmaci
perilcervellosviluppatineglianni’90delloscorsosecolo,infatti,nonfuronoingradodi
mantenere il passo con il progresso delle neuroscienze in quanto lamaggior parte di
questi non raggiungeva l’interno del cervello superando la Barriera Ematoencefalica
(BEE).Inunstudiodel2015“CNSTherapeutics–aglobalstrategicbusinessreport”,la
societàdianalisidimercatoGIA(GlobalIndustryAnalysts)affermacheoggilaricercaelo
sviluppodifarmaciperilsistemanervosohannofattopassidagigante,esonoarrivatiad
occupare una grande fetta del mercato dei farmaci negli Stati Uniti, anche a causa
dell’aumentodimalattielegateaproblemialsistemanervoso.Nelcorsodeglianni,come

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
4
sipotrànotareanchedaiprossimicapitoli,numerosiesperimentisonostaticondottisul
cervello degli animali al fine di comprendere come e in che misura questi farmaci
oltrepassino la barriera che protegge il CNS.Un altro impedimento per lo sviluppo di
questi farmaci, perlappunto, è proprio la difficoltà di eseguire test che non siano
eccessivamente invasivi, garantendo l’incolumità dei pazienti. La maggior parte dei
fallimenti nello sviluppo di nuove terapie può essere direttamente attribuito
all’insufficientesicurezzaedefficaciadeinuovifarmaci.Dibase,oltreunacertasogliadi
concentrazione tutte le sostanze sono tossiche per il corpo umano. Data la forte
restrizionedi agenti terapeutici che raggiungano il cervello, spesso ci si trova a dover
esporreglialtriorganietessutialivellidiconcentrazionemoltopiùaltidiquellinecessari
alcervello,aumentandoilrischiodi intossicazionedelpaziente(JeffreyeSummerfield,
2010).Inquestocontesto,unavoltachiaritoilmeccanismoconcuiifarmaciraggiungono
l’internodelcervello,simanifestalanecessitàdiunmodellofarmacocineticoingradodi
descrivereeprevedereilprofilodiconcentrazionesecondolemodalitàdiassorbimento,
distribuzione,metabolizzazioneedeliminazionediquestogeneredi farmaciall’interno
del SNC, che possa in un determinato modo dare un contributo allo sviluppo e al
miglioramento dei farmaci. Dal momento che la misura sperimentale della
concentrazionediunfarmacoall’internodelcervelloèunapraticainvasiva,manecessaria
per poter valutare l’efficacia dei farmaci che agiscono sul sistema nervoso centrale,
questostudionascedatalebisogno.Ilpresentelavorohadunquelafinalitàdicostruire
un modello farmacocinetico che possa indagare la concentrazione del farmaco
somministrato nel cervello dei pazienti, andando ad arricchire l’attuale scenario dei
modellifarmacocineticiesistenti.
1.2 Anatomiadelcervello
Perpotercapirecomeifarmaciattraversanolabarrieraematoencefalicaè importante
comprenderecomeèstrutturatoilcervelloe,quindi,ènecessarioavereun’ideadellasua
anatomia.
Ilcervelloèunorganochesitrovanelcranioesisuddivideinquattrosezioniprincipali:
1) Cerebro;
2) Cervelletto;

Introduzione
5
3) Troncocerebrale;
4) Diencefalo.
In Fig.1.2 si possono distinguere le sezioni sopraelencate e le principali parti che le
compongono.
Figura 1.2 Sezione sagittale del cervello, vista mediana. In basso a sinistra, ossia nella parteposteriore, si trova il cervelletto,nellapartecentraleviè il troncocerebraleesopradiesso ildiencefalo. Il cerebro ricopre tutte le altre porzioni di cervello, immagine tratta da Nielsen eTortora(2013).
1.2.1 Cerebro
Ilcerebrorappresentalaporzionepiùgrandedelcervelloe,comesipuòvedereinFig.1.3,
è suddiviso in due differenti metà: l’emisfero cerebrale destro e l’emisfero cerebrale
sinistro, separatidaunsolconotocome“fessura longitudinale”. Il cerebropuòessere
consideratolasededell’intelligenza(NielseneTortora,2013).Ègrazieadesso,infatti,che
l’uomoèingradodileggere,scrivereefarecalcoli.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
6
Figura1.3Vistadall’altodelcerebro.Sipossonofacilmentedistinguereidueemisfericerebralielafessuralongitudinalechelisepara.ImmaginetrattadaEducationalTechnologyClearinghouse–UniversityofSouthFlorida.
1.2.2 Cervelletto
Il cervelletto è la seconda parte più grande del cervello, e si trova nella porzione
posteriore-inferiore della cavità craniale. Le sue funzioni principali sono quelle di
controllareimovimentiiniziatidalleareemotorieecorreggerliquandononsonosvoltiin
maniera adeguata. In Fig.1.4 si può vedere chiaramente dove è posizionato questo
organo.

Introduzione
7
Figura 1.4 Sezione sagittaledel cervello, vistamediana. In basso adestra si puòdistinguere ilcervelletto.ImmaginetrattadaMyers(2006).
1.2.3 Troncocerebrale
Il tronco cerebrale, come si evince dalla Fig.1.5, si trova tra il midollo spinale e il
diencefalo.Questaporzionedicervelloèsuddivisaintrecomponentiprincipali:
1) Il midollo allungato, che rappresenta la parte inferiore ed è la porzione
conclusivadelmidollospinale;
2) Iponticheconnettonoilmidolloallungatoalcervelletto;
3) Ilmesencefalo,chesitrovasopraiponti.
Le funzioni di questo organo sonomolteplici: controllo della pressione sanguigna, del
respiroedeimovimentioculari,edècoinvoltonell’elaborazionedeglistimolidolorosi.
Tutte le connessioni nervose motorie e sensoriali partono dal tronco cerebrale e
raggiungonoilrestodelcorpo.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
8
Figura 1.5 Sezione sagittale e visione mediana del cervello e del midollo spinale. Si possonodistinguere lediverseparti checompongono il troncocerebrale, immagine trattadaNielseneTortora(2013).
1.2.4 Diencefalo
Ildiencefalositrovasoprailmesencefaloedècircondatodagliemisfericerebrali.Essoè
formatoda:
1) Talamo,cherappresentalaporzionepiùgrandedeldiencefaloedècoinvoltonella
trasmissionedegliimpulsinervosi;
2) Ipotalamo,partemoltopiccoladeldiencefalochecontrollal’omeostasidelcorpo,
ossia cercadimantenerecostanti alcuniparametri vitali,quale,adesempio, la
temperaturacorporea.
3) Epitalamo,unapiccolaregionechesi trovanellaparteposteriore-superioredel
talamo.Quisitrovalaghiandolapinealechesecernel’ormonemelatonina,molto
importante perché induce il sonno. L’epitalamo ha un ruolo rilevante nella
percezione degli odori: in particolare è responsabile della risposta emotiva a
quest’ultimi.
InFig.1.6ildiencefaloèrappresentatoevidenziandolesueparticostituenti.

Introduzione
9
Figura1.6Visionemedianadellasezionesagittaledeldiencefalo,immaginetrattadaMcKinleyetal.(2015).
1.3 Protezioneevascolarizzazionedelcervello
Data la grande importanza del cervello e del suo corretto funzionamento, esiste un
efficiente sistema di protezione che garantisce la difesa da ciò che potrebbe
comprometternel’integritàfisico-chimica.Ciòsitraduceancheinuncomplessosistema
diapportodisangueenutrientialcervello.Èsoprattuttoperquestomotivo,infatti,che
il trasporto di farmaci all’interno del cervello risulta così difficoltoso. Di seguito sono
descritti i sistemi di protezione presenti, ed il meccanismo di apporto del sangue al
cervello.
1.3.1 Lemeningi
Ilcraniofornisceunaprotezionemeccanicaalcervello:riduceidanniquandocisonourti
eprevieneuncontattodirettoconl’ambienteesterno.Fraleossaeilcervellocisonole
meningichecircondanoquest’ultimo.Lemeningisonoformatedatrestrati:

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
10
1) Lostratopiùesternoèchiamato“duramadre”,edèsuddivisoulteriormentein
duestrati:quello internodetto“stratomeningeo”,equelloesternonotocome
“stratoperiostale”;
2) Lo strato inmezzo è chiamato “aracnoide”, tessuto epitelialemultistrato con
giunzionimolto strette tra le cellule che garantiscono una tenuta efficace che
avvolgeilcervellocostituendolacosìdettabarrieraaracnoidea;
3) Lostratopiùinternoènotocome“piamadre”.
Iduestratichecompongonoladuramadresonosempreacontatto,eccettoneipunti
dove sonopresenti i seni venosi.Questiultimihanno la funzionedidrenare il sangue
venosodalcervelloallavenagiugulare.
Fralostratoperiostaleeleossadelcranioesisteunspazionotocome“spazioepidurale”.
Idueemisferidelcerebrosonodivisidaun’estensionedellapiamadreconosciutacome
“falxcerebri”.InFig.1.7èbenvisibilelastrutturadellemeningiappenadescritta.
Figura1.7Visioneanterioredellasezionefrontaledelcranio,sipossonodistinguereivaristratidellemeningi.ImmaginetrattadaNielseneTortora(2013).
1.3.2 Liquidocerebrospinale
Il liquido cerebrospinale (FCS, denominato anche liquor, liquido cefalo-
rachidiano o liquido rachido-spinale) fornisce un’ulteriore protezione al cervello e al
midollospinale,controeventualirischifisiciochimici.Questofluido,incoloreeformato
prevalentementedaacqua,haanchelafunzionedifornireallecelluledelcervellopiccole
quantitàdisostanzenutritivechesitrovanonelsangue,comeadesempioglucosiood

Introduzione
11
ossigeno.Ilvolumediliquorall’internodelcorpodiunadultosanoècompresofragli80
ei150mL.Essofluiscecontinuamentenellospaziocheintercorrefral’aracnoideelapia
madre, il così detto “spazio subaracnoidale”. È importante sottolineare che lo spazio
subaracnoidaleeilliquidocefalorachidianocontenutoalsuointernosonopresentianche
nelmidollospinale.
Nelcervellosonopresentiquattrocavitàchiamate“ventricoli”,essisonorappresentatiin
Fig.1.8:
1) Due si trovano in ciascuno dei due emisferi del cervello e sono noti come
“ventricolilaterali”;
2) Il terzoventricoloè localizzatosulla lineamedianasuperioreall’ipotalamoedè
compresotralametàsinistraedestradeltalamo;
3) Ilquartoventricolositrovatrailcervellettoeiltroncocerebrale.
Illiquidocerebrospinalesiformaedèraccoltoinquestequattrocavitàprimadiiniziarea
scorrere. La formazione del liquor avviene nei plessi coroidei, la cui sezione è
rappresentata in Fig.1.9. I plessi coroidei sono capillarimodificati che si trovano sulle
pareti dei ventricoli epermettono il passaggio solodipoche sostanze, tra cui l’acqua.
Questa filtrazione avviene grazie al fatto che i plessi coroidei sono formati da cellule
ependimali unite tra loro da giunzioni molto strette: esse non permettono perdite e
quindituttelesostanzedevonopassareattraversolecellulechecompongonolepareti.
Questosistemadiprotezionecostituiscelacosìdetta“barrieracerebrospinale”(Blood-
Cerebro Spinal Fluid barrier, BCS). Le cellule ependimali sono un tipo di cellule gliali.
Questenonsonodirettamentecoinvoltenellatrasmissionediimpulsinervosi,mahanno
lafunzionedisupportareineuroni.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
12
Figura1.8Visioneanterioredelcervello.Sonoevidenziati iquattroventricolie leaperturechepermettonogliscambifraessi.ImmaginetrattadaNielseneTortora(2013).
Da ogni ventricolo laterale il liquido cerebrospinale che si è formato giunge nel terzo
ventricoloattraversoduepiccoleaperture,chiamate“foriintraventricolari”.Quiraccoglie
laporzionediliquidoprodottaneiplessicoroideidiquestoventricolo,esuccessivamente
scorre attraverso l’acquedotto del mesencefalo nel quarto ventricolo, dove viene
aggiunto di contributo di liquor generato dai propri plessi coroidei. Da quest’ultimo
ventricolounapiccolaporzionediliquidocefalorachidianopassanelcanalecentraledel
midollo spinale,mentre la restantepartevanello spaziosubaracnoideoattraverso tre
aperture(unacentraleeduelaterali)presentinelquartoventricolo.NellaFig.1.10sono
riassuntiipassaggiappenaelencati.

Introduzione
13
Figura1.9Dettagliodiunasezionefrontalediunplessocoroideo.Lafrecciaindicaladirezionedellafiltrazionedalsanguealliquor,immaginetrattadaNielseneTortora(2013).
Non c’è alcun accumulo di liquido cerebrospinale perché è riassorbito nel sangue
attraversoivilliaracnoidei(NielseneTortora,2013)conlastessavelocitàconcuiviene
prodotto(20mL/h).Illiquidoriassorbitoèraccoltoneisenivenosichelodrenano,come
sivedeinFig.1.11,nellevenechefuoriesconodalcervello.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
14
Figura1.10Riassuntodellaformazione,circolazioneeassorbimentodelliquor.ImmaginetrattadaNielseneTortora(2013).
Figura1.11Vistaposterioredeisenivenosiedelleprincipalivenechefuoriesconodalcervello.ImmaginetrattadaDepartmentofMedicineandHaematology,CalicutMedicalCollege.

Introduzione
15
1.3.3 Barrieraematoencefalica
Il sangue raggiunge il cervello principalmente attraverso l’arteria carotide interna e le
arterievertebrali.ComesievincedallaFig.1.12,inunadultoquest’organorappresentail
2%delpesototaledelcorpomaconsumaquasiil20%dell’ossigenoedelglucosiopresenti
(NielseneTortora,2013).
Figura1.12Vistadalbasso (sulla sinistra)evisione laterale (sulladestra)dellacircolazionedelsanguearteriosonelcervello.ImmaginetrattadaNiekroetal.(2008).
Nelcervellocisonocirca100miliardidicapillari(VanTelligenetal,2015),circaunoper
ciascunneurone.Essisonocostituitidacelluleendotelialichesonosigillatestrettamente
l’una con l’altra e circondate da astrociti (un altro tipo di cellule gliali). Questi ultimi
premono fortemente contro i capillari e secernono sostanze che forniscono le
caratteristichedipermeabilitàallegiunzioni.Questecelluleinsiemeagliastrocitiformano
lacosiddetta“barrieraematoencefalica”(BEE),presenteinciascuncapillareadeccezione
diquellicheraggiungonoiplessicoroidei.
Generalmentemolecole piccole e lipofile possono attraversare questa barriera. Nella
Tab.1.1vengonoelencatequalisostanzepossonoononpossonoattraversarla.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
16
Tabella1.1Elencodelleprincipalisostanzechepossonoononpossonoattraversarelabarrieraematoencefalica
SostanzecheattraversanolabarrieraSostanzechenonattraversanola
barriera
Glucosio Sostanzesolubiliinacqua
Agentianestetici Proteine
Anidridecarbonicaedossigeno Antibiotici
Sostanzelipofile
Altresostanze,comel’urea,lacreatinaelamaggiorpartedegliionipossonoattraversare
labarrieraematoencefalicama solomolto lentamente.Essaè talmenteefficiente che
previeneilpassaggiodisostanzetossichema,talvolta,anchedisostanzeutilicome,ad
esempio, i farmaci. Questo è un punto cruciale perché per trattare malattie quali
Alzheimer o il cancro al cervello, i farmaci devono attraversare la barriera
ematoencefalica(Pardridge,2003).
1.4 Trasportodeifarmacialcervello
Dopoaverintrodottol’anatomiadelcervello,sipuòpassareoraallatrattazionedicome
avvieneiltrasportodifarmacialcervelloche,nonostanteletantericerche,adogginonè
ancoradel tutto chiaro, specialmentenegli umani. È doveroso ricordare che i farmaci
raggiungono il cervello tramite il sangue, dove sono presenti con una certa
concentrazione dopo la somministrazione. Come più volte ripetuto nei paragrafi
precedenti,sonomolteledifficoltàcheincontranogliagentiterapeuticinelsuperareil
complessosistemadiprotezionedelsistemanervosocentrale.Riassumendo,tresonole
barrierecheseparanoilsanguechescorreneivasisanguignidalcervello(Fig.1.13):
• Barrieraematoencefalica(BEE);
• Barrieracerebro-spinale(BCS);
• Barrieraaracnoidea.

Introduzione
17
Figura1.13Rappresentazionedelletrebarriereprincipalitrasangueecervello:(a)BEE;(b)BCS;(c)barrieraaracnoidea,immaginetrattadaAbbottetal.(2009).
Labarrieraematoencefalicaèdi gran lunga l’area superficialepiùampiapergli adulti
umani,evariatrai12ei18m2.Nessunacellulainternaalcervelloèpiùlontanadi25µm
dauncapillare,quindi,unavoltaattraversatalaBEE,ledistanzedidiffusionedeifarmaci
versoineuroniealtrecellulesonomoltobrevi.IlpassaggioattraversolaBEEè,dunque,
il cammino preferenziale per il raggiungimento da parte dei farmaci delle cellule del
cervello.Alcuni farmacie soluti entranonel cervelloancheattraverso iplessi coroidei
riversandosi nel FCS, trovandosi così a dover superare la BCS. La barriera aracnoidea,
invece, comedetto in precedenza, è privadi vasi sanguigni. I villi aracnoidali presenti
riassorbono una notevole quantità di FCS, fungendo così da “valvole”. Questi villi
permettonosolo ilmovimentodelFCSfuoridalcervello,portandoloverso ilsangue. Il
trasporto attraverso la membrana aracnoidea non è, quindi, una via importante per
l’ingressodicompostinelcervello(Abbottetal.,2009).Pertalemotivo,questabarriera
nonsaràinclusanell’analisidelmeccanismoditrasporto.Quandoinquestoparagrafosi

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
18
parleràdibarriere,sifaràriferimentoesclusivamenteallaBEEeallaBCS,cheassolvonoai
compitidi:
1. Fornirenutrientiessenzialialcervello;
2. Eliminareimetabolitieventualmenteformatiall’internodelcervello;
3. Prevenirel’ingressodisostanzetossichenelcervello.
Imeccanismi di trasporto in entrata ed in uscita dalle barriere saranno analizzati per
ciascunadelleduebarriere.
1.4.1 Sistemaditrasportoiningressosangue-cervelloattraversolaBEE
SecondolostudiodiPardridge(2003),ilsistemadiingressodifarmaciesolutiall’interno
delcervellopassandoperlaBEEpuòesseresuddivisoinduemeccanismi:
• Meccanismochimico;
• Meccanismobiologico.
Permeccanismochimicosiintendeunsistemabasatosullanaturadellasostanzachedeve
entrarenelcervello.Comeribaditonelcapitoloprecedente,infatti,solomolecolepiccole
epreferibilmentelipofilepossonoattraversarelabarrierainmanieranaturale,secondo
unprincipiodidiffusionepassivaversol’interno.Perciò,quellocheiricercatoriprovano
a fareè rendere lipofile lemolecoledei farmacidi interesse facilitandone ilpassaggio
verso l’interno del cervello, ma questo comporta un aumento del peso molecolare,
ostacolandoilpassaggioattraversolaBEE.Sicercaquindidirestareintornoadunpeso
molecolaredelfarmacoinferiorea300-400g/mol(Pardridge,2003).
L’approcciobasatosullabiologia,invece,descriveilmeccanismodiingressoattraversola
BEEsecondounsistemaditrasportoattivo.Questoavvienemedianteopportunicarrier
(e.g.GLUT1,proteinatrasportatricediglucosio,OCT,proteinetrasportatricidicomposti
cationici).Inquesticasilastrutturadelfarmacodeveimitarequelladellamolecolache
fungedatrasportatrice,inmododapotersilegareadessa.

Introduzione
19
1.4.2 Sistema di trasporto in uscita cervello-sangue attraverso laBEE
IltrasportoinuscitadallaBEEgiocaunruolopredominantenellaristrettadistribuzione
dei farmaci nei tessuti cerebrali. Il meccanismo è caratterizzato esclusivamente da
trasportoattivo(Fig.1.14).All’interfacciatramembranaeplasma(latoluminale)vièun
sistemadipompaggiocheprevieneladistribuzionedelfarmaconelcervello.Lemolecole
coinvoltesonoleproteineABC(ATP-bindingcassette),trasportatoritransmembranache
sfruttano l’energia dell’idrolisi di ATP per trasportare varie sostanze attraverso le
membrane cellulari. Una di queste è la P-glicoproteina (P-gp), che ricopre un ruolo
fondamentale nella riduzione della permeabilità della BEE (Ohtsuki e Terasaki, 2007).
L’importanzadellaP-gpèstataampiamentedimostrataattraversoesperimentisurattiin
cui,inibendolaconopportuniinibitori,risultavanoconcentrazionidifarmacopiùelevate
all’internodelcervello(Xieetal.,1999).
Figura1.14MeccanismiditrasportoinentrataeuscitadallaBEE.ImmaginetrattadaOhtsukieTerasaki(2007).
In Tab.1.2 sono riportati i principali trasportatori coinvolti nel trasporto attivo nella
barrieraematoencefalica.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
20
Tabella1.2Principali trasportatorie sistemidi trasportoattraverso laBEE. Localizzazionesullamembrana:latoluminale(L)eabluminale(A)dellecelluleendotelialideicapillari.Direzione:dalsanguealcervello(In)edalcervelloalsangue(Ef).NDnondeterminato.TabellatrattadaOhtsukieTerasaki,2007.
Transporters Substrates Localization Direction
Energytransportsystem
GLUT1 D-Glucose L,A In
MCT1 L-Lactate,monocarboxylates L,A In
CRT Creatine L,A In
Aminoacidtransportsystem
EAAT1,2,3 Anionicaminoacids A Ef
ASCT2 L-Asp,L-Glu A Ef
Neurotrasmittertransportsystem
GAT2/BGT1 γ-Aminobutyricacid ND Ef
SERT Serotonin L,A ND
Organicaniontransportsystem
OAT3 PAH,HVA,indoxylsulfate A Ef
oatp2 Digoxin,organicanions L,A In,Ef
ABCtransporters
ABCB1/MDR1 Vincristine,cyclosporinA L Ef
ABCG2/BCRP Mitoxantron,topotecan L Ef
1.4.3 SistemiditrasportoiningressoeinuscitaattraversolaBCS
Il sistema di trasporto sulla BCS gioca un ruolo importante nell’omeostasi del FCS,
preservandolo dalla presenza di farmaci al suo interno. Ilmeccanismo di trasporto di
farmaciesolutiprevedeessenzialmenteilfenomenoditrasportoattivomediantecarrier
in ingresso e mediante carrier o proteine ABC in uscita. Poiché la BCS ha un’area

Introduzione
21
superficialemolto inferioreallaBEE,questabarrieraèattraversatadaunaquantitàdi
farmaciesolutimoltoinferiorerispettoallaBEE.
In Tab.1.3 sono riportati i principali trasportatori che si trovano sulla barriera
cerebrospinale.
Nellabarrieracerebrospinaleillatobasaleèrivoltoversoilcervello,mentrequelloapicale
èrivoltoversoivasisanguigni.
Tabella1.3TrasportatoriattraversolaBCS.Localizzazione:latoapicale(BB)elatobasale(BL)dellecelluleepitelialideiplessicoroidei.Direzione:dalsanguealFCS(In)edalFCSalsangue(Ef).NDnondeterminato.TabellatrattaDrugdeliverytothebrain,AAPS2014.
Transporters Substrates Localization Direction
Energytransportsystem
GLUT1 D-Glucose BL ND
Crt Guanidinoacetate BB Ef
Peptides
Pept Dipeptides ND Ef
Organiccationtransportsystem
Pmat Monoamineneurotrasmitters BB Ef
Oct3 Creatinine BB Ef
Organicaniontransportsystem
OAT3 PAH,estronesulfate BB Ef
Pgt Prostaglandin BB Ef
Oatp1a5 Digoxin,organicanions BB Ef
ABCtransporters
ABCA1 Cholesterol BB In
ABCC4/MRP4 Topotecan BL Ef
1.5 Analgesiaeanestesia
Tra lemolteplici patologie edisturbi che interessano il sistemanervoso centraledegli
uomini, e, più in generale, degli esseri viventi, uno dei sintomi clinici più comuni, e

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
22
complessi allo stesso tempo, è il dolore (Sverrisdóttir et al.,2015). Negli anni, il suo
trattamentosièrivelatounasfidapernumerosimedici.Perridurreildoloresipossono
usarefarmacianesteticioanalgesici (notianchecomeantidolorifici).Ladifferenzache
intercorrefraquestedueclassidifarmacièilmeccanismod’azione:glianalgesiciagiscono
senzaalterarelapercezionesensorialeoinfluenzarelaconsapevolezzadelpaziente,cosa
chefanno,invece,glianestetici.Gliantidolorificiallevianoildoloreriducendolarisposta
infiammatorialocale,onelcasodeglioppioidi,diminuendoilnumerodisegnalidolorosi
inviati dal sistemanervoso.Molti analgesici sonooppioidi e quindi si ha un’attività di
ricerca,checontinuatuttora,voltaatrovareuncompromessochepermettaatalifarmaci
di dare un sollievo al dolore riducendo alminimo gli effetti collaterali di quest’ultimi.
Pertantouncontrollodellaconcentrazionedeifarmacianalgesiciall’internodeitessutiè
importanteperunadupliceragione:
1) Mantenere la concentrazione del farmaco sopra un limite inferiore cosicché si
consegual’effettoanalgesico;
2) Mantenerelaconcentrazionedelfarmacosottounlimitesuperioreaffinchénon
simanifestinoeffetticollaterali.
1.5.1 Morfina
Lamorfina (Fig.1.15)èunalcaloidenaturalederivatodall’oppiodelpapaveroPapaver
Somniferum,edèl’oppioidepiùutilizzatoperiltrattamentosiadidoloremoderatoche
più grave, acuto o cronico (Sverrisdóttir et al., 2015). Si tratta dell’alcaloide più
abbondantepresentenell’oppioedèestrattadallalinfaessiccatafuoriuscitadalprofondo
taglio effettuato sulle capsule immature prodotte dal fiore. La sua formula chimica è
C17H19NO3equestamolecolahacaratteristicheidrofile.

Introduzione
23
Figura1.15Strutturachimicadellamorfina.Adestragliatomidiossigenosonorappresentatiinrosso, inazzurroquellidi idrogeno, ingrigioquellidicarbonioe inblu l’unicoatomodiazoto.ImmaginetrattadaDrugBank.
1.5.2 ADMEdellamorfina
La morfina può essere somministrata per via orale, subcutanea, intramuscolare,
intravenosaerettale.Spessoquestoanalgesicononlositrovanellaformapura,macome
morfinasolfato:questaformaèparticolarmentevantaggiosanelcasodiassunzioneorale
inquantone favorisce l’assorbimento. Lamorfinaèassorbitaquasial100%dal tratto
gastrointestinaledopounasomministrazioneorale(Christrup,1997).Essaèunsubstrato
per la P-glicoproteina, che si trova sul tessuto epiteliale dell’intestino e su quello
endoteliale della barriera ematoencefalica (Ederoth et al.,2004; Tunblad et al.,2003):
comesipotràosservareneiparagrafieneicapitolisuccessiviquest’ultimacaratteristicaè
molto importante per lo studio effettuato. Questo analgesico viene distribuitomolto
rapidamenteneitessutimoltoperfusidalsangue,qualiipolmoni,irenieilfegato.Circa
il90%dellamorfinavieneeliminataattraversoilmetabolismoepatico.Comesivedrànel
Capitolo 3questo analgesicodà luogo aduemetaboliti principali:metil-3-glocuronide
(M3G)emetil-6-glocuronide(M6G).
Approssimativamenteil15%delladosedimorfinainizialeèespulsacomemorfinapura,
il 45-65% come M3G, 10-15% come M6G ed il restante 5% come metaboliti minori
(Christrup,1997).Circail90%dellamorfinaedeisuoimetabolitisonoeliminatiattraverso
l’urina,larestanteparteattraversolefeci.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
24
1.5.3 Meccanismod’azionedellamorfina
Primadipoterdiscuteresucomeagiscelamorfinasulsistemanervoso,ènecessariofare
unabreveintroduzioneperspiegarecosasianoirecettoridelsistemanervosocentrale.I
recettorisonomolecolechesipossonotrovaresullasuperficiedellecelluleoall’interno
delcitoplasma.Ifarmaciperpoterfunzionaredevonointeragireconquestemolecole.Le
molecolechesi leganoconirecettorisonodette“ligandi”epossonoattivareo inibire
questiultimi.Laregionedelrecettoreacuisilegailligandoèdetta“sitoaccettore”.Le
caratteristiche chimiche e fisiche di un farmaco determinano la possibilità che
quest’ultimosipossalegareomenoadundeterminatosito(Fig.1.16).
Figura 1.16 Il farmaco A può interagire con il recettore al contrario del farmaco B, a seguitodell’interazionetraiduesihal’effettofarmacologico.ImmaginetrattadaPharmacyMagazine.
Il tempo di vita del complesso farmaco-recettore influenza l’effetto farmacologico. Il
tempod’esistenzadelcomplessoèinfluenzatodaiprocessidinamicichecontrollanola
velocitàd’associazioneedissociazionetrafarmacoerecettore.Sipossonodefiniredue
tipidi ligandi: agonisti edantagonisti. I ligandiagonisti,unavolta legatisi al recettore,
attivanoquest’ultimoinmodotaledariceverelarispostadesiderata.Alcontrarioquelli
antagonisti si legano al sito accettore e disattivano il recettore. I ligandi antagonisti
possonoessereclassificatireversibilioirreversibili:reversibiliquandoiltempodivitadel
complesso è breve, mentre sono irreversibili quando il complesso che si forma è
permanenteoquasipermanente.
Se nel sistema preso in considerazione ci sono sia ligandi antagonisti che agonisti è
possibileavereduesituazioni:

Introduzione
25
1) Interazione competitiva,ossiaentrambe le specie si possono legareallo stesso
sito.Pertantosel’agonistasilegaalsitoprevienechel’antagonistapossafarelo
stesso,eviceversa.
2) Interazionenoncompetitiva,l’antagonistasipuòlegareadunsitodelrecettore
chenonèsfruttatodall’agonista,quindientrambiitipidiligandisipossonotrovare
sullo stesso recettore. Quando avviene ciò l’affinità o l’efficacia dell’agonista
diminuisce.
InFig.1.17vieneillustratounesempiodeimeccanismiappenaillustrati.
Figura1.17Asinistraeadestravienemostratoilmeccanismocompetitivodovesolounrecettorepuòinteragireconilsitoaccettore,alcentroentrambiiligandipossonointeragireconlostessorecettorequindisihaunmeccanismononcompetitivo.ImmaginetrattadaMembraneReceptors.
Avallediquesteconsiderazionièpossibileoraanalizzare ilmeccanismod’azionedella
morfina.
Lamorfinaeglioppioidiingeneralepossonointeragirecontrediversitipidirecettori:
1) µ,orecettorimu,sonorecettorichesitrovanoneltroncocerebraleeneltalamo.
Aun’attivazionediquesticonseguediminuzionedeldoloreprovato,sedazione,
euforia,depressionerespiratoria,costipazioneedipendenzafisica.Èopportuno
sottolinearecheèpossibiledistingueretraduetipidirecettorimu:µ1eµ2,ilprimo
se attivato provoca analgesia, il secondo, invece, tutti gli altri effetti
summenzionati;
2) k, o recettori kappa, sono recettori che si trovano nel diencefalo, nel tronco
cerebraleenelmidollospinale.Anch’essiseattivatiprovocanodiminuzionedel
dolore,sedazioneedipendenza;

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
26
3) d,orecettoridelta,sonorecettoriampiamentedistribuitinelcervello,nelmidollo
spinaleeneltrattodigestivo.Menocoinvoltinell’attivitàanalgesicadeglioppioidi,
seattivatiprovocanoladiminuzionedell’attivitàdeltrattointestinaleeinducono
unadepressionedelsistemaimmunitario.
Lamorfinainteragiscefortementeconirecettoriµ(inparticolarequelliµ1),conmodalità
finoa10voltepiùforterispettoaglialtriduerecettori(Sverrisdóttiretal.,2015).
Avallediquesteinformazioni,èpossibileintrodurre,apartiredalprossimocapitolo, il
lavorocheèstatosvoltoperlacreazionedelmodellofarmacocineticodellamorfina.

27
2 Modellofarmacocineticodellamorfinaneiratti
Alfinedicostruireunmodellofarmacocineticocheincludailcervelloedesprimailprofilo
di concentrazionedellamorfinaal suo interno,è stataeffettuatauna raccoltadati da
esperimenti condotti sui ratti. Stando a quanto osservato in letteratura, è su questi
animali che la morfina è stata prevalentemente studiata, cercando di capirne il
meccanismod’azioneelasuafarmacocinetica.Iratti,infatti,inqualitàdimammiferidalle
dimensionicontenute,siprestanoinmanierasoddisfacenteaquestatipologiadistudi,e
possono essere d’aiuto per affrontare lo stesso problema negli umani. In letteratura,
infatti,nonsonodisponibilidati sullaconcentrazionedimorfinanelcervelloumanodi
individui sani, ma se ne trovano alcuni ricavati da prelievi effettuati su pazienti che
avevanosubitoungravetraumacranico(Bouwetal.2001).Questoèdovutoalfattoche
sitrattadiproceduremoltoinvasiveperlamisuradellaconcentrazionedelfarmaconel
cervello.Dunque, lascarsitàdidatinegliumanie l’abbondanzadidatiestudisui ratti
hannocondottoadapprocciarequestostudiopartendodaunmodellobasatosuiratti.Il
metodo adottato prevede la costruzione di un modello farmacocinetico
tricompartimentale, inaccordoconlamaggiorpartedeglistudipresenti in letteratura,
per poi andare a costruire un modello PBPK (dall’inglese Pharmacologically Based
PharmacoKineticmodel)piùdettagliato.Nelprossimocapitolosaràpropostounmodello
analogopergliumani.
2.1 Statodell’arte
ComeribaditonelCapitolo1,laprevisionedellapenetrazionedeifarmaciattraversola
BEEdell’uomoèoggettodistudiodamoltianni.L’approcciopiùtradizionaleutilizzato
fino alla fine dello scorso secolo per la previsione della penetrazione di farmaci nel
cervello e la descrizione delmeccanismo coinvolto in questo processo consisteva nel
correlareladistribuzioneincondizionistazionariedelfarmaconelcervello,definitacome
il rapporto tra laconcentrazione totaledel farmaconel cervelloequellanelplasmao
sangue(indicatoconlasiglaKp,brain), inspeciepreclinichecomeiratti,conleproprietà

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
28
molecolaridellostessofarmaco(Feheretal.2000).Questometodohavarielimitazioni:
primafratuttequelladiprendereinconsiderazionelaconcentrazionetotaledelfarmaco
alpostodellaconcentrazionedifarmacononlegatoalleproteine.Inoltre,inquestomodo
ilrisultatononeraunprofilofarmacocinetico,masingolemisurediconcentrazione.Un
miglioramento di questo approccio si è avuto quando nel rapporto tra farmaco nel
cervelloefarmaconelsanguesièpassatiaconsiderareladistribuzionedifarmacolibero,
senza tenere in considerazione quello legato alle proteine (Kp,uu,brain). Comunque, un
approcciobasatosull’usodisingoliparametriperladescrizionedeivariprocessicinetici
coinvoltinellapenetrazionedellaBEEdapartedelfarmacorestapiuttostolimitativo.Un
approcciochenel tempostaguadagnandosemprepiùpopolaritàèquellodeimodelli
PBPK, in gradodi simulare la concentrazionedi farmaconei tessuti e negli organi dei
pazienti.Talimodellisonospessoingradodieffettuareancheprevisionitradiversespecie
epopolazioni(Espiéetal.2009).SonopochiperòimodelliPBPKingradodidescriverei
variprocessicineticichecaratterizzanoiltrasportodeifarmacinelcorpoe,quindi,nel
cervello,chepossonoesserepredettiaprioriattraversoloscalingdiparametrifisiologici
misurati in vitro.Non sonomolti imodelli cheutilizzanoquesti dati, in quanto risulta
complesso riprodurre in vitro la struttura della BEE e, a maggior ragione, altrettanto
difficoltosorisultaloscalinginvitro-invivo.
Perquantoriguardalamorfina,lamaggiorpartedeimodelliriscontratiinletteraturasono
modelliatreoquattrocompartimenti,tutticonvalidaticonmisuresperimentaliraccolte
neiratti.Giànellaprimametàdeglianni’70sonoiniziatiiprimistudisullafarmacocinetica
dellamorfina,conloscopodicorrelarnelafarmacocineticaaisuoieffettifarmacologici
(Dahlstrom et al. 1975). Il modello farmacocinetico usato da Dahlstrom è
tricompartimentaleoveuncompartimentorappresentailplasma,chescambiainmaniera
reversibileconglialtridue,unoèilcervelloeunoraccoglietuttiglialtriorganietessuti.
Inquestocasoivalorideiparametridelmodellosonoottenutiattraversounprogramma
diregressionenonlineare.UnaltromodellopresenteinletteraturaèquellodiBouwet
al.(2000).Sitrattadiunmodelloaquattrocompartimenti:uncompartimentoplasma,un
compartimento per organi e tessuti periferici, e due compartimenti per descrivere il
cervello,unoperindicarelaquantitàdimorfinatotalenelcervello,eunoperidentificare

Modellofarmacocineticodellamorfinaneiratti
29
lamorfinaliberadalegamiconleproteinedelsangue.IlmodellodiBouwhacomescopo
quellodimisurarel’effettoanalgesicodatodallamorfinacorrelandoloallaconcentrazione
dimorfinapresentenelcervello,edhacomelimitequellodinonconsiderarelamorfina
chedal cervello rientranelplasma,maessavienedirettamenteeliminatadal cervello
attraversounaclearanceinuscita.Infine,unmodellofarmacocineticoperladescrizione
dellamorfinanelSNCèquellopresentatodaBourassetetal.(2006).Inquestostudiogli
autorisonoandatimoltoafondo,costruendounmodelloaquattrocompartimentidicui
unoper il plasmae treper il cervello (i.e. fluidoextracellulare, fluido intra-cellularee
fluidocerebrospinale).Nelmodellopropostoilcompartimentoplasmaeilcervellosono
in comunicazione sia con il compartimento del FCS che con quello del liquido
extracellulare,acuiècollegatoasuavoltailcompartimentodelfluidointracellulare.Così
facendo,sonoriuscitiadottenereunadescrizionemoltodettagliatadeiprocessicinetici
dellamorfinanelcervello.D’altrocantorisultadifficilepoterapplicarequestomodellosu
largascala.Èraro,infatti,avereadisposizionedatisperimentaliditutteetreifluididel
cervello.Nellamaggiorpartedeicasilemisuresperimentalinelcervellodeirattiderivano
dallarimozionedelcervelloesuccessivaomogeneizzazioneecentrifugazione.Daquipoi
vengonoprelevatiidatisulleconcentrazionimedienelcervello.
Inquestolavoroditesivengonodescrittiduemodelli,unotricompartimentaleeunoa7
compartimenti.Ilmodellotricompartimentalepropostoèmoltosimileaquellodescritto
daDahlstrom,enascecomeprecursoredelmodelloa7compartimenti incuivengono
differenziati,perquantopossibile,iprincipaliorganidelcorpo.Ilvantaggiochesidesidera
ottenere dalla costruzione del modello a 7 compartimenti è quello di avere una
descrizione della farmacocinetica nel cervello relativamente semplice ma esaustiva,
essendo solo uno il compartimento dedicato a questo organo. In più, avendo a
disposizione il compartimento del fegato, sarà possibile, come si vedrà più avanti,
descrivereilprocessodimetabolizzazionedellamorfina,datal’importanzadialcunisuoi
metaboliti.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
30
2.2 Modellotricompartimentale
Afrontedeglistudifinquieffettuatiedell’analisideimodellipiùcomunementeusatiper
descriverelafarmacocineticadifarmacinelcervellodeiratti,sièdecisodicostruireun
modello farmacocinetico tricompartimentale. Il modello prevede, dunque, tre
compartimenti:
1. Uncompartimentocentralecheinglobaplasmaeorganimoltoperfusi;
2. Uncompartimentoperitessutipocoperfusi;
3. Uncompartimentoperilcervello.
Per organi molto perfusi si intendono tutti quegli organi che hanno più bisogno di
nutrienti dal sangue per funzionare. Questi sono il cuore, il fegato, la milza, il tratto
gastrointestinaleeireni.L’intuizionedelcompartimentocentraleèinaccordosiaconlo
studio di Hasegawa (2010) in cui la farmacocinetica dellamorfina nei ratti è studiata
medianteunmodellobicompartimentaledoveuncompartimentocentralerappresentail
plasmaegliorganipiùirrorati,euncompartimentoperifericorappresentatuttigliorgani
e i tessuti meno perfusi. Il compartimento dei tessuti poco perfusi include il tessuto
adiposo,lapelle,imuscoli,ipolmonieilsistemascheletrico.Infine,ilcompartimentodel
cervelloracchiudealsuointernotuttoilcervelloeilsuosistemavascolare.Rispettoalla
molteplicità dimetodi utilizzati in letteratura per descrivere il cervello in unmodello
farmacocinetico, si è scelto di descriverlo adottando uno schema semplificativo. In
letteratura, infatti, si possono trovare delle rappresentazioni schematiche molto
dettagliatechedescrivonoilcervellonellaquasitotalitàdellesuecomponenti,andando
adindagarelaconcentrazionedeifarmacinelfluidoextra-cellularealdilàdellaBEE,nel
fluido cerebrospinale e nel fluido intra-cellulare. In questo studio, invece, per ragioni
legatealladifficoltàdireperireinletteraturalamisuradelleconcentrazionisperimentali
in tutte le aree del cervello, si è deciso di assumere la concentrazione dellamorfina
all’interno del cervello costante fra le diverse aree e uguale a quella del fluido
extracellulare. Questa assunzione è lecita perché la quantità di fluido extracellulare
all’internodelcervelloèmoltomaggiorerispettoallaquantitàdeglialtrifluidi,inoltrele
concentrazionidimorfinaall’internodeidiversifluidipresentinelcervellononmostrano
grandidifferenzefra loro.Cosìstrutturato, ilmodelloprevedeunnumerodiequazioni

Modellofarmacocineticodellamorfinaneiratti
31
coinvoltepariatre,unaperciascuncompartimento,portandoadunasemplicitàdicalcolo
notevole. Tale approccio, nonostante sia piuttosto semplificativo, ha consentito di
ottenereunabuonaconcordanzatradatisperimentalieconcentrazionipreviste.Infigura
2.1èillustratoloschemadelmodelloadottato.
Figura2.1Schemadelmodellotricompartimentaleperiratti.Lefrecceindicanoladirezionedeiflussitraicompartimenti.Ilsignificatodeiparametriindicatisuciascunafrecciaverràspiegatopiùneldettaglioneiprossimiparagrafi.
Lacostruzionedelmodelloèavvenutaattraversol’identificazionedi12parametri,chesi
suddividono in (i) individualizzati, (ii) assegnati e (iii) gradi di libertà. I parametri
individualizzatisonoqueiparametrichehannounvalorespecificoperciascunindividuo,
dipendentiinqualchemododallecaratteristichefisichedeiratti.Iparametrisonoquelli
il cui valore è costante per tutti gli individui esaminati. Infine, i gradi di libertà sono
incognitievengonoidentificatimedianteun’opportunaottimizzazionechesaràdiscussa
piùavanti.Iparametriindividualizzatisono4,tuttilegatiall’anatomiadeiratti,esono:la
superficiediscambiotraplasmaecervelloSparia150cm2/gbrain(Fenstermacheretal.
1988)eivolumidiciascuncompartimento.Ognicompartimentodelmodello,infatti,è
statodefinitoattraversodellespecifichefisiologichequantopiùpossibileprecise,inmodo
darestarefedeliallastrutturafisicadeiratti.Questicompartimentipossonoessereintesi
comecontenitori,dotatiquindidivolumeproprioottenutodallasommadeivolumidegli
organiedei tessuti checontengono. I vari volumi sonostatiottenuti sfruttando idati
presentiinletteratura(Brownetal.1997).Nellospecifico,notaladensitàridiciascun
organoedatalafrazionemassivaFrBMidiognunorispettoalrattodimassaBM,èstato

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
32
semplice andare a ricavare il volumedei tre compartimenti: VCC, VPP, VB, seguendo la
formula:
iBM
ii
BM FrVr×
=å (1)
Nellatabella2.1siriportanoidatirelativialcalcolodelvolumedegliorgani.
Tabella2.1Frazionemassivaedensitàdiorganietessutineiratti
Organ/Tissue FrBM Density[kg/cm3]
Liver 0.0366 0.0001
Brain 0.0057 0.001035
Heart 0.0033 0.00103
Lungs 0.0050 0.0015
Skin 0.1903 0.0013
Adipose 0.06 0.000916
Bone 0.05 0.0016
Muscle 0.4043 0.00141
Spleen 0.002 0.001054
GastroIntestinaltract 0.0248 0.00104
Kidneys 0.0073 0.00105
Ilvaloredella frazionemassivadeltrattogastro intestinaleèstatomediatotra ivalori
propostidagli studidiDelpetal. (1991),PeterseBoyd(1966)eStottetal. (1983).La
densitàdegliorganièassuntalastessadegliumani,inaccordoconBrownetal.(1997).Il
plasma, invece, costituente liquido del sangue nel quale si trova il farmaco iniettato,
costituisce il 65% del volume totale di sangue nei ratti che è pari al 52% del peso
dell’animale.
Perdescrivereloscambiotraicompartimentisonostatiintrodottiunaseriediparametri
chetengonocontodeimeccanismiinterni.Inprimis,fuplasmaefubraincherappresentanola

Modellofarmacocineticodellamorfinaneiratti
33
frazionedifarmacoliberapresentenelplasmaenelcervello,cioènonlegataalleproteine
presenti al loro interno. È questa, di fatto, la porzione di farmaco che può essere
scambiatatraicompartimenti,inquantosololemolecoleliberepossonofluiretraivari
organietessuti,perpoiagireedeffettuare lapropriaazioneterapeutica.Essivalgono
rispettivamente0.66e0.45(Hammarlund-Udenaesetal.,2008).Questidueparametri
sono quelli assegnati nel modello tricompartimentale. Restano quindi sei parametri
incogniti, che sono i coefficienti di scambio tra i compartimenti. k10 rappresenta la
costante di eliminazione della morfina dal compartimento centrale. Cercando una
corrispondenzaa livello fisiologico,questa via rappresenta tutte le viedi eliminazione
dellamorfinadalcorpo,checomevistoavvieneprincipalmenteperviaepatica.k12ek21
identificano i coefficientidi trasferimentodimassa tra il compartimentocentraleegli
organipocoperfusieviceversa.
Undiscorsopiù dettagliato va fatto per i coefficienti di scambio tra il compartimento
centraleeilcompartimentocervello.QuestisonoPactiveIN,PactePdiff.PactiveINePactsonoi
duecoefficientiditrasportoattivo,rispettivamenteiningressoeinuscita,chedescrivono
ilpassaggioattraversolaBEEdellamorfinamediantedeicarrier.Pdiff,invece,rappresenta
ilcoefficientedidiffusionepassivadellamorfinanelcervello.Adifferenzadelloscambio
tra compartimento centrale e organi poco perfusi, descritto solo due flussi, uno in
ingresso e uno in uscita dal compartimento centrale, per descrivere lo scambio tra
compartimentocentraleecervellosièoptatoperl’utilizzoditreflussiinmododarestare
ilpiùfedelipossibilealrealemeccanismodiscambio,inparticolaresdoppiandoilflusso
iningressoinunflussolegatoalladiffusionedelfarmacodauncompartimentoall’altroe
inunolegatoaltrasportoattivo,cioèall’attivitàdeitransporterdelfarmaco.
Nellaseguentetabella2.2sonoriassuntii12parametricoinvoltinelmodello.
Tabella2.2Parametrichecompaiononelmodellotricompartimentaledeiratti.
Symbol Units Description TypeV1 cm3 VolumeofCentralcompartment IndividualizedV2 cm3 VolumeofPoorlyperfusedorgans
compartmentIndividualized
VBT cm3 Volumeofbraintissuecompartment IndividualizedS cm2/gbrain Surfaceofbrainvessels Individualized

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
34
fuplasma - Fractionoffreedruginplasma Assignedfubrain - Fractionoffreedruginbrain Assignedk10 min-1 ConstantofeliminationofCentral
compartmentDegreeoffreedom
k12 min-1 MasstransfercoefficientfromcentralcompartmenttoPoorlyperfuseorgans
Degreeoffreedom
k21 min-1 MasstransfercoefficientfromPoorlyperfuseorganstocentralcompartment
Degreeoffreedom
Pdiff cm/s Diffusioncoefficientfromcentralcompartmenttobraintissue
compartment
Degreeoffreedom
Pact cm/s Effluxcoefficientfrombraintissuecompartmenttocentralcompartment
Degreeoffreedom
PactiveIN cm/s Influxcoefficientfromcentralcompartmenttobraintissue
Degreeoffreedom
Di seguito sono riportate le equazioni coinvolte nel modello. Come appena detto, le
equazioni utilizzate inquestomodello sono tre. Si trattadi equazioni differenziali che
esprimono la concentrazione del farmaco all’interno di ciascun compartimento in
funzionedeltempo,tenendoinconsiderazioneiflussiiningressoeinuscitadaognunodi
essi.
1 3 31 210 12 1 21 2
1 1 1 1 1
1
1
- ( ) - ( - )
-
plasma brain act brainplasma diff
activeIN
C fu C fu P S C fudC VIR k k fu C k C P Sdt V V V V V
CP SV
× × × × ×= + × × + × × × × + +
× × (2)
2 112 1 21 2
2
( - )plasmadC V k fu C k Cdt V
= × × × × (3)
3 3 11 3 ( - ) - plasma brain brain activeIN
diff actBT BT BT BT
fudC C fu fu P S CP S C P S Cdt V V V V
× × ×= × × × × × × + (4)
L’equazione (2) esprime la concentrazione di morfina all’interno del compartimento
centraleC1neltempo.IltermineIRrappresentaladoseinng/mininiettataendovenanel

Modellofarmacocineticodellamorfinaneiratti
35
sanguedelratto,specificaperognicasostudioesaminato.Talesomministrazionenonè
considerataistantanea,mahauntempodirilasciototaledicirca2min,asecondadel
caso. Per questo motivo il suo valore è tenuto costante fino al termine del rilascio,
dopodiché si azzera, arrestando così il suo contributo. I segni dei diversi contributi
seguono la convenzione positivi se rappresentano flussi entranti, negativi se uscenti.
L’equazione(3)rappresentalaconcentrazionedimorfinanelcompartimentodegliorgani
edeitessutipocoperfusiC2neltempo,mentrela(4)rappresentalaconcentrazionedi
morfinanelcompartimentocervelloC3neltempo.
Datochel’obiettivodelsistemadifferenzialediequazionièquellodiprevedereilprofilo
di concentrazione dimorfina nel tempo all’interno del compartimento centrale e del
cervellodeiratti,sièapplicatotalesistemaadiversistudipresentiinletteraturainmodo
dariprodurreinmanierafedeleidatidelleconcentrazioniraccoltiinesperimentisuiratti
presenti in letteratura.Considerandoche iparametri individualizzatiequelli assegnati
sonodefiniti,sideveandareadagiresuigradidilibertàdelsistema,chesono,comegià
detto, i 6 parametri incogniti. L’individuazione del valore di questi parametri è stata
effettuataattraversounaregressionenonlineare,andandoaminimizzareladifferenza
tra i valoridi concentrazionedimorfina fornitidai casi studioe i corrispondentivalori
previstidalmodello.Diseguitoèriportatalafunzioneobiettivocheèstataminimizzata,
alfinedivalutareigradidilibertà:
exp model exp model
1
(| | | max( ) max( ) ||log |N
i i i iobji
C C C CfN=
- + -=å (5)
dove:
§ Nèilnumerodidatisperimentaliadisposizioneperlamorfina;
§ Ciexpidentificalaconcentrazionedellamorfinamisuratasperimentalmente;
§ Cimodelsiriferisceallaconcentrazionedellamorfinaprevistadalmodelloall’istante
i-esimoallaqualeèavvenutoilprelievodalpaziente.
Inparticolare,sièvolutorafforzarelafunzioneobiettivoimponendoanchediminimizzare
ladifferenzatralaconcentrazionedimorfinasperimentaleequelladatadalmodellonel

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
36
puntoincuiquestaèmassima, inmododaimporreunvincolosulvaloremassimodel
modello.
Comeèintuitivo,affinchél’ottimizzazioneelaconseguenteindividuazionedeivaloridei
parametri incogniti avvengano, è indispensabile ricorrere a opportuni valori di primo
tentativo da assegnare a tali parametri. È bene sottolineare chemolto spesso questi
parametrinonhannounveroepropriosignificatofisiologico,comeaccadeinveceperi
parametri individualizzati e assegnati. Il valore trovato a seguito della regressione ha,
dunque,unsignificatoprettamentematematico,edèingradodidescrivereinchemisura
avvenga il trasportodellamorfina tra i compartimenti, senzaperòessereassociatoad
alcunacaratteristicadelcorpodeiratti.Siècercatodiprocedereconuncertocriterio
nell’assegnazionedelvalorediprimotentativodeigradidilibertàdelsistema.Comevalori
dipartenzadeicoefficientidiscambiotracompartimentocentraleeorganietessutipoco
perfusik12ek21edelcoefficientedieliminazionedalcompartimentocentralek10sono
stati scelti gli stessi valori ottenuti da Hasegawa (2010) nel suo modello
bicompartimentale che descrive proprio lo scambio tra questi due compartimenti a
seguitodiinfusioneendovenosadimorfinaneiratti, incuisonoutilizzati,appunto,tali
parametri. Per quanto riguarda i coefficienti legati allo scambio tra compartimento
centraleecervelloèbeneeffettuareundiscorsopiùspecifico.Innanzitutto,tuttietrei
coefficientiimpiegatinelladescrizionediquestoscambiosidevonoricondurrealconcetto
di permeabilità della barriera ematoencefalica. A tal proposito viene introdotta la
definizionedipermeabilitàapparenteespressaincm/s,come:
/app
brain
dQ dtPC S m
=× ×
(6)
incui:
§ "#"$ è il flusso di farmaco trasportato dal compartimento donatore al ricevente,
espressoin%&';
§ 𝐶èlaconcentrazioneinizialedifarmaconelcompartimentodonatorein%&)*;
§ 𝑆èlasuperficiespecificadelcervellodeiratti,cioèlasuperficiediscambio;

Modellofarmacocineticodellamorfinaneiratti
37
§ 𝑚-./0%èlamassadelcervellodeiratti.
Daquinederivachelapermeabilitàapparentepuòesserescompostainduecontributi,
unopassivoel’altroattivo:
app diff activeP C P C P C× » × + × (7)
dove, in realtà, sia il termine di trasporto diffusivo che quello di trasporto attivo
prevedonoilflussoinentrambeledirezioni.Iltrasportopassivoèindicatodalcoefficiente
didiffusionelegatoalgradientediconcentrazione,mentreiterminiditrasportoattivo
sonoindipendentil’unodall’altroeperciòsihauncoefficienteperciascunadirezionedel
flusso.Quindilapermeabilitàapparentetotale,complessivadeiflussiiningressoeuscita
dallaBEE,diventa:
( ) ( )app plasma brain diff plasma brain activeIN plasma act brainP C C P C C P C P C× - » × - + × - × (8)
Comevalorediprimotentativopericoefficientidipermeabilitàpassivaeattiva(Pdiff,Pact
ePactiveIN)sièsceltodiutilizzareivaloriricavatisperimentalmentedaBalletal.(2012).Il
metodopiùcomunetrovatoinletteraturapermisurareperviasperimentaleicoefficienti
di permeabilità della barriera ematoencefalica rispetto ad un farmaco è attraverso
esperimenti in vitro, sfruttando una coltura di cellule Caco-2 che hanno un
comportamentoassimilabileallaBEE.LecelluleCaco-2sonocelluleepitelialichederivano
dall’intestino umano. Queste cellule formano unamembrana che, come ogni tessuto
epiteliale,haunlatocompostodacelluleapicali,rivolteversol’internodeivasisanguigni,
eunlatodicellulebasalirivolteversol’ambienteprotettodallamembrana,cioèitessuti
del cervello nel caso della BEE. In più la membrana di cellule Caco-2 è ricca di P-
glicoproteina,ritenutoilprincipaleresponsabiledeltrasportoattivodimorfinainuscita
dalcervello.Lemisuresperimentalisonocondottesusupportipermeabilidettitranswells,
ilcuischemaèillustratoinfigura2.2.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
38
Figura 2.2 Schema rappresentativo dei supporti permeabili transwells adottati per misuraresperimentalmenteilflussodifarmacoattraversolamembranaendotelialeCACO2.
Al finedivalutare il coefficientedidiffusione,un inibitorediP-glicoproteina (comead
esempioilVerapamil,principioattivoperiltrattamentodell’ipertensione)èintrodottosu
entrambi i lati della membrana Caco-2. In questo modo, eliminando il principale
responsabiledeltrasportoattivodimorfina,siècerticheilflussomisuratoèdovutoquasi
esclusivamente alla diffusione del farmaco attraverso la barriera. Il flusso legato al
trasportoattivoèricavatoperdifferenzatrailflussocheavvienesenzainibitoriequello
coninibitori,assumendocheilflussodiffusivorestilostessoinentrambiicasi.Poichéil
trasporto attivo avvienemediante carrier (P-gp) che fungono da trasportatori a cui si
leganolemolecoledelfarmaco,talefenomenopotrebbeesseredescrittoattraversola
cineticadiMichaelis-Menten.Taleapproccioèstatosperimentatodamoltistudiosinel
campodell’analisideimeccanismiditrasportodeifarmaciattraversomembrana(Tranet
al., 2005), ma non si trovano in letteratura casi studio sulla morfina. La cinetica di
Michaelis-Mentenèlaseguente:11 21
0 1 0rl
k kMC AkT C T T C¾¾¾® ¾¾¾®¬¾¾¾+ + (9)
incui,nelcasodiefflussodalcervello:
• T0rappresentailtransporterlibero;
• CMCrappresentalaconcentrazionedifarmacosullatoapicaledellamembrana;
• T1èiltransporterlegatoalfarmaco;
• CAèilfarmacodopoaversuperatolamembrana.

Modellofarmacocineticodellamorfinaneiratti
39
InquestostudiononsièriuscitoacorrelareiltrasportoattivoallacineticadiMichaelis-
Menten.Ciòpotrebbeessereunobiettivo futuro, conuno studiopiùapprofondito su
questo argomento. Per il momento si è preferito proseguire trovando il valore dei
coefficientiditrasportoattivocosìcomepresentatinelleequazioni(2-4).Nellatabella2.3
sonoillustratiivaloridiprimotentativoassegnatiaciascunparametro.
Tabella 2.3 valori di primo tentativo assegnati a ciascun parametro del modellotricompartimentale.
Parameters Lowdose
k10 0.047min-1
k12 0.022min-1
k21 0.13min-1
Pdiff 2.25 ּ◌10-6cm/s
Pact 1.5 ּ◌10-6cm/s
PactiveIN 0.1 ּ◌10-6cm/s
LaregressionelinearedelsistemaèstataeffettuatasuMatlab,attraversounmetododi
ottimizzazionenonvincolatamediantelafunzionefminsearch.Qualoraivaloriottenutia
seguitodell’ottimizzazionenonsianofisicamenteaccettabili (e.g.valorinegativi),viene
effettuataun’ottimizzazionevincolatasututtiiparametrimediantelafunzionefmincon
inmododariportarlituttiquantiadunvalorefisicamenteconsistente.
Icasistudioesaminatiperlacostruzioneeconvalidadelmodellotricompartimentaleper
i ratti sonosette,e i risultatiottenuti sarannodiscussipiùnello specificoneiprossimi
paragrafi.Nell’effettuarel’analisidiquesticasisiènotatochenontuttirispondevanoallo
stessomodounavoltaeseguital’ottimizzazionesuuninsiemedidati.Nonsièriusciti,
dunqueaconvalidareununicomodellopertuttiquantiicasidatal’elevatadifferenzatra
alcunidiquesti,riconducibilealladifferenzaditrattamentofattaperciascungruppodi
ratti.Infatti,ledosisomministrateaivarigruppidirattisonomoltodiverse.Perquesto
motivosièoptatopersuddividereicasistudioinquattrocategorie:

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
40
1. Infusione intravenosa tramite bolo di basse dosi di morfina (0.44÷2.25
mgmorfina/kgratto);
2. Infusione intravenosa tramite bolo di medie dosi di morfina (2.5÷6
mgmorfina/kgratto);
3. Infusioneintravenosatramitebolodialtedosidimorfina(10mgmorfina/kgratto);
4. Infusione intravenosa continua: rispetto al bolo, che è un’infusione quasi
istantanea, nell’infusione intravenosa continua la morfina viene rilasciata
gradualmenteinuncertoarcotemporale.
Gli intervalli delle dosi dimorfina nelle infusioni intravenose sonoda intendere come
valori indicativi, in quanto semplicemente legati alle dosi dei casi studio presi in
considerazione. In futuro si potranno stilare degli intervalli di dosi somministrate più
esattinelcasoincuisiriuscisseroatrovarenuovidatisperimentalisuiratti.Sitengaa
mentecheogniqualvoltavengafattoriferimentoalledosisomministrateneiratti,siparla
didosispecifiche,ecioèngdimorfinaperkgdiratto.
Ivaloridiprimotentativoassegnatiaiparametrisonoglistessiperciascunacategoria,ei
valorideiparametriregreditisonoespostiintabella2.4.
Tabella2.4Valorideiparametridelmodellotricompartimentaleottimizzatiperciascunatipologiadisomministrazionedellamorfina.
Parameters Lowdose Mediumdose Highdose Continuousinfusion
k10 0.28989 0.19233 0.130539 0.53956929
k12 6.0117 5.1113 30.0888197 2.85771958
k21 0.38208 0.48253 4.77426552 0.16203138 ּ◌10-7
Pdiff 0.0018972 0.00017698 0.00044879 2.9624
Pact 0.0067655 0.0018446 0.00088022 0.00086999
PactiveIN 2.13 ּ◌10-5 4.19 ּ◌10-5 5.9586 ּ◌
10-7
3.7231 ּ◌10-5
Ilmodellopersomministrazioneintravenosatramiteboloabassedosièstatoottimizzato
conidatisperimentalidellostudiodiPlompetal.(1981)condosedimorfinaparia0.44

Modellofarmacocineticodellamorfinaneiratti
41
mg/kg e convalidato con le concentrazioni sperimentali ottenute sempre dallo stesso
studio,macondoseparia1.04mg/kg.Analogamente, iparametridelmodelloadosi
medieèstatoottenutodall’ottimizzazionesuidatisperimentalidiDahlstrometal.(1975)
condosedimorfinaparia2.5mg/kgeconvalidatosuunaltroinsiemedidaticontenuto
nellostudiodiPlompcodose2.25mg/kgesuunocontenutoinKissinetal.(1991)avente
dosedimorfinainiettataparia6mg/kg. Infine,per ilmodelloperaltedosidimorfina
somministrate endovena tramite bolo e per quello per morfina iniettata mediante
infusionecontinuanonèstataeffettuatalaconvalidapermancanzadidatisperimentali,
eirisultatisonostatiottenutidall’ottimizzazionesuidatiderivatidaglistudidiBourasset
etal.(2006)edaunaltroinsiemedidatidiKissinrispettivamente.
2.3 ModelloPBPK
Come anticipato nel paragrafo introduttivo di questo capitolo, una volta costruito e
convalidatoilmodellotricompartimentale,sièvolutoapprofondirelostudioandandoa
complicare il modello farmacocinetico e di conseguenza il sistema di equazioni, con
l’obiettivodivalutaresesiapossibileottenereunlivellodiprecisionepiùelevatonella
descrizionedella farmacocineticadellamorfinanel cervellodei ratti.A tale scopo si è
costruitoilmodelloPBPK,chenelcasospecificoècompostoda7compartimenti:
1. Ilcompartimentoplasma,incuientraladosedimorfinainiettataechescambia
contuttiicompartimentidistribuendoilfarmacoatuttoilcorpo;
2. Il compartimento dei tessuti poco perfusi, che, come nel caso del modello
tricompartimentale, raggruppa: polmoni, ossa, tessuto adiposo, pelle e tessuto
muscolare;
3. Ilcompartimentodegliorganimoltoperfusicheinclude:cuore,milzaereni;
4. Il compartimentoGICS (sistema circolatorio gastro intestinale), compartimento
introdottodaDiMuriaetal. (2010)edutilizzatoanchedaAbbiatietal. (2015).
Questa regione fisiologica raggruppa i vasi sanguigni dall’intestino al fegato.
Stomaco e intestino sono stati trascurati, poiché questo modello prevede
un’iniezione endovenosa, quindi la concentrazione in questi organi è del tutto

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
42
trascurabile.Questaapprossimazionenonsarebbevalidanelcasodiassunzione
delfarmacoperviaorale;
5. Ilcompartimentodellavascolarizzazionedelcervello(brainvasculature),cioèdei
vasisanguignicheirroranoilcervello.Nonèaltrochelaporzionediplasmache
raggiunge il cervello. La costruzionediquestocompartimentoè stata fattaper
trattareinmanierapiùcomodailpassaggiodelfarmacoattraversolaBEE;
6. Il compartimento cervello (brain tissue), in cui èmisurata la concentrazionedi
farmacocheattraversalaBEE.
7. Ilcompartimentodelfegato,importantedatoilgrandecontributodieliminazione
delmetabolismoepaticodellamorfina.
Diseguito,infigura2.3,èrappresentatoloschemadelmodelloPBPK.
Figura2.3SchemadelmodelloPBPK.Le frecce indicano ladirezionedei flussidi farmaco tra icompartimenti.
Il sistema di equazioni differenziali utilizzato per descrivere la farmacocinetica della
morfinaèformatoda7equazioni,unaperognicompartimento,edèilseguente:

Modellofarmacocineticodellamorfinaneiratti
43
_ _11 2_ 1 12 13 2 21
1 1 1 1 1
33 31 1
1 1 1
( - ) - ( )
-
P GICS P LBVP BV plasma plasma
lp pl
kidneysHVL K
lp
Q QC CdC VIR Q C k fu k fu C kdt V V V j V j V
QQ VC C k C effj V V V
= + × × × + × + + + × × +× ×
+ × + × × × ××
(10)
2 112 1 21 2
2
-plasmadC V k fu C k Cdt V
= × × × × (11)
3 113 1 31 3
3
-plasmadC V k fu C k Cdt V
= × × × × (12)
1_
( - )( - ) -
-
diff BV plasma BT brainBV BV activeOUT BT brainP BV
BV BV BV
activeIN BV plasma
BV
P S C fu C fudC C C P S C fuQdt V V VP S C fu
V
× × × × × × ×= × + +
× × ×(13)
( - )- diff BV plasma BT brain activeIN BV plasmaactiveOUT BT brainBT
BT BT BT
P S C fu C fu P S C fuP S C fudCdt V V V
× × × × × × ×× × ×= + (14)
_ _1 - - P GICS P GICSGICS lil GICS
GICSGICS lp GICS pl GICS
Q QdC CL CC Cdt V j V j V
×= × ×
× × (15)
_ _ _1 - - P L P GICS P GICS H HV LL
GICS Lpl L pl L L lp lp L
Q Q Q eff Q CdC C C Cdt j V j V V j j V
× ×= × + × ×
× × × × (16)
Questa volta i parametri coinvolti nel modello sono 27, di cui 13 individualizzati, 2
assegnati,e12gradidi libertàdelmodello. Iparametri individualizzati sono,comegià
detto,specificiperciascungruppodirattiesaminati.7sonoivolumideicompartimenti
datidaivolumidegliorganietessutichelicompongono,unoèlasuperficiediscambio
delcervellomentreglialtrisonoleportatedisangue:

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
44
• QP_BV,laportatasanguignachevadalplasmaalcervelloeviceversa,lamaggior
partedelplasmacheraggiungeilcervelloèportatodall’arteriacarotide,lavena
giugulare, invece, è adibita a portare il plasma dal cervello al compartimento
plasma;
• QP_L,portatadisanguecheraggiungeilfegatoattraversol’arteriaepatica;
• QHV,laportatadisangueassociataallavenaepatica;
• QP_GICS, che rappresenta la portata di sangue associata al sistema circolatorio
gastrointestinale;
• Qkidneys,laportatadiplasmacheraggiungeireni.
Questiparametri,chesonoportatedisangue,sonoreperibiliinletteraturaeillorovalore
è stato considerato costante poiché non esistono termini che ne consentono
l’individualizzazioneperciascunindividuo.Inletteraturaquestidatisonoespressituttiin
funzionedellagittatacardiaca.Poichésifasempreriferimentoalplasma,enonalsangue,
questeportatevannopoimoltiplicateperlafrazionediplasmapresentenelsangue.Di
seguitosonoriportateleespressioniperciascunaportata,incuiCOrappresentalaportata
cardiacamentreXplasmaèlafrazionediplasmachecomponeilsangue.Ciascunaportataè
espressainmL/min.
0.02P BV plasmaQ CO X- = × × (17)
0.024P L plasmaQ CO X- = × × (18)
0.174HV plasmaQ CO X= × × (19)
0.151P GICS plasmaQ CO X- = × × (20)
0.141kidneys plasmaQ CO X= × × (21)
I2parametriassegnatisonolefrazionidifarmacononlegatealleproteinenelplasmae
nel cervello, e quindi disponibili a svolgere il loro ruolo terapeutico. I 12 parametri

Modellofarmacocineticodellamorfinaneiratti
45
incogniti, infine,sonotutti icoefficienticheregolano loscambiotra icompartimenti. I
parametri k12 e k21 identificano i coefficienti di trasferimento di massa tra il
compartimento plasma e il compartimento dei tessuti poco perfusi dal sangue, e
analogamentek13ek31rappresentanoloscambiotragliorganimoltoperfusidasanguee
plasma.Iparametrijplejlpsono,rispettivamente,icoefficientidipartizioneplasma-fegato
efegato-plasma.EffKèunparametrochemoltiplicalaportatadisanguecheraggiungei
renieneidentifical’efficienza.Essoècoinvoltonell’eliminazionedellamorfinaattraverso
l’urina,elaquantitàdifarmacoeliminatadipendedalgradodifunzionamentodeireni.
EffH,, invece, identifica l’efficienza del fegato, ossia esso definisce la percentuale di
morfinachevienemetabolizzataequindieliminataperviaepatica.CLlil,infine,identifica
un’altraviadieliminazionedellamorfinadalcompartimentocheracchiudestomacoe
intestinocheavvieneattraversolefeci,edèespressointerminidiportatavolumetrica.
Tuttiiparametriutilizzatinelmodellosonoriassuntiintabella2.5.
Tabella2.5ParametridelmodelloPBPKindividualizzati,assegnatieincogniti.
Symbol Units Description TypeV1 cm3 VolumeofPlasmacompartment IndividualizedV2 cm3 VolumeofPoorlyperfucedorgans
compartmentIndividualized
V3 cm3 VolumeofHighlyperfucedorganscompartment
Individualized
VBV cm3 Volumeofbrainvasculaturecompartment
Individualized
VBT cm3 Volumeofbraintissuecompartment IndividualizedVGICS cm3 VolumeofGICScompartment IndividualizedVL cm3 VolumeofLivercompartment Individualized
QP_BV mL/min Volumetricfluxofcardiacoutputtobrain
Individualized
QP_L mL/min Volumetricfluxofhepaticartery IndividualizedQHV mL/min Volumetricfluxofhepaticvein IndividualizedQGICS mL/min Volumetricfluxofcardiacoutputto
GICSIndividualized
Qkidneys mL/min Volumetricfluxofcardiacoutputtokidneys
Individualized
S cm2 Surfaceofbrainvessels Assignedfuplasma - Fractionoffreedruginplasma Assignedfubrain - Fractionoffreedruginbrain Assignedjpl - Plasma-liverpartitioncoefficient Degreeoffreedom

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
46
jlp - Liver-plasmapartitioncoefficient DegreeoffreedomeffH - Efficiencyofeliminationofliver DegreeoffreedomeffK - Efficiencyofeliminationofkidneys DegreeoffreedomCLlil min-1 ConstantofeliminationofGICS
compartmentDegreeoffreedom
k12 min-1 MasstransfercoefficientfromcentralcompartmenttoPoorlyperfused
organs
Degreeoffreedom
k21 min-1 MasstransfercoefficientfromPoorlyperfusedorganstocentral
compartment
Degreeoffreedom
k13 min-1 MasstransfercoefficientfromcentralcompartmenttoHighlyperfused
organs
Degreeoffreedom
k31 min-1 MasstransfercoefficientfromHighlyperfusedorganstocentral
compartment
Degreeoffreedom
Pdiff cm/s Diffusioncoefficientfromcentralcompartmenttobraintissue
compartment
Degreeoffreedom
Pact cm/s Effluxcoefficientfrombraintissuecompartmenttocentral
compartment
Degreeoffreedom
PactiveIN cm/s Influxcoefficientfromcentralcompartmenttobraintissue
Degreeoffreedom
Come valori di primo tentativo dei parametri in comune con il modello
tricompartimentale sono stati utilizzati proprio i valori identificati a seguito
dell’ottimizzazione del modello tricompartimentale. Per quanto riguarda gli altri
parametri,invece,sisonsceltideivaloridiprimotentativochefosseroinaccordoconciò
cherappresentanoequindirealmenteplausibili.Pertalemotivo,aicoefficientik13ek31
sonostatiassegnatideivaloridellostessoordinedigrandezzadik12ek21.Alleefficienze
eaicoefficientidipartizionetraplasmaefegatosonostatiassegnativaloricompresitra
0e1.Laregressioneeconvalidadellequattrocategoriedelmodelloèstataeffettuata
medianteottimizzazionevincolata,conglistessiinsiemididatiutilizzatiperlaregressione
econvalidadelmodellotricompartimentale.Ivalorideiparametriottenutisonoriportati
intabella2.6.

Modellofarmacocineticodellamorfinaneiratti
47
Tabella 2.6 Valori dei parametri del modello PBPK ottimizzati per ciascuna tipologia disomministrazionedellamorfina.
Parameters Lowdose Mediumdose Highdose Continuous
infusion
k12 0.1105 0.1357 0.1002 0.2170
k21 2.2506 1.3025 3.049 0.6035
k13 90.2114 53.6867 52.517 3.6644
k31 0.2946 0.3951 0.7464 1.2462
jpl 0.0004 0.0414 0.02478 0.0697
jlp 3.34 ּ◌10-5 0.0406 0.0249 0.0531
effH 10 ּ◌10-5 0.0524 0.0305 0.0239
effK 0.0087 0.0092 0.0043 0.0123
CLlil 0.0121 0.0103 0.0212 0.0078
Pdiff 0.0012 0.0001 0.0003 0.0001
Pact 0.0028 0.0017 0.0011 0.0024
PactiveIN 2 ּ◌10-5 7 ּ◌10-5 0.0001 2.89 ּ◌10-12
2.4 Risultatieconvalidamodellotricompartimentaleperinfusioneviabolodibassedosi
Qui di seguito sono descritti i risultati del modello a tre compartimenti con
somministrazione intravenosa tramite bolo di basse dosi di morfina discusso in
precedenza,andandoadosservareigraficiottenutiperciascunostudioeconfrontandoli
conidatisperimentali.Irisultatidiinteresseperquestolavoroditesisonoquelliottenuti
per il compartimento centrale, che corrispondono alla concentrazione di morfina nel
plasma,e,inmodoparticolare,perilcompartimentocervello.Ciascungraficocontienein
ascissailtempoespressoinminutichevadazerofinoall’ultimoistanteincuisonostate
raccolte lemisure sperimentali. Il tempo zero corrisponde all’istante in cui avviene la

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
48
somministrazione. In ordinata si ha la concentrazione di morfina nel compartimento
centraleocervelloespressainng/mL.
L’insiemedidatisperimentalisucuièstataeffettuatalaregressioneperilmodelloper
basse dosi dimorfina iniettate endovena tramite bolo, cioè il caso studio 1, è quello
presentatodaPlompetal.(1981).Inquestoesperimentounasingoladosedimorfinapari
a0.44mg/kgratto è stata iniettata direttamente nel sistema circolatorio dei ratti, e di
conseguenzasonostatieffettuatiprelievinegliintervalliditemposuccessiviall’iniezione.
Perogniprelievosonocoinvoltigruppicompostida6a12ratti,aventipesomedioparia
0.22 kg. I risultati sperimentali presentati sono lamedia ± S.Q.M. (Scarto Quadratico
Medio)deivaloriottenutiperciascungruppo.Ènecessariousaregruppidirattiperchéla
procedurapermisurarelaconcentrazionedimorfinanelcervellodell’animalerichiedela
suasoppressione:infatti,permisurarelaquantitàdimorfinanelcervello,l’organoviene
rimossodalcranio,omogeneizzatoecentrifugato.Èdaquestidatisperimentalicheivalori
finalideiparametrichecaratterizzanoilmodellosonostatiottenuti. Infigura2.4sono
illustratiigraficiottenutidalmodellochedescrivonol’andamentodellamorfina.
Figura2.4Rappresentazionedelmodellotricompartimentaleper infusioneendovenosadi0.44mgmorfina/kgrattotramiteboloneiratti.IrombiinrossoindicanolemisuresperimentalidiPlompetal. (1981), la linea blu è il risultato del modello. A sinistra è rappresentato il profilo diconcentrazionedimorfinanelcompartimentocentrale,adestra ilprofilodi concentrazionedimorfinanelcompartimentocervello.
Perconvalidareilmodellocheèrisultatodall’analisidelcasostudio1,sonostatiutilizzati
duealtriinsiemididatipresentatisemprenellostessostudioeffettuatodaPlompetal.
(1981) indicati in tabella2.7,andandoa confrontare il risultatodelmodello con idati
sperimentali.

Modellofarmacocineticodellamorfinaneiratti
49
Tabella2.7Casi studioutilizzatiper la convalidadelmodello tricompartimentaleper infusioneendovenosaviabolodibassedosidimorfina.
Injection Dose
(ngmorphine/kgrat)
Ratmass(kg) Rats
number
Plompetal.(1981)–
casostudio2
viabolo 1.04 0.22 6-12
Plompetal.(1981)–
casostudio3
viabolo 2.25 0.22 6-12
Piùavantiirisultatidelmodelloperivaricasistudioverrannoconfrontatitraloro.
2.5 Risultatieconvalidamodellotricompartimentaleperinfusioneviabolodimediedosi
Qui di seguito sono presentati i risultati del modello a tre compartimenti con
somministrazione intravenosa tramite bolo di medie dosi di morfina discusso in
precedenza,andandoadosservareigraficiottenutiperciascunodeitrestudianalizzatie
confrontandoliconidatisperimentali
Per trovare il valore dei gradi di libertà del modello in grado di prevedere la
concentrazionenel cervellonei ratti nel casodi infusioneendovenosa tramitebolodi
mediedosidimorfina,sonostatiutilizzatiidatiraccoltidagliesperimentisuiratticondotti
daDahlstrometal.(1975).Inquestostudiosonostatoanalizzatigruppidi5-10ratticon
massa corporea media di 0.17 kg, a cui è stata somministrata una dose di 2.5
mgmorfina/kgratto.Diseguito,infigura2.5,sonopresentatiirisultatidelmodellosiaperil
compartimentocentralecheperilcompartimentocervello.Anchequiidatisperimentali
delcervelloderivanodall’omogeneizzazioneecentrifugazionedell’organo,dacuièstata
ricavatapoilaconcentrazionedimorfina.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
50
Figura 2.5 Rappresentazione delmodello tricompartimentale per infusione endovenosa di2.5mgmorfina/kgrattotramiteboloneiratti.IrombiinrossoindicanolemisuresperimentalidiDahlstromet al. (1975), la linea blu è il risultato del modello. A sinistra è rappresentato il profilo diconcentrazionedimorfinanelcompartimentocentrale,adestra ilprofilodi concentrazionedimorfinanelcompartimentocervello.
Ilcasostudio2permediedosidimorfinasfruttatoperconfermarelavaliditàdelmodello
ottenutoèdescrittonellatabella2.8.
Tabella2.8Casostudioutilizzatoperlaconvalidadelmodellotricompartimentaleperinfusioneendovenosaviabolodimediedosidimorfina.
Injection Dose
(ngmorphine/kgrat)
Ratmass(kg) Rats
number
Kissinetal.(1991) viabolo 6 0.225–0.275 7
Ancheinquestocaso,piùavantiirisultativerrannoconfrontatitraloro.
2.6 Risultatimodellotricompartimentaleperinfusioneviabolodialtedosi:Bourassetetal.(2006)
In questo paragrafo è illustrato (Figura 2.6) il risultato ottenuto per il modello a tre
compartimenticoniniezioneintravenosatramitebolodialtedosidimorfinadiscussoin
precedenza. Si ricorda che in questa tipologia solo un caso studio è stato analizzato,
attraverso il quale sono stati ottenuti i valori dei parametri del modello tramite
regressione. Non è stato possibile convalidare il modello su altri insiemi di dati.
Nell’esperimento condotto in questo caso studio una dose di morfina pari a 10
mgmorfina/kgratto è stata somministrata a 5 ratti. Nello studio di Bourasset, i dati

Modellofarmacocineticodellamorfinaneiratti
51
sperimentalidelcompartimentobraincorrispondononellospecificoallaconcentrazione
dimorfinamisuratanelliquidoextra-cellulare.Poichéèilliquidochesitrovaaldilàdella
BEE,edoccupalamaggiorpartedelvolumechepuòessereraggiuntodaagentiesternial
cervello, laconcentrazionedellamorfinanel liquidoextra-cellulareèstataconsiderata
comelaconcentrazionetotaledelfarmaconelcompartimentocervello.
Figura 2.6 Rappresentazione del modello tricompartimentale per infusione endovenosa di 10mgmorfina/kgrattotramiteboloneiratti.IrombiinrossoindicanolemisuresperimentalidiBourassetet al. (2006), la linea blu è il risultato del modello. A sinistra è rappresentato il profilo diconcentrazionedimorfinanelcompartimentocentrale,adestra ilprofilodi concentrazionedimorfinanelcompartimentocervello.
2.7 Risultatimodello tricompartimentaleper infusione continua:Kissinetal.(1991)
Diseguitoèillustrato(Figura2.7)ilrisultatoottenutoperilmodelloatrecompartimenti
coniniezioneintravenosacontinuadimorfinadiscussoinprecedenza.Siricordacheper
questa tipologia solo un caso studio è stato analizzato, attraverso il quale sono stati
ottenuti i valori dei parametri delmodello tramite regressione. Non è stato possibile
convalidareilmodellosualtriinsiemididati.Inquestoesperimento,presentatonelcaso
studio3nelparagrafo2.5.3,irattisonostatitrattaticonun’infusionecontinuaparia4
mgmorfina/kgratto/hper8ore.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
52
Figura2.7Rappresentazionedelmodellotricompartimentaleperinfusioneendovenosacontinuadi4mgmorfina/kgratto/h nei ratti. I rombi in rosso indicano lemisure sperimentalidiKissin etal.(1991),lalineabluèilrisultatodelmodello.Asinistraèrappresentatoilprofilodiconcentrazionedi morfina nel compartimento centrale, a destra il profilo di concentrazione di morfina nelcompartimentocervello.
Neiparagrafisuccessiviverrannoillustratiinmanieraanalogaaquantofattosinoadorai
risultatiottenutidalmodelloPBPKa7compartimentisuglistessiinsiemididatideicasi
studiopresentatifinqui.Sarannopresentatiigraficidelprofilodiconcentrazionedella
morfinanelcompartimentoplasmaenelcompartimentocervello.
Diseguitosonoriportatiitrecasistudioanalizzatiperilcasodiinfusioneviabolodibasse
dosidimorfina.
2.8 Risultati e convalidamodello PBPK per infusione via bolo dibassedosi
Infigura2.8sonoraffiguratiigraficidelmodelloottenutidall’analisidellostudiodiPlomp
condoseparia0.44mgmorfina/kgratto.

Modellofarmacocineticodellamorfinaneiratti
53
Figura2.8RappresentazionedelmodelloPBPKperinfusioneendovenosadi0.44mgmorfina/kgrattotramiteboloneiratti.IrombiinrossoindicanolemisuresperimentalidiPlompetal.(1981),lalineabluèilrisultatodelmodello.Asinistraèrappresentatoilprofilodiconcentrazionedimorfinanelcompartimentocentrale,adestrailprofilodiconcentrazionedimorfinanelcompartimentocervello.
Irisultatidelmodelloapplicatosucasistudio2e3analogamenteaquantofattoperil
modellotricompartimentalesarannodiscussiinseguito.
2.9 Risultati e convalidamodello PBPK per infusione via bolo dimediedosi
Inquestoparagrafosonopresentatiglistudianalizzatiperilcasodidosimediedimorfina
iniettatetramitebolo.
In figura2.9sipossonoosservare i risultatidelmodelloottenutisull’insiemedidatidi
Dahlstrometal.(1975)siasulplasmachesulcervello.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
54
Figura2.9RappresentazionedelmodelloPBPKper infusioneendovenosadi2.5mgmorfina/kgrattotramiteboloneiratti.IrombiinrossoindicanolemisuresperimentalidiDahlstrometal.(1975),la lineabluè il risultatodelmodello.A sinistraè rappresentato il profilodi concentrazionedimorfina nel compartimento centrale, a destra il profilo di concentrazione di morfina nelcompartimentocervello.
PercasostudiodiKissinetal.(1991)analizzatoperilPBPKsarannodiscussipiùavantisolo
irisultatiottenuti.
2.10 Risultati modello PBPK per infusione via bolo di alte dosi:Bourassetetal.(2006)
Qui,infigura2.10,sonorappresentatiirisultatidelmodelloPBPKperaltedosidimorfina
neiratti.
Figura2.10Rappresentazionedelmodello tricompartimentaleper infusioneendovenosadi10mgmorfina/kgrattotramiteboloneiratti.IrombiinrossoindicanolemisuresperimentalidiBourassetet al. (2006), la linea blu è il risultato del modello. A sinistra è rappresentato il profilo diconcentrazionedimorfinanelcompartimentocentrale,adestra ilprofilodi concentrazionedimorfinanelcompartimentocervello.
2.11 Risultatimodello tricompartimentaleper infusione continua:Kissinetal.(1991)
Infigura2.11sonoriportatiirisultatidelmodelloPBPKperinfusionecontinuadimorfina
ottenutosuidatisperimentalidiKissin.

Modellofarmacocineticodellamorfinaneiratti
55
Figura 2.11 Rappresentazione del modello tricompartimentale per infusione endovenosacontinuadi4mgmorfina/kgratto/hneiratti.IrombiinrossoindicanolemisuresperimentalidiKissinet al. (1991), la linea blu è il risultato del modello. A sinistra è rappresentato il profilo diconcentrazionedimorfinanelcompartimentocentrale,adestra ilprofilodi concentrazionedimorfinanelcompartimentocervello.
2.12 Analisieconfrontodeirisultatideiduemodelli
A primo impatto, osservando l’andamento dei grafici risultanti dai modelli, questi
sembranoquasiuguali.Innanzituttosipossonocondurreconsiderazionicomuniatuttii
risultati.Essendol’iniezionedimorfinanelplasmaviabolo,quindiistantanea,questasi
distribuiscenelplasmamoltorapidamente,nell’arcodipochiminuti(da1a5min).Per
questioni di semplicità, all’interno del modello costruito in questo lavoro di tesi si è
assuntochetaledistribuzioneavvenganeltempocheintercorretrailtempodiiniziodella
somministrazione–tempozero–el’istanteincuièstataregistratalaprimamisurazione
sperimentaledimorfinanelplasmadelratto.Perciò,ilvaloredatodalcontributoIRnelle
equazioni2e14vieneassuntocostanteeparialvaloredelladoseiniettatafinoaltempo
dellaprimamisurasperimentaledimorfinanelplasma,ovenelprimotrattoilmodello
assume un andamento monotonamente crescente fino al raggiungimento del valore
massimodiconcentrazionedimorfinamisurataneiratti.DopodichéiltermineIRviene
posto uguale a zero. A partire da qui si osserva un repentino abbassamento della
concentrazione nel compartimento centrale che corrisponde allo smaltimento della
morfinaneiprimiistantiditemposuccessiviallaprimamisurasperimentale.Colpassare
deltempol’eliminazionerallenta.
Mentre il picco di concentrazione dimorfina nel compartimento centrale o plasma si
registra al temine all’iniezione via bolo, la concentrazionemassima nel cervello viene
raggiuntaconun leggeroritardo.Questoèchiaramentedovutoal fattoche il farmaco

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
56
necessitadi tempoperpassaredalplasmaal cervello.Anchequi la concentrazionedi
morfinasaleneiprimi istantiperpoiscendere lentamenteunavoltaraggiunto ilpicco
massimo.Altrettantoovviaèl’inferioritàdellaconcentrazionemassimadelfarmaconel
cervello rispetto a quella nel plasma, date le difficoltà dei farmaci nel raggiungere
quest’organoampiamentediscussenelprimocapitolo.
UnandamentodeltuttodiversoèquellodelcasostudiodiKissinetal.(1991)condotto
coninfusioneendovenosacontinuadimorfinaneiratti.Lungotuttele8orediinfusione,
infatti, la concentrazione sale fino a stabilizzarsi sul valore massimo raggiunto. I dati
sperimentalisonostatiraccoltisolonell’arcoditempoincuièavvenuta l’infusione.Al
terminedell’infusionelaconcentrazionedimorfinaèdestinataascendere.
Nellatabella2.9sonoriportatiivalorimassimiteoricidellaconcentrazionedimorfinanel
plasmadeirattiperciascunesperimentoesaminatodallaletteratura,ottenutidividendo
la dose dimorfina somministrata per lamassa corporeamoltiplicata per il volume di
plasma.
Tabella 2.9 Valori massimi teorici che possono essere raggiunti dalla morfina all’interno delplasma. * =Valore calcolato su8ore, la duratadell’infusionenell’esperimentodi Kissinetal.(1991).
Theoreticalmaximummorphineplasma
concentration(ng/mL)
Plompetal.(1981)–casostudio1 12535.61
Plompetal.(1981)–casostudio2 29629.63
Plompetal.(1981)–casostudio3 64102.56
Dahlstrometal.(1975) 71225.07
Kissinetal.(1991)–viabolo 170940.17
Bourassetetal.(2006) 284900.28
Kissinetal.(1991)–constantinfusion 911680.91*
Tutti i valoridellaconcentrazionedimorfinanelplasmadi ciascunostudio riportati in
letteraturamostratinellatabella2.10sitrovanoabbondantementealdisottodeivalori
massimiteorici.Perestrarredeicampionidiplasmaconunaconcentrazionevicinatali

Modellofarmacocineticodellamorfinaneiratti
57
valoribisognerebbeeffettuaredeiprelievineiprimissimiistantiaseguitodell’iniezione
nelcasodiinfusioneviabolo,mentrenelcasodiinfusionecontinuatalevaloresipotrebbe
raggiungereinunirrealisticocasoincuilamorfinasiaccumulassenelplasmasenzaalcuna
viad’uscitapertuttoiltempodell’infusione.
Tabella 2.10 Valorimassimi di concentrazione dimorfinamisurati sperimentalmente nei rattiattraversoilprelievodicampionidiplasma.
Maximummorphineplasmaconcentration
uptakenexperimentally(ng/mL)
Plompetal.(1981)–casostudio1 101.95(after5min)
Plompetal.(1981)–casostudio2 205.54(after5min)
Plompetal.(1981)–casostudio3 798.68(after5min)
Dahlstrometal.(1975) 859.408(after2min)
Kissinetal.(1991)–viabolo 2270(after5min)
Bourassetetal.(2006) 3119.33(after5min)
Kissinetal.(1991)–constantinfusion 3485.92(after8h)
È importanteverificare cheanche le concentrazioninel compartimentocentraleper il
modellotricompartimentaleenelplasmaperilmodelloPBPKsianoaldisottodeilimiti
fisiciriportati intabella2.9,equestoèfacilmenteindividuabiledaigrafici.Siriportano
nella tabella 2.11 le concentrazionimassime individuatedalmodello per ciascun caso
studio.
Tabella 2.11 Valorimassimi di concentrazione dimorfinamisurati sperimentalmente nei rattiattraversoilprelievodicampionidiplasma.
Maximummorphineplasma
concentrationmeasuredby
thetricompartimentalmodel
(ng/mL)
Maximummorphine
plasmaconcentration
measuredbythePBPK
model(ng/mL)
Plompetal.(1981)–
casostudio186.961 86.960

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
58
Plompetal.(1981)–
casostudio2205.543 205.542
Plompetal.(1981)–
casostudio3444.685 444.682
Dahlstrometal.(1975) 928.89 919.12
Kissinetal.(1991)–via
bolo
2229.4 2290.1
Bourassetetal.(2006) 4560.5 5484.8
Kissinetal.(1991)–
constantinfusion3520.1 3486.6
Inmanieraanaloga, si possonoosservare in tabella2.12 le concentrazionimassimedi
morfinanelcervelloregistratesperimentalmenteneglistudipresiinconsiderazione,ed
un confronto può essere fatto con le concentrazioni massime individuate dalla
simulazionediciascuncasostudioattraversoiduemodelliutilizzati(Tabella2.13).
Tabella 2.12 Valorimassimi di concentrazione dimorfinamisurati sperimentalmente nei rattiattraversoilprelievodicampionidiplasma.
Maximummorphinebrainconcentration
uptakenexperimentally(ng/mL)
Plompetal.(1981)–casostudio1 15.65(after5min)
Plompetal.(1981)–casostudio2 48.65(after5min)
Plompetal.(1981)–casostudio3 78.51(after5min)
Dahlstrometal.(1975) 84.27(after20min)
Kissinetal.(1991)–viabolo 288(after30min)
Bourassetetal.(2006) 1348.07(after35min)
Kissinetal.(1991)–constantinfusion 333.39(after8h)

Modellofarmacocineticodellamorfinaneiratti
59
Tabella 2.13 Valorimassimi di concentrazione dimorfinamisurati sperimentalmente nei rattiattraversoilprelievodicampionidiplasma.
Maximummorphinebrain
concentrationmeasuredby
thetricompartimentalmodel
(ng/mL)
Maximummorphine
brainconcentration
measuredbythePBPK
model(ng/mL)
Plompetal.(1981)–
casostudio120.9 21.1
Plompetal.(1981)–
casostudio249.4 50.0
Plompetal.(1981)–
casostudio3106.8 108.1
Dahlstrometal.(1975) 90.6 86.2
Kissinetal.(1991)–via
bolo
197.3 208.4
Bourassetetal.(2006) 1279.7 1315.1
Kissinetal.(1991)–
constantinfusion336.4 277.7
Inalcunicasi,nelmodellochesimulagliesperimentidisomministrazionedimorfinavia
boloilpiccodiconcentrazionedimorfinanelcervellorisultaleggermentepiùaltorispetto
aquellomisuratosperimentalmente.Questosispiegacolfattochelemisuresperimentali
avvengonoinunistantearbitrario,chepuòancheprecedereilpiccomassimoraggiunto
dallamorfina nel cervello. In altri casi ilmodello si avvicinamolto al valoremassimo
registratosperimentalmente,senzaperòraggiungerlo.
Al fine di verificare l’accuratezza del modello e poter confrontare tra loro il modello
tricompartimentaleequelloPBPK,sièadottatounindicediperformancenotocomeAUC
(AreaUnderCurve)percentuale:
exp model
exp
| |% 100AUC AUCAUCAUC-
= × (22)

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
60
AUCexp e AUCmodel rappresentano, rispettivamente, l’area sottesa dalle misure
sperimentali e dal modello nel grafico della concentrazione di morfina nel tempo.
Attraversoquest’indicatoresièingradodidirequantoilmodellosiavicinoallemisure
sperimentali. Osservando la formula è facile comprendere che più è basso il valore
dell’AUCpercentuale,minoreèladifferenzatramodellomatematicoedatisperimentali,
ediconseguenzailmodellorisultaesserepiùaccurato.
2.12.1 Analisideirisultatiottenutidalmodellotricompartimentale
Nella seguente tabella 2.14 sono presentate le AUC percentuali dei tre casi studio
esaminatiperlacategoriadisomministrazioneendovenadibassedosidimorfinaviabolo,
ecioèitrestudidiPlompetal.(1981)consomministrazionediunadosemorfinaneiratti
paria0.44mg/kg(casostudio1),unaparia1.04mg/kg(casostudio2)edunaparia2.25
mg/kg (casostudio3).Confrontando leAUCpercentuali risultantidai trecasi studioè
possibileosservarel’affidabilitàdelmodellocostruitosulcasostudio1everificareche
essodescrivainmanierasoddisfacenteanchel’insiemedidatideicasistudio2e3.
Tabella2.14AUCpercentualipericasistudiodelmodellotricompartimentaleperbassedosidimorfinasomministrataendovenaviaboloneiratti.
AUCcentralcompartment(%) AUCbrain(%)
Plompetal.(1981)–caso
studio19.54 23.72
Plompetal.(1981)–caso
studio2
13.49 34.25
Plompetal.(1981)–caso
studio315.25 2.89
In generale, stando a quanto suggerito dalla FDA (Food and Drug Administration), si
ritienecheunmodellosiaaccettabilefinoadun’AUCpercentualeintornoal30%.Sipuò
dunque affermare che in questo caso il modello rispetti i vincoli. Va sottolineata
l’eccellenterispostadelmodellonellarappresentazionedelprofilodiconcentrazionedi

Modellofarmacocineticodellamorfinaneiratti
61
morfina nel cervello ottenuto dai dati ricavati dall’esperimento di Plomp con dose
somministratapiùalta.
Perquantoriguardailmodellotricompartimentaleperlasomministrazioneendovenadi
mediedosidimorfinaviabolo,intabella2.15sipossonoosservareleAUCpercentualidi
ciascuncasostudio.
Tabella2.15AUCpercentualipericasistudiodelmodellotricompartimentalepermediedosidimorfinasomministrataendovenaviaboloneiratti.
AUCcentralcompartment(%) AUCbrain(%)
Dahlstrometal.(1975) 9.3489 13.7732
Kissinetal.(1991)–viabolo 13.3036 51.8248
Èilcasodinotarecheilmodellopuòritenersipressochécorretto,adeccezionedelvalore
dell’AUCpercentualedelcompartimentobrainnelmodellarelostudiodiKissin.Questa
infattiassumeunvaloreparia51.82%,benpiùaltodellimitediaccettabilitàdel30%.
Icasidialtedosidimorfinasomministrateviaboloediinfusionecontinuapossonoessere
commentatiinsieme,inquantoperentrambiunsolocasostudioèstatoesaminato.Per
entrambiilmodellohafornitounarispostaottima,confermatadalleAUCpercentualidei
duecompartimentidiinteressemoltobasse(Tabella2.16e2.17).
Tabella2.16AUCpercentualiper i casi studiodelmodello tricompartimentaleperaltedosidimorfinasomministrataendovenaviaboloneiratti.
AUCcentralcompartment(%) AUCbrain(%)
Bourassetetal.(2006) 0.6014 4.9401
Tabella 2.17 AUC percentuali per i casi studio del modello tricompartimentale per infusionecontinuadimorfinasomministrataendovenaneiratti.
AUCcentralcompartment(%) AUCbrain(%)
Kissinetal.(1991)–constant
infusion8.2798 8.4237

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
62
2.12.2 AnalisideirisultatiottenutidalmodelloPBPK
Passandooraall’analisidei risultatiottenutidalmodelloPBPKattraverso la letturadei
valori delleAUCpercentuali per ciascun compartimento, si potrànotare comequesto
modelloabbiamiglioratoqueicasi incui ilmodello tricompartimentale riportavadelle
lacune.
Dallatabella2.18,incuisonopresentileAUCpercentualidelcasodibassedosidimorfina
somministrataendovena,sipuòosservarecheadessotuttiivaloridelleAUCpercentuali
sonoinferiorial30%.
Tabella 2.18 AUC percentuali per i casi studio del modello PBPK per basse dosi di morfinasomministrataendovenaviaboloneiratti.
AUCcentral
compartment(%)AUCbrain(%)
Plompetal.(1981)–casostudio1 17.607 3.4511
Plompetal.(1981)–casostudio2 3.1459 16.2383
Plompetal.(1981)–casostudio3 22.9708 24.3026
Nelcasodisomministrazioneendovenadimediedosidimorfinasipuònotareintabella
2.19comeivaloridiAUCpercentualerisultantisianoaccettabili,puressendol’AUCdel
compartimento brain vasculature pari al 38.91%, cioè al di sopra del limite
dell’accettabilità.
Tabella 2.19 AUC percentuali per i casi studio del modello PBPK per medie dosi di morfinasomministrataendovenaviaboloneiratti.
AUCcentralcompartment(%) AUCbrain(%)
Dahlstrometal.(1975) 10.4078 11.1339
Kissinetal.(1991)–viabolo 5.7185 38.9117
Infine,perquantoriguardaicasidimodellazionedisomministrazioneendovenadialte
dosidimorfinaviaboloediinfusionecontinuaivaloridiAUCpercentualesonosempre

Modellofarmacocineticodellamorfinaneiratti
63
inferiorial10%,manifestandounabuonaaffidabilitàdapartedelmodello,cheriescea
riprodurreidatisperimentaliinmanierasoddisfacente(Tabelle2.20e2.21).
Tabella 2.20 AUC percentuali per i casi studio del modello PBPK per alte dosi di morfinasomministrataendovenaviaboloneiratti.
AUCcentralcompartment(%) AUCbrain(%)
Bourassetetal.(2006) 3.3326 7.8589
Tabella2.21AUCpercentualipericasistudiodelmodelloPBPKperinfusionecontinuadimorfinasomministrataendovenaneiratti.
AUCcentralcompartment
(%)AUCbrain
(%)Kissinetal.(1991)–constantinfusion 8.8307 6.7757
2.12.3 Confrontodeirisultatiottenutidaiduemodelli
In questo paragrafo simettono a confronto le AUC percentuali ottenute dalmodello
tricompartimentaleedalmodelloPBPK(tabelle2.22e2.23),evidenziandoledifferenze
traglistessicompartimenti.Partendodalcasodisomministrazioneendovenaviabolodi
bassedosidimorfina,sipuònotarecome,graziealmodelloPBPK,l’AUCpercentualedel
compartimento cervellodatadallamodellazionedeidati di Plompetal. (1981) - caso
studio2sisiaabbassataaldisottodel30%.Quindi,purperdendounpo’diprecisionenel
casostudio3rispettoall’AUCfornitadaltricompartimentale,ilmodelloPBPKgarantisce
unabuonaaffidabilitàsututtiicasi.
Tabella 2.22 Confronto AUC percentuali ottenute nel compartimento centrale dal modellotricompartimentaleenelcompartimentoplasmadalmodelloPBPK.
Tricompartimentalmodel
CentralcompartmentAUC
(%)
PBPKmodel
CentralcompartmentAUC
(%)
Plompetal.(1981)–
casostudio19.54 17.607

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
64
Plompetal.(1981)–
casostudio213.49 3.1459
Plompetal.(1981)–
casostudio315.2461 22.9708
Dahlstrometal.(1975) 9.3489 10.4078
Kissinetal.(1991)–via
bolo13.3036 5.7185
Bourassetetal.(2006) 0.6014 3.3326
Kissinetal.(1991)–
constantinfusion8.2798 8.8307
Tabella 2.23 Confronto AUC percentuali ottenute nel compartimento cervello dal modellotricompartimentaleenelcompartimentobrainvasculaturedalmodelloPBPK.
Tricompartimentalmodel
BraincompartmentAUC(%)
PBPKmodel
Brainvasculature
compartmentAUC(%)
Plompetal.(1981)–
casostudio123.72 3.4511
Plompetal.(1981)–
casostudio234.25 16.2383
Plompetal.(1981)–
casostudio32.8912 24.3026
Dahlstrometal.(1975) 13.7732 11.1339
Kissinetal.(1991)–via
bolo51.8248 38.9117
Bourassetetal.(2006) 4.9401 7.8589
Kissinetal.(1991)–
constantinfusion8.4237 6.7757

Modellofarmacocineticodellamorfinaneiratti
65
DanotareancheilmiglioramentodelmodellonelcasodellostudiodiKissinetal.(1991)
– via bolo. Anche in questo caso, infatti, il modello PBPK fornisce una performance
miglioreabbassandol’AUCpercentualedal51.82%al38.91%.Quest’ultimovalore,pur
restandoalto,siavvicinaal30%,aumentandocosìl’affidabilitàdelmodelloPBPKrispetto
altricompartimentale.
Pertuttiglialtricasisiassisteadunaleggeradiminuzioneounleggeroaumentodell’AUC
percentuale,restandosemprealdisottodel25%.

66
3 Modellofarmacocineticodellamorfinanegliuomini
3.1 Metabolizzazionedellamorfina
Comevistonelcapitolo1,circail90%dellamorfinachevienesomministrataèeliminata
perviaepatica.Questooppioidevieneassorbitorapidamentedagliorganimoltoperfusi,
tracuiilfegato,equivienemetabolizzata.
Lamaggior parte deimetaboliti ottenuti ha un’attività farmacologica ed è per questo
motivocherisultainteressanteandarneastudiarelecaratteristicheeilmeccanismodi
formazione,perpoterarricchireilmodellofarmacocinetico.Laquasitotalitàdellamorfina
viene convertita nei suoi glucoronidi: morfina-3-glucoronide e morfina-6-glucoronide,
notianchecomeM3GeM6Grispettivamente.Inparticolare,comesivedràinseguito,la
M6Ghaun’attivitàanalgesicasuperioreaquelladellamorfinastessa,alcontrariolaM3G
non ha alcun effetto analgesico. Fra i metaboliti minori si rammentano: normorfina,
codeina emorfina-3-solfato. Il primo viene ottenuto attraverso la O-transmetilazione
della morfina, il secondo attraverso la demetilazione della morfina ed infine l’ultimo
metabolitaattraversolareazionediconiugazione(Janicki,2008).
3.1.1 M3GeM6G
Lamorfina-3-glucoronidee lamorfina-6-glucoronidesono iduemetaboliti isomeripiù
importantidellamorfina.LaloroformulachimicaèC23H27NO9.Comegiàaccennatolaloro
formazionehaluogonelfegato,dovelereazionidiglucoronazioneavvengonograziealla
presenzadeglienzimiuridinadifosfatoglucuronosiltransferasi(UDPGT)checatalizzanola
reazionediglucoronazione.Inparticolare,comeillustratoinFig.3.1,l’enzimaUGT2B7è
coinvoltonellaformazionedellaM6G,mentrel’enzimaUGT1A3permettelaformazione
dellaM3G(Sverrisdóttiretal.,2015).Circa il45-55%dellamorfinavieneconvertita in
M3G, invece il 10-15%è convertito inM6G. La reazionedi glucoronazioneprevede la
reazionedellamorfinaconl’acidoglucuronico(Fig.3.2),underivatodelglucosiopresente
nelfegato.

Modellofarmacocineticodellamorfinanegliuomini
67
Figura3.1Illustrazionedeiduemetabolitiprincipalidellamorfina
Figura3.2Strutturachimicadell’acidoglucuronico
Lastechiometriadireazioneèlaseguenteperentrambiimetaboliti:
17 19 3 15 22 2 18 2 23 27 9 9 14 2 12 2C H NO C H N O P C H NO C H N O P+ ® + (23)
È stato dimostrato che il tessuto epiteliale dell’intestino tenue e dell’intestino crasso
contribuisconoallaformazionediM6G.Allostessotempo,iltessutoepitelialedeltratto
gastrico,dell’intestinoedelcolonsonocoinvoltinellametabolizzazionedellamorfinaa

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
68
dareM3G(Janicky,2008).Èimportantesottolinearecomequesticontributisianomolto
inferioririspettoaquellodelfegato.
Pergliumanièstatoosservatochelavelocitàconlaqualelamorfinavienemetabolizzata
dipendedall’etniadell’individuo:neicinesilamorfinavienemetabolizzataattraversola
reazione di glucoronazione ad una velocità molto più elevata rispetto agli individui
bianchi. A ciò consegue che in questi ultimi gli effetti, sia analgesici che collaterali,
prodottidallamorfinasonopiùevidenti,mentrerisultanomenoevidentiglieffettidei
metaboliti(Zhoutetal,1993).
La produzione diM3G eM6G è influenzata anche dalla via di somministrazione della
morfina:dopoun’infusioneintravenosadimorfinasiosservacheilrapportomolaretra
M6G e M3G è significativamente inferiore rispetto a quello ottenuto dopo una
somministrazioneorale(Osborneetal.,1990).
Comeribadito inprecedenza, lecaratteristiche idrofiledellamorfinadeterminanoche
solounapiccolaquantitàdiessapossaattraversare labarrieraematoencefalica. Idue
metaboliti glucoronidimostrano un comportamento diverso: in essi è stata osservata
un’elevata lipofilicità e ciò permette loro di attraversare la BEE a velocità più elevate
rispetto a quelle della morfina. Sia M3G che M6G sono stati osservati nel liquido
cerebrospinale,tuttavianonèancorachiaroselaloropresenzaderiviesclusivamentedal
passaggio dal sangue al cervello o se parte della morfina presente possa essere
metabolizzataall’internodiquest’organo(Janicky,2008).L’effettoanalgesicodellaM6G
risultamaggiorerispettoaquellodellamorfina,ancheperchéquestometabolitariesce
adattraversareconmaggiorefacilitàlabarrieraematoencefalicae,quindi,raggiungepiù
agevolmenteirecettoricheprovocanol’analgesia.
3.1.2 FarmacologiadiM3GeM6G
Entrambi imetaboliti si sonorivelatiessere farmacologicamenteattivi: laM6Gmostra
un’affinità maggiore con i recettori µ, ed è stato dimostrato che la maggior parte
dell’attivitàanalgesicadellamorfinaderivadaquestometabolita (Hannaetal.,1990).
Inoltre,rispettolamorfinastessa,questometabolitahaun’affinitàminoreconirecettori
µ2,eciòcomportaunadiminuzionedeglieffetticollaterali,quali:depressionerespiratoria

Modellofarmacocineticodellamorfinanegliuomini
69
eriduzionedellamotilitàintestinale.Alcontrario,laM3Gnonmostraalcunaaffinitàcon
irecettoriµequindièprivadiattivitàanalgesica.TuttaviaquestononsignificacheM3G
sia farmacologicamente inattiva: negli animali si è osservato che una sua crescente
somministrazione provoca allodinia ed iperalgesia. La prima condizione conduce a
percepiredolorosistimoli innocui, lasecondaprovocaunaumentodipercezionedegli
stimolidolorosi. Indosielevatesonostatiosservatianche i seguentieffetti collaterali:
eccitazione,prurito,tremorieminzione.
I due metaboliti sono eliminati principalmente attraverso l’urina. In pazienti con
disfunzione renale la loro espulsione è molto lenta, pertanto è possibile rilevarli
all’internodelsangueanchealcunigiornidopolasomministrazionedellamorfina.
Dal momento che solo il metabolita M6G ha effetti analgesici, lo studio della sua
variazioneneltemporisultapiùinteressanterispettoaquelladelM3G:lamaggiorparte
deglistudipresiinconsiderazione,infatti,trascuravaquest’ultimometabolita.Pertanto,
nonavendodatiadisposizioneperconvalidareimodellichedescriveremoneiparagrafi
seguenti, inquestostudioverràomessoilmetabolitaM3G.Ilprincipalemotivopercui
sonostaticondottinumerosistudisullaM6Gèproprioilsuoeffettoanalgesicosuperiore
aquellodellamorfina,conlaconseguentenecessitàdicontrollarnelaconcentrazionenel
corpoondeevitareeffettiindesiderati.
MoltistudisullamorfinaeilsuometabolitaM6Gsonostaticondottisugliuominiesono
dunquepresentiinletteratura.Partendodaquestistudi,inquestolavoroditesisièvoluto
analizzare la farmacocinetica della morfina negli uomini sfruttando gli studi
farmacocinetici e i modelli presentati nel Capitolo 2, passando così dai ratti
all’applicazionedeimodellisugliuomini.
3.2 CostruzionedelmodelloaquattrocompartimentiedelmodelloPBPK
Idueparagrafiseguentidescrivonoimetodichehannoportatoallacostruzionedeidue
modelli:quelloaquattrocompartimentiequelloPBPK.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
70
3.2.1 Modelloaquattrocompartimenti
Partendo dal modello tricompartimentale usato per prevedere la concentrazione di
morfina nel plasma e nel cervello dei ratti, si è potuto arrivare alla costruzione di un
modello che potesse simulare anche la concentrazione di M6G. Ciò è stato possibile
aggiungendo un compartimento al modello tricompartimentale, nello specifico un
compartimentometabolismo.
InFig.3.3èstatariportataunaschematizzazionedelmodelloaquattrocompartimenti.
Figura3.3Schematizzazionedelmodelloaquattrocompartimenti:ilcompartimentocentrale,ilcompartimento degli organi poco perfusi da sangue, il compartimento cervello ed infine ilcompartimentometabolismo.
Iquattrocompartimentichecostituisconoilmodellosono:
1) Compartimentocentrale,checomprendeilplasmaegliorganimoltoperfusidal
sangue;
2) Compartimentodegliorganipocoperfusidasangue;
3) Compartimentocervello;
4) Compartimentometabolismo,dovepartedellamorfinapresentenel
compartimentocentralevieneconvertitanelmetabolitaM6Geinoltrequesto
compartimentopermettel’eliminazionedelmetabolitaformatosi.

Modellofarmacocineticodellamorfinanegliuomini
71
Inquestomodellosonopresenti14parametriche,comevistonelCapitolo2,possono
esseredistintitra:(i)individualizzati,(ii)assegnatio(iii)gradidilibertà.Inparticolarein
questo sistema di equazioni differenziali sono presenti 3 parametri individualizzati, 3
parametriassegnatie8gradidilibertà.Ilnumerodigradidilibertàèelevatorispettoal
numerodiequazionichecompongonoilmodello,questosaràevidenteanchenelmodello
PBPK. Ad ogni equazione, come visto nelmodello dei ratti, corrisponde una variabile
d’integrazione.
Tuttavia,iparametricheregolanogliscambiconilcervellosonostatiassegnati.Infatti,
ottenere dati sperimentali sulla concentrazione di un farmacoo di un suometabolita
all’internodelcervelloumanorisultapraticamenteimpossibileacausadellainvasivitàche
lamisuraavrebbe.Perciònonèpossibileseguirelastessaproceduravistaperirattiossia
identificareilvaloreditaliparametriperchénonsihannoadisposizionedatisperimentali.
A seguito di queste considerazioni si è deciso di utilizzare i valori dei coefficienti di
scambio,tracompartimentocentraleecompartimentocervello,ottenutiperilmodello
tricompartimentaledeiratti.
A seguito di questa scelta i parametri assegnati diventano 6 e i gradi di libertà
diminuisconofinoa5.
Ora risulta interessante analizzare il significato dei diversi parametri. V1, V2 e VBT
rappresentano i volumidi ciascun compartimento, essi sonoparametri individualizzati
perché dipendono dalla massa dell’individuo. V1 e V2 non rappresentano un singolo
organo,maunraggruppamentodiessi,pertanto il lorovaloreèdatodallasommadel
contributodiciascunorgano.VBTrappresentailvolumedelsoloorganocervelloeisuoi
vasisanguigni.Srappresentalasuperficiedeivasisanguignicheraggiungeilcervello,che
corrisponde alla superficie di scambio utile tra il compartimento centrale e il
compartimentocervello.fuplasmaefubrainrappresentanolafrazionedifarmacoliberanel
plasmaenelcervello:unafrazionedellamorfinasomministratasipuòlegarealleproteine
presenti nel sangue, e soltanto lemolecole liberepossonoessere scambiate tra i vari
tessuti ed organi. k10 rappresenta la costante di eliminazione della morfina dal
compartimentocentrale.k12ek21identificanoicoefficientiditrasferimentodimassatra
il compartimento centrale e gli organi poco perfusi e viceversa. Il primo dei nuovi

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
72
parametri introdotti rispettoalmodello tricompartimentale sui ratti è kcin, la costante
cinetica della reazione di formazione delmetabolitaM6G, che insieme a k10 è l’unico
parametrocheregolal’eliminazionedellamorfinanelmodelloaquattrocompartimenti.
L’altro nuovo parametro è k40, che raccoglie tutte le possibili vie di eliminazione del
metabolita formatosi. Pdiff rappresenta il coefficiente di diffusione della morfina dal
compartimento centrale al cervello. Infine Pact e PActiveIN identificano i coefficienti di
trasportoattivo, inparticolareilprimosiriferiscealtrasportoinuscitadalcervelloeil
secondo al trasporto in entrata a quest’ultimo (ulteriori dettagli sono disponibili in
Tab.3.1).
Tabella 3.1 Sono riportati i parametri che compaiono nel modello a quattro compartimentiumano,essipossonoesseredistintitra:individualizzati,assegnatiegradidilibertà.
Symbol Units Description Type
V1 cm3 VolumeofCentralcompartment Individualized
V2 cm3 VolumeofPoorlyperfucedorgans
compartment
Individualized
VBT cm3 Volumeofbraintissuecompartment Individualized
S cm2 Surfaceofbrainvessels Assigned
fuplasma - Fractionoffreedruginplasma Assigned
fubrain - Fractionoffreedruginbrain Assigned
k10 min-1 ConstantofeliminationofCentral
compartment
Degreeoffreedom
k12 min-1 Masstransfercoefficientfromcentral
compartmenttoPoorlyperfuseorgans
Degreeoffreedom
k21 min-1 MasstransfercoefficientfromPoorly
perfuseorganstocentralcompartment
Degreeoffreedom
kcin min-1 Kineticconstantofthereactionof
formationofM6G
Degreeoffreedom
k40 min-1 Constantofeliminationofmetabolism
compartment
Degreeoffreedom

Modellofarmacocineticodellamorfinanegliuomini
73
Pdiff cm/s Diffusioncoefficientfromcentral
compartmenttobraintissue
compartment
Assigned
Pact cm/s Effluxcoefficientfrombraintissue
compartmenttocentralcompartment
Assigned
PActiveIN cm/s Influxcoefficientfromcentral
compartmenttobraintissue
Assigned
Il modello è costituito da quattro compartimenti, pertanto per poter conoscere la
concentrazionedi ciascuncompartimentoènecessario risolvereunsistemadiquattro
equazionidifferenziali,unaperciascuncompartimento,riportatequidiseguito(Eq.24-
27):
1 31 210 12 1 21 2
1 1 1 1
3 1
1 1
- ( ) - ( - )
-
plasma braincinplasma diff
act brainactiveIN
C fu C fudC VIR k k fu k C k C P Sdt V V V VP S C fu CP S
V V
× ×= + × + × + × × × × +
× × ×+ × ×
(24)
2 112 1 21 2
2
- plasmadC V k fu C k Cdt V
= × × × × (25)
3 3 11 3= ( - ) - plasma brain brain activeIN
diff actBT BT BT BT
fudC C fu fu P S CP S C P S Cdt V V V V
× × ×× × × × × × + (26)
4 1 40 6cin M GdC k C k Cdt
= × - × (27)
I termini C1, C2 e C3 rappresentano rispettivamente la concentrazione di morfina nel
compartimento centrale, nel compartimento degli organi e tessuti poco perfusi e nel
cervello,mentreC4rappresentalaconcentrazionedelmetabolitanelsuocompartimento.
Nellaprimaequazioneoltreadapparireiparametriprecedentementedescrittièpresente

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
74
ancheilparametroIR,essorappresental’infusionedellamorfina.Dalmomentochetutti
glistudipresiinconsiderazioneprevedonounasomministrazioneintravenosadiquesto
analgesico, appare sensato assumere che il farmaco sia inizialmente iniettato nel
compartimentocentrale,cheoltreagliorganimoltoperfusi,comprendeilplasma.
Perquantoriguardalaformazionedelmetabolita,secondolostudiodiLötschetal.(2002)
sipuòassumereunacineticadelprimoordineelavelocitàdireazioneècontrollatadalla
sola concentrazione di morfina. Come visto in precedenza la maggior parte della
metabolizzazionedellamorfinaavvienenelfegato,tuttaviainquestomodellononesiste
ilcompartimentofegato,pertantosièassuntochelavelocitàdireazionesiacontrollata
dalla concentrazione di morfina nel compartimento centrale. Questa scelta appare
sensatapoichéquestocompartimentocomprendeancheilfegato.
Per poter valutare il volume dei differenti compartimenti attraverso l’equazione (1) è
necessarioconoscerelafrazionemassivarispettoalcorpodell’individuoeladensitàdegli
organi o dei tessuti che li compongono, indicate rispettivamente con FrBmi e ri. i
compartimenti del modello sono composti allo stesso modo di quelli del modello
tricompartimentalesuiratti,equindi:
§ Ilcompartimentocentralecomprendeilplasmaegliorganimoltoperfusi,come
fegato,cuore,ilsistemacircolatoriogastrointestinale,irenielamilza;
§ Ilcompartimentodegliorganipocoperfusidasanguecomprendepolmoni,pelle,
grasso,ossaemuscoli;
§ Ilcompartimentocervellocomprendeesclusivamenteilcervello.
I polmoni non sono compresi negli organimolto perfusi da sangue a causa della loro
natura:essisonointensamentevascolarizzati,mahannounadensitàmoltobassaquando
sonoespansi,pertantoèdifficiletrovareunvaloreaffidabileperillorovolume.Gliorgani
genitali,invece,sonotrascurabiliperchéillorovolumeèmoltoinferiorerispettoaquello
degli altri organi. In Tab.3.2 sono riportati i valori della frazionemassiva rispetto alla
massadell’individuodeidifferentiorganietessuti.

Modellofarmacocineticodellamorfinanegliuomini
75
Tabella3.2Frazionemassivaedensitàdeidifferentiorganietessuti(Brownetal.,1997).
Organ/Tissue FrBM Density[kg/cm3]
Liver 0.0257 0.0001
Brain 0.02 0.001035
Heart 0.0047 0.00103
Lungs 0.0076 0.0015
Skin 0.0371 0.0013
Adipose 0.2142 0.000916
Bone 0.1429 0.0016
Muscle 0.4 0.00141
Spleen 0.026 0.001054
Kidneys 0.0044 0.00105
Brainvasculature 0.0193236 1000
GICS 0.0001761 1000
Èinteressantesottolinearecheinletteraturanonèdisponibilealcunaformulaperpoter
calcolareilvolumedelsistemacircolatoriogastrointestinale.Abbiatietal.,(2016)hanno
propostouna relazioneperpoter stimarequesto volume: considerando la venaporta
comeilcomponenteprincipalediquestosistema.Lavenaportainunuomoaventeuna
massacorporea(BM)paria80kghaunalunghezzamediaeundiametromediodi1.1e
5.8 cm rispettivamente, considerandola come un cilindro è possibile calcolare il suo
volume(VPV).Dalmomentocheilsistemacircolatoriogastrointestinalenonècostituito
dallasolavenaporta,ilvolumeottenutovienemaggioratodel35%,èpossibilevalutare
lafrazionemassivadelsistemacircolatoriogastrointestinalecomesegue:
, 0.00017611000PV
BM GICSVFr
BM= =
× (28)

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
76
Per quanto riguarda il volume dei vasi sanguigni del cervello, esso è stato trovato
rapportandoilvaloreriportatoinletteraturaperunrattoda250g,conilpesodelpaziente
considerato.
I parametri assegnati sono quelli per cui in letteratura non esistono relazioni per cui
possonoessereindividualizzati.Ilvaloredellasuperficiedeivasisanguigninelcervelloè
statoriportatodaBronzinoetal.()edèpossibileassumerlocircacostantepertuttigli
individui.Perquantoriguardalafrazionedimorfinaliberafuplasmaefubrainhannolostesso
valoreassegnatoperiratti,pertantofraleduespecienonesistedifferenzapercomela
morfinainteragisceconleproteineall’internodelplasmaenelcervello.
Infine i gradi di libertà sono quei parametri che non hanno un significato
anatomico/fisiologicoequindinonèpossibiletrovarenécorrelazioninécorrispondenze
numeriche in letteratura. Pertanto per determinare questi parametri numerici è
necessario effettuare una regressione non lineare utilizzando i dati sperimentali a
disposizione.
Perpotereffettuarelaregressionenonlineareènecessarioaveredeidatisperimentali
perminimizzareladistanzacheesistefraessieirisultatiprevistidalmodello.
Diseguitovieneriportatalafunzioneobiettivo(fobj)cheèstataminimizzataperottenere
iparametriinoggetto:
exp model exp model, , , ,
1exp model exp model, 6 , 6 , 6 , 6
1
(| | | max( ) max( ) || log |
(| | | max( ) max( ) || log |
Ni mor i mor i mor i mor
obji
Mi M G i M G i M G i M G
i
C C C Cf
NC C C C
M
=
=
- + -= +
- + -+
å
å (29)
dove:
§ NeMsono inumerididati sperimentaliadisposizioneper lamorfinaeper il
metabolitaM6Grispettivamente;
§ Ci,morexpeCi,M6G
expidentificanolaconcentrazionemisuratasperimentalmentedella
morfinaedelsuometabolita;
§ Ci,mormod e Ci,M6G
mod si riferiscono alle concentrazioni previste dal modello
all’istantei-esimoallaqualeèavvenutoilprelievodalpaziente.

Modellofarmacocineticodellamorfinanegliuomini
77
Percomeècostruitalafunzione,nonsiminimizzasemplicementelasommadeglierrori
cheesistefradatisperimentalierisultatidelmodello,maaquestisiaggiungeilvalore
assolutodellamassimadifferenzacheintercorrefradatisperimentaliequelliprevistidal
modello.Questopassaggiosirivelanecessarioaffinchéilmodelloriescaacoglierecon
maggiorprecisioneipicchidiconcentrazionemassimiraggiuntidallamorfinaedaM6G.
Inoltre,comeverràapprofonditonelparagrafo3.4,nonvieneeffettuataunasemplice
sommafrailcontributodellamorfinaequellodelmetabolita,masisommanoilogaritmi
deiduemembri:questopassaggioènecessarioperavereunamiglioreconcordanzafrale
concentrazionisperimentaliequelleprevisteabasseconcentrazioni,ossiacirca200min
dopolasomministrazione.
Questiparametrisonostatiindividuatiattraversoun’ottimizzazionevincolata,sfruttando
lafunzioneFmincondiMatlab.Igradidilibertàpossonoassumereunvaloreall’internodi
unintervallo:illimiteinferioreè0perchéessidevonoesserepositivi.Illimitesuperioreè
statosceltobasandosisuivaloridiparametrisimiliriportatiinletteratura.
IvaloriottenutiattraversolaproceduradiottimizzazionesonoriportatiinTab.3.3.
Tabella3.3Da sinistra: limite inferioredell’ottimizzazionevincolata, valoredi primo tentativo,limitesuperioredell’ottimizzazioneevalorefinaleottenuto
Parameters Lowerbounds Initialvalues Upperbounds Optimizedvalues
k10 0 0.19402 1 0.01420
k12 0 3.03853 5 0.91029
k21 0 0.373803 1 0.12893
kcin 0 0.5 1 0.03462
k40 0 0.5 1 0.02768
Comevaloridiprimotentativosonostatiutilizzati,secomuniaiduemodelli,iparametri
ottenutidallaregressionenonlinearedelmodellotricompartimentaledeiratti.Perkcine
k40 non sono stati trovati modelli simili da cui ricavare un valore di primo tentativo,
pertantosièdecisodiutilizzareunvaloreinizialecheavesselostessoordinedigrandezza
diquelliusatiperglialtriparametri.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
78
Èinteressantesottolinearecheivaloriottimizzatisiallontananoinmanierasignificativa
dal valore di primo tentativo,ma questo era prevedibile: si stanno considerando due
modellidistrutturadifferenteperduespecieanimalidiverse.
3.2.2 ModelloPBPK
Per costruire il modello PBPK umano è stata usata la stessametodologia vista per il
modello a quattro compartimenti: comebase di partenza è stato utilizzato ilmodello
PBPK dei ratti, a cui è stato aggiunto il compartimento metabolismo, il cui scopo è
prevederelaconcentrazionedelmetabolitaM6G(Fig.3.4).
Ilmodelloècostituitoda8compartimenti:
§ Compartimentoplasma;
§ Compartimentoorganimoltoperfusidasangue;
§ Compartimentoorganipocoperfusidasangue;
§ Compartimentovascolarizzazionedelcervello;
§ Compartimentotessutidelcervello;
§ Compartimentosistemacircolatoriogastrointestinale;
§ Compartimentofegato;
§ Compartimentometabolismo.
È interessante sottolineare che, rispetto al modello visto nel paragrafo precedente, i
compartimentidelmodelloPBPKnonrappresentanoesclusivamenteungruppodiorgani
oditessuti,maidentificanoancheunsoloorganoounsolotessuto.

Modellofarmacocineticodellamorfinanegliuomini
79
Figura3.4È rappresentataunaschematizzazionedegliottocompartimenti checompongono ilmodelloPBPK:ilcompartimentoplasma,ilcompartimentodegliorganipocoperfusidasangue,ilcompartimento degli organi molto perfusi da sangue, il compartimento vascolarizzazione delcervello, il compartimento tessuti del cervello, il compartimento del sistema circolatoriogastrointestinale,ilcompartimentofegatoedinfineilcompartimentometabolismo.
Inquestomodellosonopresenti29parametri,dicui12sonoindividualizzati,6assegnati
e11gradidilibertà.
V1rappresenta il volumediplasmapresentenell’individuo,V2descrive il volumedegli
organi poco perfusi da sangue, V3 si riferisce al volume degli organimolto perfusi da
sangue, ma, a differenza del modello quattro compartimenti, il fegato e il sistema
circolatoriogastrointestinalenonsonopiùcompresiinquesto,masonorappresentatida
duealtricompartimenti,divolumeVLeVGICS rispettivamente. InfineVBVeVBT indicano
rispettivamenteilsistemacircolatoriodelcervelloeitessutidelcervello.
In questo modello ci sono diversi parametri che si riferiscono alle diverse portate
sanguignecheraggiungonoidiversiorgani:
• QP_BVèlaportatasanguignachevadalplasmaalcervelloeviceversa,lamaggior
partedelplasmacheraggiungeilcervelloèportatodall’arteriacarotide,lavena

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
80
giugulare,invece,èadibitaaportareilplasmadalcervelloalcompartimento
plasma;
• QP_Lèlaportatadiplasmacheraggiungeilfegatoattraversol’arteriaepatica;
• QHVèlaportatadiplasmaassociataallavenaepatica;
• QP_GICS,infine,rappresentalaportatadiplasmaassociataalsistemacircolatorio
gastrointestinale;
• Qkidneysèlaportatadiplasmacheraggiungeireni.
Tutte questeportate sono funzionedella gittata cardiaca (CO, cardiac output): essa è
assunta pari a 5200 mL/min, tuttavia questa quantità fa riferimento al sangue,
conoscendo la frazione di plasma nel sangue umano, è possibile ottenere la gittata
cardiacadiplasma(Eq.30):
ml ml5200 0.55 2860min min
CO = × = (30)
Inrealtàlagittatacardiacanonècostante,mafunzionedimassaegenere,tuttavianei
diversistudiconsideratiilgenerenonèsemprespecificato.Essendolamassadeidiversi
pazientisimile,percomoditàsièsceltodiassumerelagittatacardiacanonvariabile.
Comeperiratti,cosìpergliumaniBrownriportanelsuolibroleseguentirelazioniper
calcolarelediverseportatepresentinelmodello(Eq.31-35):
ml0.144 326min
P BV plasmaQ CO X- = × × = (31)
ml0.175 500.5min
kidneys plasmaQ CO X= × × = (32)
ml0.227 649.2min
P GICS plasmaQ CO X- = × × = (33)
ml0.046 131.56min
P L plasmaQ CO X- = × × = (34)

Modellofarmacocineticodellamorfinanegliuomini
81
ml0.181 517.66min
HV plasmaQ CO X= × × = (35)
Perquantoriguardaiparametriassegnatiessisono:S,fubrain,fuplasma,Pdiff,PactePActiveIN.
Essi sonogli stessi presenti nelmodello aquattro compartimenti, quindiperuna loro
analisi dettagliata ci si può riferire al paragrafo precedente, fatta eccezione per S. La
superficiediscambiodelplasmacolcervelloèritenutacostanteaprescinderedallamassa
corporeadegliindividui.
I gradi di libertà presenti nel modello sono 11, in particolare k12 e k21 identificano i
coefficientidi trasferimentodimassa tra il compartimentoplasmae il compartimento
degliorganipocoperfusidasangue,k13ek31hannolostessosignificatodeidueappena
citati,peròperquantoriguardaloscambiotragliorganimoltoperfusidasangueeplasma.
jplejlpsono,rispettivamente,icoefficientidipartizioneplasma-fegatoefegato-plasma.
EffKèunparametrochemoltiplicalaportatadisanguecheraggiungeireniedidentifica
l’efficienza di quest’ultimi, esso è coinvolto nell’eliminazione dellamorfina attraverso
l’urina.
EffH,invece,identifical’efficienzaepaticadelfegato,ossiaessodefiniscelapercentuale
dimorfinachevienemetabolizzataequindieliminatadalfegato.Questoparametrotiene
conto di tutti i metaboliti ad eccezione di M6G, che si forma nel compartimento
metabolismo.
CLlilidentificaun’altraviadieliminazionedellamorfina,inparticolareattraversolefeci.
IlparametrokcinfariferimentoallacostantecineticadiformazionedelmetabolitaM6G,
infinek40èlacostantedieliminazionediquest’ultimo.
NellaTab.3.4sonoriportatiindettagliotuttiiparametridelmodello.
Tabella 3.4 Sono riportati i parametri che compaiono nelmodello PBPK umano, essi possonoesseredistintitra:individualizzati,assegnatiegradidilibertà.
Symbol Units Description Type
V1 cm3 VolumeofPlasmacompartment Individualized
V2 cm3 VolumeofPoorlyperfucedorgans
compartment
Individualized

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
82
V3 cm3 VolumeofHighlyperfucedorgans
compartment
Individualized
VBV cm3 Volumeofbrainvasculature
compartment
Individualized
VBT cm3 Volumeofbraintissuecompartment Individualized
VGICS cm3 VolumeofGICScompartment Individualized
VL cm3 VolumeofLivercompartment Individualized
QP_BV mL/min Volumetricfluxofcardiacoutputto
brain
Individualized
QP_L mL/min Volumetricfluxofhepaticartery Individualized
QHV mL/min Volumetricfluxofhepaticvein Individualized
QP-GICS mL/min Volumetricfluxofcardiacoutputto
GICS
Individualized
Qkidneys mL/min Volumetricfluxofcardiacoutputto
kidneys
Individualized
S cm2 Surfaceofbrainvessels Assigned
fuplasma - Fractionoffreedruginplasma Assigned
fubrain - Fractionoffreedruginbrain Assigned
jpl - Plasma-liverpartitioncoefficient Degreeoffreedom
jlp - Liver-plasmapartitioncoefficient Degreeoffreedom
effH - Efficiencyofeliminationofliver Degreeoffreedom
effK - Efficiencyofeliminationofkidneys Degreeoffreedom
CLlil min-1 ConstantofeliminationofGICS
compartment
Degreeoffreedom
k12 min-1 Masstransfercoefficientfromcentral
compartmenttoPoorlyperfused
organs
Degreeoffreedom
k21 min-1 MasstransfercoefficientfromPoorly
perfusedorganstocentral
compartment
Degreeoffreedom

Modellofarmacocineticodellamorfinanegliuomini
83
k13 min-1 Masstransfercoefficientfromcentral
compartmenttoHighlyperfused
organs
Degreeoffreedom
k31 min-1 MasstransfercoefficientfromHighly
perfusedorganstocentral
compartment
Degreeoffreedom
kcin min-1 Kineticconstantofthereactionof
formationofM6G
Degreeoffreedom
k40 min-1 Constantofeliminationof
metabolismcompartment
Degreeoffreedom
Pdiff cm/s Diffusioncoefficientfromcentral
compartmenttobraintissue
compartment
Assigned
Pact cm/s Effluxcoefficientfrombraintissue
compartmenttocentral
compartment
Assigned
PActiveIN cm/s Influxcoefficientfromcentral
compartmenttobraintissue
Assigned
Il modello PBPK è costituito da otto compartimenti, pertanto per conoscere le
concentrazionineivaricompartimentiènecessariorisolvereunsistemadiottoequazioni
differenzialiriportatodiseguito(Eq.36-43):
P_GICS P_LBV 11 2P_BV 1 12 plasma 13 plasma 2 21
1 1 1 lp 1 pl 1
kidneysHV 33 31 1 K
lp 1 1 1
Q Q(C -C ) VIR = + Q - C (k fu + k fu + + )+ C k + V V V j V j V
QQ V+ C + C k - C effj V V VL
dCdt
× × × × × ×× ×
× × × × ××
(36)
2 112 plasma 1 21 2
2
V k fu C -k CV
dCdt
= × × × × (37)

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
84
3 113 plasma 1 31 3
3
V k fu C -k CV
dCdt
= × × × × (38)
diff BV plasma BT brain1 BV activeOUT BT brainP_BV
BV BV BV
activeIN BV plasma
BV
P S (C fu -C fu )(C -C ) P S C fuQ - + +V V V
P S C fu -
V
BVdCdt
× × × × × × ×= ×
× × × (39)
diff BV plasma BT brain activeIN BV plasmaactiveOUT BT brain
BT BT BT
P S (C fu -C fu ) P S C fuP S C fu- + V V V
BTdCdt
× × × × × × ×× × ×= (40)
P_GICS P_GICS lil GICS1 GICS
GICS lp GICS GICS
Q Q CL CC - C - V j V j V
GICS
pl
dCdt
×= × ×
× × (41)
P_L P_GICS P_GICS H HV L1 GICS L
pl L pl L L lp lp L
Q Q Q eff Q CC + C - C - j V j V V j j V
L cin LdC k Cdt
× ×= × × × - ×
× × × × (42)
640 6
M Gcin L M G
dC k C k Cdt
= × - × (43)
Èimportantesottolinearealcuniaspettidiquestosistema:
§ Dalmomentochetuttiglistudiconsideratiprevedonoinfusioniintravenose,IR,
ossialadosesomministrata,apparenelcompartimentoplasma
§ Dalmomentochelamorfinavienesomministratatramiteinfusioneintravenosa,
è stato possibile trascurare il compartimento stomaco e il compartimento
intestino, tuttavia, come visto nel paragrafo 1.4.2, circa il 10% della morfina
somministratavieneeliminataattraversolefeci,pertantoilparametroCLlilèstato
introdottopertenerecontodiquestoaspetto
§ LavelocitàdiformazionedelmetabolitaM6Gdipendedallaconcentrazionedella
morfina presente nel fegato, questa è un’assunzione lecita perché la maggior
partedellametabolizzazionedellamorfinaavvienenelfegato

Modellofarmacocineticodellamorfinanegliuomini
85
Per poter calcolare i volumi dei singoli compartimenti sono state usate lemedesime
relazionivistenelparagrafo3.2.1.
Per individuare igradidi libertàènecessarioeffettuareunaregressione lineare,come
vistoperilmodelloaquattrocompartimenti.
Lafunzionedaminimizzareèlamedesimavistaprecedentemente(Eq.6).Peridettaglisi
rimanda al paragrafo 3.2.1. Nella Tab.3.5 sono riportati i valori ottenuti
dall’ottimizzazione.
Tabella3.5Da sinistra: limite inferioredell’ottimizzazionevincolata, valoredi primo tentativo,limitesuperioredell’ottimizzazioneevalorefinaleottenuto.
Parameters Lowerbounds Initialvalues Upperbounds Optimizedvalues
k12 0 0.135711 1 0.18203
k21 0 1.302530 2 0.14548
k13 0 53.68669 100 1.4542
k31 0 0.395084 1 0.017892
jlp 0 0.0405566 1 0.16297
jpl 0 0.0413809 1 0.032426
effK 0 0.00916 1 0.004309
effH 0 0.942388 1 0.099156
CLlil 0 0.010325 1 0.037618
kcin 0 0.5 1 0.013693
k40 0 0.5 1 0.014998
Come valore di primo tentativo sono stati usati, quando comuni ai due modelli, i
parametridelmodelloPBPKdeiratti.Gliunicidueparametrinoncomunisonokcinek40,
il lorovalore inizialeèstatosceltobasandosisull’ordinedigrandezzamediodeglialtri
parametri,dalmomentocheinletteraturanoneranoriportatidatichepotesseroessere
utilizzatiall’internodiquestomodello.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
86
Èpossibilenotarecomealcuniparametriaseguitodelcambiodispecieedellamodifica
dellastrutturadelmodellovarinosignificativamente,peròèinteressanteosservarecome
iparametricoinvoltinell’eliminazionedellamorfina(effK,effHeCLlil)abbianomantenuto
lostessoordinedigrandezza.Questocomportamentoèspiegabileperchélevietramite
le quali la morfina viene eliminata negli uomini e nei ratti sono le stesse, pertanto,
essendo i modelli PBPK basati sulla fisiologia, i parametri che hanno un significato
fisiologico,chesonocomuniaiduemodelliechenondipendonodallamassacorporea
eraprevedibilecheassumesserovalorisimili.
3.3 Risultatidelmodelloaquattrocompartimenti
Quidiseguitoverrannomostratiirisultatidelmodelloaquattrocompartimentidiscusso
neiparagrafiprecedenti.
3.3.1 Caso-studio1:Stuart-Harrisetal.(2000)
Stuart-Harrisetal. (2000)hannoinvestigato lafarmacocineticadellamorfinaedelsuo
metabolitaM6G in sei individui sani: l’etàmediadi quest’ultimi era25.8 anni, il peso
medio71.4kgetrediessieranomaschi.Ciascunodiessiharicevuto5mgdimorfina
tramite un’infusione intravenosa, in Fig.3.5 sono riportati i risultati del modello
farmacocineticocomparaticonirisultatisperimentali.
Figura 3.5 Sono riportati i risultati dellamorfina (colonna sinistra) e quelli delM6G (colonnadestra), in rosso sono rappresentati i valori dei dati sperimentali e in blu è rappresentato ilmodello.

Modellofarmacocineticodellamorfinanegliuomini
87
Caso-studio2:Lötschetal.(2002)
Lötschetal.(2002)hannocostruitounmodellofarmacocineticoperpoterprevederela
concentrazione di morfina e del suometabolitaM6G. Per poterlo convalidare hanno
somministrato a otto individui sani, attraverso un’infusione intravenosa, 5.64 mg di
morfina. Ipazientieranoquattrouominiequattrodonne,aventiun’etàmediadi26.4
anni,unpesomediodi70.5kgeun’altezzamediadi1.75m.InFig.3.6sonoriportati i
risultatiottenuti.
Figura 3.6 Sono riportati i risultati dellamorfina (colonna sinistra) e quelli delM6G (colonnadestra), in rosso sono rappresentati i valori dei dati sperimentali e in blu è rappresentato ilmodello.
Caso-studio3:Osborneetal.(1990)
Osborne et al. (1990) per poter convalidare un modello farmacocinetico hanno
somministratoadieciindividuisani5mgdimorfina,attraversoun’infusioneintravenosa.
Ipazientieranosetteuominietredonne,l’etàmediadiquestiera30.2annieilloropeso
medio72kg.InFig.3.7sonoriportatiirisultati.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
88
Figura 3.7 Sono riportati i risultati dellamorfina (colonna sinistra) e quelli delM6G (colonnadestra), in rosso sono rappresentati i valori dei dati sperimentali e in blu è rappresentato ilmodello.
Caso-studio4:Stanskyetal.(1978)
Stanskyetal.(1978)hannocondottoillorostudiosuunsingolopazientesanodi28anni.
L’individuo,aventeunpesodi75kg,ha ricevutoun’infusione intravenosadi10mgdi
morfina.Inquestostudioèstataanalizzatalasolaconcentrazionedellamorfina(Fig.3.8),
tuttaviaquestidati sperimentali si rivelanoutili perpoter convalidareulteriormente il
nostromodello.
Figura 3.8 In rosso sono rappresentati i dati sperimentali, la linea blu, invece, rappresenta ilmodello.
3.4 RisultatidelmodelloPBPK
AseguitodellaprecedentediscussionesulmodelloPBPKsiriportanoirisultatiottenuti
utilizzandoquestomodello.

Modellofarmacocineticodellamorfinanegliuomini
89
3.4.1 Caso-studio1:Stuart-Harrisetal.(2000)
Ilparagrafo1.1.1. riporta idettaglidellostudiodiStuart-Harrisetal. (2000), inFig.3.9
sonomostratiirisultatidelmodelloPBPKcomparaticonirisultatisperimentali.
Figura 3.9 Sono riportati i risultati dellamorfina (colonna sinistra) e quelli delM6G (colonnadestra), in rosso sono rappresentati i valori dei dati sperimentali e in blu è rappresentato ilmodello.
3.4.2 Caso-studio2:Lötschetal.(2002)
IdettaglidellostudiodiLötschetal.(2002)sonoriportatinelparagrafo1.1.2.InFig.3.10
sonovisibiliirisultatiottenuti.
Figura3.10AsinistrasonoriportatiirisultatidellamorfinaedestraquellidelM6G,inrossosonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.
3.4.3 Caso-studio3:Osborneetal.(1990)
IdettaglidellostudiodiOsborneetal.(1990)sonoriportatinelparagrafo1.1.3.InFig.3.11
sonovisibiliirisultatiottenuti.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
90
Figura3.11AsinistrasonoriportatiirisultatidellamorfinaedestraquellidelM6G,inrossosonorappresentatiivalorideidatisperimentalieinbluèrappresentatoilmodello.
3.4.4 Caso-studio4:Stanskyetal.(1978)
IdettaglidellostudiodiStanskyetal.(1978)sonoriportatinelparagrafo1.1.4.InFig.3.12
sonorappresentatiirisultatiottenuti.
Figura 3.12 In rosso sono rappresentati i dati sperimentali, la linea blu, invece, rappresenta ilmodello.
3.5 Discussioneeconfrontodeirisultati
Tutti icasivisti inquestatrattazioneprevedonoun’infusioneintravenosatramitebolo,
pertantolamorfinapuòraggiungereintempimoltobrevituttigliorgani,inparticolare
quellimoltoperfusidasangue.Unadelleparticolaritàdiquestofarmacoècheraggiunge
il picco di concentrazione nel plasma nei primi istanti successivi all’infusione: la sua
distribuzioneall’internodelcorpoumanoavvienetalmenterapidamentechelamisura

Modellofarmacocineticodellamorfinanegliuomini
91
sperimentaledelpiccomassimorisultamoltodifficile.NellaTab.3.6sonoriportatiivalori
delleconcentrazionisperimentalimassimemisurate:
Tabella3.6Vengonoriportatiivalorideipicchimassimineiquattrostudiconsideratiel’istanteincuisonostatimisurati.
Maximummorphineplasmaconcentration
uptakenexperimentally(ng/mL)
Stuart-Harrisetal.(2000) 55.77(after4.14min)
Lötschetal.(2002) 346.09(after1.60min)
Osborneetal.(1990) 39.2(after9.74min)
Stanskyetal.(1978) 747.88(after0.39min)
Come si evince dai valori sopra riportati il valore della concentrazione della morfina
decrescemoltovelocemente,infattisipuònotarecheipicchisonostatimisuratiinistanti
differentitraloroequestocomportaunanotevoledifferenzatraivalori.Inparticolare,
risultasignificativoparagonareiprimitrestudidoveladosedimorfinasomministrataè
moltosimilefraidifferenticasi:neiprimidieciminutilaconcentrazionedimorfinavaria
moltorapidamente.
NellostudiodiLötschetal.(2002)allamisuradellaconcentrazionedelpiccoèassociata
un’incertezzamolto grande pari a 100 ng/ml, pertanto il valore riportato pare essere
soggettoaunerroresperimentale.
Dalmomentochelamisuradelpiccomassimoraggiuntoèmoltodifficiledavalutaree
moltospessoquestanonèaccurata,perverificarel’effettivacorrettezzadeidatisipuò
calcolareilmassimovaloreteoricoraggiungibileeappurarechequestosiamaggioredi
quellomisurato. Ilmassimo valore teorico può essere calcolato dividendo la quantità
somministratadimorfinaperilvolumediplasma.NellaTab.3.7seguentesonoriportatii
risultatiottenuti:
Tabella 3.7 Valori massimi teorici della morfina nel plasma che possono essere raggiunti inciascunodeidiversistudiconsiderati.
Valorediconcentrazionemassimoteorico

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
92
raggiungibiledallamorfinanelplasma(ng/mL)
Stuart-Harrisetal.(2000) 1653.54
Lötschetal.(2002) 1889.00
Osborneetal.(1990) 1639.77
Stanskyetal.(1978) 3148.4
Tutte lemisure sperimentali riportate dai diversi studi si trovano entro questo limite
massimo,inoltresaràimportanteverificarecheancheipicchiraggiuntidaiduemodelli
consideratisianoinferioriaquestivalori.Ivalorimassimiteoricirisultanomoltosuperiori
aquelli effettivamentemisurati, probabilmenteper avvicinarsi aquesti valori sarebbe
necessario effettuare dei prelievi nei primi istanti successivi all’infusione, ad esempio
entro30s.
Per quanto riguarda ilmetabolitaM6G, il piccomassimo viene raggiuntomolto dopo
rispettoaquellodellamorfina, infattiquest’ultimahabisognodiunpo’di tempoper
raggiungereilfegatoeperesseremetabolizzata,comeèvisibileinTab.3.8.
Tabella3.8VengonoriportatiivalorideipicchimassimidiM6Gnelplasmaneitrestudiconsideratiel’istanteincuisonostatimisurati.
ValoremassimodellaconcentrazionediM6Gnelplasma
Stuart-Harrisetal.(2000) 28.44ng/mlraggiuntodopo45.65min
Lötschetal.(2002) 33.89ng/mlraggiuntodopo60.33min
Osborneetal.(1990) 32.24ng/mlraggiuntodopo59.14min
SipuòosservarechenellostudiodiLötschetal.(2002)enellostudiodiOsborneetal.
(1990)ilpiccomassimodiM6Gvieneraggiuntocircaun’oradopol’infusione,nelprimo
studio, invece, questo picco è raggiunto dopo 45.65min.Questa differenza potrebbe
esserespiegatadalfattochelaconcentrazionemisuratadopo45.65minnonsiaquella
massima e che quindi il picco non sia stato ancora raggiunto. Il prelievo di sangue
successivo è avvenuto dopo circa 60 min (i.e. al tempo 90.77 min), quando la
concentrazionediM6Gnelplasmastavagiàdiminuendo.

Modellofarmacocineticodellamorfinanegliuomini
93
ComesièvistoneiparagrafiprecedentiperognimolecoladiM6Gchesi formasene
consuma una dimorfina, pertanto la concentrazionemassima teorica che può essere
raggiuntadalmetabolitaèpariallaconcentrazionemassimateoricadellamorfina.Questo
ragionamento,tuttavia,nontienecontodellapresenzadireazioniparallele,delfattoche
unapartedellamorfinavieneeliminatacomenonconvertitaechequindinontutta la
morfina viene metabolizzata. Comunque si può osservare che il picco massimo del
metabolitamisuratoneitrestudiconsideratièabbondantementeinferiorealmassimo
teoricodellamorfinaequindinonsonovisibilicontraddizionitralemisuresperimentalie
lateoria.
3.5.1 Osservazionisulmodelloaquattrocompartimenti
Conilmodelloaquattrocompartimentisipuònotarecomeilcompartimentocentrale
nonriescaaprevedereconsufficienteaccuratezzailvaloredelleconcentrazionineiprimi
100min:ilnumerolimitatodigradidilibertàdiquestomodellononpermettedivalutare
consufficienteprecisioneilcomportamentodelfarmaconelplasmaneiprimiistantieciò
siripercuotenegliistantiditemposuccessivi.
Al contrario si può notare una buona concordanza tra la concentrazionemassimadel
metabolitaprevistadalmodelloequellamisurata,comesipuòdedurredallaTab.3.9.
Tabella3.9Vengonoriportati ipicchidelleconcentrazionidimorfinaedelmetabolitaM6Gnelplasmaprevistidalmodelloaquattrocompartimenti.
Valoremassimodella
concentrazionedimorfina
nelplasmaprevistadal
modello
Valoremassimodella
concentrazionediM6Gnel
plasmaprevistadal
modelloStuart-Harrisetal.(2000) 57.84ng/ml 28.52ng/ml
Lötschetal.(2002) 66.08ng/ml 29.19ng/ml
Osborneetal.(1990) 57.36ng/ml 28.28ng/ml
Stanskyetal.(1978) 110.14ng/ml
/

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
94
Comesievincedaivalorisoprariportati,ipicchidiconcentrazionedelmetabolitasono
moltoviciniaquellimisuratisperimentalmente.
Alcontrario,ipicchidiconcentrazionedellamorfinasonomoltoinferioririspettoaquelli
ottenutidaidatisperimentali.
3.5.2 OsservazionisulmodelloPBPK
ConilmodelloPBPKsiriesceadottenereunabuonacorrispondenzatravaloriprevistidal
modelloedatisperimentali,questovalesiaperlaconcentrazionedellamorfinasiaperla
concentrazionedelmetabolitanelplasma,comeriportatoinTab.3.10.
Tabella3.10VengonoriportatiipicchidelleconcentrazionidimorfinaedelmetabolitaM6GnelplasmaprevistidalmodelloPBPK.
Valoremassimodella
concentrazionedimorfina
nelplasmaprevistadal
modello
Valoremassimodella
concentrazionediM6Gnel
plasmaprevistadal
modelloStuart-Harrisetal.(2000) 310.97ng/ml 26.86ng/ml
Lötschetal.(2002) 352.84ng/ml 30.62ng/ml
Osborneetal.(1990) 309.76ng/ml 26.67ng/ml
Stanskyetal.(1978) 506.43ng/ml /
Dai risultati sopra riportati si può notare come il modello riesca a prevedere il picco
massimo di morfina nel plasma misurato sperimentalmente nei primi tre studi, per
quantoriguardalostudiodiStanskyetal.(1978)ilmassimoraggiuntodallacurvadella
morfina del modello è inferiore al picco sperimentale. Anche il picco massimo della
concentrazioneraggiuntodalmetabolitaèprevistoconsufficienteprecisionedalmodello
PBPK.

Modellofarmacocineticodellamorfinanegliuomini
95
3.5.3 Confrontotraiduemodelli
Si puònotare come ilmodello PBPK riesca a prevedere conun’accuratezzamaggiore,
rispettoalmodelloaquattrocompartimenti,laconcentrazionedimorfinanelplasmanei
primi minuti successivi all’infusione, inoltre esso riesce a prevedere con sufficiente
precisioneilpiccomassimodelfarmaco,alcontrarioilmodelloaquattrocompartimenti
prevedevalorimoltopiùbassirispettoaquellimisurati.
Perquantoriguardailmetabolitairisultatiottenutidaiduemodellisonoparagonabili.
Tuttaviaperpotervalutarequantitativamenteedeffettuareunconfrontononqualitativo
traiduemodelli,ancheinquestocaso,cosìcomeperimodellisuiratti,sipuòutilizzare
comeindicediperformancel’AUCpercentuale.
Per ciascuno studio considerato e per ciascun modello si calcolerà un indice di
performanceperlamorfinaeuno,sepresentiidatisperimentali,perilmetabolitaM6G,
irisultatisonoriportatiinTab.3.11eTab.3.12.
Tabella3.11Sonoriportatiivaloridell’indicediperformancedelmodelloPBPKedelmodelloaquattrocompartimentiperlamorfina.
AUC%modelloaquattro
compartimentiAUC%modello
PBPKStuart-Harrisetal.(2000) 10.52 23.99
Lötschetal.(2002) 7.17 6.99
Osborneetal.(1990) 8.77 11.01
Stanskyetal.(1978) 2.50
1.60
Tabella3.12Sonoriportatiivaloridell’indicediperformancedelmodelloPBPKedelmodelloaquattrocompartimentiperilmetabolitaM6G.
AUC%modelloaquattro
compartimentiAUC%modello
PBPKStuart-Harrisetal.(2000) 14.52 6.68

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
96
Lötschetal.(2002) 37.33 12.43
Osborneetal.(1990) 5.33 14.32
Per poter ritenere il modello affidabile si è assunto che il massimo valore che può
assumerel’indicediperformanceè30:questolimiteèsemprerispettatoadeccezione
dell’indicedeimetabolitidelmodelloaquattrocompartimentinellostudiodiLötschet
al..(1990).
Si possono ritenere entrambi imodelli sufficientemente accurati, anche se ilmodello
PBPK è in gradodi prevedere conmaggiore precisione il picco iniziale raggiuntodalla
morfina nel plasma e i valori di concentrazione di questa nei primi istanti successivi
all’infusione.
Pertanto,nonostantealmodelloPBPKsianoassociaticosticomputazionalipiùelevati,dal
momentocheilsistemadiequazionididifferenzialidarisolvereèpiùcomplesso,questi
sirivelaunostrumento,rispettoalmodelloaquattrocompartimenti,piùcompletoper
prevederelaconcentrazionedimorfinaedelsuometabolitaM6Gnelcorpoumano.
3.6 Osservazionisull’ottimizzazione
Comevistoneiparagrafiprecedenti lafunzioneobiettivochesièdecisominimizzareè
l’equazione(7).Tuttavia,laformainizialedellafunzioneobiettivoeradiversa:
exp model exp model, , , ,
1exp model exp model, 6 , 6 , 6 , 6
1
(| | | max( ) max( ) |
(| | | max( ) max( ) |
Ni mor i mor i mor i mor
obji
Mi M G i M G i M G i M G
i
C C C Cf
NC C C C
M
=
=
- + -= +
- + -+
å
å (44)
La necessità di modificare l’espressione soprariportata è stata dettata dal fatto che i
risultati ottenuti non erano soddisfacenti, in particolare a basse concentrazioni sia il
modelloaquattrocompartimenticheilmodelloPBPKnoneranoingradodiprevedere
con sufficiente accuratezza l’andamentodellemisure sperimentali delmetabolita. Per
poterdarepiùpesoaquestidatiall’internodella funzioneobiettivosièdecisodinon

Modellofarmacocineticodellamorfinanegliuomini
97
valutare la semplice sommadeidueaddendi che la compongono,bensì la sommadei
logaritmidiquestidue.
Da ora in poi, per semplicità, con il termine ottimizzazione logaritmica ci si riferirà
all’ottimizzazionecheminimizzalafunzioneobiettivoriportataineq.44perl’altrocasosi
useràiltermineottimizzazionestandard.
Neiparagrafiseguentiverrannoriportatiirisultatiottenuticoniduemetodidifferenti.
3.6.1 ConfrontodeirisultatidelmodelloaquattrocompartimentiperlostudiodiStuart-Harrisetal.(2000)
InFig.3.13è riportato il confronto tra i risultatiottenutiminimizzando ledue funzioni
obiettivoperlostudiodiStuart-Harrisetal.(2000).
Figura3.13Risultatidelmodellotricompartimentaleottenuticonlafunzioneobiettivologaritmica(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
98
3.6.2 ConfrontodeirisultatidelmodelloaquattrocompartimentiperlostudioLötschetal.(2002)
SiriportanoinFig.3.14irisultatiottenutiminimizzandoleduefunzioniobiettivoperlo
studiodiLötschetal.(2002).
Figura3.14Risultatidelmodellotricompartimentaleottenuticonlafunzioneobiettivologaritmica(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).
3.6.3 ConfrontodeirisultatidelmodelloaquattrocompartimentiperlostudiodiOsborneetal.(1990)
InFig.3.15èriportatoilconfrontotrairisultatiottenuticonlaminimizzazionedelledue
funzioniobiettivoperlostudiodiOsborneetal.(1990).

Modellofarmacocineticodellamorfinanegliuomini
99
Figura3.15Risultatidelmodellotricompartimentaleottenuticonlafunzioneobiettivologaritmica(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).
3.6.4 ConfrontodeirisultatidelmodelloaquattrocompartimentiperlostudioStanskyetal.(1978)
In Fig.3.16 è riportato il confronto tra i risultati ottenuti dall’ottimizzazione delle due
funzioniobiettivoperlostudiodiStanskyetal.(1978).
Figura3.16Risultatidelmodellotricompartimentaleottenuticonlafunzioneobiettivologaritmica
(colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
100
3.6.5 ConfrontodeirisultatidelmodelloPBPKperlostudiodiStuart-Harrisetal.(2000)
SiriportanoinFig.3.17irisultatiottenutiminimizzandoleduefunzioniobiettivoperlo
studiodiStuart-Harrisetal.(2000).
Figura 3.17 Risultati delmodello PBPK ottenuti con la funzione obiettivo logaritmica (colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).
3.6.6 ConfrontodeirisultatidelmodelloPBPKperlostudiodiLötschetal.(2002)
SiriportanoinFig.3.18irisultatiottenutiminimizzandoleduefunzioniobiettivoperlo
studiodiLötschetal.(2002).

Modellofarmacocineticodellamorfinanegliuomini
101
Figura 3.18 Risultati delmodello PBPK ottenuti con la funzione obiettivo logaritmica (colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).
3.6.7 ConfrontodeirisultatidelmodelloPBPKperlostudiodiOsborneetal.(1990)
InFig.3.19èriportatoilconfrontotrairisultatiottenuticonlaminimizzazionedelledue
funzioniobiettivoperlostudiodiOsborneetal.(1990).

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
102
Figura 3.19 Risultati delmodello PBPK ottenuti con la funzione obiettivo logaritmica (colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).
3.6.8 ConfrontodeirisultatidelmodelloPBPKperlostudiodiStanskyetal.(1978)
In Fig.3.20 è riportato il confronto tra i risultati ottenuti ottimizzando le due funzioni
obiettivoperlostudiodiStanskyetal.(1978).
Figura 3.20 Risultati delmodello PBPK ottenuti con la funzione obiettivo logaritmica (colonnasinistra);risultaticonlafunzioneobiettivostandard(colonnadestra).
3.6.9 Discussionedeirisultati
Dai risultati riportati nei paragrafi precedenti, utilizzando i parametri ottenuti con
l’ottimizzazionelogaritmica,sipuòsubitonotareungeneralemiglioramentodeigrafici,
siadellamorfinachedelsuometabolita,M6G.

Modellofarmacocineticodellamorfinanegliuomini
103
Tuttaviaancheinquestocasoappareopportunoutilizzarel’indicediperformanceprima
descrittoperpoterdisporrediunvalorequantitativodelmiglioramentoeffettivamente
conseguito.
Nelletabellesuccessivesiriportanoivaloridell’indicediperformanceperciascunostudio
eperciascunmetododiottimizzazioneutilizzato,vedasiTab.3.13,Tab.3.14,Tab.3.15e
Tab.3.16.
Tabella3.13Indicediperformancedelmodelloaquattrocompartimentiperlamorfinaottenutiutilizzandoilmetododiottimizzazionelogaritmicoequellostandard.
AUC%modelloaquattro
compartimenticon
ottimizzazionelogaritmica
AUC%modelloaquattro
compartimenticon
ottimizzazionestandardStuart-Harrisetal.(2000) 10.52 28.42
Lötschetal.(2002) 7.17 52.13
Osborneetal.(1990) 8.77 44.31
Stanskyetal.(1978) 2.5 45.60
Tabella3.14IndicediperformancedelmodelloaquattrocompartimentiperilmetabolitaM6Gottenutiutilizzandoilmetododiottimizzazionelogaritmicoequellostandard.
AUC%modelloaquattro
compartimenticon
ottimizzazionelogaritmica
AUC%modelloaquattro
compartimenticon
ottimizzazionestandardStuart-Harrisetal.(2000) 14.52 17.53
Lötschetal.(2002) 37.33 9.65
Osborneetal.(1990) 5.33 20.12

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
104
Tabella3.15Sonoriportati i valoridell’indicediperformancedelmodelloPBPKper lamorfinaottenutiutilizzandoilmetododiottimizzazionelogaritmicoequellostandard.
AUC%modelloPBPKcon
ottimizzazionelogaritmicaAUC%modelloPBPKcon
ottimizzazionestandardStuart-Harrisetal.(2000) 23.99 43.91
Lötschetal.(2002) 6.99 17.59
Osborneetal.(1990) 11.01 42.47
Stanskyetal.(1978) 1.60 20.66
Tabella3.16Sonoriportatiivaloridell’indicediperformancedelmodelloPBPKperilmetabolitaM6Gottenutiutilizzandoilmetododiottimizzazionelogaritmicoequellostandard.
AUC%modelloPBPKcon
ottimizzazionelogaritmicaAUC%modelloPBPKcon
ottimizzazionestandardStuart-Harrisetal.(2000) 6.68 15.66
Lötschetal.(2002) 12.43 15.28
Osborneetal.(1990) 14.32 22.43
Dai risultati riportati nelle tabelle precedenti si vogliono evidenziare i notevoli
miglioramenti nell’indice di performance a seguito dell’utilizzo dei parametri ottenuti
tramiteottimizzazionelogaritmica.
L’indicediperformancerisultadiminuitointuttiicasiconsiderati,adeccezionedell’indice
di performancedelmodello a quattro compartimenti ottenuto per ilmetabolitaM6G
nellostudiodiLötschetal.(2002).
Quando si utilizzano i parametri ottenuti attraverso l’ottimizzazione standard le
concentrazioni diM6G emorfina decresconomolto velocemente. Ciò comporta che i
modelliaquattrocompartimentiePBPKdai200mininpoinonriescanopiùaprevedere
in maniera corretta la concentrazione delle due specie. Al contrario, utilizzando
l’ottimizzazione logaritmicasi risolvequestoproblemaedaciòconsegueunamigliore
concordanzafradatisperimentaliemodello.

Modellofarmacocineticodellamorfinanegliuomini
105

106
4 Analisidisensitivitàparametrica
Comesièpotutoconstatare,inciascunodeimodellipresentatiinprecedenza,siainquelli
relativiai ratti che inquelli relativiagliumani,appaionodiversi termini chesonostati
ottenutiattraversounaregressione.Risulta,quindi,evidentecheilvaloreditaliparametri
non sia basato su aspetti anatomico/fisiologici dell’individuo, bensì sia frutto di una
procedura matematica. A valle di queste considerazioni, appare interessante
approfondire come la perturbazione di ciascuno di questi parametri influenzi l’intero
modello.L’analisidisensitivitàèappuntofinalizzataaquestoscopo.
4.1 Metodidianalisidisensitività
L’analisidisensitivitàinvestigalarelazionecheesistefraiparametriincertidelmodelloe
lavariazionedellarispostadelmodellostesso(Charynskaetal.,2012).Imetodipiùdiffusi
pereffettuarlasonodue:
• Analisidisensitivitàlocale;
• Analisidisensitivitàglobale.
4.1.1 Analisidisensitivitàlocale
Ilmetodopiùutilizzatoperdeterminarelasensitivitàdiunmodelloèquellodivalutarela
derivata parziale dei singoli risultati (e.g., il valore della concentrazione di un
compartimento)rispettoaciascunodeisuoiparametri.Inquestostudio,laderivatanon
èstatacalcolataanaliticamentemasièsfruttatol’approssimazionealledifferenzefinite.
Così facendo si introduce un leggero errore in quanto tale procedura prevede
un’approssimazionedicalcolo,maallostessotempopermetteunariduzionesignificativa
delcostocomputazionale.Perapprossimareladerivataprimasièoptatoperladifferenza
inavanti:
( ) ( )i i j j i j
j j
C C k k C kk k¶ + D -¶ D
(45)

Analisidisensitivitàparametrica
107
Laderivatacosìcalcolataprendeilnomedi“coefficientedisensitività”.Cirappresentala
concentrazioneall’uscitadelcompartimentoi-esimo,mentrekjraffigurailparametroj-
esimo.AssumendounincrementodelparametroDkjsufficientementepiccolo,ilvalore
chesiottienesiavvicinamoltoaquellochesideterminerebbecalcolandoanaliticamente
laderivata.Laproceduracheconsentedivalutarel’analisidisensitivitàalvariarediun
singolaparametroallavoltaprendeilnomedi“metodolocale”.Questoèilsistemache
viene maggiormente usato in campo scientifico (Charynska et al., 2012). A questo si
contrapponeilmetodoglobale,descrittonelprossimoparagrafo.
4.1.2 Analisidisensitivitàglobale
Ilmetodoglobaleèunaproceduraperilcalcolodell’analisidisensitivitàchepermettedi
valutarecomeilsistemarispondaallavariazionedipiùparametricontemporaneamente.
Ciò consente di analizzare come tali parametri interagiscano tra loro, fornendo di
conseguenzainformazionirelativeadun’eventualedipendenzachepossaintercorreretra
levariabiliincerte.Unostudiodelgenere,però,comportaelevaticosticomputazionali,in
quanto lavariazionecontemporaneadi tutti iparametrideterminaun incrementodel
numerodisimulazioninecessarie.Alnettodiquesteconsiderazionisièdecisodiutilizzare
ilmetodolocale,che,conbassicosticomputazionali,permettediottenerebuonirisultati.
4.2 Costruzionedellamatricedisensitività
Ilprimopassoperpotercostruirelamatricedisensitivitàèquellodirisolvereilsistema
ODE,utilizzandoiparametrinonperturbati.Successivamenteènecessariorisolvereun
sistemaperogniparametroperturbato.Quindiseiparametrichesivoglionoanalizzare
sono j, si avranno j + 1 sistemi ODE da risolvere sequenzialmente: j saranno quelli
perturbatiel’ultimoèquelloconivalorioriginalideiparametri.L’incrementoutilizzato
nonècostanteperogniparametrokj,madipendedalvaloredelparametrostesso:
| |j jk eps kD = (46)
Èmolto importante che l’incrementoDkj sia opportunamente piccolo, affinché venga
minimizzato l’errore derivante dal calcolo numerico della derivata. A questo scopo si

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
108
moltiplicalaradicequadratadelmachepsperilvaloreassolutodelparametropresoin
considerazione, in modo da ottenere un numero sufficientemente piccolo e sempre
positivo(datocheiparametriconsideratisonosemprecomunquediversidazeroeperciò
non è necessario aggiungere un incremento assoluto per ovviare al rischio di
perturbazione nulla). Per ogni istante temporale e per ogni parametro perturbato è
possibilecalcolareuncoefficientedisensitivitàperciascuncompartimento.Siricavauna
matrice tridimensionale che, per come è stato deciso di costruirla, ha la seguente
struttura:M = [t, i, j],dovetrappresentagliistantitemporalipresiinconsiderazione,iil
valoredellaconcentrazionealtempot-esimoejilparametrocheèstatoperturbato.Per
ridurre i costi computazionali non sono stati presi in considerazione tutti gli istanti
temporali,ma,solo,quellipiùsignificativi.
4.2.1 Normalizzazionedellamatricedisensitività
La matrice di sensitività così costruita ha di per sé poco significato. Questa, infatti,
contiene al suo interno i coefficienti di sensitività di ciascun compartimento che non
possonoessereconfrontati,avendoordinidigrandezzadiversitraloro.Perpoterrendere
talivaloricomparabili,èutilenormalizzarla.Infatti,lanormalizzazioneèparticolarmente
importanteper imodelli incui iparametri investigatidifferiscanosignificativamentein
terminidiordinedi grandezza. Si costruisce,dunque,unanuovamatricedi sensitività
normalizzataS.La letteraturascientificaproponediversimetodidinormalizzazione.Di
seguitoelenchiamoitremetodipiùutilizzati(Charynskaetal.,2012):
1) Il primo metodo prevede che la matrice di sensitività sia moltiplicata per il
rapportotrailvaloredelparametrononincrementatoedilvalorepuntualedella
concentrazione,ottenutodalsistemadiequazioniconiparametrinonperturbati.
Iterminichecostituisconolamatricedisensitivitànormalizzata,avranno,dunque,
laseguenteforma:
( , , ) i j
j i
C kS t i jk C¶
=¶
(47)

Analisidisensitivitàparametrica
109
2) Ladebolezzadelprocedimentoappenadescrittostanel fattoche inuovivalori
ottenuti abbiano un’elevata dipendenza dalla concentrazione puntuale. Per
ovviareaquestotipodiproblema,anzichédividereilparametrokjperilvaloreCi
della concentrazione del compartimento considerato nell’istante t, lo si può
dividereperilvaloremediodellaconcentrazionediquelcompartimentoi-esimo
lungotuttol’intervalloditempo:
,
( , , ) i j
j i av
C kS t i jk C¶
=¶
(48)
3) Quando anche i parametri delmodello variano nel tempo, per normalizzare il
coefficientedisensitivitàsipuòutilizzareilrapportotralavarianzadelparametro
equelladellaconcentrazione.Questometodononèapplicabilealnostrocaso.
( )( , , )( )
i j
j i
C kS t i jk Css
¶=¶
(49)
Perlacostruzionedellamatricedisensibilità,èstatodecisodiutilizzareilsecondometodo
dinormalizzazione.È interessanteosservarecomelamatricenonnormalizzatanonsia
altroche lamatrice jacobiana“dinamica”delleequazionipresentinelmodello.Lasiè
definita “dinamica” perché i valori contenuti cambiano per ogni istante temporale
consideratonell’analisi.
4.3 Risultatidell’analisidisensitività
Iseguentiparagrafiillustranoirisultatidell’analisidisensitivitàcondottasu:
1) Modellotricompartimentalerelativoairatti;
2) Modelloaquattrocompartimentiumano;
3) ModelloPBPKrelativoairatti;
4) ModelloPBPKumano;
Per tutte le analisi si è deciso di considerare tre istanti temporali: 5, 60 e 200 min
dall’infusione,checorrispondonorispettivamenteadalte,medieebasseconcentrazioni

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
110
di morfina e suo metabolita principale, M6G. Per ciascun parametro perturbato si è
stabilito di strutturare un istogramma a barre orizzontali che riporti sull’asse delle
ordinateilcompartimentoincuièmisuratalavariazionediconcentrazioneeinascissa
l’intensitàditalevariazionenormalizzata.
4.3.1 Analisidisensitivitàdelmodellotricompartimentaledeiratti
In Fig. 4.1 sono riportati i risultati dell’analisi di sensitività condotta sul modello
tricompartimentaledeiratti.Ognigraficorappresentaunparametroperturbato.

Analisidisensitivitàparametrica
111
Figura4.1Iparametriperturbatisonosei:k10,k12,k21,Pact,PdiffePactiveIN.Perognicompartimentoci sono tre differenti barre colorate, che rappresentano i diversi istanti temporali: il blurappresenta5min,ilverde60mineilgiallo200min.ANorddiciascunaimmagineèriportatoilparametrocheèstatoperturbato,sull’asseysihannoidiversicompartimentiesull’assexilvaloredell’indicedisensitività.
4.3.2 AnalisidisensitivitàdelmodelloPBPKdeiratti
InFig.4.2sonoillustratiirisultatiottenutiperilmodelloPBPKdeiratti.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
112

Analisidisensitivitàparametrica
113
Figura4.2Iparametriperturbatisonododici:k12,k21,k13k31,jlp,jpl,effH,effK,CLlil,Pact,PdiffePActiveIN.Perognicompartimentocisonotredifferentibarrecolorate,cherappresentanoidiversiistantitemporali:ilblurappresenta5min,ilverde60mineilgiallo200min.ANorddiciascunaimmagineè riportato il parametro cheè statoperturbato, sull’asse y si hanno i diversi compartimenti esull’assexilvaloredell’indicedisensitività.
4.3.3 Analisidisensitivitàdelmodelloaquattrocompartimentiumano
InFig.4.3èpossibilevedereirisultatiottenutiperilmodelloaquattocompartimentiper
l’uomo.

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
114
Figura 4.3 I parametri perturbati sono otto: k10, k12, k21, k40, kcin, Pact, Pdiff e PActiveIN. Per ognicompartimentocisonotredifferentibarrecolorate,cherappresentanoidiversiistantitemporali:ilblurappresenta5min,ilverde60mineilgiallo200min.ANorddiciascunaimmagineèriportatoilparametrocheèstatoperturbato,sull’asseysihanno idiversicompartimentiesull’assex ilvaloredell’indicedisensitività.
4.3.4 AnalisidisensitivitàdelmodelloPBPKumano
Infine,vengonoriportatiirisultatiottenutiperilmodelloPBPKumano(Fig.4.4).

Analisidisensitivitàparametrica
115

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
116

Analisidisensitivitàparametrica
117
Figura4.4Iparametriperturbatisonoquattordici:k12,k21,k13k31,jlp, jpl,effH,effK,CLlil,Pact,Pdiff,PActiveIN,kcinek40.Perognicompartimentocisonotredifferentibarrecolorate,cherappresentanoidiversiistantitemporali:ilblurappresenta5min,ilverde60mineilgiallo200min.ANorddiciascunaimmagineèriportatoilparametrocheèstatoperturbato,sull’asseysihannoidiversicompartimentiesull’assexilvaloredell’indicedisensitività.
4.4 Commentodeirisultati
Prima di analizzare nel dettaglio ogni singolo caso, risulta interessante illustrare un
commento generale riguardo al significato dei risultati ottenuti. Il segno dell’indice di
sensitivitàpermettedicapireselaperturbazionedelparametrocomportiunaumentoo
unadiminuzionedellaconcentrazione:nelcasodisegnonegativo,incorrispondenzadi
unincrementodelparametroconsegueunadiminuzionedellaconcentrazione,viceversa
nelcasodisegnopositivosihaunaumentodellaconcentrazione.
4.4.1 Modellotricompartimentaleperiratti
Inquestomodelloiparametrianalizzatisonosei.k10identifical’unicaviadieliminazione
delmodello, comesuggerisce la logica,unaumentodiquestoparametrocomporta la
diminuzione delle concentrazioni di morfina all’interno dei diversi compartimenti.
Quest’ultimirisultanotuttisensibiliallavariazionedik10,anchesenoninegualmisura:in
particolaredopo60min, il compartimentodelcervelloèquellochemostradifferenze
maggiori.Quindiamediedosisihannolevariazionimaggiori.k12ek21hannoandamenti
moltosimilimaconsegnicontrari,questoeraprevedibileperchéessihannosignificato
opposto:ilprimoidentificaun’uscitadalcompartimentocentraleeilsecondoun’entrata
inquest’ultimo.Adaltedosi,ossiadopo5min,icompartimentipiùsensibilisonoquello

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
118
centraleeilcervello.Amedieeabassedosiilcompartimentodegliorganipocoperfusi
risulta maggiormente influenzato, inoltre per quello centrale e per il cervello si ha
un’inversionedisegnorispettoallealtedosi.Quest’ultimocomportamentopuòessere
spiegatodalfattocheaseguitodiunaumentok12,siassisteadun’uscitamaggioredal
compartimentocentraleversoquellodegliorganipocoperfusineiprimiistantiditempo.
Questocomportachenegli istantidi temposuccessivi siaabbiaunaconcentrazionedi
morfinamaggiorenelcompartimentodegliorganipocoperfusi,rispettoalcasoincuinon
c’erastatalaperturbazionedelparametro.Andandoavantineltempoquestoconducead
avereunaconcentrazionedimorfinamaggiorenelcompartimentocentrale,rispettoal
casosenzak12perturbato,perchéilflussoinuscitadalcompartimentodegliorganipoco
perfusi è più elevato. Il compartimento del cervello segue l’andamento del
compartimento centrale. Ragionando al contrario, si possono trarre le medesime
conclusioniperk21.Infineiparametricheriguardanoloscambioconilcervello(Pact,Pdiff,
PActiveIN), se perturbati, modificano significativamente solo tale compartimento e in
particolareadalteconcentrazioni.
4.4.2 ModelloPBPKperiratti
I parametri presi in considerazione in questo caso sono dodici. k12, k21 e CLlil sono i
parametrilacuivariazioneinfluenzamenoilmodello.Infatti,comeillustratoinFig.4.5,gli
indici di sensitività sono diversi ordini di grandezza inferiori rispetto a quelli ottenuti
perturbandoglialtriparametri.

Analisidisensitivitàparametrica
119
Figura4.5Dettagliodeigraficiottenutidallaperturbazionedik12,k21eCLlil,sievidenziachegliindicidisensitivitàsonofinoaquattoordinidigrandezzapiùpiccolidiquelliottenutidaglialtriparametri.
A seguito di questa osservazione, si può arrivare alla conclusione che una piccola
variazione di questi tre parametri non comporti alcuna variazione significativa della
previsioneprodottadalmodelloPBPK.Aumentandoilparametrok13tuttiicompartimenti
risultanoinfluenzati,inparticolarenegliistantiditempo5e60min.Gliindicidisensibilità
sononegativipertuttiicompartimentiadeccezionediquellodegliorganimoltoperfusi.
Essendok13unparametrocheregolaloscambiocongliorganimoltoperfusiche,quindi,
sonoraggiuntidaun’elevataportatadisangue,afrontediunasuavariazioneènormale
osservare un cambiamento della risposta di tutti i compartimenti che compongono il
modello. Aumentando il valore di k13, infatti, aumenta il passaggio di morfina dal
compartimentoplasmaaquellodegliorganimoltoperfusidasangue,aciòconsegueche
la morfina disponibile per gli altri compartimenti è inferiore rispetto al caso con
parametro non perturbato. Le stesse considerazioni valgono, a segni invertiti, per il
parametrok31.Perquantoriguardaiparametrijlpejpl,èpossibileosservarechequasitutti
icompartimentirisultanosensibiliallaloroperturbazione,inparticolarequellodelGICS.
Ilcompartimentodegliorganipocoperfusimostra,inentrambiicasi,unavariazionenella
risposta trascurabileallaperturbazionediquestidueparametri.Adun incrementodei
parametrieffHedeffK,chesonocoinvoltinell’eliminazionedellamorfina,consegueuna
diminuzione della concentrazione di quest’ultima in ciascun compartimento. Questo
effettoèparticolarmenteosservabileabasseconcentrazioni.Infineperiparametriche
regolano gli scambi con il cervello (Pact, Pdiff e PActiveIN), solo il compartimento che

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
120
rappresenta quest’ultimo risulta sensibile in maniera significativa a una loro
perturbazione.
4.4.3 Modelloaquattrocompartimentipergliumani
Come si è visto nel capitolo precedente, in questo modello è stato introdotto un
compartimentocheregolalaformazioneel’eliminazionedelmetabolitaM6G.Levariabili
incertesonootto.k10èl’unicoparametrocheregolal’eliminazionedellamorfina,eun
suo incremento conduce ad una diminuzione della morfina in tutti i compartimenti.
Questoeffettoèparticolarmentemarcatoabasseconcentrazioni.Unaperturbazionedel
parametro k12modifica inmaniera significativa la risposta di tutti i compartimenti. In
particolare,laconcentrazionenelcompartimentoorganipocoperfusirisultaaumentata
intuttietregliistantiditempoconsiderati.Perquantoriguardaglialtricompartimenti,
al variare di k12 la concentrazione di morfina diminuisce per poi aumentare a basse
concentrazioni.Questopuòessere spiegato con lemedesime considerazioni che sono
state condotte per k12 nel modello tricompartimentale dei ratti. I compartimenti del
metabolitaedelcervelloseguonoilcomportamentodelplasma.Lavariazionedik21ha
conseguenzespeculariaquelledik12.UnincrementodiKcin,cheregolalaformazionedel
metabolitaM6G,comportaunaumentodella concentrazionediquest’ultimoperogni
istanteditempoconsiderato.L’effettocontrarioèvisibileperleconcentrazionideglialtri
compartimenti.Perquantoconcernelaperturbazionedelparametrok40,chepermette
l’eliminazionedelM6G,sipuònotarechel’unicocompartimentocherisultisensibilea
questavariazioneèproprioquellodelmetabolita.Questocomportamentoèquelloche
cisipotevaaspettare,poichétaleparametrodieliminazioneapparesolonell’equazione
delcompartimentodelmetabolita.Infine,periparametricheregolanogliscambiconil
compartimentocervello,ossiaPdiff,PactePActiveIN,aduna loroperturbazionesegueuna
variazionedellarispostadelsolocompartimentocervello.
4.4.4 ModelloPBPKpergliumani
Inquestomodelloiparametrisonoquattordici,erispettoalPBPKdeirattiabbiamoun
compartimentoinpiùeduenuovevariabiliincerte.Qui,unincrementodik12hauneffetto
significativosolosulcompartimentoorganipocoperfusi,inparticolarelaconcentrazione

Analisidisensitivitàparametrica
121
dimorfinaaumentaneitreistantiditempoconsiderati,questoeffettoèparticolarmente
visibileadalteconcentrazioni.Taliconsiderazionivalgonoinmanieraspeculareperk21,e
quindi,perciascuncompartimento,all’aumentodellaconcentrazioneperlavariazionedi
k12,corrisponderàunadiminuzionedovutaallavariazionedik21.Nelcasodiperturbazione
dik13ek31,sihannoandamentichepossonoessereconsideratispeculari.Glieffettidella
variazione dei parametri sono avvertiti inmaniera diffusa su tutti i compartimenti, in
particolaredalcompartimentodegliorganimoltoperfusiedaquellodelmetabolitaM6G.
Lavariazionedik40,comenelcasoaquattrocompartimenti,influenzasignificativamente
sololaconcentrazionedelmetabolita.Ciòèspiegabilefacilmenteconilfattochequesto
parametroapparesolonell’equazionedell’M6G.Alcontrario,un incrementodiKcinha
effettisututtiicompartimenti:laconcentrazionedelmetabolitaaumentaintuttietregli
istanti di tempo considerati, mentre la concentrazione di morfina negli altri
compartimenti decresce. Dal momento che insieme a Kcin aumenta la formazione di
metabolitaechelareazioneèirreversibile,aumentandonelavelocitàlaconcentrazione
di morfina disponibile nei vari compartimenti diminuisce. Anche per jpl e jlp si hanno
andamentichepossonoesseredefinitispeculari.Tuttiicompartimentirisultanosensibili
allavariazionedi taliparametri, inparticolare il compartimentoGICS. I compartimenti
risultano poco sensibili ad una perturbazione dei parametri effH ed effK, coinvolti
nell’eliminazionedellamorfina.Icoefficientidisensitivitàottenutidallaperturbazionedi
CLlil sono diversi ordini di grandezza inferiori (Fig.4.6) a quelli ottenuti per gli altri
parametri,el’interomodelloèpocosensibileallasuaperturbazione.
Figura 4.6 Sono riportati in dettaglio i valori degli indici di sensitività ottenuti perturbando ilparametroCLlil,sipuònotarechesonodiversiordinidigrandezzainferioririspettoaquellideglialtriparametri

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
122
Per quanto riguarda i parametri di scambio con il cervello, valgono le medesime
considerazionifatteperglialtrimodelli:adunaloroperturbazionesoloilcompartimento
cervellorisultasignificativamentesensibile.
4.5 Conclusioni
Avalledeicommentirelativiall’analisidisensitivitàdiciascunmodello,èpossibiletrarre
delleconclusioniriguardoaiparametriadattivi.Iparametricherisultanopiùcriticisono
quellilacuiperturbazionenoninfluenzasololeequazioniincuicompaionodirettamente,
maanchelerestantirelativeaglialtricompartimenti.Viè,infatti,uneffettoindirettodi
alcuni parametri sulle restanti equazioni, e quindi i relativi compartimenti, in cui non
compaionodirettamente (ma che condizionano tramite le variabili di integrazione). In
futuro sarà importante, per quanto possibile, sostituire i parametri adattivi con valori
individualizzatiperciascunsoggetto/paziente,inparticolaremodoperimodelliPBPK.Il
modello tricompartimentale dei ratti e quello a quattro compartimenti umano sono
difficilmenteindividualizzabili,perché,alcontrariodelmodelloPBPK,nonsonocostruiti
sullabasedellaanatomia/fisiologiadellaspecieconsiderata.
Sipossonoevidenziare,infine,ipuntiincomunetraiduemodelliPBPK:
1) I parametri Pdiff, Pact e PActiveIN influenzano in modo significativo solo il
compartimentodelcervello;
2) EssirisultanopocosensibiliaiparametriCLlil,k12ek21.
3) IparametripiùcriticiperimodelliPBPKsonok13,k31,jlpejpl.

Analisidisensitivitàparametrica
123

124
5 Conclusioniesviluppifuturi
AvalledelleanalisisuimodellifarmacocineticiillustratineiCapitoli2e3,edell’analisidi
sensitivitàsvoltanelCapitolo4,èlecitotrarreledovuteconclusioni.
Lo scopodiquesta tesieraquellodi costruireunmodello farmacocinetico ingradodi
simulare lo scambio tra il sangue e il cervello dei farmaci iniettati endovena, nello
specificodellamorfina,unpotenteanalgesico.Questostudioèstatocondottosuiratti,
partendodaunmodellopiùsempliceatrecompartimentiperarrivareinseguitoadun
modello PBPK a sette compartimenti in grado di fornire informazioni più dettagliate.
Successivamente, consapevoli della possibilità di poter applicare lo stesso modello
farmacocinetico sia ai ratti che alla specie umana, si è andato ad indagare il
comportamento dellamorfina negli uomini, approfondendo il discorso con l’aggiunta
dell’analisi del metabolita M6G della morfina, dato il suo potente effetto analgesico
addiritturasuperioreaquellodellamorfinastessa.Pertanto,nelcasodegliumani,èstato
aggiunto a ciascunmodello un compartimento, ottenendo così unmodello a quattro
compartimentieunmodelloPBPKaottocompartimenti.
DalpuntodivistadellafarmacocineticadeifarmacinelSistemaNervosoCentrale,questo
lavorosivaadaggiungereaimodellifarmacocineticigiàesistenti,conlacaratteristicadi
esseredaunapartesemplicedalpuntodivistamatematico,conuncostocomputazionale
basso in quanto composto da un sistema di equazioni differenziali ordinarie con
condizioniinizialichevadatreasetteperilmodellosuirattiodaquattroaottoperil
modellosugliumani,dall’altramoltovicinoalladescrizioneanatomico/fisiologicadegli
scambimaterialinelcorpodirattieumani.
Nelcorsodelleanalisideimodellicostruiti,sièpotutoconstatarecome,conunleggero
incrementodelcostocomputazionale,sisiapassatidaunmodelloatreadunoasette
compartimentinelcasodeiratti,edaunoaquattroadunoaottonegliumani,ingrado
diprevedereconmaggioreaccuratezzaidatisperimentali:questoèquantoemergedai
confrontidelleAUCpercentualicondottineiCapitoli2e3.

Conclusioniesviluppifuturi
125
UnmodelloPBPKpresenteinletteraturachesiavvicinamoltoalmodelloPBPKperiratti
realizzatoinquestolavoroèquellopropostodaBalletal.(2012).Nellorostudioviene
presentatounmodelloPBPK,incuilamorfinavienesomministrataviaendovenaneiratti,
basato su tredici compartimenti. Come in questo studio, anche in Ball et al. (2012) il
cervello è stato descritto tramite un compartimento denominato brain vasculature,
contenente il plasma che scambia col cervello, ed uno denominato brain tissue che
rappresentaitessutidelcervello.Allostessomodo,iltrasportodeifarmacialcervelloè
regolatodauncoefficienteditrasportopassivolegatoalladiffusioneedueportate,una
iningressoeunainuscita,perdescrivereiltrasportoattivo.Laprincipaledifferenzatrail
lavorodiBalletal.(2012)eilpresentelavoroditesirisiedenelnumerodicompartimenti
dacuiècompostoilmodello.InBalletal.(2012)sonopresentiduecompartimentiper
rappresentareilplasma,dividendoloinplasmavenosoeplasmaarterioso.Inoltre,nello
studiodiBalletal. (2012), sonoesplicitati tutti gliorganie i tessuti che,nelpresente
lavoro,sonostatiraggruppatiopportunamenteneicompartimentidegliorganietessuti
poco perfusi e molto perfusi. La scelta di raggruppare più organi in un unico
compartimento è stata dettata dalla volontà di avere unmodello dettagliatoma allo
stessotemposemplice,inoltrequestohapermessodiridurreigradidilibertàdelmodello.
LoscopodelmodelloPBPKperirattirealizzatoinquestolavoroditesirimanequellodi
esserequantopiùsemplicepossibile,eallostessotempoquellodiriuscireaprevedere
conunabuonaaccuratezzailprofilodiconcentrazionedelfarmaconelcervello.
Ungrossolimite,cheavrebbepermessodiestendereanchealmodellopergliumanile
informazioni ricavate dal modello per i ratti sul trasporto dei farmaci al cervello, è
l’assenzadimisuresperimentalidiconcentrazionenelcervellodellaspecieumana.Infatti,
ilmodellorealizzatopergliuominipotràritenersicompletamenteconvalidato,quandosi
potranno sfruttare dellemisure sperimentali che consentano di regredire i parametri
delloscambiodifarmacitraplasmaecervelloodeicoefficientidiscale-upopportuniper
adattareiparametriidentificatiperirattiagliumani.Ciòpermetteràdiprevedereanche
la concentrazione del farmaco nel cervello umano. Il passo successivo sarà quello di
implementareilmodelloPBPKalfinediapprofondirecomeavvieneladistribuzionedel
metabolitaM6Gintuttoilcorpo,compresoilcervello.Ciòsarebbedecisamenteutilein

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
126
quanto consentirebbe di tenere sotto controllo il principale responsabile dell’effetto
analgesicodellamorfina,cioèilmetabolitaM6G.Allostatoattuale,inmancanzadidati
sperimentaliditalemetabolitanelcervello,nonsièancora ingradodiconvalidareun
modellocosìdettagliato.
Imodellifarmacocineticibasatisullafisiologiadelpaziente(PBPK)sonounpotentemezzo
per losviluppodellamedicinapersonalizzata, ingradodivalutarescenariclinicimolto
complessisfruttandoleinformazionifisiologiche.Ledifferenzeanatomico/fisiologichetra
ipazientisononumeroseespessosignificative,comesipuòimmaginare.Partendodalla
semplice differenza di peso, arrivando fino alla differenza etnia, passando per la
differenzadisesso,età,esalute.Comeosservato,imodellipresentatiinquestolavorodi
tesi tengono sicuramente conto delle differenze di peso dei pazienti, caratteristica
fondamentalesucuisonostatiindividualizzatituttiiparametrifisiologici.Relativamente
allamorfina,avendoadisposizione imodelli sviluppatipresso ilPolitecnicodiMilano,
sarebbe interessante arricchirli andandoad analizzare alcunedi queste caratteristiche
anatomico/fisiologiche.Inprimis,sarebbeopportunoconsiderareladipendenzadialcuni
parametridallaetàdelpaziente.Inparticolare,essendolamorfinamoltoutilizzataperil
trattamentodeidoloripostoperatorineineonatienonessendociancoraunarelazione
chiara tra concentrazione del farmaco e risposta analgesica da parte del neonato
(Andersonetal.,2014),risulterebbeinteressantecreareunmodellofarmacocineticoche
possaessereutilizzatoneipazientineiprimiannidivita.Perquantoriguardailmodello
realizzatosugliuomini, ipazientianalizzatineicasi studiopresidalla letteraturaerano
tuttiinetàadulta,quindicongliorganicompletamentesviluppati.Neineonatisiavrebbe
achefareconorganinonancoradeltuttomaturieconalcunefunzionalitànonancora
deltuttosviluppateedinoltreivolumisarebberodecisamentepiùpiccoli.Intabella5.1
sono schematizzate leprincipali caratteristiche chedifferenziano i neonati dagli adulti
nellarispostafarmacocineticaaseguitodell’assunzionediunfarmaco.

Conclusioniesviluppifuturi
127
Tabella 5.1 Principali proprietà fisiologiche dei neonati che differiscono dagli adulti, cheinfluenzanolafarmacocinetica.(Stephensonetal.,2005).
Neonatespharmacokinetics
SlowerGastroIntestinaladsorption,fasterIntraMuscularadsorption
Limitedproteinbinding
Immatureenzymes
LargerLiver/Bodyweightratioandhigherblood-brainbarrierpermeability
Immaturerenalfunction
Lecaratteristichepresentatefannocapirecheunapprocciobasatopuramentesuscale
up/down in funzione esclusivamente delle dimensioni degli organi, che in unmodello
farmacocineticoconsentirebbeditrasformareiparametripergliuominiinparametriper
i neonati, non sia l’approccio migliore per realizzare un modello farmacocinetico
personalizzatosuineonati.
Unostacoloallarealizzazionediquestomodelloperineonatièlascarsadisponibilitàdi
datisperimentali,dovutaaproblemieticilegatiaglistudisuquestacategoriadipazienti.
Allostessotempo,però,larealizzazionediunmodelloaffidabile,capacediprevederela
concentrazione del farmaco in un neonato e, più nello specifico nel suo cervello,
consentirebbeinfuturodiridurreilnumerodipazientipediatricinecessariallaricerca.
Studi recenti (Cepeda et al., 2001 e Nihms et al., 2012) hanno evidenziato come la
differenza della risposta, a seguito dalla somministrazione di morfina, possa essere
influenzata dalle differenze dei geni che codificano gli enzimi coinvolti nella
metabolizzazionedel farmacoe i recettorideglioppiacei.Ènotochetaligenipossono
variareasecondadell’etniadeipazienti.Glistudiosisonoarrivatiquindiallaconclusione
che la risposta farmacocineticadellamorfinadipendadalla razzadeipazienti, il che si
tramutaindiverserispostedeipazientialfarmaco.Inparticolare,èrisultatocheinativi
americani siano più suscettibili alla depressione respiratoria a seguito della
somministrazionedimorfinarispettoagliindividuicaucasici.SecondoCepedaetal.(2001)
questa differenzapotrebbe essere ricondotta alle dimensioni inferiori degli organi dei
nativiamericani,inparticolaredeipolmoni.Introducendoquesteinformazioniall’interno

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
128
del modello farmacocinetico, in futuro si riuscirebbe a raggiungere un livello di
individualizzazionedellacuramoltoelevato,aprendolastradaadunamedicinasempre
piùamisuradelpaziente.
Infine,riguardoimodellipropostiinquestolavoroditesi,unmiglioramentocheinfuturo
potrebbeessereapplicatoèlariduzionedeigradidi libertà(i.e.parametriadattivi)del
sistema di equazioni differenziali che lo compongono. Molti parametri di natura
anatomico/fisiologica, infatti, sono in realtà stati regrediti numericamente seppur
partendodavaloridiprimotentativoricavatidamisureinvitroriportateinletteratura.
Sarebbe un notevole passo in avanti se si riuscisse a determinare un valore specifico
attraverso studi sperimentali. In particolare, prendendo in considerazione il modello
farmacocineticoperiratti,sifariferimentoaicoefficientidiscambiotraplasmaecervello.
Glistudiosisistannomuovendoinquestadirezione,tentandodiriprodurreinlaboratorio
loscambiomaterialedeifarmaciattraversolaBEEefornireunvaloredipermeabilitàdella
membranaperciascunprincipioattivoagentesulSNC(Summerfieldetal.,2007).Così
facendo, si andrebbero ad assegnare alcuni dei parametri attualmente adattivi del
modello,minimizzandoilnumerofinalediparametrieffettivamentedaregredire.Tutto
ciòdovrebbeconferiremaggioreaffidabilitàe robustezzastrutturaleadunmodello in
gradodifornireimportantiinformazionicircailcontrollodellaconcentrazionedeifarmaci
nelcervello.

Conclusioniesviluppifuturi
129


131
Bibliografia
Abbiati,A.R.,Manca,D.,2015.Amodelingtoolforthepersonalizationofpharmacokinetic
predictions,Comp.andChem.Eng.,91,(2016)
Abbiati, A. R., Lamberti, G., Grassi, M., Trotta, F., Manca, D., 2014. Definition and
validation of a patient-individualized physiologically-based pharmacokinetic model,
Comp.andChem.Eng.,84,(2016)
Abbot,N.J.,Patabendige,A.A.K.,Dolman,D.,Yusof,S.,Begley,D.,2009.Structureand
functionoftheblood–brainbarrier,Neurob.ofDis.,37,(2010)
Alavijeh,M. S., Chishty,M.,Qaiser,M. Z., Palmer,A.M., 2005.DrugMetabolismand
Pharmacokinetics,theBlood-BrainBarrier,andCentralNervousSystemDrugDiscovery,
TheJour.ofAmer.Soc.forExp.Neur.,2,(2005)
Ball, K., Bouzom, F., Schermann, J.,Walther, B.,Declèves, X., 2012.Development of a
Physiologically Based PharmacokineticModel for the Rat Central Nervous System and
Determinationof anInVitro–InVivo ScalingMethodology for theBlood–BrainBarrier
PermeabilityofTwoTransporterSubstrates,MorphineandOxycodone,Jour.ofPharmac.
Sci.,10,(2012)
Ball,K.,Bouzom,F.,Schermann,J.,Walther,B.,Declèves,X.,2013.PhysiologicallyBased
PharmacokineticModellingofDrugPenetrationAcrosstheBlood–BrainBarrier—Towards
aMechanisticIVIVE-BasedApproach,TheAPPSJour.,4,(2013)
Bentz,J.,Tran,T.T.,Polli,J.W.,Ayrton,A.,Ellens,H.,2005.TheSteady-StateMichaelis–
Menten Analysis of P-Glycoprotein Mediated Transport Through a Confluent Cell
MonolayerCannotPredicttheCorrectMichaelisConstantKm,Pharma.Res.,10,(2005)
Born,G.V.R.,Cuatrecasas,P.,Arbor,A.,Herken,H.,1966.HandbookofExperimental
Pharmacology,EditorialBoard,Londra

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
132
Böstrom, E., Hammarlund-Udenaes, Simonsson, S. U. H., 2008. Blood–Brain Barrier
Transport Helps to Explain Discrepancies in In Vivo Potency between Oxycodone and
morphine,Anest.,108,(2008)
Bouw, R., Gårdmark, M., Hammarlund-Udenaes, M., 2000. Pharmacokinetic-
PharmacodynamicModellingofMorphineTransportAcrosstheBlood-BrainBarrierasa
CauseoftheAntinociceptiveEffectDelayinRats—AMicrodialysisStudy,Pharma.Res.,10,
(2000)
Bouw, R., Ederoth, P., Lundberg, J., Ungerstedt, U., Nordström, C.-H., Hammarlund-
Udenaes,M.,2001.Increasedblood–brainbarrierpermeabilityofmorphineinapatient
withseverebrainlesionsasdeterminedbymicrodialysis,Acta.Anaest.Scand,(2001)
Bouwmeester,N.J.,vandenAnker,J.N.,Hop,W.C.J.,Anand,K.J.S.,Tibboel,D.,2003.
Age-andtherapy-relatedeffectsonmorphinerequirementsandplasmaconcentrationsof
morphineanditsmetabolitesinpostoperativeinfants,Brit.Jour.ofAnaes.,90,(2003)
Brown, R. P., Delp, M. D., Lindstendt, S. L., Rhomberg, L. R., Beliles, R. P., 1997.
Physiological parameter values for phisiologically based pharmacokineticmodels,Tox.
andInd.Heal.,4,(1997)
Burns, J.,Weaver,D. F., 2004.AMathematicalModel forPredictionofDrugMolecule
DiffusionAcrosstheBlood-BrainBarrier,Exp.Neur.,31,(2004)
Cepeda,M.S.,Farrar,J.T.,Roa,J.H.,Boston,R.,Meng,Q.C.,Ruiz,F.,Carr,D.B.,Strom,
B.L.,2001.Ethnicityinflucensmorphinepharmacokineticsandpharmacodynamics,The
Americ.Soc.forClin.Pharmac.andTherap.,12,(2001)
Cicero, T. J., Nock, B., Meyer, E., 1997. Sex-Related Differences in Morphine’s
AntinociceptiveActivity:RelationshiptoSerumandBrainMorphineConcentrations,The
Jour.ofPharmac.andExp.Therap.,2,(1997)
Chay, P. C. W., Duffy, B. J., Walker, J. S., 1991. Pharmacokynetic-pharmacodynamic
relationshipsofmorphineinneonates,Pharmac.Ther.,51,(1992)

Bibliografia
133
Charzynska, A., Nalecz, A., Rybinski, M., Gambin, A., 2012. Sensitivity analysis of
mathematicalmodels of signaling pathways, Jour. of Biot., Comp. Biol. andBion., 93,
(2012)
Christrup,L.L.,1997.Morphinemetabolites,Act.Anaest.Scand.,41,(1997)
Collett,A.,Tanianis-Hughes,J.,Hallifax,D.,Warhurst,G.,2003.PredictingP-Glycoprotein
EffectsonOralAbsorption:CorrelationofTransportinCaco-2withDrugPharmacokinetics
inWild-Typeandmdr1a(−/−)MiceinVivo,Pharmac.Res.,5,(2004)
Coughtrie,M.W.H.,Ask,B.,Rane,A.,Burchell,B.,Hume,R.,1989.TheEnantioselective
GlucuronidationofMorphineinRatsandHumans.EvidencefortheInvolvementofmore
thanoneUDP-glucuronosyltrasferaseIsoenzyme,Biochem.Pharm.,38,(1989)
Crowe,P.,2002.The influenceofP-glycoproteinonmorphinetransport inCaco-2cells.
Comparisonwithpaclitaxel,Eur.Jour.ofPharmac.,440,(2002)
Cuoci,A.,2015,Fluidodinamicadegliincendi
Dahan,A.,Romberg,R.,Teppema,L.,Sarton,E.,Bijl,H.,Olofsen,E.,2004.Simultaneous
MeasurementandIntegratedAnalysisofAnalgesiaandRespirationafteranIntravenous
MorphineInfusion,Anest.,101,(2004)
Dahlström,B.E.,Bolme,P.,Feychting,H.,Noack,G.,Paalzow,L.,1978.Morphinekinetics
inchildren,Clin.Pharmacol.Ther.,3,(1979)
Dahlström, B. E., Paalzow, K. L., 1975. Pharmacokinetics of Morphine in Plasma and
DiscreteAreasofRatBrain,Jour.ofPharmac.andBiop.,3,(1975)
Dershwitz,M.,Walsh,J.L.,Morishige,R.J.,Connors,P.M.,Rubsamen,R.M.,Shafer,S.L.,
Rosow,C.,2000,PharmacokineticsandPharmacodynamicsofInhaledversusIntravenous
MorphineinHealthyVolunteers,Anest.,93,(2000)
de Lange, E. C. M., Danhof, M., de Boer, A. G., Breimer, D., 1997.Methodological
considerationsofintracerebralmicrodialysisinpharmacokineticstudiesondrugtransport

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
134
acrosstheblood–brainbarrier,Br.Resear.Rev.,25,(1997)
Ederoth, P., Tunblad, K., Bouw, R., Lundberg, C., Ungerstedt, U., Nordström, C.H.,
Hammarlund-Udenaes,M.,2003.Blood–brainbarriertransportofmorphineinpatients
withseverebraintrauma,Brit.Jour.ofClin.Pharm.,57,(2003)
Emoto, C., Fukuda, T., Johnson, T. N., Neuhoff, S., Sadhasivam, S., Vinks, A. A., 2017.
Characterization of Contributing Factors to Variability inMorphine Clearance Through
PBPKModelingImplementedWithOCT1Transporter,Pharm.Syst.Pharmacol.,(2017)
Espié, P., Tytgat, D., Sargentini-Maier, M.-L-, Poggesi, I., Watelet, J.-B., 2009.
Physiologicallybasedpharmacokinetics(PBPK),Drugmet.Rew.,41,(2009)
Feher,M.,Sourial,E.,Schmidt,J.M.,2000.Asimplemodelforthepredictionofblood-
brainpartitioning,Int.Jour.ofPharmac.,201,(2000)
Gadkar,K.,Yadav,D.B.,Zuchero,J.Y.,Couch,J.A.,Kanodia,J.,Kenrick,M.K.,Atwal,J.K.,
Dennis,M.S.,Prabhu,S.,Watts,R.J., Joseph,S.B.,Ramnujan,S.,2015.Mathematical
PKPDandsafetymodelofbispecificTfR/BACE1antibodiesfortheoptimizationofantibody
uptakeinbrain,Europ.Jour.ofPhar.andBiop.,101,(2016)
Gao,W.,Liu,Y., Jing,G.,Zhao,Y.,Sha,B.,Wang,Q.,Wu,D.,2016.Rapidandefficient
crossingblood-brainbarrier:Hydrophobicdrugdeliverysystembasedonpropionylated
amylosehelixnanoclusters,Biomat.,113,(2017)
González-Alvarez,I.,Fernández-Teruel,C.,Garrigues,T.M.,Casabo,V.G.,Ruiz-Garcia,A.,
Bermejo, M., 2005. Kinetic modelling of passive transport and active efflux of a
fluoroquinolone across Caco-2 cells usinga compartmental approach in NONMEM,
Xenob.,35,(2005)
Hammarlund-Udenaes,M.,Fridé,M.,Syvänen,S.,Gupta,A.,2007.Ontherateextentof
drugdeliverytothebrain,Pharmac.Res.,8,(2007)
Hammarlund-Udenaes,M.,deLange,E.C.M.,Thorne,R.G.,2014.DrugDeliverytothe

Bibliografia
135
brain,Springer,StatiUnitid’America
Hanna,M.H.,Peat,S.J.,Woodham,M.,Knibb,A.,Fung,C.,1990.Analgesicefficacyand
CSFpharmacokineticsofintathecalMorphine-6-Glucuronide:comparisonwithmorphine,
Brit.Jour.ofAnaest.,64,(1990)
Hartmanshenn, C., Scherholz, M., Androulakis, I. P., 2016. Physiologically-based
pharmacokineticmodels:approachesforenablingpersonalizedmedicine,Jour.Pharma.
Pharma.,43,(2016)
Hasegawa,Y.,Kishimoto,S.,Shibatani,N.,Nomura,H.,Ishii,Y.,Onishi,M.,Inostume,N.,
Takeuchi,Y.,Fukushima,S.,2010.Thepharmacokineticsofmorphineanditsglucuronide
conjugateinaratmodelofstreptozotocin-induceddiabetesandtheexpressionofMRP2,
MRP3andUGT2B1intheliver,Jour.ofPharma.AndPharma.,62,(2010)
Hoskin, P., Hanks, G. W., Aherne, G., Chapman, D., Littleton, P., Filshie, 1989. The
bioavailability and pharmacokinetics of morphine after intravenous, oral and buccal
administrationinhealthyvolunteers,Br.J.Clin.Pharmac.,(1989)
Janicki,P.K.,1997.PharmacolyofMorphineMetabolites,Curr.Med.Group,1,(1997)
Jeffrey, P., Summerfield, S., 2009.Assessment of the blood-brain-barrier in CNS drug
discovery,Neur.ofDis.,37,(2010)
Jimenez,N.,Anderson,G.D.,Shen,D.D.,Nielsen,S.,Farin,F.,Seidel,K.,Lynn,A.M.,2012,
Is ethnicity associated with morphine's side effects in children? morphine
pharmacokinetics,analgesic responseandsideeffects inchildrenhavingtonsillectomy,
Paediatr.Anaesth.,22,(2012)
Kissin, I.,Brown,P.T.,Robinson,A.,Bradley,E. L.,1991.AcuteTolerance inMorphine
Analgesia:ContinuousInfusionandSingleInjectioninRats,Anes.,74,(1991)
Lam, J., Baello, S., Iqbal,M., Kelly, L. E., Shannon,P. T., Chitayat,D.,Matthews, S.G.,
Koren,G.,2015.TheontogenyofP-glycoprotein in thedevelopinghumanblood–brain

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
136
barrier:implicationforopioidtoxicityinneonates,Ped.Res.,4,(2015)
Lötsch, J., Skarke, C., Schmidt, H., Liefhold, J., Geisslinger, G., 2002. Pharmacokinetic
modeling to predict morphine and morphine-6-glucuronide plasma concentrations in
healthyyoungvolunteers,Clin.Pharma.&Therap.,2,(2002)
Meineke, I., Freudenthaler, S., Hofmann, U., Schaeffeler, E., Mikus, G., Schwab, M.,
Prange, H. W., Gleiter, C. H., Brockmöller, J., 2002. Pharmacokinetic modelling of
morphine, morphine-3-glucuronide and morphine-6-glucuronide in plasma and
cerebrospinal fluidof neurosurgical patientsafter short-term infusionofmorphine,Br.
Jour.Clin.Pharmacol.,54,(2002)
Ohno,S.,Kawana,K.,Nakajin,S.,2007.ContributionofUDP-Glucuronosyltransferase1A1
and 1A8 toMorphine-6-Glucuronidation and Its Kinetic Properties, TheAmer. Soc. for
Pharmac.andExp.Ther.,36,(2008)
Ohtsuki,S.,Terasaki,T.,2007.ContributionofCarrier-MediatedTransportSystemstothe
Blood–Brain Barrier as a Supporting and Protecting Interface for the Brain;
ImportanceforCNSDrugDiscoveryandDevelopment,Pharmac.Res.,9,(2007)
Olkkola,K.T.,Maunuksela,E.-L.,Korpela,R.,Rosemnberg,H.,1988.Kineticsanddynamics
ofpostoperativeintravenousmorphineinchildren,Clin.Pharmacol.Ther.,2,(1988)
Osborne,R.,Joel,S.,Trew,D.,Slevin,M.,1990.Morphineandmetabolitebehaviorafter
diferentroutesofmorphineadministration:Demonstrationoftheimportanceoftheactive
metabolitemorphine-6-glucuronide,Clin.Pharmacol.Ter.,47,(1990)
Pardridge, W. M., 2002. Why is the global CNS pharmaceutical market so under-
penetrated?,DrugDisc.Tod.,1,(2002)
Pardridge,W.M.,2003.Blood-brain-barrierdrugtargeting,Mol.Inter.,3,(2003)
Stain-Texier,F.,Boschi,G.,Sandouk,P.,Schermann,J.-M.,1999.Elevatedconcentrations
ofmorphine 6-beta-D-glucuronide in brain extracellular fluid despite lowblood- brain-

Bibliografia
137
barrierpermeability,Bri.Jour.ofPharm.,128,(1999)
Stansky, D. R., Greenblatt, D. J., Lowenstein, E., 1978. Kinetics of intravenous and
instramuscularmorphine,Clin.Pharmac.&Ther.,1,(1978)
Stephenson,T.,2005.Howchildren’sresponsestodrugsdifferfromadults,Brit.Jour.of
Clin.Pharm.,59,(2005)
Summerfield,S.G.,Read,K.,Begley,D.J.,Obradovic,T.,Hidalgo,I.J.,Coggon,S.,Lewis,
A. V., Porter, R. A., Jeffrey, P., 2007. Central Nervous System Drug Disposition: The
Relationship between in Situ Brain Permeability and Brain Free Fraction, The Jour. of
Pharma.andExp.Therap.,22,(2008)
Stone,A.,Mackenzie,P.,Galetin,A.,Houston,B.,Miners,J.,2003.Isoformselectivityand
kineticsofmorphine3-and6-glucuronidationbyhumanUDP-glucuronosyltransferases:
evidenceforatypicalglucuronidationkineticsbyUGT2B7,TheAmeric.Soc.forPharmac.
andExper.Therap.,31,(2003)
Stuart-Harris, R., Joel, S.P., McDonald, P., Currow, D., Slevin, M. L., 2000, The
pharmacokineticsofmorphineandmorphineglucuronidemetabolitesaftersubcutaneous
bolusinjectionandsubcutaneousinfusionofmorphine,Blackw.Sci.Ltd,49,(2000)
Sverrisdóttir,E.,MeldgaardLund,T.,Estrup,O.A.,Mohr,D.A.,Louring.C.L.,Kreilgaard,
M., 2015. A review of morphine and morphine-6-glucuronide’s pharmacokinetic–
pharmacodynamicrelationshipsinexperimentalandclinicalpain,Eur.Jour.ofPharma.
Sci.,7,(2015)
Tortora, G.J., Nielsen, M.T., 2013. Principles of human Anatonomy, Wiley, Stati Uniti
d’America
Tran,T.T.,Mittal,A.,Aldinger,T.,Polli,J.W.,Ayrton,A.,Ellens,H.,Bentz,J.,2005.The
ElementaryMassActionRateConstantsofP-gpTransportforaConfluentMonolayerof
MDCKII-hMDR1Cells,Biop.Jour.,88,(2005)

Modellazionefarmacocineticadeltrasportodifarmacialcervello:ruolodellabarrieraematoencefalica
138
Tunblad, K., Jonsson, E. N., Hammarlund-Udenaes, M., 2002.Morphine Blood–Brain
Barrier Transport Is Influenced by Probenecid Co-Administration, Pharm. Resear., 20,
(2003)
vanTellingen,O.,Yetkin-Arik,B.,deGooijer,M.C.,Wesselling,P.,Wurdinger,T.,deVrise,
H.E.,2015.Overcomingtheblood-brain-barrierforeffectivegliblastomatreatment,Drug
Resist.Updat.,12,(2015)
Wagner,J.G.,1981,Historyofpharmacokinetics,Pharmac.Ther.,12,(1981)
Zhou,H.H.,Sheller, J.R.,Nu,H.,Wood,M.,Wood,A. J. J.,1993.Ethnicdifferences in
responsetomorphine,Pharmacol.Ther.,54,(1993)


RingraziamentiRingraziamoilprof.DavideManca,checihaoffertol’opportunitàdisvilupparequesto
lavorodi tesi suuntemanuovoepernoimoltostimolante,seguendociconcostanza,
pazienzaepassione.
Unsentitoringraziamentovaancheall’ing.AdrianaSavocaperl’aiutoeladisponibilità.