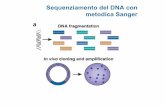
Metodi di sequenziamento Sanger (enzimatico) Maxam e Gilbert (chimico)
-
Upload
rachele-melis -
Category
Documents
-
view
230 -
download
0
Transcript of Metodi di sequenziamento Sanger (enzimatico) Maxam e Gilbert (chimico)

Metodi di sequenziamento
•Sanger (enzimatico)
•Maxam e Gilbert
(chimico)

Metodo di Sanger
primer
primernuovo DNA
dideossinucleotideterminatore
quattro dNTP (incluso 32PdNTP)DNA polimerasi
La catena neosintetizzata termina quando un ddNTP è incorporato al posto di un dNTP
Denaturare e separare su gel di poliacrilammide
ddTTP ddCTP ddGTP ddATP

Metodo di Maxam e GilbertDNA singolo filamento marcato ad una estremità
4 o 5 reazioni di modificazione base-specifiche
Rottura del filamento in corrispondenza della base modificata mediante piperidina
Es. metilazione delle G con dimetilsolfato
Separare i frammenti marcati su gel di acrilammide

Gel di poliacrilammide di sequenza

Confronto metodi di sequenziamento
Sanger
rapida e semplice attuazione
disponibilità di kit
necessità di primer
sensibile a strutture secondarie
Maxam e Gilbert
lunga preparazione del DNA
reazioni da mettere a punto
relativamente economico
strutture non influenti
utilizzabile per oligonucleotidi

Sequenziamento automatico

Sequenziamento con Taq polimerasi

Trasferimento di acidi nucleici(Blotting)
•Southern
•Northern

Schema trasferimento

Schema ibridazione

Metodi di trasferimento
•Capillare
•Elettroblot

carta 3MM
membrana nylon
gel
supporto
}
carta 3MM
tamponevaschetta
Assemblaggio del blot capillare

- +
tampone
carta 3MM
spugnettegel
membrana nylon
Assemblaggio dell’elettroblot

Analisi di espressione con Northern blot

Altre tecniche di analisi
•Estensione del primer (primer extension)
•Protezione dalla S1/RNasi
(mapping)
•RT-PCR

mRNA totale
oligo antisenso marcato
mRNA globina
cap
5’3’
ibridazione
estensione con RT
Analisi dei frammenti estesi su gel di sequenza
frammento protetto
Estensione del primer

Protezione da RNasi (RNase Protection)
mRNA totale
sonda RNA antisenso
mRNA globina
cap
5’3’
ibridazione
trattamento con RNasi
Analisi dei frammenti protetti su gel di sequenza
frammento protetto
inizio trascrizione

Analisi interazioni DNA-proteine:saggio di footprinting

Analisi interazioni DNA-proteine:saggio EMSA

Sistemi di espressione
•In vitro (estratti cellulari)
•In vivo (cellule in coltura)
•Animali transgenici

Gene reporter

•diversi tipi di vettori
•vettori “navetta” batteri-lievito
•possibilità di ricombinazione omologa
Trasformazione del lievito (Saccharomyces
cerevisiae)

Vettori di clonaggio
per lievito

Ricombinazione omologa

•transiente
•stabile
•vettori episomali
Trasfezione di cellule in coltura

Vettore di espressione in cellule di mammifero

Trasfezione in cellule in coltura

Vettori episomali

•fosfato di calcio
•liposomi (e simili)
•elettroporazione
•virus (SV40, retrovirus)
Metodi di trasfezione


Descrizione generale esercitazioni di laboratorio
Studio della localizzazione intracellulare della proteina SEC4 del lievito Saccaromyces cerevisiae
A) Clonaggio di SEC4 in vettore per l'espressione in lievito di proteine di fusione con "tag" (GFP)
B) Espressione di SEC4 in lievito e analisi della sua localizzazione mediante western
blot di estratti frazionati
Parte A
1) Isolamento di DNA genomico da lievito (I parte)
2) Isolamento di DNA genomico da lievito (II parte)Analisi spettrofotometrica del DNA preparato PCR su DNA genomico (preparazione frammento da clonare)
3) Preparazione di DNA plasmidico (vettore di clonaggio) con colonninaDigestione DNA (vettore e frammento) con enzimi di restrizione
4) Analisi su gel di agarosioReazione con enzima "ligasi"
5) Preparazione piastre di agarTrasformazione batterica
6) Analisi risultati trasformazioneMinipreparazione DNA plasmidico
7) Analisi su gel di agarosio
8) Fasi iniziali di Southern blot

Clonaggio con doppia digestione
GAATTCCTTAAG
GAATTCCTTAAG
AAGCTTTTCGAA
GCTTAA
AGCTT A
EcoRI
AAGCTT
TTCGAAGAATTC
CTTAAG
DNA ligasi
AATTC G
ATTCGA
EcoRI HindIII
AAGCTTTTCGAA
HindIII


Trasfezione con liposomi

Elettroporazione

Vettori virali

Vettori retrovirali