Lab. Chimica Organica II. - Prof. Enrico Maria...
Transcript of Lab. Chimica Organica II. - Prof. Enrico Maria...

Lab. Chimica Organica II.

Sostituzioni elettrofile aromatiche

Reazioni del benzene e derivati
H E
+ E+ + H*Sostituzioni elettrofile aromatiche
H ClFeCl3
+ Cl2 + HCl
AlogenazioneH NO2
H2SO4+ HNO3 + H2O
Nitrazione
H SO3HH2SO4
+ SO3 + HCl
SolfonazioneH R
AlX3+ RX + HX
Alchilazione
H CORAlX3
+ RCOX + HX
Acilazione

Sostituzione elettrofila aromatica

Bromurazione
Complesso molecolare conCarica (+) sul bromo e carica (-) sul ferro
Intermedio cationico stabilizzato per risonanza

Paragone ∆G± di attivazione
Perdita di aromaticità

Meccanismo

Profilo energetico bromurazione(processo esoergonico)

Nitrazione elettrofila aromatica

Alchilazione di Friedel-Crafts
La successiva perdita di un protoneporta alla formazione del prodottodi sostituzione alchilato e neutro

Limitazioni dell’Alchilazione di Friedel-Crafts
1. Nessuna reazione con gruppi disattivanti
2. Polialchilazione

Limitazioni dell’Alchilazione di Friedel-Crafts
3. Riarrangiamento del gruppo alchilico

Effetti dei sostituenti aromatici

Effetto induttivo attivante/disattivante

Effetto di risonanza disattivante

Effetto di risonanza attivante

Stabilità / reattività intermedio carbocationico

La nitrazione del toluene

La nitrazione del fenolo

La nitrazione del clorobenzene
Alogeni: Effetto –I (disattivante); effetto +R (o-/p-orientante)

La clorurazione della benzaldeide

Acilazione di Friedel-Crafts
Meccanismo
L’elettrofilo è un catione acilicostabilizzato per risonanza
Nota: i cationi acilio NON riarrangiano e non si hanno ulteriori sostituzioni

Alchilazioni di F.-C.: inconvenienti
1. Effetto attivante di Ril composto 2 (monoalchilato) è più reattivo di 1: polialchilazione
H RAlX3
R
RX
AlX3
RX
R
R
1 2 3
NO2AlX3
RXnessuna reazione
2. Effetto disattivante di R
la reazione con gruppi disattivanti – se avviene - è molto lenta

Anidridi come agenti acilanti
AlX3
RO
OO
R
+X3Al
RO
OO
R
RO
OAlX
XX R O
Ione acilio

Reazioni di Grignard

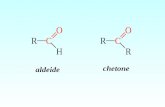
Reazioni dei composti carbonilici: Addizione
H Nu: O
R
R
+ Nu
O
RR
H
Addotto Tetraedricodi Addizione

Addizione di carbonucleofiliFormazione di nuovi legami C-C
RMgX RLi RC≡C(-) (-)C≡NGrignard Organolitio acetiluri cianuri
Formazione e struttura dei composti organometallici
Reattivi di Grignard

Composti organometallici
Organolitio
%c.i. = (Ea – Eb / Ea) x 100
Nucleofili più potenti

Basicità/nucleofilicità degli organometalli
Acido più fortepK = 15.7
Acido più debolepK = 45
2 CH3MgI + 2 H2O 2 CH4 + Mg(OH)2 + MgI2
Altri donatori di protoni per organometalli
R2NH RC≡CH ROH HOH ArOH RSH RCO2H
pKa 30-35 25 16-18 15.7 9-10 8-9 4-5

Addizione di reattivi di Grignard a composti carbonilici

Meccanismo della reazione di Grignard
Addizione nucleofiladi un carbanione aduna aldeide o unchetone seguita da deprotonazione dell’intermedio alcossido

Reazione con esteri dei reattivi di Grignard
Meccanismo
Reazione inutile per la sintesi di chetoni

Sintesi di chetoni via reattivi di Grignard
1. Reazione con ammidi N, N-disostituite
R
O
N Me
Me+ R' MgX
OMgXNMe2R
R'
H+
R
O
R'
Intermedio di addizione al carbonile
R
O
N H
H+ R' MgX R
O
NHMgX+ R' H
2. Nel caso di ammidi con almeno un H: il Grignard è una base
3. Reazioni con nitrili
R
N+ R' MgX R
NMgX
R'Intermedio di tipo imminicodi addizione al carbonile
H2O
R
NH
R'Immina
H2O
R
O
R'

Possibili reazioni competitive (1)
1. Addizione coniugata (1,4) a sistemi insaturi
Meccanismo
+ R' MgXH3O+
O
R'
OMgX O
R'
H3O+
O
R' MgX R'
OMg X R'MgX
O
R'
OH
R'
O
Attacco al doppiolegame elettronpovero
tautomeria
stato di transizione ciclico a 6 termini

Possibili reazioni competitive (2)
2. Riduzione del gruppo carbonilico(presenza di β-H nel reattivo di Grignard)
Meccanismo
• β-H del reattivo di Grignard responsabili per la riduzione• Non c’è introduzione di R’’CH2CH2 nell’alcol prodotto
+H3O+
O OMgXR
MgXα
β
R
H+
OHH
olefina Alcol
+OR
R''
MgXα
β OR
Mg
R''
Xδ+
δ−H
OHR H
R'R'
R'+ R''
R = alchile

Possibili reazioni competitive (3)
3. Enolizzazione (deprotonazione) del gruppo carbonilico(presenza di α-H nel chetone reagente)
• l’idrolisi porta al chetone di partenza• l’enolizzazione avviene con chetoni ramificati contenenti α-H• R’’MgX agisce da base
+H3O+
OR'
OMgXR'
MgXα
OR
RR''(base) R
+ R''HR'

Possibili reazioni competitive (4)Formazione di bifenile
MgX +O XMgO
2
rottura omolitica
Meccanismo radicalico non chiarito

Reazione di Wittig

Reazione di Wittig. Metodo generale per la sintesi di alcheni
Effetto globale: conversione di un carbonile in un doppio legame C=C.

I composti del fosforo
P
H
H
H
Fosfina (p. e. -87 °C)
P
H
H
H
Trifenilfosfina(p. f. 81 °C)
P con 5 elettroni nel guscio di valenza (come l’N), ma:
• fosfine nucleofili migliori delle ammine • fosfine basi più deboli delle ammine

Preparazione ilidi di fosforo
1° passaggio: sale di fosfonio2° passaggio: Rimozione H in α

Meccanismo della Wittig

1. Applicazioni della Wittig

2. Applicazioni della Wittig

Inconvenienti della Wittig
1. Ph3P: relativamente costosa2. n-BuLi: uso di tecniche particolari
Alternative alla Wittig
Reazione di Wadsworth-Emmons

Wadsworth-Emmons
1° passaggio: Reazione di Arbuzov (SN2)
2° passaggio: deprotonazione dell’estere fosfonato

Meccanismo della Wadsworth-Emmons
Nota:
La reazione diWittig presentagli isomeri geometrici (E,Z)
La variante W.-E.genera solol’isomero E.

Sintesi di sulfammidici

Sulfammidici
Antibiotici orali per il trattamento di infezioni batteriche. Sono tutti derivati della p-amminobenzensolfonammide(solfanilammide)

Meccanismo d’azione dei sulfammidici
L’attività biologica risiede nella somiglianza con il PABA che è utilizzato dai batteri nella sintesi dell’acido folico
La solfanilammide blocca la biosintesi dell’acido folicocompetendo con il PABA per il sito attivo dell’enzima che ingloba tale acido nell’acido folico. I batteri così cessano di crescere

Sintesi Multistadio (3 passaggi)
1. H3O+
2. OH-
1° stadio: clorosolfonazione dell’acetanilide2° stadio: ammonolisi del solfanilcloruro3° stadio: idrolisi della funzione acetammidica

1° passaggio: Clorosolfonazione dell’acetanilide
Idrolizza ad acido solfonicoAbbastanza rapidamente

2° passaggio:ammonolisi del solfonilcloruro
Trattamento con eccesso di NH3 acquosa

3° Passaggio:idrolisi selettiva del gruppo acetammidico
Il prodotto da idrolizzare è sia una carbossiammide che una solfonammide

L’idrolisi è selettiva perché le carbossimmidireagiscono più velocemente
S tetraedrico: maggiore ingombro sterico e dunque, attaccodel nucleofilo più difficile

Trasformazione di gruppi funzionali

La Sintesi di Nitrili da Acidi Carbossilici
RCO2H RCOCl (1)SOCl2
NH3
- H2O
RCOCl RCONH2 (2)
RCONH2 RCN (3)

1° Passaggio: clorurazione di un acido carbossilico
R
O
OH ClSO
Cl OSO
ClR
O
OSO
ClR O
ClR
O
Cl
+ + HCl
+ SO2
Cl-
- Cl-

2° Passaggio: Formazione dell’ammide
R
O
Cl NH3 Cl-R
O
R
O
NH2
+
NH3
NH3
+ NH4Cl
I cloruri sono i derivati più reattivi (il carbonile viene attivato)

3° Passaggio: disidratazione dell’ammide
a) SOCl2 come disidratante
R
O
NH2 ClSO
Cl NH
SO
ClR
O+ + HCl
+ SO2 NSO
ClR
OHHONS
O
R Cl-
SN- HClR
N
1. Attacco di NH2 allo zolfo2. Intermedio idrossiimminico3. Sostituzione interna4. Espulsione di SO2

3° Passaggio: disidratazione dell’ammide
b) P2O5 come disidratante

La sintesi di dibromuri vicinali da aldeidi (allungamento di catena ed alogenazione)
O H
Ac2O O
OH
(1)
O
OH
SOCl2
MeOH
O
OCH3
(2)
O
OCH3
HBr
H2O2
O
OCH3Br
Br
(3)

1° Passaggio: Reazione di composti CH2-acidi con carbonili
CHbase
C
O
C CO
C COH -H2O
1. rimozione di un protone2. attacco al carbonile3. formazione enolato/enolo4. disidratazione

Differenti substrati CH2-attivi e differenti carbonili

Reazione di Perkin
O H
O
O
O
O
O O
O+
O
O
O
O
OH+
+
O
O
O
O
O
O
OH
O
OO
O+
O
OHO
O O
O+
O
OHO
O O
O+O
O
O Na2CO3, H+ O
OH
(1)
(2)
(3)
(4)

2° Passaggio: Preparazione del metilcinnamato
+ MeOHSOCl2O
OH
O
OMe
+ H2O
a) formazione del cloruro acilico
R
O
OH ClSO
Cl OSO
ClR
O
OSO
ClR O
ClR
O
Cl
+ + HCl
+ SO2
Cl-
- Cl-
b) metanolisi del cloruro acilico
R
O
ClH+
R
OH
Cl
HO MeR
O
OMe- HCl

3° Passaggio: addizione al doppio legame C=C
BrBr
Br+
Br-
Br
Br
Br2
orientazione trans-coplanare
Br
Br
BrBr
trans-diassiale trans-equatoriale
metodo convenzionale (Br2/CCl4)metodo a basso impatto ambientale (HBr/H2O2)
2 HBr + H2O2 Br2 + H2O

Generazione di Br2 in situ
HBr/H2O2O
OMe
O
O MeBr
HBr
H
2,3-dibromo-3-fenilpropionato di metile

Cromatografia

Cromatografia
Definizione. E’ un processo per separare i componenti di una data miscela grazie ad una successione di distribuzioni degli stessi componenti tra 2 differenti fasi, una stazionaria e l’altra mobile.
Cromatografia per eluizione:una miscela di due diversi componenti (soluti A e B) è trasportata da una fase mobile lungo una colonna contenente una fase stazionaria
Il fenomeno è il seguente: una porzione di soluto A nella fase mobile viene in contatto con una sezione della fase stazionaria. Vi èuna prima ripartizione, ovvero A si distribuisce tra le due fasi a seconda dell’affinità che esso presenta per esse. Tale affinità è funzione della natura chimica del singolo componente, della natura della fase mobile e di quella stazionaria, della portata della fase mobile e di altre caratteristiche strutturali della colonna (lunghezza, sezione, grado di impaccamento della fase stazionaria, ecc..)
Allo stesso tempo, una porzione dello stesso soluto nella fase stazionaria viene in contatto con una differente e nuova sezione della fase mobile e si ha un’ulteriore ripartizione. Il processo si ripete numerosissime volte. Al fluire della miscela, la velocità con la quale i differenti componenti si spostano nella colonna dipende dal coefficiente di ripartizione di ogni singola sostanza tra le due fasi: KA = [A]st/[A]m; KB = [B]st/ [B]mPertanto differenti soluti (con differenti coefficienti di ripartizione), si muovono con differenti velocità in modo da separarsi in “bande” caratteristiche.

Cromatogramma: volume e tempo di ritenzione
Volume di ritenzione (VR). E’ ilvolume di fase mobile che devefluire in una data colonna per eluire un soluto alla suamassima concentrazione
Tempo di ritenzione (tR). E’ il tempo richiesto per eluire un soluto alla sua massima concentrazione. Se F è la velocità di flusso (volume x tempo), noto VR, il tempo di ritenzione è
tR = VR/F
Per convenienza, i cromatogrammi sono generalmente registrati in funzione del tempo e forniscono direttamente i tempi di ritenzione.

Gas-CromatografiaDefinizione. E’ un processo cromatografico che prevede l’impiego di una fase mobile gassosa e di una fase stazionaria che può essere solida oppure liquida.
Gas-cromatografia gas-solido (GSC): è una tecnica che si basa sull’assorbimento fisico dei soluti su di una fase stazionaria solida; si usa raramente e nel caso, viene impiegata principalmente per la separazione di gas a basso peso molecolare.Gas-cromatografia gas-liquido (GLC): è una tecnica che si basa sulla solubilità dei soluti su di una fase stazionaria liquida ed è certamente tra i metodi analitici più importanti per la separazione e l’analisi di miscele di prodotti organici.
Vantaggi nell’uso di gas come fase mobile1. Bassa viscosità. Ciò consente l’uso di colonne lunghe molto efficienti, e alte velocità di flusso (separazioni veloci)2. I gas sono “inerti”: virtualmente non ci sono interazioni tra soluto e fase mobile 3. Si possono realizzare rivelatori estremamente sensibili e veloci

Il gas-cromatografoLo strumento consta di 4 parti
1. La sorgente del gas di trasporto2. La zona di iniezione (injector) e vaporizzazione della miscela3. La colonna cromatografica (sistemata all’interno di un’opportuna camera termostatata)4. Il rivelatore all’uscita della colonna
Principio del metodo GLC:
una miscela a più componenti viene vaporizzata nell’injector e dunque introdotta sotto la spinta di un gas inerte (fase mobile) in una colonna riempita di una fase liquida (fase stazionaria). Ad una certa temperatura, la velocità con cui i componenti della miscela si muovono nella colonna dipende dalla natura chimica degli stessi, dalla portata del gas di trasporto, dalla lunghezza e sezione della colonna e dal natura della fase stazionaria.

Il gas-cromatografo: sorgente del gas La sorgente del gas di trasporto è usualmente una bombola ad alta pressione (200 atm) munita di apposito riduttore dal quale il gas esce a 3-6 atm.
La fase mobile gassosa deve essere chimicamente inerte. I gas comunemente usati sono elio ed azoto (più raramente argon o idrogeno) e le velocità di flusso tipiche vanno da pochi ml/min (1-5) a 50-60 ml/min a seconda del tipo di colonna usata.
Il gas entra nel circuito cromatografico (iniettore, colonna e rivelatore) ad una portata che viene accuratamente controllata tramite un regolatore di flusso
Azoto Elio CO2 Idrogeno Aria
Argon

Il gas-cromatografo: l’iniettoreLa maggior parte delle miscele analizzate via GLC sono liquide a temperatura ambiente. La camera di vaporizzazione (iniettore) è un opportuno volume (in genere cilindrico) racchiuso da pareti metalliche riscaldate ad una temperatura (200-300 °C) all’interno del quale i campioni da analizzare (di 0.2-0.5 µL) vengono iniettati in modo tale da essere istantaneamente vaporizzati.
L’iniezione si esegue con microsiringhedel volume di 5-10 µL.

Il gas-cromatografo: la colonna (1)
1. Colonne Impaccate: sono di vetro oppure di metallo (acciaio, rame o alluminio) con diametro tra 2 e 10 mm e lunghezze in genere, tra 1 e 4 m.
In condizioni GLC, la fase stazionaria liquida è dispersa su particelle solide di un materiale supporto ad alta area superficiale.
Il supporto deve avere:a) Inerzia chimica verso i componenti da separare e il gas di trasportob) Buona resistenza meccanicac) Granulometria controllata
Supporti comuni sono costituiti spesso da diatomee (struttura tipo silice idrata) che a seconda dei trattamenti termici cui sono sottoposte presentano strutture con differenti aree superficiali e caratteristiche adsorbenti per la fase liquida. Nomi commerciali sono Chromosorb W, Chromosorb P, Chromosorb A, Chromosorb G. Altri supporti sono Teflon polverizzato, Carbone attivato, allumina, ossido di Mg, alcuni polimeri organici, ecc…

Fasi stazionarie per colonne impaccateLa fase stazionaria è costituita da un liquido che deve essere non volatile alla temperatura di analisi. Benchè esistano moltissimi liquidi potenzialmente impiegabili in GLC, la scelta è stata limitata a circa 25 sostanze classificabili in base alla loro polarità.
O
OC9H19
O
OC9H19 Squalene
Dinonyl phtalate
O
OC9H19
O
OC9H19
OO
O
OOH
4 4
O
HOO
Ethylene glycol adipate

Il gas-cromatografo: la colonna (2)
2. Colonne Capillari: sono di vetro o silice fusa (vetro ad elevata purezza di composizione SiO2) con diametro tra 0.2 e 0.5 mm e lunghezze tra 10 e 100 m. Le colonne in silice fusa sono migliori poiché non contengono impurità metalliche che possono catalizzare reazioni chimiche nella colonna stessa.
La fase stazionaria liquida è depositata sulle pareti interne della colonna stessa (WCOT: wall coated open tubular) in uno spessore variabile tra 0.2 e 0.5 µm.

Fasi stazionarie per colonne capillariLe fasi liquide impiegate sono le stesse usate per le colonne impaccateMolto usate sono le colonne a fase legata (bonded-phase) dove la fase stazionaria èchimicamente legata alla colonna, più precisamente agli atomi di silicio sulla superficie interna della colonna
Vantaggi delle colonne capillari. Il diametro ridotto comporta “Coating” più uniformee trasferimento di calore migliore e più controllabile. Si ha inoltre miglior risoluzione e separazione

Selezione di una colonna gas-cromatografica
Regole pratiche. “Il simile scioglie il simile …”
1. Sostanze polari si separano meglio in colonne contenenti fasi liquide polari, mentre composti apolari sono separati più efficientemente in colonne apolari.2. In presenza di fasi liquide polari, composti polari sono ritenuti più a lungo di composti apolari. 3. In presenza di fasi liquide apolari, i componenti di una miscela sono separati in accordo alla loro relative solubilità nella fase liquida stessa (stazionaria) e gassosa (mobile). Poiché in generale, all’aumentare del peso molecolare di ogni componente, la sua volatilità (cioè la sua solubilitànella fase gassosa) diminuisce, esso spende più tempo per essere eluitoin colonna. Pertanto, il tempo di ritenzione di ogni componente aumenta all’aumentare del suo peso molecolare (o punto di ebollizione)

Il gas-cromatografo: il fornoLa temperatura della colonna è una variabile fondamentale per la separazione gas-cromatografica poiché altera in maniera importante il fenomeno di ripartizione di ogni soluto tra le due fasi, fissa e mobile. Per assicurare la riproducibiltà della analisi, la temperatura ècontrollata attraverso camere termostatabili (forni) con variazioni di ± 0.1 °C.
Analisi isoterma
Analisi in programmatadi temperatura

Il gas-cromatografo: il rivelatoreIl rivelatore misura la concentrazione di ogni singolo soluto presente nel gas di trasporto in uscita dalla colonna. Sebbene esistano parecchi differenti tipi di detectors, tra i più usati per la sua eccellente sensibiltà, c’è il rivelatore a ionizzazione di fiamma (FID: flame ionizationdetector). Il principio è il seguente:
il gas di trasporto in uscita dalla colonna (He, N2o Ar) si unisce ad un debole flusso di H2 ed aria e la miscela viene bruciata su di una microfiammaPer effetto della combustione in presenza di idrogeno, in presenza di composti organici, si producono ioni (specie cariche elettricamente) sebbene il numero di tali ioni vari in relazione alla natura degli stessi composti. Questa corrente ionica viene raccolta e misurata grazie a due elettrodi a cui viene applicata una differenza di potenziale di circa 300-400 V. Al positivo migrano elettroni, al negativo gli ioni positivi. Al passare di ogni singolo componente di una miscela attraverso il rivelatore si osserverà, dunque un segnale caratteristico in relazione alla natura e alla concentrazione di quella specie
Il numero di ioni generati dal composto organico bruciato è in relazione al numero di atomi di Cpresenti nello stesso: la risposta del detector migliora (corrente più intensa) per composti contenenti un maggior numero di atomi di C.Il FID è insensibile a composti inorganici, ad N2, O2, CO, CO2, acqua, NH3, SO2 … e la sua risposta diminuisce via, via che in un composto organico aumenta il numero di atomi di O, S, N, ed alogeni.

Gas-cromatogramma

Report GC

Spettrometria di massa

Lo spettro di massa

Lo Spettro di MassaUno spettro di massa contiene un certo numero di picchi ognuno
dei quali corrisponde ad un certo tipo di ioni che hanno cioèun certo rapporto massa/carica (m/z). Inoltre l’intensità del picco è proporzionale al numero degli ioni che lo hanno originato.
Nel rapporto m/z, la massa “m” non è quella esatta dello ione ma piuttosto quella nominale cioè approssimata al numero intero più vicino alla massa vera dello ione.
Tipi di ioni:
• Ione molecolare• Ioni di frammentazione• Ioni di riarrangiamento• Ioni a carica multipla• Ioni metastabili• Ioni negativi

Ione molecolare
Quando un fascio di elettroni colpisce una data molecola ABCD (dove A, B, C e D sono atomi o gruppi di atomi costituenti la molecola organica), con energia superiore a quella per la sua ionizzazione, la molecola ionizza generando uno ione positivo per espulsione di un elettrone:
ABCD + e- ⎯⎯⎯→ [ABCD]+. + 2e-
Questo ione è detto MOLECOLARE ed è radicalico poiché ha un elettrone spaiato. Dal valore della massa di questo ione si ricava la massa (peso molecolare) della molecola genitrice.

Ioni di frammentazione.
Ioni di frammentazione. La ionizzazione della molecola neutra ABCD lascia sullo ione molecolare un eccesso di energia che viene dissipata attraverso un processo di frammentazione dello ione stesso. In pratica, si scindono alcuni legami nello ione molecolare per generare ioni frammento.
[ABCD]+. ⎯⎯⎯⎯→ [AB]+ + CD.
I frammenti così formati possono a loro volta rompersi dando luogo a frammenti più piccoli e così via.

Ioni di riarrangiamento
Derivano dallo ione molecolare o da ioni frammento per rottura di almeno due legami e formazione di uno nuovo:
[ABCD]+. ⎯⎯⎯⎯→ [AD]+. + BC
Ad esempio, la formazione di AD+. richiede la rottura dei legami A-B e C-D e la formazione di un nuovo legame A-D (trasposizione di McLafferty).

Interpretazione dello spettro di massaIdentificazione e Conferma dello ione molecolare
Regola dell’azoto.La regola afferma che lo ione molecolare di una sostanza organica ha:
- Massa pari se non contiene azoto oppure un numero pari di atomi di azoto- Massa dispari se contiene un atomo di azoto (oppure un numero dispari di atomi di azoto)
La regola ha origine dal fatto che, in genere:la maggior parte degli elementi nelle molecole organiche, ha massa pari e valenza pari
C: m=12, v=4; O: m=16, v=2; S: m=32, v=2, 4, 6; …, Così, ad esempio: H2O (m/z = 18), CH3OH (m/z = 32), PhOH (m/z = 94)
ma l’azoto è un’eccezione a massa pari (14) e valenza dispari (3)EtNH2 (m/z = 45), PhNH2 (m/z = 93)

Perdite logiche di frammenti neutri. 1. Lo ione molecolare nella sua decomposizione può perdere dei frammenti neutri la cui massa può essere individuata per differenza tra la massa dello ione molecolare e quella dello ione frammento più vicino.Ad esempio,
Il composto ha formula bruta C4H10OIl picco a massa più alta è quello pari a m/z = 74 ed è lo ione molecolare M+.
I picchi immediatamente vicini sono:m/z = 73 corrispondente a M+ - 1m/z = 59 corrispondente a M+ - 15m/z = 45 corrispondente a M+ - 29
e sono tutte perdite logiche poichéla prima è relativa all’espulsione di H, la seconda è la perdita di un metile (15), la terza è la perdita di un etile (C2H5 = 29).

Perdite logiche di frammenti neutri. 2.
Se in uno spettro ci sono perdite da 1 a 3 unità di massa da M+ queste possono essere logiche (espulsione di H).
Invece, perdite da 4 a 13 sono non logiche corrispondenti cioèa frammenti neutri poco probabili.
Un altro intervallo non logico comprende perdite tra 21 e 25.

Intensità dello ione molecolare.
1. L’intensità di M+. dipende dalla sua stabilità ed aumenta in genere con il grado di insaturazione della molecola.
2. Sostanze aromatiche stabilizzano la carica dello ione molecolare per delocalizzazione
3. Sostanze aliciclche danno ioni più stabili (di quelle a catena aperta) poiché la decomposizione di M+. richiede la rottura di due legami anziché uno

Intensità ioni molecolari: confronto

Intensità dello ione molecolare per alcune classi di composti

NOTA: alcune sostanze NON danno ione molecolare. Questo perché all’impatto delle molecole di tali sostanze con gli elettroni in sorgente, l’energia trasferita è così elevata che lo ione (molecolare) stesso formato è instabile e frammenta istantaneamente.
In questi casi, è talvolta possibile rivelare lo ione M+., abbassando l’energia degli elettroni ionizzanti (la sensibilitàdello strumento tuttavia diminuisce).
70 eV 13 eV

Abbondanza isotopica naturale

Composizione dello ione molecolareLo ione molecolare è sempre accompagnato da uno o due ioni di
massa più elevata.
Es. Benzene: accanto a m/z = 78 (ione molecolare) con intensità 100%, si ha m/z =79 con intensità ∼ 6.8%. Questo picco detto “isotopico” è dovuto al fatto che la maggior parte degli elementi nelle molecole organiche esistono in natura come miscele di isotopi (stesso n° atomico, ma masse diverse).
Per il C accanto all’isotopo più abbondante (12C), c’è un isotopo di massa 13 pari all’1.1%. Le molecole di una data specie contenenti il 13C daranno allora ioni molecolari a massa 79, cioè picchi isotopici M + 1.

CONVENZIONEnella spettrometria di massa il calcolo dei pesi molecolari viene fatto sempre sugli isotopi più abbondanti (C: 12; H: 1; N: 14, O:
16; Cl: 35; Br: 79).
Metano: CH4
Per 100 molecole di metano a PM = 16 (12C), ve ne sono 1.1 a peso 17 (13C). Si trascura il contributo del deuterio.

Molecole complesse: situazione generalePer molecole complesse contenenti C, H, O, ed N, l’intensità del primo picco isotopico sarà data dalla somma delle abbondanze degli ioni che contengono uno degli isotopi più pesanti (13C, 15N, 17O).
La formula semplificata per effettuare il calcolo è:
M + 1 / M = 1.1 x C + 0.37 x NM + 2 / M = (1.1 x C)2 / 200 + 0.2 x O
dove C = n° atomi di C; N = n° atomi di N; O = n° atomi di O
Ecco allora che se è possibile determinare con precisione l’intensità dei picchi M + 1 e M + 2 nello spettro di massa di una data molecola, si può risalire alla composizione elementare della stessa (questa procedura però non sempre è applicabile).
Massimo n° di atomi di C: si ottiene dividendo l’intensità di M + 1 per 1.1

Determinazione del numero di atomi di Cloro e Bromo
Cloro: 35Cl: 75% ; 37Cl: 25% (rapporto 3 : 1)
Bromo: 79Br: 51%; 81Br: 49% (rapporto 1 : 1)
Sostanze contenenti Cl o Br danno picchi isotopici M + 2 particolarmente intensi: - nel caso del Cl, M + 2 ha intensità pari al 30% di M- nel caso del Br, M + 2 ha circa la stessa intensità di M

Esempi di sostanze clorurate e bromurate

Molecole polialogenate. 1L’intensità ed il numero dei picchi isotopici varia al variare del numero di atomi di cloro o bromo. Ad esempio, per una molecola contenente due atomi di cloro, gli accoppiamenti possibili sono a due a due:
35Cl35Cl, 35Cl37Cl, 37Cl37Cl
ovvero 3 segnali a M, M+2, M+4, le cui intensità sono calcolabili come:
(3 + 1)2
dove:3 ed 1 sono le abbondanze relative dei due isotopi (35 e 37),2 è il numero di atomi di cloro presenti.
Per cui:(3 + 1)2 = 9 + 6 + 1 e, normalizzando
100 + 67 + 11M M + 2 M + 4
quindi, se M = 100, M + 2 ∼ 67% di M, ed M + 4 ∼ il 10% di M.

Molecole polialogenate. 2
In generale, per valutare l’intensità ed il numero dei picchi isotopici per molecole contenenti più atomi di cloro o bromo, si dovrà sviluppare il binomio:
(a + b)n
dovea = abbondanza isotopo più leggerob = abbondanza isotopo più pesanten = numero di atomi di alogeno nella molecola

Molecole polialogenate. 3
Spettro di massa del diclorometano
Intensità teorica dei picchi isotopici di ioni contenenti cloro e bromo
Cl Br

Frammentazioni dello ione molecolare• Le reazioni di frammentazione dello ione molecolare sono vere
e proprie reazioni chimiche di decomposizione che avvengono in fase gassosa e coinvolgono ioni e/o radicali.
• Inoltre poiché la pressione in sorgente è estremamente bassa (elevatissima diluizione), si tratta sempre di reazioni unimolecolari (non si hanno reazioni ione-molecola)
Ioni di frammentazione
Ioni di trasposizione

Classificazione delle reazioni di decomposizione
Si distinguono 3 principali meccanismi di rottura dei legami
1. Rottura α-eterolitica
La reazione origina uno ione ad elettroni pari ed un radicale. Si osserva generalmente quando Z è un gruppo elettron-attrattore. Ad esempio,
CR Z CR +
Z
C C
R
O C R C O+

Le reazioni di decomposizione (continua 1)
2. Rottura α-omolitica
Il legame si rompe ed X è rilasciato come radicale, mentre Y si allontana con la carica positiva.
X Z X + Y
Ph
O
MeC6H5 + MeC=O
m/z 77
Ph
O
Me
C6H5 +m/z 43
MeC O

Schema di α-cleavage

Le reazioni di decomposizione (continua 2)
3. Rottura β-omolitica
In questo caso è il legame in β allo ione radicale a scindersi omoliticamente. E’ poco probabile: in genere (M-R)+ non è stabile. Tuttavia è possibile se si generano ioni tipo chetene, ad es.:
R CH2 C
R'
O H2C C
R'
OR +
R CH2 C O H2C C OR +
m/z 42

MS di interesse per le esperienze di laboratorio
• Alcoli• Composti carbonilici (aldeidi e chetoni)• Idrocarburi aromatici (frammentazioni caratteristiche
e ioni tropilio)• Ammine ed ammidi• Alcheni

Alcoli a catena lungaAlcoli a catena lunga (C≥ 5): lo ione molecolare non si vede quasi mai poiché si
decompone facilmente perdendo una molecola d’acqua. Il picco a massa più alta corrisponde a M+ - H2O e si forma attraverso
trasposizione di idrogeno e successiva rottura α.
L’elettrone non accoppiato forma un nuovo legame con un H in posizione opportuna mediante la rottura di un legame C-H pre-esistente. Si nota il picco a m/z = 31 corrispondente allo ione ossonio(CH2=O+H) generato dalla rottura α vista per gli alcoli leggeri.

n-esanolo
Me
H
Me
H
t-H
HH
- CH3
H
H
H
C5H5 m/z 69
H
t-H
H H HH
H H
H
H+
m/z 41
OH OH+
m/z 31

IdrocarburiSpettri complessiMolte vie di frammentazione
Ionizzazione iniziale: eliminazione di elettroni di tipo σLegami C-C e C-H (stessa energia) si possono rompere con eguale probabilità
C
H
C
He
C
H
C
H
C
H
C
He
C
H
C
H
Ioni molecolari moltoenergetici (poco stabili)

Idrocarburi AromaticiCaratteristiche:
• Ioni molecolari intensi (stabilizzazione notevole della carica nel nucleo aromatico)• Frammentazione scarsa e spettri ben definiti• Serie di ioni a m/z = 39, 40, 51, 52, 65, 66, 77
Il benzene

Il benzeneLo ione molecolare
Ioni frammento

Alchilbenzeni
Questi composti danno luogo a due frammentazioni caratteristiche:1. Rottura benzilica:
Il frammento a m/z = 91 è particolarmente intenso poiché il catione benzilico riarrangia intramolecolarmente per dare il più stabile catione tropilio (carica positiva delocalizzata su sette atomi di carbonio)
2. Trasposizione di McLafferty

Aldeidi e chetoniAldeidi alifatiche. Gli ioni molecolari sono facilmente osservabili Le frammentazioni più comuni sono
H2CCH2
O
H
R H
CH2
R H
H2C
OH
H+
m/z = 44
2. il riarrangiamento di McLafferty
1. la rottura α
La reazione di McLafferty avviene quando è presente un H in γ al carbonile: dà un picco caratteristico di massa pari (44)

Esempio: n-butanale
2 scissioni α: vale la regola di Stevenson

Regola degli elettroni pari
Lo spettro di massa dei composti organici contenenti C, H, O tende ad essere dominato da ioni a massa dispariCiò è legato ai meccanismi di rottura dei legami
1. Lo ione molecolare (ione radicale ad elettroni dispari) infatti, frequentemente decompone per perdita di radicali
M C + R
2. Gli ioni frammento decompongono per perdita di molecole neutre
Pertanto, poiché le molecole con C, H, O sono di massa pari, ed i radicali persi sono di massa dispari, anche gli ioni prodotti saranno di massa dispari

Ammine
Analogie con gli alcoli:
H2C NH2
H2C OH
Analogie con i fenoli:
C6H5 NH2
C6H5 OH
M = 17%, M-1 = 18%, M-CH3 = picco base

Spettri di massa: esempi

Spettri di massa: esercizi

Composto Incognito 7
La formula bruta di questa sostanza è C7H5NO3S. Di quale composto si tratta?

Risposta Composto Incognito 7
1. Il picco molecolare intenso suggerisce una sostanza aromatica. Ciò èconfermato anche da m/z 76 e m/z 50 che indicano un anello disostituito.
2. l’intensità (elevata) del picco M+2 conferma la presenza dello S.3. Le perdite che si possono identificare sono:
i) m/z 140 = M - 43; ii) m/z 120 = M - 63; i) m/z 119 = M - 64;4. Il frammento 43 non può corrispondere né a C3H7 né a CH3CO perché
questi non sono consentiti dalla formula bruta e non compare nello spettro lo ione acilio CH3CO+
5. Il frammento 64 può invece corrispondere ad SO2 (tra l’altro è presente anche uno ione a massa 64)
6. Vi sono quindi due parziali strutture: l’anello aromatico disostituito ed un gruppo SO2. Rimane da sistemare: C, H, N ed O. Le due possibilità sono (C=O)NH oppure HN=C-O. Nello spettro compare però lo ione 104 che suggerisce la formazione del catione C6H4CO+. Le due possibili strutture sono:
SO2
NH
O
NH
SO2
O
I II
Ma solo la struttura I spiegaIl frammento M-43 come [M-CONH]+. ed il frammento 63come [M-SONH]+.

Appendice: modello relazione