La regolazione dellespressione genica Tutte le cellule di un organismo multicellulare possiedono...
-
Upload
celia-vacca -
Category
Documents
-
view
216 -
download
0
Transcript of La regolazione dellespressione genica Tutte le cellule di un organismo multicellulare possiedono...

La regolazione dell’espressione genica
Tutte le cellule di un organismo multicellulare possiedono tutti i geni della propria specie; tuttavia solo una piccolissima frazione è attiva in ogni cellula; per esempio, in una cellula delle isole del pancreas è attivo il gene per l’insulina, non quelli per l’emoglobina (attivi nelle cellule dei midollo osseo, progenitrici dei globuli rossi) o per la pepsina (attivi nelle cellule della mucosa gastrica)
Durante lo sviluppo embrionale di un organismo multicellulare, le cellule destinate a costituire i diversi tessuti e organi attivano in momenti precisi i geni che codificano le proteine che stimolano o inibiscono la proliferazione cellulare e quelle caratteristiche del tessuto in formazione (per esempio osseina per le ossa, cheratina per la pelle)
Anche gli organismi unicellulari hanno bisogno di attivare alcuni geni solo in particolari circostanze (per esempio la presenza di un nutrimento che richiede particolari enzimi) per non sprecare l’energia e le molecole necessarie
Le cellule tumorali hanno perduto, anche in seguito a mutazioni somatiche, la capacità di regolare l’espressione genica relativa alle proteine che controllano la proliferazione cellulare
L’esempio che viene proposto nelle diapositive 2-5 riguarda la regolazione dell’attività dei geni (detta “espressione genica”) relativa agli enzimi per il metabolismo del galattosio in Escheirichia coli (sistema lac)
Dunque nelle prossimità dei geni ci devono essere recettori in grado di percepire segnali provenienti dall’ambiente esterno e veicolati all’interno della cellula; tali recettori devono quindi segnalare ai geni se trascrivere o no, in funzione dei segnali provenienti dall’esterno

Il sistema lac in E. coli
O
C1’
C5’
C2’C3’
HOC6’H2
C4’
OHH
OH
H
H HH
OH OH
H
HO
O
C1’
C5’
C2’C3’
HOC6’H2
C4’
OHH
OH
H
H
O
C1’
C5’
C2’C3’
HOC6’H2
C4’
OHH
OH
H
H
HH
OH
OH
OH
O
C1’
C5’
C2’C3’
HOC6’H2
C4’
OHH
OH
H
H
H
HOH
Lattosio
+ H2O
-galattosidasi
Galattosio Glucosio
L’enzima -galattosidasi, che consente di utilizzare il lattosio come fonte di carbonio e di energia, viene sintetizzato in presenza di lattosio che quindi oltre che esserne il substrato è anche l’induttore della sua sintesi
Dal lattosio è indotta la sintesi di altri 2 enzimi: permeasi e transacetilasi; anche la permeasi è coinvolta nel metabolismo del lattosio, poiché facilita l’ingresso del lattosio nella cellula.

I geni strutturali e il gene I
transacetilasi-galattosidasi
permeasi
Z Y A
Un unico mRNA policistronico
trascrizione
traduzione
F’(lac)
I
I+ = allele normale:Z, Y, A trascrivono in presenza dell’induttore;
I- = mutante costitutivo: Z, Y, A trascrivono sempre;
Is = allele inibente la risposta all’induttore: Z, Y, A non trascrivono mai
Merodiploidi per definire le relazioni funzionali tra gli alleli
I+Z-/I-Z+ Trascrive* con l’induttore
I-Z-/I+Z+ Trascrive* con l’induttore
I-Z-/I-Z+ Trascrive* sempre
IsZ+/I+Z+ Non trascrive mai
IsZ+/I-Z+ Non trascrive mai
1) Is è dominante su I+ che a sua volta è dominante su I-
2) I+ è dominante su I- indipendentemente dalla posizione in cis o in trans rispetto a Z+
Geni lac
*un mRNA per un enzima funzionale

Operatore, promotore e operone
O+Z+/OcZ+ Trascrive* sempre
O+Z+/OcZ- Trascrive* con l’induttore
O+Z-/OcZ+ Trascrive* sempre
IsO+Z+/I+OcZ+ Trascrive* sempre
O+ = allele normale:Z, Y, A trascrivono in presenza dell’induttore;
Oc = mutante costitutivo: Z, Y, A trascrivono sempre
Z Y AO
1) Oc è dominante su O+, ma solo in cis rispetto a Z+ (cis-dominanza)
P
2) Gli alleli normali di P sono cis-dominanti sui mutanti difettivi di P, che impediscono incondizionatamente la trascrizione di Z, Y, A, impedendo l’inserimento della RNA polimerasi
I
operone
Il prodotto del gene I è una proteina diffusibile che, in assenza dell’induttore, si lega ad O e impedisce la trascrizione di Z, Y , A; in presenza dell’induttore non si lega ad O e consente la trascrizione di Z, Y, A
*un mRNA per un enzima funzionale

Regolazione dell’espressione genica nell’operone lac
Z Y AOPIRNA polimerasi
repressore non legato all’induttore, che si lega ad O e impedisce la trascrizione
induttore repressore legato all’induttore, che non si lega ad O e non impedisce la trascrizione
repressore I- senza affinità per O, con cui non si lega mai e non impedisce mai la trascrizione
repressore Is senza affinità per l’induttore, che si lega sempre ad O e impedisce sempre la trascrizione
mRNA
Z Y AOPII-
Is Z Y AOPI
Z Y AOPIOc
P-
operatore senza affinità per il repressore che non lega mai e non impedisce mai la trascrizione
promotore senza affinità per l’RNA polimerasi che impedisce sempre la trascrizione
Z Y AOPI

Ingegneria genetica
Batterio
Cromosoma batterico
PlasmideDNA ricombinante (plasmide)
Batterio ricombinante
duplicazione
Inserimento del plasmide nella cellula batterica
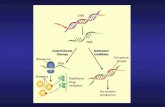
Le tecniche dell’ingegneria genetica permettono di isolare un gene che codifica per una determinata proteina e di inserirlo, mediante dei vettori adatti, nel genoma di un altro organismo. Queste tecniche sono state applicate al campo della medicina per la produzione farmaci, per la diagnosi di malattie genetiche, per la progettazione di vaccini. In agricoltura si stanno progettando piante e animali transgenici, per aumentarne la produttività e migliorarne la qualità. Ma tutto ciò pone problemi nuovi di carattere etico, economico, biologico che devono essere attentamente valutati per la tutela della vita e dell’ambiente.
Copie delle proteine come ad esempio insulina, ormone della crescita
Copie del gene isolato
Cellula contenente il gene da isolare
Plasmide isolato DNA purificato
Gene da isolare

Enzimi di restrizione
Gli enzimi di restrizione sono endonucleasi capaci di tagliare il DNA producendo rotture a doppia elica in corrispondenza di sequenze specifiche di nucleotidi (siti di restrizione); di essi si servono i batteri per distruggere i cromosomi virali
EcoRI
HaeIII
AATTC
endonucleasi
GCTTAAG
Sito di restrizione Tipo di taglio
Sfalsato, adesivo
CCCCGGGG
5’3’
5’3’
Tronco, non adesivo
I siti di restrizione sono brevi sequenze palindromiche: la sequenza posta a un lato rispetto al centro del sito è complementare alla sequenza inversa rispetto a quella posta al lato opposto
Formazione di code
CCGG
5’3’ CC
GGAATT
Si possono aggiungere al 3’ di uno dei 2 filamenti di un capo di un taglio tronco, non “adesivo”, una breve sequenza, ripetizione di un solo nucleotide e al 3’ dell’altro capo la sequenza complementare, rendendo adesivo il taglio
Un taglio è detto adesivo quando:
1) È sfalsato, o sono aggiunti nucleotidi al 3’;
2) I nucleotidi a singolo filamento, sfalsati o aggiunti, sono fra loro complementari
Le estremità di un taglio adesivo si possono unire mediante i legami idrogeno tra le basi complementari presenti a singolo filamento sui 2 segmenti di DNA; successivamente, mediante l’azione di ligasi e, se serve, di DNA polimerasi, si saldano i filamenti polinucleotidici (vedere diapositiva 8)

Mappe di restrizione
1) Si esamina un frammento di DNA, marcandolo con 32P al 5’
2) Si digerisce il frammento con diversi enzimi di restrizione
3) Si stima la lunghezza dei frammenti dallo spazio percorso su un gel mediante elettroforesi
Una mappa di restrizione consiste nell’identificazione della successione dei siti di restrizione per diverse endonucleasi in un segmento di DNA, misurando la distanza tra i siti come numero di nucleotidi
L’elettroforesi consiste nel collocare le macromolecole in un pozzetto all’estremità di un gel (gelatina) che viene poi sottoposto un campo elettrico; le molecole si spostano con una velocità proporzionale alla propria carica elettrica e inversamente proporzionale lla propria lunghezza; poiché nel DNA la carica è distribuita uniformemente, la velocità dipende solo dalla lunghezza del frammento
Siti di restrizione dell’enzima
Siti di restrizione dell’enzima
Marcatura con con 32P

Il DNA ricombinante
VETTORI
Sono cromosomi capaci di replicare e selezionabili, in cui si possono inserire segmenti di DNA di interesse
I vettori possono essere : -plasmidi, -cromosomi di fagi, -ibridi fago-plasmide (cosmidi), tutti capaci di replicarsi in E. coli, -YAC, cioè cromosomi artificiali di lievito, capaci di replicarsi in lievito
In ogni tipo di vettore si può inserire un frammento di DNA di una particolare lunghezza massima
Digestione con endonucleasi
Estremità adesive spontanee o costruite, fra loro uguali
Estremità adesive complementari alle precedenti
DNA polimerasi I + ligasi
vettoreDNA da clonare

La clonazione del DNA
Genoma da saggiare frammentato con enzimi di restrizione
Cromosomi di fago frammentati
ligasi
Genoteca di DNA ricombinante
Ibridazione su filtro con sonda radioattiva complementare al DNA da studiare
Clonazione
Individuazione dei geni clonati: Southern blotting
1) Si effettua l’elettroforesi su gel dei frammenti a doppia elica
2) Si denatura il DNA e lo si fa aderire a singolo filamento, nelle stesse posizioni, a un filtro
3) Si ibridizza con sonda radioattiva complementare al frammento cercato e si effettua l’autoradiografia, localizzando così il gene studiato

Sequenziamento
SEQUENZIAMENTO DEI NUCLEOTIDI
C
1) Si marca con 32P l’estremità 5’ del frammento da analizzare, quindi si denatura il DNA
2) Si distruggono selettivamente basi o loro combinazioni (G, G+A, C, C+T), che rendono più fragile il filamento saggiato, che quindi si rompe in quei punti
G
A
T
G G+A C C+T
3) Si stima la lunghezza dei frammenti dallo spazio percorso in una corsa elettroforetica

Reazione a catena della polimerasi (PCR)
PCR
Primer 1
Primer 2
Taq polimerasi, resistente al caldo
Regione complementare a
Regione complementare a
Si alternano cicli di denaturazione (a temperatura alta) e di replicazione ( a temperatura bassa), ciascuno dei quali porta un raddoppiamento del numero delle molecole

Costruire nuovi geni
SINTESI DI SEQUENZE NON SU STAMPO:
è possibile allungare filamenti di DNA al 5’ aggiungendo nucleotide dopo nucleotide costruendo oligonucleotidi di sequenza voluta
INDUZIONE DI MUTAZIONI SPECIFICHE
1) Si rompe il DNA con endonucleasi
2) Si digeriscono singoli filamenti in direzione 5’ con esonucleasi
3) Si modificano specifici nucleotidi sul filamento rimasto; dopo la replicazione, anche il nuovo filamento sarà mutato nello stesso sito