Elettrofisiologia cellulare Proprietà delle membrane e meccanismi di trasporto.
-
Upload
desiderio-nigro -
Category
Documents
-
view
232 -
download
0
Transcript of Elettrofisiologia cellulare Proprietà delle membrane e meccanismi di trasporto.

Elettrofisiologia Elettrofisiologia cellularecellulare
Proprietà delle membrane Proprietà delle membrane e meccanismi di trasportoe meccanismi di trasporto

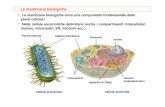
Struttura e funzioni della Struttura e funzioni della membrana cellulare membrana cellulare
La membrana cellulare ha diverse La membrana cellulare ha diverse funzioni:funzioni:
racchiude la cellula e la delimita racchiude la cellula e la delimita definendone definendone i confinii confini
mantiene la separazione fra mantiene la separazione fra citosol e ambiente extracellularecitosol e ambiente extracellulare
media e seleziona il trasporto di media e seleziona il trasporto di determinate sostanze impedendo determinate sostanze impedendo ingresso e uscita di altreingresso e uscita di altre

Le membrane hanno struttura simile a Le membrane hanno struttura simile a
doppio strato con due costituenti doppio strato con due costituenti
principali che sono:principali che sono:
Proteine:Proteine: intriseche ed estrinseche intriseche ed estrinseche
Lipidi:Lipidi: i più abbondanti sono i i più abbondanti sono i fosfolipidi che sono molecole fosfolipidi che sono molecole anfipatiche con una porzione idrofilica anfipatiche con una porzione idrofilica (testa) ed una porzione idrofobica (testa) ed una porzione idrofobica (coda). (coda).
Altri lipidi abbondanti in membrana Altri lipidi abbondanti in membrana sono: glicolipidi e colesterolosono: glicolipidi e colesterolo

Struttura della membrana cellulare con fosfolipidi (in viola) e proteine intrinseche (in azzurro) ed estrinseche (in verde)
Struttura di un fosfolipide


La membrana cellulare è in grado di permettere il passaggio di sostanze in modo selettivo grazie a meccanismi di trasporto. Ricordiamo che il doppio strato lipidico costituisce una barriera al passaggio di tutte le molecole polari cariche, mentre permette il passaggio di piccole molecole polari prive di carica. Le sostanze idrofobiche passano invece bene il doppio strato senza causare
problemi (O2, CO2, N2).

Esistono meccanismi di trasporto che avvengono senza attraversamento della membrana cellulare come:
•Fagocitosi (materiale particolato; vedi macrofagi)
•Pinocitosi (molecole solubili; endocitosi costitutiva)
•Endocitosi (materiale inglobato in seguito ad interazione con recettori; per assunzione di ormoni, fattori di crescita)
•Esocitosi (verso l’esterno. Secrezione di neurotrasmettitori, zimogeni pancreatici etc.)

fagocitosi
endocitosi
pinocitosi
esocitosi

Esistono meccanismi di trasporto che prevedono attraversamento della membrana cellulare. Fra questi ricordiamo:
•Diffusione sempliceDiffusione semplice:: regolata dalla legge di Fick J=-DA dc/dx•Diffusione facilitataDiffusione facilitata (elevata specificità chimica delle proteine trasportatrici)•Trasporto attivoTrasporto attivo (primario e secondario)


Avviene lungo un gradiente di concentrazione e non richiede energia. È un processo che continua fino a quando esiste una differenza di concentrazione.
Un altro tipo di diffusione passiva è il trasporto facilitato. Esso avviene sempre lungo un gradiente di concentrazione, ma necessita di proteine carrier a cui le sostanze trasportate si legano.



La differenza principale è che, mentre la diffusione passiva continua fino a quando esiste un gradiente, il trasporto facilitato ha una saturazione che dipende dal numero di trasportatori utilizzato

Il trasporto attivo entra in gioco tutte le volte che le sostanze sono mosse contro un gradiente di concentrazione. Questo tipo di trasporto implica un dispendio energetico che viene fornito dal consumo di ATP. Per questo tipo di trasporto vale l’equazione di Michaelis- Menten:
V=Vmax · [S] / (Km + [S])

Un esempio tipico di trasporto attivo è la pompa Na-K ATPasi che sposta 3 ioni Na+ verso l’esterno e 2 ioni K+ verso l’interno contribuendo alla negatività della membrana cellulare (pompa elettrogenica). È fosforilata durante il suo ciclo di attività e quindi è indicata come ATPasi di tipo P. È inibita dall’ouabaina che compete per il sito del potassio.Risulta costituita da due subunità:Subunità α detta catalitica di circa 100 kDaSubunità β glicoproteica di circa 50kDa.



Caratteristiche generali Caratteristiche generali degli equilibri ionicidegli equilibri ionici

Na+ Na+
out in
Na+ Na+
out in
Solo gradiente chimico
Gradiente chimico e gradiente elettrico
+-
La grandezza che tiene conto di entrambi i gradienti è il potenziale di equilibrio elettrochimico definito come:

μ = μ0 + RTlnC + zFE
Dove:
μ0= potenziale elettrochimico standard
C= concentrazione dello ionez= valenza dello ioneF= costante di FaradayE= potenziale elettrico
Il flusso netto dello ione è diretto dalla zona a potenziale chimico maggiore alla zona a potenziale chimico minore. Quindi vale:
Δμx = μA (x) – μB (x)
XA XB

Quindi se:Δμ > 0 lo ione X si muove dal compartimento A a quello BΔμ < 0 lo ione X si muove dal compartimento B a quello AΔμ = 0 non c’è flusso netto dello ione X.
Da questo assunto si ricava la legge di Nernst valida per una qualunque specie ionica in equilibrio fra ambiente extra- ed ambiente intra-cellulare. In equilibrio vale Δμ = 0 e quindi se
μA = μB si ha:
RT ln XA / XB + zF (EA – EB) = 0
ΔE = RT / ZF Log (XB / XA)

Potenziale di Nernst per Potenziale di Nernst per NaNa++ e K e K++


Alla fine del 19esimo secolo si sapeva che il citoplasma cellulare è ricco di ioni K+ e che il Na+ è poco concentrato e che questa situazione è opposta nell’ambiente extracellulare. La prima assunzione fatta è stata quella di considerare la membrana permeabile al potassio, ma non al sodio e calcolare quindi il potenziale di riposo trans-membrana come un potenziale di Nernst per il potassio. In realtà la membrana è permeabile al Cl- tanto quanto al potassio e questi due ioni sono fra loro in equilibrio secondo un equilibrio di Donnan che afferma:
[K+]out · [Cl-]out = [K+]in· [Cl-]in
Ogni volta che due ioni possono attraversare la membrana cellulare, il prodotto delle loro concentrazioni extracellulari è uguale al prodotto delle concentrazioni intracellulari

Una differenza di carica elettrica fra interno ed esterno della superficie della membrana è detta potenziale elettrico.Tutte le cellule animali e vegetali sono caratterizzate da un potenziale di membrana di riposo (resting potential) che dipende dal movimento di tutti gli ioni permeabili attraverso la membrana cellulare. Il valore del potenziale di riposo è variabile fra cellula e cellula, ma approssima il potenziale di Nernst dello ione potassio. Vediamo perché.
Quando una o più specie ioniche si distribuiscono sui due lati della membrana cellulare, ciascuna tenderà a spostare il valore del potenziale al valore del suo potenziale di equilibrio elettrochimico.

Tanto più la membrana è permeabile ad una specie ionica, tanto maggiore sarà la forza che tale specie ionica eserciterà nello spostare il valore del potenziale.
In una membrana permeabile a più ioni il potenziale trans-membrana dipende da:
I. Carica elettrica di ciascuno ioneII.Permeabilità della membrana a
ciascuno ioneIII.Concentrazione interna ed esterna
della specie ionica

La formula che meglio descrive il potenziale di riposo di una membrana cellulare è l’equazione di Goldman che considera non soltanto le concentrazioni ioniche delle specie in gioco, ma anche la permeabilità della membrana.

Poiché variazioni delle concentrazioni di cloro non modificano in maniera significativa il potenziale di membrana, il fattore cloro può essere escluso dall’equazione di Goldman. L’equazione finale considera quindi soltanto le specie ioniche Na+ e K+.
In questo modo si ottiene un valore teorico che è molto simile al valore che può essere sperimentalmente misurato. Inoltre, essendo la permeabilità al sodio molto inferiore a quella del potassio (circa 1:100), il potenziale di riposo di un membrana cellulare è molto simile al potenziale di equilibrio elettrochimico per lo ione potassio.


Il fatto che, anche se in piccola percentuale, la membrana a riposo sia permeabile anche al
Na+, fa sì che il potenziale di riposo non sia
esattamente il potenziale di Nernst del potassio, ma sia un po’ meno negativo. Questo dipende dal fatto che il Na+ tende a spostare il potenziale verso il suo potenziale di equilibrio elettrochimico (potenziale di Nernst).Vresting=-70 / -80mV EK=-90mV

The membrane potential of a cell can be measured in millivolts (mV) with the use of a microelectrode and an oscilloscope.(a) Both recording (needle) and reference (block) electrodes are outside of the cell, and no electrical potential (0 mV) is recorded. (b) The recording electrode is inside the cell, the reference electrode is outside, and an electrical potential difference of about 85 mV is recorded, with the inside of the plasma membrane negative with respect to the outside of the plasma membrane.

Consideriamo adesso i fatti visti. Affinché il potenziale di riposo si mantenga dobbiamo mantenere le differenze di concentrazione fra le specie ioniche considerate fra ambiente intra- e extra-cellulare. Per fare questo dobbiamo quindi mantenere i gradienti di concentrazione controbilanciando il movimento passivo degli ioni Na+ verso l’interno della cellula e degli ioni K+ verso l’esterno della cellula. Questo è fatto dalla pompa Na-K ATPasi che mantiene i gradienti ionici spostando ioni sodio e ioni potassio con dispendio di energia. In questo modo il potenziale di riposo può essere mantenuto.

mV
ENa
+
+61mV
0mV
-90mV
-80mVEK+
Vresting

Risposte elettriche Risposte elettriche delle membrane delle membrane
cellularicellulari

Tutte le cellule viventi, animali e vegetali
sono caratterizzate da variazioni del
potenziale di riposo se opportunamente
stimolate. Esistono due tipi di risposta:Risposta elettrica passiva o potenziale Risposta elettrica passiva o potenziale
elettrotonicoelettrotonico: si produce TUTTE le volte
che si fa passare corrente attraverso una
membrana cellulare. Questo accade
perché la membrana cellulare è
caratterizzata da proprietà elettriche di
cui adesso parleremo e che sono:
capacità
resistenza

Risposta attiva o potenziale d’azione o Risposta attiva o potenziale d’azione o
spike:spike: è presente nelle cosiddette cellule
eccitabili, vale a dire neuroni, cellule
muscolari e cellule secretorie (ad esempio
le cromaffini del surrene). Utilizza
strutture particolari e cioè canali di
membrana e in particolare canali del Na+
e canali del K+. Questa risposta può
esserci o non esserci e vedremo quali sono
le condizioni.
N.B. La risposta elettrotonica
compare sempre, indipendentemente
dall’attivazione di canali

Potenziale Potenziale elettrotonicoelettrotonico

La membrana cellulare è formata da un
doppio strato lipidico in cui sono inserite
proteine che hanno la funzione di
trasportare materiale attraverso la
membrana. Il doppio strato lipidico, dal
punto di vista elettrico si comporta come
un condensatore, cioè ha la capacità di
separare le cariche sui due lati della
membrana. Le due piastre conduttrici
sono rappresentate dal mezzo
intracellulare e da quello extracellulare.
Il dielettrico isolante è rappresentato dal
doppio strato lipidico.

Si definisce capacità la seguente
grandezza:
C= ε A / d
dove ε è la costante dielettrica del mezzo,
A è l’area della membrana e d è la
distanza fra le piastre cioè lo spessore
della membrana. Per le membrane
cellulari si preferisce parlare di capacità
specifica in modo da evitare il fattore
area. Questa si definisce come Cm= C /A da
cui si ottiene:
Cm= ε / d
Per le membrane cellulari dove A=25Å si
ha un valore di Cm=1μF/cm2

Nella membrana cellulare si trovano
anche proteine canale che permettono il
passaggio di ioni. Queste strutture sono
responsabili della seconda caratteristica
della membrana cellulare, cioè della
conduttanza (1/R). Questa grandezza è la
seconda componente del circuito elettrico
equivalente della membrana cellulare.

A questo punto dobbiamo includere
nell’equivalente elettrico della membrana
il potenziale di membrana. Questo esiste
sempre grazie alla ridistribuzione degli
ioni determinata dai gradienti elettrici e
chimici. A riposo questo potenziale è
detto resting potential e si rappresenta
come una batteria.

Sulla base di questo possiamo vedere
come risponde una membrana cellulare
opportunamente stimolata e perché la
risposta passiva compare sempre.


Il circuito equivalente deve tenere conto
di tutte le conduttanze ioniche presenti e
quindi di tutte le batterie dei diversi
sistemi ionici e del corrispondente
potenziale di inversione. Il risultato è il
seguente.

Ion Typical Internal Concentration (mM)
Typical External Concentration (mM)
Nernst Potential (mV)
Na+ 12 145 +67
K+ 155 4 -98
Ca2+ 10-4 1.5 +129
Cl- 4 120 -90
INSIDE
OUTSIDE


Quindi una membrana con queste
caratteristiche se viene stimolata in
modo opportuno, come per esempio da
un passaggio di corrente risponde con
una variazione del potenziale in modo
proporzionale al valore di resistenza e
capacità. Questa variazione di potenziale
prende il nome di potenziale
elettrotonico.
Quando la corrente è iniettata essa
comincia a fluire attraverso la capacità
che tende a caricarsi. La fase di crescita
del potenziale è data da: V= iR (1-e –t/τ)
dove τ=RC. Quando t=RC allora
Vt=63%V0.

RC si definisce
costante tempo
della membrana.
Quando sono
trascorse diverse
costanti tempo, il
potenziale
approssima un
asintoto e tutta la
corrente fluisce
attraverso la
resistenza (Ic=0
perché
Ic=dQ/dt=CdV/dt)
con un valore che
sarà proporzionale
alla legge di Ohm
V=IrR.

Le caratteristiche del potenziale
elettrotonico sono:È sempre presente, in tutti i tipi
cellulari se interviene uno stimolo sulla
membrana cellulareDipende dalle caratteristiche passive
della membrana cellulare, cioè resistenza
e capacitàNon coinvolge attività di canaliÈ proporzionale all’intensità dello
stimolo che lo genera, è cioè un segnale
di tipo analogicoDecade nel tempo e nello spazio con una
costante di spazio che dipende dalle
caratteristiche della fibra


Il potenziale decade nello spazio secondo
l’equazione:
Vx=V0 · e-x/λ
dove λ è detta costante di spazio della fibra
e fornisce informazioni su quanto si può
propagare a distanza il potenziale. Si ha
che:
λ=SQR (rm / (ri + re))
con re praticamente trascurabile rispetto a ri
e quindi:
λ=SQR (rm / ri )
La propagazione di un potenziale lungo una
fibra è maggiore se rm aumenta, mentre
diminuisce se aumenta ri. Vedremo
l’importanza di questo fatto per la
propagazione del potenziale d’azione.

Neuroni e Neuroni e
potenziale d’azionepotenziale d’azione

Prima di procedere alla descrizione del
potenziale d’azione facciamo
un’introduzione sui neuroni.
Il neurone è la cellula base del sistema
nervoso: si stima che nel sistema nervoso
ci siano circa 100 miliardi di neuroni!!
Un tipico neurone è costituito da parti
caratteristiche :
Soma o corpo cellulare:Soma o corpo cellulare: contiene il nucleo
all’interno del quale si trova il materiale
genetico.
Dendriti:Dendriti: presenti in grande numero,
rappresentano l’input del neurone. Si
ramificano dal corpo cellulare e ricevono
informazioni da altri neuroni.

Assone o neurite:Assone o neurite: si diparte dal soma. È
unico e rappresenta l’output della cellula.
Da qui si dipartono segnali elettro-chimici
per altri neuroni. Talvolta (come nei
motoneuroni) può essere molto lungo. I
neuriti più lunghi e che necessitano di
elevate velocità di connessione sono
ricoperti da mielina, uno strato isolante
che può portare la velocità di
propagazione del segnale fino a 120 m/s.
Terminale sinaptico:Terminale sinaptico: a questo livello il
segnale elettrico che si è propagato lungo
l’assone è convertito in segnale chimico
che veicola l’informazione al neurone
successivo.

Tra il terminale sinaptico di un neurone
e il dendrite del neurone successivo si
trova uno spazio molto ridotto che
prende il nome di spazio sinaptico di cui
parleremo facendo la sinapsi. Per ogni
neurone ci sono dalle 1.000 alle 10.000
sinapsi!


Una sinapsi neurone-neurone può essere:
Asso-assonica
Asso-somatica
Asso-dendritica



Passiamo ora a vedere il Passiamo ora a vedere il potenziale d’azionepotenziale d’azione

Cenni storici del potenziale Cenni storici del potenziale d’azioned’azione
19021902 Overton scopre che NaOverton scopre che Na++ è importante è importante per la genesi di APper la genesi di AP
19391939 Cole e Curtis e Hodgkin e Huxley Cole e Curtis e Hodgkin e Huxley scoprono che AP si manifesta con scoprono che AP si manifesta con un’inversione della polarità della membrana e un’inversione della polarità della membrana e non si porta semplicemente a 0mVnon si porta semplicemente a 0mV
19491949 Hodgkin e Huxley scoprono che Hodgkin e Huxley scoprono che alterazioni di [Naalterazioni di [Na++]]extracell extracell influenzano l’ampiezza influenzano l’ampiezza dello spikedello spike
19521952 Hodgkin e Huxley propongono Hodgkin e Huxley propongono l’ipotesi del sodio.l’ipotesi del sodio.

Abbiamo detto che il potenziale d’azione
è un tipo di risposta elettrica che si
manifesta solo nelle cellule cosiddette
eccitabili: neuroni, fibrocellule e cellule
secretorie.
Tradizionalmente la trattazione del
potenziale d’azione è fatta su potenziali
neuronali, anche se concettualmente i
meccanismi sono simili se non identici
anche negli altri tipi cellulari.

Condizione necessaria e
sufficiente affinché un
potenziale d’azione possa
innescarsi è che la
depolarizzazione della
membrana cellulare,
opportunamente stimolata,
raggiunga un livello di
potenziale soglia (threshold)

Le caratteristiche più salienti del
potenziale d’azione sono:Una forma particolare (spike) che
presenta un’inversione transitoria
della polarità della membrana
(OVERSHOOT)Propagazione senza decremento per
l’intera lunghezza della fibraRuolo attivo dei canali di membrana
del Na+ e del K+ dipendenti dal
potenzialeSegnale modulato in frequenza:
l’intensità dello stimolo è codificata in
base al numero di spikes per unità di
tempo

Che cosa si intende per canali dipendenti
dal potenziale?
Abbiamo già detto che i canali ionici non
sono altro che proteine trans-membrana
aventi la funzione di veicolare attraverso
la membrana cellulare ioni carichi. Questi
canali possono essere grossolanamente
suddivisi in:Canali dipendenti dal potenziale
(come quelli implicati nel potenziale
d’azione e molti canali Ca2+)Canali ligando-dipendenti: canali che
sono attivati dal legame di una
molecola ad un recettore (ad esempio il
recettore-canale di tipo nicotinico,
recettore GABAA)

Canali attivati meccanicamente: sono
canali attivati da stimoli meccanici di
distensione o stiramento (ad esempio il
canale del Na+ del corpuscolo del
Pacini o i canali del K+ delle cellule
cigliate).



+60
Il potenziale d’azione
+60

1.Depolarizzazione elettrotonica
2.Raggiungimento della soglia e avvio
del ciclo di Hodgkin
3.Fase depolarizzante rapida ascendente
e overshoot
4.Picco
5.Ripolarizzzione
6.Iperpolarizzazione
7.Resting potential

1.
Per quanto riguarda la depolarizzazione
elettrotonica, questa non è altro che una
comune risposta passiva che si
manifesta per le proprietà passive della
membrana. Se questa depolarizzazione
non è sufficiente per arrivare alla soglia,
la risposta della membrana si esaurisce
in un potenziale elettrotonico.

2.-3.
Il ciclo di Hodgkin è un esempio di feed-
back positivo nella fase ascendente dello
spike: l’aumento della conduttanza al
sodio determina un’ulteriore
depolarizzazione che aumenta
maggiormente la conduttanza.

Dipendenza della conduttanza gNa+ dal potenziale di membrana


4.
Il raggiungimento del valore di picco dell’
AP è determinato da due fattori:
I.Raggiungimento del potenziale di
Nernst per lo ione Na+ (circa +65mV).
Vicino a questo valore la forza
elettromotrice sullo ione diminuisce
(f.e.m.=Vm – ENa+) e quindi la corrente
tende a zero perché
INa+=gNa+ · f.e.m.
e se la corrente si azzera significa che
cessa il flusso ionico e quindi il potenziale
non varia più.

I.Inoltre, in maniera ritardata rispetto
ai canali del Na+, si attivano i canali del
K+ di tipo ritardato-rettificante. Al
valore del picco la f.e.m. sullo ione
potassio è massima e vale:
f.e.m. K+= Vm – EK+ = +65mV – (-
90mV)=+155mV
Lo ione potassio ha quindi un gradiente
elettrico e chimico molto favorevole per
uscire dalla cellula.

N.B. Osservare lo sfasamento tra corrente del Na+ e corrente del K+

5. – 6. La fase di ripolarizzazione è dovuta
all’apertura dei canali del potassio e al
flusso di ioni K+ dall’interno all’esterno
della cellula lungo il gradiente
elettrochimico.

L’uscita di potassio dalla cellula tende a
continuare fino al raggiungimento del
potenziale di Nernst per lo ione K+.
Questo significa che il potassio “tira” il
potenziale di membrana a valori più
negativi del valore di resting e da questo
fatto dipende l’iperpolarizzazione
postuma della fase 6. che può
pesantemente condizionare l’eccitabilità
di una cellula (caso tipico è la
modulazione colinergica sulle cellule
pacemaker cardiache).

7.Infine la pompa Na-K ATPasi entra in
gioco per riportare le concentrazioni di
sodio e di potassio ai loro valori corretti,
anche se va detto che durante il
potenziale d’azione la quantità di ioni che
si muove è di gran lunga inferiore al bulk
che determina la concentrazione.

Quindi la risposta
attiva evocata da
uno stimolo
depolarizzante
comporta:Una
componente
rapida inward di
ioni Na+
Una
componente
ritardata e
rettificante
dovuta all’uscita
di ioni K+

Quindi il potenziale d’azione si Quindi il potenziale d’azione si
instaura perché i flussi di Nainstaura perché i flussi di Na++ e e
KK++ cambiano la carica sulla cambiano la carica sulla
membrana cellulare e non perché membrana cellulare e non perché
cambiano le concentrazioni cambiano le concentrazioni
ioniche del citoplasma.ioniche del citoplasma.

Periodo Periodo refrattario refrattario assoluto e assoluto e relativorelativoComportamento dei canali Comportamento dei canali
del sodiodel sodio




PRA ca 1ms
PRR ca 2ms

Propagazione del potenziale Propagazione del potenziale d’azioned’azione
Nei neuroni il potenziale d’azione origina
in una zona particolare detta monticolo
assonico che corrisponde al punto di
emergenza del neurite dal soma cellulare.
In questa zona, non a caso, si trova
un’elevatissima percentuale di canali Na+.
Il meccanismo di propagazione dell’AP si
avvale della capacità di invertire la
polarità della membrana in zone
adiacenti all’AP, generando nuovi AP.


Il potenziale d’azione si propaga per
circuiti locali. L’overshoot determina
un’inversione della polarità della
membrana che genera flussi locali di
corrente di intensità sufficiente da
depolarizzare a soglia le zone limitrofe.
La direzione di propagazione, benché
teoricamente possa avvenire nelle due
direzioni, avviene solo verso valle del
neurite, perché la zona a monte si trova
nello stato refrattario e quindi non è
eccitabile.

Propagazione per
circuiti locali di
corrente

La frequenza massima raggiungibile è
limitata dalla durata del periodo
refrattario assoluto (circa 1ms) a circa
1000 impulsi al secondo per le grosse
fibre nervose.

Conduzione Conduzione saltatoriasaltatoria

Abbiamo visto che la propagazione di un
segnale lungo una fibra è strettamente
influenzato da rm (resistenza specifica di
membrana) e da rin (resistenza
longitudinale interna). La distanza a cui un
potenziale si propaga dipende dalla
costante spazio definita come:
λ=SQR (rm / rin )
Esistono quindi due modi per aumentare la
costante spazio:Aumentare il diametro della fibra secondo
il seguente criterio
r=ρ l/S
e quindi diminuire rin per aumento della
sezione

Creare un miglior isolamento elettrico
della fibra aumentando rm e quindi
diminuire le correnti di “fuga”
La prima situazione è quella che si verifica
per esempio nell’assone gigante di
calamaro che ha un diametro di circa
1mm. Il secondo caso è quello delle fibre
mieliniche. Questo è un avvolgimento di
materiale lipidico, e quindi da un punto di
vista elettrico isolante, che forma 100 o
più strati sul neurite, con interruzioni
ogni 1-2mm note con il nome di nodi di
Ranvier.

L’avvolgimento è determinato da oligodendrociti nel SNC e dalle cellule di Schwann nel SNP.

L’avvolgimento di questi strati fa sì che
la resistenza equivalente sia Rtotale=rm1+
rm2 + rm3 +…..+ rmn e quindi risulti molto
aumentata facendo aumentare λ. Dal
punto di vista capacitivo la capacità
totale diminuisce perché si ha, per
capacità in serie, 1/Cm=Σi 1/Ci.
Essendo C=Q/V vale che la membrana si
carica meglio per una diminuzione della
capacità.
Il potenziale d’azione si propaga da un
nodo di Ranvier all’altro per conduzione
saltatoria.


I circuiti locali si chiudono da un nodo
all’altro, dove la corrente può fluire tra
interno ed esterno e dove la
concentrazione dei canali del sodio è
molto elevata.
La membrana internodale non è in grado
di generare potenziali d’azione. Il
potenziale salta quindi per punti discreti
aumentando moltissimo la velocità di
conduzione delle fibre che può arrivare a
120m/s

La trasmissione sinaptica

L’encefalo umano contiene circa 100
miliardi di neuroni, ciascuno capace di
influenzare molte altre cellule. Pertanto è
necessario un meccanismo dotato di
grande efficienza per rendere possibile la
comunicazione fra questo numero enorme
di elementi. Questa comunicazione è resa
possibile dalle sinapsi, i contatti
funzionali fra i neuroni.
La prima distinzione fondamentale è fra
Sinapsi elettriche: flusso passivo di
corrente elettrica fra un neurone e l’altro
Sinapsi chimiche: comunicazione
possibile grazie alla secrezione di
neurotrasmettitori

Si definisce elemento pre-
sinaptico l’elemento cellulare a
monte della sinapsi e che riceve
un segnale da trasmettere.
Si definisce elemento post-
sinaptico l’elemento cellulare a
valle della sinapsi che riceve
l’informazione

Sono in minoranza rispetto alle sinapsi
chimiche, ma presenti ovunque,
specialmente dove sia necessario
sincronizzare l’attività di un gruppo di
cellule in maniera rapida ed efficiente. Le
due membrane sono molto vicine fra loro
unite da una giunzione comunicante (gap
junction). Queste strutture sono
costituite da canali esattamente allineati
fra loro sulle due membrane (pre- e post-
sinaptica) che formano un poro di
diametro molto maggiore del poro dei
canali ionici visti per il potenziale
d’azione

Questi pori consentono il passaggio anche
di molecole di relative grosse dimensioni
come ATP e alcuni secondi messaggeri.
Gli ioni fluiscono dal neurone pre-
sinaptico al neurone post-sinaptico
veicolando corrente.

Questa struttura implica diverse
conseguenze che differenziano
profondamente la sinapsi elettrica dalla
sinapsi chimica. Una sinapsi elettrica:
•È bidirezionaleÈ bidirezionale: il flusso ionico può
avvenire nelle due direzioni
•Non mostra ritardo sinapticoNon mostra ritardo sinaptico:: è un flusso
ionico estremamente veloce
•Mostra continuità citoplasmaticaMostra continuità citoplasmatica fra i
due elementi
•Distanza fra elemento pre- e post-Distanza fra elemento pre- e post-
sinaptico di 3.5nmsinaptico di 3.5nm contro i 30-50 nm della
sinapsi chimica.


La gap junction è
formata da una
struttura detta
connessone
costituita da 6 sub-
unità dette
connessine che
delimitano un poro
attraverso cui
passano gli ioni.


Le sinapsi elettriche sono diffuse in tutti
i tessuti in cui si ha bisogno di ottenere
un’azione sincrona con trasmissione
rapida dell’informazione. Questo avviene
per esempio a livello del miocardio, dove
si ha bisogno di una contrazione
muscolare contemporanea di tutte le
fibrocellule atriali e ventricolari. Avviene
in alcune aree del SNC (ipotalamo per il
controllo della secrezione ormonale), a
livello di epatociti, fibrocellule lisce
dell’intestino, cellule epiteliali del
cristallino.

Nelle sinapsi chimiche l’elemento pre- e
post-sinaptico sono separati fra loro da
uno spazio di circa 50nm detto spazio
sinaptico (synaptic cleft). Da un punto di
vista microscopico le sinapsi chimiche
sono caratterizzate da vescicole
sinaptiche nella terminazione pre-
sinaptica. Queste vescicole contengono il
trasmettitore chimico diverso a seconda
della sinapsi considerata.
La sinapsi chimica più studiata è la
giunzione neuro-muscolare.


La trasmissione sinaptica in una sinapsi
chimica segue una complessa catena di
eventi che si innesca quando un
potenziale d’azione invade la
terminazione del neurone pre-sinaptico.
Vediamo qual’è la sequenza di eventi.

Elementi di una giunzione neuromuscolare

Il potenziale d’azione causa una variazione Il potenziale d’azione causa una variazione del potenziale della membrana pre-sinaptica del potenziale della membrana pre-sinaptica in senso depolarizzante determinando in senso depolarizzante determinando l’apertura di canali del calcio dipendenti dal l’apertura di canali del calcio dipendenti dal potenziale.potenziale.
Questo, a seguito del fortissimo gradiente Questo, a seguito del fortissimo gradiente chimico esistente (2mM all’esterno e circa 10chimico esistente (2mM all’esterno e circa 10 --
77M all’interno), determina un rapido influsso M all’interno), determina un rapido influsso di ioni Cadi ioni Ca2+2+ all’interno del terminale pre- all’interno del terminale pre-sinaptico.sinaptico.
L’aumento del calcio innesca esocitosi delle L’aumento del calcio innesca esocitosi delle vescicole contenenti il neurotrasmettitorevescicole contenenti il neurotrasmettitore
Le molecole di neurotrasmettitore diffondono Le molecole di neurotrasmettitore diffondono nello spazio sinaptico e si legano a specifici nello spazio sinaptico e si legano a specifici recettori presenti sulla membrana post-recettori presenti sulla membrana post-sinaptica.sinaptica.

Il legame del neurotrasmettitore al suo Il legame del neurotrasmettitore al suo recettore determina una risposta recettore determina una risposta elettrica da parte dell’elemento post-elettrica da parte dell’elemento post-sinaptico. Nel caso della giunzione sinaptico. Nel caso della giunzione neuromuscolare si verificano neuromuscolare si verificano depolarizzazioni che prendono il nome depolarizzazioni che prendono il nome di potenziali di placca (EPP). In genere di potenziali di placca (EPP). In genere in questo tipo di sinapsi la in questo tipo di sinapsi la depolarizzazione indotta è sufficiente depolarizzazione indotta è sufficiente ad arrivare a soglia e determinare ad arrivare a soglia e determinare l’instaurarsi di un potenziale d’azione a l’instaurarsi di un potenziale d’azione a livello muscolare con conseguente livello muscolare con conseguente contrazione della fibra muscolare.contrazione della fibra muscolare.


Pre
Post

Nella giunzione neuromuscolare sono stati
fatti gli studi principali per la
comprensione del funzionamento delle
sinapsi chimiche. Una delle scoperte più
interessanti è stata che la membrana
muscolare mostra piccole modificazioni
del potenziale di membrana (circa 0.4mV)
anche in assenza della stimolazione del
motoneurone pre-sinaptico. Questi
fenomeni spontanei vanno sotto il nome di
potenziali di placca in miniatura (MEPP).
Da un’analisi statistica risulta che ogni
EPP deriva dalla somma di più MEPPs.

Quindi un singolo MEPP corrisponde al
rilascio di una singola vescicola
contenente neurotrasmettitore dal
terminale pre-sinaptico. Un EPP deriva
dall’aumentata probabilità di questo
evento e quindi dalla somma di più
MEPPs. Tale aumentata probabilità deriva
dalla stimolazione elettrica del terminale
pre-sinaptico che induce un rilascio Ca2+-
mediato delle vescicole.
Si dice quindi che a livello sinaptico il
rilascio di neurotrasmettitore è di tipo
quantico, cioè avviene per pacchetti
discreti di neurotrasmettitore.

Distribuzione dei MEPPs
Distribuzione quantica delle ampiezze degli EPPs

Nei motoneuroni che, a livello di
giunzione neuromuscolare, utilizzano
acetilcolina (ACh) come
neurotrasmettitore, le vescicole
contengono una concentrazione di ACh
di circa 100mM che corrisponde a circa
10.000 molecole di neurotrasmettitore
per vescicola.

Abbiamo detto che il rilascio di vescicole
è Ca2+-dipendente e dipende da un
aumento del calcio citoplasmatico
dovuto all’ingresso degli ioni attraverso
canali del cacio dipendenti dal
potenziale.
Nel processo di esocitosi delle vescicole
sono coinvolte numerose proteine fra cui
la sinaptotagmina che funziona come
sensore per l’aumento del calcio
intracellulare e innesca quindi il
meccanismo di fusione delle vescicole.


NeurotrasmettitoriNeurotrasmettitori
Il ciclo di attività di tutti i Il ciclo di attività di tutti i neurotrasmettitori è simile.neurotrasmettitori è simile.
Sono sintetizzati e immagazzinati nelle Sono sintetizzati e immagazzinati nelle vescicole della cellula pre-sinapticavescicole della cellula pre-sinaptica
Sono liberati in seguito ad esocitosi Sono liberati in seguito ad esocitosi delle vescicole ed interagiscono con delle vescicole ed interagiscono con recettori specifici di una o più cellule recettori specifici di una o più cellule post-sinaptichepost-sinaptiche
Sono rapidamente rimossi o degradati Sono rapidamente rimossi o degradati nello spazio sinaptico.nello spazio sinaptico.

I neurotrasmettitori sono in genere
suddivisibili in due grandi categorie:
•Piccole molecole:Piccole molecole: in genere mediano
reazioni rapide (Ach, NE, Glutammato,
GABA, Gly, Dopamina, etc..)
•Neuropeptidi:Neuropeptidi: tendono a modulare
funzioni cerebrali più lente e continue (L-
ENK, M-ENK, sostanza P, neurotensina,
etc…)
Entrambi si legano comunque a recettori
e tendono a modificare le proprietà
elettriche dell’elemento post-sinaptico.

In base a quali criteri si identifica un In base a quali criteri si identifica un neurotrasmettitore?neurotrasmettitore?
La sostanza deve essere presente nel La sostanza deve essere presente nel neurone pre-sinaptico (e anche tutti neurone pre-sinaptico (e anche tutti gli enzimi per produrla)gli enzimi per produrla)
Il rilascio della sostanza deve Il rilascio della sostanza deve avvenire in risposta ad una avvenire in risposta ad una depolarizzazione pre-sinaptica che depolarizzazione pre-sinaptica che deve essere Cadeve essere Ca2+2+-dipendente-dipendente
La membrana dell’elemento post-La membrana dell’elemento post-sinaptico deve portare i recettori per sinaptico deve portare i recettori per quella sostanza.quella sostanza.

Sostanza presente
Evento Ca2+-dipendente
Recettori presenti

Attualmente sono noti numerosissimi
neurotrasmettitori e fra questi anche
alcuni ormoni che possono in alcuni
distretti cerebrali avere una funzione in
sinapsi (ad esempio ossitocina e
vasopressina).
Inoltre si sa che i neuroni possono
liberare anche più di un tipo di
neurotrasmettitore: si parla di co-
trasmettitori.
Vediamo qualcosa , in modo schematico,
sulla sintesi dei neurotrasmettitori.


I neurotrasmettitori a piccole molecole
sono sintetizzati nelle terminazioni pre-
sinaptiche. Gli enzimi necessari sono
trasportati con trasporto assonico lento
ad una velocità di 0.5-5mm/die. Le
molecole precursore utilizzate sono
trasportate da proteine trasportatrici.

I neurotrasmettitori peptidici sono
prodotti per trascrizione genica sotto
forma di precursori che subiscono
modificazioni nel REG e poi nel Golgi. Le
vescicole sono poi trasportate alla
terminazione lungo l’assone con trasporto
assonico rapido (fino a 400mm/die) lungo
i microubuli.

Dopo che il trasmettitore ha svolto la sua
azione legandosi al suo recettore
specifico, deve essere rapidamente
rimosso per estinguere l’effetto.
Questo può avvenire per retro-trasporto
all’interno del terminale pre-sinaptico
(NE) o per degradazione ad opera di
enzimi specifici (ACh) o per la
combinazine di entrambi i processi.
Vediamo un esempio.

Diffusione al di fuori dello spazio sinaptico
Degradazione enzimatica
Re-uptake


Recettori dei Recettori dei neurotrasmettitorineurotrasmettitori
I neurotrasmettitori generano I neurotrasmettitori generano
risposte elettriche negli elementi risposte elettriche negli elementi
post-sinaptici legandosi a proteine post-sinaptici legandosi a proteine
di membrana dette recettori. Questi, di membrana dette recettori. Questi,
a loro volta determinano in modo a loro volta determinano in modo
diretto o indiretto apertura o diretto o indiretto apertura o
chiusura di canali ionici della chiusura di canali ionici della
membrana post-sinaptica. Il tipo di membrana post-sinaptica. Il tipo di
canale determinerà se l’effetto del canale determinerà se l’effetto del
trasmettitore è eccitatorio oppure trasmettitore è eccitatorio oppure
inibitorio.inibitorio.

I recettori si dividono in due classi
principali:
Recettori a gating diretto: sono recettori
che, oltre a portare il sito di legame per il
trasmettitore sono anche canali. Ad
esempio i recettore colinergico nicotinico,
il recettore GABAergico A, il recettore
NMDA per il glutammato, recettore AMPA-
kainato, recettore serotoninergico 5-HT3.
Recettori a gating indiretto: sono
accoppiati ad un canale attraverso un G-
proteina ed eventualmente un sistema di
secondi messaggeri. Ad esempio i recettori
α- e β-adrenergici, i recettori colinergici
muscarinici (M1-M5), GABAB e i recettori
per tutti i neuropeptidi.

Recettore a gating diretto: recettore nicotinico

Recettore a gating indiretto: recettore muscarinico M2

La risposta elettrica dell’elemento post-sinaptico in seguito a rilascio di neurotrasmettitore è stato studiato ancora una volta sulla giunzione neuromuscolare, che risulta essere particolarmente accessibile a misure elettrofisiologiche. ACh rilasciata nello spazio sinaptico si lega al recettore nicotinico e in particolare alle due sub-unità α determinando l’attivazione di un canale cationico che permette l’ingresso di Na+ e Ca2+ e l’uscita di K+. La risultante corrente prende il nome di corrente di placca e determina a sua volta una variazione del potenziale in senso depolarizzante (eccitatorio) di membrana noto con il nome di EPP.


Spazio sinaptico
Muscolo

Risulta formato da 5 sub-unità:2 sub-unità α: presentano il sito di legame per ACh e per neurotossine1 sub-unità β1 sub-unità γ (ε nel feto): insieme alle α e δforma il sito per ACh1 sub-unità δ
I recettori nicotinici di una giunzione
neuromuscolare sono circa 107/108 con
una densità di 20000/µm2, clusterizzati
intorno alla zona di contatto sinaptico.

Il potenziale di inversione del recettore
nicotinico, cioè quel valore di potenziale a
cui la corrente netta attraverso il canale è
zero, vale circa -10mV. Questo, attraverso
considerazioni di vario tipo, porta a
stabilire che le correnti che passano
attraverso il recettore-canale siano:
•Una corrente al Na+ in ingresso
•Una corrente al K+ in uscita
Questo significa in effetti che più o meno
vale:
VEPP = (ENa+ + EK+)/2 = (+60mV – 90mV)/2
= -17mV

Quindi, questo significa che ogni volta che
2 molecole di ACh si legano alle sub-unità
α del recettore nicotinico sulla membrana
muscolare, inizia a passare una corrente
mista Na-K attraverso il canale del
recettore. Questa corrente di placca
determina una depolarizzazione locale
(EPP) della membrana e questo flusso di
corrente continua in senso depolarizzante
fino a quando il potenziale di membrana
approssima i -17mV, cioè il potenziale di
inversione dell’EPP.

Rivediamo la sequenza completa degli eventi



Quando più EPPs si sommano fra loro, il
livello di depolarizzazione è sufficiente ad
attivare il ciclo di Hodgkin dei canali del
Na+ e quindi ad evocare il potenziale
d’azione per dare inizio alla contrazione
muscolare.

Sinapsi Sinapsi eccitatorie e eccitatorie e
sinapsi inibitoriesinapsi inibitorie

I potenziali post-sinaptici modificano la
probabilità che si produca un potenziale
d’azione nella cellula post-sinaptica.
Se la probabilità di uno spike
aumenta si parla di potenziali post-
sinaptici eccitatori EPSP (vedi
placca motrice).
Se la probabilità di uno spike
diminuisce si parla di potenziali
post-sinaptici inibitori IPSP (vedi
sinapsi GABAergiche).

Quello che distingue fondamentalmente
un EPSP da un IPSP è il valore del
potenziale di inversione rispetto al
potenziale soglia necessario per evocare
uno spike.
In una sinapsi eccitatoria il potenziale
post-sinaptico sposta il potenziale di
membrana verso il valore soglia, mentre
in una sinapsi di tipo inibitorio il
potenziale post-sinaptico sposta il valore
della membrana lontano dal valore soglia,
talvolta addirittura iperpolarizzando la
membrana. Le sinapsi inibitorie più
diffuse sono le sinapsi GABAergiche (PNS)
e glicinergiche (CNS) che attivano una
conduttanza al Cl-.

EPSP

Si può parlare di inibizione
pre-sinapticapre-sinaptica: l’azione inibitoria è sul
neurone pre-sinaptico, cioè modula
l’azione eccitatoria dell’elemento pre-
sinaptico.
post-sinapticapost-sinaptica: l’azione inibitoria è
sull’elemento post-sinaptico,
riducendone l’eccitabilità

azione inibitoria
Pre-
Pre-
Post-

Pre-
Pre-
Post-
Inhibitory synapse

Inibizione pre-sinaptica
Inibizione post-sinaptica

Sommazione dei potenziali Sommazione dei potenziali sinapticisinaptici
In generale, soprattutto a livello di CNS,
ogni neurone riceve in input il segnale
proveniente da decine a migliaia di
sinapsi. La cellula post-sinaptica è in
grado di integrare tutti questi segnali
grazie a fenomeni che vanno sotto il nome
di sommazione spaziale e sommazione
temporale.

Sommazione spaziale= è la somma
dell’effetto di input sinaptici multipli in
punti diversi del soma e dei dendriti
della cellula. Due stimoli eccitatori
sotto-soglia possono, se sommati, dare
una depolarizzazione che arriva a soglia.
Sommazione temporale= è l’accumulo di
deplarizzazioni successive dovute
all’attività ripetitiva. Ciascun potenziale
si somma al precedente sulla fase di
discesa.