De Tullio GE chim org 2 - … · gruppo -CH3). Come l’ammoniaca anche le ammine hanno carattere...
Transcript of De Tullio GE chim org 2 - … · gruppo -CH3). Come l’ammoniaca anche le ammine hanno carattere...
AMMINESono derivati dell’ammoniaca (NH3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH3). Come l’ammoniaca anche le ammine hanno carattere basico, perché come l’ammoniaca posseggono un doppietto elettronico non condiviso sull’atomo di azoto. Le ammine possono essere primarie secondarie o terziarie a seconda che all’azoto (simbolo N) siano legati al posto dell’idrogeno dell’ammoniaca rispettivamente uno, due o tre gruppi -R .
.
H N H R N H R N R R N R
H H H R
AMMONIACA PRIMARIA SECONDARIA TERZIARIA
Formalmente l’ammoniaca, le ammine primarie e secondarie reagiscono con gli acidi carbossilici liberando una molecola d’acqua e formando un’ammide.
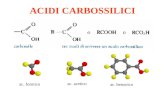
ACIDI CARBOSSILICI Sono caratterizzati dalla presenza del gruppo carbossilico o carbossile –COOH. Formula generale R-COOH. Prendono il nome dal corrispondente alcano con uguale numero diatomi di carbonio sostituendo al suffisso “-ano” il suffisso “-oico”.Per esempio dal metano (CH4) deriva l’acido metanoico che contiene solo un atomo di carbonio, detto anche acido formico H-COOH.
Sono composti a carattere acido, il gruppo funzionale è il gruppo carbossilico
Acido oleico (∆9 ottadecenoico): CH3-(CH2)7 -CH=CH-(CH2)7-COOHE’ a 18 atomi di carbonio e presenta un doppio legame “-CIS” tra il carbonio 9 e il carbonio 10. (La lettera ∆ indica l’atomo di carbonio che presenta il doppio legame e le lettere “en” indicano che deriva da un alchene che ha almeno un doppio legame)
TRIGLICERIDISono i costituenti fondamentali dei grassi e degli oli. I grassi di origine animale, come il burro, lo strutto ed il lardo sono solidi a temperatura ambiente a causa dell’elevato contenuto in acidi grassi saturi, mentre i grassi di origine vegetale, come l’olio di oliva o di semi, che contengono numerosi acidi grassi insaturi, sono liquidi nelle stesse condizioni. I trigliceridi sono esteri dell’alcol 1,2,3 propantriolo o glicerolo o glicerina, con tre molecole di acidi grassi, che possono essere uguali o diversi, nel primo caso il trigliceride èdetto semplice, nel secondo caso complesso.Gli acidi grassi più comuni non sono ramificati e possiedono un numero pari di atomi di carbonio.
CH2-OH
CH-OH
CH2-OH
O R-C-OH+3
CH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
+3 H2OCH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
CH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
CH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
CH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
CH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
CH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
FOSFOLIPIDINei fosfolipidi due gruppi ossidrilici del glicerolo sono esterificati da due acidi grassi mentre il terzo è esterificato dall’acido fosforico che ,a sua volta, è coniugato ad altre molecole (serina, colina, etanolammina, ecc.)
I fosfolipidi sono molecole anfipatiche formate da una parte polare contenente il gruppo fosfato (“testa polare”) e da una parte idrofobica formata dalle catene idrocarburiche degli acidi grassi. Essi rappresentano i principali costituenti delle membrane biologiche
O 3 R-C-O- + Na+
CH2-O-C-R
CH-O-C-R
CH2-O-C-R
O
O
O
CH2-OH
CH-OH
CH2-OH
+3 NaOH
+
SAPONIFICAZIONE
GLICEROLO
ANIDRIDI ACIDO CARBOSSILICO + ACIDO CARBOSSILICO
O O O
CH3-C-OH + CH3-CH2-C-OH CH3-C-O-C-CH2-CH3 + H2O
ESTERI ACIDO CARBOSSILICO + ALCOL ESTERE + ACQUAO O
CH3-C-OH + CH3-CH2-OH CH3-C-O-CH2-CH3 + H20
AMMIDI ACIDO CARBOSSILICO +AMMINA = AMMIDE + ACQUAO O
CH3-C-OH + CH3-CH2-N-H CH3-C N-CH2-CH3 +H20
H H
REAZIONI DEGLI ACIDI CARBOSSILICI (richiedono tutte catalisi acida)
RIBONUCLEOTIDE = base azotata + ribosio + gruppi(o) fosforici
DEOSSIRIBONUCLEOTIDE = base azotata + 2-deossiribosio + gruppi(o) fosforici
ADENINA (base azotata)
RIBOSIO (zucchero)GRUPPI FOSFORICI
nucleoside
nucleoside monofosfato
nucleoside difosfato
nucleoside trifosfato
ATP = Adenosina trifosfato (adenosina = adenina + zucchero)
Il legame AMMIDICO è, in realtà, rappresentabile come un ibrido di risonanza di due formule limite; per questo il legame ammidico ha caratteristica di parziale doppio legame
AMMIDE: Un’ammide contiene sempre un legame carboammidico (se questo legame si forma tra due amminoacidi si può chiamare anche LEGAME PEPTIDICO)
Il legame AMMIDICO è, in realtà, rappresentabile come un ibrido di risonanza di due formule limite; per questo il legame ammidico ha caratteristica di parziale doppio legame
ACIDO CARBOSSILICO +AMMINA = AMMIDE + ACQUAO O
CH3-C-OH + CH3-CH2-N-H CH3-C N-CH2-CH3 +H20
H H
Il legame peptidicoUna coppia di amminoacidi può legarsi attraverso una reazione di condensazione (con eliminazione di una molecola di acqua) fra il gruppo carbossilico di un amminoacido e il gruppo amminico dell'altro, in modo da formare un dipeptide.Il legame peptidico è un legame ammidico, come quello
che si forma fra un acido carbossilico e una ammina primaria.
La gliceraldeide è il capostipite degli zuccheri aldosi (un composto è definito zucchero se contiene almeno un gruppo aldeidico o un gruppo chetonico e almeno un gruppo ossidrilico) e contiene un atomo di carbonio chirale (il carbonio 2).
L’alanina è uno dei 20 amminoacidi (un amminoacido contiene un gruppo amminico e un gruppo carbossilico legati allo stesso atomo di carbonio) e anch’essa contiene un carbonio chirale (il carbonio 2)
ISOMERIAGli isomeri sono composti che hanno stessa formula bruta ma diversa struttura molecolare
•Isomeria di struttura (es: idrocarburi lineari o ramificati)
• Isomeria geometrica (stereoisomeria)(es: alcheni: cis e trans)
• Isomeria ottica : capacità di ruotare il piano della luce polarizzata cioè le molecole chirali hanno potere rotatorio (esempio: zuccheri)
Carbonio chirale (asimmetrico): si dice chirale un atomo di carbonio legato a quattro sostituenti diversi. Ciascun atomo chirale dà luogo a due enantiomeri (cioè a due isomeri che sono l’uno l’immagine non sovrapponibile speculare dell’altro) . Il carbonio deve quindi essere ibridizzato sp3
Sono detti anche zuccheri o idrati di carbonio, perché la formula dei monosaccaridi è Cn(H2O)n con n > 2. Si dividono in monosaccaridi, formati da unità semplici, disaccaridi costituiti da due monosaccaridi uniti con legame glicosidico, fino ai polisaccaridi, formati da moltissime unità.I monosaccaridi, sono o poli-idrossialdeidi (aldosi) o poli-idrossichetoni (chetosi), a seconda che il gruppo carbonilico in essi presente sia aldeidico o chetonico.
ALDOSIQuesti composti possono presentare da tre a sette atomi di carbonio. Sul primo atomo èpresente una funzione aldeidica e su tutti gli altri delle funzioni alcoliche.Il progenitore degli aldosi è la gliceraldeide
CHETOSI
Sul secondo atomo di carbonio èpresente una funzione chetonica e su tutti gli altri atomi di carbonio delle funzioni alcoliche (gr. –OH).
Il progenitore dei chetosi è il diidrossiacetone
Reazioni analoghe avvengono all’interno della molecola del monosaccaride, nel caso del ribosio si ha:
O C-HH-C-OHH-C-OHH-C-OOOHHH CH2OH
D ribosio
H-C-OHHH H-C-OH ΟΟΟΟΟΟΟΟΟΟΟΟ H-C-OHH-C CH2OH
α D ribofuranosio
OHH
1
23
4
5
H
OH
O
OH
H
HCH2OH
Forma ciclicaCon H al posto di OH in posizione 2-----> deossiribosio
Nella forma ciclica il primo atomo di carbonio diventa un nuovo centro chirale, perciò esistono due diasteroisomeri che si differenziano per la configurazione di questo centro detti anomeri (α e β) . Negli zuccheri più comuni l’anomero αpresenta il gruppo OH del primo atomo di carbonio a destra (nella forma furanosica in basso) ed il β a sinistra (nella forma furanosica in alto) ; questa funzione OH non è alcolica, ma semiacetalica ed è detta, nel caso degli zuccheri, glicosidica. Una funzione alcolica è legata ad un atomo di carbonio a sua volta legato ad altri atomi di carbonio. Una funzione semiacetalica è legata ad un atomo di carbonio legato ad un atomo di ossigeno.
forma furanosica
O
furano
AMIDO: è il polisaccaride presente nelle piante con funzione di riserva energetica, costituito da due diverse forme: amilosio e amilopectina. L’amilosio è formato da migliaia di molecole di α D-glucopiranosiolegate con legame α 1-4 glicosidico, la catena ha forma elicoidale. L’amilopectinaha una struttura più compatta, infatti la catena principale strutturata come quella dell’amilosio, presenta numerose ramificazioni nelle quali due molecole di glucosio si uniscono con legame α 1-6 glicosidico.
CELLULOSA: presente nei vegetali con la funzione di sostegno e protezione. Essa èformata da molecole di β D-glucopiranosiolegate fra loro con legame β 1-4 glicosidico. I vertebrati non posseggono enzimi capaci di scindere questo legame per cui non sono in grado di digerire la cellulosa.
Il glicogeno è il polisaccaride di riserva glucidica negli animali. E’ costituito da molecole di α-D-glucosio legate fra loro con legami α,1-4 glicosidici. Ogni 7-11 residui di glucosio esistono delle ramificazioni in cui le molecole di glucosio sono legate con legami α, 1-6 glicosidici. Le unità di glucosio vengono rimosse una per una dalle estremità non riducenti della catena di glicogeno. Quindi le ramificazioni consentono una rapida rimozione di glucosio da più estremità.