Chimica organica e laboratorio Alcheni, alchini Classi terze Docente: Luciano Canu Anno Scolastico...
-
Upload
michelangelo-bettini -
Category
Documents
-
view
255 -
download
14
Transcript of Chimica organica e laboratorio Alcheni, alchini Classi terze Docente: Luciano Canu Anno Scolastico...

Chimica organica e laboratorioChimica organica e laboratorio
Alcheni, alchiniClassi terze
Docente: Luciano CanuAnno Scolastico 2002/2003
Alcheni, alchiniClassi terze
Docente: Luciano CanuAnno Scolastico 2002/2003

2
PrerequisitiPrerequisiti
IdrocarburiAlcani e saturazione Isomeria di posizione e cis-transNomenclatura degli alcaniForze intermolecolariCatalizzatori

3
ObiettiviObiettiviCaratteristiche generali degli alcheni e degli alchiniNomenclatura degli alcheni e degli alchini Concetti di:
Isomero e isomeria cis-transReagente elettrofilo e nucleofilo
Carbocationi e stabilitàProprietà fisicheProprietà chimiche:
Addizioni elettrofile e regola di MarkovnikovOssido-riduzioni

4
Obiettivi operativiObiettivi operativi
Riconoscimento di alcheni e alchini con il saggio del bromo (Br)

5
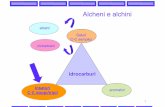
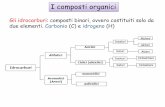
Una panoramicaUna panoramicaI più semplici composti organici sono gli idrocarburi formati da carbonio e idrogeno
Idrocarburi
Saturi
Insaturi
Aperti
Ciclici
Alcani X X
Cicloalcani
X X
Alcheni X X
Alchini X X
Aromatici
X X
Di e polieni
X X
AlcheniAlchini

6
EsercizioEsercizioCerca di riconoscere e classificare i diversi tipi di idrocarburi
CH3
CH3
Idrocarburo
Alcano
Non è un idrocarburo
Non è un idrocarburo
Idrocarburo Cicloalcadiene
Idrocarburo Alchene
Idrocarburo: Alchino
HCCHH3C
CH3
CH3
CH3
CCH
CH3
CH3
OH
H
H
CCH CH3
H
H
CH3
Br
CCH CH
CH3
CH3

7
AlcheniAlcheniLa formula generale degli alcheni (con un solo doppio legame) è
CnH2n
Ci sono 2 atomi di idrogeno in meno poiché 2 elettroni di altrettanti atomi di carbonio sono impegnati in un legame di tipo
H H
C CH H
HH
Questi atomi di carbonio sono ibridati sp2

8
StrutturaStrutturaTutti gli altri atomi di carbonio hanno ibridazione sp3
La geometria di tutti gli atomi di carbonio è trigonale planare (angoli di 120°)La molecola è formata da legami di tipo e da un legame L’alchene più semplice ha 2 atomi di carbonio e 4 atomi di idrogeno (C2H4)Il suo nome è etene
CC
H
H
H
H
CH2H2C

9
Strutture di LewisStrutture di Lewis
CnH2n
C3H6(propen
e)Formula condensata
CH2= CH – CH3
C4H8(butene)
Formula condensata
CH2 = CH CH2 CH3H H
H H
H
HC C C
C C C C
H
H
H
H
H
H
H
H
C4H8(1-
butene)
C4H8(2-
butene)Formula condensata
CH3 – CH= CH- CH2
C C C C
H
H
HH
H
H
H
H
Isomeria della posizione del doppio legame

10
AlchiniAlchiniLa formula generale degli alchini (con un solo triplo legame) è
CnH2n-2
Ci sono 4 atomi di idrogeno in meno poiché 4 elettroni di 2 atomi di carbonio sono impegnati in 2 legami di tipo
H H
C CH H
HH
Questi atomi di carbonio sono ibridati sp

11
StrutturaStrutturaTutti gli altri atomi di carbonio hanno ibridazione sp3
La geometria di tutti gli atomi di carbonio è lineare (angoli di 180°)La molecola è formata da legami di tipo e da 2 legami L’alchene più semplice ha 2 atomi di carbonio e 2 atomi di idrogeno (C2H2)Il suo nome è etino o acetilene
CCH H
CHHC

12
Strutture di LewisStrutture di Lewis
CnH2n-2
C3H4(propino
)
C4H6(butino)
C4H8(1-
butino)
C4H8(2-
butino)
Isomeria della posizione del triplo legame
Formula condensata
CHC CH3
CC CH
H
H
H
Formula condensata
CCH2CH CH3
CC CH C
H
H
H
H
H
CC CH C
H
H
H
H
H
Formula condensata
CH3C C CH3

13
sono isomeri diversi
sono isomeri diversi
non sono isomeri diversi
non sono isomeri diversi
L’isomeria di catenaL’isomeria di catena
L’isomeria di catena è complicata dalla possibilità di trovare i legami multipli in posizioni diverse
Due isomeri possono differire solamente per la posizione del legame multiplo
HCH3C CH2
1-propeneHC CH3H2C
HC
H2CH2C CH3
1-buteneHC
H2C CH2H3C
HC
HC CH3H3C
2-buteneHC
H2CH2C CH3
1-butene
CH2CH3C
CH32-metil-propene
HC
H2CH2C CH3
1-butene

14
EserciziEserciziDisegna i … isomeri del pentene ed assegna loro il nome
H2C
HCH2C
H2C CH3
HC
HCH3C
H2C CH3
HC
HCH3C CH2
CH3
HCCH3C CH3
CH3
H2CCH2C CH3
CH3CH3CH2C
CH3
CH3
1-pentene 2-pentene 3-metil-1-butene
2-metil-2-butene 2-metil-1-butenenon esiste

15
Isomeria cis-transIsomeria cis-transIl doppio legame costituisce una porzione rigida della molecola
La rotazione attorno al doppio legame è impedita (verifica con i modellini)
Alcuni composti con almeno un doppio legame possono presentarsi in due forme isomere
Le due forme possono avere differente polarità, punto di fusione e di ebollizionePossono essere separate con metodi classici di separazione
Gli isomeri cis-trans sono formate dallo stesso tipo di legami e dagli stessi gruppi ma disposti diversamente nello spazio (verifica con i modellini)

16
+
-
+
-
Un esempioUn esempioPer avere questo tipo di isomeria i due atomi di carbonio ibridati sp2 devono
Essere legati con due atomi o gruppi diversi
C CCl
H
H
ClC C
Cl
H
Cl
H1,2-dicloroetilene cistrans
C2Cl2H2
Il baricentro delle due polarizzazioni coincide = la molecola non è polare
Il baricentro delle due polarizzazioni non
coincide = la molecola è polare
pf = -80 °Cpe = +60 °C
pf = -50 °Cpe = +48 °C

17
EsercizioEsercizio
Individua i composti per cui esiste l’isomeria cis-trans
C CH
H
Br
HC C
H
C2H5
CH3
HC C
H
C2H5
CH3
CH3
C CH
H
CH3
H2CH2C CH3
C CH
C3H7
H
H2CH2C CH3
non ha isomeri non ha isomeri
non ha isomeri
ha isomeri
ha isomeri

18
NomenclaturaNomenclatura

19
Gruppi alcheniliciGruppi alcheniliciLe ramificazioni che presentano il doppio legame sono denominati alchen-iliciI 2 più importanti gruppi hanno anche nomi d’uso caratteristici
eten-ile (vinile)2-propen-ile (allile)
H2CHC H2C
HC
H2C
vinile allile

20
Alcheni e alchini sempliciAlcheni e alchini semplici
Il nome degli alcheni prende la desinenza –ene
Etene, propene, butene, pentene, esene, ecc.
Il nome degli alchini prende la desinenza –ino
Etino, propino, butino, pentino, esino, ecc.
Le regole di nomenclatura sono identiche a quelle per gli alcani ma con alcune regola aggiuntive

21
Regola aggiuntiveRegola aggiuntiveDal butene in poi si deve precisare la posizione del doppio o del triplo legame
Si deve dare la priorità al doppio o al triplo legame e numerare di conseguenza
H2CHC
H2C
H2C CH3
1-penteneH3C
HC
HC
H2C
H2C CH3
2-esene
5-metil-2-esene 2-metil-4-esene
H3CHC
HC
H2C
HC CH3
CH3H2C C C C
HC CH3
CH3CH3
C2H5
H
3-etil-2-metil-4-eptino 5-etil-6-metil-3-eptino
1

22
Regole aggiuntiveRegole aggiuntive
2Se ci sono più doppi o tripli legami ci si comporta come con i sostituenti multipli (2,3-dimetil oppure 5,5,3-trietil)
C C CH2C CH3HC
1,3-esandiino
HC C CH2H2C
CH32-metil-1,3-butandiene
HC
HC
HCH3C
HC CH3
2,4-esandiene
La catena da scegliere deve essere sempre quella più lunga ma che contiene il maggior numero di legami multipli, privilegiando quelli doppi per la numerazione
4,5-divinil-4-ottene 3,4-dipropil-1,3,5-esantriene
HC C CH2C
HC CH2
C3H7
C3H7

23
Regole aggiuntiveRegole aggiuntiveCon la presenza contemporanea di doppi e tripli legami per la numerazione si privilegiano i doppi legami ma il nome finale spetta al triplo legame
3
C C CHCHC CH2
C2H5
C3H7
4-etil-3-propil-1,3-esadien-5-ino 3-etil-4-propil-3,5-esadien-1-ino
C CHC
H2C
H2C
HC
HC
H3C CH2CH2
4-vinil-1-otten-5-ino
H2CHC
HC
HC CH2
C CH
3-etinil-1,4-pentadiene 3-vinil-1-penten-4-ino

24
EserciziEserciziDisegna la formula dei seguenti composti insaturi
2,2-dimetil-3-epteneH3C
H2C
H2C
HC
HC C CH3
CH3
CH3
ciclopentino
1,2-dimetilcicloesene
CH3
CH3 1-ciclobutil-2,3-dimetil-3-eptene
H3CH2C
H2C
HC C
HC CH2
CH3
CH3

25
EserciziEserciziScrivi il nome delle seguenti strutture
H3CHC
HC C
H2C CH3
CH3 CH2CH3
4-etil-2-metil-3-esene
C CCH2CH2CH3
CH2CH2CH3
H3CH2C
H3CH2C3-etil-4-propil-3-eptene
C CHCH3
CH2CH3CCC
HCH3C
CH2CH3
3,8-dimetil-4,6-decandiino

26
Comportamento chimicoComportamento chimico

27
Reattività chimicaReattività chimica
Gli alcheni e gli alchini hanno una reattività molto diversa dagli alcani
Sono molto più reattivi e reagiscono con modalità diverse
Perché?È il legame responsabile della maggiore reattività
Più debole del legame Più lontano dallo scheletro della molecolaRappresenta una concentrazione elettronica che attira certi tipi di reagenti
CC
E

28
Gli elettrofiliGli elettrofili
Gli alcheni sono facilmente aggredibili da alcune specie chimiche che hanno affinità con le cariche elettriche
Queste specie chimiche, cariche e no, sono chiamate elettrofile• H+, Cl+, I+, NO2
+, BF3
Sono specie povere di elettroni che cercano di colmare la loro carenza di elettroni
BF
F
F
H+

29
Addizione elettrofilaAddizione elettrofila
Alcheni ed alchini hanno la capacità di incamerare, catturare diverse sostanze e addizionarle alla propria struttura
AcquaAlogeniAcidi alogenidrici ed altri acidi
Sono denominate elettrofile poiché la fase iniziale è sempre caratterizzata dall’attacco di un reagente con tale tendenza

30
Addizione di acidiAddizione di acidiGli acidi alogenidrici (H-X) attaccano gli alcheni fornendo un alogeno alcano (alogenuro alchilico)
CC
H+
CC
H+
Cl-
CC
H
Cl
H3CHC CH2 + H Cl H3C
HC CH2
Cl
H
Le reazioni di addizione elettrofila avvengono in posizione trans

31
I carbocationiI carbocationi
L’addizione di acido cloridrico porta alla formazione quasi esclusiva del 2-cloropropano e non dell’1-cloropropano; perché?Si deve cercare la spiegazione nella formazione della seguente specie:
H3CHC CH2
Cl
H
2-cloropropano
CC
H+ Questa specie chimica
è denominata carbocatione

32
Stabilità dei carbocationiStabilità dei carbocationiIl protone (H+) attacca l’atomo di carbonio formando il carbocatione che ha l’atomo di carbonio più sostituito
I carbocationi sono stabilizzati (aiutati) dalla presenza di altri atomi di carbonio legati direttamente ad esso
C CH3C
H
CH3
CH3
C C+H3C
H
CH3
CH3H
C+ CH3C
H
CH3
CH3H
carbonio terziario
carbonio secondario
(non si forma)

33
Stabilità relativaStabilità relativaQuesto è l’ordine di stabilità dei carbocationi
R indica un qualsiasi gruppo alchilico uguale o diverso
C+R
R
R
> C+R
H
R
> C+H
H
R
> C+H
H
H
>
terziario secondario primario metilico
Queste sono le motivazioni che hanno portato a formulare la regola di Markovnikov

34
Regola di MarkovnikovRegola di MarkovnikovNell’addizione di elettrofili asimmetrici agli alcheni:
Si forma sempre l’isomero che deriva dal catione intermedio più stabile, cioè quello più sostituito
In pratica l’anione si lega al carbonio più sostituitoAnche l’alchene deve essere asimmetrico C C
H3C
H3C
CH3
CH3
C+ CH3C
H3C
CH3
CH3H
C+CCH3
CH3
H3C
H3CH

35
Altre reazioni degli alcheniAltre reazioni degli alcheniAddizione elettrofila di
Acqua in presenza di un catalizzatore acido che fornisce la specie elettrofila (H+)Segue la regola di Markovnikov
CHC CH3
CH3
H3C
H2SO4
H2OC
HC CH3
CH3
H3C
OHHAlogeni (Cl2, I2, Br2)
Non segue la regola di Markovnikov
CHC CH3
CH3
H3C CHC CH3
CH3
H3C
X X
+ X X
meccanismo

36
EserciziEserciziCompleta le seguenti reazioni elettrofile
2-butene con acqua in acido solforico
propene con bromo in CCl4
HC
HCH3C CH3
H2SO4
H2O
HC CHH3C CH3
OH
H
meccanismo
HC CH3H2C
CCl4Br2
CH CH3H2C
Br
Br

37
EserciziEsercizi
Completa le seguenti reazioni elettrofile3-metil-2-esene con HCl
CH2C
HCH3C
H2C CH3
CH3HCl
CH2CCHH3C
H2C CH3
CH3
H Cl

38
RiduzioneRiduzioneAlcheni e alchini possono essere ridotti ad alcani con idrogeno in presenza di un catalizzatoreLa reazione avviene in posizione cis (stesso lato)Alcuni catalizzatori più importanti sono
Palladio finemente suddiviso e disperso su carbonePlatino in forma di ossidoNichel in polvere
C CH3HC
H2H3C
CH3
Pd/CC CH3
HCH3C
HH
CH3

Fine
Alcheni e alchiniAlcheni e alchini

40
1a fase: attacco del protone al doppietto
Addizione di acqua (meccanismo)
Addizione di acqua (meccanismo)
L’acqua non è un elettrofilo sufficientemente forte da attaccare il doppio legame in tempi brevi (anzi è un nucleofilo)È necessario utilizzare un catalizzatore acido (H+)
HC CH3C CH3
CH3
H+
2a fase: formazione del
carbocatione più stabile (terziario)
3a fase: entra il nucleofilo
CH3
HC CH3C CH3
H
+
CH3
HC CH3C CH3
H
+
OH H

41
4a fase: si forma una specie molto
instabile con l’ossigeno carico positivamente
Addizione di acqua (meccanismo)
Addizione di acqua (meccanismo)
L’acqua non è un elettrofilo sufficientemente forte da attaccare il doppio legame in tempi brevi (anzi è un nucleofilo)È necessario utilizzare un catalizzatore acido (H+)
5a fase: l’ossigeno carico
positivamente espelle il protone
6a fase: l’ossigeno ripristina i due
doppietti e libera il protone
(catalizzatore)
CH3
HC CH3C CH3
H
+OH H
CH3
HC CH3C CH3
H
+OH H
CH3
HC CH3C CH3
H
OH
H+

42
I carbocationiI carbocationi
Un carbocatione è una specie chimica organica in cui una carica positiva si trova su un atomo di carbonioLa struttura del carbocatione è questa:
CRR
R
+Atomo di carbonio ibridato
sp2
Orbitale p vuotoOrbitale p vuoto