4.3 AGENTI BIOLOGICI E LABORATORI DI … patogenicità: è la capacità di produrre malattia a...
Transcript of 4.3 AGENTI BIOLOGICI E LABORATORI DI … patogenicità: è la capacità di produrre malattia a...
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 59 di 222
4.3 AGENTI BIOLOGICI E LABORATORI DI BIOSICUREZZA
4.3.1 Definizioni:
Ai sensi del D.Lgs 81/08 (titolo X Art 267):
o agente biologico: qualsiasi microrganismo anche se geneticamente modificato, coltura cellulare ed
endoparassita umano che potrebbe provocare infezioni, allergie o intossicazioni;
o microrganismo: qualsiasi entità microbiologica, cellulare o meno, in grado di riprodursi o trasferire materiale
genetico;
o coltura cellulare: il risultato della crescita in vitro di cellule derivate da organismi pluricellulari.
Microrganismo geneticamente modificato (MOGM): un microrganismo il cui materiale genetico è stato modificato
in modo che non avviene in natura per incrocio e/o ricombinazione naturale;
Infettività: è la capacità di un microrganismo di penetrare e moltiplicarsi nell'ospite;
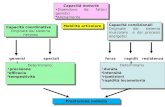
La patogenicità: è la capacità di produrre malattia a seguito di infezione;
La trasmissibilità: è la capacità di un microrganismo di essere trasmesso da un soggetto infetto ad uno suscettibile;
La neutralizzabilità: è data dalla disponibilità di efficaci misure profilattiche per prevenire la malattia o
terapeutiche per la sua cura;
4.3.2 Rischi correlati:
Gli agenti biologici sono fonti di rischio per la salute. In altre parole determinano il rischio di contrarre una
malattia attraverso l’esposizione a materiali, fluidi ed aerosol potenzialmente infetti.
4.3.3 Vie di infezione degli agenti biologici in particolare nei laboratori:
Il contatto con agenti biologici nocivi può avvenire sia nel caso di attività che ne facciano un uso deliberato, sia
nel caso che questi siano presenti per varie ragioni nel luogo di lavoro. Le vie possono essere:
Inalazione: L’inalazione di particelle di aerosol, è una delle vie più frequenti di infezione. Diverse procedure di
lavoro possono produrre goccioline invisibili di aerosol infettante. L’aerosol può essere prodotto da qualsiasi
operazione che comporta versamento o turbolenza di liquidi: pipettaggio (soprattutto se il liquido è espulso con
forza), scuotimento, omogeneizzazione, centrifugazione, liofilizzazione, trattamenti con ultrasuoni, apertura di
contenitori vari (provette piastre, flaconi), rilascio di gas da tubi di coltura. I microrganismi possono disperdersi
nell’aria anche sotto forma di polvere (spore, e preparazioni liofilizzate). Altre fonti di contagio possono essere gli
impianti di climatizzazione (rischio legionella).
Ingestione: In ambiente di lavoro è pericolosa qualsiasi operazione fatta con la bocca. L’ingestione di
microrganismi può avvenire tramite mani sigarette, bicchieri, ecc.
Per contatto o trauma: I microrganismi possono penetrare attraverso la pelle e le mucose di: occhi, naso, bocca.
La penetrazione è facilitata da tagli o graffi anche di minima entità. I banchi da lavoro, la strumentazione, il
vestiario e le superfici in genere possono rimanere contaminati per diversi giorni, mesi o anche anni, nel caso siano
in causa germi sporigeni.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 60 di 222
4.3.4 Attività che comportano rischi correlati agli agenti biologici:
Le più importanti attività lavorative che possono comportare rischio di esposizione ad agenti biologici
nell'ambito dei laboratori universitari sono le seguenti:
Attività in cui vi è impiego di biotecnologie;
Attività dei laboratori clinico-biologici, diagnostici;
Attività di raccolta e conferimento di rifiuti speciali potenzialmente infetti;
Attività nelle quali vi è contatto con animali e/o prodotti di origine animale.
4.3.5 Classificazione degli agenti biologici (DLgs 81/08, Titolo X, art. 268)
In base al DLgs 81/08 (Titolo X art. 268), gli agenti biologici sono ripartiti nei seguenti quattro gruppi a seconda
della loro pericolosità. Le caratteristiche che determinano la pericolosità di un microrganismo sono l’infettività, la
patogenicità, la trasmissibilità, la neutralizzabilità (vedi definizioni).
Agente biologico del gruppo 1: un agente che presenta poche probabilità di causare malattie in soggetti umani;
Agente biologico del gruppo 2: un agente che può causare malattie in soggetti umani e costituire un rischio per i
lavoratori; è poco probabile che si propaghi nella comunità; sono di norma disponibili efficaci misure profilattiche
o terapeutiche;
Agente biologico del gruppo 3: un agente che può causare malattie gravi in soggetti umani e costituisce un serio
rischio per i lavoratori; l’agente biologico può propagarsi nella comunità, ma di norma sono disponibili efficaci
misure profilattiche o terapeutiche;
Agente biologico del gruppo 4: un agente biologico che può provocare malattie gravi in soggetti umani e
costituisce un serio rischio per i lavoratori e può presentare un elevato rischio di propagazione nella comunità; non
sono disponibili, di norma, efficaci misure profilattiche o terapeutiche.
Nel caso in cui l’agente biologico oggetto di classificazione non può essere attribuito in modo inequivocabile ad uno
fra i due gruppi sopraindicati, esso va classificato nel gruppo di rischio più elevato tra le due possibilità. Nell’allegato
XLVI del DLgs 81/08 si riporta l’elenco degli agenti biologici classificati nei gruppi 2, 3 e 4.
4.3.6 Elenco degli agenti biologici classificati (DLgs 81/08, Allegato XLVI)
1. Sono inclusi nella classificazione unicamente gli agenti di cui è noto che possono provocare malattie infettive in
soggetti umani. I rischi tossico ovvero allergenico eventualmente presenti sono indicati a fianco di ciascun agente
in apposita colonna. Non sono stati presi in considerazione gli agenti patogeni di animali e piante di cui è noto che
non hanno effetto sull'uomo. In sede di compilazione di questo primo elenco di agenti biologici classificati non si è
tenuto conto dei microrganismi geneticamente modificati.
2. La classificazione degli agenti biologici si basa sull'effetto esercitato dagli stessi su lavoratori sani. Essa non tiene
conto dei particolari effetti sui lavoratori la cui sensibilità potrebbe essere modificata, da altre cause quali malattia
preesistente, uso di medicinali, immunità compromessa, stato di gravidanza o allattamento, fattori dei quali è tenuto
conto nella sorveglianza sanitaria di cui all’articolo 40.
3. Gli agenti biologici che non sono stati inclusi nel gruppi 2, 3, 4 dell'elenco non sono implicitamente inseriti nel
gruppo 1. Per gli agenti di cui è nota per numerose specie la patogenicità per l'uomo, l'elenco comprende le specie
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 61 di 222
più frequentemente implicate nelle malattie, mentre un riferimento di carattere più generale indica che altre specie
appartenenti allo stesso genere possono avere effetti sulla salute dell'uomo. Quando un intero genere è menzionato
nell'elenco degli agenti biologici, è implicito che i ceppi e le specie definiti non patogeni sono esclusi dalla
classificazione.
4. Quando un ceppo è attenuato o ha perso geni notoriamente virulenti, il contenimento richiesto dalla classificazione
del ceppo parentale non è necessariamente applicato a meno che la valutazione del rischio da esso rappresentato sul
luogo di lavoro non lo richieda.
5. Tutti i virus che sono già stati isolati nell'uomo e che ancora non figurano nel presente allegato devono essere
considerati come appartenenti almeno al gruppo due, a meno che sia provato che non possono provocare malattie
nell'uomo.
6. Taluni agenti classificati nel gruppo tre ed indicati con doppio asterisco (**) nell'elenco allegato possono
comportare un rischio di infezione limitato perché normalmente non sono veicolati dall'aria. Nel caso di particolari
attività comportanti l'utilizzazione dei suddetti agenti, in relazione al tipo di operazione effettuata e dei quantitativi
impiegati può risultare sufficiente, per attuare le misure di cui ai punti 2 e 13 dell'allegato XII ed ai punti 2, 3, 5
dell'allegato XIII, assicurare i livelli di contenimento ivi previsti per gli agenti del gruppo 2.
7. Le misure di contenimento che derivano dalla classificazione dei parassiti si applicano unicamente agli stadi del
ciclo del parassita che possono essere infettivi per l'uomo.
8. L'elenco contiene indicazioni che individuano gli agenti biologici che possono provocare reazioni allergiche o
tossiche, quelli per i quali è disponibile un vaccino efficace e quelli per i quali è opportuno conservare per almeno
dieci anni l'elenco dei lavoratori i quali hanno operato in attività con rischio di esposizione a tali agenti. Tali
indicazioni sono:
A: possibili effetti allergici;
D: l'elenco dei lavoratori che hanno operato con detti agenti dove essere conservato per almeno dieci anni dalla
cessazione dell'ultima attività comportante rischio di esposizione;
T: produzione di tossine;
V: vaccino efficace disponibile,
BATTERI e organismi simili
NB: Per gli agenti che figurano nel presente elenco la menzione « spp » si riferisce alle altre specie riconosciute
patogene per l'uomo.
_____________________________________________________________________________________________
Agente biologico Classificazione Rilievi
_____________________________________________________________________________________________
Actinobacillus actinomycetemcomitans 2
Actinomadura madurae 2
Actinomadura pelletieri 2
Actinomyces gereneseriae 2
Actinomyces israelli 2
Actinomyces pyogenes 2
Actinomyces spp 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 62 di 222
Arcanobacterium haemolyticum 2
(Corynebacterium haemolyticum)
Bacillus anthracis 3
Bacteroides fragilis 2
Bartonella bacilliformis 2
Bartonella (Rochalimea) spp 2
Bartonella quintana (Rochalimea quintana) 2
Bordetella bronchiseptica 2
Bordetella parapertussis 2
Bordetella pertussis 2 V
Borrella burgdorferi 2
Borrella duttonii 2
Borrella recurrentis 2
Borrella spp 2
Brucella abortus 3
Brucella canis 3
Brucella melitensis 3
Brucella suis 3
Burkholderia mallei (pseudomonas mallei) 3
Burkholderia pseudomallei (pseudomonas pseudomallei) 3
Campylobacter fetus 2
Campylobacter jejuni 2
Campylobacter spp 2
Cardiobacterium hominis 2
Chlamydia pneumoniae 2
Chlamydia trachomatis 2
Chlamydia psittaci (ceppi aviari) 3
Chlamydia psittaci (ceppi non aviari) 2
Clostridium botulinum 2 T
Clostridium perfringens 2
Clostridium tetani 2 T,V
Clostridium spp. 2
Corynebacterium diphtheriae 2 T,V
Corynebacterium minutissimum 2
Corynebacterium pseudotuberculosis 2
Corynebacterium spp 2
Coxiella burnetii 3
Edwardsiella tarda 2
Ehrlichia sennetsu (Rickettsia sennetsu) 2
Ehrlichia spp 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 63 di 222
Eikenella corrodens 2
Enterobacter aerogenes/cloacae 2
Enterobacter spp 2
Enterococcus spp 2
Erysipelothrix rhusiopathiae 2
Escherichia coli (ad eccezione dei ceppi non patogeni) 2
Escherichia coli, ceppi verocitotossigenici (es. O157:H7 3(**) T
oppure O103)
Flavobacterium meningosepticum 2
Fluoribacter bozemanii (Legionella) 2
Francisella tularensia (Tipo A) 3
Francisella tularensis (Tipo B) 2
Fusobacterium necrophorum 2
Gardnerella vaginalis 2
Haemophilus ducreyl 2
Haemophilus influenzae 2 V
Haemophilus spp 2
Helicobacter pylori 2
Klebsiella oxytoca 2
Klebsiella pneumoniae 2
Klebsiella spp 2
Legionella pneumophila 2
Legionella spp 2
Leptospira interrogans (tutti i serotipi) 2
Listeria monocytogenes 2
Listeria ivanovil 2
Morganella morganii 2
Mycobacterium africanum 3 V
Mycobacterium avium/intracellulare 2
Mycobacterium bovis (ad eccezione del ceppo BCG) 3 V
Mycobacterium chelonae 2
Mycobacterium fortuitum 2
Mycobacterium kansasii 2
Mycobacterium leprae 3
Mycobacterium malmoense 2
Mycobacterium marinum 2
Mycobacterium microti 3 (**)
Mycobacterium paratuberculosis 2
Mycobacterium scrofulaceum 2
Mycobacterium simiae 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 64 di 222
Mycobacterium szulgai 2
Mycobacterium tuberculosis 3 V
Mycobacterium ulcerans 3 (**)
Mycobacterium xenopi 2
Mycoplasma caviae 2
Mycoplasma hominis 2
Mycoplasma pneumonia 2
Neisseria gonorrhoeae 2
Neisseria meningitidis 2 V
Nocardia asteroides 2
Nocardia brasiliensis 2
Nocardia farcinica 2
Nocardia nova 2
Nocardia otitidiscaviarum 2
Pasteurella multocida 2
Pasteurella spp 2
Peptostreptococcus anaerobius 2
Plesiomonas shigelloides 2
Porphyromonas spp 2
Prevotella spp 2
Proteus mirabilis 2
Proteus penneri 2
Proteus vulgaris 2
Providencia alcalifaciens 2
Providencia rettgeri 2
Providencia spp 2
Pseudomonas aeruginosa 2
Rhodococcus equi 2
Rickettsia akari 3(**)
Rickettsia canada 3(**)
Rickettsia conorii 3
Rickettsia montana 3(**)
Rickettsia typhi (Rickettsia mooseri) 3
Rickettsia prowazekii 3
Rickettsia rickettsii 3
Rickettsia tsutsugamushi 3
Rickettsia spp 2
Salmonella arizonae 2
Salmonella enteritidis 2
Salmonella typhimurium 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 65 di 222
Salmonella paratyphi A, B, C 2 V
Salmonella typhi 3(**) V
Salmonella (altre varietà serologiche) 2
Serpulina spp 2
Shigella boydii 2
Shigella dysenteriae (Tipo 1) 3(**) T
Shigella dysenteriae, diverso dal Tipo 1 2
Shigella flexneri 2
Shigella sonnei 2
Staphylococcus aureus 2
Streptobacillus moniliformis 2
Streptococcus pneumoniae 2
Streptocoocus pyogenes 2
Streptococcus spp 2
Streptococcus suis 2
Treponema carateum 2
Treponema pallidum 2
Treponema pertenue 2
Treponema spp 2
Vibrio cholerae (incluso El Tor) 2
Vibrio parahaemolyticus 2
Vibrio spp 2
Yersinia enterocolitica 2
Yersinia pestis 3 V
Yersinia psoudotuberculosis 2
Yersinia spp 2
VIRUS
_______________________________________________________________________________________________
Agente biologico Classificazione Rilievi
_______________________________________________________________________________________________
Adenoviridae 2
Arenaviridae:
LCM-Lassa Virus complex (Arenavirus del Vecchio Mondo):
Virus Lassa 4
Virus della coriomeningite linfocitaria (ceppi 3
neurotropi)
Virus della coriomeningite linfocitaria (altri ceppi) 2
Virus Mopeia 2
Altri LCM-Lassa Virus complex 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 66 di 222
Virus complex Tacaribe (Arenavirus del Nuovo Mondo):
Virus Guanarito 4
Virus Junin 4
Virus Sabia 4
Virus Machupo 4
Virus Flexal 3
Altri Virus del Complesso Tacaribe 2
Astroviridae 2
Bunyaviridae:
Bhanja 2
Virus Bunyamwera 2
Germiston 2
Virus Oropouche 3
Virus dell'encefalite Californiana 2
Hantavirus:
Hantaan (febbre emorragica coreana) 3
Belgrado (noto anche come Dobrava) 3
Seoul-Virus 3
Sin Nombre (ex Muerto Canyon) 3
Puumala-Virus 2
Prospect Hill-Virus 2
Altri Hantavirus 2
Nairovirus:
Virus della febbre emorragica di Crimea/Congo 4
Virus Hazara 2
Phlebovirus:
Febbre della Valle del Rift 3 V
Febbre da Flebotomi 2
Virus Toscana 2
Altri bunyavirus noti come patogeni 2
Caliciviridae:
Virus dell'epatite E 3(**)
Norwalk-Virus 2
Altri Caliciviridae 2
Coronaviridae 2
Filoviridae:
Virus Ebola 4
Virus di Marburg 4
Flaviviridae:
Encefalite d'Australia (Encefalite della Valle Murray) 3
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 67 di 222
Virus dell'encefalite da zecca dell'Europa Centrale 3(**) V
Absettarov 3
Hanzalova 3
Hypr 3
Kumlinge 3
Virus della dengue tipi 1-4 3
Virus dell'epatite C 3(**) D
Virus dell'epatite G 3(**) D
Encefalite B giapponese 3 V
Foresta di Kyasanur 3 V
Louping ill 3(**)
Omsk (a) 3 V
Powassan 3
Rocio 3
Encefalite verno-estiva russa (a) 3 V
Encefalite di St. Louis 3
Virus Wesselsbron 3(**)
Virus della Valle del Nilo 3
Febbre gialla 3 V
Altri flavivirus noti per essere patogeni 2
Hepadnaviridae:
Virus dell'epatite B 3(**) V,D
Virus dell'epatite D (Delta) (b) 3(**) V,D
Herpesviridae:
Cytomegalovirus 2
Virus d'Epstein-Barr 2
Herpesvirus simiae (B virus) 3
Herpes simplex virus tipi 1 e 2 2
Herpesvirus varicella-zoster 2
Virus Herpes dell'uomo tipo 7 2
Virus Herpos dell'uomo tipo 8 2 D
Virus linfotropo B dell'uomo (HBLV-HHV6) 2
Orthomyxoviridae:
Virus Influenzale tipi A, B e C 2 V(c)
Orthomyxoviridae trasmesse delle zecche: Virus 2
Dhori e Thogoto
Papovaviridae:
Virus BK e JC 2 D(d)
Papillomavirus dell'uomo 2 D(d)
Paramyxoviridae:
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 68 di 222
Virus del morbillo 2 V
Virus della parotite 2 V
Virus della malattia di Newcastle 2
Virus parainfluenzali tipi 1-4 2
Virus respiratorio sinciziale 2
Parvoviridae:
Parvovirus dell'uomo (B 19) 2
Picornaviridae:
Virus della congiuntivite emorragica (AHC) 2
Virus Coxackie 2
Virus Echo 2
Virus dell'epatite A (enterovirus dell'uomo 72) 2 V
Virus della poliomelite 2 V
Rhinovirus 2
Poxviridae:
Buffalopox virus (e) 2
Cowpox virus 2
Elephantpox virus (f) 2
Virus del nodulo dei mungitori 2
Molluscum contagiosum virus 2
Monkeypox virus 3 V
Orf virus 2
Rabbitpox virus (g) 2
Vaccinia virus 2
Variola (mayor & minor) virus 4 V
Whitepox virus (variola virus) 4 V
Yatapox virus (Tana & Yaba) 2
Reoviridae:
Coltivirus 2
Rotavirus umano 2
Orbivirus 2
Reovirus 2
Retroviridae:
Virus della sindrome di immunodeficienza umana 3(**) D
(AIDS)
Virus di leucemie umane a cellule T (HTLV) tipi 1 e 2 3(**) D
SIV (h) 3(**)
Rhabdoviridae:
Virus della rabbia 3(**) V
Virus della stomatite vescicolosa 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 69 di 222
Togaviridae:
Alfavirus:
Encefalomielite equina dell'America dell'est 3 V
Virus Bederau 2
Virus Chikungunya 3(**)
Virus Everglades 3(**)
Virus Mayaro 3
Virus Mucambo 3(**)
Virus Ndumu 3
Virus O'nyong-nyong 2
Virus del fiume Ross 2
Virus della foresta di Semliki 2
Virus Sindbis 2
Virus Tonate 3(**)
Encefalomielite equina del Venezuela 3 V
Encefalomielite equina dell'America dell'Ovest 3 V
Altri alfavirus noti 2
Rubivirus (rubella) 2 V
Toroviridae: 2
Virus non classificati:
Virus dell'epatite non ancora identificati 3(**) D
Morbillivirus equino 4
Agenti non classici associati con le encefaliti spongiformi trasmissibili (TSE) (i):
Morbo di Creutzfeldt-Jakob 3(**) D(d)
Variante del morbo di Creutzfeldt-Jacob 3(**) D(d)
Encefalite spongiforme bovina (BSE) ed altre TSE 3(**) D(d)
degli animali a queste associato
Sindrome di Gerstmann-Stráussler-Scheinker 3(**) D(d)
Kuru 3(**) D(d)
Note
a) Tick-borne encefalitis.
b) Il virus dell'epatite D esercita il suo potere patogeno nel lavoratore soltanto in caso di infezione simultanea o
secondaria rispetto a quella provocata dal virus dell'epatite B. La vaccinazione contro il virus dell'epatite B protegge
pertanto i lavor
c) Soltanto per i tipi A e B.
d) Raccomandato per i lavori che comportano un contatto diretto con questi agenti.
e) Alla rubrica possono essere identificati due virus, un genere "buffalopox" e una variante dei virus "vaccinia",
f) Variante dei "Cowpox"
g) Variante di "Vaccinia".
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 70 di 222
h) Non esiste attualmente alcuna prova di infezione dell'uomo provocata da altri retrovirus, di origine scimmiesca. A
titolo di precauzione si raccomanda un contenimento di livello 3 per i lavori che comportano un'esposizione di tale
retrovirus.
i) Non esiste attualmente alcuna prova di infezione dell'uomo provocata dagli agenti responsabili di altre TSE negli
animali. Tuttavia a titolo precauzionale, si consiglia di applicare nel laboratori il livello di contenimento 3(**) ad
eccezione dei lavori relativi ad un agente identificato di "scrapie" per cui un livello di contenimento 2 è sufficiente.
PARASSITI
_______________________________________________________________________________________________
Agente biologico Classificazione Rilievi
_______________________________________________________________________________________________
Acanthamoeba castellanii 2
Ancylostoma duodenale 2
Angiostrongylus cantonensis 2
Angiostrongylus costaricensis 2
Ascaris lumbricoides 2 A
Ascaris suum 2 A
Badesia divergens 2
Babesia microti 2
Balantidium coli 2
Brugia malayi 2
Brugia pahangi 2
Capillaria philippinensis 2
Capillaria spp 2
Clonorchis sinensis 2
Clonorchis viverrini 2
Cryptosporidium parvum 2
Cryptosporidium spp 2
Cyclospora cayetanensis 2
Dipetalonema streptocerca 2
Diphyllobothrium latum 2
Dracunculus medinensis 2
Echinococcus granulosus 3(**)
Echinococcus multilocularis 3(**)
Echinococcus vogeli 3(**)
Entamoeba histolytica 2
Fascicola gigantica 2
Fascicola hepatica 2
Fascicolopsis buski 2
Giardia lamblia (Giardia intestinalis) 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 71 di 222
Hymenolepis diminuta 2
Hymenolepis nana 2
Leishmania braziliensis 3(**)
Leishmania donovani 3(**)
Leishmania aethiopica 2
Leishmania mexicana 2
Leishmania peruviana 2
Leishmania tropica 2
Leishmania major 2
Leishmania spp 2
Loa Loa 2
Mansonella ozzardi 2
Mansonella perstans 2
Naegleria fowleri 3
Necator americanus 2
Onchocerca volvulus 2
Opisthorchis felineus 2
Opisthorchis spp 2
Paragonimus westermani 2
Plasmodium falciparum 3(**)
Plasmodium spp (uomo & scimmia) 2
Sarcocystis suihominis 2
Schistosoma haematobium 2
Schistosoma intercalatum 2
Schistosoma japonicum 2
Schistosoma mansoni 2
Shistosoma mekongi 2
Strongyloides stercoralis 2
Strongyloides spp 2
Taenia saginata 2
Taenia solium 3(**)
Toxocara canis 2
Toxoplasma gondii 2
Trichinella spiralis 2
Trichuris trichiura 2
Trypanosoma brucei brucei 2
Trypanosoma brucei gambiense 2
Trypanosoma brucei rhodesiense 3(**)
Trypanosoma cruzi 3
Wuchereria bancrofti 2
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 72 di 222
FUNGHI
_______________________________________________________________________________________________
Agente biologico Classificazione Rilievi
_______________________________________________________________________________________________
Aspergillus fumigatus 2 A
Blastomyces dermatitidis (Ajellomyces dermatitidis) 3
Candida albicans 2 A
Candida tropicalis 2
Cladophialophora bantiana (es. Xylohypha bantiana, 3
Cladosporium bantianum o trichoides)
Coccidioides immitis 3 A
Cryptococcus neoformans var. neoformans 2 A
(Filobasidiella neoformans var. neoformans)
Cryptococcus neoformans var. gattili 2 A
(Filobasidiella bacillispora)
Emmonsia parva var. parva 2
Emmonsia parva ver. crescens 2
Epidermophyton floccosum 2 A
Fonsecaea compacta 2
Fonsecaea pedrosoi 2
Histoplasma capsulatum var. capsulatum 3
(Ajellomyces capsulatum)
Histoplasma capsulatum duboisii 3
Madurella grisea 2
Madurella mycetomatis 2
Microsporum spp 2 A
Neotestudina rosatil 2
Paracoccidioides brasiliensis 3
Penicillium marneffei 2 A
Scedosporium apiospermum, Pseudallescheria boydii 2
Scedosporium prolificans (inflantum) 2
Sporothrix schenckii 2
Trichophyton rubrum 2
Trichophyton spp 2
4.3.7 Comunicazioni ed autorizzazioni obbligatorie per l’utilizzo di agenti biologici (Artt. 269 - 270 DLgs
81/08)
Art. 269 (Comunicazione)
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 73 di 222
1. Il datore di lavoro che intende esercitare attività che comportano uso di agenti biologici dei gruppi 2 o 3, comunica
all’organo di vigilanza territorialmente competente le seguenti informazioni, almeno trenta giorni prima dell’inizio
dei lavori:
a) il nome e l’indirizzo dell’azienda e il suo titolare;
b) il documento di cui all’articolo 271, comma 5 (il Documento di Valutazione dei Rischi integrato con ulteriori
informazioni).
2. Il datore di lavoro che è stato autorizzato all’esercizio di attività che comporta l’utilizzazione di un agente biologico
del gruppo 4 è tenuto alla comunicazione di cui al comma 1.
3. Il datore di lavoro invia una nuova comunicazione ogni qualvolta si verificano nelle lavorazioni mutamenti che
comportano una variazione significativa del rischio per la salute sul posto di lavoro, o, comunque, ogni qualvolta si
intende utilizzare un nuovo agente classificato dal datore di lavoro in via provvisoria.
4. Il rappresentante per la sicurezza ha accesso alle informazioni di cui al comma 1.
5. Ove le attività di cui al comma 1 comportano la presenza di microrganismi geneticamente modificati, ai quali si
applicano i livelli di contenimento 2, 3 e 4 individuati all’allegato IV del decreto legislativo 12 aprile 2001, n. 206,
il documento di cui al comma 1, lettera b), è sostituito da copia della documentazione prevista per i singoli casi di
specie dal predetto decreto.
6. I laboratori che forniscono un servizio diagnostico sono tenuti alla comunicazione di cui al comma 1 anche per
quanto riguarda gli agenti biologici del gruppo 4.
Art. 270. (Autorizzazione)
1. Il datore di lavoro che intende utilizzare, nell’esercizio della propria attività, un agente biologico del gruppo 4 deve
munirsi di autorizzazione del Ministero della salute.
2. La richiesta di autorizzazione è corredata da:
a) le informazioni di cui all’articolo 269, comma 1;
b) l’elenco degli agenti che si intende utilizzare.
3. L’autorizzazione è rilasciata dai competenti uffici del Ministero della salute sentito il parere dell’Istituto superiore
di sanità. Essa ha la durata di 5 anni ed è rinnovabile. L’accertamento del venir meno di una delle condizioni
previste per l’autorizzazione ne comporta la revoca.
4. Il datore di lavoro in possesso dell’autorizzazione di cui al comma 1 informa il Ministero della salute di ogni nuovo
agente biologico del gruppo 4 utilizzato, nonché di ogni avvenuta cessazione di impiego di un agente biologico del
gruppo 4.
5. I laboratori che forniscono un servizio diagnostico sono esentati dagli adempimenti di cui al comma 4.
6. Il Ministero della salute comunica all’organo di vigilanza competente per territorio le autorizzazioni concesse e le
variazioni sopravvenute nell’utilizzazione di agenti biologici del gruppo 4. Il Ministero della salute istituisce ed
aggiorna un elenco di tutti gli agenti biologici del gruppo 4 dei quali è stata comunicata l’utilizzazione sulla base
delle previsioni di cui ai commi 1 e 4.
4.3.8 Obiettivi
Progettazione e organizzazione delle procedure di lavoro in modo da minimizzare i rischi per la salute e sicurezza
del personale impiegato;
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 74 di 222
Utilizzo di attrezzature idonee per il lavoro specifico e relative procedure di manutenzione adeguate;
Riduzione al minimo del numero di lavoratori che sono o potrebbero essere esposti;
Riduzione al minimo della durata e dell’intensità dell’esposizione;
Adozione di misure igieniche adeguate per prevenire e ridurre al minimo la propagazione accidentale di un agente
biologico fuori dal luogo di lavoro;
Adozione di misure d’emergenza idonee per affrontare incidenti;
Evitare l’utilizzo di agenti biologici nocivi, se il tipo di attività lavorativa lo consente;
Progettare adeguatamente i processi lavorativi, anche attraverso l’uso di dispositivi di sicurezza atti a proteggere
dall’esposizione accidentale ad agenti biologici;
Adozione di misure collettive di protezione ovvero misure di protezione individuali qualora non sia possibile
evitare altrimenti l’esposizione;
Adozione di metodi di lavoro appropriati, comprese le disposizioni che garantiscono la sicurezza nella
manipolazione, nell’immagazzinamento e nel trasporto all’interno ed all’esterno del luogo di lavoro, degli agenti
biologici pericolosi;
Predisposizione dei mezzi necessari per la raccolta, l’immagazzinamento e lo smaltimento dei rifiuti in condizioni
di sicurezza, mediante l’impiego di contenitori adeguati ed identificabili eventualmente dopo idoneo trattamento
dei rifiuti stessi;
Adozione del segnale di rischio biologico, rappresentato nell’allegato XLV del DLgs 81/08 e altri segnali di
avvertimento appropriati, nei luoghi ove gli organismi possono essere presenti.
4.3.9 Specifiche sulle misure di contenimento e livelli di contenimento (DLgs 81/08 Allegato XLVII)
Art. 275 DLgs 81/08
1. Fatto salvo quanto specificatamente previsto all’allegato XLVI, punto 6, nei laboratori comportanti l’uso di agenti
biologici dei gruppi 2, 3 o 4 a fini di ricerca, didattici o diagnostici, e nei locali destinati ad animali da laboratorio
deliberatamente contaminati con tali agenti, il datore di lavoro adotta idonee misure di contenimento in conformità
all’allegato XLVII.
2. Il datore di lavoro assicura che l’uso di agenti biologici sia eseguito:
a) in aree di lavoro corrispondenti almeno al secondo livello di contenimento, se l’agente appartiene al gruppo 2;
b) in aree di lavoro corrispondenti almeno al terzo livello di contenimento, se l’agente appartiene al gruppo 3;
c) in aree di lavoro corrispondenti almeno al quarto livello di contenimento, se l’agente appartiene al gruppo 4.
3. Nei laboratori comportanti l’uso di materiali con possibile contaminazione da agenti biologici patogeni per l’uomo
e nei locali destinati ad animali da esperimento, possibili portatori di tali agenti, il datore di lavoro adotta misure
corrispondenti almeno a quelle del secondo livello di contenimento.
4. Nei luoghi di cui ai commi 1 e 3 in cui si fa uso di agenti biologici non ancora classificati, ma il cui uso può far
sorgere un rischio grave per la salute dei lavoratori, il datore di lavoro adotta misure corrispondenti almeno a quelle
del terzo livello di contenimento.
5. Per i luoghi di lavoro di cui ai commi 3 e 4, il Ministero della salute, sentito l’Istituto superiore di sanità, può
individuare misure di contenimento più elevate.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 75 di 222
Di seguito si riportano le misure ed i livelli di contenimento riportati nell’Allegato XLVII. Tali misure debbono
essere applicate in base alla natura delle attività, la valutazione del rischio per i lavoratori e la natura dell'agente
biologico di cui trattasi.
Misure di contenimento Livelli di contenimento
2 3 4
1 La zona di lavoro deve essere separata da qualsiasi altra attività nello stesso edificio
No Raccomandato Si
2
L’aria immessa nella zona di lavoro e l’aria estratta devono essere filtrate attraverso un ultra-filtro (HEPA) o un filtro simile
No Si
Filtrazione dell’aria estratta
Si Sull’aria immessa e
sull’aria estratta
3 L’accesso deve essere limitato alle persone autorizzate
Raccomandato Si Si
Attraverso una camera di compensazione
4 La zona di lavoro deve poter essere chiusa a tenuta per consentire la disinfezione
No Raccomandato Si
5 Specifiche procedure di disinfezione Si Si Si
6 La zona di lavoro deve essere mantenuta ad una pressione negativa rispetto a quella atmosferica
No Raccomandato Si
7 Controllo efficace dei vettori, ad esempio roditore ed insetti
Raccomandato Si Si
8 Superfici idrorepellenti e di facile pulitura
Si Per il banco di lavoro
Si Per il banco di lavoro, l’arredo e il pavimento
Si Per il banco di lavoro,
l’arredo, i muri, il pavimento e il soffitto
9 Superfici resistenti agli acidi, agli alcali, ai solventi e ai disinfettanti
Raccomandato Si Si
10 Deposito sicuro per agenti biologici Si Si Si, deposito
sicuro
11 Finestra d’ispezione o altro dispositivo che permetta di vederne gli occupanti
Raccomandato Raccomandato Si
12 I laboratori devono contenere l’attrezzatura a loro necessaria
No Raccomandato Si
13
I materiali infetti, compresi gli animali, devono essere manipolati in cabine di sicurezza, isolatori o altri adeguati contenitori
Ove opportuno Si
Quando l’infezione è veicolata dall’aria
Si
14 Inceneritori per l’eliminazione di carcasse degli animali
Raccomandato Si
(disponibile) Si
(sul posto)
15 Mezzi e procedure per il trattamento dei rifiuti
Si Si Si
Con sterilizzazione 16 Trattamento delle acque reflue No Facoltativo Facoltativo
4.3.10 Sintesi di regole pratiche per laboratori di biosicurezza 1 e 2 (ove si maneggiano microrganismi di
gruppo 1 e 2)
I laboratori di pertinenza del dipartimento DiSVA sono in generale compatibili con un livello di biosicurezza 2.
Per livelli di biosicurezza superiori, sono indispensabili autorizzazioni, strutture e procedure di lavoro maggiori rispetto
a quelle riportate di seguito.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 76 di 222
4.3.10.1 Accesso:
Sulle porte dei laboratori in cui si lavora con microrganismi del gruppo di rischio 2 deve essere esposto il simbolo
internazionale di rischio biologico riportato di seguito (DLgs 81/08 Allegato XLV). Devono essere, inoltre,
riportate le informazioni relative al tipo di rischio, al Responsabile del Laboratorio, il nominativo del personale da
chiamare in caso d’emergenza con i relativi recapiti ed il nominativo del Responsabile dell’autorizzazione
all’accesso.
Solo il personale autorizzato deve poter accedere alle aree del laboratorio.
Le porte del laboratorio devono essere mantenute chiuse.
Nessun animale, ad eccezione di quelli utilizzati nel laboratorio, può accedere.
4.3.10.2 Misure individuali di protezione:
Per tutto il tempo in cui si lavora in laboratorio, devono essere indossati camici, uniformi o divise di laboratorio.
Per tutte le procedure che prevedono contatto diretto o accidentale con sangue, liquidi biologici, animali o altri
materiali potenzialmente infetti, devono essere indossati guanti adeguati. Dopo l’uso, togliersi i guanti facendo in
modo che tale manovra non comporti un’esposizione al rischio (in modo asettico) e autoclavati con gli altri rifiuti
del laboratorio prima dell’eliminazione. Poi lavarsi accuratamente le mani. I guanti riutilizzabili vanno lavati sia
prima che dopo averli tolti, e vanno puliti e disinfettati prima di riutilizzarli.
Il personale deve lavarsi le mani anche dopo aver maneggiato animali o materiale infetto e prima di lasciare l’area
di lavoro nel laboratorio.
Occhiali di sicurezza, schermi facciali o altri dispositivi di protezione devono essere utilizzati quando è valutato
necessario proteggere gli occhi ed il volto da spruzzi, urti e sorgenti di radiazione ultravioletta artificiale.
È proibito indossare gli indumenti protettivi del laboratorio in ambienti esterni (bar, mense, biblioteche, uffici,
ambienti comuni, bagni, ecc).
Nei laboratori non si devono utilizzare calzature aperte.
È proibito mangiare, bere, fumare, truccarsi e maneggiare lenti a contatto nelle aree di lavoro del laboratorio.
È vietato conservare cibi e bevande in qualunque zona delle aree del laboratorio.
Gli indumenti protettivi che sono stati utilizzati nel laboratorio non devono essere conservati negli stessi armadietti
o mobiletti usati per gli indumenti personali.
Gli indumenti per la protezione da agenti biologici devono avere le seguenti caratteristiche.
o devono proteggere tutte le parti esposte (braccia, gambe, il busto, la base del collo, ecc);
o i camici devono avere lunghezza almeno al di sotto del ginocchio;
o le maniche devono essere sufficientemente lunghe per coprire i polsi ed essere provviste di elastici per
impedire l’esposizione della parte interna delle braccia;
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 77 di 222
o gli indumenti costituiti da più arti devono essere progettati in modo da garantire la protezione di tutte le
prevedibili posture di lavoro;
o deve sempre essere assicurata un’adeguata protezione lungo le parti di chiusura;
o devono essere indossati per tutto il tempo in cui permane il rischio di esposizione agli agenti biologici;
o per gli agenti biologici del gruppo 3 è consigliabile la tuta intera, che diventa obbligatoria quando si
manipolano organismi del gruppo 4;
o nel caso si manipolino organismi dei gruppi 3 e 4, le parti di chiusura degli indumenti devono essere
posizionate sul retro;
o gli indumenti devono sempre adattarsi alle esigenze lavorative e devono garantire comfort durante tutto il
periodo del loro impiego.
4.3.10.3 Procedure
È severamente vietato pipettare con la bocca.
Non si deve portare nessun materiale alla bocca. Le etichette non devono essere leccate.
Tutte le procedure di lavoro devono essere svolte cercando di minimizzare la formazione di aerosol o goccioline.
L’uso di aghi ipodermici e siringhe deve essere limitato. Non devono essere utilizzati in sostituzione di altri
strumenti per aspirare o per qualunque altro scopo che non siano iniezioni parentali o aspirazione di liquidi da
animali di laboratorio. Il loro uso pr prelevare il contenuto di bottiglie a diaframma va limitato al minimo (sono
reperibili attrezzi per l’apertura di queste bottiglie, che permettono l’uso delle pipette). Aghi ipodermici e siringhe
non vanno usati come sostituti delle pipette nella manipolazione di fluidi infetti. Si devono usare cannule al posto
degli aghi ogni volta che sia possibile.
Il Responsabile del Laboratorio deve essere avvisato in caso di versamento di liquidi, incidente, esposizione
definita o possibile a materiali infetti. Deve essere inoltre istituito un registro degli incidenti o esposizioni
accidentali.
Predisporre e seguire una procedura scritta per la gestione di ogni versamento accidentale di liquidi.
I liquidi contaminati devono essere decontaminati (chimicamente o fisicamente) prima di essere smaltiti. Potrebbe
essere necessario un sistema di trattamento dei liquidi in uscita in base alla valutazione del rischio per il tipo di
agenti manipolati.
Il materiale cartaceo che dovrà essere portato all’esterno del laboratorio deve essere protetto dalla possibile
contaminazione.
4.3.10.4 Aree di lavoro del laboratorio
Il laboratorio deve essere mantenuto pulito e in ordine, libero dai materiali che non sono necessari al lavoro.
Le superfici di lavoro devono essere decontaminate dopo ogni versamento di liquido potenzialmente contaminato
e alla fine di ogni giornata di lavoro.
Tutti i materiali contaminati, campioni e colture, devono essere decontaminati prima della loro eliminazione o
della pulitura per il loro riutilizzo. Vanno posti in sacche di plastica a tenuta colorate secondo un codice per essere
autoclavati o inceneriti sul posto. Queste sacche vanno poste in contenitori rigidi. Se fosse necessario trasportare le
sacche in altro sito per la decontaminazione, bisogna metterle in contenitori a tenuta (ovvero con fondo solido) che
possono essere chiusi prima di rimuoverli dal laboratorio.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 78 di 222
L’imballaggio ed il trasporto dei campioni devono seguire le norme nazionali e/o internazionali esistenti in
materia.
Le finestre che si possono aprire devono essere dotate di barriere per gli artropodi (es. zanzariere).
4.3.10.5 Gestione della biosicurezza
Il Responsabile del Laboratorio (la persona che ha la responsabilità diretta del laboratorio) ha la responsabilità ed
il compito di assicurare che vengano messi a punto ed adottati, il piano d’emergenza ed il manuale operativo.
Il Preposto alla Sicurezza del laboratorio (che riferisce al Responsabile del Laboratorio) deve assicurare che il
personale venga regolarmente istruito sulla biosicurezza.
Il personale deve essere formato ed informato riguardo ai rischi specifici, deve leggere il manuale di sicurezza o
operativo e seguire le pratiche e le norme raccomandate. È compito del Responsabile del Laboratorio assicurarsi
che le pratiche e le norme vengano comprese da tutto il personale. Una copi del manuale di sicurezza o operativo
deve essere conservata a disposizione nel laboratorio.
Dovrebbe esistere un programma di controllo dei roditori e degli artropodi.
Deve essere valutata la necessità di sottoporre il personale impiegato a sorveglianza sanitaria ed a trattamenti
sanitari.
4.3.10.6 Progettazione e dotazioni del laboratorio
Nel progettare un laboratorio e nell’assegnargli un determinato compito, particolare attenzione va data a
condizioni che notoriamente possono porre dei problemi. Fra queste si ricordano:
La formazione di aerosol;
Il lavoro con grandi volumi e/o concentrazioni di microrganismi;
L’eccessivo affollamento di persone o attrezzature nel laboratorio;
Le infestazioni da roditori ed insetti;
L’accesso di persone non autorizzate.
4.3.10.6.1 Caratteristiche della progettazione
Devono essere assicurati ampi spazi per uno svolgimento sicuro del lavoro di laboratorio, delle pulizie e della
manutenzione.
Muri, soffitti e pavimenti devono essere lisci, facili da pulire, impermeabili ai liquidi e resistenti agli agenti
chimici e ai disinfettanti usati normalmente nel laboratorio. I pavimenti devono essere antiscivolo. I tubi e le
tubature a vista devono essere ben discosti dal muro. Le superfici orizzontali vanno evitate quanto più possibile
per evitare l’accumularsi della polvere.
L’illuminazione deve essere adeguata per tutte le attività. I riflessi indesiderabili e le luci troppo forti vanno
evitati.
Le superfici dei banconi devono essere unite ai muri con una sostanza sigillante, impermeabili all’acqua e
resistenti ai disinfettanti, agli acidi, agli alcali, ai solventi organici e al calore moderato.
I mobili del laboratorio devono essere robusti. Gli spazi aperti fra e sotto i banconi, gli armadi e le attrezzature
devono essere accessibili per la pulizia.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 79 di 222
Devono esserci spazi adeguati per riporre materiali di uso frequente, onde prevenire un eccessivo disordine sui
banconi e nei corridoi. Inoltre vanno assicurati altri spazi, destinati alla conservazione a lungo termine,
convenientemente studiati al di fuori delle aree di lavoro.
In ogni stanza del laboratorio vanno situati lavabi, dotati di acqua corrente, preferibilmente vicino alla porta.
Le porte devono rispondere ad adeguati standard antincendio, chiudersi da se, ed avere pannelli di ispezione.
Nello stesso edificio del laboratorio deve essere disponibile un autoclave (o una pentola a pressione adatta).
Fuori dalle aree di lavoro devono essere disponibili strutture guardaroba per riporre cappotti e oggetti personali e
luoghi dove poter mangiare e bere.
Non vi sono requisiti specifici per l’aerazione. Nel progettare nuove strutture, comunque, va tenuta in
considerazione la possibilità di un sistema di aerazione meccanica che assicuri un flusso d’aria entrante senza
ricircolo. Se non esiste aerazione meccanica, le finestre devono essere apribili, e preferibilmente dotate di reti
contro gli insetti. I lucernai vanno evitati.
Devono essere assicurati adeguati spazi e strutture per utilizzare e conservare in modo sicuro solventi, materiali
radioattivi e gas compressi e liquidi.
I sistemi di sicurezza devono comprendere un sistema antincendio, un impianto elettrico d’emergenza, docce
d’emergenza e dotazioni per i lavaggi oculari.
Devono essere disponibili aree di pronto soccorso o stanze adeguatamente equipaggiate e prontamente
raggiungibili.
È di fondamentale importanza una fornitura idrica di buona qualità e affidabile. Fra la fornitura per l’uso di
laboratorio e quella dell’acqua potabile non devono esserci interconnessioni.
Deve essere disponibile una fornitura elettrica adeguata ed affidabile e un’illuminazione d’emergenza che
permetta un’uscita sicura dal laboratorio. Sarebbe auspicabile avere un generatore d’emergenza per rifornire le
attrezzature essenziali quali gli incubatori, le cappe di sicurezza biologica, i congelatori, ecc, e per l’aerazione,
quando necessaria, delle gabbie per gli animali.
Deve esserci un’adeguata e affidabile fornitura di gas metano. Una buona manutenzione dell’impianto è
indispensabile.
Tre aspetti relativi all’eliminazione dei rifiuti hanno bisogno di speciale attenzione onde soddisfare i necessari
requisiti di efficienza e di prevenzione ambientale:
o le autoclavi per il trattamento dei rifiuti solidi necessitano di una collocazione e di servizi appositamente
studiati;
o gli inceneritori dovrebbero avere una progettazione particolare, essere dotati di post-bruciatori e di apparati
per l’eliminazione dei fumi;
o potrebbe essere necessario decontaminare le acque di scarico.
4.3.10.6.2 Attrezzature del laboratorio
Il rischio infezioni può essere minimizzato utilizzando attrezzature e dotazioni di sicurezza, e pratiche di
laboratorio sicure. Di seguito si riportano le caratteristiche delle attrezzature di laboratorio adatte a lavorare con
microrganismi del gruppo di rischio 2. Il Responsabile del Laboratorio deve assicurarsi che venga fornito un
equipaggiamento adeguato e che venga utilizzato correttamente. Le attrezzature dovrebbero essere scelte tenendo
presenti alcuni principi generali, ovvero dovrebbero essere:
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 80 di 222
progettate in modo tale da prevenire o limitare i contatti fra l’operatore e il materiale infetto;
prodotte con materiali impermeabili ai liquidi, resistenti alla corrosione e dotate di adeguata resistenza strutturale;
prive di punte, spigoli taglienti e di parti in movimento non protette o non bloccabili;
progettate, costruite ed istallate per garantire semplicità d’uso, manutenzione, pulizia, decontaminazione, e
svolgimento delle prove di funzionamento. Materiali in vetro o frangibili vanno, per quanto possibile, evitati;
Potrebbe essere necessario richiedere le specifiche di funzionamento e costruzione, per assicurarsi che le
attrezzature abbiano le necessarie caratteristiche di sicurezza.
4.3.10.6.3 Attrezzature di biosicurezza essenziali
Attrezzatura Rischio eliminato Caratteristiche di sicurezza
Cappe di sicurezza biologica (Classe I)
Aerosol, pulviscolo e schizzi Minimo flusso d’aria entrante nell’area di lavoro protetta. Adeguata filtrazione dell’aria in uscita. Non fornisce protezione del prodotto
Cappe di sicurezza biologica (Classe II)
Aerosol, pulviscolo e schizzi Minimo flusso d’aria entrante nell’area di lavoro protetta. Adeguata filtrazione dell’aria in uscita. Fornisce protezione del prodotto
Cappe di sicurezza biologica (Classe III)
Aerosol, pulviscolo e schizzi Massimo contenimento. Garantisce protezione del prodotto se il flusso laminare è incluso
Isolatori a pressione negativa con pellicole flessibili
Aerosol e pulviscolo Massimo contenimento
Schermi protettivi Schizzi di prodotti chimici Formano uno schermo tra l’operatore e il lavoro.
Propipette
Rischi legati al pipettare a bocca, come ingestione di patogeni, inalazione di aerosol prodotti dalla suzione della pipetta, dal soffiare fuori liquido, dal far gocciolare la pipetta, contaminazione della estremità di suzione delle pipette
Facilità d’uso. Controllo della contaminazione della estremità di suzione della pipetta per proteggere la propipetta, l’operatore e il circuito del vuoto. Possibilità di sterilizzazione. Controllo di eventuali perdite dalla punta della pipetta
Microinceneritori per anse Schizzi da anse batteriologiche Schermatura mediante tubo di vetro o di ceramica aperto ad un’estremità e riscaldato elettricamente o a gas.
Contenitori a tenuta per la raccolta e il trasporto di materiali infetti da sterilizzare
Areosol, perdite e fuoriuscite Realizzati in modo da garantire la tenuta e dotati di coperchio. Durevoli. Autoclavabili.
Autoclavi manuali o automatiche
Materiali infetti (resi sicuri per l’eliminazione o il riutilizzo)
Progettazione soggetta ad approvazione. Efficace sterilizzazione attraverso calore.
Bottiglie con tappo a vite Aerosol e perdite Contenimento efficace.
Protezione del circuito del vuoto
Contaminazione del sistema del vuoto del laboratorio con aerosol e liquidi in eccesso
Un filtro a cartuccia previene il passaggio degli aerosol (particelle della misura di 0,45 µm). La bottiglia per i liquidi in eccesso contiene un disinfettante appropriato. Si può usare un bulbo di gomma per chiudere automaticamente il circuito del vuoto quando la bottiglia è piena. L’intera unità è autoclavabile.
Maschere e occhiali di sicurezza
Urti e schizzi Lenti resistenti agli urti (quando necessario devono essere graduate o indossate sopra gli occhiali). Protezione laterale.
Schermi facciali Urti e schizzi Protegge l’intera faccia. Facilmente rimuovibili in caso d’incidente.
Ove disponibili, è opportuno l’utilizzo di anse e pipette pasteur monouso in plastica
Rottura di materiali frangibili, necessità di decontaminazione per il successivo utilizzo
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 81 di 222
4.3.10.6.4 Dispositivi di protezione individuale generalmente utilizzati
Dispositivo Rischio eliminato Caratteristiche di sicurezza
Tute, divise, camici da laboratorio
Contaminazione degli abiti Apertura posteriore Proteggono il normale abbigliamento dai rischi
di contaminazione Grembiuli plastificati Contaminazione degli abiti Impermeabilizzati Calzari Impatto e schizzi Chiusura ermetica
Occhiali di protezione Contatto e schizzi
Lenti resistenti agli impatti (devono essere corretti otticamente o indossabili sopra gli occhiali da vista)
Hanno schermi laterali
Schemi facciali Impatto e schizzi Scherma il viso intero Facilmente rimuovibile in caso d’emergenza
Maschere, respiratori Inalazione di aerosol
Sono disponibili maschere monouso; maschere capaci di proteggere a metà o totalmente il viso e purificare l’aria mediante filtri, maschere pieno facciali, respiratori riforniti di aria
Guanti Contatti diretti con i microrganismi; tagli
Latex, vinile o nitrile testati per la tenuta a microrganismi
Protezione delle mani
4.3.10.7 Sorveglianza sanitaria
Il Datore di Lavoro, attraverso l’operato del Medico Competente, ha la responsabilità di assicurare un’adeguata
sorveglianza sanitaria del personale del laboratorio. Gli obiettivi di tale sorveglianza sono:
fornire un mezzo per la prevenzione delle malattie da laboratorio in soggetti sani tramite l’esclusione di soggetti
altamente suscettibili alle infezioni ed il controllo del personale assunto;
mettere a disposizione, ove necessario, l’immunizzazione attiva o passiva;
fornire un mezzo per il rilievo precoce di infezioni di laboratorio;
verificare l’efficacia delle attrezzature e delle procedure di sicurezza.
4.3.10.7.1 Linee guida per la sorveglianza del personale che lavori con microrganismi del gruppo di rischio 1
La probabilità che organismi appartenenti a tale gruppo siano in grado di causare malattie di una certa
importanza nell’uomo è estremamente ridotta. Sarebbe auspicabile un controllo pre-impiego della salute, che
comprenda l’anamnesi del soggetto. È desiderabile che vengano prontamente riportate malattie o incidenti di laboratorio
e tutti i membri del personale debbono essere consapevoli dell’importanza di utilizzare sempre buone tecniche
microbiologiche.
4.3.10.7.2 Linee guida per la sorveglianza del personale che lavori con microrganismi del gruppo di rischio 2
è necessario un controllo della salute pre-impiego o pre-incarico. Questo controllo deve comprendere l’anamnesi
individuale. Sono utili, e a volte necessari, anche un esame clinico e la raccolta di un campione di siero;
i laboratori devono tenere una lista aggiornata dei medici di famiglia dei propri impiegati;
il Responsabile del laboratorio deve registrare malattie e assenze, ed è responsabilità del lavoratore e del suo
medico di fiducia informare il Direttore di tutte le assenze dovute a malattia;
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 82 di 222
le donne in età fertile vanno informate chiaramente dei rischi per il feto derivanti dall’esposizione professionale ad
agenti microbici come il virus della rosolia. I passi da compiere per la protezione del feto variano, a seconda dei
microrganismi a cui la madre potrebbe essere esposta.
4.3.10.8 Addestramento
L’errore umano ed una pratica di lavoro scarsa possono compromettere l’efficacia delle migliori misure di
sicurezza e delle apparecchiature fornite appositamente per la protezione del personale. Un gruppo di lavoro
consapevole in materia di sicurezza, ben informato sul riconoscimento ed il controllo dei pericoli presenti nel
laboratorio, è un elemento chiave nella prevenzione degli incidenti di laboratorio e delle malattie professionali. A
questo scopo è essenziale un addestramento continuo sulle misure di sicurezza. Il processo parte dalla Direzione del
laboratorio che si deve assicurare che pratiche e procedure di laboratorio sicure vengano inserite nell’addestramento
base del personale. Le informazioni inerenti le misure di sicurezza devono essere sempre parte integrante della
formazione da fornire al nuovo personale del laboratorio.
I Responsabili dei laboratori devono giocare un ruolo chiave nell’addestramento del personale all’uso di buone
tecniche di laboratorio. L’addestramento, deve sempre includere metodi per svolgere in sicurezza le seguenti operazioni
a rischio, comunemente effettuate da tutto il personale impiegato nel laboratorio:
operazioni che presentino il rischio di inalazione (es. a causa di produzione di aerosol), come usare le anse,
seminare per trascinamento campioni su piastre, pipettare, strisciare campioni, aprire colture, centrifugare;
operazioni che presentino il rischio di ingestione, come manipolare campioni, strisci e colture;
operazioni che presentino il rischio di iniezione, come l’uso di aghi e siringhe, e la manipolazione di animali che
possono mordere e graffiare;
operazioni per la manipolazione sicura di sangue e altri materiali patologici potenzialmente pericolosi;
operazioni per l’eliminazione dei materiali infetti.
4.3.10.9 Decontaminazione
I materiali destinati alla decontaminazione ed eliminazione devono essere posti in contenitori quali sacchi di
plastica autoclavabili colorati secondo un codice che indichi se i materiali in essi contenuti debbano essere autoclavati o
inceneriti.
La sterilizzazione in autoclave è il sistema migliore per tutti i processi di decontaminazione. L’autoclave deve
essere del tipo a pressione con circolazione per gravità. In mancanza di un autoclave, metodi alternativi possono essere:
usare una pentola a pressione alla massima pressione ottenibile:
bollire per 30 minuti, preferibilmente in acqua contenente bicarbonato di sodio.
4.3.10.9.1 Disinfettanti e sostanze chimiche
Devono essere presenti indicazioni scritte riguardo a quali disinfettanti usare e per quali scopi, e la diluizione
raccomandata dal fabbricante per ciascuno di essi. In generale l’ipoclorito di sodio ed i compisti fenolici sono i
disinfettanti raccomandati per l’uso in laboratorio.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 83 di 222
Per usi speciali, possono essere efficaci vari agenti attivi in superficie o solventi, quali alcool, iodio, iodofori ed
altri agenti ossidanti, nonché sostanze con valori di pH molto alti o molto bassi, purché si sia stabilito che l’agente da
distruggere non sia resistente a questa procedura.
4.3.10.10 Eliminazione
È opportuno stabilire un sistema di identificazione e separazione per i materiali contaminati ed i loro contenitori.
Le categorie possono essere:
a) rifiuti non contaminati da eliminare assieme ai rifiuti normali;
b) rifiuti “taglienti o pungenti” (aghi ipodermici, scalpelli, coltelli, vetri rotti);
c) materiale contaminato destinato ad essere autoclavato e riutilizzato;
d) materiale contaminato da eliminare;
e) rifiuti anatomici, ovvero tessuti umani o animali.
4.3.10.10.1 Rifiuti “taglienti o pungenti”
Agli aghi ipodermici non va rimesso il cappuccio né tagliata la punta, e non vanno rimossi dalle siringhe
monouso. Si deve mettere tutto l’insieme in un contenitore rigido con pareti impermeabili, che non va riempito
completamente. Quando questi contenitori sono pieni per tre quarti, vanno messi in un contenitore per “rifiuti
contaminati” ed inceneriti, autoclavandoli preventivamente se la pratica di laboratorio lo richiede.
Le siringhe monouso, usate singolarmente, devono essere messe in contenitori e incenerite, autoclavandole
preventivamente, se necessario.
4.3.10.10.2 Materiali contaminati destinati ad essere autoclavati e riutilizzati
Nota bene: non si deve tentare alcuna pulizia preliminare – qualsiasi ripulitura o riparazione fosse necessaria va
fatta dopo che il materiale è stato autoclavato.
4.3.10.10.3 Materiali contaminati da eliminare
Tutte le colture ed i materiali contaminati vanno normalmente autoclavati in contenitori a prova di perdita (ad es.
sacchi di plastica colorata autoclavabili e colorati secondo un codice) prima dell’eliminazione. Dopo essere stato
autoclavato, il materiale può essere messo in altri contenitori per il trasporto all’inceneritore o ad altro punto di
eliminazione.
Ogni postazione di lavoro deve essere dotata di contenitori per i rifiuti, bacinelle e secchi, preferibilmente
infrangibili (es. in plastica). Quando si usano disinfettanti, i rifiuti devono rimanere in contatto stretto con il
disinfettante (cioè senza aria interposta) per il tempo previsto in base al tipo di disinfettante usato. I recipienti per i
rifiuti vanno decontaminati e lavati prima di essere riutilizzati.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 84 di 222
4.3.10.11 Rischi da attrezzature, chimico, elettrico, da incendio o da radiazioni
L’efficacia del sistema di contenimento dei microrganismi patogeni può essere alterata indirettamente da cause
accidentali di natura chimica, elettrica, da radiazioni o incendio. È quindi essenziale che in tutti i laboratori
microbiologici vengano mantenuti degli standard di sicurezza elevati nei confronti di questi rischi.
4.3.11 Tecniche di buona prassi nel laboratorio microbiologico
Errori umani, procedure inadeguate e cattivo uso delle attrezzature causano la maggioranza degli infortuni
connessi alle attività di laboratorio. Di seguito si riportano misure di buona prassi di laboratorio finalizzate ad evitare o
minimizzare i problemi che più frequentemente si possono presentare.
4.3.11.1 Manipolazione dei campioni
Contenitori dei campioni: devono essere preferibilmente in plastica, robusti e tali da non lasciar fuoriuscire
materiale quando il coperchio o il tappo sono applicati correttamente. Il contenuto non deve imbrattare l’esterno
del contenitore. Etichettare correttamente i contenitori per facilitare l’identificazione.
Trasporto dei campioni nell’ambiente di lavoro: porre i contenitori dei campioni in contenitori rigidi chiusi,
attrezzati per mantenerli in posizione verticale. I contenitori esterni possono essere in metallo o plastica, con il
coperchio preferibilmente dotato di guarnizione. Devono essere autoclavabili o resistenti all’azione dei
disinfettanti chimici. Devono essere decontaminati con regolarità.
Apertura dei contenitori: i contenitori dei campioni devono essere aperti all’interno di una cappa di sicurezza
biologica. In vicinanza dell’operatore devono essere subito disponibili dei disinfettanti.
4.3.11.2 Uso delle pipette
È vietato pipettare con la bocca. Usare sempre un dispositivo di aiuto.
Tutte le pipette devono essere dotate di tamponi di cotone per ridurre la possibilità di contaminazione dei
dispositivi d’uso delle pipette.
Non soffiare mai aria attraverso un liquido contenente agenti infettivi.
Non mescolare materiali infettivi alternando con la pipetta suzione ed espulsione.
Non espellere in maniera forzata i liquidi delle pipette.
Preferire le pipette volumetriche a due tacche, che non richiedono l’espulsione dell’ultima goccia.
Immergere completamente le pipette contaminate nel disinfettante adatto, in un contenitore infrangibile. Lasciarle
nel disinfettante per il tempo appropriato prima di sottoporle alle procedure successive.
Mettere il contenitore per le pipette da eliminare all’interno della cappa di sicurezza biologica.
Per aspirare non utilizzare siringhe con aghi ipodermici.
Con flaconi a tappo perforabile usare adatti dispositivi di apertura, per evitare l’uso di aghi e siringhe e permettere
l’utilizzo di pipette.
Per evitare la dispersione di materiale infettivo che può cadere da una pipetta, coprire la superficie di lavoro con
materiale assorbente, da eliminare come rifiuto infettivo dopo l’uso.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 85 di 222
4.3.11.3 Per evitare la dispersione di materiale infettivo
Per evitare lo spargimento fortuito del loro carico, le anse per il trasferimento di materiale microbiologico devono
essere completamente chiuse, avere un diametro di 2-3 mm e lo stelo non più lungo di 6 cm per minimizzare le
vibrazioni.
Adottare un microinceneritore elettrico chiuso al posto del bunsen, per evitare il rischio di proiezione di materiale
infettivo nella sterilizzazione delle anse di trasferimento. Meglio ancora l’uso di anse monouso.
Quando si essiccano campioni liquidi evitare la creazione di aerosol.
Mettere i campioni e le colture da buttare/autoclavare in contenitori a perfetta tenuta, ad esempio nei sacchi per
rifiuti di laboratorio. Rafforzane la chiusura con del nastro da autoclave, prima di eliminarli nei contenitori
opportuni.
Decontaminare le aree di lavoro con disinfettanti opportuni al termine delle operazioni.
4.3.11.4 Uso di cappe di sicurezza biologica
Il personale che utilizza le cappe di sicurezza biologica deve essere formato adeguatamente sul loro utilizzo
(procedure scritte, manuali operativi, ecc). In particolare deve essere informato che la cappa non protegge
l’operatore da versamenti, rotture o procedure di lavoro errate.
Non utilizzare cappe che non funzionano correttamente.
Non aprire il pannello di vetro quando la cappa è in funzione.
Ridurre al minimo la presenza di attrezzature e materiali all’interno della cappa. La circolazione d’aria nella parte
posteriore della cappa non deve essere bloccata.
Nella cappa non utilizzare bruciatori bunsen, perché il calore prodotto distorce il flusso d’aria e può danneggiare i
filtri. È ammesso un microinceneritore elettrico, ma è preferibile utilizzare anse sterili monouso.
Tutte le operazioni devono essere eseguite nella parte mediana o posteriore della superficie di lavoro ed essere
controllabili attraverso il pannello di osservazione.
Traffico ed operazioni svolte alle spalle dell’operatore devono essere ridotti al minimo.
L’operatore non deve disturbare il flusso d’aria con l’introduzione e l’estrazione ripetuta delle braccia.
Non bloccare le griglie dell’aria con fogli, pipette o altri materiali, perché questo ostacola il flusso dell’aria e può
causare contaminazione del materiale ed esposizione dell’operatore.
Pulire la superficie della cappa con adatto disinfettante a lavoro eseguito ed a fine giornata.
Il ventilatore della cappa deve girare per almeno 5 minuti sia prima di cominciare il lavoro che dopo il
completamento delle operazioni.
4.3.11.5 Prevenzione dell’ingestione di materiale infetto o di contatto con pelle ed occhi Le grosse particelle o le goccioline (> 5µm di diametro) rilasciate durante le manipolazioni biologiche si posano
rapidamente sulla superficie di lavoro o sulle mani dell’operatore. Indossare guanti monouso. Chi lavora in
laboratorio deve evitare di toccarsi bocca, occhi e viso.
Cibo e bevande non devono essere consumati e conservati in laboratorio.
Nessun oggetto presente nel laboratorio deve essere inserito in bocca (penne, matite, ecc).
Non usare cosmetici in laboratorio.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 86 di 222
Faccia, occhi e bocca devono essere protetti anche mediante appositi schermi protettivi durante ogni operazione
che potrebbe causare schizzi di materiale infetto.
4.3.11.6 Prevenzione dell’inoculazione di materiale infetto
L’inoculazione accidentale può essere il risultato di ferite da oggetti taglienti, ad esempio aghi ipodermici, pipette
Pasteur in vetro, ecc. Sostituire il vetro con la plastica ogni qualvolta sia possibile.
Per minimizzare il rischio di ferite da aghi: ridurre l’uso di aghi e siringhe o, se necessario, utilizzare sistemi
automatici di sicurezza.
Gli aghi non devono essere mai rincappucciati. Eliminare gli aghi monouso in contenitori a prova di foratura dotati
di coperchio.
4.3.11.7 Uso delle centrifughe
Le centrifughe devono essere utilizzate in accordo con le specifiche fornite dal produttore.
Devono essere posizionate ad un’altezza tale che i lavoratori possano vedere bene all’interno della camera del
rotore, per posizionare correttamente portacestelli e cestelli.
Le provette da centrifuga ed i contenitori di campioni da usare in centrifuga devono essere di vetro spesso o
preferibilmente di plastica e dovrebbero essere accuratamente ispezionati prima dell’uso.
Le provette ed i contenitori dei campioni che vanno in centrifuga devono essere chiusi in modo sicuro
(possibilmente con tappo a vite).
I cestelli devono essere caricati, equilibrati, sigillati ed aperti sotto cappa di sicurezza biologica.
Cestelli e portacestelli devono essere appaiati per peso e, con le provette posizionate, bilanciati correttamente.
Lo spazio vuoto da lasciare tra la superficie del fluido e l’orlo della provetta da centrifuga dovrebbe essere indicato
nelle istruzioni fornite dal fabbricante.
Usare acqua distillata oppure alcool (propanolo al 70%) per bilanciare i cestelli vuoti. Evitare l’uso di soluzione
fisiologica o di soluzioni di ipoclorito, corrosive per metalli.
Usare cestelli sigillabili di sicurezza per centrifugare microrganismi classificati nei gruppi 3 e 4.
Quando si usano rotori ad angolo fisso fare attenzione a non riempire troppo le provette, perché potrebbero
disperdere materiale.
Ispezionare quotidianamente la camera interna della centrifuga per cercare macchie o sporco a livello del rotore. In
presenza di macchie o sporco è necessario rivedere i protocolli di centrifugazione.
Ispezionare quotidianamente rotori e cestelli per cercare segni di corrosione e fessure anche minime.
Cestelli, rotori e camera interna della centrifuga vanno decontaminati dopo ciascun uso.
Quando la centrifuga è in funzione può proiettare nell’aria particelle infettive. Queste, se la centrifuga è posta in
una cappa tradizionale di Classe I o II aperta frontalmente, viaggiano a velocità troppo alta per essere trattenute dal
flusso d’aria della cappa. Usare la centrifuga all’interno di una Cappa di sicurezza Classe III previene l’estesa
dispersione degli aerosol emessi. In ogni caso, buone tecniche di centrifugazione e provette ben tappate offrono
protezione adeguata contro aerosol infettanti e particelle disperse.
4.3.11.8 Uso degli omogenizzatori, miscelatori, agitatori ed ultrasonicatori
Non usare in laboratorio omogenizzatori da cucina, perché possono disperdere materiale o aerosol. Sono più sicuri
i frullatori da laboratorio e dispositivi per la digestione dei tessuti.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 87 di 222
Coperchi, contenitori e flaconi devono essere in buona condizione, privi di crepe od imperfezioni. I coperchi
devono chiudere bene ed avere guarnizioni efficienti.
Durante il funzionamento di omogenizzatori, agitatori e sonicatori la pressione del recipiente aumenta. Aerosol
con materiali infetti possono sfuggire tra il coperchio ed il recipiente. Sono raccomandati recipienti in plastica, in
particolare di politetrafluoroetilene (PTFE), perché il vetro può rompersi, far uscire materiale infetto e ferire
l’operatore.
Quando in funzione, omogenizzatori, agitatori e sonicatori devono essere ricoperti con una robusta protezione in
plastica trasparente, da disinfettare dopo l’uso. Quando possibile, queste macchine dovrebbero funzionare, sotto la
loro protezione di plastica, all’interno di una cappa di sicurezza biologica.
Alla fine del procedimento i recipienti devono essere aperti sotto cappa di sicurezza biologica.
Il personale che usa sonicatori deve essere provvisto di protezioni per l’udito.
4.3.11.9 Uso di macinatori di tessuti
Quelli in vetro devono essere tenuti con la mano protetta da guanti, avvolti da materiale assorbente. I macinatori in
plastica (PTFE) sono più sicuri.
Dovrebbero essere fatti funzionare ed aperti sotto cappa biologica.
4.3.11.10 Manutenzione ed uso di frigoriferi e congelatori
I frigoriferi, i congelatori ed i distributori di ghiaccio secco dovrebbero essere scongelati e puliti regolarmente ed
ogni ampolla, provetta o conduttura danneggiata o rotta durante l’immagazzinamento, dovrebbe essere sostituita.
Durante la pulizia indossare protezioni per la faccia e guanti di gomma spessa.
Tutti i contenitori riposti nei frigoriferi dovrebbero essere etichettati con il nome scientifico del contenuto, la data
dell’immagazzinamento ed il nome dell’operatore che li ha immagazzinati. Il materiale non etichettato od obsoleto
dovrebbe essere autoclavato ed eliminato.
Le soluzioni infiammabili non devono essere riposte nei frigoriferi a meno che questi non abbiano caratteristiche
specifiche per contenere tale tipo di sostanze. Avvertimenti in questo senso devono essere affissi sulla porta dei
frigoriferi.
4.3.11.11 Apertura di ampolle contenenti materiale infetto liofilizzato
Fare attenzione quando si aprono ampolle di materiale congelato-disidratato, perché il contenuto potrebbe essere
sottovuoto e l’ingresso improvviso di aria potrebbe disperdere materiale nell’atmosfera. Aprire sempre le ampolle sotto
cappa di sicurezza biologica. Si raccomandano inoltre le seguenti procedure:
Prima di tutto decontaminare l’esterno dell’ampolla.
Incidere sull’ampolla all’altezza della metà del tappo di cotone o di cellulosa se presente.
Per proteggere le mani, avvolgere l’ampolla con cotone impregnato di alcool prima di romperla a livello
dell’incisione praticata con la lametta.
Rimuovere la parte superiore del tappo con delicatezza e manipolare come se si trattasse di materiale contaminato.
Se il tappo si trova ancora sopra il contenuto dell’ampolla, rimuoverlo con pinze sterili.
Aggiungere il liquido di risospensione lentamente, per evitare la formazione di schiuma.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 88 di 222
4.3.11.12 Conservazione di ampolle contenenti materiale infetto
Non immergere mai in azoto liquido ampolle che contengono materiale infetto, perché in caso di fessure o di
chiusura imperfetta possono rompersi ed esplodere al momento della rimozione. Se sono necessarie temperature molto
basse, le ampolle dovrebbero essere posizionate solamente nella fase gassosa sovrastante l’azoto liquido. In alternativa,
i materiali infetti possono essere immagazzinati in congelatori meccanici a temperatura estremamente bassa o con
ghiaccio secco.
Quando le ampolle vengono rimosse dal congelatore, il personale del laboratorio deve indossare protezioni per
occhi e mani e disinfettare la superficie esterna delle ampolle così conservate.
4.3.12 Procedure d’emergenza per laboratori di microbiologia
4.3.12.1 Ferite da puntura, tagli ed abrasioni
Rimuovere l’abbigliamento protettivo dell’infortunato, lavare le mani ed ogni parte lesa, applicare un
appropriato disinfettante della pelle e rivolgersi ad un centro medico competente. Riferire la causa della ferita e gli
eventuali microrganismi coinvolti e registrare dati sanitari appropriati e completi.
4.3.12.2 Ingestione di materiale potenzialmente infetto
Rimuovere l’abbigliamento protettivo e rivolgersi ad un medico. Riferire la natura del materiale ingerito e le
circostanze dell’incidente e registrare dati sanitari appropriati e completi.
4.3.12.3 Fuoriuscita di aerosol potenzialmente infettante dalla cappa di sicurezza biologica
Tutte le persone devono abbandonare immediatamente l’area contaminata ed ogni individuo esposto deve essere
inviato a visita medica. Informare immediatamente i responsabili del laboratorio. Nessuno deve entrare nella stanza per
opportuno lasso di tempo (almeno 1 ora), per lasciare che l’aerosol venga allontanato e le particelle più pesanti si
possano depositare. Se il laboratorio non ha un sistema centralizzato di estrazione dell’aria, bisogna ritardare l’ingresso
delle persone (almeno per 24 ore).
È necessario segnalare con cartelli il divieto d’accesso. Trascorso il tempo dovuto, procedere alla
decontaminazione. Indossare adatto abbigliamento protettivo e protezione respiratoria.
4.3.12.4 Contenitori rotti e fuoriuscita di sostanze infette
I contenitori rotti contaminati con sostanze infette o fuoriuscita di sostanze infette dovrebbero essere coperti con
un fazzoletto o un panno. Versare poi su di essi un disinfettante e lasciarlo agire per il tempo necessario, trascorso il
quale gli asciugamani ed il materiale rotto possono essere asportati, maneggiando con pinze i frammenti di vetro.
Trattare quindi l’area interessata con disinfettante. Se vengono usate palette per rimuovere il materiale rotto, devono
essere autoclavate o immerse in un disinfettante efficace. Eliminare gli stracci e la carta utilizzati per la pulizia in un
contenitore per rifiuti contaminati. Indossare i guanti per tutte le operazioni sopra esposte.
4.3.12.5 Rottura di provette che contengono materiale potenzialmente infettante in centrifughe non dotate di
cestelli sigillabili
Se una rottura si verifica o è sospettata mentre la macchina è in moto, il motore dovrebbe essere spento e la
macchina lasciata chiusa (almeno 30 minuti) per permettere la deposizione di particelle. Se si scopre la rottura dopo che
la macchina si è fermata, il rotore dovrebbe essere sostituito immediatamente e lasciato chiuso (30 minuti). In entrambe
i casi deve essere informato il Responsabile del laboratorio.
Università Politecnica delle Marche
Dipartimento di Scienze della Vita e dell’Ambiente
MANUALE DELLA SICUREZZA
a cura del Dott. L. Lambertucci RSPP-DiSVA
Documento della sicurezza ad uso interno del DiSVA − Aggiornamento 4/2016 Pagina 89 di 222
Per tutte le operazioni successive vanno indossati guanti resistenti di gomma dura, se necessario rivestiti di
guanti monouso adeguati. Pinze o cotone dovrebbero essere usati per rimuovere i frammenti di vetro. Tutte le provette
rotte, frammenti di vetro, materiale di sostegno ed il rotore, vanno immersi in un disinfettante non corrosivo che sia
sicuramente efficace contro il microrganismo rilasciato. Le provette integre ancora sigillate possono essere poste nel
disinfettante in un contenitore separato e recuperate.
Il vano della centrifuga dovrebbe essere pulito con lo stesso disinfettante, alla diluizione appropriata, quindi
pulito ancora con acqua ed asciugato. Tutto il materiale utilizzato nella pulitura deve essere trattato come materiale
infetto.
4.3.12.6 Rottura di provette all’interno di contenitori sigillati (contenitori di sicurezza)
Caricare e scaricare i cestelli da centrifuga sotto cappa di sicurezza biologica. In caso di sospetta rottura
all’interno del cestello di sicurezza, allentare il coperchio ed autoclavare il cestello. In alternativa, l’interno del cestello
di sicurezza può essere disinfettato chimicamente.