STRUTTURE O PROCESSI CARATTERISTICI DEI PROCARIOTI ...
Transcript of STRUTTURE O PROCESSI CARATTERISTICI DEI PROCARIOTI ...

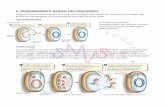
STRUTTURE O PROCESSI CARATTERISTICI DEI PROCARIOTI, RAPPRESENTANO BUONI BERSAGLI PER GLI ANTIBIOTICI
Sintesi proteica (Ribosomi differenti)
Membrane
Replicazione e ”repair” del DNA
(enzimi diversi)
parete batterica (solo procarioti)
Processo di trascrizione (RNA polimerasi diversa)
Sintesi dei folati (assente nei mammiferi)

Antibiotici beta-lattamici e antibiotici glicopeptidici bloccano la sintesi del peptidoglicano
NAG
NAM
D-A
DAP
NAG
NAM
D-A
DAP
NAG
NAM
D-A
DAP
D-A D-A
PBP

ANTIBIOTICI BETA-LATTAMICI prodotti da funghi (penicilline e cefalosporine) e da batteri
(carbapenemi) o di sintesi (monobattami)
IL LORO BERSAGLIO E’ L’ENZIMA (PBP che operano transpeptidazione e transglicosilazione per la sintesi del peptidoglicano)
Agiscono come pseudosubstrato per le PBP legandosi covalentemente al sito attivo e acilandolo
Le PBPs si deacilano con estrema lentezza e risultano quindi inattivate

Il substrato non è più disponibile per l’azione delle PBP
ANTIBIOTICI GLICOPEPTIDICI (gruppo della vancomicina): IL BERSAGLIO E’ IL SUBSTRATO
Gli antibiotici glicopeptidici sono un gruppo vasto (es.Vancomicina prodotta da una specie di Amycolatopsis-batterio Gram +)
si legano al dipeptide D-Ala - D-Ala e lo mascherano

Si legano alla topoisomerasi-II
E impediscono che il DNA venga rilegato
I CHINOLONI (di sintesi) BLOCCANO LA DUPLICAZIONE DEL CROMOSOMA BATTERICO:
Nella cellula si accumulano frammenti di DNA

σ
“Core enzima”
Le RIFAMICINE prodotte da una specie di Amycolatopsis
si legano alla subunità beta delle RNA-polimerasi batteriche
E impediscono la trascrizione genica, perché la RNA polimerasi non può più legarsi al DNA da copiare

I RIBOSOMI (LA SINTESI PROTEICA) SONO BERSAGLIO DI MOLTI ANTIBIOTICI
le tetracicline si legano alla subunita’ 30s deformando il sito “A” e impediscono l’alloggiamento degli
AA-tRNA
P A E
30S TETRACICLINE
Le tetracicline naturali sono prodotte da Streptomiceti, ne sono state anche create
molte semisintetiche

QUANDO LA SINTESI E’ GIA’ INIZIATA
vengono quindi sintetizzate proteine con mutazioni che possono renderle non funzionali
Gli aminoglicosidi, legandosi al 30S, Rendono permissivo il sito “A” che accoglie AA-tRNA non corrispondenti ai codoni del mRNA
GLI AMINOGLICOSIDI (prodotti da batteri Gram+ di diversi generi del gruppo degli attinomiceti)
SI LEGANO ALLA SUBUNITA’ 30S “BLOCCANDO” IL COMPLESSO DI INIZIO
e impediscono il legame con la subunità 50S e la lettura del messaggero

CLORAMFENICOLO, MACROLIDI E LINCOSAMIDI (da streptomiceti)
Competono per il medesimo sito di legame sulla subunità 50S
30S
50S

Macrolidi e lincosamidi possono anche fermare lo scorrimento del ribosoma sul messaggero
F-Met
A1
30S Cl
oram
fenico
lo
Mac
rolid
i Linc
osam
idi
Interferiscono con l’azione della peptidil-transferasi bloccando l’allungamento della catena

Gli involucri esterni sono critici nei batteri
La membrana esterna, tipica dei batteri Gram-negativi, delimita la cellula batterica impedendo l’accesso a molti composti
La membrana interna è vitale per la produzione di energia e il trasporto dei nutrienti

A basse dosi la POLIMIXINA (prodotta da una specie di Bacillus)
Disorganizza la membrana esterna
sensibilizzando la cellula batterica a componenti del siero o altri antibiotici
Mentre a dosi elevate
Provoca il collasso della membrana interna e la morte della cellula batterica

A differenza di noi, i batteri sintetizzano acido folico
acido folico
Sintesi DNA-RNA
Sintesi proteine PABA
acido folico Sintesi DNA-RNA
Sintesi proteine Sulfamidico
I sulfamidici (di sintesi) interferiscono con la biosintesi di acido folico dal PABA
Trimethoprim
Sintesi DNA-RNA
Sintesi proteine PABA
Il Trimethoprim (di sintesi) sostituisce l’acido folico e blocca le vie biosintetiche a valle

I BATTERI POSSONO DIVENTARE RESISTENTI
MECCANISMI BIOCHIMICI
FENOMENI BIOLOGICI
Enzimi Farmaci inattivati
β-lattamasi β-lattamici
Acetil-transferasi
Fosfo-transferasi Aminoglicosidi
Adenil-transferasi
Acetil-transferasi Cloramfenicolo
ENZIMI INATTIVANTI

Le β-lattamasi secrete nello spazio periplasmico, inattivano le penicilline e le cefalosporine prima che si leghino alle PBP
R H CH3
N
S
CH3 COO- O
β-lattamico
β-lattamasi Acido penicilloico (inattivo)
HN
R H CH3 S CH3 COO-
O O
TPasi TGasi TPasi TGasi

GLI ENZIMI DI MODIFICAZIONE NON DISTRUGGONO LA MOLECOLA
MA LA RENDONO INSERVIBILE
ENZIMI INATTIVANTI GLI AMINOGLICOSIDI
PREVENGONO IL LEGAME DELL’ANTIBIOTICO AL RIBOSOMA
Enzimi batterici in grado di:
HO
O
HO
N-acetilare
O
HN
2-O3P O-fosforilare
AMP-O
O-adenilare

per questo motivo molti enzimi sono inducibili
prodotti solo quando la loro attivita’ si rende davvero necessaria
molti degli enzimi che modificano gli antibiotici sono codificati da geni la cui espressione è regolata
i microrganismi non sprecano mai energia

Perché la resistenza si manifesti è necessario che un antibiotico β-lattamico induca la trascrizione del gene e
sia allo stesso tempo un substrato per il prodotto
La produzione di AmpC è inducibile
Tutti i ceppi di P. aeruginosa hanno nel cromosoma un gene (ampC ) che codifica una β-lattamasi (AmpC)
Pseudomonas aeruginosa
Spazio periplasmico
cromosoma

Ampicillina Cefalosporine
Carbapenemi
Carbenicillina Piperacillina Ceftazidime
In un sistema “in vitro” AmpC
DA QUESTI DATI, CI SI ASPETTEREBBE SENSIBILITA’ SOLO NEI CONFRONTI DEI
CARBAPENEMI

Ampicillina Cefalosporine Carbapenemi
Carbenicillina Piperacillina Ceftazidime
ma “in vivo”...
Sono riconosciuti come induttori e degradati da
AmpC
Sarebbero degradati da AmpC che però non viene
prodotta perché queste molecole NON sono
riconosciute come induttori
Sono riconosciuti come induttori, AmpC
È prodotta ma è inefficace su queste molecole

MODIFICAZIONI DEL BERSAGLIO
IL BERSAGLIO PUO’ ESSERE ASSENTE
I MICOPLASMI, CHE NON HANNO PARETE, SONO INTRINSECAMENTE RESISTENTI AI β-LATTAMICI

σ “Core enzima”
RESISTENZA INTRINSECA ALLE RIFAMICINE NEI MICOPLASMI
IL BERSAGLIO PUO’ ESSERE NATURALMENTE INSENSIBILE
RESISTENZA INTRINSECA ALLE CEFALOSPORINE NEGLI ENTEROCOCCHI
Le PBP degli enterococchi sono strutturate in modo da non essere legate dalle CEFALOSPORINE

IL BERSAGLIO PUO’ MODIFICARSI PER MUTAZIONE *
Gene Bersaglio modificato Resistenza acquisita a:
gyrA DNA girasi (sub.A) Chinoloni
parC Topoisomerasi IV
Chinoloni
rpoB RNA polimerasi (sub β) Rifampicina
IL BERSAGLIO PUO’ VENIRE MODIFICATO BIOCHIMICAMENTE

Alcuni microrganismi metilano il proprio rRNA , rendendolo così meno affine nei confronti di Macrolidi e Lincosamidi
CH3
Sintetizzano un dipeptide D-alanil-D-lattato
I ceppi VRE (Vancomycin-Resistant-Enterococci)
Eliminando le normali terminazioni D-ala-D-ala
I nuovi dipeptidi non sono riconosciuti dalla vancomicina

UN’ALTRA PROTEZIONE DEL RIBOSOMA PUO’ ESSERE OTTENUTA GRAZIE A UN INGOMBRO STERICO
In un altro caso il ribosoma viene protetto da una proteina, Che lo rende inaccessibile alle tetracicline

UN’ALTRA POSSIBILITÀ È QUELLA DI ALLONTANARE L’ANTIBIOTICO PRIMA CHE FACCIA DANNI
E’ quello che i microrganismi ottengono con le pompe di efflusso
I batteri sintetizzano proteine che hanno la funzione di espellere attivamente la
molecola di antibiotico..
LE POMPE DI EFFLUSSO TRANSMEMBRANA
Le pompe di efflusso impediscono alla concentrazione intracellulare
di risultare efficace
Perché un antibiotico sia efficace, la sua concentrazione all’interno della cellula batterica deve essere sufficiente a inattivare il bersaglio

ESISTONO DIVERSI TIPI DI POMPE DI EFFLUSSO
Membrana plasmatica
Citoplasma
Chinoloni (streptococchi)
Alcune sono specifiche..
Tetracicline (Gram+ e Gram-)
..altre non lo sono (Sistemi di efflusso multidrug)
Macrolidi (streptococchi stafilococchi)
Disinfettanti e Intercalanti
(Gram+ e Gram-)

IMPEDIRE ALL’ANTIBIOTICO DI RAGGIUNGERE IL BERSAGLIO E’ UN’ALTRA STRATEGIA POSSIBILE
IMPERMEABILITA’ DELLA PARETE
Resistenza intrinseca ai GLICOPEPTIDI nei batteri Gram-negativi
Resistenza intrinseca ai MACROLIDI in molti batteri Gram-negativi
Resistenza intrinseca a molti farmaci nei micobatteri

L’impermeabilita’ della parete puo’ anche essere dovuta ad una mutazione
carbapenemi
In seguito a mutazione la cellula può perdere la capacità di produrre la porina D2
Resistenza acquisita ai carbapenemi
Pseudomonas aeruginosa
La porina D2 rappresenta il canale di ingresso per i carbapenemi
carbapenemi ? ? ?

I VACCINI
PROCESSO DI IMMUNIZZAZIONE ATTIVA
L’OSPITE PRODUCE ANTICORPI CONTRO L’ANTIGENE SOMMINISTRATO
PREVENZIONE DELL’INFEZIONE A SEGUITO DI SUCCESSIVE ESPOSIZIONI ALL’AGENTE PATOGENO OGGETTO DELLA VACCINAZIONE
I SIERI IMMUNI:
PROCESSO DI IMMUNIZZAZIONE PASSIVA: SOMMINISTRAZIONE DI ANTICORPI PREFORMATI

1) Vaccini interi uccisi: influenza, Salk, epatite A, rabbia, pertosse intero
2) Vaccini vivi attenuati: BCG, MPR, Sabin, febbre gialla, varicella, Ty21a
3) Vaccini con componenti purificati: influenza a sub-unità o split, pertosse acellulare, anatossina difterica e tetanica, vaccini coniugati (Hib, pneumococco e meningococco)
6) Vaccini DNA ricombinanti: es. HBsAg
7) Vaccini a DNA: contro tutti gli agenti infettivi; non ancora in commercio
8) Vaccini da piante, geneticamente modificate
5) Reverse vaccinology: studio del genoma, individuazione dei possibili antigeni meningococco gruppo B
4) Vaccini coniugati (Haemophilus influenzae tipo b, meningococco, pneumococco): polisaccaridi coniugati con proteine carrier che li rendono maggiormente immunogeni e aumentano il coinvolgimento dei linfociti T

TECNICHE TRADIZIONALI
amplificazione su animali
rabbia
vaiolo
amplificazione su uova (es. Virus influenzale) e inattivazione
Colture batteriche inattivate

Non tutti i patogeni possono essere coltivati Problemi di sicurezza per il personale di laboratorio Costi elevati Attenuazione insufficiente Ritorno allo stato infettivo Necessità di conservazione in luoghi refrigerati Non disponibile per tutti i patogeni
LIMITI DEI VACCINI TRADIZIONALI

VACCINI RICOMBINANTI A SUB-UNITA’
Clonazione in batteri o lieviti del gene che codifica l’immunogeno più rappresentato
Antibatterici: proteine di adesione o
tossine modificate
Antivirali: una proteina del capside o dell’envelope
PURIFICAZIONE
es.: HBsAg ANTIGENE DELL’ENVELOPE DI HBV
Ottenuto in lievito

HBsAg ANTIGENE DELL’ENVELOPE DI HBV
L’antigene prodotto dal lievito presenta tutte le caratteristiche della proteina HBsAg nativa
Proteina di superficie HBs
E’ la molecola di scelta per allestire il vaccino clonandola nell’ospite SACCHAROMYCES

NON si usano virus o batteri interi, ma solo componenti
Vantaggi: non si somministrano altre molecole del patogeno
Svantaggi: La proteina manterrà la conformazione naturale? costi

VACCINI ATTIVI RICOMBINANTI OMOLOGHI: mutanti di specie patogene (delezione/mutazione dei geni di virulenza)
Allo studio:
Vibrio Cholerae : Il vaccino disponibile è a base di batteri uccisi col fenolo e l’immunità non dura più di 3-6- mesi
Virus Erpetico dopo delezione del gene TK che ne causa la virulenza
Es: Produzione di PTX inattiva da parte di B.pertussis
Vantaggio: la delezione dei geni di virulenza non permette la reversione allo stato virulento
Più efficaci dei vaccini uccisi e di quelli a subunità (proteine)

VACCINI ATTIVI RICOMBINANTI ETEROLOGHI: clonazione in virus o batteri, geneticamente modificati usati come vettori
VIRUS
Es virus del vaiolo bovino: vettore per vaccini ricombinanti, tra cui alcuni sperimentali anti-HIV

Diversi antigeni sono stati inseriti nel genoma del virus del vaccino:
Un vaccino ricombinante per la rabbia nel virus vaccinale, è in grado di immunizzare le volpi che sono i principali portatori della malattia
Proteina G (virus della rabbia) Antigene superficiale di HBV proteine NP e HA del virus influenzale
Il vaccinia virus si replica direttamente nel citoplasma, non è patogeno e il suo genoma è stato sequenziato
Queste caratteristiche ne fanno un buon candidato per portare determinanti antigenici di patogeni

MUTANTI DI BATTERI INVASIVI
Mutanti di Salmonella enterica sono stati usati per lo sviluppo di un nuovo vaccino anti-HBV
Anche batteri non invasivi ma del tutto sicuri (LAB) sono stati studiati come vettori

VACCINI A DNA
Lo scopo di un vaccino a DNA è promuovere la sintesi dell’antigene direttamente all’interno di una cellula
Mimando quello che succede nelle infezioni virali

Le cellule Dendritiche sono critiche in questo processo
vaccini uccisi o attenuati: gli antigeni penetrano dall’esterno
E i loro frammenti sono presentati su MHC-II
Seguono la via endolisosomiale; sono degradati
II

l’informazione inserita direttamente nella cellula, invece
L’antigene è prodotto nel citoplasma e segue due vie:
E’ tagliato e presentato su MHC-I
Attiva i CD8
CD8
Raggiunge il nucleo
È trascritta
Esce dalla cellula I
S.I. come i vaccini tradizionali

La forma di rilascio nella cellula è su di un plasmide
Il gene deve essere sotto un promotore eucariotico
La somministrazione può avvenire per via
INTRAMUSCOLARE INTRADERMICA
Queste vie di somministrazione hanno l’effetto di incrementare l’intercettazione dell’antigene da parte delle cellule dendritiche

Gene gun
INTRADERMICA
Inoculazione seguita da un trattamento con il laser
Il trattamento con il Laser aumenta il tasso di ingresso nelle cellule dendritiche

Particelle d’oro ricoperte di DNA
Cartuccia per le
particelle
Canale di accelerazion
e
ELIO
Porta-cartucce
Il “Gene gun” è un dispostivo che spara particelle d’oro ricoperte con l’antigene
Le particelle entrano così in contatto direttamente con DC immature situate subito sotto la pelle (cellule di Langerhans)

All’interno di microparticelle
INOCULAZIONE INTRAMUSCOLARE
seguita da un trattamento di elettroporazione
Le particelle favoriscono l’uptake
Il trattamento di elettroporazione aumenta la permeabilità delle DC al vaccino
come DNA nudo

E’ STATO ANCHE PROPOSTO UN RILASCIO ALTERNATIVO AI PLASMIDI
CLONARE IL GENE NEL GENOMA DI UN BATTERIOFAGO
INOCULARE IL FAGO PURIFICATO
LE CELLULE APC CATTURANO IL BATTERIOFAGO
IL CAPSIDE E’ DEGRADATO
L’INFORMAZIONE E’ RILASCIATA NEL CITOPLASMA..
AMPLIFICARE IL FAGO

I VANTAGGI DEI VACCINI A DNA SONO MOLTI
STABILITA’
PRODUZIONE SEMPLICE ED ECONOMICA
FACILITA’ DI MANIPOLAZIONE
DELL’ANTIGENE (SEGUIRE LE MUTAZIONI DEL PATOGENO)
SINTESI PROTEICA DIRETTA DA PARTE DELL’OSPITE
STIMOLAZIONE PROLUNGATA DEL S.I.

LE PREVISIONI SUL FUTURO DEI VACCINI:
Uccisi
A subunità
Immunoterapia
a DNA
Per mezzo di vettori che non si replicano
Attenuati
Attraverso “reverse vaccinology”
prime boost (vaccino a DNA +
richiamo successivo con antigene proteico o
microrganismo inattivato)
Mucosale
2000 2020