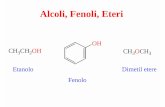
COMPOSTI CARBONILICI Aldeidi e Chetoni Gloria Schiavon – VIII Ciclo SILSIS – A060.
Sistemi Solvente Sostenibili. · 2019-10-20 · eteri, nitrili • s- EPA alogenoderivati, chetoni,...
Transcript of Sistemi Solvente Sostenibili. · 2019-10-20 · eteri, nitrili • s- EPA alogenoderivati, chetoni,...

Sistemi Solvente Sostenibili.Prof. Attilio Citterio
Dipartimento CMIC “Giulio Natta”
https://iscamapweb.chem.polimi.it/citterio/it/education/course-topics/
School of Industrial and Information Engineering
Course 096125 (095857)
Introduction to Green and Sustainable Chemistry

Attilio Citterio
2
Solventi Organici in Processi di Produzione.
Facilitazione e
mediazione di reazioni
intermolecolari
solvente/soluto via
molecole o ioni
Contaminazione da
prodotti volatili e tossici
Potenziale di
inquinamento ambientale
+
-
NB. quando si cambia un solvente, si variano MOLTI parametri!
Solvente
Tecnologia
Detergenza
Mezzo di
reazione
Separazione /
purificazione

Attilio Citterio
3
Perché Serve un Solvente?
Ampiamente usati dall’industria chimica:
Chimica Sintetica
• Mezzo in cui condurre le reazioni su scala di
laboratorio/industriale
• Dissolve i soluti e consente il trasporto di massa
• Stabilizza gli stati di transizione (talvolta
catalizzatore selettivo)
• Modera l’esotermicità dei processi
• Molto usati in lavorazioni/purificazioni dei grezzi
(ben più che un semplice mezzo di reazione).
Chimica Analitica
• Estrazione/preparazione di campioni;
• Cromatografia in fase mobile (HPLC, TLC).
Cristallizzazione
• Ricristallizzazione per purificare composti e
preparare cristalli (anche polimorfi).

Attilio Citterio
4
Altre Applicazioni dei Solventi.
Usati molto ampiamente anche al di fuori della sola chimica sintetica.
Rivestimenti:
Pitture, adesivi
• Il solvente è di norma rimosso per
evaporazione lasciando il rivestimento
• Rimozione di rivestimenti.
Pulizia
Per es. pulitura a secco – uso diffuso del percloroetilene, un noto
sospetto agente cancerogeno, che contamina anche le falde.
Estrazione
Per es.: decaffeinizzazione Caffè (EtOH,
etil lattato)
Per es.: aromi e profumi.

Attilio Citterio
5
Suddivisione del Mercato dei Solventi.
Totale 2100 : 4.1 milioni di tonnellate
EU-27 (2013) : 3.0 milioni di tonnellate
Altre; 8,2 Gomma e Plastica; 1,6
Pulizia a secco; 1,4
Estrazione oli; 2
Fitosanitari; 3,2
Adesivi; 3,7
Pulizia superfici; 3,9
Cosmetici; 6
Casalinghi; 6
Stampa; 8,4
Farmaceutica; 14,6
Pitture e rivestimenti; 41

Attilio Citterio
6
Solventi Usati in Pitture e Vernici.
Totale 2010 : 1.82 milioni di tonnellate
Altri; 1,4 Chetoni; 7,6
Alcoli; 7,6
Derivati di glicoli; 9,6
Esteri (acetici e glicoli);
12,5
Idrocarburi (Alifatici e
Automatici); 61,3

Attilio Citterio
7
Specifici Problemi dei Solventi nei Processi Chimici.
• Solubilità dei soluti e controllo della reazione
• Separazione (e riciclo?) dalla miscela di reazione
• Sicurezza e salute umana e ambientale
• Uno degli obiettivi principali è la rimozione del solvente dai soluti.
Soluto
Solvente
Applicazione
Prodotti
Solvente Ambiente
Riciclo
Importante la
tossicità o la
neutralizzazione.Importante l’energia
e l’efficienza
Importante la selettività
e la solubilità

Attilio Citterio
8
Proprietà dei Solventi.
• Solubilità (p. es. Kps)
• Polarità (vari parametri: ET, ecc.)
• Viscosità
• Volatilità
• Pericolosità
Tossicità intrinseca
Infiammabilità
Esplosività
Distruzione dell’ozono stratosferico
Produzione di ozono atmosferico
Potenziale di riscaldamento globale (gas serra).

Attilio Citterio
Proprietà di Pericolo Tossicità di vari solventi.
Tutti i valori in ppm.
Solvente Soglia
Odore
TLV IDLH Vapori saturi del
solvente a 21°C
Acido acetico 1 10 1 000 16 000
Acetone 100 750 20 000 250 000
Acetonitrile 40 40 4 000 94 000
Anilina 0.5 2 100 340
Benzene 5 10 2 000 105 000
n-Butil acetato 10 150 10 000 14 000
n-Butanolo 2.5 50 8 000 6 300
Cloroformio 250 10 1000 220 000
Diclorometano 250 100 5 000 500 000
Dietil etere 1 400 10 000 100 000
DMF 100 10 3 500 3 700
Etil acetato 1 400 10 000 100 000
9

Attilio Citterio
Proprietà di Pericolo Tossicità di vari solventi.
Tutti i valori in ppm.
Solvente Soglia
Odore
TLV IDLH Vapore saturo del
Solvente a 21°C
Etanolo 10 1000 20 000 60 000
Eptano 220 400 19 000 610 000
Isopropanolo 90 400 20 000 46 000
Metanolo 100 200 25 000 130 000
Nitrobenzene 6 1 200 270
n-Pentano 10 600 5 000 580 000
n-Propanolo 30 200 4 000 18 000
Piridina 0.02 5 3 600 22 000
Percloroetilene 5 50 500 22 000
Toluene 0.2 100 2000 31 000
Tricloroetilene 50 50 1 000 80 000
Xileni 0.05 100 10 000 9 200
10

Attilio Citterio
11Solventi in Reazioni Chimiche: Reazione di
Willgerodt.
• Reazione utile quando funziona
• Imprevedibile
• Meccanismo non chiarito
Usando metodi statistici, le condizioni di reazioni sono state
ottimizzate per 13 diversi solventi, variando 4 parametri.
R. Carlson, Acta Chem. Scand., 40. 694 (1986)

Attilio Citterio
12
SOLVENTE S Morfolina Ott. Tempo Ott. Resa %
moli moli Temp. Ore glc Isolato
Trietileneglicol 17 9.5 145 2 92.5 91
N-Metiiacetammide 2 6 120 2 82.1 80
Etanolo 3.7 13.4 80 22 86 84
3-Metiibutanolo 9.5 13.2 130 5 83.6 82
Chinolina 7.5 10.3 123 2 94 90
Benzene 11.6 12 80 22 85.1 85
Diisopropii etere 6.5 13.7 70 22 47 45
Note: 1. In MeCN, PhCOCS-morfolina è il prodotto prevalente
2. In PhCN non si ottiene prodotto
3. Maggiori reazioni collaterali in diisopropil etere e diossano
I risultati mostrano che ogni solvente ha le sue condizioni ottimali.
Reazione di Willgerodt - Condizioni Ottimali.

Attilio Citterio
13
Solubilità di Reagenti e Prodotti.
in anisolo, DMF e HMPA
in idrocarburi, CCl4
• Sciogliere A in B
KAA + KBB < KAB
• Il simile scioglie il simile
(eccezioni possibili: p. es. Metanolo in Benzene)
• I legami ad idrogeno sono molto importanti

Attilio Citterio
14Tipi di Interazioni con i Solventi:
Capacità EPD / EPA.
• p - donatori aromatici, olefine
• n - donatori alcoli, ammine
eteri, nitrili
• s - EPA alogenoderivati, chetoni, solfossidi
• p - EPA SO2
• H-donatori alcoli, acidi, acqua,
(usano legami ad H)

Attilio Citterio
15
q Alcuni composti sono più solubili in una miscela
di solventi che nei singoli componenti.
(p.es. sali di ammine in alcol/acqua)
I Solventi Influenzano la Dissociazione.
Ma
in CHCl3 in PhNO2

Attilio Citterio
16
q Effetti solvente tipici: 5-20 kJ·mol-1
q Talvolta arrivano a 40 kJ·mol-1
solvente 1
solvente 2
DG1*
DG2*
Effetti del Solvente sulle Energie di Attivazione.
reagenti
prodotti

Attilio Citterio
17
Costanti di equilibrio e frazioni molari a 33 °C
Solvente c(b) (cmol/mol) K = [cis][trans]
tert-Butanolo 24 0.32
Etanolo 45 0.82
Metanolo 62 1.63
Dimetilsolfossido 84 5.25
(b)
m = 15.8 10-30 C·m(a)
m = 8.7 10-30 C·m
Isomeria cis-trans.

Attilio Citterio
18
Solventi Aprotici.
2.3toluene
4.3dietil etere
9.1diclorometano
SolventeCostante
Dielettrica (D)Struttura
DMSO
acetonitrile
acetone
DMF
48.9
37.5
36.7
20.7
Polare
Nonpolare
CH3C≡N
(CH3)2C=O
(CH3)2S=O
CH2Cl2
(CH3CH2)2O
(CH3)2NHCHO
esano CH3(CH2)4CH3 1.9
C6H5CH3

Attilio Citterio
19
Tipo di Reazione
Reagenti iniziali
Complesso attivato
Variazioni nel corso della attivazione
Effetti dell’aumento della polarità del solvente su k
(a) SN1 R-X R+
·····X- Separazione di cariche
diverse
Forte aumento
(b) SN1 R-X R
+·····X
- Dispersione di cariche Piccola diminuz.
(c) SN2 Y + R-X
Y+
···R···X- Separazione di cariche
diverse Forte aumento
(d) SN2 Y- + R-X
Y-···R
+···X
- Dispersione di cariche Piccola diminuz.
(e) SN2 Y- + R-X
Y-···R···X
+ Dispersione di cariche Piccola diminuz.
(f) SN2 Y- + R-X
Y-···R
+···X
- Distruzione di cariche Forte diminuz.
I termini “forte” e “piccolo” derivano dalla teoria che dice che l’effetto della dispersione
della carica dovrebbe essere notevolmente inferiore dell’effetto della sua creazione o
distruzione e perciò hanno solo un significato relativo.
Effetti Solvente Previsto su Velocità di
Reazioni in Sostituzioni Nucleofile.

Attilio Citterio
20
Separazione di Carica
Solvente CCl4 Diossano CH3CO2H CH3OH H2O
k2(rel) 1 5.1 4860 1.6·105 1.1·1010
Effetti sulla Velocità di Reazione.

Attilio Citterio
21
Solvente k2(rel)
Dietil etere 1
1,4-Diossano 2.5
n-Esano 6.2
Benzene 40
Diclorometano 58
Cloroformio 122
R = Fenile
L’olefina è il cicloesene
Effetti su Velocità di Reazione (epossidazione).

Attilio Citterio
22
Solvente k2(rel)
Diisopropil etere 1
Benzene 3.5
Clorobenzene 5.0
Nitrometano 6.6
Nitrobenzene 11
o-Diclorobenzene 13
Effetti sulla Velocità di Reazione (Diels-Alder).

Attilio Citterio
23
Solvente k1(rel)
Etere etilico 1
Tetraidrofurano 17
Acetone 169
Dimetilformammide 980
Dimetilsolfossido 3600
Etanolo 1.2·104
Metanolo 3.2·104
Acido acetico 3.3·104
Acqua 1.3·106
Acido formico 5.1·106
Effetti sulla Velocità di Reazione(Trasposizioni - Reazioni del 1° ordine).

Attilio Citterio
24Solvatazione Specifica di Ioni
e Gruppi Uscenti.
• Il legame ad H su anioni può drammaticamente influenzare una reazione SN
• Il legame ad H sull’anione in uscita è preferito Velocità aumentata
• Il legame ad H sull’anione entrante è preferito Velocità ridotta
• Particolarmente importante in reazioni di decarbossilazione
q I > Br > Cl Metanolo
q Cl > Br > I DMF
q In MeCN, l’acetato è un eccellente nucleofilo

Attilio Citterio
25
Solvente k1(rel)
Acqua 1
Metanolo 34
Etanolo 135
Cloruro di Metilene 6.4·103
Etere etilico 1.2·104
Acetonitrile 3.9·105
Dimetilsolfossido 1.4·104
HMPT 9.5·107
Effetti sulla Velocità di Reazione (Trasposizioni
con dispersione di carica - Reazioni del 1° ordine).

Attilio Citterio
26
Solvente %-O %-C
1,4-Diossano 100 0
t-Butanolo 100 0
Etanolo 100 0
Dimetilformammide 100 0
Tetraidrofurano 96 4
Acqua 49 41
Trifluoroetanolo 37 42
Fenolo 22 78
Alchilazione all’O- vs. C- .

Attilio Citterio
27
Ciclizzazioni Orto vs. Para.
Solvente prodotto para prodotto orto
Tetraidrofurano 13 87
Metanolo 49 51

Attilio Citterio
28
Addizioni 1,2- vs. 1,4- .
Addizione 1,2
in THF o DMF
Addizione 1,4
in dietil etere

Attilio Citterio
29
Omolisi vs. Eterolisi.
Solventi di
bassa nucleo-
filicità
Solventi di
alta nucleo-
filicità

Attilio Citterio
30
Effetto sulla Enantioselettività.
Solvente % e.e.
Toluene 65
1,3,5-TMB 92
Toluene/PE 93
Toluene 65
1,3,5-TMB 92
Toluene/Esano 93
Toluene 65
1,3,5-TMB 92
Toluene/esano 93

Attilio Citterio
31
Sostituzione del Solvente in Chimica Sintetica.
Non è un problema semplice! Un solvente può essere molto difficile
sostituire!
Come mezzo di reazione:
I solventi hanno un sostanziale effetto sulla reazione, consentendo
un grado di controllo impossibile in sua assenza
Può influenzare:
• Le velocità di reazione
• Chemo-, regio- e stereoselettività
• Evoluzione della reazione – può non funzionare per niente, o può fare
qualcosa totalmente differente!
• Può influenzare la lavorazione delle miscele di reazione
Se si possono impiegare, allora si può avere un extra incentivo per
l’adozione di nuova tecnologia.

Attilio Citterio
32
Tipi di Solventi (Organici Volatili - VOC).
Idrocarburi: toluene, xilene, esano, cicloesano, eptano
Ammine: piridina, chinolina, trietilammina
Clorurati: diclorometano, dicloroetano, tricloroetano, cloroformio,
clorobenzene, diclorobenzene
Chetoni: acetone, metiletilchetone, MIBK
Alcoli: metanolo, etanolo, n-propanolo, IPA, t-butanolo, n-butanolo, alcoli
superiori, glicoli, glicol eteri
Esteri: acetato di etile, acetato di isopropile, acetato di butile, lattato di etile
Eteri: etere etilico, TBME, THF, diossano, dibutil etere, diossolano, dialcossi
metani (acetali), anisolo, dialcossietani, alcossietanoli
Acidi e Derivati: acido acetico, acido formico, acetonitrile,
Aprotici dipolari: DMSO, sulfolano, HMPA, uree, DMF, DMAc, NMP + altre
ammidi
Acqua

Attilio Citterio
33
Problemi con i VOC.
Diretti
La tossicità del VOC varia in dipendenza dalla loro natura, modalità e durata di esposizione.
• Per es. DMF (teratogeno), CHCl3 (sospetto cancerogeno)
Infiammabilità (pericolo di incendio)
Formazione di perossidi (comune per gli eteri)
Indiretti
Diminuzione dell’ozono
• Clorofluorocarburi (CFC) ora messi al bando
– Per es. CF3Cl, vita media in atmosfera 640 anni, GWP 14,000
– CCl4 – uso ora fortemente limitato (35 anni, GWP 1400)
Potenziale di riscaldamento globale (GWP)
• Non deve avere capacità di diminuire l’ozono per avere GWP
– HFC134a (CH2FCF3) usato in frigoriferi e condizionatori, 14 h, GWP 1300
Persistenza nell’ambiente
L’uso di solventi meno volatili può migliorare l’ambiente a meno che essi non
portino i problemi altrove.

Attilio Citterio
34
• I solventi organici volatili sono i mezzi tipici in cui si conducono le
sintesi organiche - usi pari a Euro 6,000,000,000 nel 2006
• Nell’anno 2000 l’uso dei solventi ha costituito la fonte primaria
dei VOC nell’atmosfera (27% del totale)
Le emissioni sono in
declino ma rappresentano
ancora cinque milioni di
tonnellate/anno in Europa.
Fonte: DEFRA Atmospheric
emissions estimate 2006
1970 1975 1980 1985 1990 1995 2000
450
500
550
600
650
700
Em
issio
ni di
VO
C /
10 t
onnella
te
3
Anno
Perché è Importante Disporre di Solventi
Verdi?
2005

Attilio Citterio
Andamento Emissioni (NM)VOC, distribuzione
% per settore e variazione 1990-2012 in ITALIA.35
NM = non metano
50,3
6,56,3
3,4
31,4
0,21,9
Share 19901 A3
1 A4
2 B
2
3
4 C
altri
24,9
15,2
7,14,7
44,4
0,42
Share 20121 A3
1 A4
2 B
2
3
4 C
altri
Fonte: www.isprambiente.gov.it
(Report 2014)

Attilio Citterio
36
Norme Ambientali sui Solventi.
Leggi EU
• La Direttiva 1999/13/EC (emendata con la Direttiva 2004/42/EC)
sull’emissione dei solventi VOC è il principale strumento per la
riduzione delle emissioni industriali di composti organici volatili (VOC)
nella UE. Ora Direttiva sulle Emissioni Industriali (2010/75/EU)
Leggi Italia
• D.P.R. 24/05/1988 N°203 e Modifiche D.M.A. 12/07/1990 (elenco
degli inquinanti volatili pericolosi)
• Legge sull’acqua
Leggi USA
• Clean Air Act and amendments (hazardous air pollutants list)
• Clean Water Act
• Toxics Release Inventory
• Toxic Substances Control Act
Ma anche: Protocollo di Montreal ; Protocollo di Kyoto

Attilio Citterio
37
Che Problemi Comportano i Solventi?
Intrinseca Tossicità
Infiammabilità
Esplosività
Diminuzione dell’ozono stratosferico
Produzione di ozono atmosferico
Produzione di altri inquinanti atmosferici secondari
Potenziale di riscaldamento globale

Attilio Citterio
Sistema Modello di Valutazione di Solventi
col Metodo del Ciclo di Vita.38
produzionedel solvente
Uso delsolvente
riciclo delsolvente
Smaltimentosolvente
Produzione
Petrolchimica
del solvente
Uso del
solvente
Scarto
solvente
incenerimento
scarto solvente
incenerimento
scarto solvente
distillazione
solvente scarto
Vapore Elettricità Comb. fossile
Vapore Elettricità Comb. fossileSolvente recuperato
Opzione incenerim.
Opzione distillazione
Tabella 1 Specifiche dei processi di trattamento del solvente usato per la valutazione. Gli assunti sotto indicati
riflettono le condizioni generali nell’industria chimica in base al parere di un gruppo di esperti.
Parametro Assunti Commento
Tecnologia di incenerimento
Tecnologia di distillazione
Uso di energia e ausiliari
Produzione di energia e ausiliari
Recupero del solvente
Trattamento dei residui
Incenerimento di scarto pericoloso
Distillazione a batch
Uso medio per distillazione batch
Produzione media Europea
Recupero medio del solvente: 90%
Incenerimento
Descrizione modello vedi ref. 19
Descrizione dettaglio vedi ref. 20
In base ad analisi statistica 20
Dati tratti dal ref. 16
In base all’opinione di un gruppo
di esperti ref. 21
Tecnologia più spesso usata per
solventi organici 22

Attilio Citterio
CED Totale di un'Opzione di Trattamento. 39
Tabella 2 Risultati della valutazione del ciclo di vita di 26 solventi organici. Il CED totale di opzione di trattamento
è calcolata in base a queste operazioni: CED (Opzione Distillazione) = CED (Produzione Solvente) + CED (Distil-
lazione Solvente); CED (Opzione Incenerimento) = CED (Produzione Solvente) + CED (Incenerimento Solvente)
Solvente CAS-No. Produzione del Solvente
CED per kg solv./MJ-eq.
Distillazione Solvente
CED per kg solv./MJ-eq.
Incenerimento Solvente
CED per kg solv./MJ-eq.
Acido acetico 64-19-7 55.9 -34.9 -15.5
Acetone 67-64-1 74.6 -53.6 -33.9
Acetonitrile 75-05-8 88.5 -79.6 -29.7
Butanolo (1-) 71-36-3 97.3 -74.6 -39.9
Butyl acetato 123-86-4 121.6 -95.9 -34.1
Cicloesano 110-82-7 83.2 -63.4 -53.5
Cicloesanone 108-94-1 124.7 -99.7 -40.4
Dietil etere 60-29-7 49.8 -31.9 -40.2
Diossano 68-12-2 86.6 -63.8 -27.6
Dimetilformammide 68-12-2 91.1 -67.6 -25.9
Etanolo 64-17-5 50.1 -31.2 -31.7
Etil acetato 141-78-6 95.6 -72.0 -27.6
Etil benzene 100-41-4 85.1 -64.9 -49.8
CED = Cumulative Energy Demand

Attilio Citterio
CED Totale di una Opzione di Trattamento. 40
Tabella 2 Risultati della valutazione del ciclo di vita di 26 solventi organici. (cont.). Il CED totale per opzione di
trattamento è calcolato in base a: CED (Opzione Distillazione) = CED (Produzione Solvente) + CED (Distillazione
Solvente); CED (Opzione Incenerimento) = CED (Produzione Solvente) + CED (Incenerimento Solvente)
Solvente CAS-No. Produzione del Solvente
CED per kg solv./MJ-eq.
Distillazione Solvente
CED per kg solv./MJ-eq.
Incenerimento Solvente
CED per kg solv./MJ-eq.
Formaldeide 50-00-0 49.3 -28.8 -15.9
Acido formico 64-18-6 73.9 -50.1 -4.7
Eptano 142-82-5 61.5 -43.7 -54.5
Esano 110-54-3 64.4 -46.7 -55.2
Metiletilchetone 108-10-1 64.2 -44.6 -37.6
Metanolo 67-56-1 40.7 -21.7 -22.2
Metil acetato 79-20-9 49.0 -29.2 -22.8
Pentano 109-66-0 73.2 -54.5 -55.3
Propil alcool (n-) 71-23-8 111.7 -87.3 -36.5
Propil alcool (iso-) 67-63-0 65.6 -46.1 -36.5
Tetraidrofurano 109-99-9 270.8 -230.7 -37.5
Toluene 108-88-3 80.0 -60.0 -49.3
Xilene 1330-20-7 72.5 -53.1 -49.9

Attilio Citterio
41
Accettabilità dei Solventi Molecolari.
Più accettabile Meno accettabile
Solventi
acquosi
Solventi
ossigenati
Idro-
carburi
alifatici
Idro-
carburi
aromatici
Solventi
aprotici
dipolari
Solventi
Clorurati
Riduttori
ozono
Solventi
tossici e
cancerogeni
Acqua Alcoli n-Alcani Xilene Dimetil
solfossido
Cloruro di
metilene
Fluoro-
cloro-
alcani
Benzene
Eteri Ciclo-
alcani
Toluene (Dimetil
formammide)
Cloroformio Tetracloruro
di carbonio
Esteri Mesitilene 1,2-Dicloro-
etano
Chetoni
Carbonati
organici

Attilio Citterio
Risultati di Valutazione Ambientale, Salute e
Sicurezza (EHS) per Alcuni Comuni Solventi.42
0
1
2
3
4
5
6
Water hazard
Air hazard
Persistency
Chronic toxicity
Irritation
Acute toxicity
Reaction/decomposition
Fire/explosion
Release potential

Attilio Citterio
43
Approcci Correnti alla Sostituzione dei Solventi.
Non è un problema semplice – normalmente la sostituzione è complicata da vari fattori
Considerare il processo come un insieme, non come un singolo aspetto (i solventi sono usati nelle lavorazioni e purificazioni non solo come mezzi di reazione)
Si devono considerare molti aspetti e se ne deve quantificare la relativa importanza (metrica).
Da dove deriva il solvente?
Qual è il processo usato per preparare il solvente (senza dimenticare l’uso specifico per cui sono creati)?
• Energia
• Processi pericolosi
• Materie prime
• Sotto-prodotti
• Tossicità
Poco pericoloso
Salute umana
Ambiente (Locale e Globale)

Attilio Citterio
44
Sviluppo di Solventi Sostenibili.
Costoso
Pericoloso
da usarePericoloso per
l’ambiente
L’ottimizzazione del solvente può dare molti benefici!
Prestazione
finanziaria
Prestazione
ambientale
Eco
efficienzaEtica degli
affari
SD
Giustizia
ambientalePrestazione
sociale

Attilio Citterio
Solventi Non Graditi.45
Solvente rosso Flash point (C) Ragione
Pentano -49 flash point molto basso, disponibili buone alternative.
Esano(i) -23 Più tossco dell’alternativa eptano, classificato HAP negli USA.
Di-isopropil etere -12 Forte generatore di perossidi, disponibili buone alternative.
Dietil etere -40 flash point molto basso, disponibili buone alternative.
Diclorometano n/a Usato ad alti volumi, regolato in direttive EU, classificato HAP negli USA.
Dicloroetano 15 Cancerogeno, classificato HAP negli USA.
Cloroformio n/a Cancerogeno, classificato HAP negli USA.
Dimetil formammide 57 Tossicità, molto regolato in EU, classificato HAP negli USA.
N-Metilpirrolidinone 86 Tossicità, molto regolamentato in EU.
Piridine 20 Cancerogeno/mutageno/reprotossico (CMR) cancerogeno di categoria 3, tossicità, Valore limite di soglia (TLV) molto basso per l’esposizione.
Acetato di Metile 70 Tossicità, molto regolamentato nella Direttiva UE sui Solventi.
Diossano 12 CMR cancerogeno di categoria 3, classificato HAP negli USA.
Dimetossietano 0 CMR cancerogeno di categoria 2, tossicità.
Benzene -11 Da evitare: CMR cancerogeno di categoria 1, tossico per l’uomo e l’ambiente, basso TLV (0.5 ppm), molto regolato in EU e in USA (HAP).
Tetracloruro di Carbonio n/a Da evitare: cancerogeno di categoria 3, tossico, distruttore di ozono, bandito dal protocollo di Montreal, non disponibile per uso su larga scala, molto regolamentato in EU e in USA (HAP).

Attilio Citterio
Tabella di Sostituzione dei Solventi.46
Solvente non gradito Alternativa
Pentano Eptano
Esano(i) Eptano
Di-isopropil etere o dietil etere 2-MeTHF o tert-butil metil etere
Diossano o dimetossietano 2-MeTHF o tert-butil metil etere
Cloroformio, dicloroetano o tetracloruro di
carbonio
Diclorometano (??)
Dimetil formammide, dimetil acetammide
o N-metilpirrolidinone
Acetonitrile
Piridina Et3N (se la piridina è usata come base)
Diclorometano (estrazioni) EtOAc, MTBE, toluene, 2-MeTHF
Diclorometano (cromatografia) EtOAc/eptano
Benzene Toluene
“Green chemistry tools to influence a medicinal chemistry and research chemistry based organization”
Dunn and Perry, et. al., Green Chem., 2008, 10, 31-36

Attilio Citterio
Sostituzione di Solventi con Alternative Verdi.47
Espansione

Attilio Citterio
48
Strategie per la Sostituzione dei Solventi.
• Prima di tutto evitare o minimizzare i solventi
• Usare solventi meno tossici
• Usare solventi rinnovabili (non derivati dal petrolio)
• Evitare i VOC
Tossicità acquatica dei solventi
Biodegradabilità completa
Classificazione ambientale EU
Tossicità acuta umana
Tensione di vapore
Coefficiente di ripartizione Ottanolo/Acqua (OWPC)
Fonte/Fornitore
Potenziale di Creazione dell’Ozono Fotochimico (POCP)
PIU’ Altre Significative Problematiche.

Attilio Citterio
49
La Fonte è Sostenibile?
Confrontando dei solventi si deve tener presente:
Da dove derivano?
La fonte è sostenibile?
Esistono alternative (in particolare se si può non usare)?
Dove andrà a finire?
Come si possono neutralizzare i suoi effetti, se tossico-volatile?
Quanto costa il suo riciclo?
Quanta energia si recupera dalla sua combustione?

Attilio Citterio
50
Polare
Non-polare
Si ricordi
che il simile
scioglie il
simile
Soluti
sali
organici polari
grassi
oli
amminoacidi
polimeri
Costante
Dielettrica
78
2
33
25
21
2.2
2.4
4.8
acqua
metanolo
etanolo
acetone
cloroformio
toluene
CCl4esano
alcoli
idrocarburi
etere
Solventi
DMSO
DMF
Di Quali Solventi Abbiamo Bisogno?

Attilio Citterio
51
Uso di Solventi in Ricerca.
Uso di Solventi - Giornale "Perkin Trans 1"
Clorurati
Aprotici Dipolari
Altri Nocivi
Accettabili
Eco-compatibili
Uso di Solventi sul Giornale "Green Chemistry"
Clorurati
Aprotici Dipolari
Altri Nocivi
Accettabili
Eco-Compatibili

Attilio Citterio
52
Solventi Benigni.
La sostituzione di solventi VOC è fortemente auspicata per
ridurre i rischi di sicurezza e salute e molti sforzi sono stati
posti nel raggiungere questo obiettivo.
Alternative:
sintesi prive di solvente
acqua e solventi acquosi
fluidi supercritici (anidride carbonica, acqua, etano, ecc.)
liquidi ionici
solventi polimerici/immobilizzati/derivatizzati
altri solventi compatibili (lattato di etile)
Tutti hanno vantaggi e svantaggi che devono essere considerati quando
si valuta l’opportunità di una sostituzione.

Attilio Citterio
53
Solventi Non-
Volatili
Sistemi senza
solvente
Acqua
Altri Solventi
compatibili
Sistemi
Supercritici
Solventi
Organici Volatili
e Pericolosi
Soluzioni
per
solventi
Approcci alla Scelta di Solventi Eco-compatibili.
Liquidi ionici, polimeri
CO2

Attilio Citterio
54
Chimica ‘Senza Solvente’.
• Oggetto di indagine da molti anni
• Fornisce una delle più semplici soluzioni al problema dei solventi
• Non molte reazioni sono riconducibili all’approccio senza solvente, particolarmente su larga scala
• Le reazioni esotermiche possono essere pericolose su grande scala – necessaria una stretta collaborazione con gli ingegneri chimici per superare tali problemi
• Il mescolamento efficiente può essere un problema, particolarmente quando si impiegano reagenti o prodotti solidi
• Alcune tecnologie (macinazione, reattori per solidi, etc.) possono aiutare
• I solventi sono però ancora spesso richiesti per l’estrazione, separazione e purificazione dei prodotti.
Koichi Tanaka

Attilio Citterio
55
Reazioni Senza Solvente.
• Riscaldamento a
microonde/RF
• Raggi molecolari
Il miglior solvente è…
Proprio nessun solvente!
solido liquido gas
• Macinatura/molatura
• Reattori a letto fluido
• Reagenti a supporto
catalitico
• fase fusa

Attilio Citterio
56
Reazioni Senza Solvente (2).
• Quando i reagenti sono liquidi o quando uno dei reagenti è liquido ed
in grado di disperdere almeno in parte gli altri reagenti è bene
verificare se esistano condizioni in cui la reazione avviene senza
solvente.
• In taluni casi somministrare energia tramite microonde risulta
particolarmente vantaggioso, per es. nella sintesi dell’aspirina:
Bose, Stevens Institute of Technology

Attilio Citterio
57
Zeneca
R1COCH3
R2CHO
BaseR1COCH=CHR2
Friedel Crafts
Ar-H + RCOClZnCl2
ArCOR (processo continuo)
Ar-H + Ar’COClenvirocats
ArCOAr’ (Contract Chemicals UK)
Reformatsky
ArCHO + BrCH2CO2EtZn, NH4Cl
ArCHCH2CO2EtBase
OH
Org. Synt. Yield 61-64% K. Tanaka J. Org. Chem. 1991, 56, 4333
Sintesi Senza Solvente – Esempi.

Attilio Citterio
58
Solido A + Solido BMacinaz.
Solido C (resa quantitativa)
Reazioni per Macinazione Meccanica.
Ossidazione Generale
in Stato Solido con il
Complesso 1:1
Urea/H2O2
R. S. Varma and K. P. Naiker,
Org. Letters, 1999, 1, 189.

Attilio Citterio
59
Esempio: Reazione Solido-Solido in Letto Fluido.
Opportunità
Definizione delle condizioni di
mescolamento dei reagenti
• purezza e omogeneità del
prodotto (QA)
Richiesti dati sull’interfaccia
solido/solido
• Dimensione e forma particelle
• Chimica delle superfici
• Forze e interazioni inter-
particelle
Controllo sicuro del reattore
• Termodinamica e trasf. calore
• Evitare reazioni fuggitive
Robuste tecniche analitiche in
situ.
Prodotto
Uscita gas
Alimentazione gas
e solido II
Solid
Gas
Tubo di mandata
Condotto di ritorno
Alimentazione
Solido I Piatto dispersore del gas
misure analitiche
in-linea

Attilio Citterio
60
Condizioni senza Solvente.
Sistemi di Immagi DryView™
Tecnologia di visualizzazione Fototermografica
Usa chimica non umida
Non crea effluenti
Non richiede stadi di post-processo come essicazione
Applicabile a tutte le industrie che processano film pancromatici
(radiografia medica, stampa, radiografia industriale, e in campo
militare)

Attilio Citterio
61
macro
micro
nano
Distanza
m
mm
nm
reattore
particelle
molecole
Dinamica Molecolare
su Ampia e Multi-Scala
Metodi agli Elementi Finiti
Orientati ad Oggetti
Progettazione Ingegneristica
di Reattori, Impianti e
Circuiti di Alimentazione
Modellizzazione Molecolare
Quanto Meccanica
Collaborazione Chimica e Ingegneria Chimica – Essenziale!
Reazioni Solido-Solido : Necessitano di una
Modellazione su più Scale.

Attilio Citterio
62
Solventi Molecolari – L’Acqua.
+ Una delle alternative più ovvie ai VOC.
+ Pulito, economico, innocuo, versatile – il solvente per eccellenza!
- Utile per certi tipi di reazioni ma limitato a causa di:
- Scarsa solubilità per i soluti non-polari (però: vedi tensioattivi,
emulsioni e condizioni critiche)
- Compatibilità con vari reagenti (è attivo per via redox e acido-base)
- Si smaltisce scaricandolo nei corsi d’acqua
superficiali possibili inquinamenti
- La separazione può richiedere molta energia
o tempi lunghi di essiccazione
- Utile in processi bifasici con altri solventi.

Attilio Citterio
63
Solvente Benigno – Acqua.
Isomerizzazione del Geraniolo usando Acqua ad alta temperatura
Sintesi del 2,3-Dimetil-Indolo in Acqua ad alta temperatura
Sintesi del caprolattame in Acqua supercritica ad alta temperatura.

Attilio Citterio
64
Solvente Benigno – Acqua (2).
• Reazioni con enzimi/microorganismi
• Sospensioni
• PTC ed altri processi bifasici
• Analoghi di chimica anidra (e.g. ilidi allo zolfo, organometallica).
Zeneca Agrochem
MeX

Attilio Citterio
65
L’Effetto Idrofobico.
A A BB+ + 6 H2O
La formazione di una interazione idrofobica tra due molecole di
idrocarburo A e B. (I cerchi rappresentano molecole di acqua).
LE REAZIONI IN ACQUA SONO DI GRANDE POTENZIALITA’
(in condizioni supercritiche anche gli idrocarburi sono solubili!)

Attilio Citterio
66
Solventi Acquosi.
Condizioni acquose per la reazione di Diels-Alder:
Condizioni acquose per la reazione Metallo-Mediata:

Attilio Citterio
67
• La reazione è ACCELLERATA in acqua.
• Non serve alcun catalizzatore.
• La velocità e la selettività sono simili a quelle delle reazioni
condotte sotto pressione.
Situazioni simili si hanno con le reazioni di Diels-Alder con
2 substrati insolubili in acqua.
(R. Breslow, Tetr. Lett. 1984, 1239)
(A. Lubneau, J. Org Chem. 1986, 51, 2142)
1 2 3 (syn) 4 (anti)
Reazione di Mukaiyama.

Attilio Citterio
68
Reazioni in Acqua – Letteratura.
• Reviews:
A. Lubineau Chem. Ind. 1996, 123
Synthesis 1994, 9, 741
P. Grieco Chem. Rev. 1993, 93, 2023
Aldrichimica Acta 1991, 6, 159
R. Breslow Acc. Chem. Res. 1991, 6, 159

Attilio Citterio
69
Altre Idee per Solventi.
Solventi misti
Utili nel controllare accuratamente la solubilità del
prodotto attraverso il loro rapporto, ma difficili da
recuperare
Nessun solvente
Reagenti liquidi (alla temperatura scelta)
Alta efficienza volumetrica (alta produttività per
volume)
Problemi di sicurezza se il processo è esotermico.

Attilio Citterio
70
Solubilità dell’Acqua nei Solventi.
Solvente g/L M - log KD
Acqua 1000 56
Acetato di etile 33 1.8 1.5
Etere Etilico 15 0.8 1.8
Diisopropil etere 9 0.5 2.0
Cloruro di metilene 2 0.1 2.7
Cloroformio 0.7 0.04 3.1
Toluene 0.5 0.03 3.3
Tetracloruro di Carbonio 0.1 0.005 4
Esano 0.1 0.005 4

Attilio Citterio
71
Solventi Molecolari – Organici.
+ Sciolgono un’ampia varietà di soluti – in dipendenza dalle costanti dielettriche
+ I solventi volatili richiedono meno energia per la separazione dei prodotti
+ I solventi non volatili quali i glicoli (etilen e propilen glicoli e loro telomeri PEG, glicerina, ecc.) si usano sempre più frequentemente come solventi benigni
- Spesso tossici
- Generalmente a basso costo,
- infiammabili
- I VOC sono sotto il controllo delle normative di legge.

Attilio Citterio
72
Per Es.: Esteri dell’Acido Lattico.
• Economici, gli esteri dell’acido lattico ad alta-purezza, quali il lattato di etile, sono stati proposti per l’uso come "solventi verdi" ambientalmente accettabili
• Proprietà solventi attraenti:• Biodegradabile
• Facile da riciclare
• Non corrosivo
• Non cancerogeno
• Non diminuisce l’ozono• Buon solvente per vari processi
• ottenuti da fonti rinnovabili, i carboidrati, quali quelli del grano o dagli scarti di lavorazione di alimenti
• Potrebbero sostituire circa l’80% dei solventi derivati dal petrolio –attualmente già in uso.
• Comunemente usato nell’industria di vernici e rivestimenti. Http://www.er.doe.gov/epic/html/GreenSolvents.htm
72
CH3CH(OH)CO2CH2CH3

Attilio Citterio
73
Sistemi/Miscele Solventi Alternative.
Isomet
Miscela di idrocarburi isoparaffinici, propilenglicol monometil etere,
e alcol isopropilico
Sostituisce la miscela Typewash (cloruro di metilene, toluene e
acetone)
Eccellenti prestazioni nelle stampe e nel rotocalco
Accettabili proprietà (abilita pulente, velocità di evaporazione del
solvente, odore, rispetto ambientale e costo)

Attilio Citterio
Sistemi Bifasici e Ossidazione con H2O2.
RS
R'
74
Prodotto
Acqua
Alta selettività
Nessun solvente
Sottoprodotto acqua
Ausiliari riciclatiHMoO6
- Bu3NH+Ossidazione
• Utilizza due solventi immiscibili e cerca di mantenere in fasi
separate il catalizzatore e i reagenti per facilitare la separazione
• Generalmente basata su sistemi acquoso/organici (per es.
ossidazioni con H2O2). Talvolta l'organico è solvente e reagente.
• Le fasi sono omogenizzate agitando, con ultrasuoni o riscaldamento
Bu3NH+

Attilio Citterio
75
Solventi Neoterici.
• L’obiettivo è di progettare nuovi fluidi che presentano
proprietà aggiustabili.
• Alcuni già usati su larga scala altri hanno potenzialità di
divenire i solventi sostenibili del futuro.
• Il termine copre:
• liquidi ionici (IL-QA)
• fluidi supercritici,
• gas liquefatti,
• liquidi espansi con gas,
• solventi eutettici, e
• solventi polimerici

Attilio Citterio
76
Gas Liquefatti.
• I gas liquefatti sono gas che diventano liquidi a temperature ambiente
quando sono pressurizzati in un cilindro per gas. Il cilindro è riempito
inizialmente come liquido. Il liquido quindi evapora a gas e satura lo
spazio di testa sopra il liquido e mantiene l' equilibrio liquido-vapore.
Come il gas viene rilasciato dal cilindro, evapora abbastanza liquido
nello spazio di testa, mantenendo così costante la pressione nel
cilindro. Esempi di gas liquefatti includono l'ammoniaca, il biossido di
carbonio, il cloro, il metano e il gas naturale, il propano e i CHC.
• Attualmente usati principalmente per estrazioni ma anche come propellenti per aerosol
• Generalmente usati a bassa pressione, ~ 4-10 bar
• Tipici sono gli HFC (gas che non riducono l’ozono, non-tossici, non-infiammabili, ma sono gas serra dalla vita media molto lunga!)
www.ineosfluor.co.uk
www.advancedphytonics.co.uk

Attilio Citterio
77
riciclo del solvente
soluzione omogenea
reagenti prodotti
p p
Gas Liquefatti (2).
• Le transizioni gas-liquido sono dipendenti dalla pressione – più
efficienti in energia perché reversibili.
• Utili quando i residui di solvente sono un problema.

Attilio Citterio
78
Liquidi a Gas Espanso (GXL).
• Un GXL è un solvente misto composto da un gas
compressibile (quale CO2 o etano) sciolto in un
solvente organico.
• L’obiettivo è di variare le proprietà di un liquido
pressurizzandolo con un gas – generalmente
con piccole variazione di pressione
• Attualmente un’area di ricerca – grande
potenzialità per solventi non-tossici adattabili,
p.es. CO2/H2O
• Liquidi di Classe I, come l'acqua, hanno capacità
insufficienti a sciogliere CO2 e ad espandersi. I
liquidi di Classe II come il metanolo, l'esano e
molti altri solventi organici tradizionali, sciolgono
grandi quantità di CO2, si espandono
apprezzabilmente e subiscono significative
variazioni nelle proprietà fisiche.

Attilio Citterio
79
Effetti Solvente (Riferimenti).
1. Alternative Solvents for Green Chemistry (2), F. Kerton, R. Marriott
2011 .
2. Solvent Effects in Organic Chemistry , C. Reichardt VCH, 1989, 2nd Ed.
3. Solvent Recovery Handbook, l. Smallwood, E. Arnold June 1993 ISBN
0-340-57467-4
4. Industrial Solvents Handbook E.W. Flick, Noyes Data Corporation 1985
(2nd Ed.) - ISBN 0-8155-1010-1
5. Hansen Solubility Parameters: A user's handbook, II Ed. C.Hansen,
(2007). Boca Raton, Fla: CRC Press
6. Green Solvents I and II - Properties and Applications in Chemistry
Mohammad, Ali, Dr., Inamuddin (Eds.) 2012, XVIII, 430 p.
7. Hutchenson, K., et al.; ACS Symposium Series; ACS, DC, 2009