Sinapsi e Neurotrasmettitori
-
Upload
nicola-laurora -
Category
Documents
-
view
93 -
download
1
description
Transcript of Sinapsi e Neurotrasmettitori

1
TRASMISSIONE SINAPTICA
• La sinapsi è il punto di collegamento fra due strutture eccitabili
• (neurone-neurone, neurone-muscolo)
• I neuroni che formano una sinapsi sono unità distinte
• (Golgi, Ramon y Cajal et al)
• I segnali si trasmettono da un neurone all’altro attraverso punti di
collegamento funzionali
• (Eccles, Sherrington, et al)
• Esistono due tipi di sinapsi strutturalmente e funzionalmente diverse:
sinapsi elettriche e sinapsi chimiche
La scoperta della trasmissione
sinaptica

2
Golgi: TEORIA RETICOLARE
sistema nervoso come rete continua, come interconnessione globale di tutti i centri nervosi (derivata dal fisiologo francese Pierre Flourens)
tutte le facoltà del cervello, da quelle percettive a quelle cognitive, sono il risultato di un’azione di massa dell’intero cervello (1865-1871)
postulava un’assoluta continuità tra tutti gli elementi del sistema nervoso mediata dalla connessione completa delle fibre conduttive, assoni e dendriti, e alla base della possibilità di propagazione dell’impulso elettrico tra centri e vie distanti nel sistema nervoso
Golgi pensava che i dendriti non partecipassero alla trasmissione dell’impulso nervoso e che avessero come funzione quella dell’alimentazione dei tessuti
L’idea accettata era che l’impulso nervoso potesse viaggiare indifferentemente in entrambe le direzioni lungo le fibre nervose e cioè da e verso il corpo cellulare
Cajal: TEORIA NEURONALE
1888, studiando al microscopio il cervelletto e la retina, Cajal osservava che alcuni assoni terminavano liberamente, senza nessuna interconnessione fisica con altre fibre nervose
in un lavoro del 1889, Cajal concludeva che le cellule nervose, alla pari di quelle degli altri tessuti, dovevano essere considerate come unità indipendenti
aveva compreso che la conduzione avveniva sia in dendriti che in assoni
Nel 1891 Cajal esponeva la teoria della polarizzazione dinamica del neurone secondo la quale i dendritisono preposti alla ricezione del segnale e cioè alla conduzione degli impulsi nervosi verso il corpo cellulare; mentre gli assoni conducono i segnali nervosi verso i neuroni posti in relazione di contiguità

3
Charles ScottSherrington
““synapsesynapse””
Agli inizi del 1900 attraverso gli studi sui riflessi spinali Sherrington dimostra:
• L’unidirezionalità del flusso di informazioni (se reticolare->multidirezionale)
• Ritardo sinaptico (la “rete continua” non ha ritardo)
• L’azione coordinata di diverse sinapsi
• Azioni inibitorie ed eccitatorie
• Solo le azioni eccitatorie vengono propagate, quelle inibitorie “stabilizzano” il
neurone
Nobel 1932Nobel 1932
1950, microscopia elettronica: definitiva conferma della teoria neuronale

4
Dibattito sulla natura della trasmissione sinaptica: chimica o elettrica?
KatzKufflerEccles
Vs.
La trasmissione sinaptica è mediata chimicamente o da un
trasferimento di carica?
-Evidenze che la trasmissione alla NMJ era di natura chimica erano
accettate da molti.
-Altri erano convinti che alcuni aspetti della trasmissione sinaptica
erano troppo veloci per poter essere spiegati da un mediatore
chimico.
Flusso di
corrente ai punti
di contattto
Scarica
modificata
Eccles sinapsi
NM
Eccles sinapsi
eccitatorie e
inibitorie
SINAPSI ELETTRICA
• diffusione di ioni e molecole dal neurone pre- a quello post-sinaptico (~ 3.5 nm)• il flusso passivo della corrente passa nel poro delle giunzioni comunicanti• trasmissione bidirezionale• trasmissione rapida (0.1 ms)• sincronizzazione di gruppi di cellule
SINAPSI CHIMICA
• spazio intersinaptico 20-40 nm• la terminazione presinaptica contiene vescicole con neurotrasmettitori• l’attività è iniziata dal potenziale d’azione presinaptico• ingresso di Ca2+ presinaptico• ritardo sinaptico maggiore: 0.3-1.5ms• trasmissione unidirezionale

5
Struttura della sinapsi elettrica
• il canale della giunzione comunicante è formato da 2 emicanali, (connessone) ciascuno appartenente ad una cellula • connette il citoplasma delle due cellule• ogni emicanale è costituito da 6 subunità proteiche (connessine)• il poro si apre in seguito ad una breve rotazione delle subunità• l’apertura del poro è regolata dal: voltaggio, pH e Ca2+
giunzione comunicante
Esempi: Muscoli lisci e cardiaci, cervello e cellule gliali
RUOLO FUNZIONALE
• sincronizzazione rapida dei segnali
nervosi in cellule accoppiate elettricamente
• è diffusa nel SNC e nelle fibre muscolari
lisce e cardiache
Due elettrodi nella cellula presinaptica: - uno per iniettare I- uno per registrare Vm
La depolarizzazione passiva si registra senza ritardo ma con ampiezza ridotta nella cellula postsinaptica
La trasmissione attraverso sinapsi elettriche
� la trasmissione elettrica avviene anche quando il segnale presinaptico è sotto soglia
� la variazione di potenziale nella cellula postsinaptica è proporzionale all’ampiezza e alla forma della variazione di potenziale della cellula presinaptica
� le sinapsi elettriche trasmettono con la stessa efficienza i segnali in entrambe le direzioni (o in un solo verso - rettificanti)

6
LA SINAPSI CHIMICA
• è la più diffusa: SNC, SNP, neurone-muscolo scheletrico • la trasmissione è mediata da sostanze chimiche• introduce un certo ritardo• è unidirezionale
Le sinapsi chimiche: le fasi della trasmissione

7
• Il Ca2+ presinaptico è misurato con tecniche di microscopia a fluorescenza utilizzando sonde fluorescenti (fura-2) sensibili al Ca2+
• chelanti del Ca2+ presinaptico (EGTA, BAPTA) bloccano la risposta postsinaptica
post
pre
Iniezione di Ca2+ presinaptico
potenziale postsinaptico
pre
post post
pre
Prova di controllo Iniezione di chelante del
Ca2+
Ruolo del Ca2+ e dei canali del Ca2+ presinaptici
- il Ca2+ entra nel terminale presinaptico attraverso i canali del Ca2+ V-dipendenti (N e P/Q)
La trasmissione sinaptica è bloccata :
- utilizzando chelanti intrac. del Ca2+
- sostituendo il Ca2+con Mg2+
- bloccanti dei canali del Ca2+
(Cd2+ e neurotossine)
Potenziale
presinaptico
Corrente
presinaptica
di Ca2+
Potenziale
postsinaptico
Ruolo del Ca2+ e dei canali del Ca2+
presinaptici
Mediante prove di voltage clamp e bloccanti selettivi si dimostra che il calcio
necessario alla trasmissione sinaptica dipende da quello esterno

8
I canali del Ca2+ V-dipendenti sono addensati nelle zone attive presinaptiche, di fronte a gruppi di recettori nAChR localizzati sulla membrana postsinaptica
zone attive
canali del Ca2+ presinaptici
recettori nAChR postsinaptici
pliche giunzionali
fibre muscolari
terminazioni nervoseassone mielinato
Co-localizzazione dei canali del Ca2+ presinaptici e dei nAChR postsinaptici
canali del Ca2+ presinaptici
recettori nAChR postsinaptici
Co-localizzazione dei canali del Ca2+ e delle vescicole(motoneurone di rana)
a riposo depolarizzata� i rilievi allineati sulla m. presinaptica a riposo sono presumibilmente canali del Ca2+
� fusione di vescicole secretorie sulla membrana presinaptica a seguito di una depolarizzazione del terminale
� Struttura fine dei siti di fusione vescicolare della giunzione neuromuscolare di rana
� I canali del Ca2+ sono indicati in verde.
� In giallo sono indicate le proteine di ancoraggio

9
Ancoraggio e fusione delle vescicole
� l’ancoraggio avviene attraverso l’interazione di proteine plasmatiche solubili (NSF e SNAP25) con proteine associate alla m. vescicolare (VAMP o sinaptobrevina) e proteine associate alla m. plasmatica (sintaxina)
� la sinaptotagmina è il sensore del Ca2+
� le sinapsine ancorano le vescicole al citoscheletro e facilitano l’avvicinamento alla m. plasmatica� il poro di fusione si attiva con il Ca2+ e inizia l’esocitosi
mobilizzazione
Il complesso SNARE
La vescicola si ancora Si formano i complessi SNARE per tirare le membrane
Il Ca2+ che entra si lega alla sinaptotagmina
La sinaptotagmina che ha legato il Ca2+ catalizza la fusione della
membrana
NSF (NEM-Sensitive Fusion Protein)
SNARE (SNAP Receptors)
SNAP (Soluble NSF-Attachement Protein)
VAMP (Vesicle Associated Membrane Protein)

10
Tetano
paralisi spastica (tossina tetanica, TeNT) (clostridium tetani)
Botulismo
paralisi flaccida (tossina botulinica, BoNT)(clostridium botulinum)
� TeNT e BoNT agiscono sul motoneurone e vengono internalizzate nel citoplasma tramite trasporto retrogrado, TeNT migra negli interneuroni inibitori (cellule di Renshaw) e blocca la trasmissione delle sinapsi inibitorie (paralisi spastica)
� BoNT e TeNT sono proteasi che causano la scissione del complesso SNARE.
Le BoNT bloccano il rilascio di ACh dalla giunzione neuromuscolare (paralisi flaccida)
� Le BoNT sono utilizzate come agentiterapeutici per la cura della:a) distonia cervicaleb) blefarospasmoc) emispasmo facciale
Meccanismo d’azione delle tossine tetaniche e botuliniche

11
Riempimento e riciclo vescicolare
• la membrana delle vescicole fuse viene recuperata (endocitosi), passa attraverso vari comparti endocellulari ed è riutilizzata per un nuovo ciclo
• le nuove vescicole vengono riempite da molecole di neurotrasmettitore, si ancorano alla membrana presinaptica e rimangono a disposizione per partecipare all’esocitosi
“pool” di riserva
“pool” di vescicole pronte per la fusione
Ancoraggio
Gemmazione
Fusione
Endocitosi
Preparazione
Esocitosi
Endocitosi
Endosoma
Destino del neurotrasmettitore
Ricaptazione Degradazione
Diffusione (?)
Tutti i neurotrasmettitori Sinapsi colinergica (AChE)
Sinapsi monoaminergica (MAO)

12
I NEUROTRASMETTORI ED I LORO RECETTORI
PRINCIPALI NEUROTRASMETTITORI
Acetilcolina
Glutammato
Aspartato
GABA
Purine
NEUROTRASMETTITORI A BASSO PESO MOLECOLARE
Dopamina
Noradrenalina
Adrenalina
Serotonina (5-HT)
Istamina
glicina

13
• molecole costituite da un numero variabile di aminoacidi (3-36)
• contenuti in vescicole di dimensioni maggiori
• sintetizzati come pre-proteine del reticolo endoplasmatico rugoso dove viene rimossa la sequenza segnale. La pre-proteina risultante attraversa l’apparato di Golgi e viene immagazzinata in vescicole. All’interno delle vescicole si completa la formazione del peptide: scissione proteolitica, modificazione delle estremità del peptide, glicosilazione, fosforilazione, formazione dei ponti disolfuro.
Neurotrasmettitori peptidici (più di 100 peptidi, composti da 3 a 30 amminoacidi)
• I neurotrasmettitori liberati per esocitosi dalla cellula presinaptica si legano ai recettori sulla cellula postsinaptica, facendo aprire (o chiudere) canali ionici
• I recettori postsinaptici hanno il ruolo di:
- riconoscere il neurotrasmettitore
- attivare i rispettivi effettori
• Si dividono in due classi principali: ionotropi e metabotropi
Autorecettori presinaptici: sono recettori che rispondono al neurotrasmettitore prodotto da quello stesso neurone. Probabilmente, gli autorecettori svolgono funzioni di feedback negativo. Dopo che il terminale ha rilasciato il neurotrasmettitore, alcune sue molecole fannoritorno verso il neurone presinaptico, dove attivano autorecettori che, a loro volta, inibiscono l’ulteriore rilascio di neurotrasmettitore.

14
� il recettore è un canale ionico� sono recetori ionotropi: nAChR, GABAA, glicina, Glutammato (NMDA, AMPA, kainato)� azione rapida (ms)
Recettori ionotropi
IL RECETTORE NICOTINICO (COLINERGICO)DELL’ACETILCOLINA

15
Trasmissione Colinergica
• Tutti i motoneuroni che attivano il m. scheletrico
• Tutti i neuroni pregangliari del S.N.A.
• Tutti i neuroni postgangliari del parasimpatico
Recettore nicotinico dell’ACh (nAChR): struttura
• costituito da 5 subunità (2α, β, ε, δ) (P.M. 250 kD)• forma un poro acquoso • attivato da 2 molecole di ACh• permeabile a Na+, K+, Ca2+• bloccato da: d-tubocurarina (alcaloide)αααα-bungarotossina (proteina)αααα-conotossina (proteina)
• costituito da 5 subunità (2α, β, ε, δ) (P.M. 250 kD)• forma un poro acquoso • attivato da 2 molecole di ACh• permeabile a Na+, K+, Ca2+• bloccato da: d-tubocurarina (alcaloide)αααα-bungarotossina (proteina)αααα-conotossina (proteina)
εε ε

16
Un’altra vista dell’nAChR del muscolo scheletrico
• Gli nAChR nel muscolo scheletrico
• Diversità durante lo sviluppo fetale: formati da 4 subunità (α, β, γ, δ, manca ε) secondo un rapporto 2α:β:γ:δ.
• Caratteristiche biofisiche diverse: bassa conduttanza lunghi tempi di apertura
• Differente localizzazione embriogenesi/muscolo denervato
fotografia al microscopio
elettronico dell’nAChR
•Gli nAChR dei neuroni
•sono pentameri (α2−10, β2−4) secondo un rapporto 2α:β:γ:δ..
•Formano recettori eteromerici o omomerici con caratteristiche funzionali diverse.
• Maggiormente permeabili al Ca2+ rispetto a quelli periferici
Recettori nicotinici centrali dell’Ach

17
L’enzima ACh-esterasi
• l’ACh-esterasi è presente sulla membrana post-sinaptica
• idrolizza l’ACh in acetato + colina
• è responsabile della fase decrescente del p. di placca
• inibitori dell’ACh-esterasi potenziano l’attività della sinapsi
Stimolo presinaptico
t (ms)
azione della ACh-esterasiattivazione
del
nAChR
Recettore nicotinico dell’ACh (nAChR): funzione
• legame dell’ACh con il recettore a livello della placca motrice apertura del canale: entrata di Na+ e uscita di K+
• potenziale di placca• depolarizzazione postsinaptica• successiva apertura dei canali del Na+ e K+ V-dipendenti• ingresso di Na+ e ulteriore depolarizzazione• genesi e propagazione del p.d.a.
Ciclo vitale dell’ACh

18
LA TRASMISSIONE SINAPTICA NELLA GIUNZIONE NEUROMUSCOLARE
La giunzione neuromuscolare: struttura
A livello del muscolo l’assone della cellula nervosa si
suddivide in sottili branche. Ogni branca forma
numerose espansioni dette bottoni sinaptici,
ricoperte da un sottile strato di cellule di Schwann.
Questi bottoni sinaptici riposano su una regione
specializzata della membrana muscolare detta
placca motrice.
A livello della placca motrice la membrana
presinaptica e quella postsinaptica sono separate da
uno spazio di 50 µm nel quale viene riversato il
contenuto delle vescicole sinaptiche, rappresentato
dal neurotrasmettitore acetilcolina.
La membrana postsinaptica è organizzata in pieghe
giunzionali, le quali sono ricche di recettori per
l’acetilcolina.
Le zone attive e le vescicole sinaptiche
La giunzione neuromuscolare è una struttura
altamente specializzata

19
stimolando il motoneurone (presinaptico) si registra a livello della cellula muscolare (postsinaptica) un potenziale di placca (EPP, end-plate potential), che depolarizza le membrana fino alla soglia del potenziale d’azione.
IL POTENZIALE DI PLACCA
� Il potenziale di placca è eccitatorio e ha un’ampiezza elevata (40 mV)
� il curaro riduce sotto soglia l’ampiezza dell’EPP. Si può cosìstudiare il potenziale di placca (EPP) senza il p.a.
� se l’EPP è sopra soglia, il p.d.a. che si genera si propaga lungo la fibra muscolare senza decadere e causa la contrazione del muscolo
� il curaro riduce sotto soglia l’ampiezza dell’EPP. Si può cosìstudiare il potenziale di placca (EPP) senza il p.a.
� se l’EPP è sopra soglia, il p.d.a. che si genera si propaga lungo la fibra muscolare senza decadere e causa la contrazione del muscolo
p. di placca
V soglia -55 mV
controllo+curaro
(bassa dose)
+curaro(alta dose)
Propagazione del potenziale di placca
stimolo
stimolo
50 mV
� la presenza di un’alta densitàdi canali del Na+ e K+ lungo la fibra muscolare converte l’EPP in un PdA che si propaga lungo la fibra e stimola la contrazione.
� la presenza di un’alta densitàdi canali del Na+ e K+ lungo la fibra muscolare converte l’EPP in un PdA che si propaga lungo la fibra e stimola la contrazione.
� il potenziale di placca ha la massima ampiezza nel sito di insorgenza: a livello della placca motrice� è dovuto ad un flusso netto di corrente positiva entrante� si propaga passivamente e diminuisce in funzione della distanza
� il potenziale di placca ha la massima ampiezza nel sito di insorgenza: a livello della placca motrice� è dovuto ad un flusso netto di corrente positiva entrante� si propaga passivamente e diminuisce in funzione della distanza

20
� l’insorgenza dell’EPP è causata da un aumento della concentrazione di acetilcolina (ACh) nella fessura sinaptica (fase di attivazione dell’EPP).
� l’ACh è rilasciata dalle terminazioni presinaptiche del motoneurone
� a livello della placca motrice sono concentrati i recettori nicotinici per l’acetilcolina (nAChR) che sonorecettori-canali
� l’ACh si lega agli nAChR che si attivano e sono permeabili al Na+/K+/Ca2+. Si genera un flusso netto di cariche positive entranti.
� la membrana postsinaptica si depolarizza
� la concentrazione di ACh si riduce rapidamente ad opera dell’enzima acetilcolinesterasi (ACh-esterasi) e per diffusione (fase di decadimento dell’EPP)
Chi genera il potenziale di placca?
Stimolo presinaptico
t (ms)
azione della ACh-esterasiattivazione del nAChR
Per studiare quali ioni attraversino i recettori-canale dell’acetilcolina, sono state
misurate le correnti sinaptiche evocate nel terminale postsinaptico dalla
stimolazione degli assoni presinaptici imponendo sperimentalmente diversi valori
del potenziale di membrana alla cellula postsinaptica.
Individuare a quale potenziale di membrana le correnti ioniche che attraversano i
recettori-canali si azzerano dà un’importante informazione in quanto, a seconda del
suo valore, indica se la corrente sinaptica è mediata dal sodio, dal potassio o da
entrambi.
Gli esperimenti hanno mostrato che la corrente sinaptica che attraversa i recettori
nicotinici per l’acetilcolina diventa nulla se si impone un potenziale di membrana di 0
mV. Questo potenziale viene chiamato potenziale di inversione.
Un potenziale di inversione di 0 mV non corrisponde né al potenziale di equilibrio
del potassio EK né a quello del sodio ENa. In effetti, i recettori nicotinici per
l’acetilcolina hanno permeabilità mista sodio-potassio.

21
-100mV (EK+)
-90mV
0mV
+70mV (ENa+)
Potenziale d’inversione INa+=-IK+
INa+ = gNa+ (Vm – ENa+)
Potenziale
Post‐‐‐‐sinaptico (EPP)
Corrente
Post‐‐‐‐sinaptica
IK+ = gK+ (Vm – EK+)
Correnti ioniche e potenziale di placca
NATURA QUANTICA DEL RILASCIO DEL NEUROTRASMETTITORE

22
• anche in assenza di stimolazione presinaptica, si registrano sulla cellula muscolare modificazioni spontanee del potenziale di membrana
• sono analoghe al EPP ma di ampiezza notevolmente inferiore (< 1 mV)
• hanno la stessa farmacologia; sono denominati potenziali di placca in miniatura (mEPP)
Potenziali di placca in miniatura (mEPP)
Che relazione esiste tra EPP e mEPP?
• riducendo il Ca2+ extra- cellulare, si riduce il rilascio di ACh.
• l’ampiezza degli EPP diminuisce al di sotto della soglia.
• stimolando il motoneurone in basso Ca2+ l’ampiezza degli EPP si riduce a multipli interi dell’ampiezza dei mEPP.

23
� i mEPP sono il prodotto del rilascio di una unità di mediatore, ovvero del contenuto di una vescicola presinaptica. Una vescicola (unità di mediatore) contiene 10.000-40.000 molecole di ACh e causa un mEPP di 0.5-1 mV
� durante una stimolazione viene rilasciato il contenuto di 200-300 vescicole che permettono di raggiungere con sicurezza un potenziale di placca di circa 30-60 mV (giunzione neuromuscolare)
Teoria del rilascio quantico
• l’ampiezza più piccola (unitaria o quanto) corrisponde ad un mEPP
• le altre ampiezze (gli EPP) sono multipli interi di un mEPP
Ampiezze degli EPP in basso Ca2+Ampiezze dei mEPP
Ampiezza potenziali di placca in miniatura (mV)
Ampiezza potenziali di placca (mV)
1
2X
4X
1X
- stimolo + stimolo
La quantità di neurotrasmettitore che viene rilasciato dipende dall’intensità dello stimolo iniziale, che a sua volta dipende dalla frequenza di scarica dei potenziali d’azione.
Teoria del rilascio quantico: considerazioni
Regola:L’entità dello stimolo è decodificata dalla frequenza di generazione (frequenza di scarica) del potenziale d’azione.

24
I RECETTORI IONOTROPI DEL GLUTAMMATO
principale neurotrasmettitore eccitatorio del sistema nervoso centrale
• L’attività eccitatoria dei neuroni del cervello e del midollo viene regolata dai diversi tipi di recettori del glutammato:- i recettori ionotropi (recettori-canale)- i recettori metabotropi (controllano canali ionici attraverso secondi messaggeri)
Glutammato
Recettori ionotropi del glutammato
• Tre tipi:
- AMPA (Na+, K+)- NMDA (Na+, K+, Ca2+)- kainato (Na+, K+)
• proteine formate da 4 subunità
• L’apertura del recettore NMDA è potenziata dalla glicina.
• Il Mg2+ blocca il canale NMDA a riposo

25
Al potenziale di riposo il canale NMDA non conduce perché è bloccato dal Magnesio.
Il blocco del Magnesio viene rimosso a potenziali positivi
I recettori AMPA e NMDA colocalizzano nelle strutture del SNC, il rilascio del
glutammato evoca sempre risposte miste
(APV) acido fosfoaminovalerico inibitore NMDA-R
Corrente AMPA
precoce
Formazione di spine
dendritiche durante la
long-term-potentiation
(LTP)
LTP
I meccanismi alla base del potenziamento a lungo termine (LTP, plasticitàsinaptica)
• il glutammato si lega ai recettori AMPA e NMDA.
• l’NMDA a riposo è bloccato dal Mg2+ e si apre solo quando la membrana è depolarizzata.
• ripetute depolarizzazioni della m. postsinaptica rimuovono il blocco del Mg2+, permettendo al Ca2+ di entrare (rivelatore di coincidenza)
•il Ca2+ attiva delle proteine chinasi che inducono modificazioni locali dei bottoni e producono un messaggero retrogrado (NO?) che, a livello presinaptico, causa un ulteriore aumento della liberazione di glutammato
• effetto potenziante a feedback positivo che induce plasticità sinaptica (alterazione funzionale pre- e post-sinaptica delle sinapsi)
• l’effetto può essere a lungo (LTP) o a breve termine (STP)

26
I RECETTORI IONOTROPI DELGABA E DELLA GLICINA
• il GABA (acido γ-amino butirrico) e la glicina sono neurotrasmettitori inibitori• attivano recettori-canale permeabili al Cl-
GABA e glicina
Picrotossina(antagonista)
Il recettore GABAA
• costituito da 5 subunità α, β, γ, δ, ρα, β, γ, δ, ρα, β, γ, δ, ρα, β, γ, δ, ρ• permeabile al Cl- che entra all’interno della cellula • causa iperpolarizzazioni quando èaperto dal GABA
I recettori del GABA si trovano
principalmente nelle regioni rostrali del
SNC ma anche nel midollo spinale
I recettori della glicina prevalgono nel
midollo spinale, sono coinvolti nei riflessi
e nel coordinamento motorio.

27
Modulazione del GABAA
• sito di legame per benzodiazepine(ansiolitici) e barbiturici, che potenzianol’effetto inibitorio del GABA.
• il potenziale inibitorio è più ampio e persiste più a lungo in presenza di ansiolitici.
Il recettore GABAB è un recettore metabotropo
GABA (in presenza di barbiturico
o benzodiazepina)
GABA
20 mV
L'interazione del GABA con i recettori GABAB attiva principalmente una proteina G
inibitoria (Gi), che produce una inibizione dell'enzima adenilato ciclasi. La riduzione
della concentrazione di cAMP si traduce in una riduzione dei livelli di fosforilazione
ed inibizione funzionale dei canali calcio/voltaggio dipendenti implicati nel controllo
presinaptico del rilascio di neurotrasmettitori o a livello postsinaptico sull’apertura
dei canali del K+.
• Il recettore metabotropo non è un canale. E’ una proteina con 7 α-eliche transmembranali, attiva una proteina G che a sua volta attiva altri effettori (canali e/o secondi messaggeri)
• Sono recettori metabotropi: mAChR, GABAB, αααα- e ββββ- adrenergici,
glutammato, neuropeptidi, dopamina (D1-D5), …
• Azione lenta (100 ms-100 s)
Recettori metabotropi

28
La trasmissione sinaptica indiretta (o a secondo messaggero)
Trasmettitori:
GABA (GABAB)
Glutammato (metabotropici)
Acetilcolina (muscarinici)
Noradrenalina
Dopamina
Serotonina
Oppioidi ed altri….
Trasmettitori:
GABA, glicina
Glutammato
Acetilcolina (nicotinici)
La proteina G, attivata dal recettore, attiva (o chiude) direttamente i canali ionici.
Recettori metabotropi
La proteina G, attivata dal recettore, attiva (o inibisce) enzimi che producono secondi messaggeri che, a loro volta attivano o chiudono canali ionici.

29
• I recettori accoppiati a proteine G sono formati da una sola subunitàcomposta da 7 segmenti (α-eliche) di catena polipeptidica trasmembranari• Il sito di legame per il neurotrasmettitore: sulla porzione extracellulare • Il sito di legame per la proteina G: nel III loop intracellulare• Non formano canali ionici, ma attraverso l’attivazione delle subunità a e bg delle G proteine possono aprire o chiudere canali di vario tipo (Na+, K+ o Ca2+) e quindi indurre risposte eccitatorie o inibitorie. • Si parla di un’azione sui canali ionici mediata dal recettore metabotropo
Il recettore muscarinico dell’ACh
fosfolipasi C (PLC)
attivazione, IP3 e aumento di
calcio, eccitazione
SNC, sostanza neraM5
Gi: Inattivazione adenilatociclasi diminuzione cAMP, ↓conduttanza del Ca
2+;↑
conduttanza al K+
Corteccia, striato, coordinamento
motorioM4
fosfolipasi C (PLC)
attivazione, IP3 e aumento di
calcio
contrazione muscolo liscio;
secrezione ghiandolareM3
Gi: Inattivazione adenilatociclasi diminuzione cAMP, ↓conduttanza del Ca
2+; ↑
conduttanza al K+
SNC: ubiquitario; Cuore: Inibizione
neuronale effetti inotropi e
cronotropi negativii
M2
fosfolipasi C (PLC)
attivazione, IP3 e aumento di
calcio, eccitazione
Corteccia, ippocampo:
Eccitazione SNC, memoria?M1
MeccanismoLocalizzazione/EffettiTipo di
recettore
Recettore metabotropici dell’ACh

30
• il glutammato si lega anche ad un recettore metabotropo causando:- attivazione di una proteina Gq- attivazione della PLC (fosfolipasi C)
oppure
- Attivazione di una proteina Gi- diminuzione cAMP- aumento IK+- riduzione ICa2+
Recettori metabotropi del glutammato
Recettori metabotropi del glutammato
I recettori del gruppo I sono implicati nei processi associati alla regolazione della depolarizzazione di membrana (inibizione di canali del K+ e/o- apertura dei
canali del Ca2+)
I recettori metabotropici del glutammato dei terminali presinaptici sono responsabili della regolazione del rilascio di neurotrasmettitore (gruppo II e III)
Abbondanti nello striato,
ippocampo e cervelletto

31
Dopamina
I recettori adrenergici attivati dalla A e NA sono di tipo metabotropo e sono divisi in due classi : αααα (α1, α2) e ββββ (β1,
β2, β3). Possono attivare la via dell’IP3 o del cAMP/PKA.
Recettori adrenergici
La noradrenalina è un importante mediatore nervoso del cervello emozionale:
-comportamenti d'emergenza e nella risposta allo stress.
-A livello del SNC produce attivazione cerebrale, aumentando l'attenzione e la vigilanza;
- A livello periferico, via nervoso simpatico, media gli aggiustamenti funzionali ai comportamenti di lotta e fuga(es. l'aumento del battito cardiaco, della pressione arteriosa, della mobilitazione degli zuccheri, della dilatazionedei bronchi, ecc.
Gs: attivazione adenilato
ciclasi , aumento cAMP
Lipolisi e termogenesiβ3
Gs: attivazione adenilato
ciclasi , aumento cAMP
Rilasciamento muscolo liscioβ2
Gs: attivazione adenilato
ciclasi , aumento cAMP
contrazione muscolo cardiacoβ1
Gi: Inattivazione adenilato
ciclasi diminuzione cAMP,
inibizione canali del K+
Contrazione/dilatazione (α2 gangli
simpatico e autorecettori) muscolo
liscio vasi
α2
Gq: fosfolipasi C(PLC)
attivazione, IP3 e aumento di
calcio
contrazione muscolo liscio vasiα1
MeccanismoEffettiTipo di
recettore
Recettori adrenergici

32
D2
D1
Gi/0: diminuzione adenilato
ciclasi , aumento IP3
Corteccia, limbico: umore
emozioni comportamentoD4
Gi/0: diminuzione adenilato
ciclasi , aumento IP3
limbico,ipotalamo:
comportamento, prolattinaD3
Gi/0: diminuzione adenilato
ciclasi , aumento IP3
Corteccia, limbico, Striato,
ipotalamo: umore, controllo
motorio,comportamento
prolattina
D2
Gs: attivazione adenilato
ciclasi , aumento cAMP
Sistema limbico, striato:
emozioni, controllo motorioD5
Gs: attivazione adenilato
ciclasi , aumento cAMP
Corteccia, limbico, striato:
emozioni, umoreD1
MeccanismoLocalizzazione/funzioneTipo di
recettore
Recettori dopaminergici
I sistemi a proiezione diffusaSistema noradrenergico
Sistema dopaminergico
-implicato nei processi del rinforzo
psicologico nelle funzioni cognitive.
- trasmettitore nervoso principale del
nucleo del locus coeruleus, (integra le
informazioni sensoriali proiettandole alla
neocorteccia.
-Il principali neurotrasmettitori dei nuclei
della base (coordina il comportamento
motorio, es. sostanza nera e corpo
striato sede del controllo del
coordinamento motorio).
-Proiezioni
dell’amigdala:umore/emozioni.

33
L’apertura di canali ionici nella cellula postsinaptica causa una variazione transiente del potenziale, detta potenziale postsinaptico che può essere di tipo eccitatorio oinibitorio
� il potenziale postsinaptico inibitorio è una variazione transiente del potenziale di membrana verso valori più negativi rispetto al potenziale di membrana a riposo (es. da –60 mV a –70, –80 mV).
� il potenziale postsinaptico eccitatorio è una variazione transiente del potenziale di membrana verso valori meno negativi rispetto al potenziale di membrana a riposo (es. da –60 mV a –20 mV).
Sinapsi eccitatorie e sinapsi inibitorie
� potenziale post-sinaptico inibitorio (IPSP) (inhibitory post-sinaptic potential)
� potenziale post-sinaptico eccitatorio (EPSP) (excitatory post-sinaptic potential)
-60 mV
-60 mV
IPSP
EPSP
20 mV
Attività sinaptica eccitatoria
E’ associata all’apertura di canali ionici selettivi per:
Na+
Na+ + K+
Na+ + Ca2+
Infatti, questi canali hanno potenziali di inversione (pot. di Nernst) più positivi del potenziale di riposo della cellula (Vm = - 60 mV)
ENa = + 63 mV
ENa+K = - 20 mV
ENa+Ca = + 65 mV
EPSP
-60 mV

34
Attività sinaptica inibitoria
È causata dall’apertura di canali selettivi per:
K+
Cl-
infatti questi canali hanno potenziali di inversione più negativi del potenziale di riposo della cellula (Vm = - 60 mV)
EK = - 80 mV
ECl = - 70 mV
IPSP
-60 mV
Meccanismi di integrazione sinapticasinapsi eccitatorie ed inibitorie

35
Sommazione spaziale e temporale dei potenziali postsinaptici
Nelle sinapsi centrali la convergenza di stimoli è l’elemento chiave della
comunicazione nervosa
Regola generale
Monticolo assonico
• L’eccitamento a livello somatico insorge ogni qualvolta la somma algebrica (spaziale e temporale) di tutti i potenziali postsinaptici (eccitatori e inibitori) raggiunge o supera la soglia di attivazione.
• In tal caso, a livello del monticolo assonico si genera un potenziale d’azione che si propaga lungo l’assone
• Il monticolo assonico è una zona del neurone con “soglia di attivazione” più bassa, perché contiene densità di canali del Na+ voltaggio-dipendenti più alte che nel resto del soma.

36
E’ molto importante capire come l’attività
delle varie sinapsi si integrino.
…e quindi la
localizzazione
delle sinapsi ,
che si
raggiunge
durante lo
sviluppo, e’
importante
Le proprieta’ passive sono importanti
Il risultato finale di tutta l’attivita’ sinaptica inibitoria ed eccitatoria e’ rappresentata dalla frequenza di scarica in uscita lungo
l’assone.L’inibizione modula la scarica impedendo l’instaurarsi di potenziali
di azione o diminuendo la probabilità che vengano generati.
Eccitatorio: avvicina Vm alla soglia per la generazione di un potenziale di azione
Inibitorio: diminuisce la probabilita’che si superi la soglia per la generazione di un potenziale di azione.
Presenza di inibizione
Assenza di inibizione

37
Le sinapsi indirette che non usano trasmettitori che
legano recettori-canali come il glutammato o il GABA,
influenzano l’eccitabilità della cellula postsinaptica
causando l’attivazione di cascate biochimiche che
regolano l’apertura o la chiusura di canali posti su
tutta la membrana postsinaptica.
L’attività di questi neurotrasmettittori
(neuromodulatori) è poco evidente per se, ma si
evidenzia con una facilitazione o depressione delle
risposte del neurone postsinaptico ad altri ingressi.
Questa è la neuromodulazione.
La neuromodulazione
Es. di neuromodulazione: L’azione degli oppioidi sulla trasmissione del
dolore è mediata da sinapsi che modulano l’efficacia della sinapsi tra la fibra
nocicettiva afferente e il neurone che trasmette l’informazione dolorifica
centralmente.

38
Un esempio di
neuromodulazione:
la noradrenalina
rimuove
l’adattamento
chiudendo i canali
del potassio calcio
dipendenti nei
neuroni
dell’ippocampo
+TEA
+TTX
Integrazione sinaptica

39
I circuiti nervosi possono modificarsi in risposta all’esperienza
La plasticità’ è presente in tutto il SNC, ma in particolar modo a livello
della corteccia cerebrale
Senza di essa
•Il nostro cervello non si sarebbe sviluppato in maniera
normale
•Il nostro comportamento sarebbe stereotipato ed
immodificabile dall’esperienza
•Saremmo esseri senza memoria del passato
Questa capacità si definisce plasticità neurale
I cambiamenti dei circuiti neurali in risposta all’esperienza
sono meno evidenti man mano che la plasticità corticale
diminuisce con il procedere dello sviluppo
Tuttavia, la plasticità corticale è presente nell’adulto, sia in
risposta ad aumenti dell’attività afferente (apprendimenti) sia in
risposta a riduzioni dell’attività afferente (lesioni)

40
Comprendere i meccanismi alla base della
plasticità corticale, sia durante lo sviluppo
che nell’adulto, potrebbe permettere di:
•correggere difetti insorti in seguito ad un
processo di sviluppo deficitario o scorretto
•sfruttare al meglio o potenziare i tentativi
spontanei di recupero che il sistema nervoso
mette in atto dopo una lesione
Le “regole” della plasticità
Raffinamento e maturazione dei circuiti neurali durante
lo sviluppo
Formazione di una traccia di memoria

41
Plasticità neurale: capacità dei circuiti nervosi di modificarsi,
cambiando quindi la loro uscita, in risposta all’esperienza
Cosa cambia nel circuito?
L’efficacia delle connessioni sinaptiche si modifica in risposta ai
cambiamenti nell’attività elettrica che l’esperienza induce nel
circuito
Ingresso
presinaptico
Risposta
postsinaptica
Esperienza
(cambio di attività mantenuto nel tempo)
Ingresso
presinaptico
Risposta
postsinapticao
Donald O. Hebb1904-1985
…quando un assone della cellula A (la cellula presinaptica)
prende parte ripetitivamente nel processo di eccitamento della
cellula B (la cellula postsinaptica), qualche cambiamento
strutturale o metabolico subentra in una o entrambe le cellule in
modo che l'effcienza di A, come cellula eccitatrice di B, aumenti.

42
Meccanismo Hebbiano di plasticità:
rafforzamento delle sinapsi con attivita’
sincrona
… se un neurone presinaptico A attiva ripetutamente il neurone
postsinaptico B la connessione sinaptica fra A e B si rafforza
Corollario: se A fallisce ripetutamente nell’attivare B, la
connessione fra A e B si indebolisce
Meccanismo Hebbiano di plasticità:
rafforzamento delle sinapsi con attivita’ sincrona
Neuroni presinaptici
attivi sincronicamente
Neuroni presinaptici
attivi asincronamente
Attività del neurone
postsinaptico

43
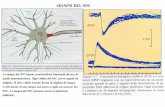
Esempio di potenziamento a
lungo termine. Uno stimolo
ad alta frequenza (treno di
impulsi, indicato con il
triangolo nero) produce un
incremento transitorio della
risposta sinaptica (LTP
precoce). Se si eseguono 4
stimolazioni ad alta
frequenza si ha un
potenziamento maggiore e
permanente nel tempo (LTP
tardivo).
Tratto da Kandel et al., 2003.
La verifica sperimentale dell’ipotesi di Hebb si ebbe con la scoperta, all’inizio degli
anni ’70, del fenomeno del potenziamento a lungo termine (LTP).
Monitorando le ampiezze degli EPSP ci si accorse che la risposta a stimoli test somministrati a bassa
frequenza (uno ogni 15-60 secondi) aumentava se la sinapsi veniva sottoposta ad un breve episodio di
stimolazione ad alta frequenza. Se venivano somministrate ripetute stimolazioni ad alta frequenza, il
potenziamento era più ampio e permanente nel tempo. Questi fenomeni sono presenti sia in vitro che in
vivo e sono stati osservati in molte aree cerebrali.
pende
nza E
PS
P m
V/m
s
Giro dentato
Via perforante
Cellule Granulari
Collaterali di
Schaffer
CA1
CA3
La funzione probabile della LTP e quella di permettere l’apprendimento di
informazioni di tipo non procedurale: struttura ippocampo

44
Nel corso della normale trasmissione sinaptica a
bassa frequenza, il glutammato liberato dalle
terminazioni presinaptiche agisce sia sui recettori
NMDA che su quelli AMPA.
Na+ e K+ tuttavia passano soltanto attraverso i
recettori AMPA in quanto, a livello di riposo del
potenziale di membrana, i canali-recettori NMDA
sono bloccati dal Mg2+.
Trasmissione sinaptica normale
Induzione di LTP
Quando la membrana postsinaptica viene
depolarizzata dall’azione dei AMPA, come accade
nel corso della stimolazioni tetaniche che danno
origine al potenziamento a lungo termine.
La depolarizzazione toglie il blocco degli Mg2+ ai
canali NMDA. Ciò consente il flusso di Na+, K+ e
Ca2+ attraverso questi canali.
L’aumento di Ca2+ che ne consegue a livello delle
spine dendritiche attiva le chinasi calcio-dipendenti
(calciocalmodulina e la chinasi C) che determinano
la comparsa di LTP.
Quando è stato indotto un LTP, la cellula
postsinaptica libera un segnale retrogrado, che
probabilmente agisce sulle chinasi presenti nella
terminazione presinaptica, e da origine al
persistente aumento della liberazione di
neurotrasmettitore che è alla base del prolungarsi
nel tempo dell’LTP.

45
Potenziamento
sinaptico
Nuovi siti
sinaptici
Crescita di nuove
connessioni
Meccanismi di plasticità sinaptica
Ingresso
presinaptico
Risposta
postsinaptica
Ingresso
presinaptico
Risposta
postsinaptica
Ingresso
presinaptico
Risposta
postsinaptica
Le modificazioni dell’efficacia sinaptica, per
consolidarsi e mantenersi stabili nel tempo
(modifiche a lungo termine) necessitano della
trascrizione genica e della sintesi di nuove
proteine




![sinapsi 1 [modalità compatibilità] - sunhope.it · Biofisica e Fisiologia Corso di Laurea Magistrale in “Medicina e Chirurgia” Sinapsi Il neurone Caratteristica peculiare delle](https://static.fdocumenti.com/doc/165x107/5c6a621509d3f27a7e8c9aed/sinapsi-1-modalita-compatibilita-biofisica-e-fisiologia-corso-di-laurea.jpg)