Ruolo del fattore di crescita delle cellule endoteliali...
Transcript of Ruolo del fattore di crescita delle cellule endoteliali...

DIPARTIMENTO MEDICINA SPERIMENTALE E PATOLOGIA
Dottorato di Ricerca in Patologia Umana-XVIII ciclo-
TESI DI DOTTORATO
Ruolo del fattore di crescita delle cellule endoteliali (VEGF)
sulla maturazione delle cellule dendritiche
DOTTORANDA: Dott.ssa Germana Castelli
Dip. Ematologia, Oncologia e Medicina molecolare Istituto Superiore di Sanità
RELATORE: Dott.ssa Cristiana Chelucci
Dip. Ematologia, Oncologia e Medicina molecolare Istituto Superiore di Sanità
CORRELATORE: Prof. Matteo Antonio Russo
Dip. Medicina Sperimentale e Patologia Università “La Sapienza” Roma

INDICE
1. SCOPO DELLA TESI ……………………………….1
2. INTRODUZIONE …………………………………3
LA DIFESA IMMUNITARIA ………………………………….3
LE CELLULE DENDRITICHE ……………………………….4
ORIGINE E LOCALIZZAZIONE DIFFERENZIAMENTO IN VITRO MATURAZIONE RUOLO NELL’ATTIVAZIONE DELLA RISPOSTAIMMUNITARIA
• Captazione e processazione dell’antigene
• Presentazione dell’antigene e attivazione linfocitaria
IL FATTORE DI CRESCITA VASCOLARE ENDOTELIALE(VEGF) E I SUOI RECETTORI ………………………….11
VEGF: STRUTTURA E FUNZIONE I RECETTORI DEL VEGF (VEGFRs)FUNZIONE DEI VEGFRs
• Flt1
• KDR
• Ftl4TRASDUZIONE DEL SEGNALE DI VEGF/VEGFRsESPRESSIONE DEI VEGFRs NEL LINEAGE DENDRITICO

LA RISPOSTA IMMUNITARIA NEI TUMORI ……………..19LE CELLULE DENDRITICHE NELLA RISPOSTAIMMUNITARIA DEI TUMORILE CELLULE DENDRITICHE E IL VEGF
3. MATERIALI E METODI …………………………...22
FATTORI DI CRESCITA EMATOPOIETICI E MEZZI DICOLTURAPURIFICAZIONE DI MONOCITI
COLTURE DI MONOCITI
DIFFERENZIAMENTO DI CELLULE DENDRITICHE DAMONOCITI
COLTURE DI CELLULE DENDRITICHE CON VEGF E PlGF
ANALISI MORFOLOGICA
ANALISI CITOFLUORIMETRICA
SAGGIO ELISA (Enzyme-Linked Immunosorbent Assay)
ANALISI DELLA VITALITÁ
SAGGIO DI PROLIFERAZIONE
TEST DI VALUTAZIONE DELL'APOPTOSI
INCORPORAZIONE DEL DESTRANO
MLR (Mixed Leukocyte Reaction)
ANALISI DELL’RNA DEI VEGFRs
STIMOLAZIONE CELLULARE E WESTERN BLOTTING

4. RISULTATI …………………………………………32
CARATTERISTICHE DELLA POPOLAZIONE DENDRITICADERIVATA DA MONOCITI MATURIANALISI FUNZIONALE DELLE CELLULE DENDRITICHE ESPRESSIONE DEI VEGFRs NELLA POPOLAZIONEMONOCITARIA E DENDRITICAATTIVAZIONE DI ERK-pathway DA PARTE DI VEGF E PlGF
ANALISI DALLA PRODUZIONE DI VEGF E PlGF DA PARTEDI COLTURE MONOCITARIE E DENDRITICHE
ANALISI DI CULTURE DENDRITICHE TRATTATE CONVEGF E PlGF
• Condizioni di coltura
• Crescita e vitalità cellulare
• Fenotipo
• Funzionalità
• Produzione di IL-12
5. DISCUSSIONE ……………………………………….63
6. BIBLIOGRAFIA ………………………………………..69
7. ACRONIMI ………..………………………………80

1
1. SCOPO DELLA TESI
Il fattore di crescita delle cellule endoteliali (VEGF, Vascular Endothelial
Growth Factor) è una citochina multifunzionale che stimola l’angiogenesi, la
rigenerazione vascolare e i processi infiammatori. Il ruolo fisiologico del
VEGF e dei suoi recettori nello sviluppo dei tessuti vascolari è stato
ampiamente dimostrato, mentre la sua importanza nel sistema ematopoietico
umano è suggerita dal fatto che diverse popolazioni cellulari producono
VEGF e/o esprimono i suoi recettori.
Il VEGF sembra svolgere un ruolo significativo anche nei processi tumorali in
quanto è prodotto da gran parte delle cellule neoplastiche ed è responsabile
della proliferazione delle cellule endoteliali, essendo determinante per la
neovascolarizzazione dei tumori solidi.
Si ipotizza, inoltre, che aumentati livelli di VEGF nel microambiente
tumorale possano svolgere un importante ruolo nella risposta immunitaria
antitumorale e, più generalmente, nei processi infiammatori agendo
direttamente sulle cellule dendritiche (DC) o sui loro precursori.
Le DC sono cellule specializzate nella cattura degli antigeni e altamente
efficienti nell’induzione della risposta immunitaria.
Diversi studi, sia in vivo che in vitro, hanno dimostrato che il VEGF inibisce
la differenziazione delle DC agendo direttamente sui loro precursori. Non è
stato invece ancora ben chiarito se il VEGF eserciti un effetto direttamente
sulla popolazione di DC.

2
Considerato il ruolo determinante sia delle DC che del VEGF nella risposta
immunitaria antitumorale, ci siamo proposti di approfondire l’effetto del
VEGF sulla differenziazione e sulla funzionalità delle DC.
Il sistema di differenziamento dendritico da monociti (Mo) maturi, utilizzato
in questo lavoro di tesi, consente di ottenere una popolazione omogenea di DC
di cui è possibile studiarne la maturazione e la funzionalità.
Inizialmente è stata analizzata l’espressione dei recettori del VEGF, Flt1 e
KDR, sulle DC ai diversi stadi maturativi. Poiché, a differenza del KDR, il
Flt1 è espresso dalla totalità della popolazione immatura, abbiamo ipotizzato
che eventuali effetti del VEGF fossero mediati da tale recettore.
Al fine di verificare questa ipotesi sono state coltivate le DC in presenza di
VEGF o PlGF (Placental Growth Factor), un omologo del VEGF in grado di
legare esclusivamente Flt1, e sono state effettuate analisi morfologiche,
citofluorimetriche e funzionali.

3
2. INTRODUZIONE
LA DIFESA IMMUNITARIA
L’evoluzione ha fornito all’uomo due distinti e sofisticati meccanismi di
difesa immunitaria nei confronti degli agenti patogeni ambientali:
1) il sistema dell’immunità innata (detto anche immunità naturale),
deputato a reagire rapidamente e in modo piuttosto semplice;
2) il sistema dell’immunità acquisita (detto anche immunità specifica),
caratterizzato da un tipo di risposta difensiva altamente specifica.
I meccanismi che sono alla base dell’immunità acquisita implicano diverse
fasi di riconoscimento e reazioni nelle quali vengono impegnati molti tipi di
cellule. Inizialmente intervengono le cellule che presentano l’antigene
(Antigen Presenting Cell, APC), ossia cellule in grado d’internalizzare
l’antigene, processarlo e riesprimerlo modificato sulla membrana cellulare in
modo da renderlo riconoscibile alle cellule immunocompetenti, deputate ad
innescare la risposta immunitaria specifica. Tra le cellule in grado di
presentare l’antigene, le DC esplicano una funzione cardine nel fornire
informazioni sugli agenti patogeni invasivi ad altri partners cellulari (cellule
effettrici) del sistema immunitario (Abbas A.K. et al. 1998).

4
LE CELLULE DENDRITICHE
ORIGINE E LOCALIZZAZIONE
Le DC sono cellule specializzate nella cattura degli antigeni e altamente
efficienti nella stimolazione dei linfociti T: sono ritenute, infatti, le cellule
APC maggiormente coinvolte nell’induzione della risposta immunitaria.
Nonostante rappresentino una popolazione estremamente eterogenea, si
possono distinguere due gruppi con origine, caratteristiche e funzioni
differenti (Hart D.N.J. 1997; Banchereau J. et al. 2000):
a) DC generate da cellule staminali ematopoietiche che possono
appartenere alla linea mieloide o linfoide;
b) DC che non derivano da precursori ematopoietici midollari, ma da
elementi stromali.
I precursori delle DC presenti nel midollo osseo passano nel sangue e si
distribuiscono nei vari organi, localizzandosi negli epiteli e negli spazi
interstiziali. In queste sedi acquisiscono le caratteristiche tipiche delle DC che
le rendono particolarmente adatte a svolgere il ruolo di sorveglianza
immunitaria. Dopo l’esposizione a stimoli antigenici o infiammatori, le DC
interstiziali migrano nei linfonodi regionali o nella milza, rispettivamente
attraverso la via linfatica o ematica; in questa fase le DC acquisiscono la loro
peculiare morfologia (vedi oltre) e modificano il loro fenotipo principalmente
esponendo sulla membrana le molecole costimolatorie necessarie per
l’attivazione dei linfociti T. Infine, una volta giunte negli organi linfatici,
possono localizzarsi nell’area parafollicolare e attivare i linfociti T “naive”, o
migrare nel centro germinativo dove presentano l’antigene a linfociti T della
memoria, avviando risposte immunitarie di tipo secondario.

5
Al gruppo mieloide, appartengono le DC presenti nei tessuti interstiziali di
molti organi, nella cute o nelle mucose epiteliali dove sono conosciute come
cellule di Langerhans.
Alla linea linfoide appartengono le DC localizzate nel timo, nelle tonsille,
negli organi linfoidi periferici e nel sangue.
Le DC del secondo gruppo, che derivano da elementi stromali, sono
denominate DC follicolari e appaiono nei centri germinativi dei follicoli
linfatici linfonodali, nonché nei tessuti associati alle mucose. Il loro ruolo è di
catturare l’antigene complessato ad immunoglobuline o a proteine
d’attivazione del complemento e, dopo averlo processato, esporlo sulla
superficie offrendolo al riconoscimento da parte dei linfociti B della memoria
che, a loro volta, stimolano ulteriormente le risposte T linfocitarie
(Banchereau J. and Steinman R.M. 1998).
La migrazione delle DC dai siti periferici agli organi linfatici secondari è un
fenomeno strettamente correlato al loro differenziamento e maturazione
funzionale non ancora completamente chiarito. Alcune molecole, dette
chemoattrattanti, quali SDF-1, MIP1α e MIP1β nonché le citochine TNFα e
IL-1 sembra svolgano un ruolo fondamentale in tale processo (Caux C. et al.
2000).

6
DIFFERENZIAMENTO IN VITRO
Le DC sono localizzate in gran parte dei tessuti, tranne il cervello, ma la loro
bassa percentuale (0,1 % in tonsille, timo, milza; < 1% nel sangue; 1-3%
nell’epidermide) ne rende difficile l’isolamento.
Frazioni cellulari numericamente abbondanti e altamente arricchite in DC si
ottengono da espianti di pelle, da progenitori ematopoietici CD34+ isolati da
midollo osseo, da sangue di cordone ombelicale o sangue periferico (PB) o da
Mo maturi purificati da PB (Hart D.N.J. 1997; Chapius F. et al. 1997).
E’ importante sottolineare che per la differenziazione/maturazione dendritica
possono essere utilizzate diverse condizioni di coltura (Montesoro E. et al.
2005): in particolare sono descritte varie combinazioni delle tre citochine più
comunemente usate GM-CSF, IL-4 e TNFα che possono essere aggiunte in
quantità e tempi diversi (Sallusto F. and Lanzavecchia A. 1994).
Le DC utilizzate in questo lavoro di tesi sono state ottenute da Mo maturi,
isolati da PB, coltivati in presenza di GM-CSF e IL-4.
MATURAZIONE
Sebbene rappresentino una popolazione cellulare estremamente eterogenea, le
DC presentano importanti caratteristiche comuni: il profilo citoplasmatico, la
motilità e la presenza di specifici antigeni di membrana, che permettono di
distinguerle dai rimanenti leucociti e di suddividerle in DC immature e
mature.

7
Le DC immature, presenti nella cute e nei tessuti interstiziali di molti organi,
sono cellule piccole con dendriti molto sottili e lunghi fino a 10 µm
(Banchereau J. & Steinman R.M. 1998). Caratteristica comune di tutte le DC
immature è l’espressione sulla membrana cellulare di alti livelli dei recettori
per immunoglobuline e di recettori per chemochine CCR1, CCR5, CCR6 che
sono persi in seguito alla maturazione. La maturazione delle DC è un evento
cruciale per l’inizio della risposta immunitaria e può essere indotta da batteri
o da componenti della loro parete come il lipopolisaccaride (LPS), da
molecole infiammatorie come CD40, TNFα, IL-1β, IFNα, IFNβ, o da
prostaglandine. Una volta attivate, le DC migrano nei linfonodi dove si
verifica un incremento dell’espressione di MHC di classe I e II, del recettore
CD83, delle molecole di adesione (CD45 e CD58) e costimolatorie quali
CD40, CD80, CD86 (Adams S. et al. 2005; tabella 1).
Teorie contrastanti riguardano l’espressione del marcatore CD1a: in alcuni
studi è indicato come recettore caratteristico delle DC immature (Steinman
R.M. et al. 1997; Young J.W. et al. 1999) altri autori affermano, al contrario,
che tale molecola compare solo in seguito alla maturazione (Hart D.N.J.
1997; Weissman D. and Fauci A. 1997).
Oltre ad un cambiamento fenotipico, le DC mature modificano il loro profilo
morfologico, in seguito allo sviluppo di lunghi processi citoplasmatici
(dendriti). Esse acquisiscono infine la capacità di secernere diverse citochine
tra cui IL-12, che favorisce la presentazione antigenica, la loro migrazione nei
linfonodi e quindi l’attivazione linfocitaria (Adams S. et al. 2005).

8
ANTIGENI DC IMMATURE DC MATURE
CD1a −+
+ (1) (2)
− (3)
CD4 + +/−
CD11a (LFA-1) ++ ++
CD13 + +CD14 − −
CD54 (ICAM-1) + +++
CD50 (ICAM-2) + +
CD102 (ICAM-3) +++ +++
CD58 (LFA-3) + ++
CD33 + +CD40 +/− ++
CD80 (B7-1) − ++CD83 − +
CD86 (B7-2) − ++CD45RO − ++
CCR1 + −CCR5 + −CCR6 + −CCR7 − +
CXCR4 − +
HLA-ABC (MHC-I) ++ +++
HLA-DR (MHC-II) ++ +++
Tabella 1
Espressione dei principali antigeni di membrana delle DC immature e mature.
(1) Hart D. N.J. 1997(2) Weissman D. and Fauci A. 1997(3) Steinman R.M. et al.1997

9
RUOLO NELL’ATTIVAZIONE DELLA RISPOSTA IMMUNITARIA
• Captazione e processazione dell’antigene
Nella maggior parte dei tessuti sono presenti DC in forma immatura incapaci
di stimolare linfociti T ma altamente specializzate nel catturare l’antigene.
Le DC possono legare diverse proteine, dotate di scarsa o nulla affinità per
molecole di superficie, e internalizzarle mediante un processo di fagocitosi o
pinocitosi. Gli antigeni internalizzati vengono compartimentati in vescicole
intracellulari (endosomi e lisosomi) e processati. Le proteine processate danno
origine a peptidi che si legano a molecole MHC di classe II; i complessi
risultanti, MHC-II/peptide sono esposti sulla membrana cellulare e
riconosciuti dai linfociti T CD4+.
I peptidi derivati da antigeni proteici endogeni, come le proteine virali, sono
invece generati proteoliticamente nel citoplasma, quindi trasportati nel
reticolo endoplasmatico dove si legano alle molecole MHC di classe I. I
complessi che si formano, presentati sulla membrana cellulare, sono
riconosciuti dai linfociti T CD8+ (Abbas A.K. et al. 1997; Banchereau J. et
al. 2000).
• Presentazione dell’antigene e attivazione linfocitaria
In seguito alla captazione ed esposizione dell’antigene, le DC migrano nei
linfonodi dove completano la maturazione e attraggono i linfociti T o B
attraverso il rilascio di citochine specifiche.
I linfociti T helper CD4+ attivati esprimono nuove molecole di membrana
(CD40L, Fas e il recettore per IL-2), producono citochine che favoriscono la
loro proliferazione, inducono la produzione di anticorpi da parte dei linfociti

10
B e attivano cellule dell’immunità naturale. La presentazione dell’antigene ai
linfociti CD8+ ne induce la maturazione e l’attivazione delle capacità litiche.
Gli eventi di attivazione linfocitaria hanno inizio quando i complessi MHC-
peptide presenti sulle APC si legano al TCR (T cell receptor). Oltre al
complesso TCR, numerose molecole accessorie costimolatorie (quali CD4,
CD8, CD28 e le integrine LFA-1 e VLA-4) svolgono un ruolo importante
nell’attivazione linfocitaria interagendo con i ligandi espressi sulle APC
(quali CD80, CD86, ICAM, VCAM-1) e fornendo forze che stabilizzano
l’adesione e permettono la trasduzione dei segnali.
Ai segnali stimolatori delle molecole accessorie si uniscono quelli di fattori
solubili secreti dalle APC in seguito all’interazione con i linfociti. Il
principale fattore che induce rilascio di citochine è il CD40 ligando (CD40L)
che è espresso dai linfociti T attivati. Il legame del CD40L con il suo recettore
(CD40) espresso sulle DC, induce queste ultime a secernere IL-12 e favorisce
la produzione di IFNγ da parte dei linfociti T. L’IFNγ, infine, favorisce le
risposte immuni verso antigeni virali o patogeni endocellulari (Banchereau J.
and Steinman R.M.1998; Adams S. et al. 2005).

11
IL FATTORE DI CRESCITA VASCOLARE ENDOTELIALE (VEGF)
E I SUOI RECETTORI
VEGF: STRUTTURA E FUNZIONE
La famiglia del VEGF comprende numerosi fattori: VEGF-A, VEGF-B,
VEGF-C, VEGF-D, VEGF-E, PlGF che si distinguono in base alla diversa
capacità di legare tre recettori Flt1, KDR/Flk1 e Flt4. L’isoforma più
abbondante del VEGF è il VEGF-A una glicoproteina omodimerica composta
da 121 amminoacidi; VEGF-A è presente anche nelle forme da 165, 189 e
206 amminoacidi, ottenute in seguito al taglio alternativo degli 8 esoni e dei 6
introni del trascritto (figura 1; Ferrara N. et al. 1997; Neufeld G. et al. 1999;
Ferrara N. et al. 2003). Essendo il VEGF-A l’isoforma più abbondante, ogni
volta che parlerò di studi condotti sul VEGF, mi riferirò appunto al VEGF-A.
Tutti i fattori appartenenti alla famiglia del VEGF sono espressi
endogenamente nei mammiferi, ad eccezione del VEGF-E che è un fattore
prodotto dal virus Orf (un poxvirus; Shibuja M. et al. 2003).
Il VEGF, inizialmente identificato per la sua capacità di aumentare la
permeabilità della parete vascolare (Dvorak H.F. et al 1995), è in grado di
stimolare le cellule endoteliali (Gerber H.P. et al.1998) e di indurre la
migrazione dei Mo (Clauss M. et al. 1990). Esso svolge, inoltre, un ruolo
essenziale nell’angiogenesi, nell’ematopoiesi (Broxmayer H.E. et al. 1995;
Gerber H.P. et al. 2002) e nell’induzione della neovascolarizzazione correlata
con la crescita tumorale (Barleon B. et al. 1996; Ferrara N. et al. 2004).

12
Figura 1
Struttura genica della famiglia del VEGF (Shibuya M. et al. 2001).
Nell’embrione, il VEGF è un fattore essenziale per la formazione della prima
rete vascolare (vasculogenesi). Nell’adulto, promuove la formazione dei vasi
sanguigni a partire da strutture preesistenti, sia in condizioni normali che in
seguito a danni (angiogenesi e neoangiogenesi; Shibuya M. et al. 2001).
Negli ultimi anni, numerosi studi hanno evidenziato il ruolo fondamentale del
VEGF nell’espansione e nel mantenimento della cellula staminale e dei
progenitori ematopoietici, sia nell’embrione che nell’adulto.

13
Ha destato molto interesse la scoperta che il VEGF svolge un ruolo anche
nell’espansione tumorale; esso è infatti prodotto da quasi tutte le cellule
tumorali (Gerber H.P. et al. 2003). Il VEGF favorisce il reclutamento dei
precursori ematopoietici midollari nelle aree tumorali (Larrivee B. et al. 2003)
e agisce sulle cellule endoteliali promuovendone la vasodilatazione e
l’angiogenesi tumorale (Barleon B. et al. 1996; Ferrara N. et al. 2003). Nel
caso dei tumori solidi, il VEGF causa la fenestrazione dei vasi sanguigni, con
successivo accumulo di fibrina extravasale, che fornisce, a sua volta, il
supporto per la crescita della massa tumorale (Dvorak H. et al.1992). Infine
sembra svolgere un ruolo importante nei processi infiammatori, delle aree
tumorali, agendo direttamente sulle DC e sui loro precursori (vedi più avanti).
I RECETTORI DELVEGF (VEGFRs)
I recettori del VEGF (VEGF Receptors, VEGFRs) sono tre:
• Il recettore del fattore di crescita vascolare endoteliale 1 (VEGFR-1),
oppure Fms-like-tyrosine kinase 1 (Flt1);
• Il recettore del fattore di crescita vascolare endoteliale 2 (VEGFR-2),
oppure Kinase insert Domain-containing Receptor (KDR);
• Il recettore del fattore di crescita vascolare endoteliale 3 (VEGFR-3),
oppure Fms-like-tyrosine kinase 4 (Flt4).
I recettori del VEGF appartengono alla famiglia delle tirosin chinasi. Tali
recettori sono caratterizzati dalla presenza di 7 domini immunoglobulinici-
simili, da una regione che lega il ligando nella parte extracellulare, e da un
dominio intracitoplasmatico tirosin chinasico (figura 2; Neufeld G. et al.
1999; Ferrara N. et al. 2001). In seguito al legame con le varie isoforme del

14
VEGF, i recettori omodimerizzano e si transfosforilano nel loro dominio
intracellulare.
Le diverse isoforme del VEGF interagiscono in modo diverso con i recettori:
il VEGF-A può legare sia il KDR che il Flt1; il VEGF-B e il PlGF
interagiscono esclusivamente con il Flt1; il VEGF-E lega il KDR; mentre il
VEGF-C e il VEGF-D legano sia il KDR che il Flt4.
Inizialmente era stata riportata l’espressione dei recettori Flt1 e KDR solo
sulle cellule endoteliali (Brown L.F. et al. 1993). Recenti studi descrivono la
presenza di questi recettori su precursori ematopoietici, Mo, DC,
megacariociti, osteoblasti, e differenti cellule tumorali (Ferrrara N. et al.
2003; Casella I. et al. 2003; bTakahashi A. et al.2004).
Figura 2
Meccanismi d’interazione tra le varie isoforme del VEGF e i relativi recettori;
sVEGFR-1 è la forma solubile del Flt1 (Karkkainen M.J. et al. 2000).

15
FUNZIONE DEI VEGFRs
• Flt1
Il Flt1 è stato il primo recettore del VEGF ad essere scoperto; esso presenta il
44% di omologia amminoacidica con il KDR, ma lega il VEGF con
un’affinità 10 volte superiore. Il gene del Flt1 codifica due polipeptidi: uno di
membrana, codificato dal gene di lunghezza completa (Flt1), e uno solubile
(sFlt1), contenente solo uno dei sette domini immunoglobulinici-simili, senza
il dominio tirosin chinasico (He Y. et al. 1999).
Al sFlt1 è stata attribuita la funzione di regolatore negativo del VEGF in
quanto, legando tale molecola, ne inibisce l’attacco ai recettori di membrana e
di conseguenza l’azione (Kendal R.L. and Thomas K.A. 1993).
Il Flt1 di membrana è importante come mediatore dell’angiogenesi e
dell’infiammazione, ed è responsabile della mobilizzazione delle cellule
endoteliali adulte (Kanno S. et al. 2000; Hattori K. et al. 2002; Ferrara N. et
al. 2003). Può mediare, inoltre, il reclutamento e la mobilizzazione delle
cellule staminali ematopoietiche ed è coinvolto nella proliferazione, nel
mantenimento, nel differenziamento e nell’attivazione del sistema
ematopoietico adulto.
E’ stato dimostrato che, attraverso la stimolazione del Flt1, il VEGF potenzia
la megacariopoiesi (Casella I. et al. 2003).
Infine alcuni autori hanno mostrato che il signaling mediato dal Flt1 è
sufficiente a bloccare l’attivazione del fattore trascrizionale NF-κB in DC
derivate da cellule staminali embrionali murine e pertanto di bloccarne la
maturazione (vedi oltre; Dikov M.M. et al. 2005).

16
• KDR
Il KDR è il maggior recettore che media gli effetti vasculogenici, angiogenici
e di permeabilità vascolare del VEGF nelle cellule endoteliali. Infatti
l’inattivazione del suo gene determina una letalità embrionale precoce a causa
del mancato differenziamento delle cellule endoteliali primitive e quindi della
mancata formazione dei vasi sanguigni.
Nell’embrione il KDR è importante per la localizzazione, lo sviluppo e la
sopravvivenza dei progenitori ematopoietici. Nell’adulto il KDR promuove la
auto-replicazione cellulare e la sopravvivenza delle cellule staminali e dei
progenitori ematopoietici (Ziegler B.L. et al. 1999; Ferrara N. 2004).
• Flt4
Il Flt4 svolge un ruolo cruciale nello sviluppo e nella crescita del sistema
linfatico. Inizialmente è espresso in tutte le cellule endoteliali embrionali dove
è essenziale per la formazione della rete primaria cardiovascolare. Nel corso
dello sviluppo la sua espressione nei grandi vasi diminuisce, mantenendosi
solo nell’endotelio linfatico dei tessuti adulti (aTakahashi M. et al. 2004).
TRASDUZIONE DEL SEGNALE DI VEGF/VEGFRs
La maggior parte degli studi sulla trasduzione del segnale dei VEGFRs è stata
condotta in cellule endoteliali.
In generale, la trasduzione del segnale mediata dai recettori tirosin chinasici
avviene attraverso i seguenti passaggi:
Il legame del ligando sul recettore
La dimerizzazione del recettore
L’attivazione della tirosin chinasi recettoriale

17
L’autofosforilazione del recettore
Il legame e l’attivazione delle molecole adattatrici ai siti di
autofosforilazione
L’attivazione di secondi messaggeri.
Gli effetti mediati dai VEGFRs variano a seconda delle molecole segnale
coinvolte nella cascata di trasduzione (Gille H. 2001).
La trasduzione del segnale del KDR stimola, nelle cellule endoteliali, la
sopravvivenza, la proliferazione e la migrazione mediante l’attivazione di
diverse vie del segnale quali AKT, Raf, MEK e ERK 1/2.
Per quanto riguarda il Flt1, il legame con il VEGF induce un aumento del
Ca2+ intracellulare, che a sua volta promuove la migrazione delle cellule
endoteliali, dei Mo e dei macrofagi. La migrazione delle cellule endoteliali è
indotta da Flt1 anche attraverso la via di p38 MAP chinasi, in seguito alla
riorganizzazione dell’actina. La stimolazione delle cellule endoteliali con il
PlGF (ma non con il VEGF) induce una risposta mitogenica e la produzione
dell’attivatore del fibrinogeno attraverso la via della MAP chinasi (Landgren
E. et al. 1998).
Recenti lavori hanno dimostrato che il VEGF induce fosforilazione di ERK
1/2 mediante attivazione di Flt1, in linee cellulari ottenute dal colon-retto
(Fan F. et al. 2005), in cellule di muscolo liscio (Kazi A.S. et al. 2004) e in
cellule di mieloma (Podar K. et al. 2001).
Infine, Selvaraj S.H e colleghi hanno osservato, nei Mo stimolati con PlGF,
una transiente attivazione di ERK 1/2 e di AKT, quest’ultima però solo a
tempi molto precoci (Selvaraj S.H. et al. 2003).

18
ESPRESSIONE DEI VEGFRs NEL LINEAGE DENDRITICO
L’espressione dei VEGFRs sulla popolazione dendritica è stata inizialmente
studiata su DC derivate da progenitori ematopoietici: Oyama T. e colleghi
hanno dimostrato che l’mRNA di Flt1 è espresso nella popolazione delle DC
e si riduce durante il processo maturativo. Parallelamente è stato dimostrato
che il legame del VEGF si riduce durante la maturazione delle DC (Oyama T.
et al. 1998). Successivamente altri autori hanno mostrato l’espressione
dell’mRNA del Flt1, ma non del KDR, in DC derivate da Mo maturi (Pujol F.
B. et al. 2001).
Per quanto riguarda l’espressione in membrana dei VEGFRs, in un recente
lavoro, si è dimostrato che entrambi i recettori sono espressi dalle DC
immature derivate da Mo, e che tale espressione è ridotta nella popolazione
matura (bTakahashi A. et al. 2004).

19
LA RISPOSTA IMMUNITARIA NEI TUMORI
LE CELLULE DENDRITICHE NELLA RISPOSTA IMMUNITARIA DEI
TUMORI
Le DC svolgono un ruolo centrale nell’immunità antitumorale captando gli
antigeni tumorali e stimolando linfociti T specifici; pertanto un importante
meccanismo attuato dai tumori per evadere il sistema immunitario è proprio
quello di inibire la funzionalità delle DC.
In diversi studi è descritto che le DC, prelevate dal PB o dai linfonodi di
pazienti con il cancro, non stimolano adeguatamente le risposte immunitarie.
Questa disfunzione è il risultato di un ridotto numero di DC competenti e di
un accumulo di DC immature dovuto ad un anormale differenziamento dei
loro precursori (Gabrilovich D. et al. 1996; aTroy A. et al. 1998; bTroy A. et
al. 1998; Almand B. et al. 2000; Della Bella S. et al. 2003). E’ stato infatti
dimostrato che le cellule tumorali possono alterare la maturazione e la
funzionalità delle DC inibendo la capacità dei progenitori ematopoietici
(Gabrilovich D. et al. 1996) o dei precursori monocitari (Kiertscher SM. et al.
2000) di differenziare in DC funzionalmente attive. Ciò nonostante DC
relativamente mature, isolate da PB e cresciute in presenza di sopranatante
ottenuto da colture di cellule tumorali, sono funzionalmente attive
(Gabrilovich D. et al. 1996).
E’ oramai noto che le cellule tumorali producono numerosi fattori
immunosoppressivi (VEGF, M-CSF, IL-6, GM-CSF, IL-10, gangliosidi;
Gabrilovich D. et al. 2004), e che la differenziazione anormale delle DC,
osservata nei pazienti con il cancro, è il risultato dell’effetto combinato di

20
questi diversi fattori. Il fattore maggiormente responsabile di quest’inibizione
è il VEGF (Kiertscher SM. et al. 2000; Ohm J.E. and Carbone D. 2001).
LE CELLULE DENDRITICHE E IL VEGF
Il coinvolgimento del VEGF nell’inibizione del differenziamento delle DC è
stato dimostrato in diversi lavori.
Inizialmente, studi in vitro eseguiti con progenitori ematopoietici, hanno
evidenziato che il blocco del differenziamento delle DC, indotto dal mezzo
condizionato di colture di cellule tumorali, può essere annullato da anticorpi
specifici anti-VEGF (Gabrilovich D. et al. 1996).
Successivi esperimenti sui topi hanno confermato che la continua infusione di
VEGF ricombinante determina una drammatica inibizione dello sviluppo di
DC (Gabrilovich D. et al. 1998) e che anticorpi anti-VEGF, infusi in topi con
tumore, aumentano il numero di DC mature circolanti (Gabrilovich D. et al.
1999; Ishida T. et al. 1998).
Negli ultimi anni diversi dati clinici hanno confermato la stretta correlazione
tra gli aumentati livelli di VEGF e il ridotto numero di DC in tessuti tumorali
e nel PB di pazienti con il cancro (Saito H. et al. 1998; Gabrilovich D. 1997;
Almad B. et al. 2000).
E’ oramai noto che il VEGF inibisce l’attivazione del fattore trascrizionale
NF-κB in progenitori ematopoietici.
L’NF-κB regola la trascrizione di molti geni coinvolti nella risposta
immunitaria, inclusi citochine e fattori di crescita; pertanto la sua inibizione
induce un blocco della maturazione e della funzionalità delle DC (Oyama T.
et al. 1998; Gabrilovich D. et al. 1998; Dikov M.M. et al. 2005).

21
Recentemente Takahashi A. e colleghi hanno mostrato che il VEGF, aggiunto
a colture di DC completamente differenziate, ma non ancora del tutto mature,
inibisce l’effetto d’attivazione indotto dall’LPS (bTakahashi A. et al. 2004).
In conclusione, è dimostrato che il VEGF è in grado di inibire sia la
differenziazione delle DC, agendo direttamente sui loro precursori, sia la loro
successiva maturazione.
Non è invece ancora chiaro l’effetto del VEGF direttamente sulla popolazione
di DC immature.

22
3. MATERIALI E METODI
FATTORI DI CRESCITA EMATOPOIETICI E MEZZI DI COLTURA
I fattori di crescita ematopoietici utilizzati per le colture cellulari sono: GM-
CSF, IL-4 (1x106 U/mg), M-CSF (Peprotec, Rocky Hill, NJ). L’FCS e
l’RPMI sono stati forniti da Hyclone (Logan, UT) e l’IMDM da GIBCO
(Grand Island, NY, USA).
PURIFICAZIONE DEI MONOCITI
I Mo sono stati purificati da PB, di donatori sani, utilizzando microbiglie
magnetiche coniugate con l’anticorpo monoclonale (MoAb) anti-CD14
(“CD14 MicroBeads” Milteny Biotec -Bergisch Glabach, Germany).
Il campione di sangue è stato diluito con soluzione fisiologica e stratificato su
un gradiente di Ficoll o Lymphoprep e quindi centrifugato a 1600 rpm per 30
minuti a temperatura ambiente, al fine di separare le cellule rosse da quelle
mononucleate. Quest’ultime sono state recuperate, lavate due volte in
soluzione fisiologica contenente 2mM EDTA e centrifugate a 1400 rpm per
10 minuti a 20°C e quindi a 800 rpm. Le cellule mononucleate sono state
incubate per 30 minuti a 4-6°C con microbiglie magnetiche coniugate con un
MoAb murino anti-CD14 umano, in presenza di immunoglobuline G (IgG)
umane. Le cellule sono state risospese e quindi separate per selezione positiva
(CD14+) mediante passaggio su colonna. La frazione risultante è stata
ulteriormente purificata con un secondo passaggio e, dopo rimozione del
magnete, eluita e monitorata per il suo grado di purezza mediante marcatura

23
con un MoAb anti-CD14 coniugato con ficoeritrina (PE). La popolazione
purificata risulta costituita dal 90% di cellule CD14+.
COLTURE DI MONOCITI
Mo maturi sono stati piastrati ad una concentrazione di 2-3 x 105 cellule/mL
in IMDM in presenza di M-CSF (125 U/mL), addizionando penicillina (100
U/mL), streptomicina (100 µg/mL), glutammina 2mM, sodio piruvato 1mM,
1% di amminoacidi non essenziali e 20% di FCS.
DIFFERENZIAMENTO DI CELLULE DENDRITICHE DA MONOCITI
Il differenziamento in DC è stato ottenuto coltivando i Mo in RPMI in
presenza di GM-CSF (50ng/mL), IL-4 (50 ng/mL), addizionando penicillina
(100 U/mL), streptomicina (100 µg/mL), glutammina 2mM, sodio piruvato
1mM, 1% di amminoacidi nonessenziali e 10% di FCS. Dopo 6 giorni di
coltura le DC sono state attivate aggiungendo nel mezzo di coltura 1ng/mL di
LPS (Sigma-Aldrich, Steinheim, Germany).
COLTURE DI CELLULE DENDRITICHE CON VEGF E PlGF
Alle colture cellulari di DC in differenziamento (dopo almeno 36 ore) sono
stati aggiunti i fattori di crescita VEGF (R&D System, Minneapolis, MN) o
PLGF (Sigma) ad una concentrazione di 50-100 ng/mL, e riaggiunti a giorni
alterni fino alla fine della coltura.

24
ANALISI MORFOLOGICA
Aliquote di circa 1x104 cellule sono state prelevate dalle colture a diversi
giorni di differenziamento, centrifugate su vetrini, colorate con May-
Grünwald Giemsa (Sigma, St. Louis, Mo) e identificate attraverso l’analisi
morfologica al microscopio.
ANALISI CITOFLUORIMETRICA
Lo studio fenotipico di alcuni antigeni di membrana è stato effettuato
mediante marcatura con MoAb specifici, direttamente coniugati con PE o con
isiotiocianato di fluoresceina (FITC).
Per la caratterizzazione fenotipica delle DC sono stati usati i seguenti MoAb
contro gli antigeni: CD1a, CD14, CD40, CD80, CD83, CD86, HLA-DR,
HLA-ABC (Pharmingen, San Diego, CA) e Flt1, KDR (R&D System).
Appropriate IgG coniugate sono state usate come controllo. Per
l’immunofenotipizzazione un’aliquota di circa 3x104 cellule è stata lavata due
volte in PBS (Hyclone, Logan, UT) e incubata per 30 minuti a 4°C con una
quantità saturante di MoAb. Dopo tre lavaggi con PBS contenente 2 mg/mL
di BSA, le cellule sono state risospese in PBS e quindi analizzate mediante
citofluorimetro FACScan (programma Lysis II, Becton Dickinson) al fine di
determinare la percentuale di cellule positive nonché l’intensità di
fluorescenza.
La popolazione cellulare identificata con i parametri fisici “scatter” diretto
(FSC) e “scatter” a 90° (SSC) è stata poi mostrata sotto forma di istogrammi o
come plot. In entrambe le immagini viene espresso in ascissa il numero di
eventi cellulari (ogni evento corrisponde ad una singola cellula), in ordinata

25
l’intensità media di fluorescenza (MFI). L’MFI rappresenta l’aumento medio
di fluorescenza del campione colorato con l’anticorpo d’interesse, rispetto al
proprio controllo isotipico.
Tutte le analisi al citofluorimetro sono state eseguite analizzando un numero
adeguato di eventi (non meno di 5000 per ogni campione).
Esperimenti di legame e di competizione sono stati eseguiti con VEGF
biotinilato (R&D System) e PlGF freddo. Per verificare il legame del VEGF,
le DC sono state incubate con differenti concentrazioni di VEGF biotinilato
(da 20 a 500 ng/mL) per 60 minuti a 4°C, quindi incubate per 30 minuti a 4°C
con avidina-FITC e analizzate al citofluorimetro. Come controllo negativo, le
cellule sono state marcate con un MoAb biotinilato.
Per i saggi di competizione, le cellule sono state pre-incubate con crescenti
concentrazioni di PlGF (10-20 µg/mL) per 30 minuti, lavate abbondantemente
e marcate, come precedentemente descritto, con VEGF biotinilato.
SAGGIO ELISA (Enzyme-Linked ImmunoSorbent Assay)
La valutazione quantitativa delle molecole VEGF, PlGF, IL-12 e sFlt, presenti
nei sopranatanti delle colture cellulari, è stata effettuata mediante saggi
immunoenzimatici ELISA (R&D System). In seguito alla reazione
immunoenzimatica, la concentrazione delle molecole è stata determinata
confrontando la densità ottica dei campioni in esame con una curva standard;
i campioni con valori di densità ottica inferiore al background sono
considerati negativi al test. I valori di densità ottica sono stati espressi in
valori di pg/mL.

26
ANALISI DELLA VITALITA’
La vitalità cellulare è vista attraverso l’esclusione del colorante Trypan Blue
(5 µg/mL in PBS; SIGMA). Questo colorante non è in grado di penetrare la
membrana plasmatica delle cellule vive, ma solo di quelle non vitali, nelle
quali l’integrità della membrana risulta compromessa. La valutazione e la
conta delle cellule vive o morte avviene al microscopio ottico.
SAGGIO DI PROLIFERAZIONE
Le DC sono state piastrate (5 x 104 cellule/50µL) in una piastra da 96 pozzetti
a fondo tondo in mezzo dendritico in presenza o meno di VEGF o PlGF ad
una concentrazione finale di 5-100 ng/mL.
La proliferazione cellulare è stata misurata aggiungendo, al 3° giorno di
coltura, 0.5µCi di timidina triziata (ICN Biomedicals, Irvine, CA) ad ogni
pozzetto.
Dopo 18 ore d’incubazione i campioni sono stati trasferiti su filtro (mediante
HARVESTER; Tomtec, Hamden, CT) e la quantità di radioattivo incorporato
dalle cellule, indicato in cpm (conte per minuto), è stata misurata al Microbeta
counter (Wallac, Turku, Finland). Il test è stato eseguito in quadruplicato e i
risultati sono stati espressi come media dei valori di cpm ottenuti ± deviazione
standard (DS).

27
TEST DI VALUTAZIONE DELL’APOPTOTOSI
La valutazione quantitativa delle cellule apoptotiche è stata determinata
utilizzando il kit “Apoptosis Detection Kits (MedSystems Diagnostics
GmbH, Vienna, Austria)
Il saggio consiste nel marcare le cellule con annessina-V coniugata FITC e
propidio ioduro coniugato PE, e analizzarle al citofluorimetro.
L’annessina-V è una proteina anticoagulante che lega preferenzialmente
fosfolipidi carichi negativamente. Nelle fasi precoci dell’apoptosi la
simmetria fosfolipidica viene alterata con conseguente esposizione, sul lato
citoplasmatico esterno, di fosfatidilserina che viene riconosciuta
dall’annessina.
Il propidio ioduro serve invece a discriminare le cellule in fase tardiva di
apoptosi o morte nelle quali, essendo la membrana plasmatica non più integra,
il propidio penetra e lega il DNA.
Le cellule sono state raccolte, lavate in PBS e quindi risospese, ad una
concentrazione di 1x105/100µL in una soluzione contenente 1% di annessina,
e 10% di Binding Buffer 10X. Dopo un’incubazione di 15 minuti al buio a 18-
24°C, le cellule sono state lavate e analizzate al citofluorimetro.
INCORPORAZIONE DEL DESTRANO
Per verificare la capacità delle DC immature di captare gli antigeni, sono stati
eseguiti saggi d’incorporazione della molecola del destrano (coniugato FITC;
Sigma-Aldrich). Un’aliquota di circa 5x104 cellule è stata e incubata per 30
minuti con 1mg/mL di destrano-FITC a 37°C o 4°C (controllo).

28
Dopo due lavaggi con PBS/0.1% BSA, le cellule sono state risospese in PBS,
quindi analizzate mediante citofluorimetro al fine di determinare la
percentuale di cellule positive nonché l’intensità di fluorescenza. Il livello
espresso di antigene captato è il risultato della differenza tra la fluorescenza
del campione incubato a 37°C e quello incubato a 4°C.
MLR (Mixed Leukocyte Reaction)
L’abilità delle DC di attivare i linfociti T è stata saggiata mediante il test
MLR, in cui linfociti T (cellule “responder”) sono coltivati con DC (cellule
“stimulator”). La proliferazione dei linfociti attivati è stata misurata in vitro
determinando la quantità di timidina triziata incorporata nel DNA
neosintetizzato delle cellule stimolate. L’incorporazione di timidina fornisce
una misura quantitativa del grado di sintesi del DNA, che è di solito
proporzionale all’attività proliferativa delle cellule.
Se le cellule “responder” e “stimulator” appartengono a diversi individui e
quindi presentano differenze negli alleli MHC, una considerevole frazione di
linfociti T andrà incontro a proliferazione in 4-7 giorni: tale saggio viene
chiamato MLR allogeneico.
I linfociti T sono stati ottenuti da un campione di sangue diluito con soluzione
fisiologica e stratificato su un gradiente di Ficoll o Lymphoprep quindi
centrifugato a 1600 rpm per 30 minuti a temperatura ambiente, al fine di
separare le cellule rosse da quelle mononucleate. Quest’ultime sono state
recuperate, lavate due volte in soluzione fisiologica contenente 2mM EDTA e
centrifugate per 10 minuti a 20°C a 1400 rpm e una volta a 800 rpm. Le
cellule mononucleate sono state piastrate e, in seguito all’adesione su piastra

29
dei Mo, i linfociti in sospensione sono stati prelevati. La popolazione
linfocitaria è stata ulteriormente purificata mediante gradiente di Percoll dalle
frazioni a 45-50% di densità.
I linfociti T (1x105 /50 µL) sono stati dispensati in una piastra da 96 pozzetti a
fondo tondo in IMDM 10% FCS. Sono state poi aggiunte DC, cresciute o non
con VEGF o PlGF e attivate con LPS, in modo tale che i rapporti tra le cellule
“stimulator” e i linfociti T “responder” fossero rispettivamente: 1:100, 1:200,
1:400 e 1:2000. Dopo 5 giorni d’incubazione a 37° C, in un’atmosfera
umidificata in presenza di 5% di CO2, è stato aggiunto ad ogni pozzetto 1µCi
di timidina. Dopo 16 ore i campioni sono stati trasferiti su filtro (mediante
HARVESTER) e la quantità di radioattivo incorporato dalle cellule, indicato
in cpm, è stata misurata al Microbeta counter.
I valori di background sono stati ottenuti dalle cpm di linfociti T e DC
incubati separatamente. Tutti i saggi sono stati eseguiti in quadruplicato e i
risultati espressi come media in cpm ± DS.
ANALISI DELL’RNA DEI VEGFRs
Cinque-10x104 DC o Mo sono stati lisati con una soluzione di guanidina e β-
mercaptoetanolo e stratificati su un gradiente di CsCl in presenza di 12 µg/mL
di RNA ribosomiale di Escherichia Coli come molecola conduttrice (che aiuta
l’RNA a precipitare). Dopo 19 ore di ultracentrifugazione a 14000 RPM, le
molecole di RNA recuperate nel pellett sono state precipitate e
successivamente trascritte in cDNA mediante l’enzima retrovirale trascrittasi
inversa (Boehringer, Mannheim, Germany). Il cDNA è stato quindi
amplificato utilizzando la tecnica della PCR con il Gene Amp PCR System

30
9600 thermal cycler (Perkin-Elmer). Il cDNA amplificato, trasferito su una
membrana di nylon, è stato successivamente evidenziato con una sonda
specifica marcata radioattivamente. Per l’amplificazione del gene della β2-
microglobulina si è utilizzato un programma di 26 cicli a 94°C per 30
secondi, 54°C per 30 secondi, 72°C per 30 secondi. Per l’amplificazione dei
VEGFRs si è utilizzato un programma di 40 cicli a 94°C per 30 secondi, 56°C
per 30 secondi, 72°C per 30 secondi. La sequenza delle coppie di
oligonucleotidi usati e le rispettive sonde sono le seguenti:
β2-microglobulina:
forward 5'-AACCACGTGACTTTGTCACAGC-3',
reverse 5'-CTGCTCAGATACATCAAACA TG-3',
probe 5'-GTGGGATCGAGACATGTAAGCAGC-3';
Flt1:
forward 5'-GATA CTCGACTTCCTCTGAA-3',
reverse 5'-ATCAAACATGGAGGTGGCATT-3,
probe 5'-GACTACATGCCAATCAATGC-3';
sFlt1:
forward 5'-ATTTTAGGACCAGG AAGCAG-3',
reverse 5'-AGCCACACAGGTGCATGTTAGAGT-3,
probe 5'-CAC CTTCATCCTCTTCTGTG-3';
KDR:
forward 5'-AGACTTTGAGCATGGAAG-3',
reverse 5'-CCATTCCACCAAAAGATG-3',
probe 5'-CATTATGACAACACAGCA GGAATCAGTCAG-3'.

31
STIMOLAZIONE CELLULARE E WESTERN BLOTTING
Al 5° giorno di coltura le DC sono state lavate con PBS e tenute per 18 ore in
RPMI/0.2% FCS e poi altre tre ore in RPMI/0.1%BSA. Aliquote di 3-5x105
cellule sono state stimolate per 4-10-20 minuti con 0.1-1 µg/mL di VEGF o
PlGF. Dopo un lavaggio con PBS freddo, le cellule sono state risospese in una
soluzione di lisi (50mM Tris, 150mM NaCl, 1mM NaF, 1%Triton X-100,
0.1mM Na3VO4 , 1mM PMSF, una pasticca di inibitori di proteasi -Complete
®; Roche-) per 15 minuti in ghiaccio. I lisati cellulari così ottenuti sono stati
centrifugati per 10 minuti a 4°C, e la concentrazione finale delle proteine è
stata determinata usando il kit protein assay (Bio-Rad, Hercules, CA).
Aliquote di 30 µg di proteine sono state denaturate a 95°-100° per 10 minuti
in loading buffer (60mM Tris, 25% glicerolo, 10% SDS, 14.4mM 2-
Mercaptoethanol, 1% Bromophenol Blue) quindi separate su un gel al 10% di
poliacrilammide con un marcatore per i pesi molecolari (Bio-Rad, Hercules,
CA).
I campioni sono stati quindi trasferiti su una membrana di nitrocellulosa e
incubati in TBST (10mM Tris-HCl, 150 mMNaCl, 0.1% Tween-20) con il
5% di latte in polvere non grasso per bloccare eventuali legami non specifici
dell’anticorpo alla membrana. La membrana è stata quindi marcata con
l’anticorpo anti-phospho-AKT (Ser-473) e anti-phospho-ERK1/2 (p42/44),
alle condizioni suggerite dal protocollo (Cell Signaling, Beverly, MA). I
rispettivi anticorpi per la forma non fosforilata sono stati utilizzati come
controllo. Come anticorpo secondario si è usata una perossidasi anti-rabbit
(Amershan, Arlington Heights, IL). Il legame del secondario è stato
evidenziato dalla chemioluminescenza su lastre fotografiche (Pierce,
Rockford, IL).

32
4. RISULTATI
CARATTERISTICHE DELLA POPOLAZIONE DENDRITICA
DERIVATA DA MONOCITI MATURI
Per ottenere le DC, i Mo maturi, isolati da PB, sono stati incubati per 4-5
giorni in mezzo di coltura contenente GM-CSF e IL-4. Al fine di indurre una
completa maturazione della popolazione dendritica è stato aggiunto al 6°
giorno l’LPS.
Durante il differenziamento dai Mo maturi, le DC non aumentano
numericamente; ciò nonostante, test di proliferazione eseguiti su cellule
immature, mostrano un lieve livello d’incorporazione di timidina (circa 400
cpm per 1x105 cellule) che indica un basso grado di sintesi di DNA.
Per monitorare le diverse fasi differenziative/maturative della popolazione,
aliquote di cellule sono state prelevate a diversi giorni e analizzate sia dal
punto di vista morfologico che per l’espressione di specifici marcatori di
membrana. I risultati ottenuti mostrano che, in presenza di GM-CSF e IL-4, le
variazioni morfologiche iniziano precocemente: la popolazione monocitaria di
partenza è caratterizzata da un nucleo reniforme, che occupa metà del volume
cellulare, e un citoplasma finemente granulato (figura 3 A); già dopo tre
giorni le cellule acquistano il caratteristico profilo dendritico. Le DC ottenute
presentano nucleo monocitoide e un abbondante citoplasma lievemente
basofilo, contenente un minor numero di granulazioni azzurrofile rispetto ai
Mo. I margini irregolari presentano numerosi e sottili prolungamenti, detti
dendriti, spesso polarizzati (figura 3 B).

33
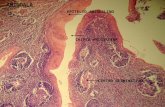
Figura 3
Analisi morfologica effettuata attraverso la colorazione diMay-Grumwald-Giemsa, di:
A) Mo isolati da PB e analizzati dopo un giorno di coltura;B) DC al 5° giorno di coltura.
Ingrandimento originale: 400X.
A
B
A
B

34
Le fasi di differenziamento delle DC sono state seguite mediante analisi
fenotipiche a diversi giorni di coltura.
Il marcatore CD14, presente sulla totalità della popolazione monocitaria di
partenza, scompare nei primi tre giorni di differenziamento; parallelamente
compare il CD1a già presente sull’intera popolazione dal secondo giorno di
coltura (figura 4).
Le molecole MHC di classe I e II (HLA-ABC e HLA-DR) sono presenti
sull’intera popolazione di DC immature. In seguito a stimolazione con LPS la
percentuale di cellule positive CD1a, HLA-DR e HLA-ABC rimane invariata,
ma si osserva un aumento nell’MFI (figura5).
L’espressione degli antigeni di superficie responsabili della funzionalità delle
DC, quali CD40, CD80, CD83, CD86, è bassa in cellule immature, ma la
percentuale di cellule positive aumenta notevolmente dopo maturazione con
LPS (figura 5).

35
Figura 4
Analisi citofluorimetrica delle DC a diversi giorni di coltura:A) controllo negativo di fluorescenza realizzato mediante doppia
marcatura con IgG coniugate PE e FITC;B) doppia marcatura con gli anticorpi CD1a-PE e CD14-FITC.
La figura mostra i risultati di un esperimento rappresentativo su sei.
3% 63%
33%
8% 85%
7%
58% 32%
1%
98%1%
0%
2° giorno3% 63%
33%
8% 85%
7%
58% 32%
1%
98%1%
0%
2° giorno

A
B
36
(Didascalia alla pagina successiva)
IgG-FITC IgG-PE
HLA-DR
CD40
CD80 CD83
CD86
HLA-ABC
CD1A

37
Figura 5
Analisi citofluorimetrica delle DC al 6° giorno di coltura (istogrammagrigio) e dopo 18 ore di stimolazione con LPS (istogramma bianco).
A) controllo negativo di fluorescenza realizzato mediante l’utilizzo diIgG direttamente coniugate con PE e FITC;
B) marcature con gli anticorpi direttamente coniugati PE: CD1a,CD40, CD80, CD83, HLA-ABC e coniugati FITC: CD86,HLA-DR.
La figura mostra i risultati di un esperimento rappresentativo su cinque.

38
ANALISI FUNZIONALE DELLE CELLULE DENDRITICHE
Per verificare che la popolazione di DC, ottenuta dai Mo, fosse
funzionalmente attiva, cioè in grado di presentare l’antigene e attivare i
linfociti T, sono stati allestiti saggi di captazione degli antigeni, e saggi di
MLR.
L’attività endocitica, caratteristica delle DC immature, è stata valutata
misurando la capacità della popolazione di incorporare il destrano. Il saggio è
stato condotto su aliquote di cellule, prelevate al 3°-4° giorno di coltura,
incubate con il destrano alla temperatura di 37°C o a 4°C per il controllo
negativo. I dati ottenuti, dopo analisi al citofluorimetro, mostrano che circa
90% delle DC immature sono in grado di internalizzare il destrano (figura 6);
tale capacità si riduce in seguito alla maturazione (dato non mostrato).
Caratteristica propria delle DC mature è invece la capacità di stimolare i
linfociti T, valutata mediante il test dell’MLR.
Le DC mature e linfociti T, purificati da PB, sono stati coincubati per 6 giorni
e nelle ultime 12 ore di coltura è stata aggiunta timidina triziata. La
proliferazione dei linfociti, e quindi la capacità stimolatoria delle DC, sono
state verificate misurando la quantità di timidina incorporata nel DNA
neosintetizzato delle cellule stimolate (linfociti T). I risultati ottenuti,
evidenziano un’ottima capacità della popolazione dendritica da noi ottenuta,
di presentare l’antigene e quindi di attivare i linfociti T (figura 7).

39
Figura 6
Saggio di captazione del destrano-FITC su DC al 3° giorno di coltura:A) campione incubato a 4°C (controllo); B) campione incubato a 37°C.
La figura mostra i risultati di un esperimento rappresentativo su sei.
A
B
destrano-FITC
A
B
destrano-FITC

40
Figura 7
Capacità delle DC, dopo stimolazione con LPS, di attivare i linfociti T. Inascissa è espressa la quantità di timidina incorporata nel DNA neosintetizzatodei linfociti T stimolati; in ordinata il rapporto tra DC, cellule “stimulator”, elinfociti T, cellule “responder”. I valori rappresentati sono la media, ± DS, disei esperimenti.
01:2000 1:660 1:220 1:74
DC: linfociti T
20
40
60
80cp
mx
103
01:2000 1:660 1:220 1:74
DC: linfociti T
20
40
60
80cp
mx
103

41
ESPRESSIONE DEI VEGFRs NELLA POPOLAZIONE MONOCITARIA E
DENDRITICA
Abbiamo analizzato su Mo e DC l’espressione dell’mRNA dei VEGFRs, Flt1
e KDR.
Mo maturi analizzati 24 ore dopo l’isolamento, da PB, mostrano una bassa
espressione dei trascritti Flt1 e KDR. Già dal 3°-4° giorno di
differenziamento dendritico si osserva un consistente aumento
dell’espressione sia del trascritto del Flt1 che del KDR. In seguito a
maturazione con LPS, l’mRNA di entrambi i recettori si riduce (figura 8).
Nonostante si sia evidenziata, mediante RT-PCR, la presenza di entrambi i
trascritti, il livello dell’mRNA del KDR risulta notevolmente più basso di
quello del Flt1. Quest’ultimo è infatti evidenziabile su lastre fotografiche già
dopo 2 ore d’esposizione del filtro marcato; mentre il segnale del KDR
compare solo dopo un’esposizione di almeno 12 ore.
La diversa espressione dei recettori del VEGF sulla popolazione dendritica è
stata confermata mediante analisi citoflurimetriche.
Diversi esperimenti hanno mostrato che il recettore KDR è presente su una
bassissima percentuale di cellule (sempre inferiore al 5%) sia nella
popolazione monocitaria (figura 9) sia sulle DC analizzate a diversi giorni di
cultura (figura 10). Inoltre l’espressione di tale recettore non sembra variare
né in seguito all’induzione dei Mo in senso dendritico, né ai diversi stadi
maturativi delle DC.

42
Figura 8
Attraverso la tecnica dell’RT-PCR, è stata analizzata la presenzadell’mRNA dei recettori Flt1 e KDR nei Mo e nelle DC a diversi giorni didifferenziamento. L’analisi dell’mRNA della β2-microglobulina (β2m)permette di controllare le quantità di mRNA, caricato sul gel.
La figura mostra i risultati di un esperimento rappresentativo su tre.
Flt-1
KDR
β2m
Mo
DC
4° g
ior n
o
DC
6° g
iorn
o
DC
6°g
iorn
o
+ 18
h LP
S
Flt-1
KDR
β2m
Mo
DC
4° g
ior n
o
DC
6° g
iorn
o
DC
6°g
iorn
o
+ 18
h LP
S

43
Figura 9
Espressione del KDR su Mo isolati da PB:A) controllo negativo di fluorescenza realizzato mediante marcatura
con IgG coniugate PE;B) marcatura dei Mo con l’anticorpo KDR-PE.
La figura mostra i risultati di un esperimento rappresentativo su tre.
IgG
-PE
KD
R-PE
A B
IgG
-PE
KD
R-PE
A B

44
Figura 10
Espressione del recettore KDR sulle DC:A) controllo negativo di fluorescenza realizzato mediante marcatura
con IgG coniugate PE;B) marcatura delle DC con l’anticorpo KDR-PE a diversi giorni di
cultura.La figura mostra i risultati di un esperimento rappresentativo su quattro.
3° giorno 7° giorno + LPS6° giorno
IgG
-PE
KD
R-P
E
A
B
3° giorno 7° giorno + LPS6° giorno
IgG
-PE
KD
R-P
E
A
B

45
Contrariamente al KDR, l’espressione del recettore Flt1 varia notevolmente in
funzione del tipo cellulare (Mo o DC) ed è modulato nei vari stadi
differenziativi/maturativi.
Come mostrato in figura 11, il Flt1 è presente su circa 20-40% dei Mo e
permane pressoché invariato nelle 24 ore successive l’induzione con mezzo
dendritico. E’ interessante notare la modulazione dell’espressione di Flt1
durante il differenziamento delle DC: difatti dal 3° giorno di coltura, in
mezzo dendritico, il recettore Flt1 è espresso dalla quasi totalità delle cellule
(90% di positività); una leggera riduzione si ha al giorno 6° di cultura, in cui
si osservano circa 70% di cellule positive; si riduce notevolmente dopo 18 ore
di stimolazione con LPS (14% di cellule positive) e scompare quasi
completamente dopo 48 ore dall’attivazione con LPS (circa 2% di cellule
positive; figura 11).
Abbiamo quindi verificato se il VEGF fosse in grado di legarsi ai recettori
espressi sulle DC. Mediante trattamento delle DC immature con VEGF
biotinilato abbiamo osservato un legame dose specifico: aumentando la
concentrazione del ligando da 20 a 500 ng/ml abbiamo ottenuto un aumento
di positività fino a 95% delle cellule (figura 12).
Successivamente è stata confermata la specificità del legame utilizzando in
esperimenti di competizione con VEGF biotinilato, il PlGF, in grado di legare
esclusivamente il Flt1.
In figura 13 è mostrato come PlGF, utilizzato ad una concentrazione pari a 10
µg/mL, cioè 100 volte di più rispetto a quella del VEGF biotinilato, inibisca il
legame del VEGF di circa 50%. La quasi totale inibizione del legame
(corrispondente ad un massimo del 4% di DC positive al VEGF- biotinilato)
si ottiene invece utilizzando una concentrazione di PlGF 200 volte superiore a
quella del VEGF (figura 13).

46
Flt1-PE
Figura 11
Espressione del recettore Flt1 su Mo isolati da PB e su DC a diversi giornidi coltura. Gli istogrammi bianchi rappresentano le cellule colorate conl’anticorpo anti-Flt1-PE, gli istogrammi grigi rappresentano le cellule coloratecon il controllo isotipico (IgG-PE).
La figura mostra i risultati di un esperimento rappresentativo su cinque.
Mo DC 1° giorno
DC 3° giorno
DC 6° giorno DC 6° giorno + 18 h LPS DC 6° giorno + 48 h LPS
Mo DC 1° giorno DC 3° giorno
DC 6° giorno DC 6° giorno + 18 h LPS DC 6° giorno + 48 h LPS
Mo DC 1° giorno DC 3° giorno
DC 6° giorno DC 6° giorno + 18 h LPS DC 6° giorno + 48 h LPS

47
VEGF bio./avidina-FITC
Figura 12
Marcatura delle DC al 5° giorno di coltura con VEGF biotinilato a diverseconcentrazioni: 20 ng/ml (b), 200 ng/ml (c), 500 ng/mL (d); o con il controllonegativo biotinilato (a). Le cellule sono state successivamente marcate conavidina-FITC e analizzate al citoflorimetro. La figura mostra i risultati di unesperimento rappresentativo su tre.
ac db
0
10
20
30
40
5
0 6
0a
c db0
10
2
0
30
40
50
60

48
VEGF bio./avidina-FITC
Figura 13
Marcatura delle DC al giorno 5° di coltura con VEGF biotinilato ad unaconcentrazione di 100 ng/ml (d) o con controllo negativo biotinilato (a). Per ilsaggio di competizione le cellule sono state pretrattate con 10 µg/mL (c) o 20µg/mL (b) di PlGF, quindi marcate con VEGF biotinilato. Le cellule sonostate infine incubate con avidina-FITC e analizzate al citoflorimetro. La figuramostra i risultati di un esperimento rappresentativo su tre.
0
20
40
60
80
a c dba c db

49
Dimostrata l’espressione in membrana del Flt1 e la capacità del recettore
stesso di legare sia il VEGF sia il PlGF, abbiamo indagato l’eventuale
presenza della forma solubile del recettore Flt1, sia come trascritto mediante
RT-PCR, sia in forma di proteina secreta mediante saggi ELISA del mezzo di
coltura cellulare.
Utilizzando specifici primers, in grado di discriminare tra la forma solubile e
di membrana, abbiamo analizzato la presenza del trascritto del sFlt1 in Mo
maturi, subito dopo il loro isolamento da PB, e in colture di DC.
Come mostrato in figura 14 A, i Mo esprimono bassi livelli del trascritto
rispetto alle DC da essi derivate in cui si osserva, invece, un aumento
d’espressione. Esattamente come la forma di membrana, il trascritto del sFlt1
si riduce in DC mature, dopo attivazione con LPS.
Come atteso, un basso livello della proteina sFlt1 è stato rilevato nei
sopranatanti delle colture monocitarie (approssimamene 200 pg/mL secreta da
per 106 cellule) e livelli più alti nelle colture dendritiche.
Più esattamente: la proteina sFlt1 è secreta a bassi livelli durante le fasi
iniziali di differenziamento dendritico; si osserva poi un picco di produzione
al 6° giorno di cultura (1450 pg/ml per 106 cellule) ed infine una riduzione
nelle cellule attivate con LPS (750 pg/mL per 106 cellule; figura 14 B). I
livelli d’espressione del sFlt1 rispecchiano esattamente l’andamento osservato
per la forma di membrana. I dati ottenuti suggeriscono un ruolo del Flt1
(solubile e/o di membrana) su DC completamente differenziate, ma ancora
immature.

50
Figura 14
Espressione del sFlt1:
A) mRNA del sFlt1 in Mo isolati da PB e in DC a diversi giorni didifferenziamento. I campioni sono stati analizzati per la β2-microglobulina (β2m). La figura mostra le bande, visualizzate sugel d’agarosio, di un esperimento rappresentativo su tre.
B) Saggio ELISA per la quantificazione del sFlt1 nei sopranatanti dellecolture di Mo e DC a diversi giorni. I valori del sFlt1 secreto dallecellule, ottenuti da un esperimento rappresentativo, sono staticorretti per 1x106 cellule.
β2m
sFlt-1
Mo
DC
6° g
i orn
o
DC
6° g
iorn
o +
1 8h
LPS
A
B DC 6°giorno
DC 6°giorno +18 h
LPSDC 3°giorno
Mo
0
200
400
600
800
1000
1200
1400
1600
pg/m
l dis
Flt-1
per
106
cellu
le
β2m
sFlt-1
Mo
DC
6° g
i orn
o
DC
6° g
iorn
o +
1 8h
LPS
A
B DC 6°giorno
DC 6°giorno +18 h
LPSDC 3°giorno
Mo
0
200
400
600
800
1000
1200
1400
1600
pg/m
l dis
Flt-1
per
106
cellu
le

51
ATTIVAZIONE DI ERK-pathway DA PARTE DI VEGF E PlGF
Abbiamo successivamente indagato l’eventuale attivazione di vie di
trasduzione del segnale da parte del recettore Flt1 stimolato con VEGF e
PlGF.
Prima di procedere alla stimolazione con i fattori, le DC immature (al giorno
5° di cultura) sono state tenute una notte in RPMI/0.2% FCS e
successivamente tre ore in RPMI/0.1%BSA al fine di annullare qualsiasi
eventuale segnale di fosforilazione.
La stimolazione è stata indotta con diverse dosi di VEGF o PlGF (da 10
ng/mL a 1 µg/mL) e poiché sono stati ottenuti risultati analoghi, i successivi
esperimenti sono stati condotti utilizzando una concentrazione di ligando pari
a 100 ng/mL.
Abbiamo inizialmente studiato la via di trasduzione del segnale di ERK 1/2 e
abbiamo osservato un transiente aumento della molecola fosforilata. Come si
può vedere nella figura 15 A, VEGF induce la fosforilazione di ERK 1/2 entro
10-20 minuti.
Risultati analoghi si sono osservati anche in seguito a stimolazione con PlGF
utilizzato alle medesime condizioni sperimentali (figura 15 B).
Successivamente abbiamo studiato l’attivazione della via di trasduzione del
segnale di AKT, ma questa chinasi non viene maggiormente fosforilata in
seguito al legame del Flt1 con VEGF o PlGF (dato non mostrato).

52
Figura 15
Western blotting di lisati proteici ottenuti da DC al 5° giorno di colturastimolate con:
A) 100 ng/mL di VEGF per 4, 10 e 20 minuti. B) 100 ng/mL di VEGF o PlGF per 10 minuti.
I lisati cellulari sono stati trasferiti su una membrana di nitrocellulosasuccessivamente marcata con l’anticorpo contro la forma fosforilata di ERK(P-ERK1/2; 42/44 kDa ), o con l’anticorpo rispettivo per la forma nonfosforilata (ERK) utilizzato come controllo. Risultati di un esperimentorappresentativo su sei.
A
B
A
BB
cont
rollo
VEG
F 4′
VEG
F 10′
VEG
F 20′
P-ERK 1/2 →
ERK 1/2 →
cont
rollo
VEG
F 10′
PlG
F 10′
P-ERK 1/2 →
ERK 1/2 →

53
ANALISI DELLA PRODUZIONE DI VEGF E PlGF DA PARTE DI
COLTURE MONOCITARIE E DENDRITICHE
Prima di studiare l’effetto del VEGF e del PlGF esogeno sulle colture di DC
in differenziamento, abbiamo verificato l’eventuale secrezione di tali fattori
da parte delle popolazioni cellulari monocitarie e dendritiche.
Il sopranatante ottenuto dai Mo tenuti per 2 giorni in cultura, e dalle DC a
diversi stadi maturativi (dal 1° giorno al 6° giorno di coltura e dopo 24 ore di
maturazione con LPS) è stato raccolto ed analizzato mediante saggi ELISA.
I risultati ottenuti mostrano che in entrambe le popolazioni cellulari non vi è
secrezione di VEGF o PlGF: i valori ottenuti sono inferiori al livello di
background (< 10 pg/mL; dato non mostrato).
ANALISI DI CULTURE DENDRITICHE TRATTATE
CON VEGF E PlGF
• Condizioni di coltura
I fattori VEGF e PlGF sono stati aggiunti alle colture dendritiche, dopo
almeno 36 ore di differenziamento dai Mo, ad una concentrazione finale di
100 ng/mL; poiché tali fattori hanno breve emivita, sono stati riaggiunti ogni
due giorni.
Il trattamento delle DC con diverse concentrazioni di tali fattori, da 5 ng/mL a
100 ng/ml, ha mostrato effetti equivalenti.

54
• Crescita e vitalità cellulare
Abbiamo inizialmente studiato l’effetto del VEGF e del PlGF sulla
proliferazione e vitalità cellulare.
Come precedentemente descritto, le DC ottenute da Mo maturi non
proliferano e incorporano bassi livelli di timidina triziata (400 cpm per 1x105
cellule/mL). Ciò nonostante, nei saggi di proliferazione si osservano
differenze d’incorporazione della timidina, tra le DC di controllo e le cellule
trattate con i fattori VEGF e PlGF. Il trattamento delle DC immature con il
VEGF (da 5 a 100 ng/mL) determina una riduzione dose-dipendente di
incorporazione di timidina di circa 20-40% rispetto al controllo (figura 16 A).
Risultati equivalenti si ottengono trattando le cellule con PLGF. Nella figura
16 B osserviamo una riduzione d’incorporazione di timidina del 30% in DC
trattate con 50 ng/mL di PlGF rispetto al controllo.
Per chiarire meglio il significato biologico di questo dato, abbiamo
parallelamente studiato l’effetto del VEGF e del PlGF sulla vitalità cellulare a
diversi giorni di coltura.
A livello morfologico non si osservano differenze tra le cellule di controllo e
le popolazioni trattate con i fattori di crescita (dato non mostrato).
Per valutare la quota di cellule apoptotiche presenti nelle colture cellulari, è
stato misurato, mediante analisi al citofluorimetro, il livello d’incorporazione
di annessina e propidio ioduro. La figura 17 mostra le DC al 2°, 6° giorno di
coltura e al 7° giorno dopo attivazione con LPS. I risultati dimostrano che non
vi sono differenze tra la popolazione di controllo e quelle trattate con VEGF o
PlGF sul numero di cellule apoptotiche (figura 17).

55
Figura 16
Saggio di proliferazione di DC:A) DC di controllo e trattate con diverse concentrazioni di VEGF (da
5 a 100 ng/mL); B) DC di controllo o trattate con 50 ng/mL di PlGF.
Al 3° giorno di coltura sono stati aggiunti ad ogni pozzetto 0.5 mCi ditimidina e dopo 18 ore ne è stata misurata l’incorporazione. I valori degliistogrammi rappresentano la percentuale della timidina incorporata rispetto alcontrollo (il cui valore è 400 cpm per 1x105 cellule/mL), considerato 100%.
A
B
0
20
40
60
80
100
120
cont
rollo
VEG
F
5ng/
mL
VEG
F 10
ng/m
L
VEG
F50
ng/m
L
VEG
F10
0ng/
mL
% c
pm
50ng
/mL
100co
ntro
llo
0
20
40
60
80Pl
GF
% c
pm
A
B
0
20
40
60
80
100
120
cont
rollo
VEG
F
5ng/
mL
VEG
F 10
ng/m
L
VEG
F50
ng/m
L
VEG
F10
0ng/
mL
% c
pm
0
20
40
60
80
100
120
cont
rollo
VEG
F
5ng/
mL
VEG
F 10
ng/m
L
VEG
F50
ng/m
L
VEG
F10
0ng/
mL
% c
pm
50ng
/mL
100co
ntro
llo
0
20
40
60
80Pl
GF
% c
pm
100co
ntro
llo
0
20
40
60
80Pl
GF
% c
pm
0
20
40
60
80Pl
GF
% c
pm

56
Figura 17
Analisi citofluorimetrica, eseguita su DC a diversi giorni di coltura dicellule in fase iniziale di apoptosi (annessina positive) e cellule in fase tardivadi apoptosi o morte (annessina e propidio positive).
Nella prima colonna sono riportate le DC di controllo, nella seconda e terzacolonna le DC cresciute rispettivamente nel mezzo integrato con i fattoriVEGF o PlGF. La figura mostra i risultati di un esperimento rappresentativosu tre.

57
• Fenotipo
Successivamente abbiamo verificato l’effetto del VEGF e del PlGF sul
differenziamento fenotipico della popolazione.
Dalle analisi citofluorimetriche è emerso che il VEGF e il PlGF non alterano
il profilo fenotipico né della popolazione immatura né di quella attivata con
LPS. Gli antigeni di membrana normalmente presenti sulle DC mature (quali
CD1a, CD40, CD83, CD86) sono infatti espressi in eguale percentuale dalle
cellule trattate con i fattori VEGF e PlGF, rispetto al controllo. In figura 18
sono mostrati i principali antigeni di membrana delle DC mature nelle tre
condizioni di coltura.
Questi dati indicano che i fattori VEGF e PlGF non esercitano un effetto sulla
maturazione fenotipica delle DC.
• Funzionalità
Abbiamo analizzato l’attività funzionale della popolazione dendritica trattata
con i fattori VEGF o PlGF, studiandone l’attività endocitica e la capacità di
stimolare i linfociti T.
Le analisi al citofluorimetro indicano che le DC immature trattate con VEGF
o PlGF, hanno una maggior capacità di internalizzare il destrano: mostrano,
infatti, una più alta MFI rispetto al controllo (figura 19).
Le DC mature perdono gradualmente tale capacità acquisendo invece l’abilità
di presentare gli antigeni ai linfociti T. In figura 20 sono presentati i risultati
dei saggi di MLR eseguiti con DC cresciute con VEGF e PlGF e poi maturate
con LPS.
E’ chiaramente evidente una minor capacità delle cellule trattate con VEGF o
PlGF, di attivare i linfociti T.

58
controllo VEGF PlGF
IgG-PE
CD1a
CD40
CD83
CD86
(didascalia alla pagina successiva)
controllo VEGF PlGF
IgG-PE
CD1a
CD40
CD83
CD86
(didascalia alla pagina successiva)

59
Figura 18
Analisi citofluorimetrica delle DC, al 7° giorno di coltura dopo stimolazionecon LPS, trattate, o non, con VEGF o PlGF. Nella prima riga sonorappresentate le cellule marcate con il controllo negativo di fluorescenza(IgG) direttamente coniugato PE; a seguire osserviamo le marcature con glianticorpi direttamente coniugati PE: CD1a, CD40, CD83, CD86. La figuramostra i risultati di un esperimento rappresentativo su sei.

60
Destrano-FITC
Figura 19
Saggio di captazione del destrano-FITC su DC al 3° giorno di coltura:A) campione di controllo e cellule crescite con VEGF o PlGF tenuti a
4°C (istogrammi sovrapposti);B) campione di controllo (istogramma grigio) e DC cresciute con
VEGF (istogramma bianco) tenute a 37°C;C) campione di controllo (istogramma grigio) e DC cresciute con PlGF
(istogramma bianco) tenute a 37°C.La figura mostra i risultati di un esperimento rappresentativo su sei.
A
B controllo
controllo
VEGF
PLGF
C
A
B controllo
controllo
VEGF
PLGF
C

61
Figura 20
Capacità delle DC mature di controllo ( ○ ) e trattate con VEGF ( □ ) o PlGF( ▲ ), di attivare i linfociti T. In ascissa è espressa la quantità di timidinaincorporata nel DNA dei linfociti T stimolati; in ordinata il rapporto tra DC,cellule “stimulator”, e linfociti T, cellule “responder”. La figura mostra irisultati di un esperimento rappresentativo su sei.
0
20000
40000
60000
80000
50 150 450 1350
CPM
x 1
03
1:2000 1:660 1:220 1:74
DC: linfociti T
cpm
x 10
3
20
40
60
80
0
20000
40000
60000
80000
50 150 450 1350
CPM
x 1
03
1:2000 1:660 1:220 1:74
DC: linfociti T
cpm
x 10
3
20
40
60
80
0
20000
40000
60000
80000
50 150 450 1350
CPM
x 1
03
1:2000 1:660 1:220 1:74
DC: linfociti T
cpm
x 10
3
20
40
60
80

62
• Produzione di IL-12
Abbiamo infine verificato il livello di produzione di IL-12 da parte di DC
mature; IL-12 è una citochina essenziale per supportate la proliferazione dei
linfociti T.
I dati ottenuti dimostrano che non vi è differenza nella produzione di IL-12 da
parte di DC trattate con VEGF o PlGF rispetto al controllo (figura 21).
Figura 21
Saggio ELISA per la quantificazione della citochina IL-12 secreta nel mezzodi coltura di DC mature trattare, o non, con 100 ng/mL di VEGF o PlGF. Ivalori medi (± DS) di tre esperimenti sono stati normalizzati per 105 cellule egraficati. I livelli di pg/mL di citochina prodotta sono rispettivamente: 166±33 pg/ml per le DC di controllo; 170 ± 10 pg/mL per DC trattate con VEGF;160± 25 pg/mL per DC trattate con PlGF.
pg/m
L di
IL-1
2 pe
r 105
cellu
le
0
50
100
150
200
controllo VEGF PlGF
pg/m
L di
IL-1
2 pe
r 105
cellu
le
0
50
100
150
200
controllo VEGF PlGF

63
5. DISCUSSIONE
La riduzione numerica e la scarsa funzionalità delle DC osservata nei pazienti
con il cancro, sono i risultati di due importanti meccanismi attuati dalle
cellule tumorali per evadere il sistema immunitario.
E’ noto che le cellule tumorali producono una grande varietà di citochine e
che il VEGF è uno dei principali fattori responsabili degli effetti osservati
sulle DC.
Diversi autori hanno dimostrato che il VEGF esercita un effetto inibitorio
sulla differenziazione dendritica agendo sui precursori delle DC (Gabrilovich
D. et al. 1996; Troy A. et al. 1998; Almand B. et al. 2000; Kiertscher SM. et
al. 2000; Della Bella S. et al. 2003).
E’ stato dimostrato, inoltre, che il VEGF impedisce la maturazione delle DC
se aggiunto alle colture contemporaneamente all’LPS (bTakahashi A. 2004).
Non è ancora noto, invece, se il VEGF eserciti un effetto diretto sulle DC
immature.
Alcuni autori hanno mostrato l’espressione di entrambi i recettori del VEGF,
sulla popolazione dendritica (bTakahashi A. 2004). Noi abbiamo confermato e
studiato più dettagliatamente tale espressione sia nei Mo maturi, da cui
derivano le DC da noi utilizzate, che nelle DC ai diversi stadi maturativi.
Mediante RT-PCR ed immunofluorescenza, abbiamo osservato che il
recettore Flt1 è espresso su 90% delle DC immature e si riduce gradualmente
in seguito alla loro maturazione. Parallelamente, il recettore del KDR si
riduce in seguito alla maturazione indotta dall’LPS, ma la sua espressione
sulle DC immature non è mai superiore al 5% della popolazione cellulare.

64
L’osservazione dell’espressione del Flt1 espresso sulla quasi totalità delle DC
immature, ci ha indotto ad ipotizzare che il VEGF, presente nel
microambiente tumorale, possa interferire con la funzionalità delle DC
agendo direttamente su di esse. Inoltre la riduzione del Flt1, osservata in
seguito alla maturazione delle DC, suggerisce un ruolo di tale recettore
durante il loro stadio immaturo.
Per comprendere la funzione del Flt1 sulle DC, abbiamo eseguito esperimenti
usando sia la molecola del VEGF che del PlGF; quest’ultimo fattore di
crescita lega il Flt1 con alta affinità e non è in grado di legare il KDR.
L’utilizzo di entrambe le molecole ci permette di attribuire gli eventuali effetti
osservati unicamente all’attivazione del recettore Flt1.
Abbiamo dimostrato, mediante marcatura con VEGF biotinilato, il legame del
VEGF sulle DC e, in esperimenti di competizione tra VEGF biotinilato e
PlGF, abbiamo confermato la specificità di legame di entrambi i fattori al
recettore Flt1.
Successivamente abbiamo verificato se in seguito a tale legame si attivassero
le vie di traduzione del segnale di AKT o della MAP chinasi ERK 1/2.
In un lavoro di Selvaraj S.K. è descritto un transiente aumento, a tempi molto
precoci (0.5 minuti), della fosforilazione di AKT in Mo maturi stimolati con
PlGF (Selvaraj S.K. et al. 2003). Nelle nostre colture dendritiche non abbiamo
osservato nessun evidente aumento della fosforilazione di AKT in seguito a
stimolazione con VEGF o PlGF. Contrariamente, abbiamo dimostrato che
entrambi i fattori inducono un aumento, tempo-dipendente, della
fosforilazione di ERK 1/2.
Questi dati sono in accordo con quelli di precedenti lavori in cui viene
mostrato, in linee cellulari ottenute dal colon-retto (Fan F. et al. 2005), in
cellule muscolari lisce (Kazi A.S. 2004) e in cellule di mieloma (Podar K. et

65
al. 2001), che il VEGF induce un aumento della fosforilazione di ERK 1/2,
mediante attivazione di Flt1; l’attivazione di ERK 1/2 è stata dimostrata anche
in Mo maturi stimolati con PlGF (Selvaraj S.K. et al. 2003).
E’ stato dimostrato, inoltre, che le via del segnale della MAP chinasi ERK 1/2
regola la maturazione delle DC (Kröger A.P. et al. 2001; Yi A. et al. 2002).
Kröger A.P. e colleghi hanno osservato, difatti, in DC derivate da Mo maturi,
che l’inibizione della trasduzione del segnale di ERK 1/2 potenzia:
l’espressione delle molecole costimolatorie, la perdita della capacità
endocitica, l’attività del fattore trascrizionale NF-κB, il rilascio di IL-12 e la
capacità delle DC attivate di stimolare i linfociti T.
Infine è stato recentemente mostrato che, in DC derivate da cellule staminali
embrionali murine, il signaling del Flt1 è sufficiente a bloccare l’attivazione
di NF-κB (Dikov M.M. et al. 2005).
Tutti questi dati dimostrano il ruolo del Flt1 come primo mediatore
nell’inibizione della maturazione delle DC mediante la via del segnale di
ERK1/2.
Al fine di valutare un possibile effetto del VEGF e del PlGF sulle DC
immature, abbiamo aggiunto tali fattori nel mezzo di coltura dopo almeno 36
ore di differenziamento dai Mo maturi.
Inizialmente abbiamo verificato se il VEGF e il PlGF avessero un effetto sulla
proliferazione e vitalità cellulare.
E’ noto che le DC che derivano direttamente da Mo maturi, non proliferano e
mostrano bassi livelli d’incorporazione di timidina (Chapuis F. et al. 1997).
Ciò nonostante abbiamo osservato che il trattamento delle DC con VEGF o
PLGF determina una riduzione, dose dipendente, dell’incorporazione di
timidina. A dosi più alte di 50 ng/ml l’effetto è però annullato; questo

66
fenomeno è stato già osservato da altri autori (Barleon B. et al. 1996; Podar
K. Et al. 2001; Sawano A. et al. 2001).
L’incorporazione di timidina fornisce una misura quantitativa del grado di
sintesi del DNA che è di solito paragonabile all’attività proliferativa delle
cellule. Abbiamo quindi valutato la vitalità delle cellule trattate con VEGF o
PlGF, ma non abbiamo osservato differenze tra le popolazioni trattate e quelle
di controllo, né a livello morfologico, né nel numero di cellule apoptotiche.
Successivamente abbiamo studiato l’effetto del VEGF e PlGF sulla
maturazione e sulla funzionalità delle DC: quello che emerge dai risultati
ottenuti è che questi fattori inibiscono la completa maturazione della
popolazione.
In un recente lavoro è stato descritto che DC, derivate da Mo maturi, e
maturate con LPS in presenza di VEGF, non presentano in membrana alti
livelli di CD80 e il CD86, producono una bassa quantità di IL-12 e sono
incapaci di attivare i linfociti T (bTakahashi A. et al. 2004).
Le nostre popolazioni dendritiche, trattate con VEGF e PlGF, risultano
attivare meno efficacemente i linfociti T nonostante siano fenotipicamente
mature e producano normali livelli di IL-12.
I diversi risultati ottenuti potrebbero essere dovuti alla differente fase
maturativa delle DC al momento del trattamento con il VEGF: nel lavoro di
Takahashi A. il VEGF viene aggiunto solo al 5° giorno contemporaneamente
all’LPS, noi lo aggiungiamo al mezzo di coltura dopo 36 ore di
differenziamento dai Mo.
Il differente effetto del VEGF aggiunto all’inizio delle colture dendritiche,
rispetto a quello osservato con DC trattate solo durante gli ultimi stadi
maturativi, suggerisce la possibile esistenza di due distinti pathways mediante

67
i quali le cellule tumorali possono sopprimere il controllo immunitario agendo
sulle DC.
Particolarmente interessante è l’osservazione che le DC trattate con VEGF o
PlGF a stadi maturativi precoci, mostrano una prolungata capacità di
internalizzare gli antigeni rispetto alle cellule di controllo.
Questi dati concordano con i risultati pubblicati da Gabrilovich G. il quale
dimostra che DC ottenute da topi trattati con VEGF hanno un’aumentata
capacità d'internalizzare il destrano (Gabrilovich D. et al. 1998).
L’internalizzazione degli antigeni è una caratteristica propria delle DC
immature; pertanto un aumento di tale capacità è un’indicazione dello stato
prolungato della fase immatura delle DC trattate con VEGF o PlGF rispetto al
controllo.
Un’ulteriore indicazione del blocco maturativo delle nostre popolazioni
dendritiche trattate, è la loro inefficienza nello stimolare i linfociti T (essendo
tale capacità caratteristica delle DC mature).
Come precedentemente commentato, Takahashi A. ha già descritto questo
effetto del VEGF sulle DC e in un lavoro di Oyama T. è stata dimostrata la
riduzione della stimolazione dei linfociti T da parte di DC derivate da
progenitori ematopoietici trattati con PlGF (Oyama T. et al. 1998).
La ridotta capacità delle DC di attivare i linfociti T, non sembra dovuta alla
loro ridotta vitalità: difatti, le DC trattate con VEGF e PlGF, mostrano una
percentuale di cellule apoptotiche simile al controllo. Suggeriamo che il
legame del VEGF o del PlGF, mediante Flt1, alteri la maturazione di DC
immature con conseguente effetto sulle attività funzionali.
Inoltre escludiamo che sFlt1 prodotto dalle DC possa mascherare o rendere
meno evidenti gli effetti osservati in vitro. La sFlt1 è un potente antagonista
del VEGF (He Y. et al. 2005), ciò nonostante la quantità di VEGF aggiunta

68
alle colture di DC è 150 volte superiore alla quantità di sFlt1 prodotto dalle
stesse DC.
La secrezione del sFlt1, così come l’espressione della forma di membrana, si
riduce nelle DC mature suggerendo un ruolo del Flt1 in particolare nella fase
immatura. Il significato biologico della produzione del sFlt1 è ad oggi ancora
da chiarire.
In conclusione, noi osserviamo che il trattamento con VEGF o PlGF,
all’inizio della differenziazione dendritica, mantiene la popolazione in uno
stato immaturo alterandone la funzionalità ed ipotizziamo che il Flt1 sia il
principale mediatore di tali effetti.
L’effetto mediato dal Flt1è verosimilmente indotto attraverso la cascata del
segnale di ERK.
Questi dati identificano un nuovo ruolo che il VEGF gioca nel sistema
immunitario e indicano un possibile meccanismo mediante il quale si ha
accumulo di DC immature e inattive nelle aree tumorali.
Queste scoperte suggeriscono, infine, che una specifica molecola target del
Flt1 potrebbe migliorare le risposte del sistema immunitario nei pazienti con
il cancro.

69
6. BIBLIOGRAFIA
Abbas A.K., Lichtman A.H. e Pober J.S. 1998. Immunologia cellulare e
molecolare. III Edizione, Piccin, Padova.
Adams S., O’Neill D.W., e Bhardawaj N. Recent advances in dendritic cell
biology. Journal of Clinical Immunology. 2005; Vol. 25. No.2: 87-97.
Almand B., Resser J.R., Lindman B., Nadaf S., Clark J.I., Kwon E.D.,
Carbone D.P., Gabrilovich D.I. Clinical significance of defective dendritic
cell differentiation in cancer. Clinical Cancer Research. 2000; 6:1755-1766.
Banchereau J. e Steinman R.M. Dendritic cells and the control of immunity.
Nature. 1998; 392: 245-252.
Banchereau J., Briere F., Caux C., Davoust J., Labecque S., Liu Y., Pulendran
B. and Palucka K. Immunobiology of dendritic cells. Annual Reviews of
Immunology. 2000; 18: 767-811.
Barleon B., Sozzani S., Zhou D., Weich H.A., Mantovani A., Marmè D.
Migration of human monocytes in response to vascular endothelial growth
factor (VEGF) is mediated via the VEGF receptor flt-1. Blood. 1996; Vol.
87: 3336-3343.

70
Brown L.F., Berse B., Jackman R.W., Tognazzi K., Manseau E.J., Senger
D.R., Dvorak H.F. Expression of vascular permeability factor (vascular
endothelial growth factor) and its receptors in adenocarcinomas of the
gastrointestinal tract. Cancer Research. 1993; 53(19):4727-35.
Broxmeyer H.E., Cooper S., Li Z.H., Lu L., Song H.Y., Kwon B.S., Warren
R.E., Donner D.B. Myeloid progenitor cell regulatory effects of vascular
endothelial cell growth factor. International Journal of Hematology. 1995;
62(4):203-15.
Casella I., Feccia T., Chelucci C., Samoggia P, Castelli G., Guerriero R.,
Parolini I., Petrucci E., Pelosi E., Morsilli O., Gabbianelli M, Testa U.,
Peschle C. Autocrine-paracrine VEGF loops potenziate the maturation of
megakaryocytic precursors through Flt1 receptor. Blood. 2003; 101:1316-
1323.
Caux C., Ait-Yahia S., Chemin K., de Bouteiller O, Dieu-Nosjean M.C.,
Homey B., Massacrier C., Vanbervliet B., Zlotnik A, Vicari A. Dendritic cell
biology and regulation of dendritic cell trafficking by chemokines. Springer
Seminars in Immunopathology. 2000; 22(4):345-69.
Chapuis F., Rosenzwajg M., Yagello M., Ekman M., Biberfeld P., Gluckman
J.C. Differentiation of human dendritic cells from monocytes in vitro.
European Journal of Immunology. 1997; 27:431-441.
Clauss M., Gerlach M., Gerlach H., Brett J., Wang F., Familletti P.C., Pan
Y.C., Olander J.V., Connolly D.T., Stern D. Vascular permeability factor: a

71
tumor-derived polypeptide that induces endothelial cell and monocyte
procoagulant activity, and promotes monocytes migration. Journal
Experimental Medicine. 1990; 172: 1535-45.
Della Bella S., Gennaro M., Vaccari M., Ferraris C., Nicola S., Riva A.,
Clerici M., Graco M., Villa M.L. Altered maturation of peripheral blood
dendritic cells in patients with breast cancer. British Journal of Cancer. 2003;
89: 1463-1472.
Dikov M.M., Ohm J.E., Ray N., Tchekneva E.E., Burlison J., Moghanaki D.,
Nadaf S., Carbone D.P. Differential roles of vascular endothelial growth
factor receptors 1 and 2 in dendritic cell differentiation. The Journal of
Immunology. 2005; 174:215-222.
Dvorak H.F. Nagy J.A., Berse B., Brown L.F., Yeo K.T., Yeo T.K., Dvorak
A.M., van de Water L., Sioussat T.M., Senger D.R. Vascular permeability
factor, fibrin, and the pathogenesis of tumor stroma formation. Annals of the
New York Academy of Sciences. 1992; Dec 4;667:101-11.
Dvorak H., Brown L.F., Detmar M., Dvorak A.M. Vascular permeability
factor/vascular endothelial growth factor, microvascular hyperpermeability,
and angiogenesis. American Journal of Pathology. 1995;146(5):1029-39.
Fan F., Wey J.S., McCarty M.F., Belcheva A., Liu W., Bauer T.W., Somcio
R.J., Wu Y., Hooper A., Hicklin D.J., Ellis L.M. Expression and function of
vascular endothelial growth factor receptor-1 on human colorectal cancer
cells. Oncogene. 2005;1-7.

72
Ferrara N. and Davis-Smyth T. The biology of vascular endothelial growth
factor. Endocrine Reviews. 1997; 18, 4-25.
Ferrara N.. Role of vascular endothelial growth factor in regulation of
physiological angiogenesis. American Journal of Physiology Cell. 2001; 280,
C1358-66.
Ferrara N., Gerber H.P. and LeCourter J. The biology of VEGF and its
receptors. Nature Medicine. 2003; 9:669-676.
Ferrara N.. Vascular endothelial growth factor: basic science and clinical
progress. Endocrine Reviews. 2004; 25:581-611.
Gabrilovich D., Chen H.L., Girgis K.R., Cunningham T., Meny G.M., Nadaf
S., Kavanaugh D., Carbone D.P. Production of vascular endothelial growth
factor by human tumors inhibits the functional maturation of the dendritic
cells. Nature Medicine. 1996; 2: 1096-1103.
Gabrilovich D., Corak J., Ciernik I.F., Kavanaugh D., Carbone D.P.
Decreased antigen presentation by dendritic cells in patients with breast
cancer. Clinical Cancer Research. 1997; 3:483-90.
Gabrilovich D., Ishida T., Oyama T., Ran S., Kravtsov V., Nadaf S., Carbone
D.P. Vascular endothelial growth factor inhibits the development of dendritic
cells and dramatically affect the differentiation of multiple hematopoietic
lineages in vivo. Blood. 1998; 92: 4150-4166.

73
Gabrilovich D., Ishida T., Nadaf S., Ohm J.E., Carbone D.P. Antibodies to
vascular endothelial growth factor enhance the efficacy of cancer
immunotherapy by improving endogenous dendritic cell function. Clinical
Cancer Research. 1999; 5(10):2963-70.
Gabrilovich D. Mechanisms and functional significance of tumor-induced
dendritic-cell defects. Nature Reviews of Immunology. 2004; 4:941-52.
Gerber H.P., McMurtrey A., Kowalski J., Yan M., Keyet B.A,. Dixit V.,
Ferrara N. Vascular endothelial growth factor regulates endothelial cell
survival through the phospatidylinositol 3’-kinase/Akt signal transduction
pathway. Requirement for Flk-1/KDR activation. Journal of Biological
Chemistry. 1998; 273: 30336-43.
Gerber H.P., Malik A.K. , Solar G.P., Sherman D., Liang X.H., Meng G.,
Hong K., Marsters J.C., Ferrara N. Vascular endothelial growth factor
regulates hematopoietic stem cell survival by an internal autocrine loop
mechanism. Nature. 2002; 417 (6892): 954-8.
Gerber H.P. and Ferrara N. The role of VEGF in normal and neoplastic
hematopoiesis. Journal of Molecular Medicine. 2003; 81:20-31.
Gille H., Kowalski J., Li B., LeCouter J., Moffat B., Zioncheck T.F., Pelletier
N., Ferrara N. Analysis of biological effects and signaling properties of Flt-1
(VEGFR-1) and KDR (VEGFR-2). Journal of Biological Chemistry. 2001;
276:3222-3230.

74
Hart D.N.J. Dendritic cells: unique leukocyte populations which control the
primary immune response. Blood. 1997; Vol. 90, No 9:3245-3287.
Hattori K., Heissig B., Wu Y., Dias S., Tejada R., Ferris B., Hicklin D.J., Zhu
Z., Bohlen P., Witte L., Hendrikx J., Hackett N.R., Crystal R.G., Moore M.A.,
Werb Z., Lyden D., Rafii S. Placental growth factor reconstitutes
hematopoiesis by recruiting VEGFR1(+) stem cells from bone-marrow
microenvironment. Nature Medicine. 2002; 8, 841-9.
He Y., Smith S.K., Day K.A., Clark D.E., Licence D.R., Charnock-Jones D.S.
Alternative splicing of vascular endothelial growth factor (VEGF)-R1 (Flt-1)
pre-mRNA is important for the regulation of VEGF activity. Molecular
Endocrinology. 1999; 13: 537-545.
Ishida T., Oyama T., Carbone D.P., Gabrilovich D. Detective function of
Langerhans cells in tumor-bearing animals is the result of detective
maturation from hematopoietic progenitors. Journal of Immunology. 1998;
161 (9): 4842-51.
Kanno S., Oda N., Abe M., Terai Y., Ito M., Shitara K., Tabayashi K.,
Shibuya M., Sato Y. Roles of two VEGF receptors, Flt-1 and KDR, in the
signal transduction of VEGF effects in human vascular endothelial cells.
Oncogene. 2000; 19, 2138-46.

75
Karkkainen M.J., Petrova T.V. Vascular endothelial growth factor receptors
in the regulation of angiogenesis and lymphangiogenesis. Oncogene. 2000;
19, 5598-5605.
Kazi A.S., Lotfi S., Gonharova E.A., Tliba O., Amrani Y., Krymskaya V.P.,
Lazaar A.L. Vascular endothelial growth factor-induced secretion of
fibronectin is ERK dependent. American journal of physiology. Lung Cellular
and Molecular Physiology. 2004; 286 (3): L539-45.
Kendall R.L. end Thomas K.A. Inhibition of Vascular Endothelial Cell
Growth Factor Activity by an Endogeneously Encoded Soluble Receptor.
Proceedings of the National Academy of Sciences. 1993; Vol. 90, 10705-
10709.
Kiertscher S.M., Luo J., Dubinett S.M., Roth M.D. Tumors promote altered
maturation and early apoptosis of monocytes-derived dendritic cells. The
Journal of Immunology. 2000; 164:1269-1276.
Kröger-Puig A., Relloso M., Fernandez-Capetillo O., Zubiaga A., Silva A.,
Bernabeu C., Corbì A.L. Extracellular signal-regulated protein kinase
signaling pathway negatively regulates the phenotypic and functional
maturation of monocytes-deriver human dendritic cells. Blood. 2001;
98:2175-2182.
Landgren E., Schiller P., Cao Y., Claesson-Welsh L. Placenta growth factor
stimulates MAP kinase and mitogenicity but not phospholipase C-gamma and
migration of endothelial cells expressing Flt 1. Oncogene. 1998; 16, 359-67.

76
Larrivee B., Lane D.R., Pollet I., Olive P.L., Humphries R.K., Karsan A.
VEGFR-2 induces survival of hematopoietic progenitor cells. Journal of
Biological Chemistry. 2003; 278, 22006-13.
Montesoro E., Castelli G., Morsilli O., Nisini R., Stafsnes M.H., Carè A.,
Peschle C., Chelucci C. Unilineage monocytopoiesis in hematopoietic
progenitor culture: switching cytokine treatment at all monocytic
development stages induces differentiation into dendritic cells. Cell Death
Differentiation. 2005 Aug 19; [Epub ahead of print].
Neufeld G., Cohen T., Gengrinovitch S., Poltorak Z. Vascular endothelial
growth factor (VEGF) and its receptors. FASEB Journal. 1999; 13, 9-22.
Ohm J.E. and Carbone D.P. VEGF as a mediator of tumor-associated
immunodeficiency. Immunologic Research. 2001; 23:263-272.
Oyama T., Ran S., Ishida T., Nadaf S., Kerr L., Carbone D.P., Gabrilovich
D.I.. Vascular endothelial growth factor affects dendritic cells maturation
through the inhibition of Nuclear Factor-kB activation in hematopoietic
progenitor cells. The Journal of Immunology. 1998; 160:1224-1232.
Podar K., Tai Y., Davies F.E., Lentzsch S., Sattler M., Hideshima T., Lin
B.K., Gupta D., Shima Y., Chauhan D, Mitsiades C., Raje N., Richardson P.,
Anderson K.C. Vascular endothelial growth factor triggers signaling cascades
mediating multiple myeloma cell growth and migration. Blood. 2001; 98:428-
435.

77
Pujol B.F., Lucibello F.C., Zuzarte M, Lütjens P., Müller R., Havemann K.
Dendritic cells derived from peripheral monocytes express endothelial
markers and in the presence of angiogenic growth factors differentiate into
endothelial-like cells. European Journal of Cell Biology. 2001; 80: 99-110.
Saito H., Tsujitani S., Ikeguchi M., Maeta M., Kaibara N. Relationship
between the expression of vascular endothelial growth factor and the density
of dendritic cells in gastric adenocarcinoma tissue. British Journal of
Cancer.1998; 78(12):1573-7.
Sallusto F. and Lanzavecchia A. Efficient presentation of soluble antigen by
cultured human dendritic cells is maintained by granulocyte/macrophage
colony-stimulating factor plus interleukin 4 and downregulated by tumor
necrosis factor alpha. Journal Experimental Medicine. 1994; 179(4):1109-18.
Sawano A., Iwai S., Sakurai Y., Ito M., Shitara K., Nakahata T., Shibuya M.
Flt-1, vascular endothelial growth factor receptor 1, is a novel cell surface
marker for the lineage of monocyte-macrophages in humans. Blood. 2001;
97:785-791.
Selvaraj S.K., Giri R.K., Perelman N., Johnson C., Malik P., Kalra V.K.
Mechanism of monocytes activation and expression of proinflammatory
cytochemokines by placenta growth factor. Blood. 2003; 102: 1515-1524.

78
Shibuya M. Structure and dual function of vascular endothelial growth factor
receptor-1 (Flt-1). The International Journal of Biochemistry & Cell Biology.
2001; 33:409-420.
Shibuja M. Vascular endothelial growth factor receptor-2: its unique
signalling and specific ligand, VEGF-E. Cancer Science. 2003; 94, 751-6.
Steinman R.M., Pack M., Inaba K. Dendritic cell development and
maturation. Advances in Experimental Medicine and Biology. 1997; 417:1-6.
aTakahashi M., Yoshimoto T., Kubo H. Molecular mechanisms of
lymphangiogenesis. Internal Journal of Hematology. 2004; 80(1):29-34.
bTakahashi A., Kono K., Ichihara F., Sugi H., Fujii H., Matsumoto Y.
Vascular endothelial growth factor inhibits maturation of dendritic cells
induced by lipopolysaccharide, but not by proinflammatory cytokines. Cancer
Immunology, Immunotherapy. 2004; 53: 543-550.
aTroy A.J., Summers K.L., Davidson P.J., Atkinson C.H., Hart D.N. Minimal
recruitment and activation of dendritic cells within renal cell carcinoma.
Clinical Cancer Research. 1998; 4:585-93.
bTroy A., Davidson P., Atkinson C., Hart D. Phenotypic characterisation of
the dendritic cell infiltrate in prostate cancer. The Journal of Urology. 1998;
160: 214-9.

79
Weissman D. and Fauci A. Role of Dendritic cells in immunopathogenesis of
human immunodeficiency virus infection. Clinical Microbiology Reviews.
1997; pp. 358-367, 1997.
Yi A.K., Yoon J.G., Yeo S.J., Hong S.C., English B.K., Krieg A.M. Role of
mitogen-activated protein kinases in CpG DNA-mediated IL-10 and IL-12
production: central role of extracellular signal-regulated kinase in the negative
feedback loop of the CpG DNA-mediated Th1 response. The Journal of
Immunology. 2002; 168(9):4711-20.
Young J.W. Dendritic cells: expansion and differentiation with hematopoietic
growth factors. Current Opinion Hematology. 1999; 6: 135-144.
Ziegler B.L., Valtieri M., Porada G.A., De Maria R., Muller R., Masella B.,
Gabbianelli M., Casella I., Pelosi E., Bock T., Zanjani E.D., Peschle C. KDR
receptor: a key marker defining hematopoietic stem cells. Science. 1999; 285:
1553.

80

81
7. ACRONIMI
APC Antigen Presenting Cell
BSA Bovine Serum Albumine
CD Cluster of Differentiation
cDNA copy DNA
cpm conte per minuto
DS Standard Deviation
DC Dendritic Cells
ELISA Enzyme-Linked ImmunoSorbent Assay
ERK Extracellular signal-Regulated Kinases
FITC Fluorescin Isothiocyanate
Flk1 Fetal liver kinase 1
Flt1 Fms-like-tyrosine kinase 1
GM-CSF Granulocyte Macrophage-Colony Stimulating Factor
HLA Human Leukocyte Antigens
KDR Kinase insert Domain-containing Receptor
ICAM Intracellular Adhesion Molecule
IgG Immunoglobuline G

82
IL Interleukin
IFN Interferon
IMDM Iscove’s modified Dulbecco’s medium
LFA Limphocyte Function-Associated Molecule
LPS Lipopolysaccharide
MAP K Microtubule Associated Proteins Kinase
M-CSF Macrophage Colony-Stimulating Factor
MFI Mean Intensity Fluorescence
MHC Major Histocompatibility Complex
MIP Macrophage Infiammatory Protein
MLR Mixed Leukocyte Reaction
Mo
MoAb
Monocytes
Monoclonal Antibody
NOD/SCID NonObese Diabetic/Severe Combined Immunodeficiency
Disease
NF-κB Nuclear Factor-κB
PE Phycoerythhrin
PBS Phosphate Buffered Saline
PB Peripheral Blood
PlGF Placental Growth Factor

83
PI3K PhosphoInositide-3 Kinase
PKC Protein Kinase C
RPM Rotazioni Per Minuto
RT-PCR Reverse Transcription-Polymerase Chain Reaction
SCF Stem Cell Factor
SDF Stromal cell-Derived Factor
SDS Sodio Dodecil Solfato
TCR T cell receptor
TGF Transforming Growth Factor
TNF Tumor Necrosis Factor
VEGF Vascular Endothelial Growth Factor
VEGFRs VEGF Receptors
VLA Very Late Antigens

![Leucemia Linfoide Acuta dell’Adulto: Esperienza GIMEMASolalettura].pdf · Leucemia Linfoide Acuta dell’Adulto: Esperienza GIMEMA Antonella Vitale Divisione di Ematologia ... Padova,](https://static.fdocumenti.com/doc/165x107/5c713a4309d3f2282f8bf73b/leucemia-linfoide-acuta-delladulto-esperienza-solaletturapdf-leucemia.jpg)