Nessun titolo diapositiva - sunhope.it. De Rosa. Lezione 22. Alcoli fenoli. 12.13.pdf · De Rosa /...
Transcript of Nessun titolo diapositiva - sunhope.it. De Rosa. Lezione 22. Alcoli fenoli. 12.13.pdf · De Rosa /...

IndiceAlcoli e fenoli: gruppo funzionale
Alcoli: nomenclatura e classificazione
Fenoli: nomenclatura
Alcoli: principali reazioni
Fenoli
Eteri
Epossidi
Tioli
TioeteriCorso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
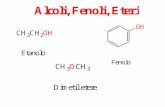
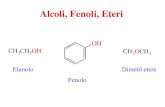
ALCOLI E FENOLIAlcoli e fenoli sono composti con lo stesso
gruppo funzionale: ossidrile –OH.
ALCOL
C-OHIl carbonio che lega la funzione ossidrilicaPuò essere un gruppo alchilico (ibridazione sp3)Può essere un gruppo alchenilico e alchinilico (ibridazione sp2 e sp)Può essere un carbonio che fa parte di un anello aromatico
OH
FENOLO
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

Il nome convenzionale di alcoli si costruisce
aggiungendo la desinenza -olo al nome dell’idrocarburo.
Nomenclatura Alcoli
I nomi tradizionali sono ancora in uso.
Regole di nomenclatura IUPAC per gli alcoli con più gruppi ossidrilici
Due gruppi OH DIOLI
Tre gruppi OH TRIOLI
Composti contenenti gruppi ossidrilici su carboni adiacenti possono essere chiamati
GLICOLI
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

CLASSIFICAZIONE DEGLI ALCOLIGli alcoli si suddividono in primari, secondari e terziari, a seconda del numero di residui alchilici (uguali o diversi) uniti al carbonio al quale è legato l’ossidrile.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
NOMENCLATURA DEI FENOLII nomi dei diversi composti aromatici contenenti uno o più gruppi ossidrilici derivano dal più semplice di essi l’idrossibenzene, comunemente chiamato fenolo.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

Gli alcoli sono composti polari
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Proprietà fisiche degli alcoli
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

Principali reazioni degli alcoli
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
C
H
H O HH
OH
H
C
H
H OH O
H
HHpKa 15.5
La costante acida varia in presenza di gruppi elettron-attrattori e di gruppi elettron-repulsori
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Gli alcoli sono acidi molto deboli.
I valori di Ka sono intorno a 1·10-16- 1·10-18
GRUPPI ELETTRON-ATTRATTORI(ALOGENI, NO2)
GRUPPI ELETTRON-DONATORI(GRUPPI ALCHILICI)
AUMENTO DELL’ACIDITA’
DIMINUZIONE DELL’ACIDITA’
ALCOSSIDO
Scaricato da Sunhope.it

C
C
H O HH
F
F F
OH
H
C
C
H OH
F
FF
OH
HHpKa 12.5
Il trifluoroetanolo è un acido più forte dell’etanolo.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Presenza di atomi elettron-attrattori
La presenza dei tre atomi di fluoro stabilizza l’anione trifluoroetanoato.
L’alcossido primario RCH2-O- è più stabilizzato dall’effetto di solvatazione rispetto agli anioni secondari e terziari nei quali l’impedimento sterico dei gruppi alchilici impedisce l’avvicinarsi dell’acqua.
Per questo motivo gli anioni degli alcol secondari e terziari sono più reattivi verso H+ e quindi più basici.
C
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Un acido è tanto più forte quanto più è stabilizzata la sua base coniugata.
Acidità e ingombro sterico
Scaricato da Sunhope.it

Trattando gli alcoli con metalli alcalini si ottengono i loro sali: ALCOSSIDI.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Ricordiamo ancora che:
BASICITA’ CRESCENTE
REAZIONI DI SOSTITUZIONE NUCLEOFILA (SN)Reazione in cui un particolare atomo o gruppo presente nella
molecola (GRUPPO USCENTE) viene sostituito da un altro atomo o gruppo (GRUPPO ENTRANTE)
Reazioni che permettono la sintesi di una larga varietà di molecole organiche fra cui gli alcoli, le ammine, gli esteri, gli eteri etc.
Alcuni composti che sottostanno a questo tipo di reazioni:Alcoli
Composti alogenatiALIFATICI
AROMATICIEsistono due tipi di meccanismi di sostituzione nucleofila
SOSTITUZIONE DEL II ORDINE
(SN2)
SOSTITUZIONE DEL I ORDINE
(SN1)Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Scaricato da Sunhope.it

C
OH
H
R
HH+
C
OH
H
R
H
H
Cl- C
OH
R
H
H H
Cl H2O
C R
Cl
H
H
+
Cl-
R
+
R
+ Cl
R
Cl
R
Reazione di un alcol I° con un acido alogenidrico (HCl)
È UNA SN2
++ Cl-
R2
R1 +
RR3
R2
R1
+R3
R1
R2
+
R3 R2
R1
Cl2 R3
R2
R1
ClR3
L’alcole terziario viene protonato dall’acido
L’alcole terziario protonato perde una molecola di acqua
formando un carbocatione terziario
che può essere attaccato dallo ione cloruro da un lato o dall’altro rispetto al piano diibridazione
CON UN ALCOL TERZIARIO LA REAZIONE CON HCl DECORRE
SECONDO UN MECCANISMO SN1
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Scaricato da Sunhope.it

Quando una SN1e quando una SN2?
La SN1 è favorita da quei reagenti che portano allaformazione di carbocationi più stabili (terziario, a voltesecondario) e dalla presenza di solventi molto polaricapaci di stabilizzare i carbocationi.
La SN2 è favorita da quei reagenti che portano allaformazione di carbocationi meno stabili (primario) edalla presenza di solventi poco polari che non solvatanoefficientemente.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
REAZIONI DI ��-ELIMINAZIONE
Quando si fa reagire con una base forte un alogenuro alchilico che abbia idrogeni in ���si ottiene una reazione di eliminazione che porta alla formazione di un alchene
Si possono scrivere due equazioni generali per la reazione:
OPPURE
H in �Atomo di idrogeno legato al carbonio
adiacente a quello che porta l’alogeno
Scaricato da Sunhope.it

C
O H
H H
C HH
H
C
C H
H
H
HOCr2O7
-- (H+)
Cr+++
etanolo etanale
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
OSSIDAZIONE
MnO4- (H+)
Mn++
CH3
C
CH3
H OH C OH3C
H3C2-propanolo propanone
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

CH3COOH CH3OH CH3COOCH3 H2OH+
FENOLI
�Anche i fenoli, come gli alcoli, formano legami a idrogeno intermolecolari e, quindi, hanno punti di ebollizione elevati.
�La formazione dei ponti idrogeno fra l’ossidrile e l’acqua rende i fenoli moderatamente solubili, nonostante la presenza dell’anello benzenico altamente idrofobo.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

O
pKa 10.0
I fenoli sono acidi più fortidegli alcoli
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
ACIDITA’ DEL FENOLO
Stabilizzazione per risonanza dello ione fenossido rispetto allo ione alcossido
OH
H
OH
HH
O H
O
O
O
O
Strutture di Kekulè
equivalenti
Queste 3 strutture limite delocalizzano la carica negativa
sugli atomi di carbonio dell’anello
OH
Na
O
Na
H22 2 2
CH3OH Na CH3O Na H22 2 2
Sia gli alcoli che i fenoli reagiscono con i metallialcalini dando, rispettivamente, alcolati e fenati.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Sono reazioni redoxScaricato da Sunhope.it

C
H
H OHH
OH
Na
C
H
H OH OH
H
Na
OH
HOH
OH
NaO
Na
NaGli alcoli non reagiscono con gli idrossidi dei metalli alcalini (l’equilibrio è completamente spostato a sinistra),mentre i fenoli si convertono quantitativamente in fenati
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
ETERI
�L’atomo di ossigeno è legato a due residui organici, con carboni ibridati sp3 o sp2.
�I residui possono essere alchilici, vinilici o arilici.
Gruppo funzionale R-O-R gruppo etereo
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

Nomenclatura degli ETERISecondo le regole IUPAC, gli eteri sono individuati con il nome dell’idrocarburo a catena più lunga i cui idrogeni sono sostituiti dal gruppo –O-R, detto gruppo alcossido.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
H+
H H
RC
O
C
H
R
HH
H H
RC
O
C
H
R
H
H HC
R
OH
H+
H2O
RC
O
HH
H
H H
RC
O
C
H
R
HH
H HC
R
OH H
Gli eteri devono essere considerati basi di Lewis: in ambiente acquoso acido sono facilmente protonati ed idrolizzati
protonazione
idrolisiScaricato da Sunhope.it

Gli eterocicli hanno nomi commerciali che sono quelli che si usano comunemente
TIOLI
�I tioli sono composti organici solforati con formula R-S-H
�La nomenclatura IUPAC dei tioli è uguale a quella degli alcoli, ma il suffisso è –tiolo.
�Sono comunemente denominati mercaptani
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

TIOLIProprietà chimico-fisiche
Il gruppo –SH è solo debolmente polare e, pertanto, i legami a idrogeno sono molto più deboli di quelli presenti
negli alcoli.
I tioli hanno punti di ebollizione più bassi rispetto ai corrispondenti alcoli.
Per esempio: l’etanolo bolle a 78,5 °C mentre l’etantiolo bolle a 35°C.
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Sono acidi più forti dei corrispondenti alcoli.
TIOLIReattività
I tioli sono facilmente ossidabili a disolfuri anche in presenza di blandi ossidanti come I2, O2 e H2O2 :
CH3
SH
CH3
SH
CH3
S
CH3
S
-2H
+2H
Metilmercaptano
dimetilsolfuro
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

TIOLIReattività
Per azione di ossidanti energici come HNO3 in forte eccesso, i tioli sono convertiti in acidi solfonici:
OH
O
O
SRxOSHR ����� ���
TIOLOAcido solfonico
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
TIOLI: REAZIONI
�La presenza dello S invece che dell’O nel gruppo SH conferisce ai mercaptani caratteristiche nucleofile più forti di quelle dei corrispondenti alcoli.
�I tioli si addizionano ad aldeidi e chetoni formando tioacetali e tiochetali.
�Con gli alogenuri alchilici, i mercaptani formano i tioeteri
2
1
3
..
....: R
R
R
CSR
H
SR H ������ ���� ��--X
C
XR3
R1 R2
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Tiolo Alogenuro alchilicoTIOETERE
Scaricato da Sunhope.it

CH 3SCH 3dimetil solfuro
I tioeteri vengono denominati come se fossero sali del solfuro di diidrogeno.
TIOETERI
CH3
CH2
CH2
S
C
H
CH3H3C
1-propil 2-propil -solfuro
H
S CH3
ciclopentil metil solfuro
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
TIOETERI
� Sono basi più forti degli eteri, per la maggioredisponibilità dei doppietti elettronici non condivisi presentisull’atomo di zolfo, che è meno elettronegativodell’ossigeno.
� Si addizionano a composti come il clorometano,cloroetano etc., formando composti ionici detti sali disolfonio
��
�����
�����
�
��������� ClCH
CH
SCHClCHCHSCH 3
3
3333 :
Dimetiltioetere + clorometano
Cloruro di trimetilsolfonio
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. SchiraldiScaricato da Sunhope.it

TIOETERI
In presenza di ossidanti sono convertiti dapprima in solfossidi e, per trattamento più energico, in solfoni.
333333 CH
O
O
SCHCHOSCHCHSCH ����� ������ ���� xO
xO
DIMETILTIOETERE DIMETILSOLFOSSIDO DIMETILSOLFONE
Corso di Chimica e Propedeutica Biochimica Proff. M. De Rosa / C. Schiraldi
Scaricato da Sunhope.it