LE PROTEINE · 2017-04-28 · ... che rompono i legami non covalenti (legami a idrogeno, legami...
Transcript of LE PROTEINE · 2017-04-28 · ... che rompono i legami non covalenti (legami a idrogeno, legami...

LE PROTEINE
Le proteine e la loro struttura

Le proteine sono biomolecole.
Le unità base sono gli amminoacidi.
Il legame che si instaura tra due amminoacidi che reagiscono per
condensazione viene detto legame peptidico ed è di tipo covalente.
Alcune catene peptidiche sono tenute insieme dal
legame disolfuro.

CONFORMAZIONE DELLE PROTEINE La struttura di una proteina determina la sua attività biologica.
La sequenza degli amminoacidi è la caratteristica posta sotto il controllo genetico.
STRUTTURA PRIMARIA
La funzione biologica si
manifesta quando la molecola assume una conformazione
spaziale.
STRUTTURA SECONDARIA STRUTTURA TERZIARIA
STRUTTURA QUATERNARIA
α elica
Foglietto β pieghettato
L’ α-elica può ripiegarsi su se stessa.
Alcune proteine sono costituite da due o più catene polipeptidiche (subunità), ciascuna ripiegata nella sua specifica struttura terziaria.

DENATURAZIONE
RINATURAZIONE
e

LA DENATURAZIONE DELLE PROTEINE
La denaturazione delle proteine è un fenomeno chimico, che consiste nel cambiamento della struttura proteica nativa con
conseguente perdita della funzione biologica.

La struttura tridimensionale delle proteine è molto sensibile alle variazioni ambientali estreme di alcuni parametri.
Variazioni di temperatura; Variazione del pH; Radiazioni ionizzanti; Luce ultravioletta; Ioni di metalli pesanti; Solventi organici; Urea; Agitazione meccanica.
AGENTI DENATURANTI

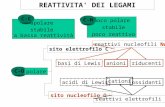
La perdita della funzione biologica e l’alterazione della conformazione della proteina è causata dall’azione degli agenti denaturanti, che rompono i legami non covalenti (legami a idrogeno, legami polari, legami idrofobici) e talvolta i legami covalenti disolfuro della molecola.
IL CALORE aumenta l’energia
cinetica e le vibrazioni delle molecole,
distruggendo in questo modo i legami a
idrogeno.
rompono i ponti salini dovuti alle interazioni elettrostatiche.
Ad esempio:
ACIDI E BASI

LA DENATURAZIONE TERMICA
L'esposizione al calore può causare la variazione delle strutture: quaternaria, terziaria o secondaria. Ciò avviene attraverso la rottura dei legami a idrogeno, dei ponti disolfuro, delle interazioni idrofobiche e ioniche. Nel caso di riscaldamento moderato la denaturazione può essere reversibile.
Denaturazione a caldo
La denaturazione termica può avvenire anche a temperature molto basse, si tratta di un processo generalmente reversibile: innalzando successivamente la temperatura le proteine si ripiegano nuovamente.
Denaturazione a freddo

ESISTONO DUE TIPI DI
DENATURAZIONE: IRREVERSIBILE REVERSIBILE
Nella maggior parte dei casi, le proteine denaturate non
possono tornare a svolgere la loro funzione iniziale.
In alcuni casi, le proteine, come le cheratine, possono riprendere la loro struttura
iniziale.

DENATURAZIONE DELLE PROTEINE DELL’UOVO
Quando la temperatura aumenta fino a circa 65°, le proteine cominciano a srotolarsi. Quando queste denaturate si incontrano si possono legare fra di loro e comincia a formarsi un reticolo tridimensionale, che con il protrarsi dell’aumento di temperatura espelle l’acqua e diventa di consistenza gelatinosa e successivamente gommosa.
L’uovo è composto da: 74% di acqua; 12% di proteine; 11% di grassi.
Si possono immaginare le proteine di questo alimento come dei gomitoli di lana sospesi in acqua.

ESPERIMENTO: DENATURAZIONE DEL LATTE Per questo esperimento occorrono:
Strumenti e materiali: Becher Provette Imbuto Carta da filtro Cucchiaio Bagnomaria Latte Aceto

Si procede mettendo a bagnomaria, circa 100 ml di latte, per 5-10 minuti. Quando il latte si sarà scaldato si aggiungono 5 cucchiai di aceto e si mescola per 4-5 minuti. Si versa a questo punto il miscuglio nell’imbuto con il filtro. Il liquido dovrà raccogliersi nella provetta sottostante. Quando sarà sceso attraverso il filtro tutto il liquido si può osservare il seguente risultato: Lo stesso risultato si può ottenere per decantazione, lasciando il liquido nel becher originale. Una prodotto caseario, simile alla ricotta, può derivare dall’aggiunta di altro aceto alle sieroproteine.
Nell’imbuto si raccoglierà la parte solida del latte che è coagulata per il calore: la
cagliata.
Nella provetta si raccoglierà un
liquido semitrasparente
di colore giallo: le sieroproteine.

RINATURAZIONE
In alcuni casi di denaturazione è possibile avere la ricostituzione della conformazione nativa della proteina.
Si dice allora che la denaturazione è reversibile.
La rinaturazione è la procedura attraverso la quale una proteina che ha perso la sua struttura ritorna al proprio stato nativo.
Per alcune proteine è talvolta possibile, ripristinando le condizioni originarie o rimuovendo l’agente denaturante, ripristinare la struttura
iniziale.

LA CHERATINA
La cheratina è una proteina filamentosa ricca di zolfo, elemento contenuto nei residui amminoacidici di cisteina; è molto stabile e resistente. Si tratta di una struttura secondaria ad α elica. È prodotta dai cheratinociti, ed è immersa nel loro citosol come filamenti intermedi. È il principale costituente dello strato corneo dell'epidermide dei tetrapodi e soprattutto degli amnioti, nei quali garantisce l'impermeabilità.

La tecnica che permette di creare i ricci a partire da capelli lisci, o viceversa, sfrutta la denaturazione della cheratina dei capelli. I ponti disolfuro vengono rotti. La nuova forma del capello è dovuta alla formazione, tramite ossidazione di nuovi legami S-S, in posizioni diverse rispetto a quelle originali.
LA DENATURAZIONE DELLA CHERATINA

A cura di:
COMPAGNONE DILETTA CUOZZO CONCETTA
Liceo Scientifico e Linguistico E.Medi, Battipaglia
Classe II F Indirizzo Scienze Applicate