Corso di Tecniche diagnostiche in ematologia · Sezione “DIDATTICA ” 3 CELLULE CD34+ • 1-2%...
Transcript of Corso di Tecniche diagnostiche in ematologia · Sezione “DIDATTICA ” 3 CELLULE CD34+ • 1-2%...

Corso di
Tecniche diagnostiche in ematologia
• Struttura e funzione del sistema emopoietico
– Inquadramento fisiopatologico
– Tecniche di studio, cliniche e sperimentali
– Trapianto di cellule staminali
• Principali patologie ematologiche
– Inquadramento fisiopatologico
– Approccio diagnostico laboratoristico
– Approcci terapeutici innovatici
• Inquadramento anemie
• Neoplasie Mieloproliferative croniche
• Leucemia mieloide cronica
• Leucemie mieloidi acute
• Malattie linfoproliferative croniche
• Patologie delle piastrine
• Patologie congenite dei fattori della coagulazione
1

Libri di testo
• Non esiste alcun testo specifico consigliato, i seguenti
permettono di estrapolare agevolmente le necessarie
informazioni di fisiopatologia e diagnostica:
– Castoldi G, “Core Curriculum” Ematologia,
McGrawHill, 2009
– Castoldi - Liso, Malattie del sangue, McGrawHill,
2008
– Corradini P, Manuale di Ematologia, Minerva, 2009
2

Il materiale didattico verrà inserito nel sito
• http://www.ematologiafirenze.com
Sezione “DIDATTICA”
3

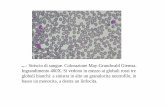
CELLULE CD34+
• 1-2% nel midollo
• 0.05% nel sangue periferico
• 0.3-0.5% nel sangue cordonale
• 0.5-3% nel sangue periferico mobilizzato
• >> in condizioni patologiche (IM)
• LTR dopo terapia mieloablativa
• Proteina transmembrana
• Funzione non nota (adesione?)
• 105-120 kD
• Altamente glicosilata
• 3 epitopi diversi (mAb di tre classi)
• Varianti molecolari 4

VALUTAZIONE DEL SISTEMA EMOPOIETICO
La valutazione morfologica del sistema emopoietico
richiede i seguenti campioni:
SANGUE PERIFERICO
CITOASPIRATO MIDOLLARE
BIOPSIA OSTEOMIDOLLARE
5

• video
6

7

BIOPSIA OSTEOMIDOLLARE ASPIRATO MIDOLLARE
•Citomorfologia
•Reazioni citochimiche
•Reazione Perls
•Organismi intracellulari
•Tesaurociti
•Infiltrati linfocitari
•Infiltrati cellule non-emopoietiche
•Cellularità emopoietica
•Espressione delle diverse
filiere emopoietiche
•Organismi intracellulari-granulomi
•Tesaurismosi
•Infiltrati linfocitari
•Infiltrati cellule non-emopoietiche
•Stroma ed osso
8

9

10

11

Trapianto di
Cellule Staminali Ematopoietiche
Obbiettivo
- Ricostituzione di una normale
funzione ematopoietica alterata da: - Patologia a carico della cellula staminale
emopoietica
- Occupazione del tessuto osseo da parte di
malattia neoplastica
- Controllo della patologia: - Controllo della crescita neoplastica
- Immunoterapia 12

Modalità
Somministrazione di una chemio-radioterapia mieloablativa avente lo scopo di:
-Creare lo spazio midollare per l‟attecchimento del
trapianto (++++Allo; + Auto)
- determinare l‟immunosppressione necessaria per impedire il rigetto del trapianto (++++ Allo)
- Eradicare il clone neoplastico (++ Allo; ++++ Auto)
Infusione per via endovenosa delle CSE
Assistenza e terapia di supporto nel periodo successivo al trapianto
13

TRAPIANTO DI CELLULE STAMINALI EMOPOIETICHE
• Autologo
• Singenico
• Allogenico • Da donatore familiare
• Da donatore non familiare volontario (MUD)
• Aploidentico
•Mieloablativo
•Non-mieloablativo; regimi ad intensità ridotta; “mini-allo”
14

“SORGENTI” DI CELLULE STAMINALI EMOPOIETICHE
• Cellule midollari
• Cellule da sangue periferico [AUTO] – Reclutamento con ciclofosfamide + G-CSF
– Sullo sblocco di un ciclo chemioterapico “convenzionale/alte dosi sequenziali” +G-CSF
• Cellule da sangue periferico [ALLO] – Reclutamento con solo fattore di crescita (G-CSF)
• Cellule da sangue di cordone ombelicale
[cellule espanse ex-vivo] 15

DP
DQ
DR
B
A
E
C
COMPL
TNF-
HeatSP
CLASSE II
CLASSE III
CLASSE I
16

*
*= cromosoma 15 17

CARATTERISTICHE MHC I MHC II
Composizione
complesso MHC-
peptide
Catena polimorfica,
2-MG, peptide
Catene polimorfiche
e , peptide
Tipo di APC Tutte le cellule nucleate APC “professionali”
Cellule T responsive CD8+ (CTL) CD4+ (helper)
Origine dei peptidi Proteine del cytosol Proteine dagli
endosomi/ lisosomi (di
orgine extracellulare)
Sede di generazione
del peptide
proteasomi Endosomi / lisosomi
Meccanismi di
trasporto del peptide
TAP Non necessari
18

Indicazioni al trapianto di cellule staminali
emopoietiche
Auto Allo/MUD
“convenz”
“mini-allo” CB Aploiden.
Emopatie
neoplastiche + + + + +
Emopatie non
neoplastiche -* + - + -
Difetti congeniti
metabolismo -* + + + -/+
Neoplasie solide + -/+ + - -
M. autoimmuni + -/+ -/+ - -
* futuribile: terapia genica
19

-196 °C
20

21

22

- Agoaspirazioni multiple in anestesia generale a
partire dalla cresta iliaca anteriore (1/3) e
posteriore (2/3).
• - Raccogliere non meno di 200-300 milioni di
cellule nucleate/kg di peso corporeo
• - Filtrazione in sala operatoria per rimuovere
microaggregati e spicule ossee.
• - Trasferimento in laboratorio per la
manipolazione.
Raccolta
Trapianto Autologo di Cellule Staminali
Ematopoietiche di origine Midollare
23

Trapianto Autologo di Cellule Staminali
Ematopoietiche di origine Midollare
Manipolazione in Laboratorio • Deeritrocizzazione
• Deplasmazione
• Purging
• T-deplezione
• Selezione positiva e/o negativa
• Valutazione del contenuto in CD34+
• Prove di vitalità
• Prove di clonogenicità
Criopreservazione
24

Trapianto Autologo di Cellule Staminali
Ematopoietiche di origine Midollare
Criopreservazione
- Deeritrocizzazione e concentrazione fino a 200 milioni /ml. - Risospensione in una soluzione di plasma omologo contenete il 10% di Dimetilsulfossido (DMSO crioprotettore). - Congelamento automatico a caduta controllata fino a –120°C. - Stoccaggio delle cellule a temperature di –190°C - - La permanenza in queste condizioni può durare fino ad >>10 anni
25

Trapianto Autologo di Cellule Staminali
Ematopoietiche di origine Midollare
Reinfusione
• Le cellule vengono scongelate in bagnomaria a 37-38°C.
• Una volta scongelate devono essere reinfuse entro 30 minuti per evitare eccesso di mortalità cellulare.
• Prima dell‟infusione il paziente deve essere premedicato con cortisone perché il DMSO può indurre manifestazioni “allergiche”.
• L‟infusione avviene mediante filtro per evitare il passaggio di “clumps” formatisi per attivazione delle DNAasi derivante dalle cellule rotte.
• Durante l‟infusione è necessario monitorare attività cardiaca e respiratoria per scongiurare i rischi connessi con l‟infusione di DMSO soprattutto a dosi superiori ai 2 mg/kg.
26

Trapianto Autologo di
Cellule Staminali Ematopoietiche
di origine dal Sangue Periferico
Vantaggi
eliminazione del rischio anestesiologico
riduzione del rischio di contaminazione neoplastica
attecchimento rapido
Svantaggi
ipotetico rischio promuovente connesso alla somministrazione del G-CSF
rischi trombotici legati alla procedura alla somministrazione del G-CSF 27

Mediante procedura aferetica utilizzando separatori cellulari
dopo:
- Chemioterapia antiblastica:
I farmaci più “mobilizzanti sono la Ciclofosfamide e
l‟Etoposide.
- Chemioterapia + Fattori di Crescita Emopoietici:
Il G-CSF si è dimostrato il più efficace alla dose di 5-10
mcg/kg/di peso corporeo
- Fattori di Crescita Emopoietici (allogenico e autologo)
G-CSF alla dose di 10-16 mcg/kg/di peso corporeo
Trapianto Autologo di
Cellule Staminali Ematopoietiche
di origine dal Sangue Periferico
Modalità di raccolta
28

Trapianto Autologo di
Cellule Staminali Ematopoietiche
di origine dal Sangue Periferico
Modalità di raccolta
• Le raccolte iniziano quando nel sangue periferico sono
presenti almeno 20 cellule CD34+/mcl e ciò avviene
mediamente dopo:
– 10-14 giorni dall‟inizio della chemioterapia
– 5-7 giorni dall‟inizio della somministrazione del G-CSF 29

Trapianto Autologo di
Cellule Staminali Ematopoietiche
di origine dal Sangue Periferico
Modalità di raccolta
- Al momento della raccolta il donatore deve avere almeno 30
di Hct (10 gr di Hb/dL) e 30.000 Plt.
- Se il donatore pesa meno di 25 kg la procedura deve essere
innescata da una unità di GRC isogruppo irradiati e filtrati.
• - Le raccolte procedono fino a quando non siano state
raccolte una quantità di cellule CD34+ sufficienti ad effettuare
il programma trapiantologico e cioè almeno:
2,5 milioni/kg di peso corporeo per ogni
procedura nell‟autologo 30

Vantaggi:
Più rapida disponibilità del donatore
Barriera immunologica immatura
Minor incidenza di GVHD acuta e cronica
Svantaggi:
Ritardo nell‟attecchimento
Ritardato recupero immunologico
Ridotta disponibilità assoluta di progenitori CSE che ne condiziona l‟impiego nell‟adulto
Trapianto Allogenico di Cellule Staminali
Ematopoietiche da sangue placentare
31

Le “fasi” del trapianto autologo
Regime di condizionamento
Infusione di
c. staminali
Aplasia
Recupero della
funzione
emopoietica
Recupero della
funzione
immunologica
-10/-7 0 +15 --- +40 +90 --- >+365
32

Le “fasi” del trapianto allogenico
Regime di condizionamento
Infusione di
c. staminali
Aplasia
Recupero della
funzione
emopoietica
Recupero della
funzione
immunologica
-10/-7 0 +15 --- +40 +180 --- >+365
GVHD acuta
< +100
GVHD cronica
> +100
“graft-failure”
33

Trapianto di
Cellule Staminali Ematopoietiche
Complicanze precoci
Danni indotti dalla chemioterapia
Complicanze infettive
- Batteriche
- Fungine
- Virali
- Protozoarie
Malattia veno-occlusiva epatica
aGVHD
Rigetto
Cistite emorragica
Complicanze polmonari 34

TOLLERANZA
• La tolleranza nel trapianto si definisce
come l‟accettazione di cellule allogeniche
nel contesto dell‟organismo ricevente, in
assenza di terapia immunoppressiva
continuativa
35

GVHD
• ACUTA
– Entro 100 gg dal TMO (..ma non sempre…)
• CRONICA
– Oltre il terzo mese
36

da J Ferrara et al.
37

GRADO CUTE FEGATO INTESTINO
+ Rash maculopapulare,
<25%
Bilirubina, 2-3
mg/dL
Diarrea 500-
1000 ml/die
oppure
Nausea
persistente
++ Rash maculopapulare,
25-50%
Bilirubina, 3-6
mg/dL
Diarrea, 1000-
1500 ml/die
+++ Eritroderma generalizzato Bilirubina, 6-15
mg/dL
Diarrea, >1500
ml/die
++++ Desquamazione e bolle Bilirubina, >15
mg/dL
Dolore
addominale e/o
ileo paralitico
GVHD acuta
38

GvHD ACUTA
CUTE
Clinica Eritema maculopapulare + prurito o
bruciore, con evoluzione in bolle
Istologia Vacuolizzazione cellule basali
Apoptosi dei cheratinociti
Bolle alla giunzione dermoepidermica
Distacco dell„epidermide
39

GvHD ACUTA
GASTROINTESTINALE
Clinica Nausea, vomito
Diarrea acquosa e mucosa
+ sangue, + dolore, fino all„ileo paralitico
Istologia Singole apoptosi nelle cripte
Distruzione di singole cripte
Ulcerazioni focali
Denudazione completa della mucosa
40

GvHD ACUTA
FEGATO
Clinica Colestasi ( bilirubina, ALP, GGT)
Citolisi ( Transaminasi)
VOD
Istologia Ingrandimento e pleomorfismo nucleare, picnosi
nucleare e perdita di nuclei; singole cellule
apoptotiche
. Dedriti cellulari nel lume dei dotti biliari
. Piccoli linfociti negli spazi portali e soprattutto
nell„epitelio dei dotti bilari
. Colestasi generalmente presente
41

GvHD CRONICA
Aspetti clinici
Immunodeficienza combinata umorale e cellulare (la causa + frequente di morte sono le infezioni).
Compromissione della qualità di vita.
Correlazione con GVL.
Istopatologia
Danno cellulare epiteliale
Infiltrato cellulare mononucleare
Fibrosi
Ipocellularità e atrofia del sistema linfoide
42

GvHD CRONICA
• Mucosa Orale: atrofia, eritema, lesioni lichenoidi, slerodermia,
contratture articolari.
• Occhio: cheratocongiuntivite sicca, congiuntivite emorragica, formazione di pseudomembrane, lagoftalmo.
• Polmone: malattia polmonare ostruttiva, dispnea, tosse cronica, bronchiolite obliterante.
• App.Gastrointestinale: disfagia, odinofagia, dismotilità esofagea, perdita di peso.
• Fegato: iperbilirubinemia, ipetrtensione portale, cirrosi, insufficienza epatica.
• App. Neuromuscolare: dolore neuropatico, crampi muscolari, polimiositi
• Miscellanee: m. autoimmuni ( S. Sjogren, SLE, cirrosi biliare primitiva, artrite reumatoide, lichen planus)
43

GvHD CRONICA
44

HOST
HVG --> rejection
GVHD
GVL
GRAFT
45

46

Tecniche per lo studio del
chimerismo
• Cariotipo
• VNTR
• STR
• SNP
47

CHIMERISMO FISH XY
48

CHIMERISMO
Patient
Donor
Mixed chimerism at +30 (PB)
Mixed chimerism at +30 (CD3+)
Full chimerism at +60 (PB)
Full chimerism at +60 (CD3+)
STR
49