ATOMI - scienze.uniroma2.it · sono formati da tre particelle ... filo di molibdeno, oggetto in...
Transcript of ATOMI - scienze.uniroma2.it · sono formati da tre particelle ... filo di molibdeno, oggetto in...

ChimicaGenerale_lezione2 1
ATOMI
Dalton formulò la sua teoria atomica avvalendosi delle conoscenze chimiche che possedeva:
➢ la legge della conservazione della massa (di Lavoisier) ➢ la legge delle proporzioni definite (di Proust)
Solo all'inizio del XIX secolo J. Dalton propose la teoria atomica moderna

ChimicaGenerale_lezione2 2
Legge della conservazione della massa
in un sistema chiuso: in una reazione chimica, la massa dei reagenti è esattamente
uguale alla massa dei prodotti
nulla si crea, nulla si distrugge, ma tutto si trasforma

ChimicaGenerale_lezione2 3
Legge delle proporzioni definite
quando due o più elementi reagiscono, per formare un determinato composto, si combinano sempre secondo proporzioni in massa definite e costanti
Secondo Proust, "...un composto è un prodotto privilegiato al quale la natura ha dato una
composizione costante".
Esempio: carbonato di rame, CuCO3, naturale o preparato in laboratorio,
contiene rame, carbonio e ossigeno sempre nelle stesse proporzioni.

ChimicaGenerale_lezione2 4
La teoria atomica di Dalton la materia è formata da piccolissime particelle
indivisibili e indistruttibili (gli atomi) che non possono essere né create né distrutte
gli atomi di uno stesso elemento sono tutti uguali tra loro
gli atomi di un elemento non possono essere convertiti in atomi di altri elementi
gli atomi di elementi diversi si combinano tra loro in rapporti di numeri interi e generalmente piccoli, dando così origine a composti

ChimicaGenerale_lezione2 5
Legge delle proporzioni definite
In un dato composto, gli elementi che lo costituiscono sono sempre
combinati nelle stesse proporzioni in peso, indipendentemente dall’origine e dal metodo di preparazione.
H2 + Cl
2 → 2 HCl

ChimicaGenerale_lezione2 6
Legge proporzioni multipleSe due elementi formano più di un composto,
i vari pesi di uno di essi che si combinano con lo stesso peso dell’altro
stanno nel rapporto di numeri interi piccoli.
N2O , NO , NO2
16 grammi di ossigeno si combinano rispettivamente con 28, 14, 7 grammi di azoto.Rapporto 4 : 2 :1

ChimicaGenerale_lezione2 7
Problema per i chimici dell’800: come determinare i pesi atomici e le formule molecolari simultaneamente
Gay-Lussac (1808)i volumi delle sostanze che si combinano (P,T costanti) stanno tra loro in rapporto di numeri interi semplici.
NH3 (g)
+ H2CO
3 (aq)
→ NH4HCO
3(aq)
2 NH3 (g)
+ H2CO
3 (aq)
→ (NH4)
2CO
3(aq)
Rapporto 1:2 (valida la legge delle proporzioni multiple)

ChimicaGenerale_lezione2 8
AvogadroIntuizione: gli atomi in fase gassosa possono essere molecole biatomiche!
azoto + ossigeno → ossido di azoto1 volume + 1 volume → 2 volumin molecole + n molecole → 2n molecole N2 + O2 → 2NO
2H2 + O2 → 2 H2O

ChimicaGenerale_lezione2 9
Cannizzaro (1858)
Ogni molecola contiene un numero intero di atomi di ogni elemento.
Ax B
y C
z
HClO HClO2
HClO3
HClO4

ChimicaGenerale_lezione2 10
facendo uso del principio di Avogadro…
“…nelle stesse condizioni di pressione e temperatura volumi uguali di gas contengono lo stesso numero di molecole, le masse di questi volumi devono stare tra loro come le masse delle molecole, ovvero come i pesi molecolari”.
Con questo insieme di pesi molecolari relativi, Cannizzaro definì che il peso molecolare dell’idrogeno doveva essere 2 e fissò i valori dei pesi molecolari assoluti degli altri elementi.
Il riferimento attuale è il peso del 12C che è definito esattamente 12.

ChimicaGenerale_lezione2 11
Elettroni, protoni e neutroni
Gli atomi, quindi tutta la materia, sono formati da tre particelle fondamentali: gli elettroni, i protoni ed i neutroni.Le masse del protone e del neutrone sono quasi uguali, mentre la massa dell’elettrone è molto più piccola.La carica del neutrone è nulla. La carica dell’elettrone è uguale a quella del protone, ma di segno contrario.

ChimicaGenerale_lezione2 12
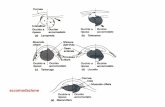
Struttura dell’atomo
L’atomo è soprattutto spazio vuoto!
La figura non è in scala: se il nucleo fosse di queste dimensioni la nube elettronica si estenderebbe per 200m!

ChimicaGenerale_lezione2 13
Proprietà delle particelle atomiche

ChimicaGenerale_lezione2 14
Numero Atomico “Z”
La carica netta di un atomo è zero, quindi il numero di protoni e di elettroni è uguale.
Il numero atomico “Z” di un elemento è definito come il numero di protoni
presenti nel nucleo.

ChimicaGenerale_lezione2 15
Numero di massa AIl numero di massa A è pari alla somma delle masse di tutti i protoni e neutroni presenti in un atomo
Quando di un elemento si vuole specificare il numero di massa, lo si scrive in alto (in posizione apice), a sinistra del simbolo chimico
AZX→simbolo elemento

ChimicaGenerale_lezione2 16
Esempio
Qual'è numero di massa di un atomo di fosforo con 16 neutroni? Se l'atomo ha una massa effettiva di 30.9738u,
qual'è la sua massa in grammi? Qual'è la massa dell'atomo di fosforo
relativamente a quella del carbonio con numero di massa 12?

ChimicaGenerale_lezione2 17
Gli atomi di P hanno 15 protoni (ricavabile da numero atomico Z); quindi posso ricavare il numero di massa pari a protoni + neutroni: (15+16)= 31
La massa dell'atomo in grammi si ottiene usando il fattore di conversione
1u = 1.66054 x 10-24 gmassa31P=(30.9738u) x (1.66054 10-24 g/u)= 15.14332 x 10-23 g La massa rispetto al carbonio sarà
30.9738/12.0000=2.58115ovvero l'atomo di fosforo-31 è 2.58115volte più pesante del carbonio-12.

ChimicaGenerale_lezione2 18
Elementi Ioni ed Isotopi Ad ogni numero atomico corrisponde un
diverso elemento chimico. In un atomo neutro il numero atomico è pari
anche al numero di elettroni; in caso contrario l'atomo è detto ione.
Atomi aventi stesso numero atomico ma diverso numero di neutroni (quindi diverso numero di massa A) sono detti isotopi.

ChimicaGenerale_lezione2 19
Abbondanza Isotopica %
(Numero atomi di un isotopo)
(Numero totale atomi di tutti isotopi dell'elemento)

ChimicaGenerale_lezione2 20

ChimicaGenerale_lezione2 21
Peso AtomicoDa dati sperimentali risulta evidente che ogni elemento ha una sua massa e che questa è relativa agli altri elementi.In base a questo è possibile definire una scala relativa delle masse atomiche.
Viene introdotta una scala di pesi atomici relativi basati sull’unità di massa atomica (uma) che è chiamata anche peso atomico.

ChimicaGenerale_lezione2 22
umal’unità di massa atomica viene definita come
1/12 esatto della massa di un particolare atomo di carbonio,
chiamato carbonio-12
In questa scala, il peso atomico dell’idrogeno è 1.00794 uma, quello del sodio 22.989768 uma.

ChimicaGenerale_lezione2 23
Peso atomico e abbondanza isotopica
La massa atomica di un elemento è sempre più vicino alla massa dell'isotopo
più abbondante.
Peso Atomico = [(abbondanza% dell'isotopo1)/100] x (massa isotopo1)+[(abbondanza% dell'isotopo2)/100] x (massa isotopo2) +.....

ChimicaGenerale_lezione2 24
Esempio
Il bromo ha 2 isotopi : uno con massa 78.918338 u e abbondanza 50.69%, l'altro di massa 80.916291 u con abbondanza 49.31%. Calcola peso atomico del bromo.
Peso atomico del bromo = [(50.69/100) x 78.918338] + [(49.31/100) x 80.916291] =79.90

ChimicaGenerale_lezione2 25

ChimicaGenerale_lezione2 26
Tavola Periodica degli elementi
La tavola periodica degli elementi
è lo schema con il quale vengono
ordinati gli elementi sulla base del
loro numero atomico Z.

ChimicaGenerale_lezione2 27
Tavola periodica di Mendeleev
Ideata dal chimico russo Dimitrij Mendeleev nel 1869,
contemporaneamente ed indipendentemente dal
chimico tedesco J. L. Meyer, inizialmente contava
numerosi spazi vuoti, previsti per gli elementi che
sarebbero stati scoperti in futuro, alcuni nella seconda
metà del 1900. Si basava sui pesi atomici, poichè il
concetto di numero atomico divenne chiaro solo agli
inizi del XX secolo.

ChimicaGenerale_lezione2 28
Gruppi e Periodi

ChimicaGenerale_lezione2 29
Gruppi
Ogni gruppo (colonna) della tabella comprende gli elementi che hanno la
stessa configurazione elettronica esterna: all'interno di ogni gruppo si trovano elementi con caratteristiche
chimiche simili

ChimicaGenerale_lezione2 30
I e II Gruppo:
metalli alcalini e alcalino-terrosi

ChimicaGenerale_lezione2 31
Gruppo 4
Carbonio (in basso)Silicio (centro a sin)Stagno (centro dx)Piombo (in alto)

ChimicaGenerale_lezione2 32
Gruppo 5
N e P non metalliAs e Sb semimetalliBi metallo

ChimicaGenerale_lezione2 33
Gruppo 7
Cloro (gassoso, a sin); bromo (liquido, al centro);
iodio (solido, a dx)

ChimicaGenerale_lezione2 34
Ogni periodo (riga) della tabella inizia con un elemento il cui atomo ha
come configurazione elettronica esterna un elettrone di tipo s, e procedendo verso gli atomi
successivi nel periodo, il numero atomico Z aumenta di una
unità ad ogni passaggio.
Periodi

ChimicaGenerale_lezione2 35

ChimicaGenerale_lezione2 36
Regioni
Metalli Metalli di transizione
MetalloidiNon metalli
Metalli: solidi, duttili malleabili, conduttori di calore ed elettricità
Metalloidi: ambiguità di comportamento
Non metalli: solidi gassosi o liquidi, non conduttori (eccezione per carbonio-grafite)

ChimicaGenerale_lezione2 37
Metalli: filo di molibdeno, oggetto in bismuto, grani di rameNon metalli: Bromo liquido, iodio solidoMetalloidi: silicio

ChimicaGenerale_lezione2 38
Le MolecoleLa molecola è la parte più piccola di un elemento o di un composto che può esistere libera e stabile in natura
Modelli in scala approssimativa delle molecole diatomiche

ChimicaGenerale_lezione2 39
Modello Molecole
Molecole di fosforo bianco P4
Molecole di zolfo rombicoS8

ChimicaGenerale_lezione2 40

ChimicaGenerale_lezione2 41
Le Formule Chimiche
La formula chimica di una sostanza descrive la sua composizione chimica
Riporta il tipo di atomo
e il numero di essi presenti
AxB
yC
z

ChimicaGenerale_lezione2 42
Formule Molecolari e Formule di Struttura
La formula molecolare fornisce il numero di atomi di ciascun tipo all’ interno della
molecola.La formula di struttura evidenzia la
connessione tra gli atomi.
I trattini che uniscono i simboli degli atomi rappresentano i legami chimici.I legami sono forze che uniscono gli atomi a distanze e angoli caratteristici.

ChimicaGenerale_lezione2 43

ChimicaGenerale_lezione2 44
Formule e modelli strutturaliBall-and-stick mette in evidenza la struttura 3D e i legami delle molecole, con sfere di colore diverso per i diversi atomi;
Space-filling mostra le dimensioni relative di atomi e la forma della molecola.

ChimicaGenerale_lezione2 45
Il metano CH4

ChimicaGenerale_lezione2 46
I Composti IoniciAlcuni composti come “NaCl” sono formati da un raggruppamento di ioni.
Ioni sono atomi o gruppi di atomi con carica elettrica
Cationi, ioni positivi, da atomi che tendono a cedere e-( es. Na+)
Anioni, ioni negativi, da atomi che tendono ad acquisire e-(es. Cl-)

ChimicaGenerale_lezione2 47

ChimicaGenerale_lezione2 48
Catione o anione?Un atomo di un elemento formerà preferenzialmente un catione o un anione?
I metalli generalmente cedono elettroni formando cationi
I non metalli frequentemente acquistano uno o più elettroni dando origine agli anioni

ChimicaGenerale_lezione2 49
Ioni
Li→Li++e-
e-+F→F-

ChimicaGenerale_lezione2 50
Ioni monoatomici- Metalli
I metalli dei Gruppi 1A-3A formano ioni positivi con carica pari al gruppo di appartenenza Gruppo 1A Na -1e- → Na+
Gruppo 2A Ca -2e- → Ca2+
Gruppo 3A Al -3e- → Al3+
I metalli di transizione formano cationi, ma il comportamento non è facilmente prevedibile.

ChimicaGenerale_lezione2 51
Ioni monoatomici-non metalli
I non metalli formano spesso ioni con carica negativa pari al (n°del gruppo-8)
5A N(7p 7e-) +3e- → N3-(7p 10e-) 6A S(16p 16e-) +2e- → S2-(p 16 18e-) 7A Br(35p 35e-) +1e- → Br-(35p 36e-)

ChimicaGenerale_lezione2 52
Cariche di cationi e anioni monoatomici

ChimicaGenerale_lezione2 53
Ioni Poliatomici
Gli ioni poliatomici sono costituiti da 2 o più atomi e l'insieme possiede carica
elettrica
NH4+, catione ammonio
CO32- , anione carbonato

ChimicaGenerale_lezione2 54

ChimicaGenerale_lezione2 55
Esercizio
Scrivere gli ioni presenti in: Li
2CO
3
Fe2(SO)
4
CaCl2
Ca3(PO
4)
2
Scrivere la formula di : anione floruro, nitrato, solfuro

ChimicaGenerale_lezione2 56
Nomi dei composti ionici
Nella formula il catione precede l'anione
Nella lettura l'anione è seguito dalla specificazione del catione
CaBr2
bromuro di calcio

ChimicaGenerale_lezione2 57
Alcuni Composti Ionici

ChimicaGenerale_lezione2 58
Proprietà dei composti ionici
Legge di Coulomb : Fattraz
= K (n+e)(n-e)
d2
In base alla legge di Coulomb la forza di attrazione tra ioni con carica opposta aumenta con
L'aumento di carica dello ione La diminuzione di distanza tra ioni

ChimicaGenerale_lezione2 59

ChimicaGenerale_lezione2 60
Proprietà strutturali
La struttura reticolare propria dei composti ionici è responsabile di:
Stato solido
Durezza

ChimicaGenerale_lezione2 61
Fratture nei solidi ionici
Un colpo sul cristallo avvicina ioni di carica uguale: la repulsione causa la rottura del cristallo.

ChimicaGenerale_lezione2 62
Composti MolecolariSebbene molte sostanze abbiano una formula chimica associata, non sempre tali sostanza sono costituite da molecole.Molte sostanze comuni sono composte da molecole (l'acqua, lo zucchero da tavola, i gas che costituiscono l'aria), mentre altre sostanze altrettanto comuni non lo sono (il sale è un composto ionico, per esempio).
saccarosio

ChimicaGenerale_lezione2 63
Composti molecolari binari (2 elementi)
Molti composti molecolari binari sono combinazione tra elementi dei gruppi 4A-7A,o tra questi e l'idrogeno.
La formula è scritta elencando gli elementi in ordine crescente
Nella pronuncia viene prima l'elemento maggioritario con il giusto prefisso
NF3 trifloruro d'azoto

ChimicaGenerale_lezione2 64
Nomenclatura composti non ionici
Scrivere la formula di
Biossido di carbonio Dicloruro di zolfo Trifluorurodi boro Triossido di fosforo