ACUTE - ematologia.unito.it · LEUCEMIE ACUTE Neoplasie ematologiche caratterizzate da accumulo,...
Transcript of ACUTE - ematologia.unito.it · LEUCEMIE ACUTE Neoplasie ematologiche caratterizzate da accumulo,...
LEUCEMIE ACUTE
Neoplasie ematologiche caratterizzate daaccumulo, nel midollo e nel sangue periferico,di cellule indifferenziate (blasti) e carenza dicellule ematiche mature.
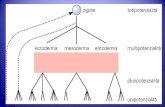
Leucemie acute mieloidi: origine da cellulastaminale pluripotente o, più raramente, daprogenitore granulo-monocitopoietico.
Leucemie acute linfoidi: origine daprogenitore B o T linfocitario, più raramenteda cellula staminale pluripotente
LEUCEMIE ACUTE MIELOIDI
- Più frequenti nell’ età adulta (mediana circa 60anni). Incidenza globale: circa 4 / 105 / anno,che aumenta con l’età.
- Primitive o secondarie a malattiamieloproliferativa cronica o sindromemielodisplastica.
- Eziologia sconosciuta in molti casi.
- In alcuni casi secondarie ad esposizione amutageni ambientali (radiazioni, benzene, altrisolventi organici, fumo tabacco, pesticidi) oterapeutici (citostatici).
LEUCEMIE ACUTE LINFOIDI
- Incidenza maggiore in età pediatrica (2-10 anni); piùrare nell’ adulto, ma aumentano dopo i 50 anni.
-Di solito primitive, ad eziologia ignota,probabilmente diversa secondo le età:
possibile esposizione a carcinogeni ambientali durantela vita fetale per le forme neonatali (1° anno);
probabili errori nel riarrangiamento geni Ig e recettoreT nelle forme dell’ infanzia – adolescenza;
carcinogeni ambientali per le forme dell’ adulto?
LEUCEMIE ACUTE
Cellule staminalio progenitori
Espansione diun clone
Alterazionegenetica
Ulteriorealterazionegenetica
Perdita differenziazioneUlteriore espansione
LEUCEMIE ACUTE
Cellula staminale leucemica
Progenitori leucemici
Blasti immaturi ±±rare celluledifferenzianti
LEUCEMIE ACUTE MIELOIDI
ALTERAZIONI GENETICHE (1)
Cromosomiche:-Traslocazioni bilanciate: t(8;21); inv.16; t(15;17);nelle LAM; t(11q…) nelle LAM e LAL; t(1;19) nelleLAL; t(9;22)(Ph1) nella LMC e nelle LAL:
comportano formazione di geni ibridi e produzionedi proteine di fusione che interferiscono con latrascrizione di geni regolanti differenziazione,proliferazione, e apoptosi.
LEUCEMIE ACUTE
ALTERAZIONI GENETICHE (2)
Cromosomiche:-Traslocazioni bilanciate:
t(8;14); t(5;14); t(9;14)… nelle LAL
Traslocano un gene codificante per fattori ditrascrizione che regolano la proliferazione sul“promoter” dei geni codificanti le catene delleimmunoglobuline (nelle LAL B ) o del recettoredei T linfociti (nelle LAL T) che sono iperattivi:
deregolazione trascrizionale
LEUCEMIE ACUTE
ALTERAZIONI GENETICHE (3)
Cromosomiche-Delezioni: -5; 5q-, -7;…. (nelle LAM):perdita di geni oncosoppressori.
-Trisomie: +8; +21…(nelle LAM) e
-Iperploidie (nelle LAL): amplificazionegenica.
LEUCEMIE ACUTE MIELOIDI
ALTERAZIONI GENETICHE (4)
Mutazioni geniche:
- mutazioni puntiformi o duplicazioni su geni checodificano per recettori di fattori di crescita oproteine che trasmettono i segnali proliferativi:FLT3, Kit, ras,…
Attivazione permanente del segnale proliferativo
- mutazioni puntiformi o delezioni su genioncosoppressori: p53, …. (perdita funzionale)
LEUCEMIE ACUTE
SINTOMI E SEGNI DI CARENZACELLULE MATURE
Anemia: astenia, dispnea da sforzo, pallore,tachicardia, edemi declivi.
Granulocitopenia: febbre, infezioni recidivanti.
Piastrinopenia: gengivorragie, epistassi,petecchie, ecchimosi.
LEUCEMIE ACUTE
SINTOMI E SEGNI DI ESPANSIONE DELCLONE NEOPLASTICO:
- dolori o tensione addominale per splenomegaliae/o epatomegalia;
- dolori ossei per espansione midollare;
- adenopatie superficiali e/o profonde (in LAL);
- cefalea, rachialgie, paralisi nervi cranici perinvasione liquor c.s. (rara, più frequente in LAL).
LEUCEMIE ACUTE
DIAGNOSI
Morfologica: esame al microscopio dello striscio disangue periferico e midollare ±biopsia ossea: blasti > 20% nel midollo o > 10% nelsangue periferico.
Colorazioni citochimiche per caratterizzare i blasti.
Immunologica: impiego di anticorpi monoclonali chericonoscono antigeni di differenziazione e linea-specificiper caratterizzare i blasti.
Citogenetica e molecolare: evidenza di anomaliecromosomiche e genetiche che caratterizzano sottotipi adiversa prognosi e terapia.
LEUCEMIE ACUTE MIELOIDISOTTOTIPI MORFOLOGICI
M0: mieloblastica indifferenziata, identificabilesolo con anticorpi monoclonali.
M1: mieloblastica senza maturazione: < 10%cellule granulopietiche maturanti.
M2: mieloblastica con maturazione: cellulegranulopoietiche maturanti > 10%.
M3: promielocitica: cellule leucemiche di aspettosimil- promielocita; alterazione citogenetica emolecolare tipica.
LEUCEMIE ACUTE MIELOIDI
SOTTOTIPI MORFOLOGICI
M4: mielo-monocitica: 20 - 80 % cellulemonocitoidi.
M5: monocitica: cellule monocitoidi > 80 %
M6: eritroleucemia: eritroblasti > 50%
M7: megacarioblastica: blasti precursorimegacariocitari, identificabili con anticorpimonoclonali o con microscopia elettronica.
DIAGNOSI LAM
Colorazioni citochimiche:POSITIVE le colorazioni per mieloperossidasi eSudan Nero (M1 – M4) o esterasi non-specifica(M4, M5).
Tipizzazione immunologica: espressioneantigeni di linea granulo-monocitopoietica(mieloperossidasi, CD33, CD13) ± antigeni dicellule immature (CD34).
DIAGNOSI DI LAL
Colorazioni citochimiche:NEGATIVE le colorazioni per mieloperossidasi,Sudan Nero, esterasi non-specifica .
Tipizzazione immunologica: espressioneantigeni precoci di linea B o T linfocitaria (CD19,CD10, Tdt, CD2) ± antigeni di cellule immature(CD34); assenza antigeni di linfociti maturi.
SOTTOTIPI IMMUNOLOGICI DILAL
LINEA B LINFOCITARIA
Pro – B: CD19 +, CD34 +, CD10 - ;
Common: CD19 +, CD34 +, CD10 + ;
Pre – B: CD19 +, CD10 +, catene µ citopl. + ,CD34 ± ;
B mature: CD19 +, CD 20 +, Ig +, CD34 -
SOTTOTIPI IMMUNOLOGICI DILAL
LINEA T LINFOCITARIA
Pre – T: CD 7 +, CD 34 +, CD3 citoplasmat. +,CD2 - ;
T : CD7 +, CD3 citoplasm +, CD2 +, CD34 ±
TERAPIA LEUCEMIE ACUTE
TERAPIA CITOSTATICA DI INDUZIONE
aplasia midollare TERAPIA DI
SUPPORTO
rigenerazione emopoiesi
remissione completa
TERAPIA POST- REMISSIONE
CHEMIOTERAPIA LEUCEMIE ACUTEINDUZIONE
• LAM Citosina arabinoside
(ARA-C) +daunorubicina oidarubicina omitoxantrone ±±etoposide o 6-tioguanina
• LAL• Vincristina +prednisone +
asparaginasi ±±daunorubicina
PROFILASSI MENINGEA
Metotrexate intra-rachide ±± Radioterapia cranica
TERAPIA DI SUPPORTOTRASFUSIONI: eritrociti se Hb < 8 g /dl; piastrine sevalore < 10- 20.000 /ul o diatesi emorragica; plasma secoagulazione intravasc. disseminata.
PROFILASSI ANTI-INFETTIVA: isolamento, cibisolo cotti, antibiotici e anti-micotici orali.
TERAPIA ANTI-INFETTIVA: indaginibatteriologiche (emocultura) e inizio precoce terapiaantibiotica e.v. ad ampio spettro e a dosi piene in caso difebbre. Terapia anti-micotica e.v. se persiste febbre dopo3 giorni di antibiotici.
ANTI-EMETICI, IDRATAZIONE E NUTRIZIONEPARENTERALE durante e dopo la chemioterapia.
TERAPIA POST-REMISSIONE LAM
CONSOLIDAMENTO
-Uno o due cicli come induzione o con ARA-C adalte dosi;
±±-Trapianto di midollo allogenico (se donatoreHLA-compatibile) o autologo se età < 60
TERAPIA POST-REMISSIONE LAL
CONSOLIDAMENTOCicli di ARA-C ad alte dosi + mitoxantrone o etoposide ociclofosfamide.
MANTENIMENTOTerapia continua (2-3 anni) con 6-mercaptopurina orale +metotrexate settimanale ± cicli di vincristina + prednisone+ daunorubicina o ciclofosfamide.
TRAPIANTO ALLOGENICONei casi a prognosi sfavorevole, se donatore compatibile
RISULTATI TERAPIA LAM(NON M3)
REMISSIONE COMPLETA
65 - 80 % dei pazienti < 60 anni10 – 20 % di casi resistenti, 10% mortalità in induzione;
40 – 60 % nei pazienti > 60 anni (se non patologieassociate)
20 – 30 % di casi resistenti e di morti in induzione.
Se NON remissione completa, sopravvivenza 1- 4 mesi.
RISULTATI TERAPIA LAM( NON M3)
REMISSIONE A LUNGO TERMINE20 – 60 % se età < 60 (secondo fattori prognostici)
< 10 % se età > 60
SE RECIDIVA: chemioterapia con ARA-C ad alte dosi +idarubicina o mitoxantrone, poi trapianto, se possibile:
40 - 60 % di seconde remissioni (< 60 anni);
10 -30 % di remissioni a lungo termine; negli altri casisopravvivenza < 1 anno dopo la recidiva.
RISULTATI TERAPIA LAL
• BAMBINI• Remissione completa:
>.90 %• Remissione a lungo
termine (> 5 anni):50 – 80 % secondo fattoriprognostici
ADULTIRemissione completa:70 – 80 %Remissione a lungo
termine (> 5 anni):< 10 – 50 % secondofattori prognostici
SE RECIDIVA: ARA-C alte dosi + idarubicina, metotrexate altedosi + corticosteroide: 50 - 60 % di seconde remissioni. Poitrapianto, se possibile.
Remissioni a lungo termine: 20 – 30 % nei bambini, < 10% negliadulti. Negli altri casi sopravvivenza < 1 anno.
FATTORI PROGNOSTICI LAM
CARIOTIPO: prognosi migliore se t(15;17) (M3),t(8;21), inv.16;
prognosi pessima se -5, -7, t(3;21), anomalie multiple.
ETA’: prognosi migliore nei giovani, pessima se > 60.
MALATTIA SECONDARIA: prognosi pessima seLAM secondaria a precedente mal. mieloproliferativacron. o sindr. mielodisplastica o precedente esposizione acitostatici o benzene o radiazioni ionizz. LEUCOCITOSI:prognosi migliore se GB < 10.000 /ul,
peggiore se > 50.000 /ul.
RISPOSTA AL 1° CICLO: prognosi peggiore se nonremissione con il 1° ciclo.
FATTORI PROGNOSTICI LAL
CARIOTIPO: prognosi pessima se t (9;22) (gene difusione BCR/ABL), t (11q;…); migliore se iperdiploide.
ETA’: prognosi migliore tra 2 e 10 anni, poi peggioraprogressivamente.
TIPO IMMUNOLOGICO: prognosi peggiore le pre-Te pro-B, migliore le “common”.
MASSA NEOPLASTICA: prognosi migliore se GB <10.000 /ul e non organomegalie, peggiore se GB >50.000 / ul o grosse adenopatie.
SESSO: prognosi un po’ migliore nelle bambine.
LEUCEMIA ACUTAPROMIELOCITICA ( M3)
5 % di LAM; più frequente nei giovani adulti.
Presenta, in oltre il 98 % dei casi fusione dei geni PMLe RARα (codifica per recettore nucleare di acidoretinoico), dovuta a traslocazione cromosomica 15;17.
Alla diagnosi è costante un quadro di coagulazioneintravascolare disseminata (C.I.D.), almeno sub-clinica.
Frequente la diatesi emorragica per piastrinopenia eC.I.D.
Diagnosi sospettata per morfologia, citochimica,antigeni (spesso CD34-), confermata da dimostrazionedel gene ibrido PML/RARα o da t (15;17).
LEUCEMIA ACUTAPROMIELOCITICA ( M3)
Le cellule di LAP differenziano in vitro e in vivoin presenza di concentrazioni farmacologiche diacido trans-retinoico (ATRA).
L’ aggiunta di ATRA alla chemioterapia haradicalmente cambiato la prognosi:
Remissione complete: 90 – 95%
Remissioni a lungo termine: 70 – 80%