Acidi e e Basi - edadda.it · Alcani. 2 Lezioni di Chimica ... Tipiche geometrie ed ibridizzazioni...
Transcript of Acidi e e Basi - edadda.it · Alcani. 2 Lezioni di Chimica ... Tipiche geometrie ed ibridizzazioni...

1Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
IdrocarburiIdrocarburiIdrocarburi
Molecole costituite solo da atomi di carbonio e idrogeno
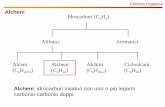
Idrocarburi alifatici
Idrocarburi saturi, solo legami singoli.
Idrocarburi aromatici
Idrocarburi insaturi, almeno un legame multiplo carbonio-carbonio
Alcheni:doppio legame C = C
Alchini:triplo legame C ≡ C
Alcani

2Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Tipiche geometrie ed ibridizzazioni del carbonio negli idrocarburi
Alcano Alchene Alchino AromaticoGeometria Tetraedrica Planare Lineare PlanareIbridizzazione sp3 sp2 sp sp2
Esempio:nome Propano Propene Propino TolueneFormulamolecolare C3H8 C3H6 C3H4 C7H8
Formula distruttura
C C
H
H
H C
H H
H
H
H
C C
H
H
C
H
H
H
H C C C
H
H
H
H
CC
C
C C
C
H
H
H
H
H HH
H

3Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano

4Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Idrocarburi ramificati
CH3
CH3
CH3
H HHCH3
CH3
CH3CH3
H H
HH
CH3 CH3
CH3
CH3
H
H
H
H
C C C
C CH3
C2H5
C
CH3
CH3
H
H
CH2
CH3
Idrocarburi Idrocarburi ramificatiramificati

5Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
C6 - C12
C11 - C16
C14 - C18
C15 - C25(olii lubrificanti)
e oltre.
Distillazione frazionata
del petrolio
Distillazione Distillazione frazionata frazionata
del petroliodel petrolio

6Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Isomeri conformazionali: esempio del n-butano: C4H10
Isomeri Isomeri conformazionaliconformazionali: : esempioesempio deldel nn--butanobutano: C: C44HH1010
CH3 H
HH
HCH3 H
CH3H
CH3
HH
CH3
CH3HH
HH
CH3H
CH3
H
H
H
H
CH3
H
H
H
CH3H
CH3
H
H
H CH3
Sgemba (C, E)
H
CH3
H
H
H
CH3
HHH
HH
HH
HH
H
4La conformazione anti è più stabile della conformazione sghemba di 0.9 kcal/mole. A temperatura ambiente il butano è al 72% in forma anti e al 28% in forma sghemba.
4Le due forme sono separabili a -230°C.
Anti (A) Eclissata (B) Eclissata (D)

7Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Composti ciclicici: anelli a 6 atomi di carbonio
Composti Composti cicliciciciclicici: : anellianelli a 6 a 6 atomiatomi didi carboniocarbonio
CicloesanoCicloesano
H
H
H
H
H
HH
H
H
H
H
H
Conformazioni a sedia Conformazione a barca
CicloeseneCicloesene AdamantanoAdamantano

8Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Energie conformazionali di alcuni cicloesani monosostituiti
4A causa delle interazioni steriche tra un gruppo in posizione assiale e gli idrogeni assiali, generalmente, le conformazioni equatoriali risultano più stabili delle corrispondenti conformazioni assiali.
4Il metilcicloesano, ad esempio, a 25°C è presente circa al 95% nella forma equatoriale.

9Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Importanza della giunzione:esempio amido - cellulosa
Importanza della Importanza della giunzionegiunzione::esempio esempio amidoamido -- cellulosacellulosa
4La polimerizzazione dell’una o dell’altra forma porta a due composti significativamente diversi: l’amido e la cellulosa.
unitàunità moltosiomoltosio
amidoamido
unità unità cellobiosiocellobiosio
cellulosacellulosa
4Il glucosio è uno zucchero che nella sua forma ciclica assume la tipica conformazione a sedia degli anelli a sei atomi. A seguito della ciclizzazione si genera un nuovo centro chirale in C1.
4La posizione assiale o equatoriale del gruppo OH su C1, determina le forme αo β del monosaccaride.

10Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Atomo di carbonio primari, secondari, terziari e quaternari.
Atomo di carbonio Atomo di carbonio primari, primari, secondari, terziari e quaternari.secondari, terziari e quaternari.
4L’atomo di carbonio si dice:4primario quando legato ad un solo atomo di carbonio4secondario quando legato a due atomi di carbonio4terziario quando legato e tre atomi di carbonio4quaternario quando legato a quattro atomi di carbonio
Energie di dissociazioneEnergie di dissociazione per alcuni per alcuni alcanialcani
CH3
CH3
CH3CH3
H H
HH
quaternario
secondario
primario
primario

11Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Alogenazione degli alcaniAlogenazione Alogenazione degli degli alcanialcani
CHCH33CHCH22CHCH33 + Br+ Br22 CHCH33CHCH22CHCH22Br + (CHBr + (CH33))22CHBrCHBrhν
1-Br-propano (8%) 2-Br-propano (92%)Stadio di iniziazione:Stadio di iniziazione:Br2 2Br·
Stadi di propagazione:Stadi di propagazione:1) C3H8 + Br · C3H7· + HBr2) C3H7· + Br2 C3H7Br + Br·
Stadi di terminazione:Stadi di terminazione:Tutte le reazioni tra le specie radicaliche.
Stadi di “strappo” dell’idrogeno:Stadi di “strappo” dell’idrogeno:1a) C3H8 + Br · CH3CH2CH2 · + HBr ∆H° = + 10.5 kcal/mole1b) C3H8 + Br · (CH3)2CH · + HBr ∆H° = + 6.0 kcal/mole

12Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Introduzione ai gruppi funzionali organici.
Introduzione ai gruppi Introduzione ai gruppi funzionali organicifunzionali organici..
4 La varietà della chimica del carbonio è alla base dell’enorme estensione e complessità della chimica organica.
4 Ciò nonostante, molte proprietà chimico-fisiche dei composti organici possono essere spiegate e previste analizzando solo piccoli gruppi di atomi, chiamati gruppi funzionali, che presentano caratteristiche strutturali e reattività chimica tipiche e peculiari, perlatro influenzate, più o meno significativamente, dal resto della molecola di cui fanno parte.
4Negli idrocarburi i gruppi funzionali sono rappresentati essenzialmente dalle insaturazioni (legami doppi, tripli, coniugati ecc.) presenti, ma la grande maggioranza dei composti organici presentano gruppi funzionali contenenti eteroatomi, vale a dire atomi diversi da carbonio e idrogeno.
4I gruppi funzionali più comuni ed importanti implicano come eteroatomi solo l’ossigeno e/o l’azoto e gli alogeni. Altri gruppi sono caratterizzati dalla presenza di zolfo, silicio e fosforo.

13Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
EteriEteriEteri R-O-R’
Sono composti aventi due gruppi organici legati allo stesso atomo di ossigeno. I residui organici possono essere gruppi alchilici, arilici, vinilici e l’ossigeno può far parte di una catena o di un ciclo.
OCH3
Metilfeniletere(Anisolo)
CH3-CH2 O CH2-CH3
Etere etilico
OTetraidrofurano
(THF)
O
Ossido di etilene

14Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Alogenuri alchiliciAlogenuri Alogenuri alchilicialchilici R-X: con X = F, Cl, Br, I
4Generalmente liquidi, immiscibili e più densi dell’acqua.4Oltre che come reagenti chimici, sono stati ampiamente usati in
grosse quantita’ come solventi e nel lavaggio a secco ma il loro uso viene attualmente molto limitato essendo risultati epatotossici e cancerogeni.
4Tipiche reazioni sono le sostituzioni nucleofile:
R X
H
HY
δ+
δ− R H
Y
H+ + X
e le eliminazioni:
CH3
Cl KOH alcolicaCH3 CH2

15Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
AlcoliAlcoliAlcoli R-OH
4Composti con punto di ebollizione abbastanza elevato a causa della presenza di legami idrogeno4Metanolo, etanolo e propanolo (C1 C2 e C3) sono perfettamente
miscibili in acqua mentre gli omologhi superiori risultano progressivamente sempre meno miscibili divenendo preponderantela componente idrofobica (idrocarburica) della molecola (vedi tabella). 4La presenza di più gruppi OH nella molecolea (es. zuccheri) ne
favorisce la solubilità in solventi polari.4Reazioni con rottura del legame R - OH
CH3 OHH2SO4
CH2
CH2 + OH2
etileneetanolo
Natura basica
delgruppo
OHCH3 OH + PCl5 CH3 Cl + POCl3 + HCl
cloroetano

16Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
4Reazioni con rottura del legame RO-H:Natura acida
del gruppo OH2Na + CH3CH2OH CH3CH2O - Na+ + H2
4Reazioni di ossidazione del gruppo alcolico:
CH3
CH3
OH
n.o. 0 K2Cr2O7
H2SO4CH3
CH3
O
n.o. +2
chetone
CH3OH
K2Cr2O7
H2SO4CH3
OH
On.o. -1
n.o. +3CH3O
Hn.o. +1 K2Cr2O7
H2SO4
aldeideacido carbossiclico

17Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano

18Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Ammine alifaticheAmmineAmmine alifatichealifatiche R-NH2; R-NHR’; R-NR’R”
4Si tratta di composti che formalmente possono essere visticome derivati dell’ammoniaca dove uno o più atomi di idrogeno sono stati sostituiti con uno o più gruppi alchilici.4Si hanno così ammine primarie, secondarie e terziarie:
NRH
H
. . . .
NRH
R'
. . . .
NR"R
R'
. .
4 Le ammine sono molecole polari e basiche che possono formare energici legami idrogeno (meno afficaci nelle ammine terziarie). Ciò giustifica l’andamento dei punti di ebollizione e la notevole solubilità in acqua di quelle a minor peso molecolare.

19Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano

20Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
4Oltre a essere tipiche basi di Lewis, le ammine si comportano come basi di Brønsted:
R2NH(aq) + H2O(l) [R2NH2]+(aq) + OH-
(aq)
4Le ammine come nucleofili:. .
NRH
R'
. .
ICH3 N
RHR'
CH3
+I
Saled’ammonio quaternario

21Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
OR
R'
OR
R'
E
C OO
sp2
sp2
2pz
2pz≈
σ(C-O)
σ(C-O)*
π(C-O)
π(C-O)*
OR
R'
δ+δ-
attacco nucleofilo
attacco elettrofilo
4Polarizzazione delgruppo carbonilico esua tipica reattività:
Composti carboniliciComposti carboniliciComposti carbonilici

22Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano

23Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Tautomeria cheto-enolicaTautomeria Tautomeria chetocheto--enolicaenolica
CH3 CH3
O O
HH
CH3 CH3
O OH
H
CH3 CH3
O O
H
H
CH3 CH3
O O
H
acetilacetone
CH3 CH3
O O
HH
Ione acetilacetona
to
OH-
-H2O

24Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano

25Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
R OH
O
R OH
OAcidi carbossiliciAcidi carbossilici

26Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
R OH
O
+ H2OR O
O
+ H3O+

27Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
R Cl
O
+ R'OH +R OR'
O
HCl
acilcloruro esterealcol
R OR'
O
+ R"NH2R NHR"
O
+ R'OH
estere ammina ammide alcol
R OH
OPCl5
2 -H2O R O
O
R
O
acido carbossilico anidride

28Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
PolimeriPolimeriPolimeri
44Polimerizzazione Polimerizzazione radicalicaradicalica
R + CH2
CH2R CH2
.
R CH2. R CH2
.CH2
CH2+
R CH2.
CH2
CH2+ R CH2n
.

29Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano

30Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
44Steroisomeria Steroisomeria nei polimerinei polimeri
4Polipropileneisotattico
sindiottico
atattico

31Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano

32Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
44PolicondensazionePolicondensazione
O
OHO
OH+ OH-CH2CH2-OH
O
OO
O
n
n
Acido tereftalico glicol etilenico Poliestere(Dacron)
R
H3N
O
O
R'
H3N
O
O+ ++
R
H3N
O
NH
R'
O
O+-H2O
aminoacido aminoacido Legame peptidico
dipeptide

33Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Preparazione Nylon 6,10Preparazione Nylon 6,10Preparazione Nylon 6,10

34Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Struttura delle ProteineStruttura delle ProteineStruttura delle Proteine
• Planarità del gruppo ammidico (-CO-NH-)legame ammidico
(parzialmente doppio)
CC
C
O
N
H
NRH
O
CC
O
N
H
H
C
R1H
C NR2H
O
CCC
O
N
H
H
C
R3H
CC
O
N+H
CC
O
Ncoinvolto inlegami ad idrogeno
H
Proteina = Poliamminoacido
gruppi ammidici planari
Rn = Residui organicisu carboni tetraedrici
sp3
sp2

35Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Struttura delle ProteineStruttura delle Proteine• proteine fibrose a catene ad α-
elica
passo dell’elica piccola - 5,1 Å
passo dell’elica grande - 61,2 Å
N
N
N
N
N
N
N
N
N
N
N Avvolgimento di catene ad α-elica con formazione dicavi a tre o sette fili .

36Lezioni di Chimica Generale Elementi chimica organica Prof. Roberto Sebastiano
Struttura delle Proteine Struttura delle Proteine Struttura delle Proteine
• Proteine globulari (emoglobina, enzimi vari)
+N
HC
O
O-
O - H O = C
HH
S S
HCH
HH CH
H
Principali Interazioni che stabiliscono la strutturaterziaria delle proteine.
Elettrostatica
Ponti disolfuro
Idrofobica
Altri legami ad H