12 Linfoma Non Hodgk
-
Upload
api-3806335 -
Category
Documents
-
view
1.010 -
download
0
Transcript of 12 Linfoma Non Hodgk

1
Linfomi non-Hodgkin
• Sono neoplasie delle cellule del sistema immunitario e dei loro precursori.
• Hanno caratteristiche genetiche, immunitaria, morfologiche e cliniche diverse, in rapporto con il tipo cellulare coinvolto dalla trasformazione neoplastica.
• Presentano numerosi caratteri clinici comuni che li distinguono dal linfoma di Hodgkin.

2
Linfomi non-Hodgkin: epidemiologia (1)
• Rappresentano il 2% di tutte le neoplasie.• L’incidenza aumenta negli ultimi decenni.• Mortalità: M.: 7100.000 – F.: 4.6100.000• Fattori di rischio: 1100.000 <10 aa.;
77.9100.000 a 80 aa.• Sesso: 1.4 volte più frequente nei maschi.• Razza: 1.7 volte più bianchi che neri.

3
Linfomi non-Hodgkin: epidemiologia (2)
• Fattori genetici: familiarità, Kinefelter, trisomia 11, traslocazioni cromosomiche.
• Radiazioni (dosi oltre 100 cGy).• Patologie immunitarie: immunodeficienze
primarie, congenite, acquisite (AIDS), secondarie a trattamenti immunosoppressori.
• Infezioni: HBV, HIV, schistosoma, lebbra.• Farmaci, pesticidi, tinture per capelli,
urbanizzazione.

4
Linfomi non-Hodgkin: sintomatologia
• Adenopatie cervicali indolenti, elastiche (80%), ascellari ed inguinali (più rare).
• Anello del Waldeyer: 15-30% spesso con tratto gastro-enterico. Linfonodi epitrocleari.
• Sintomi generali 20% all’esordio.• Massa mediastinica 20% (< in linfomi T)• Massa addominale (linfonodi o intestino).• Splenomegalia.• Cute (linfomi a cellule T): micosi fungoide.• Testicolo, tiroide, SNC, ecc.

5
Linfomi non-Hodgkin: classificazione
• Classificazione in stadi, come Ann-Arbor, che tiene conto del numero di sedi interessate, estensione rispetto al diaframma ed invasione extra-linfonodale, presenza di segni sistemici.
• Classificazione anatomo-patologica (Rappaport, Working formulation, Kiel), in funzione del grado di malignità e dell’aspetto istologico.

6
Linfomi non-Hodgkin: W. F.
• Basso grado:A. L.M. (linfomi maligni) a piccoli linfociti,
compatibile con LLC linfoplasmocitoide).
B. L.M. follicolare, a piccole cellule clivate: aree diffuse – sclerosi.
C. L.M. follicolare misto, a piccole cellule clivate e grandi cellule: aree diffuse – sclerosi.

7
Linfomi non-Hodgkin: W. F.
• Grado intermedio:D. L.M. follicolare prevalentemente a grandi
cellule: aree diffuse – sclerosi.
E. L.M. diffuso a piccole e cellule clivate.
F. L.M. diffuso misto, a piccole e grandi cellule: sclerosi – componente epitelioide.
G. L.M. diffuso: – grandi cellule – cellule clivate – cellule non clivate – sclerosi.

8
Linfomi non-Hodgkin: W. F.
• Alto grado:
H. L.M. a grandi cellule, immunoblastico:
I. L.M. a piccole cellule non clivate: tipo
Burkitt – aree follicolari.

9
Linfomi non-Hodgkin: esami di inquadramento clinico (1)
• Anamnesi (sintomi generali).• Biopsia con adeguata valutazione istologica.• Esame clinico (linfonodi, faringe, addome sup.)• Esami di laboratorio: emocromo, VES,
fosfatasi alcalina, LDH, funzionalità epatica e renale.
• Esami radiologici: torace, TC addome, ecografia addome superiore.
• Biopsie midollari.

10
Linfomi non-Hodgkin: esami di inquadramento clinico (2)
• T.C. del torace• Scintigrafia ossea• Linfografia• Esame radiologico del tratto digerente• Scintigrafia con Gallio 67• Biopsia epatica• Puntura lombare ed esame del liquor• Laparotomia di stadiazione.

11
Linfomi non-Hodgkin: terapia
• Dipende principalmente da:– Tipo istologico
– Stadio di malattia
– Condizioni cliniche del paziente

12
Terapia dei linfomi non-Hodgkin: stadi I – II con istologia favorevole
• 20% dei pazienti con stadiazione clinica e 10% con stadiazione patologica.
• Radioterapia esclusiva su volumi interessati e regioni contigue.
• Guarigione nell’80% dei casi.
• Fattori favorevoli: età < 60 anni e tumefazioni < 2.5 cm.

13
Terapia dei linfomi non-Hodgkin: stadi III – IV con istologia favorevole• Si tratta della gran maggioranza dei pazienti con
istologia favorevole• Alta probabilità di recidiva dopo R.C.• Atteggiamenti terapeutici contrastanti: vigile
attesa, chemioterapia, radioterapia estesa, interferone
• Irradiazione nodale totale (TLI) in stadi IIIA: 60% - 40% - 40%vivi a 5 – 10 – 15 anni (se meno di 5 sedi interessate e linfonodi < 10 cm)
• Chemioterapia aggressiva + TLI (24 Gy)

14
Terapia dei linfomi non-Hodgkin: istologia aggressiva
• Stadio I:– Radioterapia esclusiva (TLI)
• Stadio II:– Associazione chemioterapia e radioterapia con
TLI– Chemioterapia esclusiva con radioterapia sulle
sole sedi “bulky”• Stadio III-IV:
– Chemioterapia aggressiva– Radioterapia palliativa in casi particolari.

15
Terapia dei NHL: aspetti particolari
• Anello del Waldeyer: trattamento come per i linfomi di Hodgkin
• Tratto gastro-enterico: chirurgia• Cute: radioterapia radicale (ed eventuale
chemioterapia), radioterapia cutanea totale.• Sistema nervoso centrale: radioterapia dell’intero
encefalo (WBI)• Linfomi pediatrici: chemioterapia esclusiva.
Radioterapia per emergenze• Recidive: trapianto di midollo osseo.

16
Terapia dei NHL: aspetti particolari della radioterapia
• Dose:– 40 – 50 Gy per linfomi a grandi cellule– 40 Gy per linfomi nodulari
• Frazionamento:– 1.8 – 2 Gy per 5 gg.settimana (fr.
convenzionale)• Volume:
– Campi limitati, TLI, TBI• Sequele (acute e tardive)

17
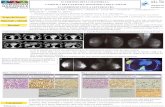
Linfoma non-Hodgkin che interessa soltanto il mediastino posteriore (frecce)

18
Tumore polmonare, che metastatizza i linfonodi della regione del dotto arterioso (frecce)

19
Linfoma a basso grado di malignità, che si presenta come una massa nel mediastino anteriore. La formazione presenta un enhancement periferico, ma la porzione centrale non mostra
alcun enhancement.

20
Linfoma a grandi cellule che interessa il mediastino anteriore, medio, posteriore e la parete toracica. L’ehancement è disomogeneo. Dislocamento spiccato delle strutture vascolari.

21
Linfoma non-Hodgkin. Massa ipodensa, disomogenea, con scarso enhancement, che circonda l’aorta, la vena cava
inferiore e la vena renale sinistra (freccia) e causa dislocazione anteriore e laterale della vena cava. É coinvolto anche il muscolo psoas sinistro. Non si riscontra idronefrosi. La linfoadenopatia tende a dislocare gli organi lateralmente, mentre la fibrosi retroperitoneale medialmente. Quest’ultima
presenta anche un enhancement più pronunciato e tende a determinare più frequentemente idronefrosi.

22
Tricoleucemia. Pacchetto linfonodale ingrandito in sede para-aortica, con intenso ma disomogeneo
enhancement.

23
Metastasi da seminoma del testicolo. Un linfonodo ingrandito ed ipodenso (freccia) è visibile in sede
inter-aorto-cavale, a livello dell’ilo renale.