Volume 3 Indice - MediPrint · in un caso di linfoma mantellare recidivato A. Fragasso La...
Transcript of Volume 3 Indice - MediPrint · in un caso di linfoma mantellare recidivato A. Fragasso La...
L’associazione fra bendamustina e anticorpo monoclonale anti-CD20 2è altamente efficace nella leucemia linfatica cronica con importanteinteressamento extranodaleA. Cuneo, E. Lista
Leucemia linfatica cronica insorta in paziente di 84 anni affetto 4da insufficienza renale cronicaC.G. Giannitto, G. Caputo, S. Condorelli, F. Spinnato, C. Di Rosa
Bendamustina e rituximab in paziente anziano 7con leucemia linfatica cronica multitrattataM. Maccaferri, E. Colaci, L. Faglioni, F. Soci, G. Leonardi, M. Luppi, R. Marasca
Terapia con bendamustina in un paziente affetto da leucemia 9linfatica cronica, refrattario a trattamento con PCR (pentostatina, ciclofosfamide e rituximab) e alemtuzumabM. Sassone, F. Rossini, E.M. Pogliani
Sicurezza ed efficacia di bendamustina e rituximab in un caso 11di leucemia linfatica cronica in progressioneR. Scalone
Efficacia del regime di combinazione rituximab e bendamustina 13nel linfoma indolente resistente al trattamento di prima linea: presentazione di un caso clinicoG. Quintini, C. Maugeri
L’associazione di bendamustina e bortezomib è efficace e tollerata 15in un caso di linfoma mantellare recidivatoA. Fragasso
La bendamustina come possibile terapia di salvataggio 18nel linfoma di Hodgkin refrattarioF. Castagna, S. Impera, U. Consoli
Un caso di linfoma mantellare “indolente” in un paziente anziano “fragile” 21M. Montanari
La bendamustina funziona anche nelle leucemie acute? 23G. Musuraca, D. Cangini, M. Ceccolini, M.B. Giannini, A. Lucchesi, S. Ronconi, G. Poletti, A. Valenti, M. Tonelli, P. Fattori
Esperienze cliniche in ematologia sul territorio nazionaleVolume 3
Indice
2
Presentazione del caso
Paziente e anamnesiQuesto report si riferisce a unuomo di 54 anni in buone condi-zioni cliniche (ECOG 0), senzacomorbidità, con pregressa epati-te B. La diagnosi di leucemia linfa-tica cronica (LLC) era stata postanel 2000, in seguito al riscontrooccasionale di linfocitosi conmorfologia e immunofenotipocaratteristici, stadio II/B secondoRai e Binet, categoria di rischiobassa per la contemporanea pre-senza di CD38 negatività, carioti-po normale, TP53 non mutato,stato mutato dei geni IgVH. I lpaziente, asintomatico, venivasottoposto a visite periodiche difollow-up.Nel 2006 si osservava la progres-sione della linfocitosi con febbri-cola, splenomegalia (19 cm allaTC) e diffuso infiltrato linfocitariomidollare; il paziente veniva quin-di trattato con fludarabina 25mg/m2/die e ciclofosfamide 250mg/m2/die per 3 giorni, per untotale di 6 cicli con ottenimentodi risposta completa (RC). NelSettembre del 2011 si osservavaun incremento della linfocitosi(14.230/µl) con CD38 negatività,comparsa di delezione 13q14 iso-lata, piastrinopenia (82.000/µl) edisfagia ingravescente.
Approccio terapeutico,valutazione a distanza eaggiustamentiterapeutici
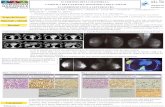
Alla ristadiazione di malattia unaTC total body evidenziava unamarcata ipertrofia tonsillare bila-terale simmetrica, con netta ridu-zione del lume faringeo, linfoade-nopatie sovra- e sottodiaframma-tiche fino a 26 mm, splenomegaliadi 17 cm, mentre la biopsia osteo-midollare mostrava un infiltratolinfocitario pari all’80% della cellu-larità. Una visita ORL deponevaper la natura linfomatosa dellatumefazione tonsillare e il pazien-te è stato trattato con l’associazio-ne di bendamustina e ofatumu-mab per 6 cicli di 28 giorni, nel-l’ambito di un protocollo GIMEMA.Al 1° ciclo sono stati somministratibendamustina (75 mg/m2 giorni1-2) e ofatumumab (300 mg gior-no 1 e 1000 mg giorno 8); il ciclochemioimmunoterapico prevede-va, inoltre, una terapia ipourice-mizzante con allopurinolo, profi-lassi antimicrobica con trimeto-prim/sulfametossazolo, aciclovir elamivudina; è stata effetuata unapremedicazione di ofatumumabcon paracetamolo, metilpredniso-lone e clorfenamina maleato. Lacomparsa di neutropenia di gradoIII ha richiesto la somministrazione
di G-CSF (granulocyte colony-sti-mulating factor). Dal 2° ciclo, la cuisomministrazione è stata riman-data di 4 settimane, il dosaggiodella bendamustina è stato ridot-to del 25%, mentre ofatumumab èstato mantenuto alla dose previ-sta di 1000 mg al giorno 1; la tera-pia è proseguita per il totale dei 6cicli previsti, senza ulteriori ritardie senza effetti collaterali significa-tivi. La ristadiazione, al termine deltrattamento, ha mostrato un qua-dro di RC secondo i criteri NCI, conscomparsa della linfocitosi perife-rica (640/µl), normalizzazione del-la cellularità midollare, negativiz-zazione della TC e scomparsa dellevoluminose masse tonsillari; 4mesi dopo il completamento dellaterapia compariva una neutrope-nia di grado IV (120/µl), in assenzadi infiltrato patologico midollare;la conta neutrofila si è poi norma-lizzata spontaneamente dopo 2mesi in assenza di complicanzeinfettive. Il quadro di RC ottenutosi è mantenuto a 15 mesi dall’ini-zio del trattamento.
Discussione del caso erazionale delle scelteterapeutiche
La recidiva di malattia presentavacaratteristiche diverse rispetto
L’associazione fra bendamustina e anticorpo monoclonaleanti-CD20 è altamente efficace nella leucemia linfaticacronica con importante interessamento extranodaleA. Cuneo, E. ListaAzienda Ospedaliero-Universitaria di Ferrara
L’ASSOCIAZIONE FRA BENDAMUSTINA E ANTICORPO MONOCLONALE ANTI-CD20 È ALTAMENTE EFFICACE NELLA LEUCEMIALINFATICA CRONICA CON IMPORTANTE INTERESSAMENTO EXTRANODALE
3
all’esordio, poiché prevaleva lacomponente extranodale, concoinvolgimento tonsillare eimportante stenosi faringea sinto-matica; era quindi necessario ini-ziare, con urgenza, un trattamentodi 2ª linea. Per questi motivi, nono-stante la prima RC si fosse mante-nuta per 5 anni, si è scelto di cam-biare regime terapeutico utilizzan-do l’anticorpo monoclonale anti-CD20 ofatumumab e associando-lo a bendamustina. Il risultato,ottenuto sulle lesioni tonsillari, è
degno di nota poiché non vi sonodati, in letteratura, sulla rispostaalla terapia delle localizzazioniextranodali nella LLC.Meritevoli di commento sonoanche la comparsa e l’evoluzionespontanea favorevole della “lateonset neutropenia” (LON) osserva-ta in questo paziente: casi di LONsono stati infatti riportati in un 20-30% dei casi in seguito all’utiliz-zo dell’anticorpo monoclonaleanti-CD20 associato a fludarabinae ciclofosfamide (1), si verificano
da 38 a 175 giorni dopo la sommi-nistrazione del farmaco e hannouna durata variabile da 5 a 77 gior-ni (2). Il meccanismo patogeneticoè ignoto poiché la tossicità direttasembra improbabile; si è osservataun’associazione con un polimorfi-smo di FCGR3A, che è un recettoreFc implicato nella citotossicità cel-lulare anticorpo-dipendente (3).Uno studio suggerisce, infine, chela LON possa essere considerata unfattore prognostico favorevole peril raggiungimento della RC (4).
Bibliografia
1. Tam CS, O’Brien S, Wierda W et al. Long-term results of the fludarabine, cyclophos-phamide, and rituximab regimen as initialtherapy of chronic lymphocytic leukemia.Blood 2008;112(4):975-980.2. Rozman S, Sonc M, Novakovic BJ. Late-onset neutropenia following primary treat-
ment of diffuse large B-cell lymphoma withrituximab-containing therapy. LeukLymphoma 2012;53(10):1945-1948.3. Weng WK, Negrin RS, Lavori P, HorningSJ. Immunoglobulin G Fc receptorFcgammaRIIIa 158 V/F polymorphism cor-relates with rituximab-induced neutrope-
nia after autologous transplantation inpatients with non-Hodgkin’s lymphoma. J Clin Oncol 2010;28(2):279-284.4. Hincks I, Woodcock BE, Thachil J. Is ritux-imab-induced late-onset neutropenia a goodprognostic indicator in lymphoproliferatvedisorders? Br J Haematol 2011;153(3):411-413.
Presentazione del caso
Paziente, anamnesiSi descrive il caso clinico di unpaziente affetto da insufficienzarenale cronica, giunto alla nostraosservazione nel mese di Giugno2011, inviato dal reparto di otori-nolaringoiatria dove era stato sot-toposto a biopsia di linfoadeno-patia laterocervicale sinistra conesito di “tessuto fibroadiposoinfiltrato da elementi linfoidi dipiccola e media taglia atipici”.L’immuno istochimica eraCD20++, CD5++, CD23+-, CD10--, bcl2--, ciclina D1---. Il quadromorfologico e l’algoritmo immu-noistochimico erano coerenticon LLC/LSL (leucemia linfaticacronica/leucemia di sindrome dilinfoma); il paziente esibiva, inol-tre, una TAC torace senza mezzo dicontrasto, che evidenziava unaformazione solida in sede latero-cervicale sinistra dai diametri di65x27x50 mm con estensione insede retrosternale, da riferire acolata linfonodale; si evidenziavaanche la presenza di un nodulomillimetrico al segmento basalelaterale del lobo polmonare infe-riore sinistro e di un ulteriore milli-metrico no dulo nel segmentoanteromediale dello stesso lobo. Riscontro di anemia con HgB paria 8 mg/dl, leucocitosi con globuli
bianchi pari a 30.000/mm3 e linfo-citosi assoluta con linfociti pari a10.000 linfociti/mm3. Ri lievo diinsufficienza renale con creatini-na pari a 2,9 mg/dl, azotemia di88 mg/dl e clearance della creati-nina pari a 20 ml/min. Il pazienteveniva quindi sottoposto a PET,con evidenza di patologica con-centrazione del probe glucidiconella colata linfonodale laterocer-vicale e retrosternale si ni stra, evi-dente alla CT (computed tomo-graphy) di correzione, con SUV(standardized uptake value) mas-simo di 16,2; lo stesso comporta-mento metabolico, ma con mino-re uptake, presentava linfoadeno-patia retroclaveare controlateralecon SUV massimo di 5,6.
Esame obiettivo e indaginidiagnosticheAll’esame obiettivo si riscontrava-no una voluminosa linfadenopatialaterocervicale sinistra di diametrotrasverso massimo pari a circa 10cm, una splenomegalia con organodebordante 4 cm dall’arcata costa-le; inoltre, come comorbilità, si rile-vava un’insufficienza renale cronicapresente da circa 10 anni, in tratta-mento con dieta ipoproteica. Il 20/6/2011 il paziente eseguivauna biopsia osteomidollare conrapporto midollo/tessuto adiposo1/2; erano presenti 4 aggregati
linfoidi costituiti da elementi dipiccola taglia monomorfi a celluleB. CD20++ CD3-- glicoforina+ mie-loperossidasi++ CD5-+ CD34--CD10-- ciclina D1--. Compatibilecon LLC-LSL. Alla citofluorimetriaemergeva la presenza di unapopolazione linfocitaria CD20+CD10- CD5+ CD23+ FCM 7--. Siconcludeva per LLC, allo stadio IVdi Rai in paziente anziano coninsufficienza renale cronica di gra-do moderato.
Approccio terapeutico
Il paziente veniva sottoposto achemioimmunoterapia con sche-dula rituximab-bendamustina (labendamustina veniva sommini-strata al dosaggio di 70 mg/m2 neigiorni 1 e 2 ogni 28, mentre ilrituximab veniva somministratoalla dose di 500 mg/m2 al giorno 1ogni 28) e venivano eseguiti 3 ciclidi trattamento. Il 12/09/2011 ilpaziente era sottoposto a TAC-PETdi rivalutazione che indicava che”l’odierno controllo evidenzia unsignificativo decremento dell’up-take di probe glucidico nell’ade-nopatia laterocervicale e retro-strernale sinistra (SUV massimo di4,5) apprezzandosi peraltro unariduzione volumetrica della stessaalla TC di correzione”. Venivano
4
Leucemia linfatica cronica insorta in paziente di 84 anniaffetto da insufficienza renale cronicaC.G. Giannitto, G. Caputo, S. Condorelli, F. Spinnato, C. Di Rosa S. C. di Oncologia Medica, Ospedale Gravina, Caltagirone
LEUCEMIA LINFATICA CRONICA INSORTA IN PAZIENTE DI 84 ANNI AFFETTO DA INSUFFICIENZA RENALE CRONICA
5
effettuati poi ulteriori 3 cicli dichemioimmunoterapia e la PETdel 13/12/11 indicava che “l’odier-no esame non documenta aree dipatologico uptake del radio-far-maco”. Il 30/11/11 veniva ripetutauna biopsia osteomidollare: rap-presentate le 3 serie cellulari, spar-si elementi linfoplasmacitoidiintorno al 2%.
Discussione del caso erazionale delle scelteterapeutiche
La schedula FCR (fludarabina,ciclofosfamide e rituximab) costi-tuisce la terapia elettiva per ipazienti fit affetti da LLC in assen-za di alterazione della TP53. Il clo-rambucil rimane un’opzione ditrattamento per i pazienti unfit;nondimeno la bendamustina rap-presenta un farmaco molto pro-mettente nella gestione di talipazienti.
Uno studio di fase III (Knauf et al.,2009) ha evidenziato la superioritàdella bendamustina, rispetto alclorambucil, sia in termini di rispo-sta (68% versus 31%), che di remis-sione completa (31% versus 2%) eprogression free survival (PFS) (22mesi versus 8 mesi). La neutropeniaG3-4 era pari al 23% nel bracciobendamustina rispetto all’11% delbraccio clorambucil; inoltre lacombinazione rituximab-benda-mustina ha determinato una rispo-sta obiettiva nel 59% (CR-rispostacompleta 9%) dei 78 pazientiarruolati nello studio di Fisher del2011. L’età media dei pazienti trat-tati era di 67 anni (2 è il numeromedio dei precedenti trattamenticui i pazienti erano stati sottoposti)mentre la PFS è risultata pari a 15mesi: ancora una volta venivariscontrata una neutropenia G3-4nel 23% dei pazienti trattati.Nel lavoro di Iannitto et al. del 201187 pazienti, trattati con la combi-nazione rituximab-bendamustina,
hanno ottenuto una rispostaobiettiva pari al 70% (CR pari a32%); la PFS è risultata pari a 16mesi mentre la OS (overall survival)è stata valutata in 17 mesi. Per quelche riguarda i pazienti treatment-naïve ancora Fisher et al. hannoevidenziato, con la combinazionerituximab-bendamustina, unarisposta obiettiva pari al 91% in117 pazienti affetti da LLC, di cui il26% di età superiore a 70 anni; infi-ne la combinazione rituximab-clo-rambucil ha prodotto una rispostaobiettiva pari all’80%. Nonostante idati relativi al trattamento ottimalein 1ª linea dei pazienti affetti daLLC e unfit siano sicuramente limi-tati, è possibile concludere che lacombinazione di rituximab e ben-damustina rappresenta una possi-bile opzione terapeutica. Nel casoda noi presentato un paziente di84 anni, affetto da LLC, ha ottenutouna remissione completa di ma -lattia e, a oggi, resta libero da pro-gressione.
C.G. GIANNITTO, G. CAPUTO, S. CONDORELLI, F. SPINNATO, C. DI ROSA
6
Bibliografia
• Fischer K, Cramer P, Bush R et al. Benda -mustine combined with rituximab inpatients with relapsed and/or refractorychronic lymphocytic leukemia: a multi-center phase II trial of the German ChronicLymphocytic Leukemia Study Group. JClin Oncol 2011;29(26):3559-3566.
• Fischer K, Cramer P, Stligenbauer S et al.Bendamustine combined with rituximab(BR) in first-line of therapy of advanced
CLL: a multicentre phase II trial of theGerman CLL study Group (GCLLSG). Blood114, abstract 205.
• Hallek M, Fischer K, Fingerle-Rowson G etal. Addition of rituximab to fludarabineand cyclophosphamide to patient s withchronic lymphocytic leukemia, a rando-mized, open-label, phase 3 trial. Lancet2010;376(9747):1164-1174.
• Iannitto E, Morabito F, Mancuso S et al.
Bendamustine with or without rituximabin the treatment of relapsed chronic lym-phocytic leukemia: an Italian retrospectivestudy. Br J Haematol 2011;153(3):351-357.
• Knauf WU, Lissichkov T, Aladaoud A et al.Phase III randomized study of bendamus-tine compared with clorambucil in previ-ously untreated patients with chroniclymphocytic leukemia. J Clin Oncol2009;27(26):4378-4384.
Presentazione del caso
Paziente di 83 anni con diagnosi,nel 2002, di leucemia linfatica cro-nica (LLC) stadio II B di Rai e Binet.La caratterizzazione biologica hamostrato uno stato non mutato diIgVH (catena pesante delle immu-noglobuline), positività per CD38,negatività per ZAP70 e trisomiadel cromosoma 12.
Paziente, anamnesi, esameobiettivo e indagini diagnosticheIl paziente è stato sottoposto, nel2002, al trattamento con fludarabi-na per os alla dose di 40 mg/m2 per5 giorni al mese ogni 28 giorni, per6 mesi, ottenendo la remissioneparziale. A Settembre del 2008, perprogressiva linfocitosi, il pazienteha effettuato altri 7 cicli di fludara-bina, ottenendo nuovamente laremissione parziale. Ad Agosto del2009, per progressiva linfocitosi esplenomegalia, ha iniziato un trat-tamento con clorambucil (15mg/m2 per 5 giorni), per un totaledi 13 cicli (più 10 di rituximab), otte-nendo la remissione parziale. ADicembre del 2010 si è assistito auna progressiva linfocitosi e piastri-nopenia e alla comparsa di linfoa-denomegalie di 3 cm in sede ascel-lare e laterocervicale. La TC totalbody ha confermato la presenza dilinfoadenomegalie di 3 cm in sede
sopra- e sottodiaframmatica, unacolata pericavale estesa in sensolongitudinale per 14,5 cm e spleno-megalia di 19x13x17 cm.
Approccio terapeutico
Per la progressione dell’emopatia,in considerazione delle buone con-dizioni cliniche generali, nonostan-te l’età e le precedenti linee tera-peutiche, a Febbraio 2011, all’età di82 anni, il paziente ha iniziato untrattamento con bendamustina100 mg/m2 (gg 1 e 2) e rituximab375 mg/m2 la 1ª somministrazionee 500 mg/m2 le successive; a taletrattamento è stata associata unaprofilassi antivirale con valacyclovire anti-Pneumocystis carinii con tri-metoprim/sulfametossazolo. Il paziente ha effettuato, in totale, 6cicli (ciascuno della durata di 28giorni) e il trattamento è stato com-plessivamente ben tollerato; sisegnalano, inoltre, una tossicitàematologica (neutropenia) di gra-do IV (per cui si è reso necessario,più volte, il ricorso a una terapia disupporto con G-CSF-granulocytecolony-stimulating factor) e unatossicità infettiva di grado IV (que-st’ultima è insorta dopo il 6° ciclo ditrattamento ed è stata caratterizza-ta da una sepsi da Streptococcusgallolyticus e dalla comparsa di
addensamento polmonare basaledestro). La TC total body, effettuatadopo 4 cicli di chemioterapia,mostrava inifine la risoluzione dellasplenomegalia e la scomparsa ditutte le linfoadenomegalie. Al termine del trattamento la TCtotal body confermava l’ottimorisultato, la tipizzazione su sangueperiferico e midollare risultavanegativa per linfociti B e la BOM(biopsia osteomidollare) non evi-denziava la presenza di infiltratolinfocitario patologico. Gli esami ematochimici mostrava-no la parziale ripresa ematologica,con globuli bianchi 2000/mm3,neutrofili 50%, emoglobina 12 g/dle piastrine 110.000/mm3; si confi-gurava pertanto un quadro diremissione completa e tale rispo-sta si sta mantenendo per più di 16mesi dal termine del trattamento.
Discussione del caso erazionale delle scelteterapeutiche
Attualmente il trattamento conbendamustina, nei pazienti affettida B-LLC (leucemia linfatica croni-ca a B cellule) è indicato in 1ª lineanei pazienti che, per età o copato-logie, non sono candidabili ai trat-tamenti con fludarabina, in parti-colare allo schema FCR (fludarabi-
7
Bendamustina e rituximab in paziente anziano con leucemia linfatica cronica multitrattataM. Maccaferri, E. Colaci, L. Faglioni, F. Soci, G. Leonardi, M. Luppi, R. MarascaUO-C e Cattedra di Ematologia, AOU Policlinico di Modena
M. MACCAFERRI, E. COLACI, L. FAGLIONI, F. SOCI, G. LEONARDI, M. LUPPI, R. MARASCA
8
na, ciclofosfamide e rituximab); labendamustina appare tuttaviaanche molto efficace nei pazientirefrattari/recidivati, mantenendouna ORR (overall remission rate)attorno al 60% con una EFS (so -prav vivenza libera da eventi) me -dia di 14 mesi. Tale efficacia sembramantenersi, anche se in misuraminore, non solo nei pazienti giàtrattati con fludarabina (come ilnostro paziente), ma anche inquelli refrattari; questo perché talefarmaco agisce sia come agenteantimetabolita, sia come alchilan-te; generalmente il trattamento
con bendamustina è ben tollerato,e quindi proponibile, anche apazienti anziani in buone condi-zioni cliniche generali. Le piùcomuni tossicità di grado severo(grado III e IV) sono quella emato-logica, circa 20% (soprattutto neu-tropenia), più frequente se ilpaziente è stato già sottoposto atrattamento con fludarabina, equella infettiva, con incidenzaattorno al 10%. Da ricordare ancheun 11% di riattivazione di Herpeszooster, percentuale che scendeattorno allo 0%, se il paziente assu-me una profilassi antivirale; si
segnala infine che, attualmente, ildosaggio consigliato di bendamu-stina è inferiore a quello effettuatodal nostro paziente: in modo parti-colare si raccomandano 90 mg/m2
nei giorni 1-2 in 1ª linea e 70mg/m2 nei casi di recidiva o refrat-tarietà. In conclusione il trattamen-to con bendamustina, se si esclu-dono i pazienti con del17p, appareefficace e ben tollerato e rappre-senta una valida opzione terapeu-tica, non solo nei pazienti giovani,ma anche nei pazienti anziani, inbuone condizioni cliniche, senzacopatologie di rilievo.
Bibliografia
• Cheson BD, Rummel MJ. Bendamustine:rebirth of an old drug. J Clin Oncol 2009;27(9):1492-1501.
• Fischer K, Cramer P, Busch R et al.Bendamustine combined with rituximabin patients with relapsed and/or refractorychronic lymphocytic leukemia: a multicen-ter phase II trial of the German ChronicLymphocytic Leukemia Study Group. J ClinOncol 2011;29(26):3559-3566.
• Fischer K, Cramer P, Busch R et al.Bendamustine in combination with ritux-imab for previously untreated patientswith chronic lymphocytic leukemia: a mul-
ticenter phase II trial of the GermanChronic Lymphocytic Leukemia StudyGroup. J Clin Oncol2012;30(26):3209-3216.
• Hallek M, Fischer K, Fingerle-Rowson G et al.;International Group of Investigators;German Chronic Lymphocytic LeukaemiaStudy Group. Addition of rituximab to flu-darabine and cyclophosphamide inpatients with chronic lymphocyticleukaemia: a randomised, open-label, phase3 trial. Lancet2010;376(9747):1164-1174.
• Iannitto E, Morabito F, Mancuso S et al.Bendamustine with or without rituximab inthe treatment of relapsed chronic lympho-
cytic leukaemia: an Italian retrospectivestudy. Br J Haematol2011;153(3):351-357.
• Knauf WU, Lissitchkov T, Aldaoud A et al.Bendamustine compared with chloram-bucil in previously untreated patients withchronic lymphocytic leukaemia: updatedresults of a randomized phase III trial. Br JHaematol 2012;159(1):67-77.
• Knauf WU, Lissichkov T, Aldaoud A et al.Phase III randomized study of bendamus-tine compared with chlorambucil in previ-ously untreated patients with chronic lym-phocytic leukemia. J Clin Oncol 2009;27(26):4378-4384.
Presentazione del caso
Paziente e anamnesiPresentiamo il caso di un uomo di68 anni, giunto alla nostra osserva-zione nel Marzo del 2009 per riscon-tro, agli esami di controllo, di linfoci-tosi assoluta (38.000/mm3) associa-ta a lieve piastrinopenia (85.000/m3,in calo rispetto agli esami di prece-denti). Il paziente si presentava allavisita in discrete condizioni generali,asintomatico; in anamnesi si rivelaun portatore occulto di epatite B evengono riferiti frequenti episodi diinfezioni delle vie aeree.
Esame obiettivo e indaginidiagnosticheAll’esame obiettivo emergonoadenopatie palpabili in tutte le sta-zioni superficiali, con diametromassimo di 3 cm a livello ascellaredestro, non epatosplenomegalia.All’analisi dell’immunofenotipo,eseguito su sangue periferico, vie-ne evidenziato un quadro compati-bile con LLC (leucemia linfatica cro-nica) (CD5, CD19, CD20, CD23 posi-tivi, FMC7 e CD38 negativi), conrestrizione monoclonale per cate-ne leggere κ. All’analisi FISH (fluore-scence in situ hybridization) vienedimostrata la presenza di delcr(13)nel 70% dei nuclei; all’analisi dellostato mutazionale IgVH (regionevariabile delle immunoglobuline),
viene dimostrata omologia com-pleta. Alla TAC collo-torace-addo-me viene confermata la presenza dimultiple adenopatie sovra- e sotto-diaframmatiche, le maggiori inambito addominale fino a 4 cm; siconcludeva pertanto con diagnosidi LLC, stadio C secondo Binet, percui si poneva indicazione a terapiadi 1ª linea (1,2).
Approccio terapeutico
Il paziente ha quindi iniziato untrattamento immunochemiotera-pico secondo lo schema PCR (pen-tostatina, rituximab, ciclofosfami-de) a dosaggio standard (3). Al termine del 6° ciclo si è osservatala normalizzazione della crasi ema-tica, senza tuttavia variazioni delleadenopatie; si poneva quindi ilpaziente in follow-up clinico men-sile, con sostanziale stabilità delquadro clinico e della crasi ematica. Al controllo a 5 mesi si verificava,tuttavia, la comparsa di astenia edi sudorazioni progressivamenteingravescenti; il paziente venivaquindi sottoposto a nuova rivalu-tazione radiologica con dimostra-zione di aumento volumetrico ditutte le adenopatie, in particolarea livello mediastinico, dove siosservava una lieve compressioneal III medio dell’esofago.
Agli esami la crasi ematica si man-teneva nei limiti; il paziente venivaquindi sottoposto a terapia di 2ªlinea con alemtuzumab, eseguito adosaggio standard per 12 settima-ne, senza complicanze significati-ve. Al termine del trattamento ilpaziente riferiva una riduzione del-le sudorazioni e la crasi ematica simanteneva nella norma; alla rivalu-tazione della TAC veniva dimostra-ta, tuttavia, una progressione dimalattia a livello addominale, conmasse confluenti fino a 15 cm; ilpaziente è stato quindi avviato atrattamento di 3ª linea con benda-mustina (90 mg/m2 gg 1-2) in asso-ciazione a rituximab (375 mg/m2
gg 1). Sono stati eseguiti in tutto 5cicli; il previsto 6° ciclo non è statosomministrato per la persistenza dineutropenia di grado 3; non sisono verificate, comunque, compli-canze febbrili e la crasi ematica si ènormalizzata in 2 mesi. Alla valuta-zione radiologica è stata dimostra-ta una riduzione di tutte le adeno-patie fino a un diametro di 2,5 cm;il paziente ha quindi iniziato un fol-low-up osservazionale clinico-radiologico, che confermava il qua-dro di remissione. Il paziente, a 18mesi dal termine del trattamento,permane in remissione con ulte-riore regressione delle adenopatiea 2 cm, dimostrata all’ultima eco-grafia dell’addome.
9
Terapia con bendamustina in un paziente affetto daleucemia linfatica cronica, refrattario a trattamento conPCR (pentostatina, ciclofosfamide e rituximab) ealemtuzumabM. Sassone, F. Rossini, E.M. PoglianiClinica Ematologica A.O. San Gerardo, Monza
M. SASSONE, F. ROSSINI, E.M. POGLIANI
10
Discussione del caso erazionale delle scelteterapeutiche
L’indicazione al trattamento di 1ªlinea è stata posta per la progressi-va riduzione della conta piastrini-ca e la presenza di multiple e volu-minose adenopatie (1,2).La terapia più indicata sarebbe sta-ta un trattamento secondo lo sche-ma FCR (fludarabina, ciclofosfami-de, rituximab) (4); tuttavia, vistal’età “borderline”, i frequenti episo-di infettivi delle vie aeree e lo statodi portatore occulto del virus del-l’epatite B, si è deciso di sostituirela fludarabina con la pentostatina,per ridurre il rischio infettivo (3).In considerazione della refratta-
rietà dimostrata a un regime con-tenente un analogo delle purine,le scelte per una terapia di 2ªlinea consentite e disponibiliall’epoca in cui il paziente è statotrattato, erano alemtuzumab eschemi di polichemioterapie tipoCVP (ciclofosfamide, vincristina,prednisone).Nonostante la presenza di masselinfoadenopatiche, la scelta è rica-duta sull’utilizzo dell’anticorpomonoclonale alemtuzumab,anche alla luce degli scarsi risulta-ti ottenuti con la recente terapiacontenente ciclofosfamide. Almomento dell’inizio della terapiadi 3ª linea era disponibile la ben-damustina, che si è deciso di utiliz-zare in combinazione con rituxi-
mab, sulla base dei dati disponibiliin letteratura (5-7).L’unica tossicità verificatasi è stataematologica; dal 3° ciclo è statointrodotto un supporto con G-CSF(granulocyte colony-stimulatingfactor), che ha permesso di mante-nere il timing del trattamento ogni28 giorni, senza comunque la com-parsa di eventi febbrili. Il previsto 6°ciclo non è stato somministrato peril persistere di neutropenia di gradoG3. Nei 2 mesi successivi si ècomunque assistito a una ripresaspontanea della conta dei neutrofilie non si sono verificati eventi infet-tivi. Il trattamento con bendamusti-na si è quindi dimostrato efficace epoco tossico, in un paziente over 65refrattario a due linee di terapia.
Bibliografia
1. Hallek M, Cheson BD, Catovsky D et al.International Workshop on ChronicLymphocytic Leukemia. Guidelines for thediagnosis and treatment of chronic lympho-cytic leukemia: a report from theInternational Workshop on Chronic lynm-phocytic leukemia updating the NationalCancer Institute Working Group 1996 guide-lines. Blood2008;111(12):5446-5456.2. Cheson BD, Wendtner CM, Pieper A et al.Optimal use of bendamustine in chronic lym-phocytic leukemia, non-Hodgkin lym-phomas, and multiple myeloma: treatmentrecommendations from an international con-sensus panel. Clin Lymphoma Myeloma Leuk2010; 10(1):21-27.
3. Kay NE, Wenting Wu, Kabat B et al.Pentostatin and rituximab therapy for previ-ously untreated patients with B-cell chroniclymphocytic leukemia. Cancer2010;116(9):2180-2187.4.Hallek M, Fischer K, Fingerle-Rowson G et al.;International Group of Investigators; GermanChronic Lymphocytic Leukaemia Study Group.Addition of rituximab to fludarabine andcyclophosphamide in patients with chroniclymphocytic leukaemia: a randomised, open-label, phase 3 trial. Lancet 2010;376(9747):1164-1174.5. Fischer K, Cramer P, Busch R et al.Bendamustine in combination with ritux-imab for previously untreated patients with
chronic lymphocytic leukemia: a multicenterphase il trial of the German ChronicLymphocytic Leukaemia Study Group. J ClinOncol2012;30(26):3209-3216.6. Knauf WU, Lissichkov T, Aldaoud A et al.Phase III randomized study of bendamustinecompared with chlorambucil in previouslyuntreated patients with chronic lymphocyticleukemia.J Clin Oncol 2009;27(26):4378-4384. 7. Fischer K, Cramer P, Busch R et al.Bendamustine combined with rituximab inpatients with relapsed and/or refractorychronic lymphocytic leukemia: a multicenterphase II trial of the German ChronicLymphocytic Leukaemia Study Group. J ClinOncol 2011;29(26):3559-3566.
11
Presentazione del caso
Paziente, anamnesi, esameobiettivo e indagini diagnosticheMaschio di anni 59, con nessunacomorbidità. Nel Marzo del 2010viene effettuata una diagnosi diLLC (leucemia linfatica cronica)stadio B: spiccata l infocitosi(230.000/mm3), positività perCD38 e ZAP 70, presenza di dele-zione di 11q, linfoadenomegaliepalpabili in sede laterocervicale,ascellare e inguinale bilaterale,con diametri compresi tra 3 e 5cm, masse adenopatiche sotto-diaframmatiche, con diametrifino a 10 cm, in sede retroperito-neale, omentale e lungo il lega-mento gastro-splenico, volumi-nosa splenomegalia con diame-tro longitudinale di 25 cm. I lpaziente riceveva 12 cicli con clo-rambucil 10 mg/2/die per 7 gior-ni, ogni 28 giorni, più ofatumu-mab 1000 mg al 1° giorno di ogniciclo. La rivalutazione della malat-tia, effettuata a un mese dal ter-mine del programma terapeuti-co, documentava la scomparsadella linfocitosi, delle linfoadeno-megalie, della splenomegalia,persistendo un infiltrato linfoidemidollare pari al 25%. Nel Settembre del 2011 si verificala ricomparsa della linfocitosi(75.000/mm3), delle linfoadeno-
megalie superficiali e profonde,con diametri compresi tra 2 e 4cm, della splenomegalia, con dia-metro longitudinale di 20 cm, ilmieloaspirato documentava unamassiva infiltrazione linfoideCD5+, CD19+, CD20+.
Approccio terapeutico evalutazioni
Nel Settembre del 2011 veniva ini-ziata un’immunochemioterapia di2ª linea con associazione di benda-mustina e rituximab (BR) secondoil seguente schema: bendamustina70 mg/m2/die per 2 giorni, ogni 28giorni, rituximab 375 mg/m2 al 1°giorno del 1° ciclo, 500 mg/m2 al 1°giorno dei successivi 5 cicli. Ilpaziente completava i previsti 6cicli BR senza riportare alcuna tos-sicità extraematologica. Al giorno1 del 2° ciclo BR si documentava lascomparsa della linfocitosi. Al gior-no 1 del 3° ciclo BR non risultavanopiù palpabili i linfonodi e la milza.Nel corso dei 6 cicli BR non si ripor-tavano tossicità ematologichesuperiori al grado 2 (CTCAE - com-mon terminology criteria foradverse eventsgrading v.3) e, inparticolare, non si riportava unaneutropenia maggiore di grado 2,pur non avendo adottato alcunaprofilassi con G-CSF (granulocyte
colony-stimulating factor). A un mese dal termine del pro-gramma terapeutico il pazienteveniva sottoposto a rivalutazionedi malattia con TC di collo, torace eaddome e osteomielobiopsia. LaTC non evidenziava linfonodi condiametri superiori a 1 cm né epa-tosplenomegalia, mentre l’osteo-mielobiopsia documentava qual-che piccolo aggregato linfoidenodulare costituito da linfociti adhabitusmaturo.All’ultima valutazione di malattia,effettuata con esame clinico edemocromo a 9 mesi dal terminedel programma immunochemio-terapico, non si documentavanolinfoadenomegalie, epatospleno-megalia, linfocitosi, anemia o pia-strinopenia.
Discussione del caso erazionale delle scelteterapeutiche
Bendamustina si è dimostrata effi-cace e sicura nella terapia dellaLLC recidivata o refrattaria, siacome singolo agente (1), sia inassociazione a rituximab (2),ottenendo in combinazione conl’anti-CD20, in pazienti pesante-mente pretrattati, il 59% di RR,con il 9% di RC e una EFS (soprav-vivenza libera da eventi) media-
Sicurezza ed efficacia di bendamustina e rituximab in uncaso di leucemia linfatica cronica in progressioneR. ScaloneU.O. di Oncoematologia e TMO, Dipartimento Oncologico di III livello, “La Maddalena”, Palermo
12
R. SCALONE
na di 14,7 mesi (2). Sulla scorta diquesti risultati, un panel di esper-ti (3) ha dato indicazione all’im-piego di bendamustina nella LLCrecidivata o refrattaria alla dosedi 70 mg/m2 per 2 giorni, siacome singolo agente, sia in asso-ciazione a rituximab, con possibi-lità di elevare la dose a 90mg/m2, se ben tollerata.Oltre che sulla comprovata sicu-rezza dell’associazione BR neipazienti con LLC recidivata, la scel-ta di questa combinazione, per iltrattamento del paziente del casosopra riportato, si è basata anche
sulla sua efficacia nei diversi sotto-gruppi genetici, del(11q) (RR92,3%), trisomia del 12 (RR 100%),IgHV (immunoglobulin heavychain variable) non-mutato (RR58,7%), eccezion fatta per del(17p)(RR 7,1%) (2).Nel paziente qui presentato la tol-lerabilità al trattamento è stataelevata, riportandosi neutropeniadi grado 2 (CTCAE v.3) soltanto nel5° e 6° ciclo. Il completo recuperodella conta dei neutrofili si è otte-nuto spontaneamente a 40 giornidall’ultima dose di bendamustina. Particolare attenzione deve essere
comunque riposta nell’impiego dirituximab 500 mg/m2. Infatti taleempirico incremento di dose,adottato negli studi di fase I/II confludarabina e ciclofosfamide, chene hanno dato indicazione nellaterapia della LLC, potrebbe nonessere necessario, in quanto evi-denze pre-cliniche non dimostre-rebbero la necessità di una com-pleta saturazione dei CD20 comepre-requisito all’ottenimento dellachemiosensibilizzazione (4). Dicontro, r ituximab 500 mg/m2
espone il paziente a un maggiorrischio di mielotossicità.
Bibliografia
1. Bergmann MA, Goebeler ME, Herold M,Emmerich B, Wilhelm M, Ruelfs C,Boening L, Hallek MJ; German CLL StudyGroup. Efficacy of bendamustine inpatients with relapsed or refractorychronic lymphocytic leukemia: results ofa phase I/II study of the German CLLStudy Group. Haematologica 2005;90(10):1357-1364.
2. Fischer K, Cramer P, Busch R et al.Bendamustine combined with rituximabin patients with relapsed and/or refracto-ry chronic lymphocytic leukemia: a multicenter phase II trial of the German ChronicLymphocytic Leukemia Study Group. J ClinOncol 2011;29(26):3559-3566.3.Cheson BD, Wendtner CM, Pieper A et al.Optimal use of bendamustine in chronic
lymphocytic leukemia, non-Hodgkin lym-phomas, and multiple myeloma: treat-ment recommendations from an interna-tional consenus panel. Clin LymphomaMyeloma Leuk 2010;10(1):21-27.4. Tam CS, Keating MJ. Selection of ritux-imab dosage in chronic lymphocyticleukemia: where is the evidence? LeukLymphoma 2012. [Epub ahead of print].
13
Presentazione del caso
Paziente, anamnesi, esameobiettivo e indagini diagnosticheUn uomo di 64 anni è giunto allanostra osservazione nel Marzo del2011 per sospetta neoplasia linfa-tica: a causa della comparsa di unaneoformazione al cavo ascellareera infatti stata eseguita una TC,che aveva evidenziato la presenzadi linfoadenomegalie in sede sot-tomentoniera e sottomandibolarebilateralmente (max 1,2 cm), insede ascellare sinistra (max 4,2cm) e destra, mediastinica sottoca-renale (2,5 cm) e cardiofrenicadestra (1,2 cm). Inoltre, a livelloaddominale, pacchetti linfonodali,in parte confluenti, erano presentiin sede celiaca (2,6 cm), ilare epati-ca (4,3 cm), paraortica (3 cm), inte-raortocavale (3 cm), iliaca comuneed esterna destra (4,5 cm), nell’adi-pe mesenteriale (3,5 cm) e ingui-nale bilateralmente (2,5 cm); fega-to e milza erano invece nei limitimorfovolumetrici. Le principaliindagini laboratoristiche, in parti-colare la lattato-deidrogenasi e l’emoglobina, erano nei limiti dinorma e la diagnosi è stata postasu biopsia escissionale di un pac-chetto linfonodale in sede ascella-re sinistra. La diagnosi istologicaera di linfoma non Hodgkin (LNH)follicolare, con pattern di crescita
nodulare, grado I-II WHO; la bio-psia osteomidollare non mostravaevidenza di infiltrazione da linfo-ma e si concludeva, pertanto, perLNH follicolare, stadio III A, FLIPI 3.
Approccio terapeutico
Nei linfomi a basso grado la malat-tia si presenta più spesso in stadioavanzato fin dal momento delladiagnosi. Il trattamento di 1ª linea,per il linfoma follicolare e gli altrilinfomi indolenti, è l’immunoche-mioterapia, che combina l’anticor-po monoclonale anti-CD20 rituxi-mab (R) con gli schemi di chemio-terapia CHOP (ciclofosfamide,doxorubicina, vincristina, predni-sone) o CVP (ciclofosfamide, vincri-stina, prednisone) o FM (fludarabi-na, novantrone). Per il paziente si èoptato per il regime R-CHOPq21 (x6). La TC finale ha evidenziato lapersistenza (per quanto associataa una riduzione numerica e di -mensionale) delle linfoadenome-galie segnalate al controllo prece-dente; il giudizio è stato, pertanto,di malattia resistente. Per talemotivo, nel Novembre del 2011, èstata avviata una terapia di 2ª lineacon il regime di combinazione R-BENDAq28 (bendamustina 90mg/m2/die e.v. ai giorni +1 e +2 erituximab 375 mg/m2 in perfusio-
ne venosa lenta al giorno +1); èstata praticata una profilassi anti-biotica e antivirale e antiemetici.Dopo 6 cicli, condotti con buonatolleranza individuale e modestatossicità ematologica o extraema-tologica (WHO grado 0-1), i lpaziente è stato sottoposto a unanuova TC, che ha evidenziato larisoluzione, pressoché completa,delle multiple linfoadenomegaliedescritte in precedenza in sedeascellare sinistra, mediastinica eaddominale; il giudizio è stato dirisposta completa. Nel Giugno del 2012 è stata avvia-ta la terapia di mantenimento conil rituximab a cadenza bimestrale(ne sono previste 12 somministra-zioni); al controllo più recente(Ottobre 2012) il paziente conser-va uno stato di remissione.
Discussione del caso erazionale delle scelteterapeutiche
Nonostante i risultati ottenuti dallamoderna chemioterapia dei linfo-mi indolenti, recentemente miglio-rati dalla combinazione con ilrituximab, circa il 15% dei pazientiha una malattia resistente; per talecategoria di pazienti è quindinecessario uno switch a un tratta-mento alternativo. Tra le opportu-
Efficacia del regime di combinazione rituximab ebendamustina nel linfoma indolente resistente al trattamento di prima linea: presentazione di un caso clinicoG. Quintini, C. Maugeri UO Ematologia Policlinico “P. Giaccone”, Palermo
G. QUINTINI, C. MAUGERI
14
nità più promettenti vi è, senzadubbio, la bendamustina, farmacocitostatico di vecchia generazionerecentemente rivalutato, concaratteristiche affini agli agentialchilanti e agli analoghi purinici. Il suo meccanismo d’azione è uni-co, grazie alle proprietà di antime-tabolita, che gli conferiscono unacross-resistenza solo parziale congli altri farmaci alchilanti; neglistudi clinici, condotti sui pazienticon linfoma indolente, la combi-nazione tra bendamustina e rituxi-mab si è dimostrata sinergica ed
estremamente efficace in soggettirefrattari/recidivati dopo che-mioimmunoterapia convenziona-le, inducendo una remissionecompleta in oltre il 90% dei casi,con PFS (sopravvivenza libera daprogressione) mediana di oltre 24mesi. Il caso da noi descritto sipone in linea con tali osservazioni,confermando l’efficacia di tale far-maco in un paziente con linfomafollicolare refrattario al trattamen-to di 1ª linea. Un altro argomento,a favore di questa combinazione, èla modesta tossicità (il nostro
paziente ha potuto effettuare tuttii cicli nei tempi previsti e senza ilricorso ai fattori di crescita e/o allatrasfusione di emocomponenti)con la schedula di somministrazio-ne da noi adottata e con la quale èstato approvato. Concludendo la bendamustina sipropone come un farmaco estre-mamente efficace e ben tolleratonel trattamento dei linfomi indo-lenti refrattari/recidivati; la combi-nazione con il rituximab ne mi -gliora l’efficacia senza aumentar-ne la tossicità.
Bibliografia
• Cheson BD, Friedberg JW, Kahl BS, Van derJagt RH, Tremmel L. Bendamustine pro-duces durable responses with an accept-able safety profile in patients with ritux-imab-refractory indolent non-Hodgkinlymphoma. Clin Lymphoma MyelomaLeuk 2010;10(6):452-457.
• Hoy SM. Bendamustine: a review of itsuse in the management of chronic lym-phocytic leukaemia, rituximab-refracto-ry indolent non-Hodgkin’s lymphomaand multiple myeloma. Drugs 2012;72(14):1929-1950.
• Korycka-Wołowiec A, Robak T. Pharmaco -kinetic evaluation and therapeutic activi-
ty of bendamustine in B-cell lymphoidmalignancies. Expert Opin Drug MetabToxicol 2012;8(11):1455-1468.
• Ohmachi K, Ando K, Ogura M et al.Japanese bendamustine lymphomastudy Group: multicenter phase II studyof bendamustine for relapsed or refracto-ry indolent B-cell non-Hodgkin lym-phoma and mantle cell lymphoma.Cancer Sci 2010;101(9):2059-2064.
• Rigacci L, Puccini B, Cortelazzo S et al.Bendamustine with or without rituximabfor the treatment of heavily pretreatednon-Hodgkin’s lymphoma patients: amulticenter retrospective study on
behalf of the Italian LymphomaFoundation (FIL). Ann Hematol 2012;91(7):1013-1022.
• Rummel MJ, Al-Batran SE, Kim SZ et al.Bendamustine plus rituximab is effectiveand has a favorable toxicity profile in thetreatment of mantle cell and low-gradenon-Hodgkin’s lymphoma. J Clin Oncol2005;23(15):3383-3389.
• Vidal L, Gafter-Gvili A, Gurion R, Raanani P,Dreyling M, Shpilberg O. Bendamustinefor patients with indolent B cell lymphoidmalignancies including chronic lympho-cytic leukaemia. Cochrane Database SystRev 2012;9:CD009045.
15
Presentazione del caso
Paziente, anamnesiIl paziente, maschio di 73 anni, siricovera nel Marzo del 2012. All’anamnesi patologica remotaemergono una gastroresezionerelativa al 1975 e una colecistecto-mia nel 2002. Nell’Aprile del 2010era pervenuto, alla nostra osserva-zione, per linfoma mantellare(MCL-mantle cell lymphoma),varietà polimorfa, stadio IV; dopo iltrattamento chemioterapico conrituximab, antraciclina liposomia-le, steroidi e vincristina (R-COMP)(6 cicli completati a Settembre del2010), era stata evidenziata unarisposta completa (RC).
Esame obiettivo e indaginidiagnosticheDa circa 2 mesi il paziente accusadispnea e marcata astenia, associa-te alla presenza di feci picee, men-tre all’esame obiettivo presentaottusità alla base polmonare sini-stra, milza debordante 4 cm dall’ar-cata costale, toni cardiaci tachiarit-mici; risultano nella norma la fun-zionalità epatorenale, mentre all’e-same emocromocitometrico si evi-denziano anemia (Hb 9,7 g/dL) conleucocitosi (GB 18,33x109/L) elinfocitosi (12,46x109/L), PLT neilimiti (297x109/L). Risultanoaumentati LDH (lattato deidroge-
nasi) (343 UI/L) e beta2-microglo-bulina (8,99 mg/l), ridotte ferritinae sideremia; negativi i marker perHIV, HCV (Hepatitis C virus) e HBV(Hepatitis B virus). All’esofagogastroduodenoscopiasi documenta una gastrite delmoncone, mentre con la colonsco-pia virtuale si evidenzia un infiltra-to sottomucoso a valle della valvo-la ileo-cecale. Alla TC total body simanifesta la presenza di linfoade-nomegalie del mediastino (9 cm) eretroperitoneali (4 cm); si associa-no anche splenomegalia e massi-vo versamento pleurico sinistro.Alla biopsia osteomidollare è pre-sente, invece, un infiltrato linfoidediffuso, coerente con localizzazio-ne da MCL, mentre dall’ECG simanifesta una fibrillazione atrialee all’ecocuore la FE (frazione diiniezione) risulta del 55%, ma condisfunzione diastolica.
Approccio terapeutico
Dopo aver eseguito un breve ciclodi terapia marziale per via e.v., conmiglioramento della crasi ematica,il paziente inizia una terapia di sal-vataggio con bendamustina alladose di 90 mg/m2 (giorni 1 e 4),associata a bortezomib alla dose di1,3 mg/m2 (giorni 1, 4, 8, 11) concicli della durata di 28 giorni; al 1°
ciclo si somministra anche rituxi-mab alla dose di 375 mg/m2 (ma ilpaziente risulta intollerante pergrave reazione con insufficienzarespiratoria durante la prima infu-sione, per cui prosegue il tratta-mento solo con bendamustina ebortezomib) e si associano profilas-si con sulfometossazolo, per 3 gior-ni alla settimana, e aciclovir alladose di 400 mg x 2/die p.o., nonchédigitale e diuretici. Dopo 2 cicli siregistra un miglioramento sogget-tivo, con normalizzazione dell’emo-globina e riduzione del versamen-to pleurico; i cicli programmati ven-gono quindi completati ad Agostodel 2012 con discreta tolleranza.Dopo il 1° ciclo si manifestano feb-bre per 4-5 giorni, in assenza diinfezioni evidenziabili, nonchéastenia, disturbi dispeptici e costi-pazione di grado 2 per tutta ladurata del trattamento; la tossicitàè prevalentemente ematologica,con neutropenia di grado 4 dopo il2° ciclo, in assenza di febbre e/osepsi; è stata associata terapia conG-CSF (granulocyte colony-stimu-lating factor) dopo il 2° ciclo e pro-filassi con levofloxacina quandoN<0,5x109/L. A Set tembre del 2012è stata effettuata la stadiazione conbiopsia osteomidollare e TC totalbody, che hanno documentato unaRC, mentre persiste la remissione aun breve follow-up di 3 mesi.
L’associazione di bendamustina e bortezomib è efficace etollerata in un caso di linfoma mantellare recidivatoA. FragassoU.O. di Ematologia, Ospedale “Madonna delle Grazie”, ASM Matera
A. FRAGASSO
16
Discussione del caso erazionale delle scelteterapeutiche
Il MCL ha un decorso clinico spes-so aggressivo, invariabilmentecaratterizzato da recidive. La so -pravvivenza è migliorata negli ulti-mi anni, grazie alle attuali terapiedi combinazione e di supporto, mal’esito è infausto: non esiste infatti,allo stato attuale, un trattamentostandard sia alla diagnosi che nel-le recidive (1). Nei pazienti non eleggibili a untrattamento ad alte dosi, con sup-porto di cellule staminali, in 2ªlinea sono stati utilizzati sia ilrituximab, più spesso in associa-zione con chemioterapia (ad es. R-FCM-r i tux imab-f ludarabina ,ciclofosfamide e mitoxantrone)(2), sia il bortezomib in monotera-pia (3) o in associazione con rituxi-mab con schedula settimanale (4).
La bendamustina è un alchilantebifunzionale di recente utilizzo,anche se nato nel 1963, è statoapprovato per il trattamento deilinfomi indolenti recidivati; inassociazione con rituximab hapro dotto risultati rilevanti in pa -zien ti con MCL recidivato (5,6) e lacombinazione di bendamustinacon bortezomib e rituximab è sta-ta utilizzata in 7 pazienti con MCL,ampiamente pretrattati, alcunirefrattari, con risposte globali del71% e PFS (progression free survi-val) a 2 anni del 47% (7). In questostudio la schedula era la seguente:bendamustina 90 mg/m2 (giorni 1e 4); bortezomib 1,3 mg/m2 (giorni1, 4, 8, 11), rituximab 375 mg/m2
(giorno 1); erano programmati 6cicli di 28 giorni e su una popola-zione di 30 pazienti (22 con linfo-ma follicolare) il 61% completava iltrattamento previsto. Com ples -siva men te si registravano eventi
avversi seri nel 26% dei casi. Nel nostro paziente abbiamoadottato la stessa schedula, anchese il rituximab non è stato utilizza-to per intolleranza; tuttavia il trat-tamento è risultato efficace contossicità accettabile, considerandola situazione complessa del pa -ziente con anemizzazione im por -tante, conseguente all’infiltrazio-ne midollare e al sanguinamentodigestivo, sia alla situazione car-diocircolatoria (fibrillazione atrialee versamento pleurico significati-vo). Per età e condizioni clinichenon era proponibile l’utilizzo diantracicline (in 1ª linea era statautilizzata la formulazione liposo-miale) né di trattamenti più ag -gressivi; per altro verso l’importan-za della sintomatologia suggerival’opportunità di un trattamento dirapida efficacia e un più lungo fol-low-up è necessario quindi pervalutare l’outcome a distanza.
L’ASSOCIAZIONE DI BENDAMUSTINA E BORTEZOMIB È EFFICACE E TOLLERATA IN UN CASO DI LINFOMA MANTELLARE RECIDIVATO
17
Bibliografia
1. McKay P, Leach M, Jackson R, Cook G,Rule S. Guidelines for the investigation andmanagement of mantle cell lymphoma. BrJ Haematol 2012;159(4):405-426.2. Forstpointner R, Dreyling M, Repp R etal.; German Low-Grade Lymphoma StudyGroup. The addition of rituximab to acombination of fludarabine, cyclophos-phamide, mitoxantrone (FCM) signifi-cantly increases the response rate andprolongs survival as compared with FCMalone in patients with relapsed andrefractory follicular and mantle cell lym-phomas: results of a prospective ran-domized study of the German Low-Grade Lymphoma Study Group. Blood
2004;104(10):3064-3071.3. Goy A, Bernstein SH, Kahl BS et al.Bortezomib in patients with relapsed orrefractory mantle cell lymphoma: updat-ed time-to-event analyses of the multi-center phase 2 PINNACLE study. Ann Oncol2009;20(3):520-525.4. Agathocleous A, Rohatiner A, Rule S etal. Weekly versus twice weekly borte-zomib given in conjunction with ritux-imab, in patients with recurrent follicularlymphoma, mantle cell lymphoma andWaldenström macroglobulinaemia. Br JHaematol 2010;151(4):346-353.5. Rummel MJ, Al-Batran SE, Kim SZ et al.Bendamustine plus rituximab is effective
and has a favorable toxicity profile in thetreatment of mantle cell and low-gradenon-Hodgkin’s lymphoma. J Clin Oncol2005;23(15):3383-3389.6. Robinson KS, Williams ME, van der JagtR et al. Phase II multicenter study of ben-damustine plus rituximab in patients withrelapsed indolent B-cell and mantle cellnon-Hodgkin’s lymphoma. J Clin Oncol2008;26(27):4473-4479.7. Friedberg JW, Vose JM, Kelly JL et al. Thecombination of bendamustine, borte-zomib, and rituximab for patients withrelapsed/refractory indolent and mantlecell non-Hodgkin lymphoma. Blood2011;117(10):2807-2812.
18
Presentazione del caso
PazienteLa paziente è una donna di 45anni, con anamnesi negativa peraltre patologie degne di nota.
AnamnesiLa sintomatologia ha inizio nelFebbraio del 2007, con la comparsadi astenia, e la paziente viene quin-di sottoposta a terapia multivitami-nica ricostituente senza tuttaviaottenere un particolare beneficio. AOttobre dello stesso anno si verifi-ca la comparsa di linfoadenomega-lia laterocervicale destra (del dia-metro di circa 3 cm), non dolentealla palpazione e si registra, inoltre,la presenza di febbricola, doloreosseo diffuso al rachide, sudorazio-ne notturna, tosse secca e dimagri-mento di circa 5 kg.
Esame obiettivo e indaginidiagnosticheNell’ambito dell’inquadramentodiagnostico la paziente effettuaun esame TC, che evidenzia:• un cospicuo slargamento delmediastino superiore con margi-ni marcatamente irregolari esegni di irregolare incrementodensitometrico dopo contrasto;
• la presenza di numerosi linfono-di delle stazioni laterocervicali disignificato linfomatoso;
• una notevole ipertrofia del lobodestro della tiroide e linfonodi didimensioni aumentate delle sta-zioni ilari e delle catene mammarie.
All’esame bioptico del linfonodolaterocervicale viene posta quindidiagnosi di linfoma di Hodgkin(LH) a sclerosi nodulare, grado II,con ampie aree di necrosi. La dia-gnosi conclusiva è quella di LH asclerosi nodulare, stadio IV-B. Almomento della diagnosi sono pre-senti leucocitosi (GB 10.300/mm3),anemia (11,4 g/dl), piastrinosi (PLT708.000/mm3), incremento dellaVES (62), PCR e ipoalbuminemia.
Approccio terapeuticoIl programma terapeutico ha pre-visto una polichemioterapia anti-blastica di 1ª linea secondo loschema ABVD (adriamicina, bleo-micina, vinblastina, dacarbazina)per un totale di 6 cicli. Dopo il 2° ciclo di terapia è stataeffettuata una rivalutazione adinterim PET (Febbraio 2008), che hadocumentato la scomparsa delleplurime aree di aumentata fissa-zione del tracciante metabolico,descritte nella precedente imma-gine in sede mediastinica, linfono-dale sovra- e sottodiaframmatica,splenica e scheletrica; non è piùevidenziabile, invece, il versamen-to pleurico sinistro. Dopo il 6° ciclodi terapia è stata effettuata una
rivalutazione TC (Maggio 2008),che ha mostrato la regressione del-le tumefazioni linfonodali e la per-sistenza del tessuto mediastinico,anche se in evidente regressionevolumetrica rispetto all’esame pre-cedente; viene quindi classificatacome risposta parziale e avviata aprogramma di follow-up. Nel mese di Luglio del 2008 (unmese dalla remissione parziale) siverifica la comparsa di tumefazio-ne linfonodale laterocervicaledestra, che viene sottoposta aescissione chirurgica ed esamebioptico, sul quale viene posta dia-gnosi di recidiva linfonodale di LHsclerosi nodulare. La paziente viene sottoposta aulteriore staging diagnostico eavviata a terapia di 2ª linea secon-do lo schema DHAP (desametaso-ne, cisplatino, Ara-C, prednisone)per 3 cicli, con raccolta di cellulestaminali emopoietiche (CSE)autologhe. Nel Settembre del 2008, primadell’autotrapianto, effettua unarivalutazione di malattia tramitePET, che documenta la scomparsadi accumuli patologici. A Ottobredel 2008 viene effettuato un tra-pianto autologo di CSE periferi-che (condizionamento conFEAM- fotemustina più etoposi-de, citarabina e melfalan) e si regi-stra una remissione completa alla
La bendamustina come possibile terapia di salvataggio nel linfoma di Hodgkin refrattarioF. Castagna, S. Impera, U. ConsoliARNAS Garibaldi Catania, P.O. Nesima, U.O.C. di Ematologia, Catania, Italia
19
rivalutazione post-trapianto. NelFebbraio del 2009 si verifica laricomparsa di linfoadenomegalielaterocervicali, sulle quali vieneposta diagnosi di recidiva dimalattia linfonodale; la paziente,quindi, viene avviata a poliche-mioterapia antiblastica di 3ª lineasecondo lo schema BEACOPP(bleomicina, etoposide, adriami-cina, ciclofosfamide, vincristina,procarbazina, prednisone) inten-sificato per un totale di 6 cicli, daMarzo a Ottobre del 2009. Alla valutazione TC/PET post-trat-tamento, la paziente ottiene laremissione completa. Nel Marzo del 2010 la pazienteviene sottoposta a trapianto diCSE al logeniche da cordoneombelicale e nel Luglio del 2011,per la comparsa di linfoadenome-galie e addensamenti polmonari,vengono effettuati prelievi biop-tici, che documentano una rica-duta di LH (CD20-/CD30+) conimportante fibrosi. La pazienterifiuta ulteriori cicli di poliche-mioterapia aggressiva ma, allaluce della prospettata buona tol-lerabilità e del profilo di tossicitàdi bendamustina, accetta unaproposta di trattamento di salva-taggio post-allotrapianto conbendamustina (90 mg/m2 per 2giorni consecutivi ogni 28 giorniper 6 cicli). Da Marzo ad Agosto
del 2012 vengono praticati 6 ciclidi bendamustina; a una rivaluta-zione intermedia, dopo 3 cicli, vie-ne documentata un’inizialeregressione delle linfoadenome-galie e delle dimensioni dellelesioni polmonari, con negativitàdel quadro PET. Alla rivalutazionefinale TAC post-trattamento, con6 cicli di bendamustina, si registraun quadro di risposta completaPET e la remissione completa allaTAC; la paziente, allo stato attuale,è in programma per un ulterioretrattamento con brentuximab.
Discussione del caso erazionale delle scelteterapeutiche
I risultati terapeutici, conseguiti nelLH, costituiscono uno dei principa-li successi della medicina oncoe-matologica e la maggior parte deipazienti, che oggi si ammala di talepatologia, può ragionevolmentesperare in una guarigione; nono-stante ciò, alcune problematicherestano aperte, come l’approccioterapeutico ottimale per i pazientirefrattari o con ricaduta dopo tra-pianto di CSE; infatti, ad oggi, aldilàdella terapia con alte dosi e auto-trapianto con CSE, non vi è unaterapia di salvataggio standard;esistono tuttavia dei nuovi farma-
ci, come il brentuximab vedotin, icui risultati sono incoraggianti mail cui impiego, al momento nellapratica clinica, è ristretto a unnumero esiguo di pazienti (1). Le altre opzioni terapeutiche, nelLH refrattario, sono rappresentateda diversi farmaci, facilmentedisponibili, che hanno dimostratodi avere una qualche efficacia cli-nica. Tra questi vi è il rituximab (nelLH a predominanza linfocitaria), lalenalidomide, il bortezomib e labendamustina (2-4). Diverse segnalazioni dimostranoche la bendamustina, utilizzatada sola o in associazione al rituxi-mab, in pazienti affetti da LH inricaduta, ha mostrato buoni risul-tati in termini di risposta allaterapia e a fronte di una bassatossicità (4,5) . I l caso cl inicodescritto, insieme ai dati presentiin letteratura, rafforza l’idea che,in pazienti estremamente fragili,la cui terapia ha già previsto varielinee di trattamento, la benda-mustina possa rappresentareuna valida opzione terapeutica intermini di rapporto tra efficacia ebassa tossicità; ci sembra giusto,dunque, ipotizzare un ruolo dellabendamustina nella strategiaterapeutica da mettere in attonel la dif f ic i le gestione deipazienti con LH sottoposti a tera-pia di salvataggio.
LA BENDAMUSTINA COME POSSIBILE TERAPIA DI SALVATAGGIO NEL LINFOMA DI HODGKIN REFRATTARIO
20
Bibliografia
1. Gopal AK, Ramchandren R, O’ConnorOA. Safety and efficacy of brentuximabvedotin for Hodgkin lymphoma recurringafter allogeneic stem cell transplantationBlood 2012;120(3):560-568. 2. Jona A, Younes A. Novel treatmentstrategies for patients with relapsed clas-sical Hodgkin lymphoma. Blood Rev
2010;24(6):233-238. 3. Mendler JH, Kelly J, Voci S et al.Bortezomib and gemcitabine in relapsedor refractory Hodgkin’s lymphoma. Annalsof Oncology 2008;19(10):1759-1764. 4.Magyari F, Simon Z, Barna S, Udvardy M,Varoczy L, Illes A. Successful administrationof rituximab-bendamustine regimen in the
relapse of Hodgkin lymphoma after autol-ogous hemopoietic stem cell transplanta-tion. Hematol Oncol 2012;30(2):98-100.5. Mian M, Farsad M, Pescosa N et al.Bendamustine salvage for the treatment ofrelapsed Hodgkin’s lymphoma after allo-geneic bone marrow transplantation. AnnHematol 2012;92(1):121-123.
F. CASTAGNA, S. IMPERA, U. CONSOLI
21
Presentazione del caso
Paziente e anamnesiNell’Aprile del 2010 giunge, allanostra attenzione, un paziente di 67anni, per il riscontro di una modestalinfocitosi (WBC 14.350/mm3,L=65%), persistente da almeno 2anni in assenza di sintomi B.L’esame obiettivo mostra un’epato-megalia di 1° grado e i restanti esa-mi ematochimici risultavano nellanorma. In anamnesi patologicaremota si segnalano malattia diver-ticolare intestinale, broncopneu-mopatia cronica ostruttiva (BPCO)moderata, cardiopatia ischemicacronica, diabete mellito di tipo II.
Esame obiettivo e indaginidiagnosticheIl work-up diagnostico include gliaccertamenti di seguito indicati.• Tipizzazione linfocitaria: linfoci-tosi matura con fenotipo CD19+,CD20+, S-Ig lambda +, CD5+,CD22+, CD23-, CD38+.
• Biopsia osteo-midollare: localiz-zazione midollare pari al 30-40%di linfoma non-Hodgkin (LNH)mantellare.
• FISH su midollo: t (11; 14).• TAC torace-addome con mdc:non evidenza di linfoadenome-galie significative.
Si conclude quindi per LNH man-tellare stadio IV A.
Approccio terapeutico,valutazione a distanza eaggiustamentiterapeutici
Il paziente viene avviato a follow-up clinico-laboratoristico, fino adAprile del 2011 quando, per l’in-cremento della linfocitosi (WBC40.780/mm3; L 84%), viene sotto-posto a terapia citoriduttiva con 6cicli di clorambucil al dosaggio 10mg/die per 10 giorni al mese, ter-minati, a Settembre del 2011, conl’ottenimento di una remissioneparziale. Nel Marzo del 2012 sievidenzia una progressione dimalattia con linfocitosi (WBC57.790/mm3 e L 48.660/mm3) esplenomegalia (17 cm) al control-lo ecografico; il paziente vienequindi sottoposto a chemiotera-pia di 2ª linea secondo lo schemabendamustina-rituximab, di cuiha eseguito 6 cicli, terminati nelSettembre del 2012. La terapia èben tollerata, ad eccezione di unatransitoria tossicità epatica (iper-transaminasemia di grado 2secondo il WHO), che determina ilprocrastinarsi del 2° ciclo di circa15 giorni. La rivalutazione finaledi malattia mostra una remissio-ne completa della patologia linfo-matosa e il paziente, pertanto, èstato avviato a follow-up clinico-laboratoristico.
Discussione del caso erazionale delle scelteterapeutiche
Il LNH mantellare è, a tutt’oggi,una malattia incurabile con la che-mioterapia convenzionale; studirecenti ne hanno evidenziatoun’eterogeneità clinica (1) per lapresenza di forme indolenti (2),che potrebbero beneficiare di untrattamento “light”, soprattutto nelcaso di pazienti over 65 anni. Nel nostro caso il LNH mantellareè apparentemente indolente, perla presenza di una linfocitosi croni-ca ed esclusivo interessamentomidollare, sebbene l’immunofe-notipo non evidenzi una CD23positività e una restrizione per lecatene κ, associate in un recentestudio (3) ad alcune forme nonaggressive. Il decorso clinico indolente, l’etàanagrafica e le significative co -morbidità hanno suggerito un’i-niziale fase di “wait and see”,seguita poi da una terapia conclorambucil con la finalità di con-tenere la linfocitosi e di non alte-rare la qualità di vita del paziente.La decisione circa la terapia di 2ªlinea poteva invece rappresenta-re un problema clinico ben piùsignificativo, in quanto le comor-bidità avevano un ruolo fonda-mentale nell’influenzare la scelta
Un caso di linfoma mantellare “indolente” in un paziente anziano “fragile”M. Montanari Clinica di Ematologia, Azienda Ospedaliero-Universitaria Ospedali Riuniti Ancona
M. MONTANARI
22
del chemioterapico da associareal rituximab. Regimi CHOP (ciclofosfamide,doxorubicina, vincristina, predni-sone)-like erano controindicati dacardiotossicità delle antracicline,neurotossicità intestinale dellavincristina, uso dello steroide nel
diabete. La bendamustina rappre-sentava il farmaco ideale in quan-to monoterapia efficace (assenzadi cross-resistenza con altri agentialchilanti) (4) con moderata tossi-cità ematologica ed extra-emato-logica.Il prolungarsi dell’aspettativa di
vita e l’età mediana di esordio delLNH mantellare determinerannouna sempre maggiore frequenzadi pazienti anziani affetti da questapatologia e con comorbidità asso-ciate, che richiederanno unapproccio sistematico e omoge-neo a questa problematica (5).
Bibliografia
1. Shah BD, Martin P, Sotomayor EM. Mantlecell lymphoma: a clinically heterogeneousdisease in need of tailored approaches.Cancer Control 2012;19(3):227-235.2. Furtado M, Rule S. Indolent mantle celllymphoma. Haematologica 2011;96(8):1086-1088.3. Ondrejka SL, Lai R, Smith SD, Hsi ED.
Indolent mantle cell leukemia: a clinico-pathological variant characterized by iso-lated lymphocytosis, interstitial bone mar-row involvement, kappa light chainrestriction, and good prognosis. Haema -tolo gica 2011;96(8):1121-1127. 4.Warsch S, Hosein PJ, Maeda LS, AlizadehAA, Lossos IS. A retrospective study evalu-
ating the efficacy and safety of ben-damustine in the treatment of mantle celllymphoma. Leuk Lymphoma 2012;53(7):1299-1305.5. Vose JM. Mantle cell lymphoma: 2012update on diagnosis, risk-stratification,and clinical management. Am J Hematol2012;87(6):604-609.
23
Presentazione del caso
Paziente e anamnesiPaziente maschio di 76 anni,affetto da cardiopatia ischemicacronica e sindrome delle apneenotturne in terapia con CPAP(continuous positive airway pres-sure), seguito per un linfoma nonHodgkin (LNH) follicolare grado3A e per una leucemia acuta mie-loide (LAM) evoluta da displasiatrilineare.
Approccio terapeutico
L’esordio del linfoma è avvenutonel 2004, in stadio III A, FLIPI inter-medio (1); il paziente viene quindisottoposto a chemioterapia confludarabina-ciclofosfamide (6 ciclida Febbraio e a Luglio del 2004): laremissione completa (RC) è statadocumentata attraverso una TAC ela recidiva di malattia si è verificatanel 2008, sempre tramite TAC. Labiopsia confermava un LNH folli-colare grado 3A e il paziente era instadio III A FLIPI (follicular lympho-ma international prognosticindex) alto; inizia quindi una tera-pia con rituximab, ciclofosfamide,vincristina, doxorubicina liposo-miale, prednisone (2) (Aprile-Agosto 2008), ottenendo II RCconfermate dalla TAC.
A Ottobre-Novembre del 2008 simanifestano ripetuti episodi infet-tivi e con lo sviluppo di pancitope-nia transitoria e si pone, quindi, lanecessità di ricovero e di tratta-menti antibiotici. Nel Dicembredel 2008 il paziente viene ricovera-to in urgenza per la perforazioneintestinale su ileite acuta ischemi-ca e nuovo sviluppo di pancitope-nia. L’aspirato midollare (BM) indi-cava anemia refrattaria con ecces-so di blasti tipo 1 (RAEB1) (3),cariotipo normale, IPSS INT 1 (4).Dopo la dimissione proseguono icontrolli e lento ma completorisulta il recupero dei valori dell’e-mocromo. Nel Dicembre del 2009si presenta una recidiva di LNH, instadio III. I l paziente viene sottoposto arituximab in monoterapia (4 som-ministrazioni tra Dicembre eGennaio del 2010), con una conse-guente remissione parziale. NelFebbraio del 2010 inizia il manteni-mento con rituximab bimestrale ea Febbraio del 2011: III RC (TC e PETnegative). Il paziente prosegue il manteni-mento ma a Settembre 2011 simanifesta lo sviluppo di neutrope-nia persistente di grado III; il man-tenimento viene a questo puntosospeso. A Ottobre del 2011 ese-gue un BM: emerge un quadro diLAM con alterazioni mielodispla-
stiche correlate, blasti 30%. Il cario-tipo è normale. A Novembre del2011 si manifesta una recidiva dilinfoma (TC e PET positive), stadioII, ma il paziente è asintomatico; sidecide pertanto di iniziare unaterapia con 5 azacitidina (5) (Di -cembre 2011) e, eseguiti 2 cicli,viene sospesa a Febbraio del 2012per peggioramento dei valoriematici e progressione del linfo-ma. Inizia quindi una terapia conbendamustina-rituximab (6) (Feb -braio-Agosto 2012) e si ottiene laIV RC (TC e PET negative). La panci-topenia migliora, inoltre, in corsodi terapia. Esegue un BM (a Set -tembre del 2012) dove si eviden-ziano aspetti mielodisplastici acarico della mielopoiesi, con unariduzione della quota blasticaattualmente <5%.
Discussione del caso erazionale delle scelteterapeutiche
Il paziente permane, tutt’ora, in RCper il linfoma e mantiene valoridell’emocromo stabilmente all’in-terno dei limiti di norma, in asso-luta assenza di necessità trasfu-sionali. La scelta di sottoporlo pri-ma a una terapia con 5-azacitidinasi rifaceva ad alcune segnalazionidi efficacia della terapia epigene-
La bendamustina funziona anche nelle leucemie acute?G. Musuraca*, D. Cangini*, M. Ceccolini*, M.B. Giannini*, A. Lucchesi*, S. Ronconi*, G. Poletti**, A. Valenti**, M. Tonelli**, P. Fattori**Istituto Scientifico Romagnolo per lo Studio e la Cura dei Tumori IRCSS**Laboratorio Unico Area Vasta Romagna
G. MUSURACA, D. CANGINI, M. CECCOLINI, M.B. GIANNINI, A. LUCCHESI, S. RONCONI, G. POLETTI,A. VALENTI, M. TONELLI, P. FATTORI
24
tica anche in malattie linfomatose(5) oltre che nelle LAM e alla nonsintomaticità del linfoma in quelmomento; invece la successivaterapia con bendamustina erituximab, che ha sicuramentecomportato dei rischi, per i valoriematologici dovuti alla presenzadella LAM, tuttavia in quelmomento è sembrata la terapiache maggiormente presentavacaratteristiche di scarsa tossicità,di efficacia antilinfoma ed even-tualmente anche di possibileazione citoriduttiva nei confronti
della LAM (6). I sintomi principalidel paziente difatti , in quelmomento, erano dovuti alla pro-gressione del linfoma piuttostoche alla LAM. La terapia epigeneti-ca peraltro, se anche avesse potu-to funzionare, avrebbe comunqueverosimilmente impiegato varimesi. L’esito del BM pre- e post-terapia è stato valutato dallo stes-so esaminatore, a conferma deldato e la risposta midollare si èconfermata nel persistente mi -glioramento dei valori ematiciperiferici, dopo il trattamento. Le
nostre osservazioni sono coerenticon le successive pubblicazioni,che hanno confermato il profilo disicurezza/efficacia di bendamu-stina nelle LAM (7) e che suggeri-scono ulteriori investigazioni delfarmaco in questa patologia;abbiamo pertanto proposto unprotocollo pilota che preveda l’u-so di bendamustina in combina-zione con ulteriori farmaci neltrattamento di pazienti con LAM.Tale proposta è attualmente infase di valutazione da parte dellacasa farmaceutica.
Bibliografia
1. Buske C, Hoster E, Dreyling M et al. TheFoll icular Lymphoma InternationalPrognostic Index (FLIPI) separates high-r isk from intermediate- or low-riskpatients with advanced-stage follicularlymphoma treated front-line with ritux-imab and the combination of cyclophos-phamide, doxorubicin, vincristine, andprednisone (R-CHOP) with respect totreatment outcome. Blood 2006;108(5):1504-1508. 2. Visani G, Ferrara F, Alesiani F et al. R-COMP 21 for frail elderly patients with
aggressive B-cell non-Hodgkin lym-phoma: a pilot study. Leuk Lymphoma2008; 49(6):1081-1086.3. Vardiman JW, Harris NL, Brunning RD.The World Health Organization (WHO)classification of the myeloid neoplasms.Blood 2002;100(7):2292-2302.4. Greenberg P, Cox C, LeBeau MM et al.International scoring system for evaluat-ing prognosis in myelodysplastic syn-dromes. Blood 1997;89(6):2079-2088.5. D’Alò F, Leone G, Hohaus S. Response to5-azacytidine in a patient with relapsed
Hodgkin lymphoma and a therapy-relat-ed myelodysplastic syndrome. Br JHaematol 2011;154(1):141-143. 6. Strupp C, Knipp S, Hartmann J,Gattermann N, Haas R, Germing U. A pilotstudy of bendamustine in elderly patientswith high-risk MDS and AML. LeukLymphoma 2007;48(6):1161-1166.7. Chacar C, Jabbour E, Ravandi F. Phase I-IIstudy of bendamustine in patients withacute leukemia and high risk myelodys-plastic syndrome. Clin LymphomaMyeloma Leuk 2012;12(3):197-200.