Tecnologia del silicio Perche il silicio Crescita del cristallo Preparazione del wafer La tecnologia...
-
Upload
robertina-amore -
Category
Documents
-
view
233 -
download
2
Transcript of Tecnologia del silicio Perche il silicio Crescita del cristallo Preparazione del wafer La tecnologia...

Tecnologia del silicioPerche’ il silicio
• Crescita del cristallo• Preparazione del wafer
La tecnologia planare•Ossidazione termica•Tecniche litografiche•Diffusione dei droganti•Impiantazione ionica•Tecniche di epitassia
Tecniche di deposizione•Silicio policristallino•Dielettrici e passivazione•Metallizzazioni•Planarizzazione
Packaging

Perche’ il silicio
I primi dispositivi a semiconduttore utilizzavano il Germanio (Ge), con la formazione di giunzionitramite “lega”, un processo piu’ facile nel Ge (che fonde a937 ºC) rispetto al Si (che fonde a 1412 ºC)
Ge: ridotto energy gap
• alte correnti inverse• limitato campo operativo ad alta T (max 70°C)• basse tensioni di breakdown
Il Germanio non possiede un ossido stabile

Germanio vs. Silicio
Germanio Silicio
Mobilita’ (e-) 3900 1417 [cm2/V s]
Mobilita’ (h+) 1900 471 [cm2/V s]
Energy-gap (300K) 0.67 1.12 [eV]
Concentrazione diportatori intrinseci ni
@300K: 2.41013 1.451010 [cm-3]@400K: 1015 7.51012 [cm-3]
Campo elettrico critico 810 3105 [V/cm]

Processo planare del silicio
Il silicio possiede un ossido stabile (SiO2)
•L’SiO2 e’ un ottimo isolante
•L’acido fluoridrico (HF) rimuove il biossido di silicio ma non il Si
•L’SiO2 agisce come maschera nei confronti della diffusione di drogante
•L’SiO2 riduce la densita’ di stati di interfaccia sulla superficie del Si
•L’SiO2 puo’ essere usato come dielettrico delle strutture MOS

SiO2
Si
wafer di silicio con uno strato di ossido termico in superficie

SiO2
Si
SiO2
selettivamenterimosso

SiO2
Si
deposizione di drogante

SiO2
Si
atomi droganti depositati sulle superfici esposte

SiO2
Si
Durante un trattamento termico gli atomidroganti diffondono nel Si ma non apprezzabilmente
nell’ossido

Crescita del cristallo
Obiettivi:•monocristallo di Si privo di difetti•di grande diametro (fino a 12”)•di purezza di 1 parte per miliardo
(1013 cm-3 impurezze su 51022 cm-3
atomi di silicio)
Tecniche:•Metodo Czochralski•Metodo float-zone (zona fusa mobile)




Metodo Czochralski
Peso del lingotto: da 20 a 150 kg
Velocita’ di crescita:

Metodo float-zone(a zona fusa mobile)
Le impurezze vengono segregate nella zona fusa
Adatto per silicio ultrapuro( = 20-100 -cm)
Meno dell’1% dell’ossigenopresente con Czochralski

Dopo taglio
Dopo arrotondamentodel bordo
Dopo lappatura
Dopo attacco chimico
Dopo lucidatura
1 mil = 25 m


Ossidazione termica del silicio
Ossido nativo: 2 nm a 300 K
Ossidazione termica: gli atomi di silicio in superficie si legano con ossigeno
ossido stechiometrico (SiO2)buona qualita’ dell’interfaccia Si/SiO2
proprieta’ elettriche stabili e controllabili
Deposizione: sia il silicio che l’ossigeno sono trasportatisulla superficie del wafer dove reagiscono tra loro
strati di passivazione

Ossidazione termica
in tubo di quarzo a temperature tra 850°C e 1100°C
la velocita’ di reazione aumenta con la temperaturasecondo la legge di Arrheniusv A exp (-Ea/kT) Ea = energia di attivazione [eV]
Ossidazione “dry” Si(s) + O2(g) SiO2(s)
Ossidazione “wet” (con vapore acqueo - piu’ rapida !)
Si(s) + 2H2O(g) SiO2(s) + 2H2(g)



Ossidazione termica del silicio
L’ossidazione avviene all’interfaccia Si-SiO2
le specie ossidanti devono attraversare lo stratodi ossido precedentemente formato
nella fase iniziale, a basse T, con strati di SiO2 sottili : crescita limitata dallavelocita’ di reazione superficiale
a T elevate e con ossidi spessi:crescita limitata dalla diffusione dellespecie ossidanti attraverso l’SiO2 gia’formato.

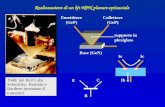
F(1) = flusso della corrente gassosa alla superficieF(2) = diffusione delle specie ossidanti attraverso SiO2
F(3) = velocita’ di reazione all’interfaccia SiO2/Si
C0 = concentrazione delle specie ossidanti alla superficieC1 = concentrazione delle specie ossidanti all’interfaccia SiO2/Si

Ossidazione termica
Tre fasi:
(1) trasferimento dalla fase gassosa all’SiO2
(2) diffusione attraverso l’SiO2 gia’ formato
(3) reazione con il Si sottostante

Trasferimento dalla fase gassosa all’SiO2
F(1) = h(C* - C0)
Ossidazione termica
F(1) = flusso della corrente gassosa alla superficie h = coefficiente di trasferimento di massa in fase gassosa C*= concentrazione delle specie ossidanti nell’ossido all’equilibrio C0= concentrazione alla superficie

F( DC C
xi
ox
2 0)( )
Ossidazione termica
Diffusione attraverso l’SiO2 gia’ formato
D = diffusivita’
xox = spessore dell’ossido
(C0 - Ci)/xox = gradiente di concentrazione in SiO2

Ossidazione termica
Reazione con il Si all’ interfaccia SiO2/Si
F(3) = ks Ci
A regime:F(1)=F(2)=F(3)=F
h C C DC C
Xk C Fo
o i
oxs i( )
( )*

DC C
XFo i
ox
( )
F xDk
DCoxs
oFHG
IKJ
k C Fs i
CFki
s

FDC
xDk
o
oxs
F h C Co ( )* CFh
Co*
FD C F
hx D
koxs
( )*

FD C F
hx D
koxs
( )*
F(x D k DC F(D h
F(x D k D h DC
F(x k D k h k C
Fk C
k h x k D
ox s
ox s
ox s s s
s
s ox s
) )
)
)
( )
*
*
*
*
1
1

Nox=n. molecole della specie ossidante nell’ossido per unita’ di volume
2.2 1022 molecole/cm3 di SiO2
Nox = 2.2 1022 cm-3 per O2 seccoNox = 4.4 1022 cm-3 per H2O
Velocita’ di crescita dell’ossido:
Rdxdt
FN
k CN k h x k D
ox
ox
s
ox s ox s
*
( )1

Rdxdt
FN
k CN k h x k D
ox
ox
s
ox s ox s
*
( )1
( )*
1 k h x k D dxk CN
dts ox s oxs
ox
Dk
Dh
x dxDCN
dts
ox oxox
FHG
IKJ
*
Dk h
x dxDCN
dts
ox oxox
1 1
FHG
IKJ
FHG
IKJ
*

Dk h
x dxDCN
dts
ox oxox
1 1
FHG
IKJ
FHG
IKJ
*
x Dk h
xDCN
toxs
oxox
2 21 1 2
FHG
IKJ
*
( )
xA t
A Box
LNMM
OQPP2
14
12
( )
A Dk hs
LNM
OQP2
1 1
BDCN ox
2 *

xA t
A Box
LNMM
OQPP2
14
12
( )
e’ lo shift temporale legato al fatto chea t=0 e’ gia’ presente l’ossido nativo xox(0)
tempi brevi: crescita limitata dalla reazione superficiale
tempi lunghi: crescita limitata dalla diffusione attraverso l’SiO2
x B t Btox ( )
x B A tox ( )

A Dk hs
LNM
OQP2
1 1coefficiente di crescita
parabolico
coefficiente di crescita lineare:dipende dall’orientazione cristallografica del cristallo: in (111) piu’ rapida che in (100)
BA
La velocita’ di crescita dipende da:
•temperatura•ambiente ossidante•drogaggio del substrato

Durante l’ossidazione, parte del silicio in superficie viene “consumato”:
Si02 : 2.2 1022 atomi/cm3
Si: 5 1022 atomi/cm3
Lo spessore di silicio consumato e’0.44 volte lo spessore del SiO2 che si forma

D = D0 exp(-EA/kT)


Spessore dell’ossido : Si (111)
Dry Wet