Regolazione della trascrizione I - BioPD della... · l’attivazione di una proteasi (DegS) che...
Transcript of Regolazione della trascrizione I - BioPD della... · l’attivazione di una proteasi (DegS) che...
Regolazione della trascrizione I:sigma diversi → oloenzimi diversi → preferenza per
promotori diversi → tx geni diversi
Regolazione della trascrizione II:L' OPERONE del lattosio
TESTO: LEWIN’s GENES X, CAPITOLI 19 E 26
LEWIN IL GENE VIII CAPITOLI 9, 10 e un po’ di 11
UNA POLIMERASI CHE CONTIENE UN SIGMA SPECIFICO RICONOSCE
LA PROPRIA SERIE DI PROMOTORI
QUINDI LA Tx DI UNA SERIE DI GENI ESCLUDE/SPEGNE IL VECCHIO
PROGRAMMA E NE ACCENDE (transientemente) DI NUOVI.
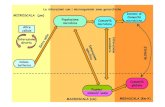
l’azione dei sigma alternativi
deve essere regolata
controllando la sua concentrazione
sequestrando il fattore sigma
sintetizzando sigma con affinità crescente
per core enzima
producendo dei pro-sigma che vengono
attivati da taglio proteolitico
cascate
l’esempio della risposta al calore
due sigma s32 e sE (s24) finemente regolati
s32 è sottoposto a controllo a feedback (heat shock proteine citosol)
in condizioni normali il livello di s32 è mantenuto basso da proteasi (che si
occupano anche della degradazione di proteine malripiegate)
quando la temperatura aumenta e provoca la denaturazione delle proteine
le proteasi vengono indirizzate alla eliminazione delle proteine mal-
ripiegate s32 viene preservato
il livello di s32 aumenta,compete con s70 che viene spiazzato comincia la
trascrizione dei geni dell’Heat shock prinicalmente chaperoni e proteasi che
ripiegano o eliminano le proteine mal-ripiegate
quando il livello delle proteine mal-ripiegate si riduce, perché diminuisce la
temperatura e per il lavoro eseguito da chaperoni e proteasi, queste ultime
sono libere di degradare s32 il cui livello torna ai valori basali
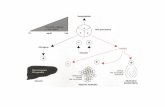
l’esempio della risposta al calore
due sigma s32 e sE (s24) finemente regolati
sE è controllato da anti-sigma factor (heat shock proteine periplasma)
in condizioni normali sE è legato (sequestrato) ad una proteina della
membrana interna RseA
l’accumulo di proteine mal-ripiegate nello spazio periplasmico provoca
l’attivazione di una proteasi (DegS) che taglia il C-terminale di RseA .
questo taglio attiva un’altra proteasi (YaeL) posta sul lato
citoplasmatico che taglia l’N-terminale di RseA liberando sE
sE può trascrivere i geni dell’Heat shock prinicalmente chaperoni e
proteasi che ripiegano o eliminano le proteine mal-ripiegate
specificamente nello spazio periplasmico
Sigma E risponde a
modificazioni più
estreme di temperatura
di Sigma32
SigmaE è stabile ma
dormiente perché
sequestrato
Nota!! Fai un parallelo
con eucarioti!…
Si pensi alla cascata di
trasduzione di TGFb o
di Notch.
Segnale Accumulo di
proteine denaturate
fuori dalla cellula
Proteina di membrana con
dominio esterno e
citoplasmatico lega il fattore
sigmaE, sequestrandolo.
In questo caso SigmaE e'
stabile MA
DORMIENTE/LATENTE
Il taglio proteolitico di Notch richiede due diverse proteasi
che lavorano in serie
L’azione delle proteasi è attivata dal cambio conformazionale
di Notch indotto dall’interazione con i ligandi di tipo Delta
L’interazione ligando-recettore coinvolge anche la cellula
sorgente, in cui l’endocitosi di Delta è parte integrante
dell’attivazione di Notch (l’endocitosi “tira” su Notch
cambiandone la conformazione)
il fago di B.subtilis (SPO1) per
realizzare la transizione tra le diverse
fasi di infezione ( precoce, intermedia
e tardiva) a cui corrispondono
l’espressione di diversi gruppi di geni
utilizza sigma alternativi
Geni precoci trascritti dalla polimerasi
dell’ospite batterico
Geni intermedi trascritti utilizzando un
sigma prodotto di un gene fagico della
fase precoce
Geni tardivi trascritti utilizzando un
sigma prodotto da due geni fagici della
fase intermedia
una cascata di fattori sigma
coordina eventi complessi:
controllo temporale
gp28
gp33
gp34
s70
la mancanza di nutrimenti
innesca la sporulazione
due diversi destini
LA SPORULAZIONE comporta l’espressione
di geni specifici
coordinamento tra eventi così diversi che
avvengono nel batterio vegetativo (che si
liserà) e nella spora.
Non ci puo' essere sfasamento temporale tra
i due eventi..!
una cascata di fattori sigma coordina
eventi complessi:
controllo comunicazione cellula/cellula
NON SERVE SAPERE A MEMORIA TUTTI I NOMI DEI
GENI e MECCANISMI DELLA SPORULAZIONE !
COCETTI IMPORTANTI:
•la sporulazione e' controllata da due cascate di vari sigma
•in ciascun compartimento (batterio vegetativo e spora) vengono attivati
IN SUCCESSIONE DIVERSI SIGMA, ognuno dirige la trascrizione di
gruppi di geni specifici
•spesso tra questi geni ci sono i sigma della fase successiva
•il "trucco" per realizzare il coordinamento è la sintesi di un PRO-SIGMA
(latente, ma "ready-to-go", attivato da taglio proteolitico)
•il taglio è controllato dalla localizzazione (in membrana del setto) del
ProSigma e dagli eventi che avvengono nell'altra cellula..!!!. Cio' realizza
la COORDINAZIONE spazio-temporale nelle e tra le due cellule con
destini così diversi ….
i batteri vivono in un mare di nutrienti diversi e per
ottimizzare il dispendio energetico hanno evoluto dei
sistemi di percezione di segnali (quale metabolita è
presente) e hanno collegato questi segnali a precisi
programmi di regolazione genica
elementi trans attivi - elementi cis attivi
un regolatore è elemento trans attivo (diffusibile): RNA pol,
fattori di trascrizione, miRNA ecc.
agisce su qualunque copia del suo bersaglio
il sito di legame (bersaglio) sul DNA/RNA è elemento cis attivo
(promotore, operatore, enhancer ecc.)
ha effetto solo sul DNA adiacente
REGOLAZIONE NEGATIVA E POSITIVA
REPRESSORI E ATTIVATORI
basso livello di tx
costitutiva (non regolata)
basale
un repressore si lega alla
regione OPERATORE,
parzialmente sovrapposta
al promotore
un attivatore, si lega ad
una sequenza vicina al
promotore e recluta la
RNA pol al promotore:
esempio di legame
cooperativo
in altri casi, non è il legame della polimerasi ad essere limitante, ma la
sua attività. Attivatori e repressori legati nelle vicinanze possono
interferire a questo livello.
l’attivatore influenza la polimerasi
causando in essa un cambiamento
conformazionale con cui si passa
al complesso aperto
complesso chiuso, tx
inefficientemente bassa
elementi trans attivi: attivatore/i
i geni sono controllati da segnali extracellulari
come fa questa informazione ad arrivare ai promotori?
soluzione: questi segnali sono comunicati, attraverso dei mediatori
molecolari (piccole molecole, metaboliti, cataboliti, altre proteine) ai
regolatori trascrizionali
In molte proteine regolatrici
si distinguono due domini:
il sito di legame al DNA ed
il sito allosterico, che
spesso funziona come
INTERRUTTORE che
influenza il legame al DNA
predisponendolo in due
possibili configurazioni:
funzionale e NON
funzionale
= ALLOSTERIA
ALLOSTERIA vedi
definizione
Allosterismo e cooperatività
È importante precisare che il termine "allosterico" è spesso usato impropriamente per descrivere la cinetica cooperativa, esibita da alcuni enzimi multimerici.Il termine allosterico, in accordo con il significato originale, dovrebbe essere riservato per quegli enzimi la cui attività è regolata da ligandi (effettori o modulatori - che a loro volta possono essere proteine o piccole molecole) che interagiscono con un sito diverso da quello attivo o catalitico.Il termine fu infatti introdotto da Monod, Jacob e Changeux per descrivere il comportamento di enzimi inibiti competitivamente da composti strutturalmente (stereos) molto diversi (allos) dal substrato. Poiché la maggior parte di questi enzimi mostra anche una cinetica sigmoide, tipica dei catalizzatori oligomerici con siti multipli interagenti, il termine allosterico è spesso usato come sinonimo di cooperatività, pur in assenza di una reale regolazione allosterica.IN BIOCHIMICA, una macromolecola esibisce LEGAME COOPERATIVO SE LA AFFINITA' PER IL SUO LIGANDO CAMBIA CON LA QUANTITA' DI LiGANDO GIA' LEGATOLa cooperatività può essere positiva o negativa (a seconda che l'effetto sia di attivazione o di inibizione)
"An allosteric effector is one that acts by binding to the enzyme at a site different from the active site. There is no necessary connection between allosteric effects and co-operative effects, though they often occur together in real systems." da Recommendations on Biochemical & Organic Nomenclature della International Union of Biochemistry (198
regolazione fine dell’espressione genica,
controllo integrato (postivo e negativo) per
l'operone lac
“adattamento” enzimatico dei batteri
curva di crescita di E. coli in terreno contenente glucosio e lattosio
preferenza per il glucosio
viene chiamata repressione da glucosio (o da cataboliti)
una strategia utilizzata dai batteri è quella di riunire
gruppi di geni funzionalmente collegati in modo che essi
possano ricevere regolazione coerente dalle stesse
sequenze regolatorie
un esempio classico: LacZ operon
3 geni in un messagero policistronico
gli elementi regolatori corrispondenti in 5' (a monte)
operoni
locus lac
lac Z = codifica b-galattosidasi
lac Y = codifica galattoside permeasi
lac A = codifica galattoside transacetilasi
lac I = codifica il repressore NON fa parte dell’operone
è un gene regolatore
operone lac
gruppo di geni che codificano gli enzimi coinvolti
nel metabolismo del lattosio
P/OCAP
permeasi
lattosio
transacetilasi
b-galattoside
b-galattosidasi
mutazioni
l'operatore lac è un palindromo, viene contattata
da DUE "TESTE" del repressore in due giri
consecutivi nel solco maggiore del DNA,
ogni testa si lega a mezzo sito
solo 26 paia di basi sono contattate "direttamente“
un piccolo numero di contatti specifici essenziali
all'interazione proteina DNA (come per RNA polimerasi)
principio universale: i fattori di trascrizione molto raramente
agiscono come singola molecola
quasi sempre agiscono in coppia, come tetramero etc.
questo si riflette nella struttura del loro consensus sul DNA.
ciascun monomero stabilisce contatti quasi identici
aumentando l'affinità di legame, in generale:
raddoppiare i contatti →2xG→costante di affinità al quadrato
Asse di simmetria
l’operone lac possiede tre sequenze operatore
la repressione si manifesta quando un TETRAMERO di
repressore si lega al DNA prendendo contatto con due siti
operatore
stabilità del legame aumentata dalle quattro interazioni
legame cooperativo
COOPERATIVITA’ NEI FATTORI DI TRASCRIZIONE
le interazioni molecolari deboli sono alla base della regolazione dei sistemi biologici;
regolazione =reversibilita’, come un semaforo; tanto piu’ fine e’ la frequenza on-off, tanto piu’ fine sara’ la
regolazione
Le molecole che lavorano assieme si contattano e si staccano continuamente.
Nelle molecole la interazione fisica (formazione complesso) e’ dettata da 1) affinita’ reciproca (valore
termodinamico); 2) dalla loro concentrazione
Tipicamente I fattori di trascrizione non agiscono da soli ma come dimero, tetramero, ottamero etc
Perche’?? ==> COOPERATIVITA’, legame cooperativo. Due ligandi si legano fra loro in modo tale che il
legame al DNA di uno di questi ligandi aiuti il legame al DNA dell’altro.
La cooperativita’ puo' anche essere percepita come aumento di affinita’ di una molecola al DNA se ce ne
un’altra gia’ legata.
C’e’ piu’ ordine=maggiore G.
Per es. Questo vale non solo nel caso del legame a sequenze palindrome di due teste del lac repressor…
ma anche per il contato di diversi operatori nel tetramero. Se il repressore di lac e’ legato al suo
operatore canonico, si potra’ legare con maggiore efficienza (cioe’ con migliore forza) ad un operatore piu’
prossimale (5’). NB la relazione tra energia di legame ed equilibrio chimico e’ di tipo esponenziale (2x
energia di legame = 10x di affinita’)
L’idea della cooperativita’ puo’ essere intuitivamente spiegata
ance come un aumento di concentrazione locale. Una molecola
trattiene quell’altra in vivinanza, aumentanto le probabilita’ di
incontrare il target.
PERCHE’ LA COOPERATIVITA’ E’ IMPORTANTE
Permette ad una proteina di legarsi meglio di quanto la sua affinita’ le permetterebbe.
Un fattore di tx, per essere funzionale, non solo deve legare il suo sito target (consensus) sul DNA
al alta affinita’ ma deve anche avere la una affinita’ piu’ bassa possibile per il resto del DNA ( un
“reagente” che e’ enormemente piu’ concentrato…) . In altre parole e’ il rapporto di affinita’
specifico/non specifico che conta!. Se si aumenta la affinita’ (rendendo la proteina piu’ grande e
sofisticata), si potrebbe aumentarla anche per I falsi bersagli==> inutile !! perche il ns fattore di Tx
rimarrebbe troppo tempo legato a siti non corretti. LA COOPERATIVITA’ RISOLVE IL PROBLEMA: e’
una strategia che si e’ evoluta per aumentare l’affinita’ senza pagarne I rischi. Legandosi a due siti
adiacenti in modo cooperativo, una proteina aumenta drasticamente la propria affinita’ senza
aumentare quella per gli altri siti aspecifici. Sono dei multimeri: e’ praticamente impossibile che due
molecole della stessa proteina si leghino a due siti sbagliati, per caso, nello stesso momento. La
cooperativita’ scatta sono nei loro siti consensus giusti.
induzione operone lac
le molecole di induttore
interagiscono con il tetramero
ne causano una modifica
conformazionale che riduce
drammaticamente l'affinità
delle teste del repressore per il
DNA.
il repressore è una
proteina allosterica
la repressione non è mai totale, trascrizione basale:
presenza di poche molecole di permeasi e di b-galattosidasi
induttore = allolattosio
prodotto da b-galattosidasi
come può entrare il lattosio e come si produce allolattosio
se l’operone è represso?
il paradosso dell’induzione
10 molecole
di repressore
tetramerico
per cellula
nella cellula batterica non c’è mai
repressore lac libero
i batteri sono aploidi (una sola copia ci ciascun gene)
Jacob e Monod hanno realizzato dei batteri parzialmente diploidi
(merodiploidi) per l’operone del lattosio (lacZ, lacY e lacA) e le sequenze
vicine (lacI) (locus lac) e osservato come cambiava il fenotipo quando i
merodiploidi contenevano una copia mutata e una wild type
LA FORZA DELLA GENETICA: gli esperimenti di Jacob e Monod
LA SCOPERTA DELL'OPERONE
mutanti di tipo diverso
Mutare il repressore o il sito operatore avrà lo stesso
effetto?
derepressione e trascrizione costitutiva dei geni lac
ma c'e' una differenza:
una mutazione nella sequenza dell'operatore non potrà
che agire in cis sullo stesso filamento di DNA
(mutazione cis-agente)
al contrario, LacI codifica una proteina, cioè un prodotto
solubile diffusibile e quindi avrà effetti anche su una
molecola di DNA separata (mutazione trans-agente)
concetto di mutazioni CIS e TRANS:
mutazioni costitutive cis agenti
mutazioni nell’operatore (Oc) causano l’espressione
costitutiva dei geni strutturali
il repressore non si può legare
agiscono in cis interferendo solo sui geni che si
trovano contigui ad esse, sullo stesso tratto di DNA
mutazioni nel promotore (che impediscono il
legame della RNA pol) operone mai inducibile
mutazioni dominanti
LA MUTAZIONE nell’operatore di lac, NON viene complementata da una
copia aggiuntiva del locus lac wild-type. L’espressione rimane costitutiva
nel cromosoma mutante.
Le mutazioni
nell'operatore sono
Cis-dominanti
preché l’operatore è
inseparabile dai
geni che controlla
mutazioni trans-agenti
mutazioni del repressore
lacI- impediscono la sintesi del repressore o
producono un repressore non funzionante
i geni strutturali sono sempre espressi
lacI-d il repressore non è in grado di legare
l’operatore
i geni strutturali sono sempre espressi
lacIs il repressore non è in grado di legare o
rispondere all’induttore
i geni strutturali sono sempre repressi
recessive
dominanti
negative
LA MUTAZIONE in lacI VIENE complementata da una copia aggiuntiva
del locus lac wild-type. Il repressore wild type diffonde e lega l’operatore
del cromosoma mutante e della copia aggiuntiva
questa mutazione trans è recessiva
Le modalità di azione di attivatori diversi o dello stesso
attivatore su promotori diversi possono essere varie
Nota come possano agire
anche a distanza