OSTEOMALACIA - win.mnlpublimed.comwin.mnlpublimed.com/public/0505A12.pdf · secondario con moderato...
Transcript of OSTEOMALACIA - win.mnlpublimed.comwin.mnlpublimed.com/public/0505A12.pdf · secondario con moderato...
-
Osteomalacia - pp. 310/318 R. Nuti et al. pag.310
INTRODUZIONE
La osteomalacia una osteopatia metabolica demineralizzantecaratterizzata dalla presenza di tessuto osteoide non calcificato inmisura superiore alla norma (1, 2). Si realizza tipicamente nel sog-getto adulto ed espressione di una alterazione dei meccanismi dimineralizzazione; quando il difetto di calcificazione insorge nelloscheletro in accrescimento si usa il termine di rachitismo. Il difet-to di mineralizzazione del rachitismo interessa, oltre che la matri-ce osteoide dellosso, anche la matrice cartilaginea delle cartilaginidi accrescimento prima che si realizzi la loro fusione .
Il meccanismo patogenetico responsabile della difettosa mineraliz-zazione della matrice organica neodeposta tipico dellosteomalacianon del tutto chiaro: la teoria chimico-fisica del ridotto prodot-to calcio-fosforo nei liquidi organici resta tuttora una ipotesisostanzialmente valida. E' noto infatti come nella matrice osseanon ancora calcificata siano presenti specifiche vescicole all'inter-no delle quali si realizza, per un fenomeno di reazione fra gli ionicalcio e fosfato, la formazione di cristalli di idrossiapatite.Condizione indispensabile perch questo processo si verifichi lapresenza dei due ioni in concentrazioni adeguate nel sangue eall'interno dell'osso: quando il prodotto della concentrazione pla-
OSTEOMALACIA
Ranuccio Nuti, Luigi Gennari, Giuseppe Martini
Dipartimento di Medicina Interna, Scienze Endocrinologiche e Biochimica dell Universit di Siena
Indirizzo per corrispondenza: Prof. Ranuccio Nuti Dipartimento di Medicina Interna, Scienze Endocrinologiche e Biochimica dell Universit di Siena Viale Bracci - 53100 Siena - tel: +39 0577 233425; fax: +39 0577 233446; e-mail: [email protected]
ABSTRACT
Osteomalacia is a metabolic bone disorder characterized by reduced mineralization and increase in osteoid thickness. This disorder tipicallyoccurs in adults due to different conditions impairing matrix mineralization. Its major symptoms are diffuse bone pain, muscle weakness andbone fractures with minimal trauma. When occurs in children, the disorder is called rickets. Many cases of osteomalacia are related to vita-min D deficiency. This condition, also named nutritional osteomalacia, can be due to either estrinsic or intrinsic vitamin D deficiency. Theformer is mainly related to low dietary intake or reduced sunligth exposure, while intrinsic vitamin D deficiency is caused by an impaired inte-stinal absorption of vitamin D. Osteomalacia may also occur due to impaired vitamin D metabolism. In rare circumstances, rickets may bedue to hereditary disorders of vitamin D metabolism (1alfa-hydroxylase deficiency, causing type I vitamin D dependent rickets) or vitamin Dresistance due to impaired vitamin D receptors (causing type II vitamin D dependent rickets). Finally, different conditions, such as phospha-te depletion, renal tubular acidosis, or treatment with fluorides and etidronate, may cause vitamin D independent syndromes leading to osteo-malacia.Key words: Osteomalacia; rickets; vitamin D; calcium; bone remodeling
RIASSUNTO
La osteomalacia una osteopatia metabolica demineralizzante caratterizzata dalla presenza di tessuto osteoide non calcificato in misura superiore alla norma.Si realizza tipicamente nel soggetto adulto ed espressione di una alterazione dei meccanismi di mineralizzazione. Quando il difetto di calcificazione insor-ge nello scheletro in accrescimento si usa il termine di rachitismo. I suoi sintomi principali sono il dolore osseo, la debolezza muscolare, e aumentata suscet-tibilit alle fratture.Questa osteopatia, che pu essere presente in varie condizioni patologiche, di solito causata da deficit di vitamina D. Tale forma, detta anche osteomala-cia nutrizionale pu essere dovuta ad un carente apporto alimentare o ad un deficit di sintesi della vitamina D spesso legato ad una ridotta esposizione allaluce solare (deficienza estrinseca) oppure da un difettoso assorbimento intestinale della vitamina D (deficienza intriseca). Vi sono poi forme legate ad alte-rato metabolismo della vitamina D e, pi raramente, cause geneticamente determinate come nel caso del rachitismo vitamina D dipendente di tipo I e ditipo II, legati rispettivamente ad alterata sintesi di (deficit di 1alfa-idrossilasi renale) o insensibilit recettoriale all'azione del metabolita attivo della vita-mina D. Esistono infine quadri di osteomalacia vitamina D indipendenti legati a cronica indisponibilit di fosfato, ad acidosi renale, e a terapia con fluo-ruri od etidronato. Parole chiave: Osteomalacia; rachitismo; vitamina D; calcio; rimodellamento osseo
-
Riv. It. Ost. Gin. - Vol. 5
smatica in mg% del calcio e del fosforo inferiore a 25 la matriceorganica non va incontro al fiosiologico processo di mineralizza-zione, da cui la formazione di tessuto osteoide.Esistono sostanzialmente tre categorie etiologiche di osteomalacia:le forme vitamina D dipendenti, quelle correlate ad alterazioni delmetabolismo del fosfato e quelle dove non sono presenti disturbidel metabolismo della vitamina D e del fosfato (2). Le forme vita-mina D-dipendenti sono legate essenzialmente a ridotta disponibi-lit o alterato metabolismo della vitamina D. La vitamina D esistein natura in due forme, l'ergocalciferolo o vitamina D2, presentein molti vegetali, ed il colecalciferolo o vitamina D3, che vienesintetizzato nella pelle per azione dei raggi solari. La sintesi cuta-nea rappresenta la pi importante fonte di vitamina D ed almenoalle nostre latitudini sufficiente a garantire il fabbisogno fisiolo-gico. La vitamina D, per essere efficace, deve sottostare a due tappemetaboliche, la prima nel fegato, dove idrossilata in posizione 25con formazione de1 25-idrossicolecalciferolo [25(OH)D3]; laseconda tappa avviene a livello renale con idrossilazione dello ste-roide in posizione l e formazione dell'1,25-diidrossicolecalciferolo[1,25(OH)2D3] che rappresenta il metabolita attivo.Losteomalacia si realizza quando i livelli di 25(OH)D3 risultanoinferiori a 5 ng/ml, condizione che viene definita come deficienzadi vitamina D. Esiste anche uno stato intermedio, fra i 5 ng/ml ei 12 ng/ml, che pu essere definito come insufficienza di vitaminaD in cui si viene a determinare una perdita ossea prevalentementecorticale, in ragione delliperparatiroidismo secondario, che puarrivare a dei veri e propri quadri di osteoporosi. Se il deficit vita-minico persiste e progredisce si arriver allimpossibilit di sintesidi 1,25(OH) 2D3 per la mancanza di un adeguato substrato equindi si realizzer il difetto di mineralizzazione della matrice tipi-co della osteomalacia (3, 4). Uno schema della classificazione deirachitismi/osteomalacie riportato nella Tabella 1.
MANIFESTAZIONI CLINICHE E DIAGNOSI DELLE OSTEOMALACIE
Le caratteristiche cliniche essenziali del rachitismo-osteomalaciasono rappresentate dal dolore osseo, dalle fratture patologiche conrelative deformit scheletriche, e dalla debolezza muscolare (2).Quando le alterazioni della mineralizzazione si realizzano nelloscheletro in accrescimento, il rachitismo si manifesta con uningrossamento delle metafisi, una esuberanza di tessuto cartilagi-neo non calcificato a livello delle articolazioni condro-costali, aformare il cosiddetto rosario rachitico, ed un rallentamento dellosviluppo scheletrico. In casi particolarmente gravi si possono veri-ficare anche crisi ipocalcemiche con tetania fino allo spasmo larin-geo e alle convulsioni. Nei lattanti e nei bambini piccoli la sinto-matologia dominata dalla irritabilit, mancanza di vitalit e spes-so marcata ipotonia. Nei bambini pi grandi la sintomatologia dominata dalle deformazioni scheletriche, in rapporto allinfluen-za del carico su ossa poco mineralizzate, e dallipotonia muscolare.Le deformazioni scheletriche possono colpire il cranio con unanormale appiattimento delle ossa parietali ed una protuberanzadellosso frontale (cranio natiforme e fronte olimpica) associati aduna perdita di consistenza della volta cranica (craniotabe) e ad unallargamento delle suture; la gabbia toracica che presenta, oltre alrosario rachitico, linfossamento delle ultime coste a livello del-linserzione del diaframma (solco di Harrison); le ossa lunghe degliarti inferiori con varismo o valgismo. Le fratture sono frequenti ela dentizione spesso ritardata con difetti nello smalto. La miopatia,tipica del rachitismo, pu interessare anche il cuore con la com-parsa di una cardiomiopatia dilatativa (5). Unaltra caratteristicadel rachitismo tipica nei paesi in via di sviluppo laumento del-lincidenza di infezioni polmonari che possono portare ad unaumento della mortalit (6). Losteomalacia che si istituisce nelle-t adulta spesso asintomatica, almeno nelle fasi iniziali, e posso-no essere necessari molti anni prima che raggiunga la espressivitclinica. In alcuni casi possono essere presenti deformit residue diun rachitismo, soprattutto nelle forme genetiche e in quelle secon-darie ad un morbo celiaco, associate ad una ridotta statura (2, 7).Esempi di alterazioni scheletriche espressione di un pregressorachitismo sono la presenza di cifosi, la coxa vara, il petto a pic-cione, la protrusio acetaboli e le deformit degli arti inferiori. Ledeformit dell'osteomalacia ad insorgenza nellet adulta sono diminore entit dato che lo scheletro, pur sottoposto a continui pro-cessi di rimodellamento, ha terminato la sua fase di accrescimento.Si possono comunque realizzare cedimenti vertebrali tali da pro-vocare una cifosi con diminuizione staturale, incurvamenti deisegmenti diafisari delle ossa degli arti inferiori e deformazionetriangolare del bacino. I dolori ossei sono solitamente diffusi epossono interessare anche gli arti inferiori. La comparsa del dolo-re presumibilmente legata a fenomeni di deformazione cui il seg-mento osseo malacico va incontro sotto la pressione del peso cor-poreo e della tensione muscolare, dato che nel periostio sono pre-senti in abbondanza terminazioni nervose sensitive. Il dolore undolore cupo, non ben localizzato ma riferito sicuramente alle ossapiuttosto che alle articolazioni; persistente, peggiora con il cari-co e la contrazione muscolare, non migliora con il riposo a letto,ma solo con ladozione di particolari posture (8, 9). La compres-sione laterale delle coste e dello sterno in grado di evocare dolo-re e rappresenta un utile indagine semeiologica. Altro aspetto cli-nico caratteristico dell'osteomalacia la miopatia prossimale. Untempo interpretata come consequenza dell'osteopatia, in realt
pag.311
Tabella I. Cause di Osteomalacia e Rachitismo
-
Osteomalacia - pp. 310/318
una vera e propria miopatia che coinvolge prevalentemente il cin-golo scapolare e pelvico ed causa, oltre che di dolori muscolari,anche di una grave incapacit funzionale: tipica a questo proposi-to l'andatura anserina e la difficolt nel passaggio dal clino all'or-tostatismo come alzarsi dalla sedia e dal letto oppure salire e scen-dere le scale senza lausilio delle braccia. La contrazione isometri-ca dei quadricipiti ridotta raggiungendo al massimo il 70% delprevisto (10), mentre latrofia muscolare inferiore a quella attesain considerazione del grado di debolezza presentato dai pazienti. Iltono muscolare ridotto, ma i riflessi osteotendinei sono presentie vivaci e le fascicolazioni assenti (2). Lesame elettromiograficomostra dei potenziali delle unit motorie ridotti in durata eampiezza e a volte polifasici sebbene la biopsia muscolare nonmetta in evidenza segni inequivocabili di una malattia muscolareprimitiva (11).Nell'approccio diagnostico all'osteomalacia un posto di primopiano deve essere attribuito alle indagini di laboratorio. Una con-dizione di ipocalcemia e ipofosforemia associata ad uno stato diiperattivita' osteoblastica, documentata da un aumento dei livellidi fosfatasemia alcalina e osteocalcina, deve far sospettare la pre-senza di una osteomalacia. Nelle forme legate a deficit di vitaminaD sono generalmente presenti ipocalcemia ed iperparatiroidismosecondario con moderato ipofosforemia mentre nelle forme fosfa-to-dipendenti la normocalcemia la regola, l'iperparatiroidismosecondario lieve o assente, ma l'ipofosforemia pi severa.Anche dal dosaggio dei metaboliti della vitamina D possono esse-re tratte utili indicazioni diagnostiche. Nelle osteomalacie nutri-zionali i livelli del 25(OH)D3, che esprime lo stato vitaminico Ddell'organismo, sono solitamente molto bassi. Per altro anche nel-l'osteomalacie da indisponibilita' di 25(OH)D3 sono presentiridotti livelli di 25(OH)D3, cosi' come in quelle da indisponibili-ta' di 1,25(OH)2D3, i livelli di questo metabolita risultano dimi-nuiti. Per quanto riguarda il dosaggio dell'ormone paratiroideo, ilsuo dosaggio puo' risultare utile solo nel sospetto di un iperpara-tiroidismo secondario. Le alterazioni radiologiche presenti nell'o-steomalacia possono derivare sia dalla difettosa mineralizzazionesia dall'iperparatiroidismo secondario. Sono tipiche del quadroradiologico una riduzione del tono calcico con radiotrasparenzadiffusa dello scheletro ed un disegno sfumato delle trabecole per lascarsa calcificazione che la presenza di fratture patologiche e dipseudofratture di Looser-Milkman (8, 9). Queste ultime si presen-tano come linee di frattura parziale o completa senza spostamentodei margini, simmetriche e perpendicolari all'asse maggiore delsegmento osseo. Le pseudofratture di Looser-Milkman sono pato-gnomoniche dell'osteomalacia: sono fratture da durata ad anda-mento cronico, non eccessivamente dolenti. Spesso sono bilateralie simmetriche e si localizzano preferibilmente nel terzo prossima-le dei femori, nei bordi laterali delle scapole, alle coste, alle clavi-cole, alle branche ischio e iliopubiche (Figura 1). Non infre-quente anche il rilievo radiologico di aree di sclerosi ossea osserva-bili soprattutto a carico delle mani. Le fratture patologiche, speciequelle costali e quelle delle ossa appendicolari, si possono avere pertraumi minimi. A livello delle vertebre si possono realizzare delledeformazioni a lente biconcava con la concavit simmetrica allas-se orizzontale di ciascuna vertebra e di grado simile alla vertebraadiacente (12). Questo aspetto contrasta con la distribuzione irre-golare delle deformit vertebrali che si riscontra nella osteoporosi.Da segnalare come la frattura dello sterno sia una caratteristica chelosteomalacia divide solamente con il mieloma multiplo. Le areeosteomalaciche delle pseudofratture captano avidamente i trac-
cianti ossei, per cui la scintigrafia ossea pu risultare utile per evi-denziare tali lesioni in sedi pi difficilmente esplorabili radiologi-camente come le arcate costali. Il ridotto contenuto minerale delloscheletro potr essere quantizzato per mezzo della densitometriaossea computerizzata a raggi X. Cosi come nell'osteoporosi, anchenell'osteomalacia i valori di densit ossea sono compromessi: lariduzione del contenuto minerale risulter proporzionale alla gra-vit della malattia. L'aspetto istopatologico caratteristico dell'o-steomalacia e' rappresentato dalla presenza di tessuto osteoide noncalcificato (1, 2). Nei preparati istologici non decalcificati colora-ti con le tecniche di Goldner e von Kossa il tessuto osteoide si pre-senta di color rosso, ben distinto dal rimanente tessuto osseo nor-malmente mineralizzato che appare rispettivamente verde oppurenero (Figura 2). Il tessuto osteoide si accumula per un difetto nelprocesso di mineralizzazione della matrice organica neodeposta.
Mentre in condizioni di normalita' l'osteoide e' presente in unapercentuale di circa 0-4%, ed in forme modeste di osteomalaciapuo' limitarsi a tappezzare per lunghi tratti le superfici trabecolarie haversiane, in varieta' della malattia particolarmente severe puo'addirittura interessare anche il 70% di tutto l'apparato scheletrico.La diagnosi istologica di osteomalacia si fonda, oltre che sulriscontro di un aumento di spessore dei bordi osteoidi, sulla valu-tazione dei dati istomorfometrici ottenuti con la doppia mercatu-ra con tetracicline. Un ruolo chiave nella comprensione dei mec-
R. Nuti et al. pag.312
Figura 1. Fratture di Looser-Milkman delle scapole
Figura 2. Agobiopsia ossea con prelievo dalla cresta iliaca. La colorazione di Goldner mostra la presenza di ampi bordi osteoidi colorati in rosso, mentre losso normalmente calcificatoappare di colore verde
-
Riv. It. Ost. Gin. - Vol. 5
canismi patogenetici alla base della osteomalacia quello svoltodal ritardo del tempo di mineralizzazione, cio del tempo necessa-rio perch la matrice neodeposta si mineralizzi (13): dai 10-15giorni che occorrono normalmente, questo intervallo pu oltre-passare anche i 100 giorni. Altro dato caratteristico della osteoma-lacia laumento dello spessore dellosteoide che supera i 12.2 _m(14). Partendo da questi due parametri istomorfometrici, la osteo-malacia pu essere divisa in tre forme (2): una lieve dominata dal-l'iperparatiroidismo secondario e caratterizzata da un accumulo diosteoide di normale spessore ed aumento del turnover osseo conelevata attivit osteoclastica; una intermedia in cui sono presentiaree con bordi osteoidi aumentati di spessore frammiste ad areecon numerose lacune di riassorbimento, osteoblasti ed osteoclastiin numero elevato, osso a fibre intrecciate e fibrosi midollare; infi-ne la forma avanzata di osteomalacia ("end stage osteomalcia")caratterizzata da una riduzione del turnover osseo con osteoblastiappiattiti che tappezzano i grossi bordi osteoidi. La differenza fon-damentale fra le ultime due forme che nella seconda solamentela matrice deposta in una fase tardiva non viene mineralizzatamentre nella forma avanzata la matrice osteoide non subisce alcunprocesso di mineralizzazione.
OSTEOMALACIA DA DEFICIT DI VITAMINA D
Queste osteomalacie, dette anche nutrizionali, sono dovute ad uncarente apporto o ad un deficit di sintesi della vitamina D soste-nuto o da una ridotta esposizione alla luce solare e/o da un defici-tario apporto alimentare (deficienza estrinseca) oppure da undifettoso assorbimento intestinale della vitamina D (deficienzaintrinseca).La ridotta esposizione alla luce solare pu essere dovuta ad abbi-gliamento inidoneo legato a motivi razziali, religiosi o personali(ad es. monache di clausura, immigrati indiani, pakistani o nord-africani emigrati a latitudini pi elevate) oppure all'abitudine dellepersone anziane di trascorrere gran parte del tempo in ambientiscarsamente soleggiati (15, 16). Inoltre gli anziani sono soggetti adun declino et-correlato dell'efficienza dell'assorbimento digestivodella vitamina D e dell'abilit del rene di produrre 1,25-(OH)2D3(17). Un apporto di vitamina D inferiore alle aumentate necessitsi pu inoltre verificare nella gravidanza e nell'allattamento.L'assorbimento intestinale della vitamina D e del calcio pu esse-re ostacolato dall'elevato contenuto di fitati e fibre nella dieta tipi-co dei soggetti che usano cereali e pane integrale come fonte calo-rica principale. A questo riguardo una interessante ipotesi sullagenesi dellosteomalacia stata formulata osservando le popolazio-ni di Indiani trasferitisi in Scozia: la prevalenza e la severit delrachitismo e dellosteomalacia sono correlati alla dieta vegetarianamentre una dieta onnivora esercita un effetto protettivo che nonpu essere dovuto allaumentato apporto di vitamina D vista lascarsa quantit presente nella carne (18). Quindi si pu supporreche a parit di esposizione solare la dieta vegetariana presenti unfattore di rischio per lo sviluppo di una osteomalacia. Alterazioni del metabolismo del calcio e della vitamina D che pos-sono portare ad una deficienza o insufficienza con iperparatiroidi-smo secondario, si possono realizzare nelle malattie croniche del-lapparato digerente, del fegato e del pancreas (19). In queste con-dizioni difficile riscontrare il quadro classico della osteomalaciaperch spesso la sintomatologia complicata dagli effetti delladeficienza di altre vitamine e micronutrienti, dalla malnutrizioneproteica e calorica cos come dagli effetti dei farmaci usati per trat-
tare le patologie di base, come i glucocorticoidi e/o gli immuno-soppressori. Losteomalacia comunque sempre dovuta al deficitdi vitamina D, mentre losteopenia e losteoporosi, che risultanoaddirittura pi frequenti, sono solo parzialmente spiegate dalli-perparatiroidismo secondario. La gastrectomia da lungo tempoassociata a malattie osteometaboliche come losteoporosi o losteo-malacia. Il malassorbimento pu essere alla base della osteomala-cia, ma non sempre presente steatorrea e, quando stato studia-to, lassorbimento della vitamina D risultato normale (20).Daltra parte frequente un malassorbimento calcico ed unaosteopenia con ridotti livelli di 25(OH)D3 e alti di 1,25(OH)2D3nellambito di un iperparatiroidismo secondario che potrebbe esse-re quindi responsabile dellaumentato catabolismo del calcifediolo(21). La malattia celiaca una causa comune di malassorbimentointestinale e, poich interessa le prime porzioni del piccolo inte-stino, frequentemente si accompagna a malassorbimento calcico.La osteomalacia stata considerata a lungo la malattia ossea prin-cipale associata alla celiachia, ma ormai accertato come sia moltopi frequente la osteoporosi che pu essere presente anche nelleforme asintomatiche o paucisintomatiche della malattia (22, 23).Ridotti livelli di 25(OH)D3 con valori di massa ossea compatibilisia con osteoporosi che con osteomalacia sono relativamente fre-quenti nelle malattie infiammatorie intestinali, soprattutto nelmorbo di Chron, e nei by-pass intestinali eseguiti per la cura del-lobesit, mentre linsufficienza pancreatica raramente responsa-bile di osteopatie a meno che non sia secondaria ad una fibrosicistica o rappresenti un epifenomeno dellalcolismo.La prevenzione delle osteomalcie nutrizionali si basa sulla rimo-zione delle cause etiologiche di malattia e sulla fortificazione delcibo (latte e derivati). Se la dieta non contiene supplementi di vita-mina D pu essere utile la somministrazione di ergocalciferolo ocolecalciferolo alla dose di 400 U.I. die anche ai prematuri ed aineonati allattati al seno nonch ai pazienti sottoposti a nutrizioneparenterale totale. Negli adulti la dose per la prevenzione di 100U.I. al di. E' necessario inoltre che la dieta contenga adeguatequantit di calcio e fosforo. Quando la malattia conclamata sononecessarie dosi molto elevate: 1.500-5000 U.I./die di ergocalcife-rolo o colecalciferolo per os oppure, soprattutto nelle forme secon-darie a malassorbimento intestinale, 10.000-50.000 U.I. al meseper via im. I primi effetti della terapia si hanno dopo pochi giornidall'inizio del trattamento: dopo 10 giorni si normalizzano i livel-li di calcemia e fosforemia ed entro 3 settimane si evidenziano iprimi segni radiologici di guarigione delle lesioni. Nelle fasi pre-coci del trattamento, poich la mineralizzazione scheletrica puessere molto rapida, si pu osservare una ulteriore riduzione dellacalcemia e della calciuria: quindi utile associare calcio per os alladose di 1-3 g di calcio elemento in dosi refratte. Anche la fosfata-si alcalina pu inizialmente aumentare, per poi normalizzarsi nelcorso dei mesi. Ottenuta la guarigione, di solito entro 6 mesi, sufficiente instaurare una dieta con normale contenuto di vitami-na D (100-400 U.I./die) e di calcio (800-1000 mg/die).
OSTEOMALACIA DA INDISPONIBILIT DI 25(OH)D3
La forma tipica di osteomalacia da indisponibilt di 25(OH)D3 rappresentata da quella secondaria a trattamenti cronici con far-maci anticonvulsivanti: fenobarbitale, idantoina e carbamezapina.Queste sostanze diminuiscono gli effetti della vitamina D sull'as-sorbimento intestinale del calcio e sul rimodellamento osseo.
pag.313
-
Osteomalacia - pp. 310/318
Spesso le terapie prolungate si accompagnano a ridotti valori di25(OH)D3 ed stato quindi ipotizzato che questi farmaci accelle-rino il catabolismo della vitamina D per induzione del citocromoP450 epatico e conseguente formazione di prodotti inattivi (24).Daltra parte la idantoina sembra agire direttamente anche sullas-sorbimento intestinale del calcio producendo quindi ipocalcemia econseguente iperparatiroidismo secondario (25). Un tempo si rite-neva che anche le epatopatie croniche, come la cirrosi epatica o l'e-patite cronica, potessero causare un' osteomalacia per una presuntaimpossibilit da parte del fegato di convertire la vitamina D in 25-(OH)D: in realt numerosi studi hanno dimostrato che anche nelcorso di gravi malattie del fegato la vitamina D viene comunqueidrossilata in posizione 25 e che quando una osteopatia si realizza,essa ha i caratteri dell'osteoporosi (26). L'eccezione rappresentatadalla cirrosi biliare e dall'atresia delle vie biliari nei bambini: l'o-steomalacia si sviluppa, oltre che per il difetto di idrossilazionedella vitamina D, per il ridotto apporto alimentare della vitaminasecondario all'anoressia e per il ridotto assorbimento.La terapia di queste forme di osteomalacia si basa sulla sommini-strazione del metabolita 25-idrossilato della vitamina D, il calcife-diolo alla dose di 20-50 mcg al di per os aggiustando le dosi inmodo da mantenere dei valori di 25(OH)D3 circolanti fra 30 e 50ng/ml. La terapia va proseguita indefinitivamente, se non possi-bile la rimozione della causa responsabile della osteopatia, e quin-di sar opportuno un periodico monitoraggio anche della calcemiae della funzionalit renale per il rilievo di eventuali condizioniipercalcemiche che andranno adeguatamente trattate.
OSTEOMALACIA DA INDISPONIBILIT DI 1,25-(OH)2D3
Si realizza nel corso della insufficienza renale cronica quando lamassa renale si riduce a meno del 20%: il 25(OH)D3 non vienepi convertito in 1,25(OH)2D3 da cui il difetto nell'assorbimen-to intestinale del calcio con ipocalcemia che, associata all'iperfo-sforemia secondaria alla ridotta escrezione, condiziona l'instaurar-si di un iperparatiroidismo secondario. Le manifestazioni schele-triche nella insufficienza renale cronica si possono dividere in unaforma di osteopatia ad alto turnover (legata all'iperparatiroidismosecondario) ed in una a basso turnover. Quest'ultima pu decorre-re come una osteomalacia, legata ad un effetto inibitorio direttosulla mineralizzazione operato dall'alluminio (somministrato peros per ridurre l'assorbimento intestinale dei fosfati o presente nelliquido di dialisi), o come una osteopenia cosiddetta adinamica incui non presente una responsabilit dell'alluminio, ma proba-bilmente legata alla soppressione dell'attivit paratiroidea ottenu-ta con la somministrazione di calcio carbonato, calcitriolo o alfa-calcidolo (27). In questo gruppo di osteomalacie rientra anche ilrachitismo vitamina D-dipendente di tipo I, detto anche pseudo-deficienza di vitamina D o rachitismo tipo Prader. Questa malat-tia legata ad un difetto genetico autosomico recessivo del genedell1a-idrossilasi localizzato nel cromosoma 12q13-q14, chedetermina una riduzione nell'attivit enzimatica renale (28-29).Conseguente a tale deficit il riscontro di elevati livelli circolantidi 25(OH)D3, mentre le concentrazioni di 1,25(OH)2D3 saran-no particolarmente ridotte. La malattia si manifesta entro i primidue anni di et, spesso nei primi 6 mesi di vita, con debolezzamuscolare e rachitismo (28). La terapia si basa sulla somministra-zione di calcitriolo in dosi fisiologiche: 0.25-1 mcg per os per tuttala vita. Il rachitismo vitamina D-dipendente di tipo II, detto
anche resistenza ereditaria alla 1,25(OH)2D3, invece una condi-zione autosomica recessiva caratterizzata dall'insensibilit deirecettori cellulari all'azione del metabolita attivo della vitamina D(28, 30). Il rachitismo insorge di solito entro i primi due anni divita, ma sono stati descritti anche casi ad esordio pi tardivo. Allealterazioni ossee si possono associare alopecia, cisti epidermiche eoligodonzia. I pazienti con la malattia presentano dei livelli altis-simi di 1,25(OH)2D3 con ipocalcemia, ipofosforemia ed iper-paratiroidismo secondario. La terapia prevede la somministrazionedi dosi elevate di calcitriolo o di alfacalcidolo (6 mcg/Kg/die peros per un totale di 30-60 mcg) associata a supplementazione calci-ca fino a 3g di calcio elemento al di. La terapia va proseguita per3-6 mesi onde permettere la mineralizzazione dell'osteoide e ilsuperamento della ipocalcemia secondaria alla sindrome dell'"hungry bone".
OSTEOMALACIE DA INDISPONIBILIT DI FOSFATO
Il fosfato, componente essenziale dell'organismo umano, moltodiffuso in natura ed abbondantemente presente negli alimenti sia diorigine vegetale che animale. L'assorbimento intestinale del fosfato un processo attivo, condizionato dalla vitamina D, che si verificaa livello del tenue mesenteriale. In condizioni normali l'assorbimen-to del fosfato altissimo: solo quote modeste sono eliminate con lefeci. Con le urine vengono escreti 400-800 mg/24 ore di fosfato chesubisce anche un processo di riassorbimento tubulare. Il deficit dietetico di fosfato molto raro, ma una osteomalacia stata osservata in soggetti che assumevano farmaci antiacidi (idros-sido di alluminio e/o idrossido di magnesio) in grandi quantit eper periodi di tempo superiori ai due anni. Il fosfato, chelato dagliantiacidi, non era pi disponibile per l'assorbimento da cui la ipo-fosforemia e la ipofosfaturia con ipercalciuria e nefrolitiasi. Tuttele manifestazioni, sia biochimiche che scheletriche, sono rapida-mente reversibili con la sospensione della assunzione degli antiaci-di ed, eventualmente, con la somministrazione di fosfato per os(31, 32). Le malattie del metabolismo del fosfato possono quindi esserericondotte alle seguenti condizioni: ipofosfatemia correlata a difet-to di assorbimento intestinale del fosfato ed ipofosfatemia secon-daria a difettoso riassorbimento tubulo-renale del fosfato (2). Lacompromissione dei recettori intestinali per la vitamina D, da cuiil malassorbimento di fosfato, si realizza nei by-pass digiuno-ilealirealizzati per la cura dell'obesit oppure nell'enteropatia da gluti-ne dove al difetto nutrizionale (deficienza intrinseca di vitaminaD) si associa, per l'appiattimento dei villi e l'interessamentoinfiammatorio della mucosa e della sottomucosa, una distruzionepi o meno estesa dei recettori per la 1,25(OH)2D3. La sommini-strazione di vitamina D o dei suoi metaboliti, sia per via orale cheparenterale, ha scarso effetto sino a quando il glutine non vienecompletamente escluso dalla dieta. Altre cause che possono porta-re ad una alterazone dei recettori intestinali per la 1,25(OH)2D3sono la sindrome dell'ansa cieca oppure l'abuso di lassativi. La ipo-fosforemia pu essere secondaria ad un difetto nel riassorbimentotubulo-renale del fosfato: il caso del rachitismo ipofosfatemicovitamino D resistente (XLH: X-Linked Hypophosphatemia). E' unamalattia ereditaria X-legata con una prevalenza di 1:20.000 indivi-dui, in cui la calcemia tende ad essere normale mentre la fosfore-mia particolarmente ridotta (0.9-1.5 mg%) (33). Alcuni sogget-ti con la malattia presentano solamente una ipofosforemia senza
R. Nuti et al. pag.314
-
Riv. It. Ost. Gin. - Vol. 5
interessamento osseo che quando evidente clinicamente si mani-festa con difetto staturale, rachitismo con deformit delle ossa lun-ghe delle gambe, dolore osseo, entesopatie (calcificazioni di tendi-ni, legamenti e capsule articolari), e ascessi dentari (34). Nei casipi gravi sono presenti anche deformit craniche e stenosi midol-lare (35). Il gene responsabile stato denominato PHEX (pho-sphate regulating gene with omologies to endopeptidase on the X chro-mosome) e codifica per una proteina che fa parte delle metallopro-teasi di membrana (36, 37). Unaltra forma di rachitismo ipofo-sfatemica, pi raro del precedente, viene ereditato come carattereautosomico dominante (ADHR: Autosomic DominantHypophosphatemic Rickets). Le caratteristiche cliniche e di labora-torio sono simili al precedente ed il gene interessato localizzato alivello del cromosoma 12p13 che codifica per il fibroblast growthfactor (FGF)-23 (38). Nel 1986 stato descrittauna forma di rachitismo ipofosfatemico associatoad ipercalciuria (HHRH: HereditaryHypophosphatemic Rickets with Hypercalciuria)caratterizzato da perdita renale di fosfato, iper-calciuria con normocalcemia, livelli elevati dicalcitriolo e soppressione della secrezione diparatormone (39). Il gene responsabile non stato ancora identificato e la trasmissione puessere sia dominante che recessiva. I sintomi ini-ziano generalmente da 6 mesi a 7 anni e sonorappresentati da debolezza muscolare, doloriossei e deformit scheletriche con bassa statura.La terapia di queste forma di rachitismo/osteo-malacia si basa essenzialmente sulla somministra-zione di fosfato inorganico per os ad alte dosi: ilfosfato pu essere somministrato sia come salesodico o, preferibilmente, come sale di potassioperch l'espansione del volume extracellularelegata al sodio pu deprimere il riassorbimentotubulare del fosfato e quindi ostacolarne l'au-mento nel plasma. Il dosaggio del supplementova progressivamente aumentato da 1 a 3 g. finoalla comparsa di diarrea che l'effetto collaterale pi fastidioso.Ad eccezione che nel HHRH, utile l'aggiunta di calcitriolo (1-3mcg/die) per evitare l'insogenza di iperparatiroidismo secondariodovuto all'ipocalcemia fosfato-indotta. Sono opportuni periodicicontrolli della calciuria onde evitare l'ipercalciuria farmaco-indot-ta. Una variante acquisita di osteomalacia vitamina D resistente l'o-steomalacia oncogenica (OHO: Oncogenic HypophosphatemicOsteomalacia): anche in questo caso la ipofosforemia viene gene-ralmente attribuita ad una diminuizione del riassorbimento tubu-lo-renale del fosfato secondaria all'immissione in circolo da partedel tumore di sostanze ad azione fosfaturica. Le neoplasie pi fre-quenti sono di origine mesenchimale con sede variabile nei tessutimolli o nel tessuto osseo. Variabili sono anche le caratteristicheistologiche che spesso comunque corrispondono agli emangioperi-citomi. Sono state descritte forme secondarie a carcinomi, neuro-fibomatosi e displasia fibrosa dello scheletro (40). La terapia confosfati e calcitriolo solo parzialmente efficace mentre l'asporta-zione del tumore risolutiva. Recentemente stato rilevato come colture di cellule ottenute datumori mesenchimali responsabili della osteomalacia oncogenicapresentano una sovraespressione di FGF-23, lo stesso fattore dicrescita il cui gene alterato nellAHDR. Inoltre i livelli plasmati-
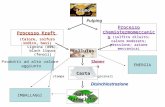
ci di FGF-23 sono risultati elevati sia nei pazienti con osteomala-cie oncogeniche che in molti con XLH. Questi dati hanno fattoformulare una ipotesi unificante per spiegare la eziologia della ipo-fosforemia nel XLH, ADHR e OHO (41, 42). Nel XLH La muta-zione inattivante il PHEX determina una incapacit a degradare ilFGF-23, mentre nel ADHR la proteina mutata FGF-23 non sub-isce la clearance da parte del PHEX perch la mutazione ha aboli-to il sito di clivaggio: il risultato sar un aumento dei livelli circo-lanti di FGF-23. Al contratio, nella OHO leccessiva produzionedi FGF-23 eccede la capacit disattivante del PHEX. In conclusio-ne nelle tre sindromi meccanismi differenti portano ad un aumen-to delle concentrazioni del FGF-23 a supporto che questo fattore il substrato per lattivit del PHEX ed il pi importante fatto-re fosfaturico (Figura 3).
Quando l'alterazione tubulare renale riguarda, oltre che al fosfato,altre sostanze come il glucosio, gli aminoacidi, l'acido urico e icitrati, si rientra nel quadro della sindrome di Fanconi (43, 44). Idifetti tubulari possono essere sia congeniti che acquisiti come lemalattie da deposito lisosomiale e la cistinosi nei bambini, e ilmieloma multiplo negli adulti. La diagnosi si basa oltre al riscon-tro della anomalie biochimiche tipiche, sulla normalit della cal-cemia, del paratormone, del 25(OH)D3 e della 1,25(OH)2D3. Lapresenza di bicarbonaturia con acidosi metabolica pu esseredovuta allassociazione con una acidosi renale tubulare di tipo II.Daltra parte la presenza di una acidosi metabolica cronica puessere sufficiente, da sola, a condizionare la insorgenza di unaosteomalacia per una compromissione dei processi di mineralizza-zione (45, 46). La terapia basata sulla correzione dell'acidosimediante somministrazione di bicarbonato di sodio per os a dosivariabili da 1-2 mg/Kg/die. Nei bambini le dosi devono esseremaggiori mentre vanno ridotte in caso di simultanea assunzione didiuretici tiazidici (ad es. idroclorotiazide) che determinano unariduzione del volume plasmatico e quindi un aumento del riassor-bimento tubulare del bicarbonato. La correzione dell'acidosi siste-mica porter alla regressione della ipercalciuria e del riassorbimen-to osseo.
pag.315
Figura 3. Sistema del FGF23 ed eziopatogenesi dellosteomalacia oncogenica (OHO),rachitismo ipofosfatemico autosomico dominante (ADHR) e rachitismo ipofosfatemicovitamina D resistente legato al cromosoma X (XLH).
-
Osteomalacia - pp. 310/318
OSTEOMALACIA CON METABOLISMO DELLAVITAMINA D E DEL FOSFATO NELLA NORMA
I processi di mineralizzazione possono essere inibiti direttamenteanche da alcuni farmaci quali l'etidronato sodico, i fluoruri e l'al-luminio (2). L'etidronato, un bisfosfonato utilizzato nella terapiadel morbo di Paget e dell'osteoporosi postmenopausale, si lega allasuperficie dei cristalli di idrossiapatite deprimendo l'attivit dirimodellamento osseo in maniera dose-dipendente (47). Un altrofarmaco impiegato nella terapia dell'osteoporosi, il fluoruro disodio, se impiegato a dosi elevate (>75 mg/die) determina in alcu-ni pazienti una inibizione della mineralizzazione: il difetto non prevenuto dalla presenza di fisiologici livelli di vitamina D, non correlato ad un alterato metabolismo della vitamina D stessa, non causato dalla mancanza di substrati per la mineralizzazione e non associato ad un iperparatiroidismo primitivo. Probabilmente rap-presenta un effetto tossico diretto del farmaco sugli osteoblasti(48). Dei sali di alluminio abbiamo gi accennato trattando dellaosteopatia dell'insufficienza renale cronica.Un quadro di osteomalacia per incapacit di mineralizzzaione dellamatrice in assenza di alterazioni della vitamina D si riscontra nellafibrogenesis imperfecta ossium (49), malattia rara in cui presen-te un ridotto contenuto proteico della matrice. Si presenta nellaquinta o sesta decade di vita con fratture multiple e dolore intrat-tabile e il dato radiologico pu essere confuso con quello delmorbo di Paget. Il ruolo della fosfatasi alcalina nei processi di mineralizzazione non stato ancora completamente chiarito, ma il deficit ereditariodella sintesi di questo enzima responsabile di una malattia defi-nita ipofosfatasia caratterizzata dalla presenza di unrachitismo/osteomalacia (50). La malattia ha una trasmissione ditipo autosomico recessivo ed caratterizzata da una deficienzavariabile, dal 10% al 30%, degli isoenzimi osseo, epatico e renaledella fosfatasi alcalina, mentre risultano nella norma gli isoenzimidi provenienza intestinale e placentare (105-106). Sono statedescritte quattro forme di ipofosfatasia in funzione dellet di pre-sentazione delle alterazioni scheletriche. Nella forma perinatale lasopravvivenza rara e, durante la gravidanza, la gestante pu svi-luppare un polidramnios. Nella forma infantile lipofosfatasia simanifesta nei primi sei mesi di vita con rachitismo, ipertensioneendocranica e ipercalcemia. Nei mesi successivi alla diagnosi pos-siamo assistere ad un miglioramento spontaneo o ad un progressi-vo deterioramento scheletrico. Circa il 50% dei pazienti muoionoentro un anno dalla diagnosi, ma la prognosi migliora con il pas-sare del tempo (50). Se lipofosfatsia si manifesta nei bambini, lagravit della malattia pu essere variabile. Quasi sempre presen-te la perdita precoce dei denti decidui con ipo-aplasia del cemen-to dentale: le alterazioni dentarie possono far porre la diagnosi diodontoipofosfatasia in assenza di interessamento scheletrico.Quando presente il rachitismo saranno evidenti ritardo nelladeambulazione con andatura anserina, bassa statura e deformitcraniche. La malattia pu migliorare spontaneamente durante lapubert, ma i sintomi si possono ripresentare nellet adulta.Lipofosfatasia del soggetto adulto molto pi comune di quellocomunemente ritenuto fino a poco tempo fa. Lesordio di solitosui 30-40 anni e il primo sintomo spesso rappresentato da frat-ture metatarsali da stress, particolarmente dolorose e con scarsatendenza alla guarigione, mentre la comparsa di coxalgia pu esse-re espressione di pseudofratture femorali. Nel 50% circa deipazienti sono presenti le manifestazioni scheletriche di un pregres-
so rachitismo (51). Frequente anche la precoce caduta dei dentipermanenti e la condrocalcinosi con periartriti calcifiche. La dia-gnosi di ipofosfatasia si basa sui rilievi anamnestici, clinici, radio-grafici e istologici di un rachitismo o osteomalacia a cui si associa-no dei bassi livelli di fosfatasi alcalina. I livelli di fosforo sono nor-mali e pu essere presente ipercalcemia e ipercalciuria soprattuttonelle forme perinatali e infantili perch lassorbimento intestinaledello ione normale, ma non viene depositato nello scheletro.Nelladulto addirittura frequente il riscontro di una iperfosfore-mia legata allaumentato riassorbimento tubulare dello ione; lastato vitaminico D normale e lattivit paratiroidea pu esseresoppressa. Tipico, sebbene non specifico, laumento plasmatico eurinario della fosforiletanolamina, che pu comunque esseresecondario ad un sofferenza epatica (50), e lincremento dei livellidi pirofosfato inorganico. Comunque, in assenza di supplementa-zione con vitamina B6, il test pi sensibile per la diagnosi di ipo-fosfatasia il dosaggio del piridossal 5-fosfato (50). Ad oggi non stata stabilita una terapia per lipofosfatasia. Potrebbe essere utileuna restrizione dei fosfati nella dieta per correggere liperfosfore-mia e quindi ridurre linibizione esercitata dal fosfato stesso sul-lattivit della TNSALP (52), mentre non trovano indicazione gliususali trattamenti del rachitismo/osteomalacia (vitamina D o suoimetaboliti, supplementazione calcica) che possono peggiorare laipercalcemia e la ipercalciuria.
R. Nuti et al. pag.316
-
Riv. It. Ost. Gin. - Vol. 5
BIBLIOGRAFIA
1. Stanbury SW, Mawer EB: Metabolic Disturbances in Acquired Osteomalacia. In: Cohen RD, Lewis B, Alberti KGMM, Denman AM (eds): The Metabolic and Molecular Basis of Acquired Disease. Bailliere Tindall, London, 1990; pp 1717-1782
2. Parfitt AM: Osteomalacia and related disorders. In Avioli LV, Krane SM (eds): Metabolic Bone Disease and Clinically RelatedDisorders. Academic Press, London, 1998; pp 327-386
3. Malabanan A, Veronikis IE, Holick MR. Redefining vitamin D insufficiency. Lancet 1998; 351:805-64. Sahota O, Masud T, San P, et al. Vitamin D insufficiency increases bone turnover markers and enhances bone loss at the hip in
patients with established vertebral osteoporosis. Clin Endocrinol 1999; 51:217-215. Mustafa A, Bigras JL, McCrindle BW. Dilated cardiomyopathy as a first sign of nutritional vitamin D deficiency rickets in
infancy. Can J Cardiol 1999; 16:699-7016. Banajeh SM, al-Sunbali NN, al-Sanahani SH. Clinical characteristics and outcome of children aged under 5 years hospitalized
with severe pneumonia in Yemen. Ann Trop Paediatr 1997; 17:321-67. Aaron J: Histological aspects of the relationship between vitamin D and bone. In Lawson DEM (ed): Vitamin D. Academic Press,
London, 19788. Stamp TCB, Walker PP, Peiry W, et al. Nutritional osteomalacia and late rickets in greater London 1974-1979: Clinical and
metabolic studies in 45 patients. J Clin Endocrinol Metab 1980; 9:81-1059. Parftt AM, Duncan H. Metabolic bone disease affecting the spine. In Rothman R, Simeone F (eds): The Spine. WB Saunders
Co, Philadelphia, 1982; pp 775-90510. Young A, Edwards RHT, Jones DA, Brenton DP. Quadriceps, muscle strength and fibre size during the treatment of
osteomalacia. In: Stokes IAF (ed): Mechanical Factors and Skeleton. John Libbey, London, 1981; pp 137-4511. Skaria J, Katiyar BC, Srivastava TP, et al. Myopathy and neuropathy associated with osteomalacia. Acta Neurol Scand 1975;
51:37-5812. Parfitt AM: Hypophosphatemic vitamin D refractory rickets and osteomalacia. Orthop Clin North Am 1972; 3:653-8013. Baylink D, Stauffer M, Wergedal J, et al. Formation, mineralization and resorption of bone in vitamin D-deflcient rats. J Clin
Invest 1970; 49:1122-3414. Eriksen EF, Steiniche T, Mosekilde Le, et al. Histomorphometric analysis of bone in metabolic bone disease. Endocrinol Metab
Clin North Am 1989; 18:919-5415. Need AG, Morris HA. Horowitz M. et al. Effects of skin thickness, age, body fat and sunlight on serum 25-hydroxyvitamin
D. Am J Clin Nutr 1993: 58:882-516. Holick MF, Matsuoka LY, Wortsman J. Age, vitamin D and solar irradiation. Lancet 1989; ii: 1104-517. Heaney RP, Recker RR, Stegman MR, et al. Calcium absorption in women. Relationships to calcium intake, estrogen status and
age. J Bone Miner Res 1989: 4:460-7518. Dunnigan MG, Henderson JB. An epidemiological model of privational rickets and osteomalacia. Proc Nutr Soc
1997: 56:939-5619. Mawer EB, Davies M. Bone Disorders Associated with Gastrointestinal and Hepatobiliar Disease. Vitamin D. Academic Press,
San Diego, 1997, pp. 831-4720. Davies M, Mawer EB, Krawitt EL. Comparative absorption of vitamin D3 and 25- hydroxyvitamin D3 in intestinal disease.
Gut 1980: 21:287-9221. Davies M, Heys SE, Selby PS, et al. Increased catabolism of 25-hydroxyvitamin D in patients with partial gastrectomy and
elevated 1,25-dihydroxyvitamin D levels. Implications for metabolic bone disease. J Clin Endocrinol Metab 1997: 82:209-1222. Corazza GR, Di Sario A, Cecchetti L, et al. Bone mass and metabolism in patients with celiac disease. Gastroenterology
1995: 109:122-823. Nuti R, Martini G, Valenti R, et al. Prevalence of undiagnosed coeliac sindrome in osteoporotic women. J Intern Med
2001; 250:361-624. Hahn TJ, Birge SJ, Scharp CR, et al. Phenobarbital induced alterations in vitamin D metabolism. J Clin Invest 1972: 51:741-825. Clements MR, Davies M, Fraser DR, et al. Metabolic inactivation of vitamin D is enhanced in primary hyperparathyroidism.
Clin Sci 1987: 73:659-6426. Krawitt EL, Grundman MJ, Mawer EB. Absorption, hydroxylation and excretion of vitamin D3 in primary biliary cirrhosis.
Lancet 1977; ii:1246-927. Goodman WG, Coburn JW, Slatoposky E, et al. Renal osteodistrophy in adults and children. In: Primer on the metabolic bone
diseases and disorders of mineral metabolism. Favus MJ (Ed). American Society of Bone and Mineral Research, Washington D.C., 2003, pp. 430-47
28. Miller WL, Portale AA. Genetic causes of rickets. Curr Opin Pediatr 1999; 11:333-929. St-Arnaud R, Messerlian S, Moir JM, et al. The 25-hydroxyvitamin D l-alpha-hydroxylase gene maps to the pseudovitamin
D-deficiency rickets (PDDR) disease locus. J Bone Miner Res 1997; 12:1552-930. Haussler MR, Haussler CA, Jurutka PW, et al. The vitamin D hormone and its nuclear receptor: molecular actions and disease
states. J Endocrinol 1997; 154:S57-57331. Dominguez JH, Gray RW, Lemann J. Dietary phosphate deprivation in women and men. Effects on mineral and acid balance,
parathyroid hormone and the metabolism of 25-OH-vitamin D. J Clin Endocrinol Metab 1976; 43:1056-68
pag.317
-
Osteomalacia - pp. 310/318
32. Lotz M, Zisman E, Bartter FC. Evidence for a phosphorus-depletion syndrome in man. N Engl J Med 1968; 278:409-5233. Winters R, Graham J, Williams T, et al. A genetic study of familial hypophosphatemia and vitamin D resistant rickets with a
review of the literature. Medicine 1958; 37:97-14234. Econs M, Drezner M. Bone disease resulting from inherited disorders o renal tubule transport and vitamin D metabolism.
In: Favus M, Coe F (eds). Disorders of Bone and Mineral Metabolism. Raven Press Lld, New York, 1992; pp. 935-5035. Coleman E, Foole J. Craniostenosis with familial vitamin-D-resistant rickets. Brit Med J 1954; 1:561-236. HYP consortium. A gene (PEX) with homologies to endopeptidases is mutated in patients with X-linked hypophosphatemic
rickets. Nat Genet 1995; 11:130-637. Francis F, Strom TM, Hennig S, et al. Genomic organization of the human PEX gene mutated in X-linked dominant
hypophosphatemic rickets. Genome Res 1997; 7:573-8538. White K, Speer M, Biber J, et al. Refining the autosomal dominant hypophosphalemic rickets (ADHR) interval on chromosome
12p13 and localization of two candidate ADHR genes. Bone 1998; 23:S37939. Tieder M, Modai D, Samuel R, et al. Hereditary hypophosphatemic rickets with hypercalciuria. N Engl J Med 1985; 312:611-740. Weidner N, Santa CD. Phosphaturic mesenchymal tumors. A polymorphous group causing osteomalacia or rickets. Cancer
1987; 59:1442-5441. Jonsson KB, Zahradnik R, Larsson T, et al. Fibroblast growth factor 23 in oncogenic osteomalacia and X-linked hypophosphatemia.
N Engl J Med 2003; 348:1656-6342. Kumar R. Tumor-induced osteomalacia and the regulation of phosphate homeostasis. Bone 2000; 27:333-843. Sebastian A, McSherry E, Morris RC Jr. On the mechanism of renal potassium wasting in renal tubular acidosis associated with
the Fanconi syndrome (type 2 RTA). J Clin Invest 1971; 50:231-4344. Rodriguez Soriano J, Houston IB, Boichis H, et al. Calcium and phosphorus metabolism in the Fanconi syndrome. J Clin
Endocrinol Metab 1968; 28:1555-6345. Bushinsky DA, Frick KK. The effects of acid on bone. Curr Opin Nephrol Hypertens 2000; 9:369-7946. Eiamong S, Kurtzman NA. Metabolic acidosis and bone disease. Miner Electrolyte Metab 1994; 20:72-8047. Boyce BF, Smith L, Fogelman I, et al. Focal osteomalacia due to low-dose diphosphonate therapy in Paget's disease. Lancet
1984; 1:821-448. Compston JE, Chadha S, Merrett AL. Osteomalacia developing during treatment of osteoporosis with sodium fluoride and
vitamin D. Br Med J 1980; 281:910-149. Baker SL, Dent CE, Friedman N, Watson L. Fibrogenesis imperfecta ossium. J Bone Joint Surg 1966; 48B:804-2550. Whyte MP. Hypophosphatasia. In: Scriver CR, Beaudet AL, Sly WS, Valle D, Childs B, Vogelstein B (eds.) The Metabolic and
Molecular Bases of Inherited Disease, McGraw-Hill, New York, 2001; pp.5313-2951. Weinstein RS, Whyte MP. Heterogeneity of adult hypophosphatasia: Report of severe and mild cases. Arch Intern Med
1981; 141:727-3152. Wenkert D, Podgornik MN, Coburn SP, et al. Dietary phosphate restriction therapy for hypophosphatasia: Preliminary
observations. J Bone Miner Res 2002; 17:S384
R. Nuti et al. pag.318