Nutrienti,integratori alimentari, fitoterapia e ... · endogeno della serotonina. Griffonia...
Transcript of Nutrienti,integratori alimentari, fitoterapia e ... · endogeno della serotonina. Griffonia...

Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
FABRIZIO MURATORI Unitagrave Operativa di Endocrinologia Nutrizione Clinica e Obesitagrave
Ospedale SantrsquoAnna di Como
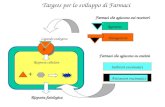
FITOTERAPICI
Stimolanti Guaranagrave Mategrave Citrus Aurantium Ephedra sinicaMa Huang Fucus Vescicolosus
Metabolici Garcinia Cambogia Estratto del fagiolo
Modulatori umore eo adattogeni Rhodiola rosea Griffonia Iperico
Drenanti Orthosiphon Pilosella
Fibre Psyllio Gomma guar ALTRI AGENTI
NOPE + EGCG
AGENTI COADIUVANTI IL CALO PONDERALE
Coleretici Epatoprotettori Boldo Cardo mariano Tarassaco
Principali piante medicinali impiegate nel sovrappesoobesitagrave
Nome comune della droga Principali costituenti chimici Dose consigliata die
Arancia amara Sinefrina Non superare i 30 mg die
Efedra sinicaMa Huang Efedrina pseudoefedrina Non piugrave in commercio in Italia
Guaranagrave Alcaloidi purinici (caffeina)
tannini
1-3 grammi
Fucus vesciculosos (Fuco) Iodio polisaccaridi Non sono disponibili dati
attendibili
Griffonia simplicifolia 5 OH triptofano (5OHT) 100 ndash 600 mg die in 5OHT
Rhodiola Rosea Rosavin Salidroside
Garcinia Cambogia Acido idrossicitrico 15 grammi
Fagiolo Faseolamina
Orthosiphon Flavonoidi cumarine terpenoidi Secondo prescrizione medica
Tarassaco Olio essenziale flavonoidi
derivati dellrsquoacido caffeico
Secondo prescrizione medica
Gomma Guar Galattomannano proteine 9-30 grammi
Psillio mucillagini 10-30 grammi
Serotonina (5-HT) Favorisce la sazietagrave
Noradrenalina (NA) Inibisce lrsquoassunzione di cibo (sistema β-adrenergico)
Dopamina (DA) Inibisce lrsquoassunzione di cibo
1 Obesity advances in understanding and treatments 1995 (May 22) 22 6 (2-3) 26-41
2 Hoebel et al Brain Behav Bodily Dis 1981 59 103-142
Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
Talamo Ipotalamo
Ipofisi
NUTRIENTI MODULANTI LrsquoASSUNZIONE DI CIBO
TRIPTOFANO Il triptofano egrave uno degli amminoacidi essenziale quindi deve essere assunto attraverso gli alimenti ne sono ricchi i legumi le carni il pesce i latticini e le uova Il triptofano egrave precursore della niacina (vitamina PP) e della serotonina (5-HT) il suo uso come integratore egrave dovuto essenzialmente al suo ruolo nella sintesi di serotonina La serotonina egrave una monamina presente in vari animali dai celenterati ai vertebrati nei batteri e in molte piante Negli esseri umani egrave sintetizzata nelle cellule cromaffini intestinali o nei neuroni del sistema nervoso centrale e periferico Tale sostanza si trova in alte concentrazioni in vari tessuti del corpo tra cui la mucosa intestinale il corpo pineale e il sistema nervoso centrale La serotonina ha molte proprietagrave fisiologiche (ad esempio inibisce la secrezione gastrica stimola la muscolatura liscia funge da neurotrasmettitore centrale ed egrave un precursore della melatonina) Lrsquoinnalzamento dei livelli di questa monamina nel Sistema Nervoso Centrale egrave sfruttato nel trattamento della depressione ed egrave stato utilizzato per ridurre lrsquoassunzione di cibo
Griffonia Simplicifolia
Linteresse verso questa pianta in Europa egrave relativamente recente ed egrave dovuto alla scoperta che i suoi semi contengono la sostanza definita con la sigla 5-HTP (5-idrossitriptofano) un precursore endogeno della serotonina
Griffonia simplicifolia
L-5-Idrossitriptofano Intermedio di trasformazione del triptofano in serotonina presente ad elevate concentrazioni nei semi della Griffonia Simplicifolia Applicazioni Depressione Obesitagrave Emicrania cefalea e sindromi dolorose Morbo di Parkinson Disturbi del sonno
Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

FITOTERAPICI
Stimolanti Guaranagrave Mategrave Citrus Aurantium Ephedra sinicaMa Huang Fucus Vescicolosus
Metabolici Garcinia Cambogia Estratto del fagiolo
Modulatori umore eo adattogeni Rhodiola rosea Griffonia Iperico
Drenanti Orthosiphon Pilosella
Fibre Psyllio Gomma guar ALTRI AGENTI
NOPE + EGCG
AGENTI COADIUVANTI IL CALO PONDERALE
Coleretici Epatoprotettori Boldo Cardo mariano Tarassaco
Principali piante medicinali impiegate nel sovrappesoobesitagrave
Nome comune della droga Principali costituenti chimici Dose consigliata die
Arancia amara Sinefrina Non superare i 30 mg die
Efedra sinicaMa Huang Efedrina pseudoefedrina Non piugrave in commercio in Italia
Guaranagrave Alcaloidi purinici (caffeina)
tannini
1-3 grammi
Fucus vesciculosos (Fuco) Iodio polisaccaridi Non sono disponibili dati
attendibili
Griffonia simplicifolia 5 OH triptofano (5OHT) 100 ndash 600 mg die in 5OHT
Rhodiola Rosea Rosavin Salidroside
Garcinia Cambogia Acido idrossicitrico 15 grammi
Fagiolo Faseolamina
Orthosiphon Flavonoidi cumarine terpenoidi Secondo prescrizione medica
Tarassaco Olio essenziale flavonoidi
derivati dellrsquoacido caffeico
Secondo prescrizione medica
Gomma Guar Galattomannano proteine 9-30 grammi
Psillio mucillagini 10-30 grammi
Serotonina (5-HT) Favorisce la sazietagrave
Noradrenalina (NA) Inibisce lrsquoassunzione di cibo (sistema β-adrenergico)
Dopamina (DA) Inibisce lrsquoassunzione di cibo
1 Obesity advances in understanding and treatments 1995 (May 22) 22 6 (2-3) 26-41
2 Hoebel et al Brain Behav Bodily Dis 1981 59 103-142
Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
Talamo Ipotalamo
Ipofisi
NUTRIENTI MODULANTI LrsquoASSUNZIONE DI CIBO
TRIPTOFANO Il triptofano egrave uno degli amminoacidi essenziale quindi deve essere assunto attraverso gli alimenti ne sono ricchi i legumi le carni il pesce i latticini e le uova Il triptofano egrave precursore della niacina (vitamina PP) e della serotonina (5-HT) il suo uso come integratore egrave dovuto essenzialmente al suo ruolo nella sintesi di serotonina La serotonina egrave una monamina presente in vari animali dai celenterati ai vertebrati nei batteri e in molte piante Negli esseri umani egrave sintetizzata nelle cellule cromaffini intestinali o nei neuroni del sistema nervoso centrale e periferico Tale sostanza si trova in alte concentrazioni in vari tessuti del corpo tra cui la mucosa intestinale il corpo pineale e il sistema nervoso centrale La serotonina ha molte proprietagrave fisiologiche (ad esempio inibisce la secrezione gastrica stimola la muscolatura liscia funge da neurotrasmettitore centrale ed egrave un precursore della melatonina) Lrsquoinnalzamento dei livelli di questa monamina nel Sistema Nervoso Centrale egrave sfruttato nel trattamento della depressione ed egrave stato utilizzato per ridurre lrsquoassunzione di cibo
Griffonia Simplicifolia
Linteresse verso questa pianta in Europa egrave relativamente recente ed egrave dovuto alla scoperta che i suoi semi contengono la sostanza definita con la sigla 5-HTP (5-idrossitriptofano) un precursore endogeno della serotonina
Griffonia simplicifolia
L-5-Idrossitriptofano Intermedio di trasformazione del triptofano in serotonina presente ad elevate concentrazioni nei semi della Griffonia Simplicifolia Applicazioni Depressione Obesitagrave Emicrania cefalea e sindromi dolorose Morbo di Parkinson Disturbi del sonno
Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Principali piante medicinali impiegate nel sovrappesoobesitagrave
Nome comune della droga Principali costituenti chimici Dose consigliata die
Arancia amara Sinefrina Non superare i 30 mg die
Efedra sinicaMa Huang Efedrina pseudoefedrina Non piugrave in commercio in Italia
Guaranagrave Alcaloidi purinici (caffeina)
tannini
1-3 grammi
Fucus vesciculosos (Fuco) Iodio polisaccaridi Non sono disponibili dati
attendibili
Griffonia simplicifolia 5 OH triptofano (5OHT) 100 ndash 600 mg die in 5OHT
Rhodiola Rosea Rosavin Salidroside
Garcinia Cambogia Acido idrossicitrico 15 grammi
Fagiolo Faseolamina
Orthosiphon Flavonoidi cumarine terpenoidi Secondo prescrizione medica
Tarassaco Olio essenziale flavonoidi
derivati dellrsquoacido caffeico
Secondo prescrizione medica
Gomma Guar Galattomannano proteine 9-30 grammi
Psillio mucillagini 10-30 grammi
Serotonina (5-HT) Favorisce la sazietagrave
Noradrenalina (NA) Inibisce lrsquoassunzione di cibo (sistema β-adrenergico)
Dopamina (DA) Inibisce lrsquoassunzione di cibo
1 Obesity advances in understanding and treatments 1995 (May 22) 22 6 (2-3) 26-41
2 Hoebel et al Brain Behav Bodily Dis 1981 59 103-142
Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
Talamo Ipotalamo
Ipofisi
NUTRIENTI MODULANTI LrsquoASSUNZIONE DI CIBO
TRIPTOFANO Il triptofano egrave uno degli amminoacidi essenziale quindi deve essere assunto attraverso gli alimenti ne sono ricchi i legumi le carni il pesce i latticini e le uova Il triptofano egrave precursore della niacina (vitamina PP) e della serotonina (5-HT) il suo uso come integratore egrave dovuto essenzialmente al suo ruolo nella sintesi di serotonina La serotonina egrave una monamina presente in vari animali dai celenterati ai vertebrati nei batteri e in molte piante Negli esseri umani egrave sintetizzata nelle cellule cromaffini intestinali o nei neuroni del sistema nervoso centrale e periferico Tale sostanza si trova in alte concentrazioni in vari tessuti del corpo tra cui la mucosa intestinale il corpo pineale e il sistema nervoso centrale La serotonina ha molte proprietagrave fisiologiche (ad esempio inibisce la secrezione gastrica stimola la muscolatura liscia funge da neurotrasmettitore centrale ed egrave un precursore della melatonina) Lrsquoinnalzamento dei livelli di questa monamina nel Sistema Nervoso Centrale egrave sfruttato nel trattamento della depressione ed egrave stato utilizzato per ridurre lrsquoassunzione di cibo
Griffonia Simplicifolia
Linteresse verso questa pianta in Europa egrave relativamente recente ed egrave dovuto alla scoperta che i suoi semi contengono la sostanza definita con la sigla 5-HTP (5-idrossitriptofano) un precursore endogeno della serotonina
Griffonia simplicifolia
L-5-Idrossitriptofano Intermedio di trasformazione del triptofano in serotonina presente ad elevate concentrazioni nei semi della Griffonia Simplicifolia Applicazioni Depressione Obesitagrave Emicrania cefalea e sindromi dolorose Morbo di Parkinson Disturbi del sonno
Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Serotonina (5-HT) Favorisce la sazietagrave
Noradrenalina (NA) Inibisce lrsquoassunzione di cibo (sistema β-adrenergico)
Dopamina (DA) Inibisce lrsquoassunzione di cibo
1 Obesity advances in understanding and treatments 1995 (May 22) 22 6 (2-3) 26-41
2 Hoebel et al Brain Behav Bodily Dis 1981 59 103-142
Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
Talamo Ipotalamo
Ipofisi
NUTRIENTI MODULANTI LrsquoASSUNZIONE DI CIBO
TRIPTOFANO Il triptofano egrave uno degli amminoacidi essenziale quindi deve essere assunto attraverso gli alimenti ne sono ricchi i legumi le carni il pesce i latticini e le uova Il triptofano egrave precursore della niacina (vitamina PP) e della serotonina (5-HT) il suo uso come integratore egrave dovuto essenzialmente al suo ruolo nella sintesi di serotonina La serotonina egrave una monamina presente in vari animali dai celenterati ai vertebrati nei batteri e in molte piante Negli esseri umani egrave sintetizzata nelle cellule cromaffini intestinali o nei neuroni del sistema nervoso centrale e periferico Tale sostanza si trova in alte concentrazioni in vari tessuti del corpo tra cui la mucosa intestinale il corpo pineale e il sistema nervoso centrale La serotonina ha molte proprietagrave fisiologiche (ad esempio inibisce la secrezione gastrica stimola la muscolatura liscia funge da neurotrasmettitore centrale ed egrave un precursore della melatonina) Lrsquoinnalzamento dei livelli di questa monamina nel Sistema Nervoso Centrale egrave sfruttato nel trattamento della depressione ed egrave stato utilizzato per ridurre lrsquoassunzione di cibo
Griffonia Simplicifolia
Linteresse verso questa pianta in Europa egrave relativamente recente ed egrave dovuto alla scoperta che i suoi semi contengono la sostanza definita con la sigla 5-HTP (5-idrossitriptofano) un precursore endogeno della serotonina
Griffonia simplicifolia
L-5-Idrossitriptofano Intermedio di trasformazione del triptofano in serotonina presente ad elevate concentrazioni nei semi della Griffonia Simplicifolia Applicazioni Depressione Obesitagrave Emicrania cefalea e sindromi dolorose Morbo di Parkinson Disturbi del sonno
Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

NUTRIENTI MODULANTI LrsquoASSUNZIONE DI CIBO
TRIPTOFANO Il triptofano egrave uno degli amminoacidi essenziale quindi deve essere assunto attraverso gli alimenti ne sono ricchi i legumi le carni il pesce i latticini e le uova Il triptofano egrave precursore della niacina (vitamina PP) e della serotonina (5-HT) il suo uso come integratore egrave dovuto essenzialmente al suo ruolo nella sintesi di serotonina La serotonina egrave una monamina presente in vari animali dai celenterati ai vertebrati nei batteri e in molte piante Negli esseri umani egrave sintetizzata nelle cellule cromaffini intestinali o nei neuroni del sistema nervoso centrale e periferico Tale sostanza si trova in alte concentrazioni in vari tessuti del corpo tra cui la mucosa intestinale il corpo pineale e il sistema nervoso centrale La serotonina ha molte proprietagrave fisiologiche (ad esempio inibisce la secrezione gastrica stimola la muscolatura liscia funge da neurotrasmettitore centrale ed egrave un precursore della melatonina) Lrsquoinnalzamento dei livelli di questa monamina nel Sistema Nervoso Centrale egrave sfruttato nel trattamento della depressione ed egrave stato utilizzato per ridurre lrsquoassunzione di cibo
Griffonia Simplicifolia
Linteresse verso questa pianta in Europa egrave relativamente recente ed egrave dovuto alla scoperta che i suoi semi contengono la sostanza definita con la sigla 5-HTP (5-idrossitriptofano) un precursore endogeno della serotonina
Griffonia simplicifolia
L-5-Idrossitriptofano Intermedio di trasformazione del triptofano in serotonina presente ad elevate concentrazioni nei semi della Griffonia Simplicifolia Applicazioni Depressione Obesitagrave Emicrania cefalea e sindromi dolorose Morbo di Parkinson Disturbi del sonno
Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Griffonia Simplicifolia
Linteresse verso questa pianta in Europa egrave relativamente recente ed egrave dovuto alla scoperta che i suoi semi contengono la sostanza definita con la sigla 5-HTP (5-idrossitriptofano) un precursore endogeno della serotonina
Griffonia simplicifolia
L-5-Idrossitriptofano Intermedio di trasformazione del triptofano in serotonina presente ad elevate concentrazioni nei semi della Griffonia Simplicifolia Applicazioni Depressione Obesitagrave Emicrania cefalea e sindromi dolorose Morbo di Parkinson Disturbi del sonno
Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Griffonia simplicifolia
L-5-Idrossitriptofano Intermedio di trasformazione del triptofano in serotonina presente ad elevate concentrazioni nei semi della Griffonia Simplicifolia Applicazioni Depressione Obesitagrave Emicrania cefalea e sindromi dolorose Morbo di Parkinson Disturbi del sonno
Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Griffonia Simplicifolia
Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Griffonia Simplicifolia
Phytomedicine 2011 Aug 1518(11)947-52 Influence of Griffonia simplicifolia on male sexual behavior in rats behavioral and neurochemical study Carnevale G Di Viesti V Zavatti M Benelli A Zanoli P Source Department of Biomedical Sciences University of Modena and Reggio Emilia Via Campi 287 I-41100 Modena Italy Abstract The seeds of Griffonia simplicifolia Baill are rich in 5-HTP (5-hydroxytryptophan) a direct precursor of the neurotransmitter serotonin In the present study we investigated the influence of the plant extract on male sexual behavior The seed extract was orally administered to Sprague-Dawley male rats at three dose levels (25 50 and 100 mgkg) both acutely and subchronically (daily for 9 days) Mating test with receptive female rats was performed 60 min after the acute treatment or the last dose when repetitively administered Mount intromission and ejaculation latencies and post-ejaculatory interval were recorded Food intake and body weight were measured over the 9-day period of treatment Microdialysis technique was used to detect the extracellular levels of serotonin (5-HT) and its metabolite 5-hydroxyindoleacetic acid (5-HIAA) in rat brain following the acute administration of the extract dosed at 100mgkg The acute treatment significantly increased mount latency (at any dosage) intromission and ejaculation latencies (at 100 mgkg) and post-ejaculatory interval (at 50 and 100 mgkg) On the contrary the subchronic treatment failed to exert a significant influence on copulatory behavior The daily administration of the extract dosed at 50 and 100 mgkg for 9 days significantly reduced food intake and body weight Finally in the microdialysis experiments we found a dramatic increase in 5-HT and its metabolite 5-HIAA Copyright copy 2011 Elsevier GmbH All rights reserved
Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Citrus Aurantium
Il principale composto farmacologicamente attivo del Citrus egrave la p-sinefrina (para-sinefrina o ossedrina)
Lrsquoimpiego di Citrus Aurantium egrave consentito e regolamentato dal Ministero della Salute
Dose massima giornaliera di sinefrina 30 mg come integratore
Corrispondenti a 800 mg di Citrus titolato al 4
Altre formalitagrave bull Va riportata la titolazione in sinefrina bull Si sconsiglia lrsquouso in gravidanza e durante lrsquoallattamento e al di sotto dei 12 anni bull Consultare il medico prima dellrsquouso se le condizioni CV non sono nella norma
Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Sinefrina Octopamina
Il composto principale farmacologicamente attivo del Citrus egrave la p-sinefrina (para sinefrina o ossedrina)
Esistono 6 possibili isomeri della sinefrina (orto meta para e per ciascuno di essi la forma d (+) o l (-)
La p-sinefrina avrebbe unrsquoazione stimolante i beta 3 recettori e quindi lipolitica termogenetica
Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Citrus Aurantium
A causa della somiglianza strutturale della p-sinefrina con m-sinefrina efedrina noradrenalina e amfetamina egrave diffusa la percezione che tutte queste molecole abbiano proprietagrave simili e simile profilo di rischio
Invece esistono notevoli differenze bull La p-sinefrina non passa facilmente
la barriera ematoencefalica bull La p-sinefrina egrave meno lipo-solubile
dellrsquoefedrina bull Ha unrsquoazione stimolante il SNC e CV
minima o assente rispetto a efedrina noradrenalina amfetamina
bull Diversa affinitagrave recettoriale
Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Citrus Aurantium
Citrus Aurantium
Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Garcinia Gambogia
Il costituente attivo e piugrave studiato della Garcinia egrave lrsquoacido idrossicitrico (HCA)
Possibile meccanismo drsquoazione di HCA
bull Inibizione competitiva dellrsquoenzima adenosin-trifosfato-citrato-liasi
bull Incremento del rilascio o della disponibilitagrave di serotonina
bull Inibizione della alfa-amilasi pancreatica e dellrsquoalfa-glucosidasi intestinale con riduzione del metabolismo dei carboidrati
Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Garcinia Gambogia
Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Garcinia Gambogia
Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Rhodiola rosea Da secoli conosciuta ed ampiamente utilizzata nei paesi di origine noncheacute in tutta lrsquoAsia per le sue innumerevoli proprietagrave la Rhodiola rosea ha visto in questi ultimi anni crescere la propria popolaritagrave anche nei paesi occidentali grazie soprattutto alle sue caratteristiche di modulatore dellrsquoumore anti depressivo e coadiuvante nel controllo del peso corporeo
Le proprietagrave adaptogene della radice di Rhodiola rosea sono probabilmente ascrivibili alla presenza di alcuni particolari composti di tipo fenolico In particolare sono stati identificati ben ventotto composti di diversa natura tra questi il primo ad essere individuato egrave stato il rhodioloside del quale piugrave tardi egrave stata scoperta lrsquoidentitagrave con il salidroside (glicoside del tirosolo) giagrave notoriamente presente in altre piante quali ad esempio il salice Successivamente sono stati isolati altri composti di natura glicosidica ovvero rosavin rosarin rosin rodiosin rhodalin rhodionin astragalin tricin 5-O-glucoside e campferolo-7-ramnoside
Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Rhodiola rosea
Meccanismi drsquoazione Rhodiola rosea
bull Inibizione della catecol-O-metil transferasi (COMT) e effetto stimolante condotto nei confronti del trasporto del precursore della molecola della serotonina il 5-idrossitriptofano (5-HTP) attraverso la barriera emato-encefalica
bull Modulazione della disponibilitagrave cerebrale di noradrenalina e dopamina bull Stimolazione dellrsquoattivitagrave della lipoprotein-lipasi (LPL) bull Miglioramento delle performance sportive con riduzione dei tempi di recupero
Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Rhodiola rosea
Applicazioni Rhodiola rosea
Depressionefame nervosa Memoria Mantenimento del peso Prestazioni sportive
250 mg per 1-3 volte al giorno come razione giornaliera 500 mg prima di attivitagrave importanti o situazioni che richiedano unrsquoattenzione ed energia straordinarie
Posologia Rhodiola rosea
Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Lrsquoorthosiphon (orthosiphon stamineus) egrave utile come diuretico-depurativo Lrsquoeffetto diuretico non elimina solo lrsquoacqua ma anche i cloruri lrsquourea e altri cataboliti per cui puograve essere un ottimo aiuto nei casi in cui i valori di azotemia uricemia colesterolemia risultano aumentati
Orthosiphon
Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Epigallocatechingallato EGCG
Egrave una catechina del tegrave particolarmente abbondante nel tegrave verde ha ndash azione ipolipemizzante ndash azione sul dispendio energetico ndash azione antiossidante
Epigallocatechingallato EGCG
EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

EFFICACIA DI UN ESTRATTO DI TE VERDE RICCO IN CATECHINE E CAFFEINA NELLrsquoAUMENTARE IL
DISPENDIO DI ENERGIA IN 24 ORE E LrsquoOSSIDAZIONE DEI GRASSI NELLrsquoUOMO
Nello studio viene dimostrato come il trattamento con estratto di te verde rispetto al placebo in 24 ore aumenta il dispendio di energia (4)
Lrsquoescrezione urinaria di norepinefrina risulta maggiore durante il trattamento con te verde
In conclusione lrsquoestratto di te verde puograve giocare un ruolo importante nel controllo del peso corporeo tramite lrsquoattivazione simpatica della termogenesi e dellrsquoossidazione dei grassi
Am J Clin Nutr 1999 Dec70(6)1040-5 Efficacy of a green tea extract rich in catechin polyphenols and caffeine in increasing 24-h energy expenditure and fat oxidation in humans Dulloo AG Duret C Rohrer D Girardier L Mensi N Fathi M Chantre P
EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
ndash Uno studio pubblicato nel 2008 su The American Journal of Clinical Nutrition ha dimostrato come in soggetti giovani sani lrsquoesercizio fisico associato ad integrazione con ECGC aumenti lrsquoossidazione lipidica e la sensibilitagrave periferica allrsquoinsulina
Am JClinNutr 2008 87778-84
Tass
o d
i oss
idaz
ion
e lip
idic
a (k
Jm
in)
8
3
4
6
Tempo (minuti) 20 30
5
7
10
EGCG Placebo
p lt 001
In
dic
e d
i se
nsi
bili
tagrave in
sulin
ica
9
0
3
6
EGCG Placebo
Placebo
p lt 005
EGCG
IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

IL RUOLO DEL FARMACO NELLA TERAPIA INTEGRATA
Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Guida per la Scelta del Trattamento Integrato
The Practical Guide Identification Evaluation and Treatment of Overweight and Obesity in Adults October 2000 NIH Pub No00-4084
Dieta Esercizio Behavior Tx Farmaco- terapia Chirurgia
25ndash269 27ndash299 30ndash349 35ndash399 ge40
Categorie di BMI (kgm2)
+ + + + +
Con co- morbilitagrave
Con co- morbilitagrave
+ + +
+
Trattamento
Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
Anno Farmaco Motivo dellrsquoabbandono eo ritiro - 1893 Estratti tiroidei Ipertiroidismo - 1933 Dinitrofenolo Cataratta neuropatia - 1937 Amfetamina Dipendenza e abuso - 1967 Pillole Arcobaleno Morte - 1971 Aminorex Ipertensione polmonare - 1997 Fenfluramina Ipertensione polmonare e e Dexfenfluramina Insufficienza valvolare - 2008 Rimonabant Depressione - 2010 Sibutramina aumento di eventi - cardiovascolari in soggetti - con preesistenti malattie - cardiovascolari
La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

La situazione attuale
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica in Italia ultimi 15 anni
In commercio
Ritiro dal commercio
Solo magistrale
Sospensione dal commercio
Entrata e ritiro dal commercio
1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

1995 1996 1997 1998 1999 2000 2001 2002 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011
Fenfluramina Dex-fenf
Fendime-trazina
Dietil-propione
fentermina
orlistat
sibutramina
rimonabant
Storia della terapia farmacologica negli USA ultimi 15 anni
In commercio
Ritiro dal commercio
Rinuncia dellrsquoazienda produttrice
How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

How Physician Obesity Specialists Use Drugs to Treat Obesity
Ed J Hendricks Richard B Rothman and Frank L Greenway
Published online 19 March 2009
Farmaci prescritti nel trattamento dellrsquoobesitagrave dai medici specialisti statunitensi
Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Farmaco Frequenza drsquouso Fentermina 97 Dietilpropione 64 Fendimetrazina 60 Metamfetamina 3 Sibutramina 49 Orlistat 43 Topiramato 50 Zonisamide 9 5-HTPCarbidopa 20
Hendricks EJ et al How Physician Obesity Specialists Use Drugs to Treat Obesity Obesity 2009 Mar 19
Farmaci prescritti dai medici specialisti in obesitagrave e la percentuale dei medici che utilizza i vari farmaci nella pratica clinica in USA
ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

ORLISTAT E CALO PONDERALE
MECCANISMO DrsquoAZIONE
Le lipasi rompono i trigliceridi in monogliceridi ed acidi grassi liberi Orlistat si lega al sito attivo delle lipasi inibendo il 30 dellrsquoattivitagrave lipasica In questo modo orlistat previene lrsquoassorbimento di circa il 30 dei lipidi introdotti con la dieta Orlistat viene assorbito in minima parte ( lt3 ) dal tratto gastrointestinale e non interferisce con le lipasi sistemiche
1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

1 Sjostrom et al Lancet 1998352167 n= 688 2 Davidson et al JAMA 1999281235 n= 450 3 Rossner et al Obes Res 2000849 N = 720
4 Finer et al Int J Obes Relat Metab Disord 200024306
Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
Plt005 orlistat vs placebo
0
10
20
30
40
50
60
70 ge5 Weight Loss ge10 Weight Loss
Subj
ects
()
Study
Placebo Orlistat
1 2 3 4 1 2 3 4
ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

ORLISTAT E COMORBILITArsquo
143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

143 158 Normale Diabete
143 421
IGT Diabete
491 716 IGT Normale
Miglioramento
Heymsfield S et al Arch Intern Med 2000 160(9) 1321-26
plt005 per i pazienti con tolleranza al glucosio normale o diminuita (IGT) al basale
Orlistat migliora la tolleranza al glucosio uno studio di due anni
Placebo n= 316 Orlistat 120 mg n= 359
0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

0ndash5 5ndash10 10ndash15 gt15
Cha
nge
in P
lasm
a
LDL-
Cho
lest
erol
Con
cent
ratio
n (m
mol
L)
Weight Loss Category ( initial body weight)
-03
00
-05
-04
-02 -01
-06
-08
-10
-09
-07
Independent Effect of Orlistat on Plasma LDL-Cholesterol
Segal et al FASEB J 199913A873
Orlistat Placebo
Plt001 vs placebo
Data pooled from 5 trials (Total n=1773) Orlistat = 1072 Placebo = 701
Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Orlistat caused a 25 Dietary Cholesterol Absorption
Baseline Orlistat
50
20
10
60
40
30
Plt005 vs baseline Mittendorfer et al Obes Res 20019599
0
C
hole
ster
ol A
bsor
bed
(
inge
sted
)
Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Orlistat e prevemzione delle comorbilitagrave
Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Risultati di XENDOS Incidenza cumulativa di diabete di tipo 2
Placebo + stile di vita Orlistat + stile di vita
0
26
52
78
104
130
156
182
208
0
2
4
6
8
10
Settimane
p=00032 RR^ 37
90
62
^ Riduzione del rischio relativo vs placebo + stile di vita
Sjostrom et al Diabetes Care 27 155-161- 2004
0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

0 4 8 12 16 2
0 24 30 34 38 42 46 50 54 60
96
92
88
84
80
76
Week
Mea
n W
eigh
t Los
s K
g plusmn
SEM
N=54 N=54
Placebo
N=58
N=58
Combination
N=54
N=52
+ Combination
N=12 N=7
Augmentation
Open-Label Therapy Double-Blind Therapy B Mod + Diet +
Exercise
N=21 N=23
Weintraub et al Clin Pharmacol Ther 51 1992
Esempio di terapia farmacologica con associazione di due principi attivi
Phen-fen
Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Fentermina + Topiramato (Qnexa)
Fentermina bull Farmaco noradrenergico bull In commercio dagli anni lsquo50 bull Ersquo tuttora il farmaco anti-obesitagrave piugrave usato bull Non ha azione sul sistema serotoninergico bull Dose massima giornaliera 30 mg
Topiramato bull Farmaco GABAergico bull In commercio dal 1996 bull AIC anti epiletticoprofilassi emicrania bull Dose massima giornaliera 400 mg
46 23
375
92
Topiramate
150 0 100 350 50 250 200 400 300
Phentermine
10 0 75 5 20 15 30 25
Low Mid Full
Dose max approvata
Mono-somministrazione orale a rilascio prolungato di fentermina e topiramato
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Studio Equip
Studio Conquer
BMIgt35 (n=1267)
Placebo (n=514)
Qnexa Low Dose (n=241)
Qnexa Full Dose (n=512)
titration
4 settimane
trattamento
52 settimane
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Placebo (n=994)
Qnexa Mid Dose (n=498)
Qnexa Full Dose (n=995)
titration
4 settimane
trattamento
52 settimane
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Efficacia PLACEBO Qnexa low dose
Qnexa full dose
ITT -LOCF
Perdita di peso 16 51 110
pazienti calo gt 5 17 45 67
PLACEBO Qnexa mid dose
Qnexa full dose
ITT -LOCF
Perdita di peso 18 84 104
pazienti calo gt 5 21 62 70
Fentermina + Topiramato (Qnexa)
Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Studio Equip
Studio Conquer
BMIgt35 (n=1267)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
Categorie di perdita di peso PLACEBO
(47)
Qnexa low dose (57)
Qnexa full dose (59) completers
gt 15 5 11 43
gt 10 12 27 60
gt 5 26 59 84
PLACEBO
(57)
Qnexa mid dose
(69)
Qnexa full dose (64) completers
gt 15 4 26 36
gt 10 10 49 64
gt 5 26 75 85
p lt0026 plt00001
Fentermina + Topiramato (Qnexa)
Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Miglioramento delle comorbilitagrave
Studio CONQUER Fattori di rischio CV
Qnexa Mid
Valore di
p
Qnexa Full
Valore di
p
Circ vita darr lt00001 darr lt00001 PAS darr 0002 darr lt00001 PAD darr ns darr 00031 TG darr lt00001 darr lt00001 Colest totHDL
darr lt00001 darr lt00001
Colest tot darr 0035 darr 00014 LDL darr ns darr 00069 HDL uarr lt00001 uarr lt00001
Fentermina + Topiramato (Qnexa)
BMI = 27-45 con Due o piugrave co-morbilitagrave (n=2487)
EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

EQUIP (N=1264) CONQUER (N=2485)
Placebo Qnexa Low
Qnexa Full
Placebo Qnexa Low
Qnexa Full
Secchezza fauci 37 67 170 24 135 208
Formicolii 19 42 188 20 137 205
Stipsi 68 79 141 59 151 174
Infezioni respiratorie alte 109 158 123 129 122 134
Disgeusia 10 13 84 11 74 104
Insonnia 49 50 78 47 58 103
Cefalea 101 104 119 91 70 102
Vertigini 41 29 57 31 72 100
Raffeddrore 72 125 90 87 106 99
Sinusiti 55 75 72 67 68 86
Mal di schiena 51 54 55 49 56 72
Nausea 47 58 72 42 36 68
Offuscmento della vista 31 63 45 36 40 60
Bronchiti 43 67 55 43 44 52
Diarrea 45 50 47 48 64 58
Infezioni vie urinarie 35 33 47 37 52 54
Fentermina + Topiramato (Qnexa)
Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Effects of low-dose controlled-release phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER) a randomised placebo-controlled phase 3 trial
Gadde KM Allison DB Ryan DH Peterson CA Troupin B Schwiers ML Day WW
Lancet 2011 Apr 16377(9774)1341-52
wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

wwwthelancetcom Published online April 11 2011 DOI101016S0140-6736(11)60205-5
Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Figure 3
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
SBP=systolic blood pressure DBP=diastolic blood pressure TC=total cholesterol LDL-C=LDL-cholesterol HDL-C=HDL-cholesterol
Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Table 2
Source The Lancet (DOI101016S0140-6736(11)60205-5)
Terms and Conditions
Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Presentazioni orali o poster su fentermina + topiramato
al Congresso Europeo sullrsquoObesitagrave ad Istanbul
CARDIOMETABOLIC RISK REDUCTION IS DIRECTLY RELATED TO MAGNITUDE OF WEIGHT LOSS WITH LOW DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE Stephan Rossner Craig A Peterson Barbara Troupin
EFFICACY AND TOLERABILITY OF TOPIRAMATE ALONE AND IN COMBINATION WITH PHENTERMINE George A Bray Louis J Aronne Alok K Gupta Wesley W Day Barbara Troupin
WEIGHT LOSS WITH LOW-DOSE CONTROLLED-RELEASE PHENTERMINETOPIRAMATE THERAPY IMPROVES GLYCAEMIC STATUS AND PREVENTS PROGRESSION TO TYPE 2 DIABETES MELLITUS W Timothy Garvey Craig A Peterson Barbara Troupin
LONG-TERM TREATMENT WITH CONTROLLED-RELEASE PHENTERMINETOPIRAMATE DEMONSTRATES SUSTAINED WEIGHT LOSS OVER 108 WEEKS W Timothy Garvey Wesley W Day Charles H Bowden
Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Fentermina + Topiramato (Qnexa)
VIVUS Files European Marketing Authorization Application for QNEXAreg in the Treatment of Obesity MOUNTAIN VIEW Calif Dec 20 2010 PRNewswire -- VIVUS Inc(Nasdaq VVUS) today announced that the company filed a Marketing Authorization Application (MAA) with the European Medicines Agency (EMA) for QNEXAreg (phenterminetopiramate)controlled Release Capsules in the European Union (EU) The proposed indication in the EU is for the treatment of obesity including weight loss and maintenance of weight loss and should be used in conjunction with a mildly hypocaloric diet If approved in the EU QNEXAreg could be
recommended for obese adult patients (BMI ge 30 kgm2) or overweight patients (BMI ge 27 kgm2) with weight-related co-morbidities such as hypertension type 2 diabetes dyslipidemia or central adiposity(abdominal obesity)
Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Anti-obesity drugs to be or not to be
Dvorak RV Sharma AM Astrup A Obes Rev 2010 Dec11(12)833-4
Farmaci anti-obesitagrave essere o non essere
Gli estensori di quellrsquoeditoriale contestano lrsquoincompetenza dei membri delle commissioni sui temi dellrsquoobesitagrave sottolineando che tranne in un caso nessuno di questi ldquoespertirdquo ha al centro della sua pratica clinica quotidiana la gestione dei pazienti obesi e ciograve impedisce loro di valutare correttamente il rapporto rischibenefici dei farmaci anti-obesitagrave
FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

FORTRESS for Fetal Outcome Retrospective TopiRamate ExpoSure Study is a retrospective observational study utilizing existing electronic healthcare databases to assess fetal outcomes in the offspring of women who were exposed to topiramate during the first trimester of pregnancy FORTRESS is expected to include approximately 2500 topiramate exposed mother-infant pairs or dyads and is believed to be the largest retrospective topiramate medical claims study ever completed The co-primary endpoints will be the relative risk of major congenital malformations and oral cleft in the offspring of women exposed to topiramate during pregnancy as compared to a control group that was not exposed to topiramate FORTRESS is expected to include four distinct medical and pharmacy claim databases
ABOUT FORTTRESS verifica se il topiramato possa indurre malformazioni fetali o labbro leporino in chi lrsquoha assunto
Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Riunione avvenuta in data 22 febbraio della Commissione Fda
per approvazione Q-Nexa
bullLa Commissione ha approvato la possibilitagrave dellrsquoentrata in commercio di Q-Nexa con un punteggio di 20 commissari favorevoli a 2
bullIn data 17 luglio FDA si riuniragrave per lrsquoapprovazione ( o non ) definitva
Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Bupropione bull Farmaco dopaminergico e noradrenergico bull In commercio dagli anni lsquo85 e rsquo89 come SR bull AIC depressione disassuefazione al fumo bull Dose massima giornaliera 450 mg
Naltrexone bull Farmaco antagonista oppiacei bull In commercio dal 1984 bull AIC disintossicazione da dipendenze (alcool oppiacei) bull Dose massima giornaliera 50 mg
32
360
Bubropione
150 0 450 300
Naltrexone
10 0 40 50 20
Dose max approvata
Somministrazione due volte al giorno di bupropione SR e naltrexone
Bupropione + Naltrexone (Contrave)
30 48 16
Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Bupropione + Naltrexone azione sinergica
Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Categorie di perdita di peso PLACEBO (511)
Contrave (471)
ITT - LOCF
gt 15 2 119
gt 10 74 246
PLACEBO (290511) 56
Contrave (296471) 62 completers
gt 15 31 172
gt 10 107 345
gt 5 231 618
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1
Studio COR 1
Completers (n=982)
Completers (n=586)
In soggetti sani obesi Non diabetici
Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Miglioramento delle comorbilitagrave nei soggetti con aumentato rischio CV
PLACEBO (511)
Contrave (471)
Circonferenza vita (cm) -24 (282)
-71 (279)
Trigliceridi a digiuno gt 150 mgdL)
-32 (82)
-663 (87)
HDL (mgdl) lt50 o lt40
+13 (122)
+50 (121)
LDL (mgdl) -225 (29)
-128 (31)
HsPCR gt 3 mgL
-07 (163)
-29 (177)
p lt005
Bupropione + Naltrexone (Contrave)
Studio COR 1 (n=982)
Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Tollerabilitagrave e sicurezza
Bupropione + Naltrexone (Contrave)
Gli eventi avversi piugrave comuni sono stati Nausea Stipsi Cefalea
Gli eventi avversi piugrave gravi osservati in tutto il programma COR Colecistite Convulsioni Palpitazioni Parestesia Vertigini Anche se la nausea egrave stata la causa piugrave frequente di abbandono dello studio nella maggior parte dei pazienti in cui si egrave manifestata egrave stata lieve-moderata e transitoria
ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

ANCHE PER CONTRAVE NUOVE PROSPETTIVE
SAN DIEGO 20 settembre 2011 PRNewswire via COMTEX - Orexigen reg Therapeutics Inc (Nasdaq OREX) ha annunciato oggi che a seguito di un recente incontro con gli alti funzionari in carica della FDA di nuovi farmaci (OND) la Societagrave ha ricevuto scritta corrispondenza dettagli OND i requisiti di progettazione per una prova esiti cardiovascolari (CVOT) per Contrave reg che affrontare la lettera di risposta completa
(CRL) ha ricevuto nel gennaio 2011
Inizio studio 2012 e termine 2014 10000 pazienti per valutare lrsquoimpatto sulla sicurezza cardiovascolare
Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Effects of Liraglutide in the treatment of obesity a
randomised double-blind placebo-controlled study
Arne Astrup Stephan Roumlssner Luc Van Gaal Aila Rissanen Leo Niskanen Mazin Al Hakim
Jesper Madsen Mads F Rasmussen Michael E J Lean THE LANCET October 23 2009 DOI101016S0140-6736(09)61375-1
Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Placebo
Liraglutide
Orlistat
Trial profile
564 patients
BMI 30 ndash 40
stable bodyweight
FPGlt7mmmoll
Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Figure 1 Change in bodyweight Data are mean (95 CI) (ANCOVA estimate) for the intention-to-treat population with the last observation carried forward
Change in bodyweight
Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Safety tolerability anfd sustained weight loss over 2 years with the once-daily human GLP-1 analog Liraglutide
Astrup A Carraro R Finer N Harper A Kunesova M Lean ME Niskanen L Rasmussen MF Rissanen A Roumlssner S Savolainen MJ Van Gaal L
INTERNATIONAL JOURNAL OF OBESITY 2011 1-12 Aug 16 doi 101038ijo2011158
Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Lrsquoobesitagrave egrave una malattia cronica e i risultati vanno valutati nel lungo periodo
Con dieta attivitagrave fisica e intervento comportamentale solo una quota estremamente minoritaria di soggetti riesce a mantenere un calo di peso accettabile
I farmaci attuali hanno di per seacute unrsquoefficacia limitata Anche lrsquouso di integratori se supportato da letteratura
puograve essere preso in considerazione per il calo ponderale
Conclusioni
Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

Conclusioni
bullEsistono farmaci di tipo anoressante in fase avanzata di studio ma la storia recente di sibutramina fa pensare che non esista la volontagrave ldquopoliticardquo nelle Agenzie di controllo di approvare nuovi farmaci di questo tipo
bullDopo lrsquoarticolo di Astrup le posizioni intransigenti appaiono piugrave deboli e non in linea con I tempi
GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-

GRAZIE PER LrsquoATTENZIONE
- Nutrientiintegratori alimentari fitoterapia e farmcoterapia dellrsquoobesitagrave
- Diapositiva numero 2
- Diapositiva numero 3
- Circuiti Monoaminergici che Intervengono nella Assunzione di Cibo e nella Sazietagrave
- Diapositiva numero 5
- Diapositiva numero 6
- Diapositiva numero 7
- Diapositiva numero 8
- Diapositiva numero 9
- Diapositiva numero 10
- Diapositiva numero 11
- Diapositiva numero 12
- Diapositiva numero 13
- Diapositiva numero 14
- Diapositiva numero 15
- Diapositiva numero 16
- Diapositiva numero 17
- Diapositiva numero 18
- Diapositiva numero 19
- Diapositiva numero 20
- Epigallocatechingallato EGCG
- Diapositiva numero 22
- EGCG evidenze sperimentali sullrsquoaumento del dispendio energetico e del catabolismo lipidico
- Diapositiva numero 24
- Guida per la Scelta del Trattamento Integrato
- Gli insuccessi della terapia farmacologica dellrsquoobesitagrave
- Diapositiva numero 27
- Diapositiva numero 28
- Diapositiva numero 29
- Diapositiva numero 30
- Diapositiva numero 31
- Diapositiva numero 32
- Clinical Trials Evaluating Effect of 1-Year Orlistat Therapy on Body Weight
- Diapositiva numero 34
- Orlistat migliora la tolleranza al glucosio uno studio di due anni
- Independent Effect of Orlistat on PlasmaLDL-Cholesterol
- Orlistat caused a 25 Dietary Cholesterol Absorption
- Diapositiva numero 38
- Risultati di XENDOSIncidenza cumulativa di diabete di tipo 2
- Diapositiva numero 40
- Diapositiva numero 41
- Diapositiva numero 42
- Diapositiva numero 43
- Diapositiva numero 44
- Diapositiva numero 45
- Diapositiva numero 46
- Diapositiva numero 47
- Diapositiva numero 48
- Diapositiva numero 49
- Diapositiva numero 50
- Diapositiva numero 51
- Diapositiva numero 52
- Diapositiva numero 53
- Farmaci anti-obesitagrave essere o non essere
- Diapositiva numero 55
- Riunione avvenuta in data 22 febbraio della Commissione Fda per approvazione Q-Nexa
- Diapositiva numero 57
- Bupropione + Naltrexone azione sinergica
- Diapositiva numero 59
- Diapositiva numero 60
- Diapositiva numero 61
- ANCHE PER CONTRAVE NUOVE PROSPETTIVE
- Diapositiva numero 63
- Diapositiva numero 64
- Diapositiva numero 65
- Diapositiva numero 66
- Diapositiva numero 67
- Diapositiva numero 68
- Diapositiva numero 69
- Conclusioni
- Diapositiva numero 71
-