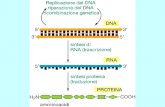
Lez 7 Processamento dellRNA negli eucaroti: RNA splicing..\Animations\ch12 _transcription.html.
-
Upload
mariano-mantovani -
Category
Documents
-
view
225 -
download
1
Transcript of Lez 7 Processamento dellRNA negli eucaroti: RNA splicing..\Animations\ch12 _transcription.html.

Lez 7
• Processamento dell’RNA negli eucaroti: RNA splicing
..\Animations\ch12_transcription.html

Fattori per la maturazione e processamento del RNA
• La CTD fosforilata recluta gli enzimi per il capping e per lo splicing
• Il capping viene effettuato subito dopo la sua sintesi

RNA factory
• Gli enzimi per il processamento del DNA sono portati dalla coda CTD della RNA Pol II.

RNA capping
Tre enzimi:
• Fosfatasi
• Guanil transferasi
• Metil transferasi
Fosfatasi
Guanil transferasi
Metil transferasi

3’ terminale di mRNA eucariotici
Sequenze consenso• AAUAAA è riconosciuta da cleavage and
polyadenylation specific factor (CPSF)• La regione GU-rich da Cleavage stimulation
factor F (CstF)

Produzione del 3’ terminale di mRNA eucariotici
• La sequenza AUAAA è riconosciuta da CPSF, la GU-rich da CstF, poi reclutano altri fattori che tagliano il DNA e viene reclutata poli-A-polimerasi (PAP)

Lo splicing

RNA Processing
Esoni introni: esempi di due geni umani

Esempi di splicing alternativo

Sequenze consenso per gli introni

Consensus sequence
• Un’alte conservazione si trova solo immediatamente all’interno degli introni alle giunzioni presunte. Questo identifica la sequenze di un introne generico come la regola : GU##AG: o GT-AG.
• I due siti hanno sequenze diverse e definiscono le terminazione degli introni direzionalmente .

Che meccanismo fa in modo che i due siti sono tagliati insieme?
Tutti i site 5e 3sites sono funzionalmente equivalenti, ma lo splicing segue delle regole che assicurano che il sito 5è sempre collegato al sito 3che viene dopo nel RNA.

Il meccanismo dello splicing
Attacco del 2’OH al 5’ splicing site con formazione del cappio
Attacco del 3’OH libero al 3’ splicing site
Liberazione del cappio

Meccanismo dello splicingLa giunzione a tre vie
del cappio

• Il branch site nei lieviti è conservato ed la sequenza consenso è UACUAAC..
• Il branch site si trova 18-40 nucleotidi a monte del 3 splice site.
• gli eucarioti superiori hanno sequenze correlate (cryptic sites)
• Il ruolo del the branch site è di identificare il 3’ più vicino come bersaglio per collegarlo al 5 splice site
transesterificazione• Il primo passaggio è un attacco
nucleofilo dal 2 –OH della A invariante del UACUAAC
• Nel secondo passaggio, il 3–OH libero dell’esone attacca il legame al 3splice site.

caratteristiche• Gli Splice sites sono generici: non
hanno specificità per gli RNA individuali,
• L’apparato dello splicing non è tessuto specifico;
• Lo splicing avviene solo tra siti 5’ e 3’ dello stesso introne.
• Lo splicing segue un cammino preferito.
• la reazione non procede sequenzialmente lungo il precursore.

spliceosomaIl complesso si assembla
sequenzialmente sul pre-mRNA, e lo splicing avviene solo dopo che tutti i componenti si sono assemblati
Il nucleo e il citoplasma contengono molti piccoli RNA (200-300 bp)
Quelli nel nucleo sono chiamati small nuclear RNAs (snRNA); e quelli nel citoplasma small cytoplasmic RNAs (scRNA).
lo spliceosome include un 50-60S ribonucleoprotein particle (più grande di quella del ribosoma), con 150 proteine
Le snRNPs coinvolte nello splicing sono U1, U2, U5, U4 e U6. Ogni snRNP contiene un solo snRNA e alcune (<20) proteine. Un nucleo strutturale comune per ogni snRNP consiste in un gruppo di 8 proteine, tutte riconosciute da un antisiero autoimmune chiamato anti-Sm

Gli snRNAs sono necessari per lo splicing
I cinque snRNPs coinvolti nello splicing sono U1, U2, U5, U4, e U6.
Insieme ad altre proteine addizionali, gli snRNPs formano lo spliceosome. Tra esse: U2AF (U2 Auxillary Factors) e BBP (branch point Binding Proteins).
Le proteine agiscono in modo coordinato con la formazione di tre complessi intermedi

Splicing stepsU1 snRNP inizia lo splicing legandosi allo
5splice mediante una reazione di appaiamento RNA-RNA.
Si forma il complesso E (early) che contiene U1 snRNP legato allo 5splice site, la proteina U2AF legata al tratto di pirimidine tra il branch site e allo 3splice site, e le SR proteine che collegano U1 snRNP a U2AF.
(Le SR si legano ai siti di splicing degli esoni: ESE =exonic splicing enhancer)

complesso E: early presplicing
contiene U1 snRNP legato al 5’splice-site
U2AF legata a Py tract ed al 3’ splice-site
Questa recluta BBPche si lega al branch site.
Quindi tutti i siti sono riconosciuti

Complesso A
U2 sostituisce BBP al branch site
L’appaiamento tra i due RNA spinge in fuori la A del Branch site, che diventa disponibile all’attacco

Complesso B• Il complesso A si
riarrangia e si avvicinano i 3 siti di splicing
• Questo avviene con l’ingresso della tripla U4/U5/U6
• Poi U6 sostituisce U1 al 5’splice -site

Complesso CU4 viene rilasciato, così U2 e U6
possono interagire con appaiamento degli RNA
Questa conformazione produce il sito attivo, che sembra essere composto principalmente da RNA.
il 5’Splice site è avvicinato al branch site (U2-U6). U5 avvicina i siti 3’ e 5’.
Il cappio e le SnRNP vengono rilasciati

RNA splicingPassaggi dello spliceosoma Complesso E (early) A: (Branch site) B1: (spliceosoma
completo) B2: U1 è rilasciato e si ha
un riarrangiamento C1: U4 è rilasciato ed
inizia la catalisi C2: sito 3’ tagliato e gli
esoni ligati• animazione
A
B
E
C

Accoppiamento RNA-RNA
• Il sito al 5’ è riconosciuto prima da U1 e poi da U6.
• U6 e U2 indirizzano la catalisi.

introni Self-splicing di gruppo II.
Rari introni di organelli.
Dimensione di 400-1000 nt
Lo splicing non necessita della presenza di proteine
Il meccanismo è simile a quello dello spliceosoma

introni Self-splicing di gruppo I.
Rari introni di eucarioti, rRNA o organelli.
Dimensione di 400-1000 nt
Una G si lega ad una tasca ed attacca il 5’splicing site
Hanno una sequenza di guida interna che si appaia alla sequenza del sito al 5’.
Lo splicing non necessita della presenza di proteine


Splicing alternativo
Nel gene DSCAM di drosofila gli ipotetici mRNA alternativi sono circa 38,000

Errori di splicing
• Uno esone può essere saltato
• Si possono usare siti criptici

Accuratezza dello splicing• Il sitema di splicing è sulla CTD della RNA
polimerasi ed interagisce sequenzialemente con l’RNA neosintetizzato
• Le proteine SR (ricche in Ser e Arg) si legano a sequenze esoniche dette Exonic splicing enhancer, ESE. Queste reclutano U2AF al 3’ ed U1 al 5’

Exon definition hypothesis

Splicing alternativo• La troponina dà luogo a due forme con due esoni
diversi: o il 3 o il 4• In genere le alternative possono essere costitutive
o regolate

Splicing alternativo• Ci sono almeno 5 modi diversi di fare
splicing alternativo

Esempio di Splicing alternativo costitutivo
L’antigene T del virus della scimmia SV40 ha 2 5’ splicing site alternativi (5’SST e 5’sst).
5’sst da luogo a un trascritto più lungo con uno stop codon (t-antigen)
5’SST and un trascritto più corto e peptide più lungo (T-ag)
Il rapporto tra i due è regolato dai livelli delle proteina di splicing SF2/ASF

Esempio di Splicing alternativo regolato Repressori: intronic-exonic splicing silencers (ESS o ISS).
Si legano a hnRNP (heterogenous nuclear ribonucleoproteins) e non hanno il dominio SR per il legame a U1 o U2AF. Bloccano i siti di enhancer
Gli attivatori (ESE o ISE) riconoscono una sequenza specifica e col dominio RS reclutano i fattori di splicing

hnRNPI è un inibitore dello splicing
Nasconde gli esoni con due meccanismi
• unendo le regioni fiancheggianti l’esone,
• coprendo cooperativamente l’esone.

Spliceosoma minore
Negli eucarioti superiori esiste una forma più rara di spliceosoma che ha siti di riconoscimento diversi:
Spliceosoma AT-AC
(normale GT-AG)
Il meccanismo di base è analogo, ma le proteine sono in parte distinte

Spesso gli esoni codificano domini strutturali con funzioni distinte. (Es: DNA-binding e dimerizzazione)

Gli esoni: ruolo evolutivo• Molti geni si sono evoluti
duplicando egli esoni
• Esoni simili si possono trovare in proteine molto diverse

Esempio: enzimi che modificano la cromatina
Y= lievito, W= verme, F= mosca, H= uomo

RNA editingRappresenta un altro modo
per modificare la sequenza di un mRNA – deamminazione sito-
specifica (CU o A Inosina)
– Inserzione o delezione di U diretta da RNA guida

Esempio di deamminazione sito-specifica
Gene dell’apolipoproteina-B umana.
La deamminazione, introduce uno stop codon, e quindi una proteina troncata

Editing con inserzione di U, mediato da RNA guida
Forma trovata nel mitocondrio di tripanosoma
Vengono aggiunte delle U, modificando il frame di lettura.
I RNA guida (gRNA) hanno un’ancora di attacco al 5’, la regione di editing ed un tratto poli-U al 3’.

Meccanismo
Il gRNA si attacca con l’ancora
Induce la formazione di anse sul mRNA da modificare
Taglio endonucleasico
Inserimenti di U da parte di uridil-transferasi 3’ terminale (TUTasi)
Poi la Ligasi.
Il tratto PoliU potrebbe aumentare la complementarietà dell’attacco.
Lo stesso gRNA può modificare siti diversi

Il trasporto del mRNA
mRNA maturo (con capping, splicing, PoliA e proteine aggiunte) viene rilasciato dal nucleo con un meccanismo regolato
Attrevarso il poro nucleare, che usa la GTPasi Ran.