LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino...
Transcript of LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino...
Amnios
epiblasto
ipoblasto Entoderma del
sacco vitellino
POST
ANT
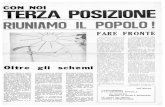
La comparsa della
linea primitiva al 15°
giorno indica l’inizio della gastrulazione
LA TERZA SETTIMANA
• Movimenti cellulari (frecce) nell’epiblasto prima (A) e dopo (B) la comparsa della linea primitiva.
• Estesi movimenti simmetrici e bilaterali di cellule verso il bordo
posteriore del disco, dove origina la linea primitiva, si combinano con
movimenti in direzione cefalica lungo la linea mediana. Cause e
meccanismi restano ancora sconosciuti.
LA TERZA SETTIMANA
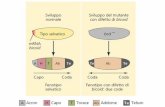
a) Formazione della linea
primitiva e del nodo di
Hensen (14°-15° g)
c) Formazione del
mesoderma (16° g)
b) Formazione
dell’endoderma (15° g)
I movimenti
delle cellule
dell’epiblasto durante la
gastrulazione
dei mammiferi
Ant.
Post. LA TERZA SETTIMANA
Transizione
epitelio-
mesenchimale
(EMT)
I movimenti delle cellule dell’epiblasto comportano cambiamenti di forma, proliferazioni, migrazioni e invaginazioni.
LA TERZA SETTIMANA
• EMT: le cellule epiteliali cambiano forma:
cellule epiteliali a fiasco aspetto stellato delle cellule mesenchimali (sono staminali pluripotenti) migranti (modifiche in: adesione, caderine, citoscheletro).
• Al termine della EMT, le cellule mesenchimali possono assumere di nuovo un aspetto epiteliale (transizione mesenchimale-epiteliale, MET)
• EMT coinvolta in: organogenesi, sviluppo tumori
LA TERZA SETTIMANA
Regolazione molecolare della EMT
• I segnali molecolari responsabili della induzione
di EMT e, quindi, della formazione di endoderma
e mesoderma, verrebbero innescati da molecole
appartenenti alla superfamiglia del transforming
growth factor-beta (TGF-beta). Altri segnali
induttivi (quali quelli del fibroblast growth
factor o FGF) sono coinvolti nella organizzazione
e nel mantenimento dell’endoderma più che nella sua induzione.
Segnali molecolari regolano la
formazione della linea primitiva
• In cellule della zona posteriore dell’epiblasto che entrano a far parte della
linea primitiva stessa, si esprimono geni appartenenti alla famiglia del TGF-beta come nodal, Wnt e bone morphogenetic proteins (BMPs). Anche FGF, interessato alla formazione del mesoderma ed alla organizzazione dell’endoderma, collabora con nodal per la formazione della linea primitiva.
• Ma come mai la linea primitiva non si forma nella parte anteriore dell’epiblasto e resta confinata alla parte posteriore? Da studi eseguiti nel pollo, si è scoperto che la parte cefalica dell’ipoblasto esprime geni che antagonizzano i segnali nodal e Wnt necessari per il programma di sviluppo del mesoderma. Ad esempio, geni come Dickkopf (Dkk1, che antagonizza Wnt), Cerberus 1 homolog (Cer1, che antagonizza nodal, BMP-4 e Wnt), e LEFTY1 (un gene della superfamiglia dei TGF-beta che antagonizza nodal) rivestono identico ruolo inibitorio nel pollo come anche in mammiferi quali il topo. La soppressione della formazione del mesoderma nella regione cefalica dell’embrione spiegherebbe così la comparsa e lo sviluppo della linea primitiva nella sola regione posteriore, lasciando libera la regione anteriore di iniziare lo sviluppo della testa.
LO SVILUPPO
DELL’EMBRIONE DIPENDE ANCHE DAL microRNA
• Il microRNA è un ssRNA di circa 22-nucleotidi che si lega a molti mRNA silenziandone la traduzione. Un tempo ritenuto privo di funzioni, si scopre oggi in grado di regolare una delle fasi più delicate dello sviluppo dell’embrione. Lo afferma uno studio del Sanford Children’s Health Research Center pubblicato dalla rivista Genes and Development. Il microRNA serve per allocare le cellule embrionali nelle tre diverse linee di ectoderma, mesoderma ed endoderma. Per verificare l’influenza del microRna i ricercatori ne hanno studiato circa 900 tipi contenuti nel genoma umano. Dai vari test è emerso che due famiglie di microRNA bloccano la formazione dell’endoderma favorendo invece la formazione delle altre due linee cellulari.
• Per approfondimenti
• paper
miR control of germ layer segregation in vertebrate embryos. let-7 and miR-18 family members repress Acvr1b and Smad2 protein production, rendering cells less sensitive to
Nodal signaling and sharpening a border between endoderm versus ectoderm and mesoderm.
©2012 by Cold Spring Harbor Laboratory Press
Colas A R et al. Genes Dev. 2012;26:2567-2579 November 14, 2012
LA TERZA SETTI MANA
ANT
POST
ANT
con solco
primitivo
Sacco
vitellino
Cavità amniotica
Peduncolo di
connessione
16° giorno:
compaiono
-membrana
faringea e
membrana
cloacale, dove
non c’è mesoderma
interposto
17° giorno:
-allantoide
(induce la
formazione di
arterie e vene
ombelicali)
Le frecce in (a) indicano la direzione di
migrazione delle cellule del mesoderma.
(b) mostra la formazione del processo cefalico.
Membrana
faringea
Membrana
cloacale Allantoide
POST
Processo
cefalico
LA TERZA
SETTIM..
17° giorno:
1. le cellule che si
invaginano attraverso il
nodo di Hensen formano un
cordone (processo cefalico
o notocordale);
2. le cellule che si
invaginano lungo la linea
primitiva si espandono in
tutte le direzioni.
19° giorno
formazione dell’area cardiogena;
22° giorno
setto trasverso.
17 giorno
pro
c.
noto
c.
16° giorno: compaiono
-membrane faringea e cloacale, dove non c’è mesoderma interposto
17° giorno:
-allantoide (emopoiesi, arterie e vene ombelicali)
LA TERZA
SETTI……NA
GAST-high.mov
Setto
trasverso
Membrana
faringea
Membrana
cloacale
Area
cardiogena
LA TERZA
SETTIMANA
Sviluppo e regressione della linea primitiva
• Durante la 3^ settimana l’embrione si allunga (soprattutto l’estremità cefalica). L’invaginazione attraverso la linea primitiva continua fino alla 4^ settimana. Al 17° giorno la linea primitiva è lunga circa il 50% del disco embrionale; alla 4^ settimana sarà solo il 15%. Linea e nodo primitivi scompaiono alla fine della 4^ settimana (26° g).
• Residui eventuali portano a tumori sacro-coccigei comprendenti strutture ossee, nervose, peli, denti, ecc.
50%
15%
LA TERZA SETTIMANA
+ • Teratoma (tumore con tessuti differenziati) sacro-coccigeo (1 su 35.000 nati)
• 3 volte più frequente nelle femmine
• Può diventare maligno già nell’infanzia;
• Soluzione: chirurgica.
LA TERZA
SETTIMANA
Destino delle membrane
bucco-faringea e cloacale
1. La m. bucco-faringea si aprirà alla 4^
settimana (apertura della cavità orale)
2. La m. cloacale si dividerà alla 7^
settimana in una membrana urogenitale
e in una membrana anale. L’apertura verso l’esterno del tratto urogenitale e del canale anale si avrà solo con la
perforazione di tali membrane alla fine
del secondo mese.
1
2
17° g
18° g
19° g
Stadio di placca
cordale
Stadio di corda dorsale
o notocorda
Sacco vitellino
Stadio di canale cordale
I 3 stadi di trasformazione del processo cefalico in notocorda
• Il passaggio
dallo stadio di
placca cordale a
quello di corda
dorsale inizia
all’estremità cefalica e si
estende poi in
senso cranio-
caudale
Veduta schematica, in sezioni trasversali, di
un embrione durante la gastrulazione
1
2
3
4
1. Sezione
a livello di
corda
dorsale
2. Sezione
a livello di
placca
cordale
3. Sezione a
livello del nodo
di Hensen
4. Sezione a
livello della linea
primitiva
Destino della notocorda (tessuto cordoide)…
Allora, qual è la sua funzione?
…residua solo come nucleo polposo
dei dischi intervertebrali
LA TERZA SETTIMANA
La notocorda induce la formazione
del neuroectoderma
(sviluppo del sistema nervoso)
C’è un parallelismo tra l’evoluzione della notocorda e della placca
neurale
Neurulazione
(a) stadio di placca
neurale (17° g)
(b) stadio di
doccia neurale
(19° g)
(c) stadio di
tubo neurale
(21° g)
I 3 stadi di induzione
dell’ectoderma neurale
Pieghe
neurali
Chiusura
del tubo:
inizia dalla
regione
cervicale
Fotografia delle pieghe che trasformano la placca neurale prima
in doccia e poi in tubo neurale
LA TERZA SETTIMANA
Cellule delle creste neurali
Le cellule delle creste neurali
subiscono una transizione
epitelio-mesenchimale (EMT)
e migrano in
varie direzioni del corpo per
formare strutture molto diverse
(quasi un 4° foglietto
embrionale)
Come le cellule si assemblano per formare un tessuto
Alcune cellule del tubo neurale modificano le loro
proprietà di adesione e si distaccano dall’epitelio per
formare le creste neurali sulla superficie superiore del
tubo neurale. In seguito, le cellule migrano nell’embrione
e formano una varietà di tipi cellulari e di tessuti.
Gangli nel SNP. Nel ganglio,
altre cellule delle creste
neurali differenziano e
diventano cellule di sostegno
(satelliti) che circondano i
neuroni. Le cellule delle cr.
neurali migrano in gruppetti
e proliferano rapidamente
durante la migrazione.
Tratto da: Cell-Cell
Adhesion
LA TERZA SETTIM…
Lo sviluppo delle pieghe neurali. (a) Stadio di
placca neurale, a 17 giorni; (b) stadio di doccia
neurale, a 19 giorni; (c) stadio di tubo neurale, a
22 giorni; (d) stadio di tubo neurale, a 24 giorni.
17 gg Sviluppo
dell’ectoderma
neurale
19 gg 22 gg
24 gg
LA TERZA SETTIMANA
Il neuroporo
anteriore si
chiude, in
media, al giorno
24
Il neuroporo
posteriore si
chiude al giorno
26
Neuropori
anteriore e
posteriore.
Embrione umano
al giorno 25.
LA TERZA
SETTIMANA
Correlazioni cliniche
• Mancata chiusura del neuroporo posteriore: spina bifida o mielomeningocele (circa 1 feto su 1000). Il midollo spinale fuoriesce dalla colonna vertebrale lesioni neurologiche con perdita di funzionalità a carico degli arti inferiori, incontinenza urinaria e fecale. Una delle cause: deficit di acido folico in gravidanza
LA TERZA SETTIMANA
Correlazioni cliniche
• Mancata chiusura del neuroporo anteriore=anencefalia, con grave
deficit di sviluppo dell’encefalo e delle ossa del cranio. Colpisce (circa 1 feto su 1000); incompatibile con la vita post-natale.
La carenza di acido folico nella dieta dei padri nel periodo
precedente al concepimento può portare a gravi
malformazioni del nascituro, esattamente come accade per la
stessa carenza nella dieta della madre durante la gravidanza. Il
fenomeno è legato ad alterazioni nella capacità di espressione
dei geni sui cromosomi presenti negli spermatozoi
Riferimento bibliografico:
R. Lambrot et al.
Low paternal dietary folate alters the mouse sperm epigenome and is associated with negative pregnancy outcomes
Nature Communications 4, Article number: 2889 doi:10.1038/ncomms3889 Published 10 December 2013
Il parallelismo tra l’evoluzione della notocorda e della placca neurale si
spiega perché:
il cordo-mesoderma induce* l’ectoderma a differenziarsi in tessuto nervoso.
*Induzione=spinta verso il differenziamento
L’INDUZIONE DEL SISTEMA NERVOSO E’ REGIONALIZZATA
• Trapiantando pezzettini della regione cefalica
della notocorda in posizione caudale, vengono
indotte strutture cerebrali dove, invece, dovrebbe
formarsi midollo spinale e viceversa.
• Questo fa supporre che il cordomesoderma emetta
un agente neuralizzante anteriore ed uno
posteriore a differenti combinazioni lungo gli assi
embrionali.
Regolazione molecolare della
neurulazione nella regione anteriore
• Ectoderma neurale (circa 50% del totale) tess. nervoso
• Ectoderma non neurale (circa 50%) epidermide;
• L’ectoderma viene indotto in senso epidermico da proteine della famiglia delle BMP (bone morphogenetic proteins,
superfamiglia dei TGF-beta, come ad es.: BMP-4).
• Dall’ectoderma possono formarsi strutture neurali solo se viene bloccata l’azione di BMP-4.
Regolazione molecolare della
neurulazione nella regione anteriore
• Ad es., durante la induzione neurale del prosencefalo e mesencefalo, sia il nodo di Hensen che il mesoderma notocordale producono molecole come chordin, noggin e follistatina che inibiscono l’attività di BMP-4.
• In particolare, chordin e noggin legano il BMP-4 impedendogli di riconoscere il recettore specifico mentre la follistatina formerebbe complessi di trimeri inattivi.
• Poiché BMP-4 non può agire, può aver via libera il programma di espressione di geni neurali specifici (come, ad esempio, N-CAM).
• La parte di ectoderma che non riceve segnali che bloccano BMP-4 è indotta a formare epidermide.
• FGF, acido retinoico e WNT-3a sono
responsabili dello sviluppo della regione
posteriore (rombencefalo e midollo spinale)
Regolazione molecolare della
neurulazione nella regione posteriore
Cellule delle creste neurali
• Sono indotte da segnali al confine tra neuroectoderma in formazione ed ectoderma non neurale. BMP, WNT ed FGF prodotti dall’ectoderma non neurale e dal mesoderma sottostante sono i segnali induttori: le cellule delle creste neurali subiscono una transizione epitelio-mesenchimale (EMT) e migrano in
varie direzioni del corpo.
Fotografia al microscopio a scansione della notocorda e del tubo neurale. La
rete di fibrille che li circonda ha un ruolo importante nelle interazioni cellulari
e nelle migrazioni della cresta neurale
LA TERZA SETTIMANA
Sviluppo del mesoderma: suddivisione
in 5 aree organo-formative.
19° g
(a) Formazione
delle lamine
mesodermiche e
del processo
cefalico; (b)
ispessimento del
mesoderma
parassiale e
comparsa di cavità
intercellulari nel
mesoderma
laterale (frecce);
(c) formazione del
celoma embrionale
e separazione fra
mesoderma
somatico e
splancnico; (d)
completamento
della distinzione
fra 5 tipi di
mesoderma
(cordale,
parassiale,
intermedio,
somatico e
splancnico).
Fotografia del
mesoderma
parassiale e
del
mesoderma
intermedio
che si
formano ai
lati del tubo
neurale e
della
notocorda
(fine della 3^
settimana)
LA TERZA SETTIMANA
Fotografia al microscopio a scansione dei somiti che si formano ai
lati del tubo neurale durante la 4^ settimana
LA TERZA SETTIMANA
Suddivisioni del mesoderma alla fine
della 3^ settimana
• Si formano 5 aree organo-formative:
mesoderma cordale (dorsale)
parassiale
intermedio
somatico
splancnico
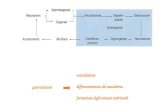
Qual è la causa di tutti questi
differenziamenti visti finora?
Alcune cellule dell’ipoblasto inducono le vicine cellule dell’epiblasto a diventare linea e nodo primitivi e a gastrulare. Si tratta della prima induzione che compare nell’embrione.
Quali molecole inducono in vivo
cellule dell’epiblasto a diventare linea primitiva e nodo di Hensen?
• Il transforming growth factor-beta
(TGFbeta) e il fibroblast growth factor
(FGF) sono le principali molecole induttrici.
Seconda serie di induzioni
• La notocorda viene suddivisa, da segnali (TGFbeta, FGF) provenienti dal nodo di Hensen, in regioni con diverse proprietà induttrici.
Terza serie di induzioni
• Segnali provenienti dalle regioni della notocorda inducono, a loro volta, l’ectoderma soprastante a formare parti diverse del sistema nervoso.
• Sui lati della notocorda, questi segnali inducono i diversi tipi di mesoderma.
Asimmetria sinistra-destra
(lateralizzazione)
• Le differenze tra parte destra e parte sinistra del corpo
sarebbero dovute ad un evento iniziale (symmetry breaking-
event)
• Una ipotesi suggerisce il ruolo delle monociglia (ciglio primario = 9+0 ) presenti su alcune cellule del nodo cefalico
La rotazione del ciglio avverrebbe in senso orario
dando luogo ad un gradiente (FLUSSO
NODALE) verso SX dei fattori (SHH = Sonic
Hedgehog e IHH=IndianHedgehog) responsabili
dell’induzione dell’espressione di Nodal
• a seguito di ciò Nodal prevale sul lato sinistro dell’embrione
• La maggiore espressione di Nodal nel mesoderma di sinistra si accompagna a maggiore
espressione di Lefty
• Ciò provoca a cascata l’espressione di PITX2 fattore che stabilisce la lateralità sinistra
Le isole sanguigne si
formano verso la metà della
3^ settimana di sviluppo (17-
18 gg) nel mesoderma
splancnico del sacco
vitellino.
Eritropoiesi
Gli emangioblasti periferici delle isole sanguigne diventano
angioblasti e formano la parete dei vasi vitellini. Le cellule più
interne diventano emoblasti, precursori degli eritroblasti
primitivi, poi eritrociti primitivi ed infine eritrociti definitivi,
senza nucleo. In seguito l’emopoiesi si sposta nel fegato, nella milza e nel midollo osseo.
emoblasti
Vasculogenesi
Il primo sistema vascolare si
forma alla fine della 3^
settimana.
Rete vascolare nel sacco vitellino, nel peduncolo
di connessione, nel corion, nell’embrione.
Gli angioblasti poi si
aggregano in vescicole dette
angiocisti. Queste si
dispongono in sequenze dette
cordoni angioblastici.
Vasculogenesi
E’ l’origine di vasi de novo.
Angiogenesi
Procede a partire da vasi
preesistenti
Apparato circolatorio primitivo (3^-4^
settimana)
Dal mesoderma
splancnico derivano sia
il sangue (dalle isole
sanguigne), che i vasi
sanguigni e gli abbozzi
del cuore (dagli
angioblasti).
Apparato circolatorio primitivo: cuore
tubulare e rete vascolare
-nel sacco vitellino,
-nel peduncolo di connessione,
-nel corion,
-nell’embrione.
Il primo sistema vascolare si
forma alla fine della 3^
settimana. Rete vascolare nel sacco vitellino, nel
peduncolo di connessione, nel corion,
nell’embrione.
Apparato
circolatorio
primitivo (3^-4^
settimana)
![Page 1: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/1.jpg)
![Page 2: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/2.jpg)
![Page 3: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/3.jpg)
![Page 4: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/4.jpg)
![Page 5: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/5.jpg)
![Page 6: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/6.jpg)
![Page 7: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/7.jpg)
![Page 8: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/8.jpg)
![Page 9: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/9.jpg)
![Page 10: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/10.jpg)
![Page 11: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/11.jpg)
![Page 12: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/12.jpg)
![Page 13: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/13.jpg)
![Page 14: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/14.jpg)
![Page 15: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/15.jpg)
![Page 16: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/16.jpg)
![Page 17: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/17.jpg)
![Page 18: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/18.jpg)
![Page 19: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/19.jpg)
![Page 20: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/20.jpg)
![Page 21: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/21.jpg)
![Page 22: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/22.jpg)
![Page 23: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/23.jpg)
![Page 24: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/24.jpg)
![Page 25: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/25.jpg)
![Page 26: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/26.jpg)
![Page 27: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/27.jpg)
![Page 28: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/28.jpg)
![Page 29: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/29.jpg)
![Page 30: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/30.jpg)
![Page 31: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/31.jpg)
![Page 32: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/32.jpg)
![Page 33: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/33.jpg)
![Page 34: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/34.jpg)
![Page 35: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/35.jpg)
![Page 36: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/36.jpg)
![Page 37: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/37.jpg)
![Page 38: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/38.jpg)
![Page 39: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/39.jpg)
![Page 40: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/40.jpg)
![Page 41: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/41.jpg)
![Page 42: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/42.jpg)
![Page 43: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/43.jpg)
![Page 44: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/44.jpg)
![Page 45: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/45.jpg)
![Page 46: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/46.jpg)
![Page 47: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/47.jpg)
![Page 48: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/48.jpg)
![Page 49: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/49.jpg)
![Page 50: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/50.jpg)
![Page 51: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/51.jpg)
![Page 52: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/52.jpg)
![Page 53: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/53.jpg)
![Page 54: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/54.jpg)
![Page 55: LA TERZA SETTIMANA - TERZA SETTIMANA.pdfAmnios epiblasto ipoblasto Entoderma del sacco vitellino POST ANT La comparsa della linea primitiva al 15 JLRUQRLQGLFDO L QL]LR della gastrulazione](https://reader030.fdocumenti.com/reader030/viewer/2022021913/5c695fa709d3f25c6a8cf716/html5/thumbnails/55.jpg)