La pompa sodio-potassio ed il potenziale di membrana a riposo 14-15... · La subunità alpha lega...
Transcript of La pompa sodio-potassio ed il potenziale di membrana a riposo 14-15... · La subunità alpha lega...
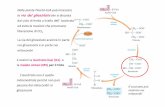
Le pompe ioniche, al contrario dei canali ionici, mobilizzano gli ioni attraverso la membrana plasmatica contro il loro gradiente elettrochimico, e quindi con un trasporto di tipo attivo effettuato grazie ad una continua spesa energetica.Le pompe ioniche sono molteplici, ma per il neurone la più importante fra queste è senza dubbio la pompa Na+/K+, detta anche ATPasi Na+/K+ -dipendente.
La pompa sodio-potassio
La notevole importanza di questa pompa è resa evidente dal fatto che il suo funzionamento richiede circa il 25% del fabbisogno totale di ATP cellulare dell’intero organismo in fabbisogno di riposo, e nei neuroni questa percentuale sale a circa il 70%.La funzione principale di tale pompa è il mantenimento dell’omeostasi cellulare attraverso la regolazione del bilancio osmotico e la costruzione del gradiente transmembrana degli ioni Na+.
La pompa sodio-potassio
La pompa sodio-potassio
Dal punto di vista strutturale la pompa Na+/K+ è composta da 2 sub-unità alpha e beta.La subunità alpha lega l’ATP, gli ioni Na+ e K+ e inoltre contiene i siti di fosforilazione che regolano il funzionamento della pompa stessa.La subunità beta è responsabile della localizzazione della pompa sulla membrana plasmatica e dell’attivazione dell’unità alpha.
La pompa sodio-potassio
Il funzionamento della pompa può essere schematizzato secondo un modello basato sull’acquisizione sequenziale di modificazioni conformazionali, ciascuna delle quali è conseguenza della precedente e causa della successiva.Queste modificazioni, indotte da una serie di fosforilazioni e defosforilazioni la pompa si apre in modo alterno verso l’interno e verso l’esterno per poi tornare alla configurazione iniziale, pronta per eseguire un nuovo ciclo di funzionamento.
Durante ciascun ciclo, la pompa estrude dall’interno della cellula 3 ioni Na+ e vi fa entrare 2 ioni K+, ricavando l’energia perentrambi i trasporti contro-gradiente, attraverso la degradazione di una molecola di ATP in ADP.
La pompa sodio-potassio
1) Nella configurazione iniziale aperta verso l’interno, la pompa lega 3 ioni Na+
2) Il legame con i 3 ioni, attiva la capacità enzimatica di legare 1 ATP ed autofosforilarsi rilasciando un ADP.
3) La condizione di fosforilazione, induce un cambiamento conformazionale che consiste nella chiusura della pompa sul versante intra-cellulare e la contemporanea apertura sul versante opposto. Allo stesso tempo i legami e l’affinità della pompa con gli ioni Na+ si riduce e questi vengono rilasciati all’esterno del citoplasma.
4) Il rilascio dei 3 ioni Na+, permette ai 2 ioni K+ di legarsi al versante esterno della pompa facendo si che il fosfato sul versante interno si stacchi sotto forma di fosfato inorganico (defosforilazione). Questo evento induce un secondo cambiamento conformazionale che chiude la pompa all’esterno ri-aprendola all’interno e rilasciando i due ioni K+.
La pompa sodio-potassio
Riassumendo: ad ogni ciclo la pompa, consumando 1 ATP, causa la fuoriuscita di 3 ioni Na+ ed immette 2 ioni K+.
Quindi, se consideriamo solo le cariche elettriche, il risultato complessivo si può riassumere nella perdita netta di una carica elettrica positiva nell’ambiente intra-cellulare OPPURE nell’aumento nel citoplasma di una carica elettrica negativa.
Per tale ragione, la pompa Na+/K+ è definita elettrogenica, cioè generatrice di una differenza di potenziale tra cariche elettriche intra- ed extra-cellulari. Tuttavia il contributo della pompa alla differenza di potenziale fra i due comportamenti è pari solo al 10%
Trasporto di membrana
Trasporto passivo Trasporto attivo Trasporto vescicolare
Diffusione semplice
Diffusione facilitata
Primario (ATP)Secondario (Gradiente
elettrochimico)
Endocitosi Esocitosi
UNIPORTO
Co-Trasporto
• Proteine Carrier (interazione diretta con il materiale di trasporto)
• Canali ionici• Regolati da voltaggio (alta
specificità Na+, K+, Ca2+, etc…)
• Recettori ionotropi• Nicotinici o
Pentamerici• Glutammato• cAMP e cGMP• Ca2+• Altre modalità di
attivazione
• Trasportatori ABC
• Proteine Carrier
Antiporto -Simporto
• Pompa Na+/K+
• Altre pompe ioniche
• Pompe protoniche
Antiporto -Simporto
• Recettori metabotropi legati ad attività enzimatica (ligandi = fattori di crescita/ormoni)
• Tirosin Chinasi• Istidina Chinasi• Serina/Treonina Chinasi
• Recettori metabotropi legati alla proteina G• Famiglia A, recettori per le monoamine (dopamina,
norepinefrina, epinefrina, serotonina) ed i neuropeptidi• Famiglia B, recettori per secretina, glucagone e calcitonina• Famiglia C, recettori per glutammato e per il Ca2+
RECETTORI METABOTROPINON MEDIANO IL TRASPORTO DIRETTAMENTE, SEBBENE FRA I RISULTATI DELLA TRASDUZIONE DEL
SEGNALE POSSA ESSERCI L’ATTIVAZIONE DI TRASPORTATORI DI MEMBRANA
UNIPORTO
Co-Trasporto
• Proteine Carrier (interazione diretta con il materiale di trasporto)
• Canali ionici• Regolati da voltaggio (alta
specificità Na+, K+, Ca2+, etc…)
• Recettori ionotropi• Nicotinici o
Pentamerici• Glutammato• cAMP e cGMP• Ca2+• Altre modalità di
attivazione
• Trasportatori ABC
• Proteine Carrier
Antiporto -Simporto
• Pompa Na+/K+
• Altre pompe ioniche
• Pompe protoniche
Antiporto -Simporto
• Recettori metabotropi legati ad attività enzimatica (ligandi = fattori di crescita/ormoni)
• Tirosin Chinasi• Istidina Chinasi• Serina/Treonina Chinasi
• Recettori metabotropi legati alla proteina G• Famiglia A, recettori per le monoamine (dopamina,
norepinefrina, epinefrina, serotonina) ed i neuropeptidi• Famiglia B, recettori per secretina, glucagone e calcitonina• Famiglia C, recettori per glutammato e per il Ca2+
RECETTORI METABOTROPINON MEDIANO IL TRASPORTO DIRETTAMENTE, SEBBENE FRA I RISULTATI DELLA TRASDUZIONE DEL
SEGNALE POSSA ESSERCI L’ATTIVAZIONE DI TRASPORTATORI DI MEMBRANA
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
+ + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + +
I neuroni sono in grado di sfruttare i gradienti di concentrazione e quindi le cariche elettrostatiche degli ioni a valle e amonte della loro membrana plasmatica per generare e trasmettere lungo la membrana stessa e tra cellule diverse gli stimoli nervosi
- - - - - - - - - -
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - -+ + + + + + + +
+ + + + + + + + + + + + + + + + + + + + + + + +
I neuroni sono in grado di sfruttare i gradienti di concentrazione e quindi le cariche elettrostatiche degli ioni a valle e amonte della loro membrana plasmatica per generare e trasmettere lungo la membrana stessa e tra cellule diverse gli stimoli nervosi
Cosa accade alla membrana quando è permeabile ad un solo ione?
Si raggiunge l’equilibrio elettrochimico:
La forza dovuta al gradiente di concentrazione eguaglia la forza
dovuta al gradiente elettrico.FLUSSO NETTO NULLO.
Due forze agiscono su una particella carica:
La FORZA DI DIFFUSIONE,generata dal gradiente di
concentrazione
La FORZA ELETTRICA,generata dal gradiente
elettrico
La concomitanza di queste due forze spinge il flusso ionico all’interno o all’esterno della cellula.
La natura delle cariche negative intracellulari corrisponde per la maggior parte ai gruppi fosfato elettronegativi delle principali macromolecole che compongono la cellula:
• Acidi nucleici• Proteine fosforilate• ATP• Nucleotidi mono-, di- e tri-fosfati
Tutte queste strutture conferiscono larga parte dell’elettronegatività stabile della cellula, in quanto per natura non possono abbandonare il citoplasma, essendo associate a costituenti strutturali ed obbligati.
Per tale ragione vengono definiti come anioni fissi (A-). In contrapposizione agli ioni liberi (Na+, K+, Cl-, Mg2+, Ca2+ etc…) che invece possono muoversi velocemente attraverso la membrana plasmatica qualora venga loro fornito un passaggio (canale ionico).
L’elettronegatività causata dagli anioni fissi all’interno della cellula, rende quest’ultimo fortemente attrattivo per i cationi liberi e fortemente repulsivo per gli anioni liberi
Potassio+
Gli ioni potassio rappresentano un buon esempio di equilibrio rispetto alle concentrazioni interne ed esterne della cellula (ioni che entrano = ioni che escono).Questo è possibile grazie all’azione sia della pompa Na+/K+ che fa entrare il potassio, sia della presenza di molteplici canali leak o resting per il potassio, perennemente aperti. che ne consentono l’uscita per diffusione facilitata secondo gradiente di concentrazione.
In altre parole si può definire la membrana plasmatica come altamente permeabile agli ioni K+.
Nonostante questo, la concentrazione del potassio è più alta all’interno della cellula perché la maggior parte degli ioni potassio rimane attratta dalla forte carica negativa dell’ambiente intracellulare. In altri termini, solo gli ioni K+ ineccesso sui cui la forza di attrazione elettrostatica operata dall’ambiente citoplasmatico non ha effetto, riescono ad uscire dalla cellula secondo gradiente.
Sodio+
Nel caso degli ioni Na+, la loro esclusione dall’ambiente intra-cellulare ad opera della pompa Na+/K+ non è controbilanciata dalla presenza di canali costantemente aperti, e l’unico sodio che riesce ad entrare lo fa grazie ad alcuni trasportatori di membrana che operano co-trasporto attivo secondario, utilizzando il gradiente di Na+ come forma di energia.
In altri termini, la membrana plasmatica è altamente impermeabile agli ioni Na+.
Il risultato di questa impermeabilità è la generazione di due diverse concentrazioni di Na+ altamente sbilanciate fra interno ed esterno (circa 10 volte).
Cloro-
Per quanto concerne gli ioni Cl-, le concentrazioni e quindi l’equilibrio relativo fra interno ed esterno è paragonabile alla situazione descritta per il K+, sebbene a valori invertiti.Infatti anche il Cl- può attraversare facilmente la membrana grazie alla presenza di canali resting sempre aperti.Tuttavia rispetto al K+, l’ingresso secondo gradiente è ostacolato dalla carica generale negativa dell’ambiente intracellulare.In condizioni normali questo ione si distribuisce quindi attorno alla membrana.
Come già visto, il calcio è un importante secondo messaggero cellulare (canali metabotropi) per tali ragioni la sua concentrazione all’interno della cellula è mantenuta molto bassa grazie all’azione di pompe per il Ca2+ che eliminano questi ioni appena la loro concentrazione sale oltre un determinato livello, così da poter utilizzare l’aumento di calcio come segnale per una serie di processi:
Calcio+
Gli ioni Mg2+, sono invece essenziali per numerosi fenomeni connessi con l’attività enzimatica e con il metabolismo degli acidi nucleici. Per esempio la presenza del Mg2+ è necessaria all’assemblaggio della sub-unità minore e maggiore dei ribosomi, nonché per l’attività dei vari enzimi ed è come già visto, implicata nell’attività dei recettori NMDA.
Magnesio+
Riassumendo:
• L’interazione degli ioni liberi più abbondanti (Na+, K+ e Cl-) con gli anioni fissi, contribuisce nel costituire un ambiente intracellulare più elettronegativo dell’ambiente extracellulare
• Mentre gli anioni fissi sono non diffusibili, la membrana è altamente permeabile al K+ e al Cl- che si trovano in condizioni pressoché di equilibrio, e scarsamente permeabile al Na+ facendo si che questo sia in un forte stato di disequilibrio elettrochimico, attivamente mantenuto grazie alla pompa Na+/K+.
• Un improvvisa apertura dei canali ionici per il Na+ può causare una immediata ed imponente alterazione delle distribuzioni trans-membrana degli ioni e quindi del bilancio complessivo extra- intra-cellulare.
L’elettrofisiologia intra-cellulare
Un campo di studio che nasce dalle ricerche di Young, Hodgkin& Huxley.
Si basa sull’idea che l’ambiente esterno ed interno della cellula siano due compartimenti distinti caratterizzati da un’elevata conduttività elettrica, separati da una membrana con una elevata resistenza elettrica.
E’ pertanto possibile misurare la differenza di potenziale elettrico (differenza di voltaggio) proprio come si fa nei circuiti elettrici, grazie al Voltmetro.
Volt = unità di misura della differenza di potenziale
Ampere = intensità della corrente elettrica
La misurazione del potenziale di membrana
Grazie alla tecnica del patch (regione cellulare contenuta nel diametro della micropipetta) clamp è possibile studiare ed analizzare il flusso di ioni attraverso pochi od addirittura un singolo canale ionico.
Tutte le cellule (non solo le cellule eccitabili) hanno un potenziale di riposo (resting): una carica elettrica attraverso la membrana plasmatica, con l’interno della cellula negativo rispetto all’esterno. Il valore del potenziale di riposo varia, ma nelle cellule eccitabili si aggira tra -90 e -70 mV.
La misurazione del potenziale di membrana
La misurazione del potenziale di membrana
R = costante dei Gas
T= temperatura in gradi Kelvin
F = costante di Faraday (96500 coulomb/grammo equivalente di carica)
Ln = logaritmo naturale
Pna, PK, PCl = permeabilità della membrana agli ioni in questione
[…] = concentrazioni interne ed esterne
L’equazione di Goldman
Consente di calcolare il valore del potenziale di membrana a riposo in funzione delle variabili che ne determinano il valore,quali la concentrazione e la resistenza della membrana.
ERT
zFx ln
[ ]
[X]
X
E
I
La relazione che esiste all’equilibrio tra gradiente chimico e gradiente elettrico fu stabilita dal chimico-fisico tedesco WalterNernst, grazie alla sua formula che consente di calcolare il potenziale di equilibrio del singolo ione, ovvero il valore delpotenziale di membrana nella condizione di massima permeabilità della membrana per quello ione
R= costante dei gas
T= temperatura assoluta (Kelvin)
z= valenza dello ione
F= costante di Faraday (96500 coulomb/grammo equivalente di carica)
[X]i = Concentrazione intracellulare dello ione X
[X]E= Concentrazione extracellulare dello ione X
La misurazione del potenziale di membrana
L’equazione di Nernst
Equilibrio elettrochimico
Equilibrio elettrochimico
Disequilibrio elettrochimico
Disequilibrio elettrochimico
La misurazione del potenziale di membrana
L’equazione di Nernst consente di calcolare il valore di equilibrio elettrochimico del singolo ione. Nel caso del neurone èpossibile osservare un forte disequilibrio a carico del Sodio e del Calcio.
In conclusione, la condizione di elettronegatività dell’ambienteintra-cellulare rispetto all’esterno ha importanti conseguenze perquanto concerne la distribuzione delle cariche elettriche negliimmediati dintorni dei due versanti della membrana plasmatica.
Tale condizione causa un addensamento di cariche elettrichepositive sulla facciata esterna della membrana e questoaddensamento richiama cariche elettriche negative all’interno.
Pertanto le due facce della membrana sono ricoperte di caricheopposte che si attraggono ma che non possono annullarsi per viadella separazione della membrana.
Se analizziamo la natura di queste cariche, appare chiaro che lecariche positive sulla faccia esterna non possano essere altro cheioni Na+, che dei tre ioni principali (Na, K e Cl) sono gli unici inforte disequilibrio elettrochimico ed una forte concentrazionenell’ambiente extra-cellulare.
Il potenziale a riposo
Il potenziale d’azione consiste in una brusca e transitoria modificazione del potenziale di membrana neuronale che può essere suddiviso in 3 fasi ben distinte fra loro:
• Fase di salita (forte depolarizzazione)• Fase di discesa (forte iperpolarizzazione)• Fase di recupero (lieve depolarizzazione)
Il potenziale d’azione è innescato dal raggiungimento da parte della membrana, del valore soglia (-55 mV) d’apertura dei canali voltaggio-dipendenti del Na+
Le fasi del potenziale d’azione
In aggiunta alle 3 fasi descritte in precedenza, Il potenziale è caratterizzato anche da due importanti parametri:
• Durata. Nella maggior parte dei casi, corrisponde a circa 4-6 msec e dipende in modo diretto dalle cinetiche di apertura e successiva obliterazione dei canali voltaggio dipendenti del Na+ e K+, e quindi dagli specifici sottotipi di canali (isoforme) espressi sulle membrane neuronali.
• Ampiezza. Corrisponde invece alla variazione del potenziale fra il picco di massima depolarizzazione ed il picco di massima iperpolarizzazione. Non dipende direttamente dai canali, ma dalla concentrazione degli ioni liberi presenti nell’ambiente intra- ed extra-cellulare.
La conseguenza di questo è che tutti i potenziali generati nello stesso neurone hanno sempre un’ampiezza simile e che per il neurone, l’unica alternativa possibile è l’emissione o la non-emissione di un potenziale d’azione (fenomeno tutto-o-nulla).
Durata e ampiezza del potenziale d’azione
Auto-rigenerazione del potenziale d’azione
Il potenziale d’azione si svolge in una regione specifica della regione di membrana, di estensione molto limitata, e pertanto rappresenta un fenomeno locale.
Tuttavia il potenziale d’azione influenza fortemente anche la distribuzione delle cariche elettriche nei suoi immediati dintorni generando un gradiente di depolarizzazione che porterà i canali voltaggio-dipendenti, negli immediati dintorni a raggiungere il loro valore soglia, consentendo la propagazione del potenziale.
Modulazione dello stimolo nervoso
Come detto, il potenziale d’azione è definito come un fenomeno tutto o nulla pertanto non è possibile modularne la sua intensità così come avviene ad esempio con il volume della nostra voce.
Si pone a questo punto il problema di come i neuroni possano modulare l’intensità degli stimoli nervosi.
La soluzione adottata è nella variazione della frequenza di emissione (treni di potenziali)
Le giunzioni sinaptiche chimiche hanno il compito di trasformare l’informazione elettrica in informazione chimica e sono composte da:
Le sinapsi
Giunzione pre-sinaptica
Spazio inter-sinaptico
Giunzione post-sinaptica
I neurotrasmettitori
Sono molecole che mediano la trasmissione uni-direzionale dello stimolo nervoso a livello delle sinapsi chimiche.
Vengono convenzionalmente divisi in:
• Neurotrasmettitori classici o amminici (piccole dimensioni, reazioni elettriche o metaboliche rapide)
• Neuropeptidi (grandi dimensioni, funzioni più complesse, dinamica lenta e continua)
I neuropeptidi, invece, vengono sintetizzati come parti di grosse molecole proteiche dai ribosomi del soma neuronale. Tali proteine sono subito trasportate all'interno del reticolo endoplasmatico e quindi all'interno dell'apparato del Golgi, dove avvengono due cambiamenti. Dapprima, la proteina da cui originerà il neuropeptide viene scissa enzimaticamente in frammenti più piccoli, alcuni dei quali costituiscono il neuropeptide come tale oppure un suo precursore; successivamente, l'apparato di Golgi impacchetta il neuropeptide in piccole vescicole che gemmano da esso. Grazie al flusso assonale le vescicole sono trasportate alle estremità delle terminazioni nervose, pronte per essere liberate nel terminale nervoso all'arrivo di un potenziale d'azione. In genere i neuropeptidi vengono liberati in quantità molto minori rispetto ai neurotrasmettitori a basso peso molecolare, ma ciò è compensato dal fatto che i neuropeptidi sono assai più potenti.
I neurotrasmettitori a basso peso molecolare vengono sintetizzati nel citosol della terminazione presinaptica e, successivamente, mediante trasporto attivo, sono assorbiti all'interno delle numerose vescicole presenti nel terminale sinaptico. Quando un segnale giunge al terminale sinaptico, poche vescicole alla volta liberano il loro neurotrasmettitore nella fessura sinaptica. Tale processo avviene in genere nell'arco di un millisecondo.Monoamine:
• Catecolamine (Dopamina, Epinefrina, Norepinefrina)• Indolamine (Melatonina, Serotonina)
L’acetilcolina ha come principale luogo di sintesi il nucleo del setto ed il nucleo basale (situati nel proencefalo basale)
Ha un ruolo fondamentale in
• memoria e apprendimento (Alzheimer)• Neurotrasmettitore muscolare
Recettori nicotinici (ionotropi) e muscarinici (metabotropi)
Monoamine:
La dopamina è presente in circa un milione di cellule nervose, la sua diffusione nel cervello può essere riassunta in due vie separate
• Via meso-striatale origine substantia nigra striato, i.e. caudato e putamen – Importante per il controllo motorio (Parkinson)
• Via meso-limbo-corticale origine mesencefalo amigdala, ippocampo, nucleus accumbens – reward, dipendenze e schizofrenia
Cinque recettori (D1, D2, D3, D4 e D5) tutti metabotropi
Monoamine:
I neuroni che rilasciano la noradrenalina o norepinefrina sono organizzati in tre agglomerati principali (tutti con origine nel tronco encefalico)
• Nel locus coeruleus (nel ponte)• Nel sistema segmentale laterale del mesencefalo• Nel gruppo midollare dorsale
Tutti questi gruppi proiettano a vaste aree del cervello inclusa la corteccia, sistema limbico, talamo ed il cervelletto. Per tale motivo questo neurotrasmettitore è responsabile della regolazione di una vastità di comportamenti (umore, arousal, comportamento sessuale)
I recettori sono tutti metabotropi.
Monoamine:
La serotonina è presente in sole 200.000 dei 100 miliardi, quasi tutte ad origine mesencefalica, principalmente nei nuclei del rafe
La serotonina è coinvolta nei processi di controllo degli stadi del sonno, umori, comportamente sessuale e numerose altre funzioni
Tutti i recettori sono metabotropici (tranne uno).I farmaci che regolano la maggiorparte delle funzioni mediate dalla serotonina, agiscono selettivamente su un sottotipo recettoriale.
Monoamine:
Neurotrasmettitori peptidici
Neurotrasmettitori composti da un singolo amminoacido
Glutammato
Aspartato
GABA
Glicina
Neurotrasmettitori composti da brevi catene peptidiche
1. Peptidi oppioidi od oppiacei (met-encefalina, leu-encefalina, B-endorfina e dinorfina)2. Peptidi presenti in intestino, midollo spinale e cervello (Sostanza P, colecistochinina, neurotensina, neuropeptide Y)3. Ormoni pituitari (es. ossitocina, vasopressina)
Il terminale pre-sinaptico
Colina-Acetil-Transferasi (ChAT)Acetilcolina = Colina + Gruppo acetato (AcetilCoA)
Trasportatore vescicolare Acetilcolina (VAChT) + pompa vescicolare a protoni
Aceticolina inserita nelle vescicole e pronta ad essere rilasciato in modo quantico nello spazio inter-sinaptico, dopo l’arrivo del Ca2+
Il terminale post-sinaptico
Il terminale post-sinaptico si contraddistingue per l’assenza delle vescicole, e per la presenza della membrana post-sinaptica, sulla quale sono posti i recettori ionotropi o metabotropi sensibili al neurotrasmettitore che trasformeranno l’impulso chimico nuovamente in un impulso elettrico.
Nello spazio sottostante la membrana post-sinaptica è presente la densità post-sinaptica, un aggregato di proteine, enzimi etc…
Quando il ligando apre i canali presenti sul versante post-sinaptico si genera il cosi detto potenziale post-sinaptico eccitatorio o inibitorio (PPSE, PPSI).
L’eliminazione del neurotrasmettitore dallo spazio inter-sinaptico
Il corretto funzionamento di una sinapsi chimica, si basa sulla relazione costante tra potenziali d’azione in arrivo e quantità di neurotrasmettitore rilasciato nello spazio intersinaptico. Ciò presuppone l’esistenza di meccanismi di smaltimento del neurotrasmettitore nello spazio inter-sinaptico. Tali meccanismi devono essere molto precisi perché è evidente che una eccessiva o una insufficiente rimozione di quest’ultimo causerebbe una ipo- o una iper-attivazione della sinapsi.
Questi meccanismi di rimozione sono di tre tipi:
• Degradazione enzimatica (degradato da enzimi posti sulla faccia esterna della membrana post-sinaptica, i.e. acetilcolinesterasi, COMT, sulfotransferasi; poi riportato nella membrana pre-sinaptica da appositi trasportatori)
• Ricaptazione retrograda (ricaptazione ad opera di uno specifico trasportatore retrogrado, i.e. DAT, NET, SERT. Una volta riportati nel bottone pre-sinaptico possono essere reinseriti nelle vescicole, oppure degradate da un altro enzima denominato monoamminossidasi - MAO)
• Diffusione extrasinaptica (meccanismo utilizzato per il GABA e per il Glutammato, consiste nella diffusione al di fuori dello spazio intersinaptico, e nella successiva ricaptazione a carico sia dei trasportatori retrogradi che degli astrociti)
Le sinapsi elettriche
Chiamate anche giunzioni gap, consentono il trasferimento veloce e bidirezionale delle informazioni nervose, connettendo due cellule come se fossero un’unica cellula, chiamata sincizio metabolico.
Principi di psico-farmacologia
Le droghe (farmaci e droghe) che agiscono sui neuroni, nella maggiorparte dei casi agiscono tramite interazione con un recettore.
Al contrario dei ligandi endogeni che possono interagire con tutte le tipologie di recettore loro dedicati, le sostanze esogene normalmente agiscono solo con una precisa tipologia di recettore (isoforma) e quindi sono in grado di esercitare la loro funziona solo nella zona cerebrale dove la specifica isoforma viene espressa.
Interazioni forti ed interazioni deboli a seconda del recettore
LIVELLO DI AFFINITA’
Tolleranza ai farmaci
Diminuzione dell’efficacia di un farmaco
Tolleranza metabolica
Gli organi responsabili del metabolismo (es. fegato) diventano più efficienti nell’eliminare una sostanza dal sangue, così che la concentrazione diventi molto bassa prima di poter fare effetto.
Tolleranza funzionale
• Up-regulation (antagonisti)
• Down-regulation (agonisti)
Antipsicotici / Neurolettici
Scoperti tramite l’utilizzo della cloropromazina(antistaminico)
Utili nel trattare i cosiddetti sintomi positivi (allucinazioni e deliri)
• Neurolettici tipici antagonisti selettivi dei recettori dopaminergici D2 Aloperidolo 100 volte più selettivo per D2 che per D1
• Neurolettici atipici meccanismi non dopaminergici ma serotoninergici (clozapina), più utili per i sintomi negativi (isolamento sociale, anedonia)
Antidepressivi
Trattamento del disturbo depressivo maggiore e affini
• Inibitori delle monoaminossidasi (MAOI) bloccano la degradazione delle monoammine da parte di MAO (tranilcipromina, isocarbossazide)
• Antidepressivi triciclici bloccano la ricaptazione di norepinefrina e serotonina, sono chiamati così per via della loro struttura chimica a tre anelli (imipramina)
• Inibitori selettivi della ricaptazione della serotonina (SSRI) fluoxetina, sertralina e citalopram; privi degli effetti collaterali tipici dei triciclici, ma occorre più tempo per rilevare effetti significativi
Ansiolitici / tranquillanti
Attacchi di panico, fobie, ansia generalizzata vengono di norma trattati con una classe di farmaci chiamate depressivi (inibiscono attività generalizzata del SNC). Tutti questi farmaci agiscono sul recettore GABA-A
• Benzodiazepine
• Oppiacei
• Barbiturici
• Alcool
Grigio periacuqeduttale
Eroina
Potenti analgesici (antalgici) che creano dipendenza, legandosi a specifici recettori chiamati recettori oppioidi (orfani)
Oppiacei
Cannabinoidi
Derivati ottenuti dalla cannabis sativa (marijuana, hashish) che normalmente vengono assimilati tramite il fumo. Il loro principio attivo è il tetraidrocannabinolo (THC).
Come per gli oppiacei, nel nostro cervello vi sono recettori orfani per i cannabinoidi, concentrati nella substantia nigra, ippocampo, cervelletto e corteccia.
Vi sono due tipologie di recettori cannabinoidi (Entrambi metabotropici)
• CB1 (l’unico espresso nel sistema nervoso)
• CB2 (sistema immunitario)
La scoperta dei recettori ha portato alla ricerca degli endocannabinoidi, fra i quali il più studiato è l’anandamide(ananda=felicità in sanscrito)
Stimolanti
Il livello di attività del SNC è ottenuto tramite il bilanciamento di attivazione ed inibizione. Gli stimolanti spostano l’equilibrio verso l’eccitazione tramite due modalità:
1. Aumentano direttamente il numero di PPSE• Nicotina• Cocaina• Anfetamina• Allucinogeni e droghe dissociative
2. Bloccando i processi inibitori• Caffeina
Nicotina
Il tabacco ha origine americane da dove fu importato dai primi conquistatori.Divenne particolarmente diffuso con la trasposizione da pipa a sigaretta.Attraverso l’ampia superficie polmonare la nicotina entra nel circolo sanguigno, attraverso il quale:
• Aumenta battito cardiaco• Aumento pressione sanguigna• Secrezione acido cloridrico nello stomaco/peristalsi• Nel cervello interagisce con i neuroni dell’area
tegmentale ventrale (reward/dipendenza)
Interagisce con i recettori nicotinici (in particolar modo tutti quelli posti nel SNA)
Cocaina
Si ricava dalle foglie di Erythroxylon coca, una pianta tropicale.Se usata sottoforma di foglia per infusione/masticazione aumenta la resistenza, contrasta il senso di fame ed induce un senso di benessere, senza o con limitati effetti collaterali.Al contrario, l’estratto sinteticamente purificato è un alcaloide che venne inizialmente usato per scopi commerciali (coca-cola), antidepressivo ed anestetico locale (stesso principio attivo della Novocaina).Successivamente alla scoperta delle forti capacità psico-attive divenne una sostanza d’abuso per inalazione, insieme successivamente alla sua versione da assumere tramite il fumo (crack).
La cocaina inibisce la ricaptazione delle monoammine, in particolar modo della dopamina
Anfetamina
L’anfetamina è una sostanza sintetica con una struttura molecolare molto simile a quella delle monoammine.
Dopamina
Anfetamina
Norepinefrina Epinefrina
Anfetamina
L’anfetamina è una sostanza sintetica con una struttura molecolare molto simile a quella delle monoammine.
Insieme alla sua versione ancora più potente (metanfetamina) esercitano la loro azione stimolante in due modi:
1. Bloccano la ricaptazione delle catecolammine2. Diventano bersaglio alternativo per gli enzimi
monoamminossidasi venendo così distrutte al posto del neurotrasmettitore che rimane disponibile per la sinapsi.
A breve termine aumentano attenzione, provocano euforia e consentono grossi sforzi senza periodo di riposo (quantità ma non qualità). A lungo termine inducono psicosi simili a schizofrenia paranoide. La tolleranza viene sviluppata molto rapidamente
Anfetamina
Un particolare derivato dell’anfetamina è la metilenediossimetanfetamina o MDMA (ecstasy) che agisce aumentando il rilascio di prolattina, dopamina e serotonina nel cervello, con la stimolazione dei suoi recettori 5HT2a
Questo causa una serie di sensazioni positive come euforia, benessere e fenomeni visivi con immagini variopinte.
Tuttavia anche una sola dose causa effetti persistenti sui neuroni serotoninergici con successivi sintomi psichiatrici (depressione e disturbi di memoria)
Allucinogeni e droghe dissociative
Negli 30-40 il farmacologo svizzero Albert Hofmann studiava alcuni composti di un fungo che cresce sul frumento (ergot) con la speranza di ricavarne nuovi farmaci.
Un giorno dopo aver ingerito accidentalmente una piccola dose della sostanza su cui lavorava:
“... affected by a remarkable restlessness, combined with a slight dizziness. At home I lay down and sank into a not unpleasant intoxicated[-]like condition, characterized by an extremely stimulated imagination. In a dreamlike state, with eyes closed (I found the daylight to be unpleasantly glaring), I perceived an uninterrupted stream of fantastic pictures, extraordinary shapes with intense, kaleidoscopic play of colors. After some two hours this condition faded away”
Allucinogeni e droghe dissociative
Hofmann scoprì una sostanza che anche in bassissime dosi (pochi milionesimi di grammo) era in grado di provocare i sintomi da lui esposti.
L’acido lisergico o LSD è un allucinogeno (in realtà distorce percezioni esistenti) con effetti simili alle sostanze che derivano dalla mescalina (peyote) e dalla psilocibina (funghi allucinogeni) che consistono principalmente in esperienze visive.
L’LSD ha una struttura simile alla serotonina e per tale motivo agisce sui recettori serotoninergici (principalmente quelli posti nella corteccia visiva)
Stimolanti
Il livello di attività del SNC è ottenuto tramite il bilanciamento di attivazione ed inibizione. Gli stimolanti spostano l’equilibrio verso l’eccitazione tramite due modalità:
1. Aumentano direttamente il numero di PPSE• Nicotina• Cocaina• Anfetamina• Allucinogeni e droghe dissociative
2. Bloccando i processi inibitori• Caffeina
Caffeina
Fa parte dei neuromodulatori la cui funzione è aumentare il rilascio di neurotrasmettitore o la risposta del recettore a quest’ultimo.
Nello specifico, la caffeina blocca l’effetto di un neurotrasmettitore endogeno (adenosina) entrando in competizione per l’accesso all’auto-recettore A2.
L’adenosina agisce normalmente sui terminali presinaptici per inibire il rilascio di catecolamine.
Quindi, bloccando l’adenosina si ottiene l’effetto inverso, ovvero il rilascio di catecolamine eccitazione, aumento dell’arousal e dello stato di allerta.