DESTINI METABOLICI DEL PIRUVATO -...
Transcript of DESTINI METABOLICI DEL PIRUVATO -...
Piruvato Glicolisi
Acetil-CoA
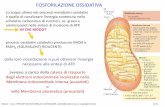
Metabolismo aerobico: il piruvato entra nel mitocondrio
Ciclo di Krebs
Piruvato Acetil-CoA
Complesso della Piruvato deidrogenasi (PDH)
Piruvato
La reazione produce oltre all’acetil-CoA anche un equivalente riducente di NADH che può essere indirizzato alla catena di trasporto di e- mitocondriale.
Partendo da 1 molecola di glucosio si ottengono 2 Acetil-CoA e 2 NADH
Catena di trasporto degli elettroni
Complesso della Piruvato deidrogenasi (PDH)
Complesso multienzimatico contenente copie multiple di 3 distinte attività
enzimatiche (E1 - E2 - E3)
E1 = piruvato deidrogenasi (24 subunità)E2 = diidrolipoammide acetiltransferasi (24 subunità)E3 = diidrolipoammide deidrogenasi (12 subunità)
Decarbossilazione ossidativa del
piruvato.È un processo irreversibile.
Piruvato
Idrossietil-
E1
Subunità E1 Contiene come cofattore la TPP. Catalizza la decarbossilazione del
piruvato e la formazione dell’intermedio idrossietil-TPP
Subunità E2 Contiene come cofattore la Lipoammide. La subunità E1 trasferisce il
gruppo idrossietilico dalla TPP sulla lipoammide della subunità E2: nel trasferimento l’idrossietile viene gruppo Acetilico e e ilponte disolfuro della lipoammide viene
ridotto. Si forma un legame tioestere ad alta energia.
Piruvato
Idrossietil-
E1
Lipoillisina ridotta
Acetil-CoA
E2
Lipoillisina ossidata
La subunità E2 catalizza, quindi, la transacetilazione del gruppo acetilico dalla Lipoammide al Coenzima A con conseguente formazione di Acetil-CoA. La
lipoammide rimane nella forma ridotta.
Piruvato
Idrossietil-
E1
E2
E3
Lipoillisina ossidata
Lipoillisina ridotta
Acetil-CoA
Subunità E3Contiene come cofattore il FAD.Catalizza l’ossidazione della lipoillisina (si riforma il ponte disolfuro) con riduzione del FAD a FADH2 il quale trasferirà poi 2 e- sul NAD+ con conseguente produzione finale di NADH.
alte concentrazioni di Acetil-CoA e NADH informano l’enzima che non è più necessario metabolizzare il
piruvato (le esigenze cellulari sono soddisfatte)
REGOLAZIONE DEL COMPLESSO DELLA PIRUVATO DEIDROGENASI
DISPONIBILITA’ DEL SUBSTRATOMODULAZIONE ALLOSTERICAMODIFICAZIONI COVALENTI (fosforilazione/defosforilazione)
reazione irreversibile
I prodotti della reazione funzionano da modulatori allosterici negativi:Acetil-CoA (sulla transacetilasi, E2)NADH (sulla diidrolipoil deidrogenasi, E3)
L’attività della PDH è connessa anche al metabolismo dei lipidi: una elevata degradazione dei lipidi che
incrementa il livello di Acetil-CoA rallenta la PDH e porta al risparmio di glucosio.
CICLO DI KREBS (o DELL’ACIDO CITRICO)
È un processo ossidativo che ha un ruolo centrale nel metabolismo energetico delle cellule eucariotiche. Avviene nella matrice mitocondriale.
È alimentato soprattutto dall’Acetil-CoA, metabolita chiave prodotto dal catabolismo ossidativo dei carboidrati, dei lipidi, di vari amminoacidi.
L’energia rilasciata dalle ossidazioni del ciclo di Krebs è conservata come potere riducente (NADH e FADH2) che alimenta la sintesi di
ATP mitocondriale.
Acetil-CoA
Ossalacetato
Citrato
Isocitrato
chetoglutarato
Succinil-CoA
Succinato
Fumarato
Malato
Ciclo dell’acido citrico
Per ogni molecola di Acetil-CoA che viene ossidata nel ciclo vengono prodotti: 3 NADH1 FADH2
1 GTP (ATP)
CITRATO Cis-ACONITATO
ISOCITRATO
ACONITASI ACONITASI
Isomerizzazione: il gruppo –OH viene spostato dal C-3 al C-2.
3
2
3
2
Nella cellula la reazione è spinta in avanti dal consumo di isocitrato nella reazione successiva.
È un metabolita del FLUOROACETATO
(Tossina usata come pesticida)
Reagisce con l’ossalacetato per formare FLUOROCITRATO
FLUOROACETIL-CoA:INIBITORE SUICIDA DELL’ACONITASI
Il fluoroacetil-CoA entra quindi nel ciclo di Krebs, inizia ad essere trasformato dalla citrato-sintasi ma quando entra nel sito attivo
dell’ACONITASI interagisce fortemente con essa inibendola in modo definitivo e bloccando quindi tutto il ciclo e la respirazione cellulare
H|
F — C — C|
H
O
O
- Na+
α-chetoglutarato
ISOCITRATO DEIDROGENASI
Isocitrato
Decarbossilazione ossidativa dell’isocitratoIl gruppo –OH in C-2 dell’isocitrato subisce un’ossidazione che porta alla
produzione di NADH (NADPH) e alla formazione di un α-chetoacido
:H- (ione idruro trasferito sul NAD+
H+ rilasciato dall’ossigeno
a) Isoenzima NAD-dipendente nella matrice mitocondriale.b) Isoenzima NADP-dipendente nel mitocondrio e nel citosol
(serve a generare NADPH).
CO2
α-chetoglutarato Succinil-CoA
Complesso dell’α-chetoglutarato deidrogenasi (TPP, Lipoammide,
FAD-dipendente).
Simile per struttura e funzione al complesso della piruvato deidrogenasi (sono utilizzati gli stessi
coenzimi e avviene la decarbossilazione ossidativa di un α-chetoacido)
Ossidazione dell’α-chetoglutarato: questa reazione porta alla formazione di un legame TIOESTERE ad alta energia e alla produzione di NADH
L’idrolisi del legame tioestere ad alta energia è accoppiata alla fosforilazione di un nucleoside-difosfato (GDP o ADP).
Si ottiene GTP o ATP. Le cellule animali hanno 2 isozimi, 1 specifico per l’ADP e 1 per il GDP.
Succinil-CoA sintetasi
Succinil-CoA Succinato
Legame tioestere ad alta energia
Un fosfato inorganico spiazza il CoAdalla molecola di succinil-CoA e si forma
un anidride mista: succinil-fosfato
Il gruppo fosfato viene ceduto ad un residuo di
His dell’enzima e si libera succinato
Il fosfo-enzima cede il gruppo fosfato al GDP e si forma GTP
GTP + ADP GDP + ATP
Nucleoside difosfato-chinasi
Il GTP scambia il gruppo fosfato con l’ADP per formare ATP
SUCCINATO DEIDROGENASI
SUCCINATO FUMARATO
Ossidazione del succinato a fumaratoCOMPLESSO II della catena di trasporto di e- mitocondriale
QQH2
Trasferisce gli e- al complesso III
FUMARATO Stato di transizione carbanionico
L-MALATO
FUMARASI
FUMARASI
Aggiunta STEREOSPECIFICA TRANS di acqua al doppio legame.
Quando il fumarato è nel sito attivo dell’enzima l’aggiunta della molecola d’acqua può avvenire
solo in una direzione.
Il ciclo di Krebs si conclude con un’ossidoriduzione che riforma l’ossalacetato e produce NADH
MALATODEIDROGENASI
L-MALATO OSSALACETATO
Nelle cellule la reazione è fortemente spinta in avanti perché l’ossalacetato è continuamente rimosso dalla citrato sintasi la quale mantiene bassa la concentrazione di ossalacetato nel mitocondrio.
BILANCIO ENERGETICO: Se partiamo dall’ossidazione di 1 molecola di glucosio possiamo ottenere energia sufficiente a sintetizzare 36 (o 38) molecole di ATP
glucosioGlicolisi 2 ATP + 2 NADH
sistema navetta malato/aspartato
2 NADH
sistema navetta diidrossiacetone-fosfato/glicerolo 3-fosfato
2 FADH2
2 piruvato → 2 Acetil-CoA(PDH) 2 NADH
TOTALE: 4 ATP 10 NADH >>>> ~ 30 ATP2 FADH2 >>>> ~ 4 ATP
~ 38 ATP
Ciclo di Krebs 6 NADH + 2 FADH2 + 2 GTP(ATP)
TOTALE: 4 ATP 8 NADH >>>> ~24 ATP4 FADH2 >>>> ~ 8 ATP
~ 36 ATP