Composti del carbonio idrocarburi alifaticiaromatici catena apertaciclici saturiinsaturi alcani C n...
-
Upload
umfredo-vacca -
Category
Documents
-
view
226 -
download
4
Transcript of Composti del carbonio idrocarburi alifaticiaromatici catena apertaciclici saturiinsaturi alcani C n...

Composti del carbonioidrocarburi
alifatici aromatici
catena aperta ciclici
saturi insaturi
alcani
CnH2n+2
alcheni alchini
CnH2n CnH2n-2 CnH2n CnH2n-2 CnH2n-6
saturi insaturi
cicloalcani cicloalcheni
serie benzenica
policiclici

Proprietà fisiche degli idrocarburi alifatici
Insolubili in acqua, solubili in etere, e altri solventi apolari
Dipendono dal numero di C, dal peso molecolare e dalle ramificazioni della catena:
• stato fisico (primi gas, poi liquidi, da C16 solidi)• punto ebollizione• punto di fusione• densità

alcani
C
H
H
H
C C CH
H
H
H
H
H
H
metano etano propanobutano
CnH2n+2
catena lineare
catena ramificata
CH4C2H6 C3H8
C4H10
C
H
H
C C C
H
H
H
H
H
H
H
C C CH
H
H
H
H
H
H
C
H
H C
H
HC C
C
H
H
H
HH H
H
C C CH
H
H
H
H
H
H
C
H
H
2 metil eptano 2,4 dimetil esanoC8H18
C8H18
Ibridazione sp3
4 legami tetraedro
C
H
C
H
C
H
H
H
H
H
H

Reazioni chimiche degli alcani• Sostituzione radicalica (formazione di
alogenuri alchilici che partecipano con le basi di Lewis alle reazioni di sostituzione nucleofila –SnN- per preparare i derivati degli alcani)
• Combustione (reazioni fortemente esotermiche)
• Cracking (reazioni endotermiche per stabilità del legame : rottura delle catene per ottenere alcani a breve catena –materia prima per le sintesi industriali- poi separati per distillazione frazionata)

alcheniCnH2n
legame doppio
Ibridazione sp2 3 legami a 120°
Legame orbitale p non ibridato
etene
più legami doppi
2: dieni
3: trieni
1 legame
1 legame
C C CH
H H
H
H
H
C C CH
H H
H
H
H
C
H
H
propene-1
C3H6
butene-2C4H8

Giulio Natta, Nobel 1963 per la sintesi del polipropene
Reazioni degli alcheni• Addizione al doppio legame
(il doppio legamereagente nucleofilo –base di Lewis- che partecipa con gli acidi di Lewis a reazioni di addizione elettrofila secondo la regola di Markovnikov)
• Polimerizzazione (isotattici o sindiotattici: con C* con stessa disposizione dei sostituenti o alternata: possono essere cristallizzati)
• Isomeria cis-trans (isomeri con diverse proprietà chimiche)
isotattico sindiotattico atattico

alchini CnH2n-2
legame triplo
Ibridazione sp Legami a 180°
Legami 2 orbitali p non ibridati
1 legame
2 legami Etino
oacetilene
C C CH
H
H
H
C C C
H
H
H
C
H
H
Hpropino Butino-2
C3H4 C4H6

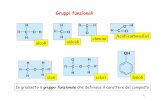
Derivati ossigenati degli idrocarburi
Acidi carbossiliciH
O HC
H
R
alcoliH
C
H
R O
aldeidi
CR R
O
chetoni
C
H
R OO
H
C
H
R O
H
R'C
H
eteri H
CR O
H
R'C
HO
esteri
R: indica il “resto” della molecola – radicale -
In grassetto il gruppo funzionale che definisce il carattere del composto
OH
fenoli

Derivati azotati degli idrocarburi
R NH
Hammine
R CN
H
H
O
ammidi
C NH
H
R
H
CO
OH
amminoacidi
CN
H
H
O
NH
H
urea
ammide prodotta dal fegato come catabolita degli amminoacidi;
materia prima per la sintesi di farmaci e macromolecole –resine-
••
molto basiche
neutre: per compensazione con O
monomeri delle proteineR 20 tipi diversi, ciascuno codificato da 1 o più triplette di nucleotidi

benzeneC6H6
Anello a 6 atomi di carbonio legati ciascuno a 1 atomo di idrogeno
legami
I 6 orbitali p –uno per ciascun atomo C- partecipano alla formazione di
3 legami
Gli elettroni in p sono delocalizzati
2 forme limite –mesomeri-
L’anello benzenico agisce come una base di Lewis

alcuni derivati del benzene
O H
fenolo
N HH
anilina(amminobenzene)
toluene
C HH
H
(metilbenzene)
C
H H
C H
stirene
O O HC
O HNO2 NO2
CH3
tritolo acido salicilico
.
radicale fenile
oacido fenico
con un elettronespaiato, reattivo

ARENI
antracene fenantrene
Gli anelli si definiscono
concatenati quando siano uniti per 1 atomo C ciascuno
condensati quando condividono atomi di C
difenilen
polifenile
naftalene
derivati policiclici del benzene