Un gruppo funzionale è una porzione della molecola ...
Transcript of Un gruppo funzionale è una porzione della molecola ...

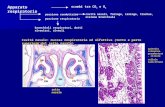
Gruppi funzionali in chimica bio-organicaUn gruppo funzionale è una porzione della molecola, costituita da un gruppo di atomi, che presenta un comportamentochimico caratteristico.
C C
COH
CO
CN
CSH
CS
C
CS C
S
CO
PO
O
O
CO
PO
O
OP
O
O
O
alchene(doppio legame)
arene(anello aromatico)
alcol
etere
ammina
tiolo
solfuro
disolfuro
fosfato
difosfato

CC
OP
O
O
O
aldeide
chetone
acido carbossilico
estere
tioestere
ammide
acilfosfato
CH
O
C
O
CC OH
O
CC O
O
C
CC S
O
C
OC
CC N
O
CC C
Nimmina(base di Shiff)
CO N
OCC
O O
OC C carbonato carbammato
Gruppi funzionali in chimica bio-organica

Gruppo Struttura a segmenti
suffisso o
gruppo funzionale
prefisso Struttura
Nome IUPAC
Radicali
HC
H
H
-ile ----
metile
Anioni
HC
H
H
-ide ----
metanide o metil anione
Cationi N
H
H
HH
-io es. -ammonio -fosfonio -ossonio -solfonio
ammonia- fosfonia- ossonia- sulfonia-
trimetilammonio
Zwitterioni N
H
H
CH2H
O
O
-io (per il catione) e -ide o -oato (per l’anione)
----
2-ammonio-N,N,N -trimetiletanoato
Acidi
R
O
OH
Acido alcanoico carbossi-
acido propanoico

Perossi acidi
R
O
O OH
acido perossialcanoico idroperossicarbonile
acido perossietanoico
Anidridi
R
O
O
O
R
anidride alcanoica -----
anidride alcanoica
Esteri
R
O
OR
alchil alcanoato alcossicarbonil-
carbalcossi-
etil etanoate o etanoato di etile
Alogenuri acilici
R
O
X
Alcanoil alogenuro aloalcanoil-
propanoil cloruro
Ammidi R
O
NR
R
-ammide carbammoil-
etanammide
Nitrili R C N
-nitrile -onitrile
alchil cianuro
ciano-
propanonitrile o etil cianuro

Aldeidi CR
O
H
-ale alcanoil-
-oxo-
propanale
Chetoni CR
O
R
-one
alchil alchil chetone
-oxo-
carbonile
propanone o dimetil chetone
Alcoli (e Fenoli) R O H
-olo
alcool alchilico
idrossi-
(fenossi-)
propanolo o alcol propilico
Tioli R S H -tiolo
alchil mercaptano
sulfanil-
mercapto-
propantiolo
Ammine NR
R
R
-ammina ammino-
-aza-
propanammina
Eteri R O R alchil alchil etere alcossi-
-ossa-
dimetil etere

Solfuri R S R alchil alchil solfuro
-alchiltio -alchilsulfanil-
-tia-
dimethyl sulfide
Perossidi O O
H
R
alchil idroperossido o alchil alchil perossico
idroperoddi-
alchilperossi-
methyl hydroperoxide or hydroperoxymethane
Alcheni
-ene alchenil-
propene
Alchini -ino alchinil-
propyne
Alogenuri R X alogenuro alchilico
bromo- cloro- fluoro- iodo-
bromopropano or propil bromuro
Nitro R N
O
O
----- nitro-
nitropropane

Alcani -ano -il
alchil
propano
Areni o
Aromatici
(la priorità dipende dal
gruppo funzionale presente
sull’anello)
H
H
H
H
H
H
benzene fenil
benzene

COH
CO
C CN
CSH
CS
C CS C
S
CO
PO
O
Oδ+δ−
δ+ δ+δ−
δ+δ−
δ+δ−
δ+ δ+ δ+ δ+δ+δ− δ− δ−
δ−
Polarizzazione dei legami dei gruppi funzionali
CC
OP
O
O
O
CH
O
C
OC
C OH
OC
C O
O
C
CC S
O
CC
OCC
C N
O
δ+ δ+ δ+ δ+
δ− δ− δ−
δ− δ−
δ−
CC O
O
CCOδ−
δ−
δ−
δ−
δ−
δ−
δ− δ−
δ−δ+ δ+δ+δ+δ+
anidride

Un acido è una sostanza in grado di donare un protone (ione idrogeno, H+ o H3O+) euna base è una sostanza in grado di accettare un protone.
Acidi e basi di Brønsted-Lowry
La forza di un acido HA in soluzione acquosa viene espressa dal pKa, ossia dal logaritmo negativo della sua costante di acidità Ka
HC
N
H H
HH
CC
H
H HO
O
H CC
H
H HO
O
HC
N
H H
HH
H+ +

Acidi e basi di Brønsted-Lowry
BH+ + H2O B + H3O+
[B] [H3O+]Ka =[BH+]
Ka × Kb = = [H3O+] [OH-] = Kw = 1.00 × 10-14
B + H2O BH+ + OH-
[BH+] [OH-]Kb =[B]
[B] [H3O+][BH+]
[BH+] [OH-][B]
da cui pKa + pKb = 14

Acido piùdebole
Acido piùforte
acido carbossilico
ione imidazolio
ione ammonio
tiolo
ione alchilammonio
β-cheto estere
acqua
alcol
chetone
tioestere
estere
CH3COHO
4.76
6.95
9.26
10.3
10.66
Gruppo Funzionale Esempio pKa
NN
HH
NH4+
CH3SH
CH3NH4+
CH3CCH2COCH3
O O
H2O
CH3OH
CH3CCH3
O
CH3CSCH3
O
CH3COCH3
O
16.00
19.3
21
25
15.75
10.6

base piùforteione idrossido
guanidina
ammina
ammoniaca
imidazolo
acqua
alcol
chetone
Gruppo Funzionale Esempio pKa di BH+
NN
HH
CH3NH2
OH- H2O
CH3OH
CH3CCH3
O
-1.74
-7.5
15.75
10.66
H2NCNHCH2CH3
NHH2NCNHCH2CH3
NH2
12.5
CH3NH3+
NH3NH4+ 9.26
NN
H 6.95
H2O
CH3OH2+
H3O+
-2.05
CH3CCH3
OHbase piùdebole

The Henderson–Hasselbalch Equation
• A compound will exist primarily in its acidic form at a pH < its pKa
• A compound will exist primarily in its basic form at a pH > its pKa
• A buffer solution maintains a nearly constant pH upon addition of small amount of acid or base
[ ][ ]−+=AHAlogpHp aK
The pH indicates the concentration of hydrogen ions (H+)

• When atoms are very different in size, the stronger acid will have its proton attached to the largest atom

• When atoms are similar in size, the stronger acid will have its proton attached to the more electronegative atom
• Inductive electron withdrawal increases the acidity of a conjugate acid

Acetic acid is more acidic than ethanol
CH3COHO
CH3CH2OH
pKa = 4.76 pKa = 15.9acetic acid ethanol
The delocalized electrons in acetic acid are shared by more than two atoms, thereby stabilizing the conjugated base
CH3CO-O
CH3CO-O

• acido di Lewis : acido che non dona protoni; accettaelettroni
• base di Lewis : donatore di una coppia di elettroni
Acidi e basi di Lewis


La basicità è una misura di quanto prontamente un atomodona la sua coppia di elettroni al protone ed è unaproprietà termodinamica.
La nucleofilicità è invece la misura di quanto prontamenteun atomo dona la coppia di elettroni ad atomi diversi daH+. E' una proprietà cinetica
CONFRONTO TRA NUCLEOFILICITÀ E BASICITÀ