Spettrometro a Reticolo - theremino.com · Reticolo di diffrazione : reticolo olografico 1000...
Transcript of Spettrometro a Reticolo - theremino.com · Reticolo di diffrazione : reticolo olografico 1000...
Sistema Theremino – Spettrometro_ITA – Pag. 1
Spettrometro
a Reticolo
Schemi costruttivi e Spettri acquisiti
Sistema Theremino
Sistema Theremino – Spettrometro_ITA – Pag. 2
Sommario
Componenti e Schemi costruttivi ...................................................................................................................... 6
Teoria del reticolo di diffrazione ................................................................................................................... 6
Dati dei reticoli utilizzati ................................................................................................................................ 8
Costruzione spettrometro portatile .................................................................................................................. 9
Costruzione spettrometro da tavolo ............................................................................................................... 10
Spettri di lampade ........................................................................................................................................... 11
Spettri di fiamma / plasma .............................................................................................................................. 14
Spettri di emissione / assorbimento atomico ................................................................................................. 15
Spettri di LED ................................................................................................................................................... 16
Spettri di Laser ................................................................................................................................................. 18
Spettro solare .................................................................................................................................................. 20
Legge di Wien / Black body radiation .......................................................................................................... 22
Confronto con spettri di riferimento ............................................................................................................... 23
Lampada CFL ................................................................................................................................................ 23
Lampada neon ............................................................................................................................................. 24
Lampada ai vapori di sodio .......................................................................................................................... 25
Spettrometria di assorbimento ....................................................................................................................... 26
Schema spettrometro di assorbimento ....................................................................................................... 26
Acqua ........................................................................................................................................................... 27
Vino Rosso ................................................................................................................................................... 27
Colorante Alimentare Blu ............................................................................................................................ 28
Colorante Alimentare Giallo ........................................................................................................................ 28
Inchiostro blu ............................................................................................................................................... 28
Spettrometria di fluorescenza ......................................................................................................................... 29
Schema spettrometro di fluorescenza ........................................................................................................ 29
Sorgenti di eccitazione della fluorescenza .................................................................................................. 30
Teoria della Fluorescenza ............................................................................................................................ 31
Analisi Spettrometrica di Pigmenti Organici.................................................................................................... 33
Clorofilla ...................................................................................................................................................... 33
Ficoeritrina................................................................................................................................................... 35
Antocianina come indicatore di pH ............................................................................................................. 36
Carotenoidi .................................................................................................................................................. 38
Betalaina ...................................................................................................................................................... 39
Sistema Theremino – Spettrometro_ITA – Pag. 3
Analisi Spettrometrica di coloranti fluorescenti .............................................................................................. 41
Stilbene – Triazina (Sbiancanti Ottici) .......................................................................................................... 41
Fluoresceina Sodica ..................................................................................................................................... 42
TetrabromoFluoresceina (eosina) ............................................................................................................... 43
Arancio di Acridina ...................................................................................................................................... 44
Rodamina B .................................................................................................................................................. 45
Rodamina 6G ............................................................................................................................................... 46
Verde Fluorescente ..................................................................................................................................... 47
Blu di Metilene ............................................................................................................................................ 48
Violetto di Genziana .................................................................................................................................... 49
Blu Metilene – Verde Malachite – Violetto genziana – Acriflavina (Miscela antifungina) .......................... 50
Ftalocianine ................................................................................................................................................. 51
Eritrosina ..................................................................................................................................................... 52
Cumarina ..................................................................................................................................................... 53
Analisi Spettrometrica di olii alimentari .......................................................................................................... 54
Olio d’Oliva Extra Vergine ............................................................................................................................ 54
Olio di Semi d’Arachide ............................................................................................................................... 55
Olio di Semi di Girasole ................................................................................................................................ 56
Olio di Semi di Mais ..................................................................................................................................... 56
Olio di Soia ................................................................................................................................................... 56
Olio di Mandorle .......................................................................................................................................... 57
Olio di Sesamo ............................................................................................................................................. 57
Olio di Ricino ................................................................................................................................................ 57
Analisi Spettrometrica di vitamine .................................................................................................................. 58
Cobalamina (Vitamina B12) ......................................................................................................................... 58
Riboflavina (Vitamina B2) e Piridossina (Vitamina B6) ................................................................................ 59
Retinolo (Vitamina A) .................................................................................................................................. 59
Analisi Spettrometrica di sostanze alimentari ................................................................................................. 60
Vino Bianco .................................................................................................................................................. 60
Aceto di Vino ............................................................................................................................................... 60
Isoflavoni (Salsa di Soia) .............................................................................................................................. 61
Estratto di noci verdi (Liquore Nocino) ....................................................................................................... 61
ProtoPorfirina (Guscio Uovo) ...................................................................................................................... 62
Miele ............................................................................................................................................................ 63
Sciroppo di rose ........................................................................................................................................... 64
Sistema Theremino – Spettrometro_ITA – Pag. 4
Estratto di Rabarbaro .................................................................................................................................. 64
Birra Chiara .................................................................................................................................................. 65
Birra Scura ................................................................................................................................................... 65
Birra Doppio Malto ...................................................................................................................................... 65
Estratto di Pistacchio ................................................................................................................................... 66
Te Verde ...................................................................................................................................................... 66
Analisi Spettrometrica di farmaci .................................................................................................................... 67
EmatoPorfirina (Farmaco Tonogen) ............................................................................................................ 67
Salicilato di Sodio ......................................................................................................................................... 68
Piroxicam ..................................................................................................................................................... 69
Analisi Spettrometrica di varie sostanze ......................................................................................................... 70
Piranina ........................................................................................................................................................ 70
Acqua di colonia .......................................................................................................................................... 70
Composto Sbiancante .................................................................................................................................. 70
Salicilato di Metile ....................................................................................................................................... 71
Chinino ......................................................................................................................................................... 71
Urina ............................................................................................................................................................ 72
Emoglobina .................................................................................................................................................. 73
Benzina ........................................................................................................................................................ 74
Antracene .................................................................................................................................................... 74
Tetracene (Naftacene) ................................................................................................................................. 75
Olio Lubrificante per Motore ....................................................................................................................... 75
Olio Essenziale di Bergamotto ..................................................................................................................... 76
Olio Essenziale di Camomilla ....................................................................................................................... 77
Olio Essenziale di Arancio ............................................................................................................................ 78
Acqua di Fiori d’Arancio ............................................................................................................................... 78
Olio Essenziale di Curcumina ....................................................................................................................... 79
Analisi Spettrometrica di sostanze inorganiche .............................................................................................. 80
Alluminato di stronzio attivato con Europio................................................................................................ 80
Vetro arricchito con Uranio ......................................................................................................................... 81
Bulbo lampada alogena ............................................................................................................................... 81
Spettroscopia Raman....................................................................................................................................... 82
Spettroscopia di Composti ChemioLuminescenti ............................................................................................ 83
Luce Chimica Blu .......................................................................................................................................... 84
Luce Chimica Verde ..................................................................................................................................... 84
Sistema Theremino – Spettrometro_ITA – Pag. 5
Luce Chimica Gialla ...................................................................................................................................... 84
Luce Chimica Rosa ....................................................................................................................................... 85
Luce Chimica Arancione .............................................................................................................................. 85
Luce Chimica Rossa ...................................................................................................................................... 85
Sistema Theremino – Spettrometro_ITA – Pag. 6
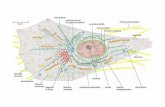
Componenti e Schemi costruttivi
Webcam : NEW TRUST MEGAPIXEL WEBCAM PRO 1.3MP 1024x1280
Reticolo di diffrazione : reticolo olografico 1000 linee/mm monoassiale – reticolo 600 linee/mm
monoassiale
Ottiche di collimazione
fessura 100micron su foglio di acetato / fessure da 0,1- 0,5mm - 1mm con lame affiancate / fessura
micrometrica regolabile manualmente
Spettrometro portatile assemblato
Teoria del reticolo di diffrazione
Un fascio luminoso monocromatico che incide su un reticolo dà origine ad un fascio trasmesso e a vari fasci diffratti, ad angoli che dipendono dal rapporto fra la distanza tra le righe del reticolo e la lunghezza d'onda della luce. Quindi, se il fascio luminoso è composto di più lunghezze d'onda si ottiene la scomposizione del fascio nelle sue componenti. La luce con una lunghezza d'onda più grande viene deviata ad un angolo più grande rispetto alla direzione incidente (angolo di diffrazione). Per ogni lunghezza d'onda si possono osservare più righe. Il numero di righe che si contano dalla riga centrale, che non risulta deviata rispetto al fascio incidente ed è presa come riferimento, è detto «ordine» o «modo» di diffrazione ed è spesso indicato con la lettera m . I reticoli a diffrazione possono agire sia per trasmissione, sia per riflessione della luce incidente a seconda che la dispersione della luce avvenga sullo stesso lato o dal lato opposto della sorgente luminosa. I reticoli in trasmissione sono composti da una lastra trasparente sulla quale vengono create tante piccole strisce che non consentono il passaggio della radiazione. In questo modo si ottengono molte fenditure la cui figura generata su uno schermo si risolve con un metodo analogo a quello impiegato per l'interferenza. I reticoli in riflessione sono costituiti da uno strato riflettente (specchio) sul quale vengono create tante piccole strisce o solchi che non consentono la riflessione della radiazione. Sono utilizzati nei monocromatori e negli spettrometri. La distanza tra le fenditure, detta "passo del reticolo", nei reticoli usati in spettroscopia è dello stesso ordine di grandezza della lunghezza d'onda della luce da analizzare. Nella pratica i reticoli sono solitamente caratterizzati dal numero di incisioni per unità di lunghezza, spesso espressa in linee per millimetro (l/mm).
Sistema Theremino – Spettrometro_ITA – Pag. 7
La proprietà fondamentale dei reticoli è che l'angolo di deviazione di tutti i fasci rifratti dipende dalla lunghezza d'onda della luce incidente. Quindi, un reticolo separa un fascio di luce policromatica nelle varie lunghezze d'onda che lo compongono, esso è uno strumento dispersivo. Ogni lunghezza d'onda in ingresso è deviata in una direzione diversa dalle altre: utilizzando della luce bianca si possono ottenere molte delle tonalità dell'iride. Il risultato visivo è simile a quello che si ottiene con un prisma, tuttavia questi due strumenti sfruttano metodi diversi per separare le diverse lunghezze d'onda. Quando un fascio di luce incide su un reticolo è diffratto in diversi fasci. Il fascio corrispondente alla trasmissione diretta è chiamato ordine zero di diffrazione. Ricordando la convenzione in uso denotiamo il fascio non deviato con m=0. Rispetto alla direzione individuata dal fascio di riferimento è possibile misurare l'angolo di diffrazione che caratterizza ogni fascio deviato. m può assumere valori positivi o negativi a seconda che il fascio deviato si trovi a destra o a sinistra del fascio di ordine zero (ciò dipende dalla convenzione utilizzata per il segno degli angoli). Indicando con d il passo del reticolo e con λ la lunghezza d'onda della radiazione incidente si può scrivere:
Quando il fascio incide con un angolo θi sul reticolo. Il segno presente nella formula dipende dalla scelta della convenzione sul segno degli angoli. Dalla relazione precedente si può notare che un fascio di luce policromatica viene suddiviso nelle sue componenti dal viola (che è il colore caratterizzato dalla lunghezza d'onda minore) al rosso; in un prisma di vetro invece l'angolo di deviazione è maggiore per il viola, quindi la successione dei colori è invertita.
Confronto degli spettri ottenuti da un reticolo per diffrazione (1), e da un prisma per rifrazione (2). Lunghezze d'onda più grandi (rosso) sono diffratte di più, mentre quelle più piccole (viola) sono difratte di meno.
La luce di una lampada vista attraverso un reticolo in trasmissione, che mostra tre ordini di diffrazione. L'ordine m = 0 corrisponde alla trasmissione diretta della luce attraverso il reticolo.
Nel primo ordine positivo (m = +1), i colori con lunghezze d'onda crescenti (dal viola al rosso) sono diffratti ad angoli crescenti. I raggi diffratti di colori diversi e corrispondenti a ordini consecutivi possono sovrapporsi, questo fenomeno diventa più probabile al crescere dell'ordine di diffrazione. Inoltre in un esperimento le linee di diffrazione osservate non sono mai infinitamente strette (come previsto dalla teoria), questo fenomeno è una conseguenza delle condizioni sperimentali non ideali e dell'effetto doppler termico. L'equazione del reticolo mostra che l'angolo di diffrazione dipende solo dal passo del reticolo e non dalla forma delle fenditure. L'efficienza del reticolo può anche dipendere dalla polarizzazione della luce incidente.
Sistema Theremino – Spettrometro_ITA – Pag. 8
Dati dei reticoli utilizzati
Tipo di
reticolo
Linee/mm Spazio
tra le
linee
(nm)
Deflessione per varie lunghezze d’onda
400nm 500nm 600nm 700nm 800nm 900nm
Reticolo
Paton
600 1600
14 18 22 26 30 34
Reticolo
olografico
1000 1000 24 30 37 44 53 64
Reticoli usati
Reticolo olografico da 1000 righe/mm e reticolo Paton olografico da 600 righe/mm
Schema costruttivo dello spettrometro portatile :
Schema costruttivo dello spettrometro da tavolo :
40o
Fenditura
Webcam
Reticolo
Fenditura
Webcam Reticolo
Collimatore
Obiettivo telecamera
Sistema Theremino – Spettrometro_ITA – Pag. 9
Costruzione spettrometro portatile
Particolare della webcam e del reticolo di diffrazione
Fenditura frontale da 0,1mm, fenditura da 0,5mm e fenditura da 1mm
schermo diffusore di plastica translucida
Webcam Reticolo
Sistema Theremino – Spettrometro_ITA – Pag. 10
Costruzione spettrometro da tavolo
Interno dello strumento con obiettivo collimatore, reticolo e webcam
Dettaglio della fenditura micrometrica e vista dello spettrometro assemblato
Lampada CFL per la taratura
Webcam Reticolo
Collimatore
Fenditura
Sistema Theremino – Spettrometro_ITA – Pag. 11
Spettri di lampade
CFL appena accesa – spettro discreto con righe allargate dalle sostanze fluorescenti – presenza emissione infrarossa (λ > 750nm)
CFL dopo il riscaldamento (dettaglio 400nm – 800nm) – emissione infrarossa assente
Righe Infrarosse
579nm 576nm 546nm 436nm
Sistema Theremino – Spettrometro_ITA – Pag. 12
Lampadina a incandescenza 25W – spettro continuo con picco ca 800nm
Lampadina alogena 70W – spettro continuo – maggiore emissione a λ minori (Temperatura maggiore)
Lampadina al gas neon a bassa pressione – spettro discreto con molte righe non allargate
Lampada di wood – emissione UV ca 370nm con piccola “coda” visibile oltre i 380nm
Sistema Theremino – Spettrometro_ITA – Pag. 13
Lampada ai vapori di sodio (lampione stradale) – evidente la riga d’assorbimento sdoppiata del sodio a 589nm – evidenti anche le righe a 568nm, 616nm, 514nm, 498nm tutte corrispondenti a righe di emissione dello spettro del sodio
Lampada allo Xenon Data l’estensione della emissione su di una ampia gamma di lunghezze d’onda, dai 350nm ai 950nm, questa lampada viene utilizzata in apparecchiature per misure di assorbimento e fuorescenza
Sistema Theremino – Spettrometro_ITA – Pag. 14
Spettri di fiamma / plasma
Candela – emissione concentrata su λ elevate
Plasma prodotto da arco elettrico HV (High Voltage) – notevole emissione di radiazione UV
Spettro di emissione dell’azoto atmosferico (da letteratura). Riispetto allo spettro del plasma vi è corrispondenza dei picchi di emissione a 400nm e 430nm. Si deduce che l’emissione luminosa del plasma da arco elettrico è principalmente dovuta alla emissione delle molecole di azoto.
Sistema Theremino – Spettrometro_ITA – Pag. 15
Spettri di emissione / assorbimento atomico
Nel primo spettro di plasma arco elettrico HV con cloruro di sodio si evidenzia la riga a 589nm del sodio. Nel dettaglio del secondo spettro viene mostrato come viene risolto il “doppietto” del sodio a 589,0nm e 589,6nm. Nel terzo e quarto spettro viene mostrato il dettaglio della linea di assorbimento del sodio in una lampada al sodio ad alta pressione
Spettro di fiammifero al clorato di potassio – si evidenziano le righe del doppietto del potassio a ca 770nm
Doppietto del Potassio
Doppietto del Sodio
Sistema Theremino – Spettrometro_ITA – Pag. 16
Spettro da arco HV con righe di emissione di sodio e potassio sovrapposte al continuo termico
Spettri di LED
LED infrarosso - ca 930nm
LED rosso
LED giallo
Emissione Sodio 590nm
Emissione Potassio 770 e 780nm
Sistema Theremino – Spettrometro_ITA – Pag. 17
LED verde
LED blu
LED viola – ca 400nm
LED bianco “luce fredda”
Sistema Theremino – Spettrometro_ITA – Pag. 18
Spettri di Laser
Diodo laser viola – ca 410nm
Diodo laser rosso – emissione 650nm
Diodo laser verde – dettaglio riga di emissione con due massimi ravvicinati a 532 e 530nm
Diodo laser verde – Sono visualizzate le righe spettrali corrispondenti alle emissioni di pompaggio
Sistema Theremino – Spettrometro_ITA – Pag. 19
Schema di funzionamento del diodo laser verde a 532nm. Vi è l’emissione del laser di pompaggio IR che
emette a ca 800nm. Questa emissione viene convertita dal cristallo Nd:YVO4 nella emissione a 1064nm
che, a sua volta, viene raddoppiata in frequenza, a 532nm, dal cristallo KTP.
Sistema Theremino – Spettrometro_ITA – Pag. 20
Spettro solare
Spettri di luce solare in momenti diversi
H2O Atm
O2 Atm
O2 Atm
Hα
Na
Mg Fe
Hγ Hβ
Sistema Theremino – Spettrometro_ITA – Pag. 21
Massimo ca 530nm => Si deduce T = 5500Ko (da black body radiation / legge di Wien) Si nota presenza di radiazione UV (<400nm) e IR (>750nm) Bande di assorbimento che si possono individuare nello spettro di luce solare
Banda assorbimento ossigeno atmosferico O2 ca 760nm – Fraunhofer A
Banda assorbimento del vapore acqueo atmosferico ca 720nm
Banda assorbimento ossigeno atmosferico O2 ca 684nm – Fraunhofer B
Assorbimento Hα ca 657nm (serie di Balmer nello spettro dell’idrogeno) Fraunhofer C
Assorbimento Hβ ca 480nm (serie di Balmer nello spettro dell’idrogeno) Fraunhofer F
Assorbimento Hγ ca 430nm (serie di Balmer nello spettro dell’idrogeno) Fraunhofer G
Riga di assorbimento del sodio a 589nm Fraunhofer D
Riga di assorbimento del ferro a ca 530nm Fraunhofer E
Riga di assorbimento del magnesio a ca 520nm Fraunhofer b
Spettro solare con indicazione delle principali linee di Fraunhofer
Spettro solare 650nm - 800nm con indicazione delle bande d’assorbimento dei gas atmosferici
Sistema Theremino – Spettrometro_ITA – Pag. 22
Legge di Wien / Black body radiation
In fisica la legge di Wien, detta anche legge dello spostamento di Wien, è una legge fisica sperimentale, scritta dal fisico tedesco Wilhelm Wien nel 1893, che consente di individuare per quale lunghezza d'onda è massima l'emissione radiativa di un corpo nero di massa generica posto ad una certa temperatura .
,
Spettro solare con indicazione delle
bande d’assorbimento atmosferico
Sistema Theremino – Spettrometro_ITA – Pag. 23
Confronto con spettri di riferimento
Lampada CFL
Numero del massimo λ teorica (nm) Elemento λ misurata (nm) 1 405.4 mercury 402 - 404
2 436.6 Mercury 437
3 487.7 terbium from Tb3+ 488
4 542.4 terbium from Tb3+ 542
5 546.5 Mercury 546
6 577.7 likely terbium from Tb3+ or mercury
576
7 580.2 mercury or terbium from Tb3+
579
8 584.0 possibly terbium from Tb3+ or europium in Eu+3:Y2O3
584
9 587.6 likely europium in Eu+3:Y2O3 587
10 593.4 likely europium in Eu+3:Y2O3 592
Sistema Theremino – Spettrometro_ITA – Pag. 24
11 599.7 likely europium in Eu+3:Y2O3 600
12 611.6 europium in Eu+3:Y2O3 612
13 625.7 likely terbium from Tb3+ 625
14 631.1 likely europium in Eu+3:Y2O3 630
15 650.8 likely europium in Eu+3:Y2O3 649
16 662.6 likely europium in Eu+3:Y2O3 661
17 687.7 likely europium in Eu+3:Y2O3 689
18 693.7 likely europium in Eu+3:Y2O3 693
19 707 and 709 likely europium in Eu+3:Y2O3 707 – 709
20 712.3 likely europium in Eu+3:Y2O3 712
21 760.0 likely argon
22 811.0 likely argon
Lampada neon
Lampada neon con spettrometro professionale. Corrispondenza di tutte le righe di emissione. Vengono visualizzate distintamente oltre 25 righe di emissione
Sistema Theremino – Spettrometro_ITA – Pag. 25
Lampada ai vapori di sodio
Lampada ai vapori di sodio – evidente la riga d’assorbimento sdoppiata del sodio a 589nm – evidenti anche le righe a 568, 616, 514, 498 e 467 tutte corrispondenti a righe di emissione del sodio
Sistema Theremino – Spettrometro_ITA – Pag. 26
Spettrometria di assorbimento
Gli spettri di assorbimento vengono ottenuti utilizzando una lampada alogena ed una lampada allo xenon con emissione il più possibile costante su di un ampio intervallo di lunghezze d’onda. Le variazioni nello spettro vengono compensate dal software che le linearizza su di un valore di intensità costante. L’intervallo utile va dai 370nm agli 1000nm.
Schema spettrometro di assorbimento
Vista costruttiva con la lampada alogena e la cella porta-campione
Lampada allo xenon
Spettrometro Lampada alogena /
xenon Campione
Cella porta-campione
Lampada
alogena
Sistema Theremino – Spettrometro_ITA – Pag. 27
Riferimento Linearizzato ottenuto con lampada alogena
Riferimento linearizzato da 400nm a ca 1000 nm
Riferimento Linearizzato ottenuto con lampada allo xenon
Riferimento linearizzato da 370nm a ca 700 nm
Acqua
Spettro assorbimento (in trasmissione) dell’acqua. Si nota come l’acqua assorba a partire dal vicino IR
Vino Rosso
Spettro assorbimento (in trasmissione) del vino rosso. Banda di assorbimento principale con λ inferiore a 550nm dovuta al contenuto di antociani
Assorbimento IR
Assorbimento
Antociani
Sistema Theremino – Spettrometro_ITA – Pag. 28
Colorante Alimentare Blu
Spettro assorbimento (in trasmissione) di colorante alimentare blu E131 (blu patentato V) E514 (solfato di sodio). Vengono filtrate tutte le λ eccetto quelle che vanno dai 420nm ai 500nm e superiori ai 700nm
Colorante Alimentare Giallo
Spettro assorbimento (in trasmissione) di colorante alimentare giallo E102 (tartrazina) E110 (giallo arancio S) E514 (solfato di sodio). Vengono filtrate tutte le λ eccetto quelle superiori ai 550nm
Inchiostro blu
Spettro assorbimento (in trasmissione) di inchiostro blu . Vengono filtrate le λ comprese tra 470nm e 700nm
Banda
Assorbimento
Banda
Assorbimento
Sistema Theremino – Spettrometro_ITA – Pag. 29
Spettrometria di fluorescenza
Schema spettrometro di fluorescenza
Schema costruttivo con i laser di eccitazione e la cella porta-campione
Esempio di fluorescenza di un campione (olio d’oliva) contenuto in cuvette ed eccitato da laser viola a 405nm.
Spettrometro Laser a 405nm Laser a 532nm Laser a 650nm lampada wood 370nm
Campione
Cella porta cuvette
Cella porta laser
Sistema Theremino – Spettrometro_ITA – Pag. 30
Sorgenti di eccitazione della fluorescenza
Laser viola
Potenza: 20mW Lunghezza d’onda: 405nm Corrente: <280mA @ 2.9 ~ 3V input Colore: blu violetto
Laser verde Potenza : 30mW Lunghezza d’onda: 532nm Tensione: 2.9 ~ 3V input Colore: verde
Laser rosso Potenza: 5mW Lunghezza d’onda: 650nm Tensione: 2.9 ~ 3V input Colore: rosso
Lampada di Wood Lunghezza d’onda : 370nm
Sistema Theremino – Spettrometro_ITA – Pag. 31
Teoria della Fluorescenza
A temperatura ambiente la maggior parte delle molecole occupa il livello vibrazionale più basso del livello elettronico di base (S0), l'assorbimento di luce porta a produrre stati eccitati della molecola. Il diagramma semplificato seguente mostra l'assorbimento di un fotone da parte della molecola al fine di produrre il primo stato eccitato S1.
L’eccitazione può portare la molecola a raggiungere qualsiasi sub-livello vibrazionale associato ad uno stato elettronico eccitato. Poiché l'energia viene assorbita come quanto, questo dovrebbe tradursi in una serie distinta di bande di assorbimento. Tuttavia, il semplice diagramma mostrato trascura i sub-livelli rotazionali associati a ciascun livello vibrazionale, sub-livelli che normalmente aumentano il numero di possibili bande di assorbimento a tal punto che diventa impossibile risolvere le singole transizioni. Per questo motivo, la maggior parte dei composti ha uno spettro di assorbimento piuttosto allargato, piuttosto che discreto. Avendo assorbito energia e raggiunto uno dei maggiori livelli
vibrazionali di uno stato eccitato, la molecola perde rapidamente il suo eccesso di energia vibrazionale grazie alle collisioni con il solvente e scende al livello vibrazionale più basso dello stato eccitato. Inoltre, quasi tutte le molecole che occupano uno stato elettronico superiore al secondo (Sn) subiscono conversione interna e passano dal livello vibrazionale più basso dello stato superiore ad un livello vibrazionale più elevato di uno stato eccitato inferiore avente la medesima energia. Da lì le molecole nuovamente perdono energia fino a raggiungere il livello vibrazionale più basso del primo stato eccitato (S1). Da questo livello, la molecola può ritornare ad uno qualsiasi dei livelli vibrazionali dello stato fondamentale, emettendo la sua energia sotto forma di fotone di fluorescenza. Se questo processo avviene per tutte le molecole che hanno assorbito luce, allora l' efficienza quantica della soluzione sarà massima, cioè efficienza 1. Se, invece, vengono seguite anche altre vie di diseccitazione, allora l' efficienza quantica sarà minore di uno e al limite nulla. La transizione che dal livello vibrazionale più basso nello stato elettronico fondamentale porta al livello vibrazionale più basso nel primo stato eccitato, la transizione 0-0, è comune ad entrambi i fenomeni di assorbimento e di emissione, mentre tutte le altre transizioni di assorbimento richiedono più energia rispetto qualsiasi transizione nella emissione di fluorescenza. Possiamo quindi aspettarci che lo spettro di emissione si sovrapponga parzialmente allo spettro di assorbimento in corrispondenza della lunghezza d'onda corrispondente alla transizione 0-0, mentre il resto dello spettro di emissione sia ad energia inferiore, o lunghezza d'onda maggiore. In pratica, le transizioni 0-0 negli spettri di assorbimento ed emissione di rado coincidono esattamente, la differenza rappresenta una piccola perdita di energia per interazione della molecola assorbente con le circostanti molecole di solvente. Questa differenza viene chiamata “stokes shift”. λem > λa λa e λem sono i picchi degli spettri di assorbimento ed emissione.
Esempio di “Stokes Shift” Spettri di assorbimento ed emissione di Arancio di Acridina. Si nota che la differenza tra i massimi è piuttosto contenuta : stokes shift = 537 – 525 = 12nm
λa 525nm
λem 537nm
Sistema Theremino – Spettrometro_ITA – Pag. 32
L'assorbimento di energia per produrre il primo stato eccitato perturba poco la forma della molecola e questo significa che la distribuzione dei livelli vibrazionali dei primi stati eccitati è molto simile a quella dello stato fondamentale. Le differenze di energia tra le bande dello spettro di emissione saranno simili a quelle nello spettro di assorbimento e spesso lo spettro di emissione sarà approssimativamente una immagine speculare dello spettro di assorbimento.
Esempio di spettri speculari Spettri di assorbimento ed emissione della ematoporfirina. Il primo picco di assorbimento e quello di emissione coincidono quasi perfettamente tra loro. La forma dei due spettri inoltre segue fedelmente la regola della immagine speculare. Poiché l'emissione della fluorescenza avviene sempre dal livello vibrazionale più basso del primo stato eccitato, la forma dello spettro di emissione è praticamente sempre la stessa, anche cambiando la lunghezza d'onda della radiazione di eccitazione. Questa è nota come la legge di Kasha.
Esempio di spettri di emissione eccitati da differenti lunghezze d’onda Spettri di emissione della fluoresceina. I massimi e la forma degli spettri coincidono nonostante le due differenti lunghezze d’onda di eccitazione. Nel secondo spettro sono visibili sia l’emissione anti-stokes (shift negativo) che l’emissione stokes (shift positivo). La regola di Kasha non si applica sempre, viene violata per numerose molecole semplici, un esempio è la molecola di azulene che emette fluorescenza dalla transizione S2-S0 invece che dalla solita transizione S1-S0. Per i dettagli si veda il paragrafo sull’olio essenziale di camomilla ricco di azulene. La fluorescenza è soprattutto influenzata dalla struttura della molecola. Per esempio le molecole rigide che presentano doppi legami coniugati, ben si adattano alla fluorescenza : in particolare le molecole dove ci sono strutture aromatiche, in cui il fenomeno della risonanza dei doppi legami è distribuito lungo tutta la struttura, quando eccitate danno luogo ad transizioni a π → π *, e quindi facilitano la fluorescenza.
Max Abs. 620nm
Max Em. 620nm Mirror Rule
UV exc. 532nm exc.
Sistema Theremino – Spettrometro_ITA – Pag. 33
Analisi Spettrometrica di Pigmenti Organici
Clorofilla
La clorofilla (di qualsiasi tipo) presenta colore verde-giallastro, come visibile da una semplice cromatografia su carta. Da un punto di vista fisico, questo vuol dire che la clorofilla assorbe tutto le lunghezze d'onda dello spettro visibile tranne quelle in prossimità dei 490-590 nm. Nel periodo autunnale la concentrazione di clorofilla nel fogliame diminuisce, quindi questo assume una colorazione bruno-rossiccia, che è data dalla presenza dei carotenoidi. La misurazione dello spettro di assorbimento (ovvero del colore) della clorofilla viene svolta con metodiche di spettrofotometria. La misura dell'assorbanza della luce è complicata dal solvente utilizzato
per estrarre la clorofilla dalla materia vegetale, il che influenza i risultati ottenuti; I picchi di assorbimento della clorofilla A sono a 665nm e 465nm. La clorofilla A diviene fluorescente a 673 nm. Il fatto che le clorofille A e B abbiano degli spettri di assorbimento differenti si traduce in un migliore assorbimento della radiazione solare per la fotosintesi clorofilliana. La soluzione alcolica di clorofilla posta in analisi è stata ricavata dalla macerazione delle foglie di spinaci in etanolo al 95%
Spettri di assorbimento (in trasmissione) di clorofilla disciolta in etanolo 95% Viene trasmessa la banda del verde dai 500 ai 600nm ca. Vi sono quindi due bande di assorbimento, una sul rosso ed una sul blu. Sul rosso i minimi tra 600nm e 700nm corrispondono ai picchi di assorbimento della clorofilla A e della clorofilla B. Anche l’andamento sulla banda del blu si spiega con la somma degli assorbimenti dei due tipi di clorofille.
Clorofilla A
Clorofilla B
Riferimento
Clorofilla B
Clorofilla A
Dettaglio
Sistema Theremino – Spettrometro_ITA – Pag. 34
I : Spettro di fluorescenza di Clorofilla eccitata da emissione laser a 405nm. Picco di emissione della Clorofilla A centrato a ca 670nm con spalla a ca 700nm e coda fino a 740nm. II : Spettro di fluorescenza eccitato da emissione laser a 532nm. Picco di emissione a ca 670nm della Clorofilla A. III : Spettro di fluorescenza eccitato da emissione laser a 650nm. Picco di emissione a ca 670nm della Clorofilla A
Eccitazione
Eccitazione
Eccitazione
Fluorescenza
Clorofilla A
Fluorescenza
Clorofilla A
Fluorescenza
Clorofilla A
Diffusione
Raman
I
II
III
Sistema Theremino – Spettrometro_ITA – Pag. 35
Ficoeritrina
La ficoeritrina è un pigmento rosso contenuto nei cromatofori delle alghe Rodoficee, che maschera i pigmenti normali dei cloroplasti (clorofilla e carotina) e che dà a tali piante la colorazione rossa più o meno intensa. Se le cellule di tali alghe muoiono, allora si mette in libertà la ficoeritrina, facilmente solubile in acqua, e le alghe prendono la colorazione verde, propria di tutte le piante autotrofe. La soluzione acquosa di ficoeritrina (un po' diversa di colorazione a seconda delle specie vegetali di provenienza) è intensamente rossa a luce trasmessa, mentre a luce riflessa mostra una fluorescenza spiccatamente giallo-aranciata. Dalla soluzione acquosa cristallizza facilmente; risulta di un gruppo pigmentato legato a un complesso proteico; la scissione avviene facilmente per azione degli acidi e delle basi. Il pigmento rosso sembra abbia parte importante per l'attività dei cloroplasti, rendendo possibile a questi l'utilizzazione di radiazioni luminose che di norma non sono utili per la fotosintesi, e permettendo così la vita delle alghe a una profondità dell'acqua, dove le radiazioni luminose arrivano solo parzialmente. La soluzione acquosa di ficoeritrina posta in analisi è stata ricavata dalla macerazione in acqua delle foglie della alga rodofita palmaria palmata.
La Ficoeritrobilina è il cromoforo contenuto nella ficoeritrina. E’ simile alla porfirina della clorofilla ma il gruppo tetrapirrolo è lineare e non chiuso in un anello con uno ione metallico al centro.
I : Spettro di fluorescenza eccitata da emissione laser a 405nm. Si individuano diverse bande di fluorescenza : attorno a 670nm dovuta alla clorofilla e attorno a 570nm per la ficoeritrina. La due bande a 475nm e 535nm sono presumibilmente dovute al contenuto in polifenoli e riboflavina II : Spettro di fluorescenza eccitato da emissione laser a 532nm. L’eccitazione a 532nm evidenzia il picco di emissione a 570nm del cromoforo della ficoeritrina
Fluorescenza
Clorofilla A
Fluorescenza
Ficoeritrina
Fluorescenza
Ficoeritrina
Fluorescenza
Polifenoli
Fluorescenza
Riboflavina
I
II
Sistema Theremino – Spettrometro_ITA – Pag. 36
Antocianina come indicatore di pH
Gli antociani (dal greco anthos = fiore, kyáneos = blu) o antocianine sono una classe di pigmenti idrosolubili appartenente alla famiglia dei flavonoidi. Le antocianine sono tra i più importanti gruppi di pigmenti presenti nei vegetali, e si ritrovano nei fiori e frutti così come negli arbusti e nelle foglie autunnali. Il colore delle antocianine può variare dal rosso al blu e dipende dal pH del mezzo in cui si trovano e dalla formazione di sali con metalli pesanti presenti in quei tessuti. Per esempio, la cianina costituisce il colore di alcune dalie e del fiordaliso. Le antocianine sono presenti, seppur con diverse
quantità, in quasi tutte le piante superiori (ma non nel cactus e in altre ancora). Si trovano specialmente nei frutti e nelle infiorescenze e si possono riscontrare anche su foglie e radici, molto spesso insieme ad altri pigmenti quali carotenoidi e flavonoidi. Le antocianine appartengono alla famiglia dei flavonoidi. Queste molecole sono costituite da una molecola di benzene fusa con una di pirano (anello eterociclico contenente ossigeno), collegata a sua volta con un gruppo fenilico che può essere a sua volta legato a diversi sostituenti. Questa molecola complessa prende il nome di catione flavilio (vedi figura) che è la struttura di base di tutte le antocianine. Le antocianine derivano dai rispettivi agliconi (antocianidine), da cui si differenziano per l'aggiunta di un gruppo glicosidico (uno zucchero), di norma in posizione R3 e/o R4 (vedi figura). In natura esistono circa una ventina di agliconi, mentre il numero dei derivati è fino a 15-20 volte maggiore. Tra i primi, più frequenti in natura vi sono: delfinidina, petunidina, cianidina, malvidina, peonidina e pelargonidina, i cui nomi derivano dalle piante che ne sono ricche. La soluzione alcolica di antocianina posta in analisi è stata ricavata dalla macerazione in etanolo 95% delle foglie di cavolo rosso ed anche dalla macerazione, sempre in etanolo, della carota viola. Spettro di fluorescenza della antocianina (estratto di carota viola) eccitata da emissione a 405nm
Risulta evidente una fluorescenza rossa che può essere attribuita alla antocianina e non alla clorofilla perché quest’ultima non è contenuta nella carota viola
Soluzione di antocianina in etanolo al 95% in ambiente neutro, al centro, in ambiente acido a sinistra ed in ambiente basico, a destra.
pH neutro pH basico pH acido
Sistema Theremino – Spettrometro_ITA – Pag. 37
Spettro riferimento
Spettro assorbimento (in trasmissione) degli antociani (succo cavolo rosso) in pH neutro
Spettro assorbimento (in trasmissione) degli antociani (succo cavolo rosso) in pH acido
Spettro assorbimento (in trasmissione) degli antociani (succo cavolo rosso) in pH basico
pH neutro
min 470nm
pH acido
min 500nm
pH basico
min 620nm
Riferimento
Sistema Theremino – Spettrometro_ITA – Pag. 38
Carotenoidi
I carotenoidi sono una classe di pigmenti organici che possono essere rinvenuti nelle piante o in altri organismi fotosintetici, come le alghe ed alcune specie di batteri. Esistono oltre 600 tipi di carotenoidi conosciuti;
vengono normalmente suddivisi in due classi: i caroteni (che sono idrocarburi quindi privi di ossigeno) e le xantofille (che invece lo contengono). Sono pigmenti accessori che nella fotosintesi consentono di assorbire lunghezze d'onda differenti rispetto alla clorofilla e che proteggono quest'ultima dalla foto ossidazione. I carotenoidi sono molecole costituite da una lunga catena di atomi di carbonio (costituita da 35-40 atomi e definita catena polienica), spesso terminante in un anello. La struttura della catena permette di dividere i carotenoidi in due classi:
le xantofille, costituite da catene contenenti atomi di ossigeno; appartengono a questa classe importanti pigmenti come la luteina e la zeaxantina.
i caroteni, costituiti invece da molecole prive di ossigeno e formate solo da idrogeno, oltre che da carbonio. Appartengono a questa classe il licopene ed il carotene, che è forse il più conosciuto di questi pigmenti e che dà il nome alla classe, contenuto nelle carote e responsabile del tipico colore arancione di questa radice.
Il tipico colore dei carotenoidi, che spazia dal giallo pallido all'arancione fino al rosso acceso, è una diretta conseguenza della struttura molecolare di questi composti. Le catene polimeriche che li compongono sono infatti caratterizzate dalla presenza di doppi legami, che interagiscono tra di loro permettendo agli elettroni degli atomi interessati di muoversi più liberamente; all'aumentare dei doppi legami nella catena, aumenta anche la libertà di movimento degli elettroni. Questo fa sì che lo spettro della luce assorbita da queste molecole diminuisca; come conseguenza di ciò, aumenta la lunghezza d'onda della luce riflessa, ed essa appare perciò di un colore tendente al rosso. La soluzione di β carotene posta in analisi è stata ricavata dal riscaldamento in olio di carote grattugiate.
Spettro di assorbimento del β carotene in olio : due picchi di assorbimento a 480nm e 450nm
Spettro di assorbimento del β carotene da letteratura
Assorbimento
β carotene
Sistema Theremino – Spettrometro_ITA – Pag. 39
Betalaina
Le Betalaine sono una classe di pigmenti rossi e gialli che si trovano nelle piante della categorie delle cariofille, dove sostituiscono i pigmenti antociani. Le betalaine si trovano anche in alcuni funghi di ordine superiore. Si trovano molto spesso nei petali di fiori, ma possono colorare frutti, foglie, gambi e radici delle piante che le contengono. Questa categoria include i pigmenti come quelli che si trovano nelle rape rosse. Il nome "betalaina" deriva dal nome latino della comune rapa (Beta vulgaris), dalla quale la betalaina è stata estratta la prima volta. L’intenso colore rosso delle rape, delle bouganville, dell’amaranto e del fico d’india è dovuto alla presenza dei pigmenti di betalaina. Le particolari tinte che vanno dal rosso al porpora sono distintive e differenti dai pigmenti
antociani che si trovano nella maggior parte delle piante. Ci sono due categorie di betalaine:
Betacianine : include i pigmenti rossi-viola. Tra le betacianine presenti nelle piante citiamo la betanina, isobetanina, probetanina e neobetanina.
Betaxantine : include I pigmenti che appaiono gialli-arancioni. Tra le betaxantine presenti nelle piante citiamo la vulgaxantina, miraxantina, portulaxantina, e indicaxantina.
Non vi è certezza sulla funzione delle betalaine presenti in alcune piante, vi è però qualche evidenza che possano avere proprietà antimicotiche ed antifungine. Le betalaine sono state anche rinvenute nei petali di fiori fluorescenti. La soluzione acquosa di betalaina posta in analisi è stata ricavata dalla macerazione in acqua di fette di rapa rossa. Spettro di assorbimento
Banda di assorbimento nel visibile centrata a 500nm e per lunghezze d’onda inferiori a ca 400nm Spettro di fluorescenza della soluzione “fresca” eccitato da emissione UV
Bande di fluorescenza a 476nm – 523nm – 603nm. La fluorescenza, sul giallo-verde, dovuta alle betaxantine è in parte assorbita dalle betacianine che filtrano una banda centrata a 540nm
Eccitazione
Assorbimento
Betaxantina
480nm
Emissione
Dettaglio emissione
di fluorescenza
Betanina
Assorbimento
Betacianina
540nm
Sistema Theremino – Spettrometro_ITA – Pag. 40
Spettro di assorbmento della soluzione “invecchiata” (la betacianina si è degradata)
Banda di assorbimento con picco a ca 480nm del pigmento betaxantina Spettro di fluorescenza della soluzione “invecchiata” (la betacianina si è degradata)
La banda di fluorescenza con picco a ca 540nm è dovuta alla betaxantina. La banda viene resa visibile nella soluzione “invecchiata” perché la concentrazione della betacianina è notevolmente diminuita nel tempo. Nella soluzione “fresca” questo picco di fluorescenza non è visibile perché l’emissione viene assorbita della betacianina che ha il picco di assorbanza proprio a 540nm. L’assenza della betacianina è anche evidente dallo spettro di assorbimento che mostra soltanto l’assorbimento del pigmento betaxantina. L’eccitazione a 532nm produce sola una debole fluorescenza a lunghezze d’onda maggiori.
532nm Ecc.
410nm Ecc.
Emissione
Betaxantina
Assorbimento
Betaxantina
480nm
Sistema Theremino – Spettrometro_ITA – Pag. 41
Analisi Spettrometrica di coloranti fluorescenti
Stilbene – Triazina (Sbiancanti Ottici)
Gli agenti sbiancanti ottici (OBA), agenti brillantanti fluorescenti (FBA) o agenti sbiancanti fluorescenti (FWA) sono composti chimici che assorbono luce nella banda violetta ed ultravioletta (solitamente 340-370 nm) dello spettro elettromagnetico e la riemettono nella banda del blu (tipicamente 420-470 nm).
La fluorescenza è una riemissione rapida a differenza della fosforescenza che è una emissione ritardata Questi additivi sono spesso usati per incrementare la brillantezza dei tessuti e della carta, producendo un effetto “sbiancante”, e facendo apparire questi materiali meno gialli e incrementando l’ammontare totale della luce blu riflessa.
I composti chimici con queste proprietà sono gli stilbeni e triazine, nome commerciale FBA 28, I quali assorbono radiazione nella banda UV e la riemettono nella banda visibile del blu. Una superficie bianca trattata con queste sostanze può emettere più luce visibile di quanta ne arriva sulla sua superficie, facendola apparire più brillante. La luce blu emessa da questi composti compensa la diminuzione di luminosità nella banda del blu e sposta la tinta con la quale appare la superficie trattata dal giallo/marrone verso il bianco. Spettro di assorbimento dello stilbene - triazina in acqua
Spettro di fluorescenza dello stilbene / triazina in acqua eccitato da emissione UV
Riferimento
Picco Assorb.
380nm
Stilbene
Stilbene
Triaz
.
Sistema Theremino – Spettrometro_ITA – Pag. 42
Fluoresceina Sodica
La fluoresceina sodica (o sale sodico della fluoresceina o uranina) è un indicatore. A temperatura ambiente si presenta come un solido rosso-bruno inodore, che emette una intensa fluorescenza nella gamma 520-530 nm (di colore giallo-verde, molto caratteristica) quando viene eccitata da raggi ultravioletti a 254 nm e nella gamma del blu (465-490 nm). Trattandosi di un colorante attivo anche ad elevatissime diluizioni, viene utilizzato in speleologia per individuare rami di corsi d'acqua sotterranei che,
scomparendo nel sottosuolo per ricomparire altrove, diventerebbero problematici da seguire. Per questo tipo di applicazione, una certa quantità di fluoresceina viene disciolta nel corso d'acqua che si addentra nel sottosuolo e, successivamente, si cercano corsi d'acqua che a loro volta sono stati colorati. Spettro di assorbimento della fluoresceina diluita in acqua. Secondo spettro con dettaglio zona UV
Spettro di fluorescenza della fluoresceina diluita in acqua eccitata da emissione UV e da laser a 532nm
Eccitazione
Eccitazione
Emissione
Stokes
Emissione
Anti-Stokes
Sistema Theremino – Spettrometro_ITA – Pag. 43
TetrabromoFluoresceina (eosina)
L'eosina è un colorante di contrasto dell'ematossilina, utilizzato in istologia per effettuare la colorazione del citoplasma. L'eosina è chimicamente una tetrabromofluoresceina della quale esistono anche derivati mono e di-bromo. Più precisamente, sono di comune utilizzo due molecole di eosina denominate eosina Y e eosina B: rispettivamente sono analoghi strutturali che presenta quattro sostituenti bromo ovvero due sostituenti bromo e due nitrogruppi -NO2. È il più importante colorante citoplasmatico e rappresenta il colorante di
contrasto di elezione dell'ematossilina, colora i cosiddetti granuli eosinofili (acidofili) delle cellule. Trova numerosi usi in microscopia, per esempio entra nella composizione di alcuni coloranti ematologici. In soluzione al 2% è utilizzata anche come disinfettante al posto della merbromina. In particolar modo viene utilizzata nelle affezioni dermatologiche (eritemi, candidosi) per tenere "pulita" la pelle.
Spettro di assorbimento della eosina
Spettro di fluorescenza della eosina eccitata da emissione UV e da laser a 532nm
Eccitazione
Riferimento
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 44
Arancio di Acridina
L'arancio di acridina è un composto eterociclico aromatico. Viene utilizzato in citologia e istologia come colorante. L’ arancio di acridina (AO) è un fluorocromo della famiglia delle Acridine, specifico per gli acidi nucleici (DNA/RNA) definito metacromatico , ossia con due diversi spettri di emissione : l’AO a
bassa concentrazione e con rapporto colorante/proteine basso si lega al DNA doppia elica ed emette fluorescenza verde attorno ai 525 nm ; all’aumento del rapporto colorante/proteine , l’AO provoca condensazione dell’acido nucleico a singola elica (RNA o DNA singola elica) ed emette fluorescenza rossa attorno ai 575 nm . Questa differente sensibilità’ degli acidi nucleici alla condensazione indotta dall’ AO è la base della differente colorazione del DNA versus RNA.
Spettro di assorbimento di arancio di acridina in acqua
Spettro di fluorescenza di arancio di acridina in acqua eccitata da emissione UV e da laser a 532nm
Riferimento
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 45
Rodamina B
La Rodamina B è un composto chimico ed un colorante A temperatura ambiente si presenta come un solido rosso quasi inodore. È un composto irritante, pericoloso per l'ambiente. E’ spesso utilizzata come tracciante all’interno di corsi d’acqua per determinare velocità e direzione del flusso. La rodamina emette fluorescenza e quindi può essere rilevata facilmente con strumenti chiamati fluorimetri. La rodamina è ampiamente utilizzata in biologia, in istologia ed in microscopia come indicatore e colorante.
La Rodamina B è “regolabile” attorno ai 610nm quando utilizzata nei laser a colorante. La sua resa quantica di fluorescenza è di 0.65 in etanolo basico, 0.49 in etanolo, 1.0, and 0.68 in etanolo al 94%.
Spettro di assorbimento della rodamina B
Spettro di fluorescenza della rodamina B eccitata da emissione UV e da laser a 532nm
Riferimento
Eccitazione
532nm Ecc.
Sistema Theremino – Spettrometro_ITA – Pag. 46
Rodamina 6G
La Rodamina 6G è un composto altamente fluorescente appartenente alla famiglia delle rodamine. E’ spesso utilizzata come tracciante all’interno di corsi d’acqua per determinare velocità e direzione del flusso. La rodamina emette fluorescenza e quindi può essere rilevata facilmente con strumenti chiamati fluorimetri. La rodamina è ampiamente utilizzata in biologia, in istologia ed in microscopia come indicatore e colorante. La Rodamina 6G è anche utilizzata come colorante laser, o mezzo di
guadagno, nei laser a colorante, e viene pompata dalla seconda armonica (532 nm) della emissione del laser Nd:YAG o del laser ad azoto. Il colorante ha una notevole fotostabilità, una alta efficienza quantica di fluorescenza (0.95), basso costo, e la sua emissione laser è prossima al suo picco di assorbanza (approssimativamente 530 nm). Il range della emissione laser di questo colorante va da 555nm a 585nm con un massimo a 566nm.
Spettro di assorbimento della rodamina 6G
Spettro di fluorescenza della rodamina 6G eccitata da emissione UV e da laser a 532nm
Riferimento
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 47
Verde Fluorescente
Il verde fluorescente è una miscela di fluoresceina con blu cresile brillante. La fluoresceina sodica (o sale sodico della fluoresceina o uranina) è un indicatore. A temperatura ambiente si presenta come un solido rosso-bruno inodore, che emette una intensa fluorescenza nella gamma 520-530 nm (di colore giallo-verde, molto caratteristica). Vedi paragrafo sulla fluoresceina. Il Blu Cresile Brillante (mostrato nella figura a lato) è un colorante impiegato principalmente in microscopia.
Spettro di assorbimento. Secondo spettro con dettaglio zona UV
Spettro di fluorescenza eccitata da emissione UV e da laser a 532nm
Eccitazione
Assorbimento
Fluoresceina
Assorbimento
Blu Cresile
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 48
Blu di Metilene
Il blu di metilene (BdM) è un composto organico della classe degli eterociclici aromatici. Trova impiego in molti campi differenti. A temperatura ambiente si presenta come un solido cristallino inodore di colore verde scuro, stabile all'aria e alla luce. Dissolto in soluzione acquosa assume intensa colorazione blu scuro. Si ottiene
industrialmente per ossidazione di una miscela di dimetil-p-fenilendiammina, tiosolfato sodico e dimetilanilina. Date le sue proprietà riducenti viene usato in dosi di 60 – 70 mg al giorno per ridurre la metaemoglobina in occasione di metaemoglobinizzazione. Nell'industria alimentare e tessile è usato come colorante. Trova uso anche in biologia (più specificamente in istologia) per colorare nucleo e nucleolo delle cellule. Quando ingerito in quantità non nocive modifica la colorazione delle urine, tingendole di un colore che può variare dal blu intenso al verde.
Spettro assorbimento (in trasmissione) del blu di metilene in etanolo Banda di assorbimento tra 550nm e 700nm con picchi a 665nm e 610nm
Spettro di fluorescenza del blu di metilene in etanolo eccitata da emissione UV, da laser a 532nm e da laser a ca 650nm. Banda di fluorescenza a ca 700nm
Banda
assorbimento
Eccitazione
650nm ca
Eccitazione
532nm
Eccitazione
UV
Fluorescenza
ca 700nm
Fluorescenza
ca 700nm
Fluorescenza
ca 700nm
Diffusione
Raman
Sistema Theremino – Spettrometro_ITA – Pag. 49
Violetto di Genziana
Il violetto di genziana (o violetto cristallo, violetto metile 10B, cloruro di esametilpararosanilina) è un colorante antimicotico, usato nel metodo di colorazione Gram. All'interno della procedura della colorazione di Gram esso rappresenta il colorante primario, che viene trattenuto dai batteri Gram-positivi anche dopo la decolorazione con alcol o acetone, facendoli apparire viola una volta visualizzati al microscopio. I suoi componenti sono: cloruro di esametile pararosanilina, cloruro di tetrametilpararosanilina, cloruro di pentametilpararosanilina. Viene anche utilizzato negli ospedali per il trattamento delle ustioni gravi ed altri infortuni alla pelle e alle
gengive. In acqua la soluzione di violetto di genziana ha un colore blu-viola con un massimo di assorbimento ai 590 nm. Il colore del pigmento dipende dalla acidità della soluzione. Per un pH di 1.0 la soluzione è verde con un massimo di assorbanza a 420nm e 620nm mentre in una soluzione fortemente acida (pH di −1), il colore è giallo con un picco di assorbanza a 420 nm. In soluzione alcaline una reazione chimica produce la forma trifenilmetanolo o carbinolo della sostanza, la quale risulta priva di colore.
Spettro assorbimento (in trasmissione) del violetto genziana
Banda di assorbimento tra 450nm e 650nm Spettro di fluorescenza del violetto genziana in etanolo eccitata da laser a 532nm.
Banda di fluorescenza a ca 610nm
Banda
assorbimento
Fluorescenza
ca 610nm
Diffusione
Raman
Sistema Theremino – Spettrometro_ITA – Pag. 50
Blu Metilene – Verde Malachite – Violetto genziana – Acriflavina
(Miscela antifungina)
Il blu di metilene (BdM) è un composto organico della classe degli eterociclici aromatici. Il verde malachite è un colorante organico. Viene commercializzato sotto forma di sale contenente l'anione cloruro (numero CAS569-64-2) o l'anione ossalato (numero CAS 18015-76-4). Il violetto di genziana (o violetto cristallo, violetto metile 10B, cloruro di esametilpararosanilina) è un colorante antimicotico, usato nel metodo di colorazione Gram.
Acriflavina (sinonimi: flavina o tripaflavina) (mostrata in figura). Cloridrato del clorometilato di diamino-acridina, derivato dall'acridina: appartiene al gruppo delle sostanze coloranti antisettiche. Formula di costituzione: È una polvere rosso-bruna, in soluzione acquosa giallo-citrina, con
fluorescenza verde. Non si altera alla sterilizzazione all'autoclave. Energico antisettico, particolarmente efficace contro i tripanosomi, donde il nome di tripaflavina; relativamente poco tossica per gli elementi vivi dei tessuti. Spettro di assorbimento della miscela blu metilene / verde malachite / violetto genziana / acriflavina
Spettro di fluorescenza della miscela blu metilene / verde malachite / violetto genziana / acriflavina
Riferimento
Assorbimento
Blu Metilene
Assorbimento
Verde Malachite
Violetto Genz.
Eccitazione Emissione
Acriflavina
Assorbimento
Acriflavina
Sistema Theremino – Spettrometro_ITA – Pag. 51
Ftalocianine
La ftalocianina è un composto eterociclico la cui struttura chimica è simile a quella delle porfirine naturali e strettamente correlata a quella delle porfirazine. La molecola possiede una cavità centrale in grado di legare ioni idrogeno o cationi metallici attraverso legami molto forti fra lo ione e quattro atomi di azoto di altrettanti gruppi isoindolo. Molti elementi sono stati coordinati all'interno delle ftalocianine e come accade per le porfirine naturali, spesso sono in grado di legare altri gruppi, fungendo da molecola trasportatrice. La ftalocianina, caratterizzata da un intenso colore verde-blu, è ampiamente
utilizzata come colorante. La ftalocianina forma complessi coordinati con molto elementi della tavola periodica. Anche questi composti risultano intensamente colorati e trovano svariate applicazioni come coloranti e pigmenti. Spettro di assorbimento
Si individuano tre bande di assorbimento : λ<450nm, 620nm, 720nm
Riferimento
Assorbimento
Ftalocianina
Sistema Theremino – Spettrometro_ITA – Pag. 52
Eritrosina
L'eritrosina (E127) è il colorante rosso del catrame di carbon fossile, contenente iodio e quindi in grado di provocare disturbi alla tiroide. Attualmente è utilizzato quale colorante alimentare in caramelle, farmaci ed è molto utile quale colorante della placca dentale ("pastiglie rivelatrici di placca"). È frequentemente usato per sensibilizzare al rosso le emulsioni fotografiche. E’ inoltre utilizzato in microscopia ed istologia come colorante.
Spettro assorbimento (in trasmissione) della soluzione acquosa di eritrosina
La banda di assorbimento presenta un picco di assorbanza a 530-540nm ed una spalla a ca 500nm Spettro di fluorescenza della soluzione acquosa di eritrosina eccitata da emissione UV e da laser a 532nm
Riferimento
Assorbimento
Eritrosina
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 53
Cumarina
La cumarina è un composto aromatico. A temperatura ambiente si presenta in forma di cristalli incolori, dall'odore caratteristico. Isolata per la prima volta da Dipteryx odorata, il cui nome popolare era per l'appunto coumarin, la cumarina è presente in più di 27 famiglie di vegetali, ed è responsabile dell'odore dolce dell'erba appena tagliata.
È la capostipite di una classe di composti derivati - detti cumarine - che hanno in comune la struttura benzopiranica della cumarina. Anche le idrossicumarine sono presenti in molte famiglie: umbelliferone, esculetina e scopoletina sono le più comuni in natura. Cumarine più complesse come le furanocumarine sono limitate a poche famiglie (Rutaceae e Apiaceae); tipico esempio gli psoraleni fototossici presenti nell'olio essenziale di Bergamotto (esempio il bergaptene). La cumarina è usato anche come un mezzo di guadagno in alcuni laser a colorante e come sensibilizzante in tecnologie fotovoltaiche. Assorbe a lunghezze d’onda inferiore a 400nm e presenta forte fluorescenza a 460nm. Spettro di fluorescenza della soluzione in etanolo della cumarina eccitata da emissione UV a 405nm
Fluorescenza
ca 460nm
Sistema Theremino – Spettrometro_ITA – Pag. 54
Analisi Spettrometrica di olii alimentari Gli olii alimentari (olio d’oliva, olio di semi) presentano interessanti proprietà ottiche (assorbimento, fluorescenza) dovute al contenuto di composti otticamente attivi, come la clorofilla, il beta carotene e altri. Queste proprietà possono essere utilizzate per riconoscere e caratterizzare i vari tipi di olio. Nello spettro dell’olio d’oliva extravergine, ottenuto attraverso spremitura a freddo si nota l’assenza dei prodotti della perossidazione degli acidi grassi, che danno fluorescenza a ca 470nm. Questo avviene sia perché l’olio viene lavorato a freddo e sia perché l’elevato contenuto di anti-ossidanti naturali (caroteni e polifenoli) preserva l’olio dalla degradazione ossidativa. Gli olii di semi mostrano tutti invece, in misura variabile, una evidente fluorescenza a ca 470nm, segno del contenuto in perossidi derivanti dalla degradazione ossidativa degli acidi grassi, sia perché vengono presumibilmente lavorati a caldo e sia a causa del minore contenuto di molecole anti-ossidanti. Queste caratteristiche rendono gli oli di semi meno adatti ad utilizzi ad alta temperatura.
Olio d’Oliva Extra Vergine
Spettro assorbimento (in trasmissione) dell’olio d’oliva Si notano i picchi di assorbimento nella banda del rosso a ca 660-670nm e nella banda del blu, inferiore a ca 500nm. L’assorbimento dell’olio d’oliva è dovuto a carotenoidi e clorofille.
Spettro di fluorescenza dell’olio d’oliva eccitata da emissione UV a 405nm (primo spettro) e da emissione laser a 532nm (secondo spettro) Il picco a 680nm è dovuto al contenuto in clorofilla A
Clorofille
Clorofille
Carotenoidi
Clorofilla A
Clorofilla A
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 55
Spettro di fluorescenza dell’olio d’oliva sottoposto a riscaldamento (degradazione termica) eccitata da emissione UV. Risulta diminuita la fluorescenza dovura alle clorofille mentre è comparso il segnale della presenza dei perossidi da degradazione termica degli acidi grassi.
Olio di Semi d’Arachide
Spettro di fluorescenza dell’olio di arachidi eccitato da emissione UV (visibile nello spettro) La banda di fluorescenza centrata a 664nm è dovuta al contenuto in clorofille La banda di fluorescenza con i picchi a 463nm e ca 475nm presumibilmente è dovuta ai prodotti della perossidazione (degradazione) degli acidi grassi polinsaturi presenti nell’olio (acido oleico e linoleico)
Spettro di fluorescenza dell’olio d’arachide sottoposto a riscaldamento (degradazione termica) eccitata da emissione UV. Si nota l’aumento della intensità della fluorescenza a 470nm-530nm dovuta alla degradazione termica degli acidi grassi ed alla conseguente produzione di perossidi. E’ praticamente sparita la fluorescenza delle clorofille che quindi sono state degradate dal riscaldamento.
Eccitazione
Clorofilla A Emissione
da perossidi
Olio Oliva dopo
riscaldamento
Olio Arachide dopo
riscaldamento
Emissione
da perossidi
Clorofilla A
Sistema Theremino – Spettrometro_ITA – Pag. 56
Olio di Semi di Girasole
Spettro di fluorescenza dell’olio di girasole eccitato da emissione UV (visibile nello spettro) La banda di fluorescenza con i picchi a 464nm e ca 476nm presumibilmente è dovuta ai prodotti della perossidazione (degradazione) degli acidi grassi polinsaturi presenti nell’olio (acido oleico e linoleico)
Olio di Semi di Mais
Spettro di fluorescenza dell’olio di mais eccitato da emissione UV (visibile nello spettro) La banda di fluorescenza con il picco a 464nm presumibilmente è dovuta ai prodotti della perossidazione (degradazione) degli acidi grassi polinsaturi presenti nell’olio (acido oleico e linoleico) L’attribuzione della banda di fluorescenza con il picco a 520nm è incerta e potrebbe essere anch’essa legata al processo di degradazione termica degli acidi grassi. In alternativa (o in aggiunta) potrebbe essere dovuta ai composti della vitamina B2 (flavine).
Olio di Soia
Spettro di fluorescenza dell’olio di soia eccitato da emissione UV (visibile nello spettro) La banda di fluorescenza con il picco a 477nm presumibilmente è dovuta ai prodotti della perossidazione (degradazione) degli acidi grassi polinsaturi presenti nell’olio (acido oleico e linoleico). Lo stesso vale pr la banda con picco a 533nm, da valutare il contributo degli isoflavoni per le emissioni di fluorescenza sul verde. Vedi paragrafo sulla soia.
Eccitazione
Eccitazione
Eccitazione Clorofilla A
Sistema Theremino – Spettrometro_ITA – Pag. 57
Olio di Mandorle
Spettro di fluorescenza dell’olio di mandorle eccitato da emissione UV (visibile nello spettro) La banda di fluorescenza con il picco a 477nm presumibilmente è dovuta ai prodotti della perossidazione (degradazione) degli acidi grassi polinsaturi presenti nell’olio (acido oleico e linoleico) La banda di fluorescenza con i picco a 533nm e 596nm presumibilmente è dovuta ai composti della vitamina B2 (flavine) – Vedi anche paragrafo sulla fluorescenza della riboflavina
Olio di Sesamo
Spettro di fluorescenza dell’olio di sesamo eccitato da emissione UV (visibile nello spettro) La banda di fluorescenza con il picco a 475nm presumibilmente è dovuta ai prodotti della perossidazione. L’attribuzione della banda di fluorescenza con il picco a 533nm è incerta e potrebbe essere anch’essa legata al processo di degradazione termica degli acidi grassi, oppure dovuta ai composti della vitamina B2 (flavine)
Olio di Ricino
Spettro di fluorescenza dell’olio di ricino eccitato da emissione UV (visibile nello spettro) La banda di fluorescenza con il picco a 479nm presumibilmente è dovuta ai prodotti della perossidazione.
Eccitazione
Eccitazione Clorofilla A
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 58
Analisi Spettrometrica di vitamine
Cobalamina (Vitamina B12)
La cobalamina (o vitamina B12) venne isolata e caratterizzata a seguito di una serie di ricerche in merito all'anemia perniciosa. Nel 1926 si scoprì che nel fegato vi è un fattore capace di curare tale patologia ed esso venne isolato e cristallizzato nel 1948. La struttura della vitamina B12 venne chiarita nel 1956. La vitamina B12 è una sostanza di colore rosso, cristallina, igroscopica, fotosensibile e altamente solubile in acqua; è formata da un anello corrinico (composto da 4 anelli pirrolici e tre ponti metinici) con al centro un atomo di cobalto coordinato da quattro atomi di azoto. Il cobalto presenta, inoltre, due legami di coordinazione perpendicolari rispetto al piano dell'anello. Il primo di essi si stabilisce con una molecola di 5,6 dimetilbenzimidazolo legata, a sua volta, a un ribosio 3-fosfato. Il secondo legame si stabilisce con diversi gruppi (R) i quali possono essere:
cianidrico -CN (cianocobalamina) ossidrilico -OH (idrossicobalamina)
metile -CH3 (metilcobalamina)
5-deossiadenosile (5'-deossiadenosilcobalamina)
Spettro assorbimento (in trasmissione) della cobalamina.
Banda di
assorbimento
Sistema Theremino – Spettrometro_ITA – Pag. 59
Riboflavina (Vitamina B2) e Piridossina (Vitamina B6)
La riboflavina è un composto eterociclico ottenuto da una molecola di flavina cui è legata una catena formata da ribitolo. È un composto di colore giallo poco solubile in acqua, stabile al calore e fluorescente qualora sottoposto a luce ultravioletta. La piridossina, il piridossale e la piridossamina (e i corrispondenti esteri fosfati tra cui il più noto è il piridossalfosfato) sono le forme con cui si presenta la vitamina B6.
Spettro di fluorescenza di composto mltivitaminico con vitamine del gruppo B eccitata da emissione UV
Retinolo (Vitamina A)
La vitamina A è una vitamina liposolubile, in natura si trova in diverse forme. Con il termine di vitamina A vengono indicati sia il retinolo che i suoi analoghi, detti retinoidi, di cui si conoscono almeno 1500 tipi diversi, tra naturali e sintetici. Anche i carotenoidi posseggono l'attività biologica della vitamina A in quanto possono
fungere da provitamine (se ne conoscono almeno 600 tipi diversi, di cui solo il 10% possiede una simile attività).
Spettro di fluorescenza del retinolo (con eccipienti) eccitato da emissione UV con laser a 405nm
Eccitazione Riboflavina
Piridossina
Fluorescenza
Retinolo Fluorescenza
Eccipienti
Sistema Theremino – Spettrometro_ITA – Pag. 60
Analisi Spettrometrica di sostanze alimentari
Vino Bianco
Spettro di fluorescenza del vino bianco eccitato da emissione UV
Banda di fluorescenza a 478nm Banda di fluorescenza a 520-540nm Le bande di fluorescenza evidenziate sono di difficile attribuzione. L’insieme di composti organici contenuti nel vino bianco, ad esempio stilbeni, polifenoli e flavonoidi concorrono tutti a determinare l’emissione finale. La complessità dello spettro si deduce anche dal contorno frastagliato delle bande, segno che vi sono più composti che emettono fluorescenza a diverse lunghezze d’onda leggermente diverse fra loro.
Aceto di Vino
Spettro di fluorescenza di aceto di vino eccitato da emissione UV
Banda di fluorescenza a 480nm Banda di fluorescenza a 520-540nm La bande di fluorescenza nell’aceto di vino sono molto simili a quelle che si riscontrano nel vino.
Eccitazione
Dettaglio emissione
di fluorescenza
Flavonoidi Stilbeni
Sistema Theremino – Spettrometro_ITA – Pag. 61
Isoflavoni (Salsa di Soia)
L'Isoflavone è il capostipite di una serie di composti chimici naturali nota col nome di isoflavoni, una sottoclasse dei composti fenolici di origine vegetale appartenenti alla più ampia classe dei flavonoidi. La struttura chimica è basata su uno scheletro C15 di atomi di carbonio composto da due anelli aromatici ed uno eterociclico; un anello aromatico (anello A) risulta condensato con l'eterociclico (anello C) ed il terzo (anello aromatico B) collegato a questi. La differenza con la struttura dei flavoni risiede nel legame in posizione 3 anziché 2 dell'anello B sull'anello C. Gli
isoflavoni sono contenuti nei prodotti alimentari derivati dalla soia, come la salsa di soia e l’olio di soia.
Spettro di assorbimento della salsa di soisa diluita in acqua
Spettro di fluorescenza della salsa di soia diluita in acqua eccitata da emissione UV
Estratto di noci verdi (Liquore Nocino)
Spettro di fluorescenza eccitato da emissione UV
Banda di fluorescenza a 480nm, a 540nm e a 600nm Le bande di fluorescenza evidenziate sono di difficile attribuzione. L’insieme di composti organici contenuti nell’estratto ad esempio polifenoli e flavonoidi concorrono tutti a determinare l’emissione finale.
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 62
ProtoPorfirina (Guscio Uovo)
Le protoporfirine sono tetrapirroli contenenti le seguenti catene laterali:
metile
acido propionico
vinile La protoporfirina IX è una porfirina particolare che sfrutta cationi metallici bivalenti, in particolare Fe++, per trasportare piccole molecole come O2. Insieme al catione Fe++ costituisce il nucleo del Gruppo eme della emoglobina, mioglobina e molti altri enzimi. Insieme con lo ione magnesio (Mg 2+) costituisce la parte
principale della clorofilla. Insieme allo ione zinco (Zn 2+) forma la zinco protoporfirina. Il numero (ad esempio IX) indica storicamente la posizione di diverse catene laterali, ma, dato che la nomenclatura è nel frattempo cresciuta, viene utilizzato solo in misura parziale. La protoporfirina IX è un diretto precursore dell’eme e si accumula nei pazienti che soffrono di protoporfiria eritropoietica, che è una delle malattia genetiche riguardanti la biosintesi dell’eme. Questa malattia causa una grave fotosensibilità nei confronti della luce visibile. La sensibilità della protoporfirina IX nei confronti della luce viene anche usata come terapia contro diverse forme di cancro (terapia fotodinamica, PDT). Le protoporfirine vengono depositate nel guscio delle uova di alcuni uccelli sottoforma di pigmenti marroni o rossi, sia come colore uniforme che come puntinatura. Le protoporfirine rafforzano il guscio dell’uovo, e vengono depositate laddove il guscio è più sottile a causa della penuria di calcio. La puntinatura del guscio tende quindi ad essere maggiore laddove il suolo è povero di calcio, ed anche nelle uova che vengono deposte per ultime. La soluzione di protoporfirina posta in analisi è stata ricavata dallo scioglimento in acido cloridrico di frammenti di guscio d’uova. Spettro di assorbimento della protoporfirina
Spettro di fluorescenza della protoporfirina eccitata da emissione UV
Banda di fluorescenza a 605nm Banda di fluorescenza a 662nm
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 63
Miele
Spettro di assorbimento del miele: due bande di assorbimento da 430nm a 490nm e oltre i 550nm
Spettro di fluorescenza del miele
Si possono individuare due picchi di emissione: ca 475nm e ca 520-540nm Da letteratura la banda di fluorescenza verde attorno ai 520nm potrebbe essere attribuita al contenuto di flavine (vedi paragrafo sulla fluorescenza della vitamina B2), mentre la banda attorno ai 470nm potrebbe essere attribuita alla sostanza enzimatica NADH.
Riferimento
Miele Acacia
Miele Tarassaco
Miele Acacia
Miele Tarassaco
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 64
Sciroppo di rose
Spettro di fluorescenza eccitata da emissione UV a 405nm Si possono individuare due picchi di emissione: ca 480nm e ca 540nm La banda di fluorescenza verde dai 520nm ai 540nm potrebbe essere attribuita al contenuto di flavine, mentre la banda attorno ai 480nm potrebbe essere attribuita alla sostanza NADH. NAD(P)H Il nicotinammide adenina dinucleotide fosfato (a cui ci si riferisce spesso con la formula NADP(H), che comprende sia NADP+, la forma ossidata, che NADPH, la forma ridotta, a volte indicata anche come NADPH2[2]) è un nucleotide simile per funzioni biologiche e struttura al NAD, da cui differisce per la presenza di un gruppo fosfato aggiuntivo esterificato al gruppo ossidrilico del carbonio 2' dell'adenosina. È un coenzima ossidoriduttivo. Flavine Le flavine (dal latino flavus, giallo), sono un gruppo di composti organici basati su un derivato della pteridina, la isoallossazina. Un'importante sostanza appartenente al gruppo delle flavine è la riboflavina (vitamina B2) un costituente dei coenzimi implicati nel trasferimento di idrogeno, la flavin adenina dinucleotide (FAD) e la flavina mononucleotide (FMN). La riboflavina è formata dall'unione della flavina con il ribitolo, un derivato del ribosio. Le flavine sono composti idrosolubili.
Estratto di Rabarbaro
Spettro di fluorescenza eccitata da emissione UV a 405nm Si può individuare un picco di emissione a ca 600nm La banda di fluorescenza rossa attorno ai 600nm è attribuibile al composto antrachinone contenuto nelle radici di rabarbaro.
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 65
Birra Chiara
Spettro di fluorescenza eccitata da emissione UV a 405nm Si possono individuare due picchi di emissione a ca 480nm e 530nm Le bande di fluorescenza evidenziate sono di difficile attribuzione. L’insieme di composti organici contenuti nella birra, ad esempio polifenoli e flavonoidi concorrono tutti a determinare l’emissione finale. Possiamo comunque ipotizzare che la banda sul blu sia dovuta ai polifenoli mentre la banda sul verde sia dovuta alla riboflavina.
Birra Scura
Spettro di fluorescenza eccitata da emissione UV a 405nm Si possono individuare tre picchi di emissione a ca 480nm, 530nm e 600nm
Birra Doppio Malto
Spettro di fluorescenza eccitata da emissione UV a 405nm Si possono individuare tre picchi di emissione a ca 480nm, 530nm e 600nm
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 66
Estratto di Pistacchio
Spettro di fluorescenza eccitata da emissione UV a 405nm Si può individuare un picco di emissione a ca 670nm La banda di fluorescenza rossa attorno ai 670nm è attribuibile alla clorofilla, responsabile del colore verde del pistacchio
Te Verde
Spettro di fluorescenza di infuso di te verde eccitato da emissione UV
Banda di fluorescenza a 540nm Banda di fluorescenza a 680-690nm La banda a 680nm è attribuibile al contenuto in clorofille mentre la banda sul verde-azzurro a 540nm è presumibilmente dovuta al complesso di sostanze organiche contenute nella foglia della pianta del te, tra le quali ricordiamo i polifenoli ed i flavonoidi.
Clorofilla
Flavonoidi Clorofille
Sistema Theremino – Spettrometro_ITA – Pag. 67
Analisi Spettrometrica di farmaci
EmatoPorfirina (Farmaco Tonogen)
Ematoporfirina Composto porfirinico, C34H38O6N4. Si ottiene dall’emina e dall’emoglobina per azione di un acido forte. Differisce dalla protoporfirina dell’emoglobina per la presenza di due gruppi idrossietilici al posto di due gruppi vinilici. La sua importanza è soprattutto storica in quanto è stata la prima porfirina preparata per sintesi (a partire dalle emine). Il suo ruolo biologico sembra di scarso rilievo e la sua presenza in natura non è attualmente certa. La ematoporfirina viene utilizzata come fotosensibilizzante nella terapia fotodinamica (PDT)
Spettro di assorbimento della ematoporfirina. Secondo spettro con dettaglio zona UV
Spettro di fluorescenza della ematoporfirina eccitata da emissione UV e da laser a 532nm
Banda di fluorescenza a 620nm Banda di fluorescenza a 682nm
532nm Ecc.
410nm Ecc.
Sistema Theremino – Spettrometro_ITA – Pag. 68
Salicilato di Sodio
Il salicilato di sodio è il sale di sodio dell'acido salicilico. A temperatura ambiente si presenta come un solido cristallino bianco inodore. Viene ottenuto facendo reagire l’acido acetilsalicilico (la comune aspirina) in sospensione acquosa con una soluzione basica di idrossido di sodio, al termine della reazione si ottiene una soluzione di salicilato di sodio dal tenue colore azzurro. Presenta fluorescenza blu quando esposto a radiazione UV.
Spettro di assorbimento
Spettro di fluorescenza eccitato da emissione UV
Banda di fluorescenza centrata su ca 470nm
Assorbimento
λ < 400nm
Eccitazione
Dettaglio emissione
di fluorescenza
Riferimento
Sistema Theremino – Spettrometro_ITA – Pag. 69
Piroxicam
Il piroxicam è un farmaco antinfiammatorio non steroideo, appartenente alla serie degli oxicam, che possiede attività antiinfiammatoria, analgesica e antipiretica. È un composto anfotero con proprietà sia di acido debole sia di base debole.
Spettro di fluorescenza
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 70
Analisi Spettrometrica di varie sostanze
Piranina
Spettro di fluorescenza di piranina in etanolo eccitata da emissione UV
La Piranina è un colorante fluorescente idrofilico, sensibile al pH appartenente al gruppo di sostanze chimiche note con il nome di arilsolfonati. La piranina è solubile in acqua e trova applicazioni come agente colorante, come colorante biologico, reagente ottico e indicatore di pH. La piranina viene inoltre utilizzata negli evidenziatori gialli, dando loro la caratteristica e brillante tinta giallo-verde fluorescente. Viene anche utilizzata in alcuni tipi di saponi.
Acqua di colonia
Spettro di fluorescenza di acqua di colonia eccitata da emissione UV. La fluorescenza è dovuta alla cumarina
Composto Sbiancante
Spettro di fluorescenza dello sbiancante contenuto in detersivo eccitato da emissione UV a ca 370nm Dallo spettro si può dedurre la presenza di sostanze del tipo stilbeni
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 71
Salicilato di Metile
Il salicilato di metile è l'estere dell'acido salicilico e del metanolo. A temperatura ambiente si presenta come un liquido incolore dall'odore aromatico. Il salicilato di metile è utilizzato come vasodilatatore cutaneo, nel trattamento del dolore muscolare e articolare. Nel corpo viene metabolizzato a salicilati in particolar modo ad acido acetilsalicilico. Contenuto nell’olio essenziale della pianta gaulteria, è noto come olio “wintergreen”. Confrontare con il paragrafo relativo al salicilato di sodio.
Spettro di assorbimento
Spettro di fluorescenza eccitato da emissione UV
Banda di fluorescenza centrata su ca 476nm
Chinino
Spettro di fluorescenza del chinino (acqua tonica) eccitato da emissione UV a 370nm (lampada wood).
Il chinino, formula chimica C20H24N2O2, è un alcaloide naturale avente proprietà antipiretiche, antimalariche e analgesiche. Da letteratura il picco di emissione da fluorescenza del solfato di chinino è di 450nm.
Assorbimento
λ < 400nm
Sistema Theremino – Spettrometro_ITA – Pag. 72
Urina
Spettro assorbimento (in trasmissione) della urina Si nota il picco di assorbimento a ca 460nm dovuto alla bilirubina.
La bilirubina è un pigmento di colore giallo-rossastro, contenuto nella bile ed è un prodotto del catabolismo dell'emoglobina. La parola deriva dal latino bilis, bile, e ruber, rosso.
Spettri di fluorescenza dell’urina eccitata da emissione UV Banda a ca 480nm, dovuta alla sostanza NAD(P)H. Banda a ca 520nm, dovuta al contenuto di flavine
Eccitazione
Eccitazione
Bilirubina
Riferimento
Sistema Theremino – Spettrometro_ITA – Pag. 73
Emoglobina
Spettro assorbimento (in trasmissione) della emoglobina Si notano i picchi di assorbimento a 579nm, a 540nm e a 413nm e per λ inferiori a 390nm
L'emoglobina è una proteina globulare la cui struttura quaternaria consta di quattro sub-unità. È solubile, di colore rosso (è una cromoproteina), ed è presente nei globuli rossi del sangue dei vertebrati, esclusi alcuni pesci antartici. È responsabile del trasporto dell'ossigeno molecolare da un compartimento ad alta concentrazione di O2 ai tessuti che ne hanno bisogno. Ognuno dei suoi 4 globuli proteici, detto globina, ha al suo interno una molecola di protoporfirina che coordina uno ione ferro Fe (II), posto leggermente al di fuori del piano della molecola, nell'insieme chiamata Gruppo Eme. Quando si lega all'ossigeno l'emoglobina viene chiamata ossiemoglobina, nella forma non legata deossiemoglobina.
Assorbimento della emoglobina da letteratura
Riferimento
Emoglobina
Emoglobina Diluita
Abs. Max 579nm Abs. Max 540nm
Abs. Max 413nm
Sistema Theremino – Spettrometro_ITA – Pag. 74
Benzina
Spettro di fluorescenza della benzina eccitata da emissione UV Picco di emissione a 445nm Picco di emissione a 474nm Picco di emissione a 498nm La fluorescenza della benzina è dovuta al suo contenuto di idrocarburi poliaromatici. Lo spettro che si ottiene è una miscela di picchi distinti di intensità variabile :
- Composti monociclici (benzene, toluene, etilbenzene, xylene) : 250-290nm (noti come BTEX) - Composti policiclici (noti come IPA)
o Composti con due anelli (naftalene) : 310-330nm o Fenantrene (tre anelli) : 345-355nm o Antracene : 447nm o Tetracene (Naftacene) : 473nm, 498nm
Lo spettro viene ottenuto con eccitazione a 405nm e quindi vengono evidenziati solo le emissioni a lunghezza d’onda maggiore, tra le quali si riconoscono i picchi dell’antracene e del tetracene
Antracene
L'antracene è un composto idrocarburico policiclico aromatico (IPA) solido costituito da tre anelli benzenici condensati e possiede struttura lineare. I doppi legami fra gli atomi di carbonio danno origine alla fluorescenza. L'antracene è utilizzato nell'industria dei coloranti per la sintesi del colorante Rosso d'alizarina. Era utilizzato anche come conservante
nell'industria del legname, grazie alle sue proprietà insetticide. L'antracene è incolore, ma presenta fluorescenza blu se investito da una fonte di luce ultravioletta. L'antracene subisce con estrema facilità fotodimerizzazione per irradiazione con UV. L'antracene ha trovato ultimamente spazio come semiconduttore organico, è inoltre utilizzato come scintillatore per il rilevamento di elettroni e particelle alfa.
Spettro di fluorescenza del difenil antracene (da glowstick) eccitato da emissione UV
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 75
Tetracene (Naftacene)
Il tetracene (o naftacene) è composto chimico idrocarburico policiclico aromatico, costituito da 4 anelli benzenici condensati tra loro. Come per l’antracene anche in questo caso i doppi legami fra gli atomi di carbonio danno origine alla fluorescenza. Al crescere della lunghezza
della catena, cresce la lunghezza d’onda di fluorescenza. La sua formula bruta è C18H12. Fa parte della serie degli aceni. Il naftacene si comporta da materiale semiconduttore organico e viene impiegato nell'ambito della tecnologia OFET (Organic Field-Effect Transistor) e OLED (Organic Light Emitting Diode). Viene impiegato inoltre nella tecnologia laser a coloranti e in applicazioni della chemiluminescenza.
Spettro di fluorescenza del tetrafenil naftacene (da glowstick) eccitato da emissione UV
Olio Lubrificante per Motore
Spettro di fluorescenza eccitata da emissione UV
Spettro di fluorescenza eccitata da laser a 532nm
Gli oli lubrificanti per motori vengono additivati con coloranti fluroescenti al fine di facilitare la ricerca di eventuali perdite. Dagli spettri si possono notare la bande di fluorescenza dovute a questi additivi. La banda sul blu-verde è probabilmente dovuta ad una miscela di stilbene / triazina mentre la banda sull’arancione potrebbe essere dovuta ad un colorante simile all’arancio di acridina.
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 76
Olio Essenziale di Bergamotto
L'essenza si presenta come un liquido limpido (a volte è presente un deposito formato da cere) di colore da verde a giallo verdastro. Da un punto di vista chimico-fisico è costituita per la maggior parte (mediamente il 95%) da una frazione volatile e da una frazione (o residuo) non volatile (il restante 5%). Chimicamente è una miscela altamente complessa di numerose classi di sostanze organiche, in particolare terpeni, esteri, alcoli e aldeidi, per la frazione volatile, composti eterociclici ossigenati, cumarine e furanocumarine, per la frazione non volatile. I componenti principali della frazione non volatile sono costituiti da cumarine (citroptene, 5-geranilossi-7-metossicumarina) e furanocumarine (bergaptene, bergamottina). Le sostanze furanocumarine (note anche come psoraleni) sono fototossiche.
I : Spettro di fluorescenza eccitata da emissione laser a 405nm. Picco di emissione di Clorofille a ca 680nm. Bande su blu–verde-giallo dovute presumibilmente a cumarine e furanocumarine. II : Spettro di fluorescenza eccitato da emissione laser a 532nm. Picco di emissione di Clorofille a ca 680nm. III : Spettro di fluorescenza eccitato da emissione laser a 650nm. Picco di emissione di Clorofille a ca 680nm.
III
II
I
Eccitazione
Eccitazione
Clorofille
Clorofille
Clorofille
Cumarine
Furanocumarine
Sistema Theremino – Spettrometro_ITA – Pag. 77
Spettro di assorbimento dell’essenza di bergamotto Picchi di assorbimento a 480 e 660nm dovuti a clorofille
Olio Essenziale di Camomilla
L’olio essenziale di camomilla contiene sostanze interessanti tra le quali citiamo l’azulene. L'azulene è un idrocarburo aromatico, isomero del naftalene. È anche un monoterpene. A temperatura ambiente si presenta come un solido cristallino di colore intermedio tra il blu-violetto e il nero, insolubile in acqua. Trova principalmente impiego come colorante e nell'industria cosmetica.
La sua molecola è planare ed è composta da due anelli condensati, uno a 5 atomi di carbonio, l'altro a 7. Caretteristica peculiare dell’azulene è la sua fluorescenza anomala. Questa molecola infatti emette fluorescenza dalla transizione S2-S0 invece che dalla consueta transizione S1-S0.
Spettro di assorbimento dell’essenza di camomilla
Spettro di fluorescenza dell’essenza di camomilla eccitata da emissione UV
Azulene
Flavonoidi
Sistema Theremino – Spettrometro_ITA – Pag. 78
Olio Essenziale di Arancio
L'olio essenziale di arancio (Citrus aurantium) viene estratto dalla scorza dei frutti dell'omonimo albero, tramite spremitura a freddo o distillazione. Si utilizzano frutti giunti a maturazione in modo naturale. A seconda della tipologia dei frutti utilizzati, avremo olio essenziale di arancio dolce o olio essenziale di arancio amaro.
Spettro di fluorescenza eccitata da emissione UV
Acqua di Fiori d’Arancio
Alla fine della distillazione dei fiori d’arancio si ottiene un liquido che è composto da due fasi: una fase acquosa, che stratifica in basso perché più pesante, e una fase oleosa, che si porta in alto perché più leggera. Separata l’una dall’altra, la fase acquosa rappresenta appunto l’acqua di fiori di arancio, mentre quella oleosa, più pregiata, costituisce l’olio essenziale di fiori d’arancio. L’olio essenziale di maggior produzione si ricava dai fiori dell’arancio amaro (essenza di neroli). La fluorescenza blu-violetta è dovuta al contenuto di antranilato di metile. L'antranilato di metile è l'estere metilico dell'acido antranilico. Viene utilizzato come repellente per gli uccelli. È considerato uno dei primi aromi artificiali, ma è presente in natura in numerosi olii essenziali.
Spettro di fluorescenza eccitata da emissione UV
Eccitazione
Eccitazione Clorofille
Flavonoidi
Antranilato di
Metile
Sistema Theremino – Spettrometro_ITA – Pag. 79
Olio Essenziale di Curcumina
La curcumina è un colorante alimentare, usato per impartire alle preparazioni un colore giallo simile a quello
dello zafferano. A temperatura ambiente si presenta come una polvere cristallina di colore giallo-arancione intenso. È poco solubile in acqua, ma è solubile in etanolo e nell'acido
acetico. La curcumina si ottiene per estrazione con solvente dal rizoma essiccato e macinato della pianta di Curcuma longa (Curcuma domestica Valeton). L'estratto deve essere separato dagli aromi presenti, per cui viene purificato per cristallizzazione. Ad essa si accompagnano piccole quantità dei suoi derivati demetossi- e bis-demetossi-, ovvero privi di uno o di entrambi i gruppi -OCH3. Il prodotto ottenuto è liposolubile, di un colore giallo brillante tendente al verdastro.
Spettro di assorbimento della soluzione in etanolo di curcumina Massimo relativo di assorbimento a ca 420nm
Spettro di fluorescenza della soluzione in etanolo di curcumina eccitata da emissione UV Picco a ca 535nm
Eccitazione
Fluorescenza della
Curcumina
Riferimento
Assorbimento
della Curcumina
Sistema Theremino – Spettrometro_ITA – Pag. 80
Analisi Spettrometrica di sostanze inorganiche
Alluminato di stronzio attivato con Europio
Stronzio Alluminato (SRA, SrAl, SrAl2O4) è un solido inodore, non infiammabile, più pesante dell’acqua e si presenta sottoforma di polvere giallo pallida. E’ biologicamente e chimicamente inerte. Quando viene attivato con un apposito drogante (ad esempio Europio, in tal caso viene indicato come SrAl2O4:Eu), diventa un fosforo fotoluminescente con una persistenza particolarmente lunga della luminosità. L'alluminato di stronzio attivato dall'europio, SrAl2O4:Eu:Dy, è un nuovo materiale con luminosità più alta ed una persistenza decisamente più lunga; emette luce verde e color acqua, dove il verde emette la più alta luminosità, mentre l'acqua è caratterizzata dalla durata più lunga. SrAl2O4:Eu:Dy emette una luce 10 volte maggiore, 10 volte più duratura, e 10 volte più costosa rispetto al ZnS:Cu. Le lunghezze d'onda di eccitazione per l'alluminato di stronzio variano tra i 200 e i 450 nm. La lunghezza d'onda per la fluorescenza verde è di 520 nm, per la versione verde-azzurra è di 505 nm, mentre per la versione blu è di 490 nm. Colori con lunghezza d'onda più lunga possono essere ottenuti sempre dall'alluminato di stronzio, a scapito di una perdita in luminosità. La lunghezza d’onda prodotta dipende dalla struttura cristallina del materiale. Piccole modifiche nel processo di produzione possono causare variazioni sensibili nella lunghezza d’onda d’emissione. La luminosità dipende dalla dimensione del particolato; in genere maggiore è la dimensione dei grani e maggiore è la luminosità. Spettro di fluorescenza eccitata da emissione UV
Dettaglio del picco di emissione a ca 520nm
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 81
Vetro arricchito con Uranio
Spettro di fluorescenza del vetro all’uranio eccitato da emissione UV
Bulbo lampada alogena
Spettro di fluorescenza del bulbo di una lampadina alogena eccitato da emissione UV. La fluorescenza è presumibilmente dovuta al quarzo di cui è costituita l’ampolla interna che racchiude il filamento di tungsteno.
Eccitazione
Eccitazione
Sistema Theremino – Spettrometro_ITA – Pag. 82
Spettroscopia Raman
La spettroscopia Raman è una tecnica spettroscopica basata sull'effetto Raman. Per le sue caratteristiche, è considerata complementare alla spettroscopia infrarossa e rappresenta una tecnica comunemente utilizzata in analisi chimica e in studi sulla struttura dei composti chimici. In questo modo è possibile indagare anche molecole quali N2, inattive all'infrarosso. Nella spettroscopia Raman si utilizza normalmente una luce laser nel campo visibile, nel vicino infrarosso o nel vicino ultravioletto. In questo modo è possibile eccitare i livelli energetici vibro-rotazionali delle molecole, osservando, nel relativo spettro, transizioni che sottostanno alla regola di selezione ΔJ=0, ±2 per vibro-rotori lineari e ΔJ=0, ±1, ±2 per vibro-rotori simmetrici. Devono essere soddisfatte le regole di Pauli: non tutte le rotazioni saranno permesse dal momento che i bosoni devono mantenere invariato il segno della loro funzione d'onda durante la rotazione e i fermioni devono cambiarla. Affinché si abbia l'eccitazione dei livelli vibrazionali la regola di selezione implica Δν=±1. La spettroscopia Raman è una spettroscopia di scattering dove si fa incidere sul campione la radiazione elettromagnetica monocromatica iniziale di intensità e frequenza nota e viene misurata la radiazione diffusa tramite rivelatore posto a 90º o 180º rispetto al cammino ottico lungo il campione. La radiazione può essere diffusa in tre modi: Stokes, anti-Stokes e Rayleigh (scattering elastico). La radiazione Stokes possiede energia minore rispetto alla radiazione originaria incidente, visto che una parte di tale energia è utilizzata per promuovere una transizione a un livello superiore. La radiazione anti-Stokes riceve invece un contributo energetico dallo stato eccitato quando passa a un livello inferiore, per cui è caratterizzata da maggiore energia. La radiazione Rayleigh risulta invece da scattering elastico e possiede la stessa energia della radiazione incidente.
Spettro di scattering Raman di etanolo 95% - Eccitazione laser 532nm
Spettro di scattering Raman di clorofilla in etanolo 95% - Eccitazione laser 532nm
Diffusione
Rayleigh
Diffusione
Rayleigh
Diffusione
Raman
Diffusione
Raman
Sistema Theremino – Spettrometro_ITA – Pag. 83
Spettroscopia di Composti ChemioLuminescenti
La chemiluminescenza (a volte si usa il termine chemioluminescenza) è l'emissione di radiazione elettromagnetica (in particolare nel visibile e nel vicino infrarosso) che può accompagnare una reazione chimica. Considerando una reazione tra i reagenti A e B a dare il prodotto P: A + B → P* → P + hν
In pratica la reazione porta al prodotto P in uno stato eccitato ed il decadimento allo stato fondamentale non porta alla formazione di calore ma di un fotone (hν). È quindi necessario che i meccanismi di decadimento radiativo siano più competitivi rispetto a quelli non radiativi. Un esempio di reazione che porta a chemiluminescenza è quella del luminol con il perossido di idrogeno ed un catalizzatore metallico. Quando il fenomeno si verifica in sistemi biologici, ad esempio nelle lucciole, si parla di bioluminescenza. In questi casi le reazioni sono catalizzate da enzimi. La chemioluminescenza è utilizzata nei cosiddetti “lighstick”. Il lightstick, noto anche come starlight, cyalume, glowstick o più semplicemente luce chimica, è un cilindro di silicone, o altro materiale plastico morbido, auto-luminescente di dimensioni variabili da pochi cm a più di 30 cm. I componenti chimici principali di un lightstick sono acqua ossigenata, difenil ossalato (un estere dell'acido ossalico) e un pigmento fluorescente da cui dipende il colore: giallo, blu, verde, viola, rosso, arancione o bianco. Per accendere la luce è sufficiente piegare la bacchetta rompendo in questo modo la fiala contenuta al suo interno. Ciò fa mescolare i composti chimici e dà avvio alla reazione luminescente. Il meccanismo consiste nella reazione tra l'acqua ossigenata e l'estere che forniscono l'energia necessaria per eccitare gli elettroni del colorante fluorescente. Gli elettroni passano dal livello energetico fondamentale a quello eccitato e tornando al livello fondamentale emettono luce.
“Glowsticks” attivati
Sistema Theremino – Spettrometro_ITA – Pag. 84
Luce Chimica Blu
Spettro di chemioluminescenza blu La chemioluminescenza blu viene ottenuta dalla sostanza colorante fluorescente difenil antracene.
Luce Chimica Verde
Spettro di chemioluminescenza verde La chemioluminescenza verde viene ottenuta dalla sostanza colorante fluorescente bis(feniletinil) antracene. Questo composto aromatico presenta una forte fluorescenza e viene anche utilizzato nei componenti OLED. Luce Chimica Gialla
Spettro di chemioluminescenza gialla La chemioluminescenza gialla può venire ottenuta dalle sostanze coloranti fluorescenti cloro bis(feniletinil) antracene e tetrafenil naftacene.
Sistema Theremino – Spettrometro_ITA – Pag. 85
Luce Chimica Rosa
Spettro di chemioluminescenza rosa La chemioluminescenza rosa viene presumibilmente ottenuta miscelando le sostanze coloranti fluorescenti difenil antracene (blu) e violantrone (arancione). Luce Chimica Arancione
Spettro di chemioluminescenza arancione La chemioluminescenza arancione viene presumibilmente ottenuta dalla sostanza colorante fluorescente violantrone. Luce Chimica Rossa
Spettro di chemioluminescenza rossa La chemioluminescenza rossa viene probabilmente ottenuta da un derivato della sostanza colorante fluorescente violantrone.