Psoriasi, una complessa interazione...Psoriasi e Th17 Nelle lesioni psoriasiche si ha un notevole...
Transcript of Psoriasi, una complessa interazione...Psoriasi e Th17 Nelle lesioni psoriasiche si ha un notevole...
-
Psoriasi, una complessa interazione
tra segnali molecolari…………………
-
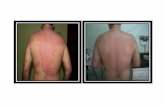
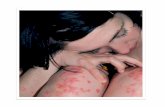
La PSORIASI è una malattia infiammatoria cronica della
cute, caratterizzata da una eccessiva proliferazione
associata ad una anomala differenziazione dei
cheratinociti dell’epidermide, proliferazione vascolare, infiltrazione leucocitaria del derma e dell’epidermide.
-
Risulta da una complessa e aberrante
relazione tra la cute ed il sistema
immunitario, su di uno sfondo di
predisposizione genetica e fattori
ambientali (epigenetica). Gli aspetti
clinici della psoriasi rispecchiano le
alterazioni della popolazione cellulare
residente della cute:
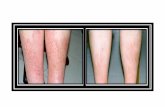
Desquamazione: anomala
maturazione dei cheratinociti
Ispessimento: rapida proliferazione
de cheratinociti
Arrossamento: proliferazione e
dilatazione vascolare cutanea
-
Le prime tappe consistono nel riconoscimento e
successiva captazione degli antigeni da parte
delle APC (antigen-presenting cells). Nella
psoriasi le APC più comuni sono le cellule
dendritiche che, solitamente, presentano
l’antigene associato alle HLA-2, che possono
essere riconosciute dalle cellule effettrici Th
(CD4).
Inoltre le cellule dendritiche possono anche
presentare l’antigene associato al sistema HLA-1
e stimolare le cellule T CD8. La cellule
dendritiche aumentano anche la produzione di
fattori di adesione molecole co-stimolatorie, per
facilitare l’interazione con le cellule T.
Sabal et al, Exp Dermatol 2007. 16: 779-798
Le cellule Th0 possono differenziarsi in Th1 o Th2 o Th17 o Treg, in base al tipo di citochine
presenti nel microambiente. Dopo l’attivazione le cellule T esprimono antigeni associati ai linfociti
cutanei (CLA) che dirigono i linfociti attivati verso la cute.
A questo contribuiscono anche le selettine P ed E espresse dalle cellule endoteliali.
-
Le selettine P ed E sono up regolate nella psoriasi. Le molecole più importanti per il
reclutamento nella psoriasi sono le ICAM-1 e le LAF-1.
A livello cutaneo le cellule T sono riattivate da diversi tipi di APC che comprendono
anche i cheratinociti. L’IFN-γ prodotto dalle APC ha un ruolo importante nella
riattivazione e proliferazione delle cellule T. Le cellule T della psoriasi presentano una
risposta aumentata e prolungata all’IFN-γ. Anche altre citochine prodotte dalle APC sono
importanti per la riattivazione: IL-6 e IL-23. Dopo la riattivazione le cellule T producono
varie altre citochine.
I Th17 e varie citochine prodotte dai macrofagi, dalle cellule dendritiche e dai
cheratinociti attivano i cheratinociti. I cheratinociti attivati proliferano producono
dei mediatori che promuovono ulteriormente il reclutamento di cellule infiammatore
e inducono l’angiogenesi, tutti fenomeni rilevanti per la patogenesi della psoriasi.
-
Le APC attivano i linfociti Th0 (naive) che, in base alle citochine che prevalgono nel microambiente sono spinti a differenziarsi in:a) Linfociti Th1 IFN-γ + Tbet+ (se nel pool citochinico prevale l’IL-12) oppureb) Linfociti Th17 IL-17+ RORγ+ (se ne pool citochinicoprevalgono IL-6, IL-1, TGF-β, IL-23a) STAT4 (attivato da IL-12) e STAT1 (attivato da IFN.γ) sono
necessari per la differenziazione dei Th1b) STAT3 (attivato da IL-6 e IL-23) sono necessari per la
differenziazione dei Th17
Il Dimetil fumarato (DMF) e l’aprenilast (PDE4i) modulano l’espressione delle citochine nelle cellule dendritiche attivate.Gli inibitori del segnale JAK (JAKi) contrasta il segnale citochinico. GSH=gutatione; NFkB= Nuclear Facto Kappa B; PDE4 (fosfodiesterasi tipo 4)
-
Psoriasi e Th17
Nelle lesioni psoriasiche si ha un notevole aumento dell’IL-23,
fattore che induce i Th17, prodotta dai cheratinociti, dalle cellule di
Langherans e dai macrofagi.
L’asse IL-23/IL-17 è molto attivo nelle lesioni psoriasiche.
L’IL-22 (induce acantosi) è rilasciata dai Th17 e, come l’IL-17, può
essere indotta dall’IL-23.
L’IL-6 da sola può indurre IL-22 ma non IL-17, l’addizionale presenza
di TGF-β, in modo dose-dipendente, inibisce l’espressione di IL-22,
mentre promuove la produzione di Il-17.
-
La psoriasi è una patologia immunitaria della cute che
dipende dai linfociti T helper. Quelli che producono
IL-17, IL-22, TNF-α sono le popolazioni cellulari
immunitarie chiave. Sono, infatti, proprio queste
cellule che orchestrano la reazione infiammatoria
della cute da cui parte la proliferazione dei
cheratinociti e delle cellule endoteliali.
Oltre ai Th17, altre cellule immunitarie capaci di
produrre IL-17 contribuiscono all’infiammazione
psoriasica.
L’importanza della citochina TNF-α è nota da tempo
ed è confermata dalla efficacia dell’anticorpo anti
TNF-α.
Un’altra citochina importante, per la sua potente
azione favorente IL-17/IL-22 è l’IL-23.
IL-23
I cheratinociti, nella psoriasi, sono caratterizzati da una abnorme tendenza alla
proliferazione e dalla alterata espressione di certe cheratine come la cheratina 16.
-
IL-15
IL-8
Sono alcune delle citochine riscontrate nelle
lesioni psoriasiche a promuovere la proliferazione
dei cheratinociti che, a loro volta sono produttori
di citochine, principalmente l’IL-8.
Epidermal IL-15Rα acts as an endogenous antagonist of psoriasiform inflammation in mouse and man.Bouchaud G, Gehrke S, Krieg C, Kolios A, HafnerJ, Navarini AA, French LE, Boyman O J Exp Med. 2013 Sep 23; 210(10):2105-17.
Anche l’IL-15 è importante in quanto protegge i
cheratinociti dall’apoptosi. L’IL-15Rα solubile
blocca l’infiammazione psoriasica sopprimendo
la secrezione di citochine da parte dei
cheratinociti e l’espansione delle cellule T
producendo IL-17.Identification of C5ades arg and an anionic neutrophil-activating peptide (ANAP) in psoriaticscales.Schröder JM, Christophers E J Invest Dermatol. 1986 Jul; 87(1):53-8.
Inoltre i cheratinociti sono la maggiore sorgente
di IL-1Inflammasome activators induce interleukin-1α secretion via distinct pathways with differential requirement for the protease function of caspase-1.Gross O, Yazdi AS, Thomas CJ, Masin M, Heinz LX, Guarda G, Quadroni M, Drexler SK, Tschopp JImmunity. 2012 Mar 23; 36(3):388-400.
IL-1
-
‘’Take Home message’’
Quindi, alterazioni genetiche ed
epigenetiche (fattori ambientali)
attivano delle risposte immunitarie
che alterano il turnover e le funzioni
dei cheratinociti, dando luogo alle
lesioni cutanee tipiche della
psoriasi.
-
E’ stato dimostrato che alterazioni genetiche ed epigenetiche del pool di fattori di trascrizione
dell’epidermide possono causare lesioni cutanee simili a quelle riscontrate clinicamente ed
istologicamente nella psoriasi. Topi con alterata espressione del JunB/B-Jun o fosforilazione del
fattore STAT3 sviluppano lesioni cutanee con caratteristiche e molecolari sovrapponibili a
quelle della psoriasi. Psoriasis-like skin disease and arthritis caused by inducible epidermal deletion of Jun proteins.Zenz R, Eferl R, Kenner L, Florin L, Hummerich L, Mehic D, Scheuch H, Angel P, Tschachler E, Wagner EF Nature. 2005 Sep 15; 437(7057):369-75.Stat3 links activated keratinocytes and immunocytes required for development of psoriasis in a novel transgenic mouse model.Sano S, Chan KS, Carbajal S, Clifford J, Peavey M, Kiguchi K, Itami S, Nickoloff BJ, DiGiovanni J Nat Med. 2005 Jan; 11(1):43-9.
-
Alcuni dei polimorfismi genici
associati alla psoriasi riguardano i geni
codificanti per:
IL23A,
IL23R,
STAT3, RUNX3,
TYK2.
Tutti questi geni sono associati alla
risposta immunitaria di tipo Th17
-
L’IL-23 stimola i Th17, il cui profilo citochinico comprende: IL-17, IL17F, IL-22, IL-21. IL-17 e
IL-17F mediano il danno tissutale mediante meccanismi che comprendono l’attivazione delle
metalloproteasi della matrice ed il reclutamento dei neutrofili. L’IL-22 induce infiammazione
della cute. L’IL-21 amplifica l’attivazione del fenotipo Th17. Il Th17 produce anche TNF-α. I
Th17 producono anche il GM-CSF. Alcune popolazioni di Th17 producono anche IL-9 e IL-10, in
funzione del tipo di segnale iniziale di attivazione che ricevono.
-
IL-6 IL-23
IL-21 IL-1
TGF-β Th17
La differenziazione e
l’attivazione dei Th17 dipende
dalle citochine IL-6, IL-1, IL-
21, IL-23, TGF-β
Generation of pathogenic T(H)17 cells in the absence of TGF-β signalling.Ghoreschi K, Laurence A, Yang XP, Tato CM, McGeachy MJ, Konkel JE, Ramos HL, Wei L, Davidson TS, Bouladoux N, Grainger JR, Chen Q, Kanno Y, Watford WT, Sun HW, Eberl G, Shevach EM, Belkaid Y, Cua DJ, Chen W, O'Shea JJNature. 2010 Oct 21; 467(7318):967-71.
IL-23, IL-23R e STAT3 sono
collegati alla predisposizione
genetica alla psoriasi.
Il fattore di trascrizione
STAT3 è anche attivato
dalIL-6 e dall’IL-21. STAT3,
insieme a RORγ è
responsabile
l’iperespressione di IL-17A
e IL-17F
Signal transduction pathways and transcriptionalregulation in Th17 cell differentiation.Hirahara K, Ghoreschi K, Laurence A, Yang XP, Kanno Y, O'Shea JJCytokine Growth Factor Rev. 2010 Dec; 21(6):425-34.
IL-21
IL-6STAT3
RORγ
IL-17AIL-17F