Predizione della struttura terziariam.docente.unife.it/matteo.ramazzotti/bioinfo/10... · Linee...
Transcript of Predizione della struttura terziariam.docente.unife.it/matteo.ramazzotti/bioinfo/10... · Linee...

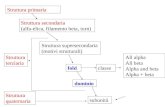
Predizione della struttura terziaria

Metodi di predizione
La predizione della struttura tridimensionale è di gran lunga la predizione più complessa che si possa fare su una proteina.
Esistono 3 metodi principali di predizione:
1 - Homology modelling:
se si conoscono proteine simili con struttura nota
2 - Fold recognition:
se si va alla ricerca di strutture simili, cercando il folding migliore
3 - Ab initio:
simulazioni di ripiegamento in silicio, molto complesse dato chesi valutano tutte le possibili interazioni di tutti gli atomi con il solvente

Confronto con banche dati di sequenze proteiche
Allineamento delle sequenze. C’è una proteina con struttura
nota?
Predizione della struttura secondaria
Homology modellingcon le coordinate delle
strutture note
Valutare l’accuratezza della predizione
Threading
Foding ab initio
Ricerca di motivi
Come approcciarsi al problema

Homology modelling
Assunzione di base : due proteine che presentano una identitàmaggiore del 30% circa, molto probabilmente derivano da un antenato comune e avranno una struttura simile.
Si va a valutare la
r.m.s.d. (root mean square distance)
cioè la distanza quadratica media tra gli atomi, generalmente i carboni α,
ma si può calcolare anche su tutti gli atomi.
Minore è il r.m.s.d. maggiore è la similarità strutturale
=> è stato osservato che proteine che condividono un’identità di sequenza del 50% mantengono circa il 90% dei residui in posizioni conservate

L’approccio al modelling per omologia è abbastanza intuitivo, ma è bene seguire delle considerazioni pratiche che possono essere definite
Linee guida per costruire un modello
1- Analizzare la struttura secondaria prima di quella tridimensionale, dato che se ci sono regioni fortemente disordinate, è bene escluderle dalla modellazione (sono, per definizione, non modellabili).
2 - Identificare in banca dati una proteina a struttura nota che abbia una alta identità (> 50%) con la propria, o identità globale o identità locale.
3 - Allineare al meglio le due proteine. Rifinire l’allineamento a mano, se necessario. Questa tappa è critica, perché la modellazione verràfatta sulle proteine allineate.
Homology modelling: procedura (1)

4 - Cercare in banca dati il più alto numero di proteine simili tra loro e identificare dopo il multiallineamento le regioni di struttura secondaria conservate (in genere se ci sono dal multiallineamento si vede).
5 - Costruire il pre-modello, utilizzando l’allineamento multiplo come guida per la “superimposizione” della struttura nota (stampo)
6 - Modellare le regioni altamente variabili (in genere i loop) che connettono regioni a struttura secondaria definita. Esistono database anche dei loop.
7 - Aggiustare le catene laterali modellandole su quelle dello stampo. Esistono anche delle librerie di ROTAMERI, cioè isomeri posizionali delle catene laterali con angoli di torsione adeguati alle torsioni del backbone.
Homology modelling: procedura (2)

7 – Risolvere, se possibile, i problemi relativi alle collisioni (clashes) dei vari atomi, o manualmente o con programmi che indicano l’energia minima delle strutture.
Alla fine gli atomi di una proteina non dovranno co llidere, e la proteina dovrà essere alla minor energia possib ile.
Nonostante ci siano delle regole abbastanza precise, l’homology modelling è molto complesso, richiede un
grande lavoro, molta esperienza e molto tempo.
E poi serve la verifica sperimentale !!!
Homology modelling: procedura (3)

Fold recognition (threading)
Il concetto che sta alla base di questa tecnica è:
le proteine presenti in natura hanno un numero finito di strutture possibili, o almeno un numero finito di topologie
(ad oggi 1233 secondo la banca dati CATH).
David Heisenberg nel 1991 sviluppò il metodo dei profili 1D-3D . Si tratta di catalogare tutti i FOLD possibili in termini di INTORNO per ogni aminoacido di ogni fold.
L’intorno è definito con:
1 - Struttura secondaria.2 - Accessibilità al solvente.3 - Tipo di residui circostanti (polari, apolari, idrofobici).
Ogni fold viene descritto come una sequenza (1D) di simboli associati a frequenze di ritrovamento in una data struttura.

E’ possibile così confrontare una sequenza proteica allineandola con tutti i possibili profili di tutti i fold conosciuti, ricavando un punteggio che valuti il best fitting della sequenza.
Facendo così si è in grado di identificare strutture di proteine anche molto divergenti tra loro, al punto di non essere riconosciute da nessun
programma di allineamento o di similarity search.
Un esempio tipico è l’individuazione della struttura di proteine che hanno la stessa funzione a causa di una evoluzione convergente :
originandosi da geni diversi non correlati, la sequenza sarà molto diversa, ma la struttura terziaria, almeno nell’intorno del sito catalitico, deve essere costante per garantire una stessa funzionalità.
Fold recognition (threading)

Metodo Rosetta
Messo a punto dal gruppo di David Baker nel 1997, non si basa sulle banche dati di fold di riferimento predeterminati, ma segue tre fasi empiriche con alta capacità predittiva:
1 - Divide la sequenza primaria in gruppi (da 3 a 9) residui, ed effettua una ricerca tra le proteine a struttura nota. Si generano così, per ogni frammento, una serie di strutture 3D possibili.
2 - Tutte le possibili combinazioni di strutture 3D locali vengono generate, e considerate inizialmente ugualmente possibili.
3 - Si applicano funzioni di scoring, di minima energia, di comparazione, per assegnare dei punteggi che indicano la qualità di ogni struttura.
Tra i sistemi di fold recognition, è quello che stabilm ente ottiene i migliori risultati al CASP.

CASP
E’ una “gara” tra i gruppi che sviluppano metodiche di predizione 3D e 2D che si basa sulla predizione delle strutture data una serie di sequenze proteica e basta .
Le predizioni migliori vengono valutate sulla base della loro somiglianza con le strutture 3D ottenute sperimentalmente ma tenute segrete fino al giorno delle presentazioni.
Vengono valutati separatamente i tre diversi modi di fare predizioni di struttura.
Il CASP permette di valutare quale è il miglior metodo per generare un modello, tenendo aggiornati tutti sui progressi dei vari gruppi di ricerca e garantendo così agli utenti finali di utilizzare la tecnica predittiva più aggiornata e più affidabile.
Inoltre, essendo una competizione a premi, stimola la ricerca e la continua innovazione alla ricerca del metodo predittivo migliore.
Critical Assessment of techniques for protein Structure Predictionhttp://predictioncenter.org/

Swiss-PDB Viewer
E’ molto più complesso e con una interfaccia meno immediata di RasMol, ma ha delle potenzialità enormi da un punto di vista di analisi, modellazione e rendering 3D delle proteine.
Vengono implementati svariati metodi per:
1 - Homology modeling2 - Structure alignment3 - Manual refining delle strutture4 - Calcolo delle energie minime5 - Introduzione delle mutazioni strutturali

Possiede 2 finestre di lavoro principali:
1 - Control panel : dal quale si guidano tutte le impostazioni grafiche di visualizzazione e di colorazione
2 - Graphic window : nella quale viene visualizzata la struttura della proteina
Swiss-PDB Viewer - interfaccia

Imparare come lavorare con il control panel è, per la parte di visualizzazione, la cosa più importante, dato che non è intuitivo.
su quale layer si sta lavorando
layer visibile e/o layer mobile
gruppo, inteso come residuo, quello corrente è in grassetto, quelli selezionati sono rossi. Nella colonna viene riportata la struttura secondaria ricavata elaborando il file PDB.
show: l’elemento selezionato è visibile.side: la sua catena laterale è visibile.labl: la sua etichetta (group) è visibile.
Swiss-PDB Viewer - interfaccia

controllo della superficie, che va prima calcolata:Van der Waals : una sfera punteggiataSuperficie molecolare : renderizzabileSuperficie accessibile : al solvente
Superficie di Van der Waals
Superficie molecolare
Superficie molecolare (rendered view)
Swiss-PDB Viewer - interfaccia

Molecola Superficie di Van der Waals
Superficie molecolare
Superficie accessibile
La superficie proteica non è un concetto unico: immaginando una sfera di raggio noto (il solvente, e.s. 1.4 Å) che rotola sulla superficie di Van derWaals della proteina, si può considerare l’insieme dei
- punti più bassi della sfera : superficie molecolare
- punti centrali della sfera: superficie accessibile
r = 1.4Å
La superficie della proteina

Ribn : controllo dei “nastri” (ribbons): il gruppo selezionato avrà il suo ribbon visibile, ma bisogna prima scegliere il tipo di visualizzazione da utilizzare. I triangoli neri verso il basso aprono menu a tendina.
Visualizzazioni : si configurano tutti i tipi di visualizzazione, definendo le proprietà per ognuno dei diversi tipi.
La configurazione delle visualizzazioni e il fatto che esse siano visibili oppure no non sono dipendenti nel control panel: questo permette di configurare tutto all’inizio e poi decidere cosa e come visualizzarlo.
Ogni tipo elemento può essere visualizzato contemporaneamente nella finestra grafica.
Swiss-PDB Viewer - interfaccia

La gestione dei colori è una cosa particolarmente importante e complicata in Swiss PDB Viewer: dato che molte cose possono essere visualizzate contemporaneamente, tramite la colonna colori (col) si impostano tutte una per volta.
Ogni residuo ha il suo colore, ma il colore che si sceglie èsubordinato alla struttura che ho selezionato prima con la scelta delle visualizzazioni.
Per selezionare tutta la colonna si usa il tasto destro del mouse oppure si trascina una selezione su tutta la colonna.
IMPORTANTE: se si seleziona un’altra visualizzazione, sarà visibile la colorazione per quella visualizzazione
soltanto. Tutte le altre, anche se non sono visibili, rimangono, però.
Swiss-PDB Viewer - interfaccia

Porta la proteina al centro, dovunque si
trovi
Lega il bottone sinistro del mouse alla traslazione della
proteina
Lega il bottone sinistro del mouse allo zoom
Lega il bottone sinistro del mouse alla rotazione della
proteina
Visualizza il testo nel file PDB
Swiss-PDB Viewer - interfaccia

Distanza tra due atomi
Angolo tra due atomi
Angoli diedri tra i legami dell’atomo
Etichetta
Seleziona atomi compresi in un raggio r dall’atomo selezionato e viene chiesto che tipo di selezione effettuare
Posiziona al centro
Mai capito
Le informazioni richieste vengono visualizzate sotto i bottoni
Swiss-PDB Viewer - interfaccia

Selezioni predefinite Colori predefiniti Personalizzazione
Swiss-PDB Viewer - interfaccia

La superficie molecolare e altre cose vanno calcolate prima di poterle usare (es. colorare)
Visto che il programma non è dedicato esclusivamente alla parte grafica, come RasMol, il rendering può essere acceso o spento per risparmiare risorse per il calcolo.
Per vedere i ribbons tridimensionali, le superfici ed altro, il rendering deve essere acceso a mano o con quegli acceleratori. Se il rendering è spento, solo la visualizzazione wireframe è disponibile, MA QUI NON SI CHIAMA WIREFRAME, perché le visualizzazioni non hanno un nome.
Swiss-PDB Viewer - interfaccia