Potenziale di membrana mc di membrana mc.pdf · •Campo Elettrico Energia chimica è l’energia...
-
Upload
vuongnguyet -
Category
Documents
-
view
223 -
download
0
Transcript of Potenziale di membrana mc di membrana mc.pdf · •Campo Elettrico Energia chimica è l’energia...
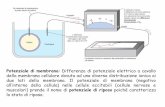
Genesi del Potenzialedi Membrana
In tutte le cellule è possibile misurare unadifferenza di potenziale a cavallo del plasmalemma
Forze agenti sugli ioni• Gradiente di Concentrazione• Campo Elettrico
Energia chimicaè l’energia contenuta in un
gradiente di concentrazione
Energia elettricaè l’energia dovuta alle cariche
in un campo elettrico
Cosa accade quando la membrana è permeabile solo ad uno ione?
elettroneutralità elettroneutralitànessuna differenza di potenziale
nessuna differenza di potenziale
elettroneutralità elettroneutralità
Cosa accade quando la membrana è permeabile solo ad uno ione?
un catione si muove dallazona ad alta a quella abassa concentrazione
Cosa accade quando la membrana è permeabile solo ad uno ione?
- voltaggio +eccesso di carica - eccesso di carica +
Su entrambi i lati lecariche non sono piùbilanciate
Cosa accade quando la membrana è permeabile solo ad uno ione?
- voltaggio +eccesso di carica - eccesso di carica +
l’eccesso di cariche + tende arespingere i cationi da questo lato
Cosa accade quando la membrana è permeabile solo ad uno ione?
- voltaggio +eccesso di carica - eccesso di carica +
viene raggiunto un equilibrio:
la forza dovuta al gradiente di concentrazioneuguaglia
la forza dovuta al gradiente elettrico
++
++
--
--
++++
++++
--------
K+Cl-100 mM
Na+Cl-100 mM
K+ K+K+ K+K+
ΔCΔE ΔCΔE ΔCΔE
0
GENESI DI UNPOTENZIALE D’EQUILIBRIO
All’equilibrio:flusso dovuto al gradiente di conentrazione = flusso dovuto al potenziale elettrico
Il potenziale di equilibrio può esserecalcolato dall’Equazione di Nernst
R= 8.3 J/mol oK =1.98 cal/mol oK (cost. dei gas)T = 293 oK (20 oC)z = +1 (per Na+, K+, H+ etc)z = -1 (per Cl-)z = +2 (per Ca2+ etc)F = 96,500 coulomb (costante di Faraday)
!!"
#$$%
&'=
2
110
][
][58
C
CLogmVE
!!"
#$$%
&'=
2
1
][
][ln
C
C
zF
RTE
----
----
++++
++++
K+K+
1 2
una cellula
Un esempio pratico
Supponendo che la membrana di unacellula sia permeabile solo al K+,calcolare il potenziale di membrana
!!"
#$$%
&'=
int
10][
][58
C
CLogmVE est
Un altro esempio
Supponendo che la membrana di unacellula sia permeabile solo al Na+,calcolare il potenziale di membrana
una cellula
!!"
#$$%
&'=
int
10][
][58
C
CLogmVE est
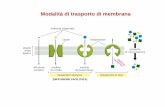
The Goldman-Hodgkin-KatzEquation
Tiene conto di più specie ioniche con i proprio coefficienti dipermeabilità
Il potenziale di membrana circa -70 mV
Molto vicino al potenziale di equilibrio del K+ (- 90 mV). Non lo raggiunge perché unapiccola quantità di Na+ fluisce all’interno della cellula rendendola meno negativa diquanto sarebbe se fosse completamente impermeabile al Na+.Ulteriore Na+ che fluisce all’interno viene pompato all’esterno dalla Na-K- ATPasi.Contemporaneamente il K+ viene pompato all’interno.
K+Cl-100 mM
Na+Cl-100 mM
1 2 1 2 1 2
K+
Na+
K+
Na+++
++
--
--
++++
+++
----
---
GENESI DI UNPOTENZIALE DI DIFFUSIONE
t1
t2
pK>pNa
fK>fNa fK=fNa
pK>pNa
Si genera quando la membrana è permeabile in misura diversa alle varie specie ioniche
Il suo raggiungimento comporta:Equilibrio elettrico ma squilibrio elettrochimicoFlusso netto non nullo delle varie specie ionicheUn potenziale di diffusione non si mantiene indefinitivamente
Potenziale di equilibrio:Le specie ioniche diffusibili sono all’equilibrio elettrochimico(vale l’equazione di Nernst)Il potenziale di membrana coincide con il potenziale diequilibrio di ciascuna specie ionica diffusibile (Vm=Ei)Il potenziale di equilibrio si mantiene indefinitamente
Potenziale di diffusione:Le specie ioniche diffusibili non sono all’equilibrioelettrochimico (non vale l’equazione di Nernst)Il potenziale di membrana non coincide con il potenziale diequilibrio di alcuna delle specie ioniche diffusibili (Vm≠Ei)Il potenziale di diffusione non si mantiene indefinitamente
Confronto tra potenziale d’equilibrio e di diffusione
RiassumendoIl potenziale di membrana è una conseguenza di unapermanente differenza di concentrazione ionica ai duecapi della membrana
Questa è prodotta da:• una membrana selettivamente permeabile (potenzialedi diffusione)• la presenza di specie ioniche non permeanti•un trasporto attivo degli ioni Na+ e K+
Cl-
Pr-
Na+