L'interfase è il periodo tra successive mitosi e consiste in tre fasi: G 1, S, e G 2. Durante la...
-
Upload
malvolio-antonucci -
Category
Documents
-
view
214 -
download
0
Transcript of L'interfase è il periodo tra successive mitosi e consiste in tre fasi: G 1, S, e G 2. Durante la...

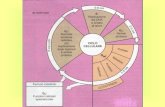
L'interfase è il periodo tra successive mitosi e consiste in tre fasi: G1, S, e G2. Durante la fase S (sintesi), le molecole di DNA di ogni cromosoma vengono replicate producendo un identico paio di molecole di DNA chiamate cromatidi (talvolta cromatidi "fratelli"). Ogni cromosoma replicato quindi entro in mitosi con due molecole identiche di DNA. Sottili filamenti di cromatina appaiono comunemente come materiale granulare amorfo nel nucleo colorato di cellule in interfase.

Prima e dopo la fase S vi sono due periodi di intensa attività metabolica, crescita e differenziamento, detti G1 (gap = intervallo 1) G2 (gap 2). Durante la fase G1 le cellule si preparano per la sintesi di DNA (fase S) e durante la G2 hanno luogo la crescita e l'espansione cellulare. Le cellule possono uscire dal ciclo cellulare in fase G1 ed entrare in uno stato di riposo, o G0. Le cellule in G0 non proliferano ma sono vitali e metabolicamente attive, e possono rientrare nel ciclo attraverso la fase G1. Una volta in G1 la cellula è obbligata a completare il ciclo.

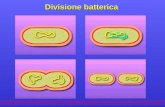
La fase M, o mitosi, comprende quattro tappe principali considerate in dettaglio più avanti: profase, metafase, anafase e telofase. La mitosi è di solito la fase più breve del ciclo cellulare, occupando 1 h del tempo totale di 18-24 h richiesto per il ciclo completo in una cellula animale ideale. Il tempo trascorso in ogni fase della mitosi varia notevolmente. La profase richiede molto più tempo delle altre; la metafase è la più breve.


Cyclin/cdk complexes are required at specific cell cycle transitions

G1 cyclins segnalano alla cellula di preparare i cromosomi per la replicazione S-phase promoting factor (SPF) preparano la cellula a entrare in fase S e duplicare il DNA* durante la sintesi di DNA la ciclina E si degrada e compaiono le cicline di fase M (mitotiche)M-phase promoting factor (MPF) inizia:- L’assemblaggio del fuso mitotico- Dissolvimento dell’involucro nucleare- Condensazionedei cromosomiInizia la metafase A questo punto MPF attiva il copmesso APC (Anaphase Promoting Complex)che permette:
1) la separazione dei cromatidi fratelli e la migrazione ai poli 2) la degradazione delle cicline mitotiche (M-phase)3) avvia la sintesi delle cicline della fase G1per il ciclo successivo 4) degradazione della geminina, una proteina che blocca la replicazione pre-mitotica del DNA sintetizzato in fase S. ,
E
B
A



Control of Cell Cycle• The cell cycle has checkpoints where feedback
information from the cell can trigger the next phase
• Proteins are responsible for the control through bonding to signal receptors.
• 3 checkpoints: G1 checkpoint- makes the decision as to whether the cell will divide. If conditions are favorable. Like the cell is healthy and large enough proteins will stimulate the cell to start the S Phase. The cell cycle can also be stopped or sent to a resting point, Ex. Muscle and nerve cells, at this checkpoint.

• G2 checkpoint- DNA replication is checked hear by DNA repair enzymes. If the DNA is copied correctly with no errors proteins then signal mitosis phase.
• Mitosis Checkpoint- Triggers the exit from mitosis phase.

• Cell Cycle Arrest
• DNA Repair
G1 Checkpoint

• Apoptosis
G1 Checkpoint


G1/S checkpoint
Arresto rapido della replicazione, dovuto alla degradazione della fosfatasi Cdc25A
la cui normale funzione e di defosforilare e così attivare la chinasi Cdk2 del complesso SMP, che a sua volta attiva la proteina Cdc45, che è essenaziale per l’assemblaggio del complesso di replicazione sull’origine di replicazione del DNA
Mediato dalle chinasi Chk1 e Chk2
Rapido e transiente Mantenimento prolungato
Danno prima dell’entrata in S

Il gene p53
Poco più del 50% dei tumori umani presenta mutazioni di questo gene. Nella maggior parte dei casi, le mutazioni inattivanti che colpiscono entrambi gli alleli p53 sono acquisite dalla cellula somatica. Meno frequentemente alcuni soggetti ereditano un allele p53 mutato (sindrome Li-Fraumeni) e possono sviluppare numerosi tipi di neoplasie quali:
1. Sarcomi;2. Carcinomi della mammella;3. Leucemie;4. Tumori cerebrali;5. Carcinomi della corticale del surrene.Rispetto alle forme sporadiche, le forme ereditarie si presentano in soggetti piùgiovani.La proteina p53 è localizzata nel nucleo ed entra in gioco come frenod’emergenza quando il DNA è danneggiato da radiazioni ionizzanti, raggi UV osostanze chimiche.

p21
Puma, Bax
Rilasco del citocromo c
apoptosi
Attivazione di p53 in risposta al danno del DNA
IR,UV, MMC.etposide,ROS
p53, inattivo e stabileGeni target on

p53 si lega al DNA e stimola la trascrizione di alcuni geni che mediano due funzioni fondamentali: l’arresto del ciclo cellulare e l’apoptosi.


Sono stati identificati studiando malattie rare come il retinoblastoma, che colpisce 1 bambino su 20.000.
60% = casi sporadici, un singolo tumore si sviluppa in un occhio nella prima infanzia.
40% = casi familiari con trasmissione autosomica dominante, tumori multipli si sviluppano nella retina di entrambi gli occhi nella prima settimana dalla nascita.
Affinché il retinoblastoma si sviluppi è necessario che entrambi gli alleli siano inattivi.

Prodotti proteici degli oncosoppressori.
1. Molecole che regolano la trascrizione nucleare ed il ciclo cellulare.
Il gene RbRb è stato il primo gene oncosoppressore scoperto. Il suo prodotto è una fosfoproteina nucleare, pRb, che nel suo stato attivo (IPOfosforilato) costituisce un freno al passaggio dalla fase G1 alla fase S del ciclo cellulare.

La forma attiva di pRb complessata ai fattori di trascrizione E2F si lega al DNA ed inibisce la trascrizione dei geni i cui prodotti sono necessari alla fase S del ciclo cellulare.
Quando i complessi ciclina D/CDK4,6 e ciclina E/CDK2 la inattivano IPERfosforilandola, rilascia i fattori E2F.
I fattori E2F formano eterodimeri con la famiglia di proteine DP ed attivano la trascrizione di diversi geni bersaglio
Quindi, se la proteina pRb è assente o alterata da mutazioni, la cellula progredisce verso la fase S senza alcun freno.


REGOLAZIONE DEL CICLO CELLULAREREGOLAZIONE DEL CICLO CELLULAREDA PARTEDA PARTE
DEI NUTRIENTIDEI NUTRIENTI

VitaminaVitamina A A


A/B C D E/F
Nuclear Hormone ReceptorSuperfamily
Steroid family Non-steroid family
ER ,
GR TR ,
RAR ,
PPAR ,
VDR RXR ,
PRAR
DBD
Type I family Type II family
Helix 12
AF1 LBD - AF2
CAR, SXR/PXR
MR
LXR ,, FXR

Conserved domains of transcription factors in nuclear-hormonereceptor superfamily
Fig 11.41 Lodish et al. Molecular Cell Biology
Two non-repeating C4 Zn finger motif
A/B C E
AF-2 domainAF-1 domain

Retinoid X Receptor (RXR)
E’ espresso in tutte le cellule
Regola numerosi processi eterodimerizzando con altri recettorinucleari (PPAR, VDR, LXR, FXR…….)
Il suo ligando naturale e’ l’acido 9 cis retinoico, …..altri ?

Diverse Structure of Ligands for Nuclear Receptors

Ligand Induces a Conformational Change in the LBD that Repositions helix 12
No Ligand Agonist

NR Antagonists Alter the Position of Helix 12
No Ligand Agonist(ER)
Antagonist(ER)


Consensus sequences of DNA response elements for differentnuclear hormone receptors
Fig 11.42 Lodish et al. Molecular Cell Biology
The glucocorticoid receptor and oestrogenreceptor bind to their respective response elements as homodimers. The response element is an inverted repeat
The vitamin D receptor, the thyroid hormone receptor and the retinoic acid receptor bind to their respective response elements as heterodimers (with RXR). The response element is an direct repeat. The spacing betweenthese repeats determines the specificity ofthe interaction.

RAR
A B C D E F
A/B dominio di transattivazione INDIPENDENTE dal ligandoC dominio che lega il DNAD cernieraE dominio che lega il ligando e dimerizzazioneF funzione non conosciuta

RAR-RXR AGGTCAnnnnnAGGTCA (DR5)
RXR-RXR AGGTCAnAGGTCA (DR1)
RARE
RXRE


Nuclear Hormone Receptor-Ligand Complex Action 2
DNA Response Element TATA Box
RNA polymerase IIor pol II complex
actually transcribes,starting at TATA box
DNA site
NH – receptorLigand Bound
LNH – receptorLigand Bound
L
Recruitment of Coactivators is NecessaryThey are an Obligate ‘Bridge’ to Pol II complex*
* Receptor-ligand can bind DNA and NOT recruit pol II = Antagonist


In tumori sensibili l’acido retinoico causa un arresto dellacrescita cellulare
cellule normali tumori sensibili t. resistenti
Trattamentocon + + -a.retinoico
TrasfezioneCon crescita crescita crescitaRAR inibita inibita inibita

RAR ha 2 sottotipi: RAReRAR
RAR funziona come un gene soppressore di tumore
RARcome un dominante negativo
Topi transgenici con poco RARo con moltoRARsviluppano tumori.
Quindi l’acido retinoico agisce come soppressore della crescitacellulare legandosi a RAR2, mentre elevati livelli di RAR4sopprimono questo effetto (tumori resistenti all’acido retinoico)

RETINOIDI e NEUROBLASTOMA
Retinoidi inducono differenziamento in cellule nervose
Nei neuroblastomi inducono apoptosi
DNA Microarray hanno dimostrato l’induzione di geniPro-apoptotici da parte di retinoidi

Estrazione dell’mRNA dai 2 campioni di cellule che si vogliono confrontare
Conversione in cDNA
Marcatura con 2 fluorocromi diversi
Riconoscimento tra i cDNA
Eccitazione della fluorescenza tramite laser
Immagine a colori raffigurante il microarray
provenienti dai 2 campioni e quelli già presenti sul microarray
(1)
(2)
(3)
(4) (5)
(6)
Confronto dei profili di espressione genica in due campioni cellulari diversi


L’Acido retinoico induce arresto della crescita cellulare oppure proliferazione a seconda del tipo cellulare (es. epidermide o epitelio tracheale).
Topi privati di vitamina A sviluppano molti tumori specialmente da epitelio tracheale.Trattamento con acido retinoico le blocca in G1:
Ac. Retinoico - +
ciclinaD1
mRNA

Ciclina D1 Ciclina D1
UbUb
Ub
Ub
Acidoretinoico
Degradazione e arresto in G1
Induzione dei geniAddetti alla Ubiquitinazione

EFFETTO ANTIPROLIFERATIVODELL’ACIDO RETINOICO SU
VARI TUMORI
Tumore ciclina repressa
Trachea D1Neuroblastoma D3Mieloide (U937) A, B, D2, D3, EEpatoma D1

VitaminaVitamina D D

Produzione della Vitamina D da UVB
• UVB (290-315 nm) converte 7-deidrocolesterolo in pre-vitamina D
• Previtamina D3 subisce una isomerizzazione che risulta nella formazione della vitamina D3 (25 idrossivitamina D (25(OH)D))
• Questa e’ convertita in 1,25-diidrossivitamina D3 (1,25(OH)2D3) nel fegato e nei reni


A/B C D E/F
Nuclear Hormone ReceptorSuperfamily
Steroid family Non-steroid family
ER ,
GR TR ,
RAR ,
PPAR ,
VDR RXR ,
PRAR
DBD
Type I family Type II family
Helix 12
AF1 LBD - AF2
CAR, SXR/PXR
MR
LXR ,, FXR

Diverse Structure of Ligands for Nuclear Receptors


Consensus sequences of DNA response elements for differentnuclear hormone receptors
Fig 11.42 Lodish et al. Molecular Cell Biology
The glucocorticoid receptor and oestrogenreceptor bind to their respective response elements as homodimers. The response element is an inverted repeat
The vitamin D receptor, the thyroid hormone receptor and the retinoic acid receptor bind to their respective response elements as heterodimers (with RXR). The response element is an direct repeat. The spacing betweenthese repeats determines the specificity ofthe interaction.

VDR+1
Gene Transcription
RNA Polymerase II
CYTOPLASM
NUCLEUS
VITAMIN D (V) RECEPTOR (VDR)ACTIVATION OF A VDR RESPONSIVE GENE
Hormone Regulated GeneVDRE
V
VDR
RXR
RXR VDR
V
V
V

La vitamina D causa un arresto della proliferazione cellulare e differenziamento in
cheratinocitiosteoblasticellule ematopoietiche
VDR e’ specialmente espresso nelle sopracitate cellule quando sono proliferanti

Crescita dopo trattamento con Vitamina DCellule di tumore prostatico Alva-31(linea cellulare)
50% 0%
Arresto in G1

La mortalita’ del tumore alla prostata aumenta con la diminuzione alla esposizione alla luce solare
I livelli di vitamina D circolanti diminuiscono con l’eta’
Alti livelli di sintesi di melanina correlano con un aumento dell’incidenza di tumori alla prostata
Crescita dopo trattamento con Vitamina DAlva-31(linea cellulare) Alva-31(linea cellulare)
+ VDR antisenso0% 100%

La forma attiva di pRb complessata ai fattori di trascrizione E2F si lega al DNA ed inibisce la trascrizione dei geni i cui prodotti sono necessari alla fase S del ciclo cellulare.
Quando i complessi ciclina D/CDK4,6 e ciclina E/CDK2 la inattivano IPERfosforilandola, rilascia i fattori E2F.
I fattori E2F formano eterodimeri con la famiglia di proteine DP ed attivano la trascrizione di diversi geni bersaglio
Quindi, se la proteina pRb è assente o alterata da mutazioni, la cellula progredisce verso la fase S senza alcun freno.

Vitamina D X
Induzione di p21
Rilascio di citocromo C
Repressione di geniAntiapoptotici



Promotore di p27 Gene Luciferasi




Vitamina D
p27 p27fosforilata
(proteina: piu’ stabile meno stabile)
Arresto in G1

Paracalcitolo (analogo della vitamina D)
HL60 (linea leucemica)
A concentrazione nanomolare riduce le cellule in fase SAumenta le cellule in fase G1Ha effetto pro-differenzianteAumenta il numero di cellule che vanno incontro ad apoptosi


or Vit D3
(geneOncosoppressore)
Trattamento con Vit D3 aumenta l’espressione della Tuberina



Attivita’ del promotore dip21

TGF-b e Vit D3 aumentano l’espressione della Tuberina, di p21 e diminuiscono la ciclina A





Cellule ERa+
Il trattamento con vitamina D induce i geni per:
Molecole di adesione
p53p21RetinoblastomaVarie caspasi
TGFb e il gene per il retinoblastoma sono indotti in tutti e due i tipi cellulari

Lo svantaggio maggiore per un suo impiego come farmaco antitumorale e’ la sua enorme influenza
sul metabolismo del calcio e dell’osso.