LEZIONE CARDIOCHIRURGIA 4/11/16: LA CIRCOLAZIONE … · pompato al paziente in una grossa arteria,...
Transcript of LEZIONE CARDIOCHIRURGIA 4/11/16: LA CIRCOLAZIONE … · pompato al paziente in una grossa arteria,...

LEZIONE CARDIOCHIRURGIA 4/11/16: LA CIRCOLAZIONE EXTRACORPOREA
Iniziamo a parlare della circolazione extracorporea. La maggior parte degli interventi di
cardiochirurgia avvengono in circolazione extracorporea cioè una macchina che consente di
escludere dalla circolazione sistemica il cuore e i polmoni in maniera tale che si ha un campo
esangue e quindi si può eseguire un intervento chirurgico sul cuore o sulle grosse arterie, perchè
in assenza di sangue. alla fine dell' intervento questa macchina di circolazione extracorporea
consente la ripresa dell' attività del cuore e quindi lo svezzamento della macchina di circolazione
extracorporea la quale fa parte di quel capitolo dei mezzi di assistenza meccanica del circolo.
Ora capite bene che la prima cosa che è importante per un paziente che entra in sala operatoria
è il suo monitoraggio, cioè noi dobbiamo avere tutta una serie di parametri vitali e monitorizzarli
in maniera continua e questi sono: l' elettrocardiogramma, la pressione arteriosa, la pressione
venosa centrale, l'emogas analisi, la temperatura corporea, la diuresi e in alcuni casi l'
elettroencefalogramma. L' elettrocardiogramma è in continuo ed è importante per monitorare
l' attività elettrica del cuore e tutte le sue variabili. La pressione arteriosa è importantissima per
avere idea della perfusione periferica degli organi e del post carico, cioè della pressione che si
sviluppa nelle arterie, la quale è naturalmente condizionata dal precarico, cioè dalla pressione
venosa centrale, che è indice del riempimento venoso del paziente. L'emogas analisi è un altro
punto fondamentale perchè ci da idea di come è ossigenato il sangue, oltre naturalmente al
valore del ph e alle altre variabili. la temperatura corporea in un soggetto che va a sottoporsi ad
un intervento di cardiochirurgia è altrettanto importante e il motivo vi sarà spiegato
successivamente. La diuresi è indice di perfusione degli organi addominali e quindi anche questa
deve essere monitorizzato di continuo. L' elettroencefalogramma serve a monitorare,
specialmente in alcuni casi, l' attività elettrica del cervello.
Come si monitorizzano questi vari parametri? l' elettrocardiogramma mettendo degli elettrodi
su entrambe le spalle dell' ammalato, la pressione arteriosa si monitorizza introducendo un ago
in genere nell' arteria radiale destra o sinistra o in entrambe o nelle arterie femorali e poi questo
ago viene collegato ad un trasduttore che manda su un monitor un segnale quindi noi sappiamo
in ogni momento sia la curva che i valori assoluti della pressione arteriosa. Altrettanto si
ottiene per la pressione venosa centrale che si monitorizza introducendo attraverso la vena
giugulare interna destra un catetere che poi andrà in cava superiore e in atrio di destra e quindi
va a monitorizzare la pressione atriale destra. L'emogas analisi si fa prelevando il sangue
arterioso (a volte anche venoso se si vogliono monitorare altri parametri) e si valutano la
pressione parziale d'ossigeno, di anidride carbonica, bicarbonati, lattati, ph, emoglobina,
ematocrito ed elettroliti semplici. Una delle cose piu complicate della monitorizzazione del
paziente è monitorare la temperatura del paziente, proprio perchè la temperatura varia a
seconda dei distretti in cui viene rilevata e varia in seguito alle modifiche che ci sono nella

circolazione extracorporea; in genere o viene monitorizzata la temperatura orofaringea
introducendo un elettrodo nell' orofaringe o viene monitorizzata la temperatura rettale
introducendo un catetere nel retto oppure può essere monitorizzata la temperatura urinaria
introducendo un particolare catetere vescicale collegato ad un elettrodo che misura la
temperatura dell' urina, indice della temperstura corporea. La diuresi viene monitorizzata
introducendo un catetere vescicale; essa è importantissima perchè è indice di una buone
perfusione del distretto splancnico. L'elettro encefalogramma è misurato con elettrodi posti sulla
fronte.
Vediamo più approfonditamente cos' è la circolazione extracorporea : è un sistema di assistenza
meccanica del circolo che consente di sostituire le funzioni del cuore e dei polmoni, cioè
consente di escludere dal circolo generale il cuore e i polmoni mantenendo in vita il paziente.
La strada che ha portato al miglioramento delle tecniche di circolazione extracorporea è molto
lunga e in effetti si fa risalire al 1916, quando fu scoperta l'eparina. Naturalmente quando si
sottopone il paziente a circolazione extracorporea, il suo sangue entra a contatto con superfici
estranee per cui si attiva la cascata della coagulazione quindi la prima cosa da fare è
anticoagulare il paziente in maniera completa e questo è possibile con l'uso dell'eparina.
Naturalmente alla fine dell' intervento questa attività anticoagulante dell' eparina deve essere
contrastata,annullata. Nel 1937 Chagraff scoprì la protamina, antagonista elettrico dell' eparina.
cioè la protamina si lega molecola per molecola interagendo elettricamente all' eparina,
annullandone l' azione in pochissimo tempo. Gli studi sperimentali sulla circolazione
extracorporea iniziarono nel 1937 da John e Mary Gibbon poi ci fu la seconda guerra mondiale
che portò molte innovazioni per la cardiochirurgia perchè per curare i feriti di guerra si apriva il
torace e si curavano ferite cardiache etc.. Gibbon riprese i suoi studi caratterizzati da esperimenti
risultati poi disastrosi su animali di laboratorio che morirono tutti. Per cui nel 1954 un altro
padre della cardiochirurgia, John Lillehei, che doveva operare un bambino cianotico affetto da
tetralogia di Fallot, visti i risultati catastrofici finora dati dall' utilizzo della macchina di
circolazione extracorporea, pensò di utilizzare uno dei due genitori, sicuramente compatibile
per gruppo sanguigno, come ossigenatore e come attività pompa per il piccolo e fece questa
circolazione crociata genitore‐figlio. Successivamente nel 1955 Kirklin modifica la macchina di
Gibbon e parte la cardiochirurgia con un enorme sviluppo da quegli anni ad oggi. [ Fa vedere una
slide, cioè una circolazione crociata di un arteria e una vena femorale di uno dei due genitori,
una pompa, con sangue arterioso immesso nella aorta del bambino e il sangue venoso prelevato
dall' atrio destro del piccolo.] Questo è uno dei pochi casi in medicina in cui il rischio operatorio è
del 150% perchè non solo moriva il bambino ma anche il genitore era in forte rischio. Ritornando
al discorso: la circolazione extracorporea da una parte sostituisce il cuore attraverso una pompa,
dall' altra i polmoni, la cui funzione principale è quella di estrarre anidride carbonica e immettere
ossigeno nel sangue per cui vengono vicariati da un ossigenatore. Quesi due elementi
fondamentali, ossigenatore e pompa, devono essere connessi al paziente attraverso un sistema
di cannule.
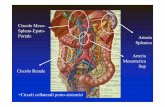
Il prof mostra uno schema di come avviene la circolazione extracorporea: il paziente è sul

tavolo operatorio, il sangue viene prelevato da una grossa vena, va nella macchina di circolazione
extracorporea. Raggiunge il reservoir, cioè un serbatoio dove viene raccolto il sangue venoso del
paziente; come vedete nella diapositiva il paziente sta più in alto della macchina perchè il sangue
venoso va dal paziente al reservoir per caduta.( Il reservoir oggi è un tutt'uno con l' ossigenatore
e lo scambiatore di calore.) Dal reservoir il sangue viene veicolato alla pompa, che spinge il
sangue all' ossigenatore ed allo scambiatore di calore, da qui poi il sangue ossigenato esce e
viene poi pompato al paziente. Naturalmente su questo circuito ci sono vari filtri. Viene quindi
pompato al paziente in una grossa arteria, in genere l' aorta. Il prof spiega che le altre linee
visibili nella slide sono gli aspiratori, perchè naturalmente c'è sangue quando si apre il paziente;
questi aspiratori aspirano il sangue che è naturalmente venoso tramite una pompa e lo veicolano
nel reservoir con un' altra pompa. quindi quali sono i componenti di un circuito di circolazione
extracorporeo? ossigenatore, pompa, scambiatore di calore, filtri, il sistema di cannule.
Il prof mostra a confronto una delle prime macchine di circolazione extracorporea risalente al
1953 e una macchina moderna.
Componenti del circuito di circolazione extracorporea ( ricordiamo che oggi è tutto monouso):
1‐ LE POMPE: la funzione della pompa è quello di sostituire la pompa del cuore, per cui di
muovere il flusso di sangue nel circuito e nel sistema vascolare dell'organismo. Tipi di pompa
attualmente in uso : 1) pompe a rulli 2) pompe a centrifuga
Pompa a rulli: c'è una parte fissa, lo STATORE circolare, e un ROTORE che gira dove ci sono due
rulli. Il rotore gira, e i rulli schiacciano un tubo di silastik ( chiamato SOTTOPOMPA) che si trova
tra i rulli e lo statore facendo progredire il liquido presente nel suddetto tubo dando un flusso
unidirezionale; è presente poi una manopola che serve a distanziare i rulli dallo statore perchè la
portata di questa pompa dipende da vari fattori: dimensioni tubo, viscosità liquido che vi scorre
dentro , occlusione (distanza tra uno dei due rulli e lo statore); tanto più il rullo è spinto verso lo
statore tanto più il tubo è occluso e tanto più il tubo è occluso tanto più la pompa è efficace però,
un' occlusione troppo spinta determina emolisi. Per cui la posizione di questi rulli deve essere
regolata in modo tale da dare una buona efficacia della pompa associata a un minimo grado di
emolisi. In base alla direzione di rotazione dei rulli si può determinare pompaggio o asopirazione
del sangue. Il flusso del sangue quindi dipende dalle dimensioni del tubo, dalla lunghezza dello
statore e dal numero di giri dei rulli. Quindi con questa pompa noi possiamo controllare uno
degli elementi più importanti della circolazione e cioè la portata cardiaca: aumentando o
diminuendo il numero di giri aumentiamo o diminuiamo la portata cardiaca. Il vantaggio di
questa pompa è che è abbastanza economica, lo svantaggio è che da emolisi quindi è utilizzata
per interventi cardiochirurgici brevi.
Pompe centrifughe: sono fatte a campana, al cui interno è presente una chiocciola che gira
grazie ad un magnete; la rotazione di questa chiocciola attraverso cui passa il sangue da al centro
una forza 0 mentre alla periferia una grossa forza, la forza centrifuga per cui il sangue scende
attraverso l'Outlet. Lo svantaggio di questa pompa è il prezzo, i vantaggi sono la mancata

formazione di emboli e soprattutto che c'è un traumatismo ematico quasi pari a zero, Per cui
pompe di questo tipo si utilizzano soprattuto quando la macchina di circolazione extracorporea
viene adoperata per giorni, mesi o anni.
OSSIGENATORE: il moderno ossigenatore è composto da reservoir, filtri, ossigenatore e
scambiatore di calore,il tutto in un unico sistema. Ci sono due tipi di ossigenatore: 1) esposizione
diretta (a gorgogliamento) 2) esposizione indiretta (a membrana e/o fibre cave)
Ossigenatore a Esposizione diretta: i gas a contatto con le proteine del sangue producono
schiuma così come si produce schiuma nell' edema polmonare. (caratterizzato da fuoriuscita di
schiuma dalla bocca dovuta ad un aumento della pressione idrostatica nei capillari alveolari
con fuoriuscita di proteine e formazione di schiuma a contatto con l'aria)In tal caso si ha contatto
tra l'aria e le proteine del sangue con formazione di microbolle; le microbolle che si formano
cedono ossigeno e prendono anidride carbonica per cui i globuli rossi vengono ossigenati.
Questo tipo di ossigenatore non si usa più perchè ha una cospicua emolisi e un' embolia
gassosa notevole, inoltre provoca denaturazione delle proteine plasmatiche.
Esposizione indiretta: in questi ossigenatori, data la presenza della membrana, non vi è contatto
diretto tra sangue e gas, i quali sono da un lato e dall' altro della membrana e tramite questa
scambiano O2 e CO2, proprio come avviene a livello alveolare. Questi vengono utilizzati molto
spesso visti i numerosi vantaggi che hanno rispetto ai precedenti. in primis un ridotto volume di
priming(liquido per riempire il circuito), un trasferimento ottimale dei gas, una maggiore
efficienza dello scambiatore di calore, alta affidabilità, minore traumatismo sulla parte
corpuscolata del sangue e ridotta formazione di emboli gassosi.
SCAMBIATORE DI CALORE: serve sia a mantenere la normotermia (37°C) o a raffreddare o
riscaldare il sangue del paziente. Sono caratterizzati da una parte in cui circola acqua calda o
fredda e dall' altra in cui circola il sangue del paziente.
FILTRI: devono localizzarsi nel circuito di circolazione extracorporea a diversi livelli; devono stare
sulla linea venosa, specialmente su quella degli aspiratori che aspirano sangue da torace,dal
mediastino; sulla linea dell' ossigenatore perchè noi abbiamo parlato di pompe a rulli con tubo di
silastik che col passare delle ore può perdere elementi di plastica per cui è necessario un
filtraggio.
CANNULE: per collegare il paziente alla macchina si utilizzano le cannule, che si inseriscono in
una grossa arteria o in una grossa vena e tubi che collegano le cannule alla macchina, fatti
entrambi di materiale plastico biocompatible.
Processo di incannulazione: il principio fondamentale per incannulare è scegliere una grossa
vena da cui prendere il sangue , in genere si preferisce l' atrio di destra. Si incannula o solo la
cava inferiore o entrambe, superiore ed inferiore. In altri casi può essere incannulata la vena
femorale o per doppia incannulazione sia la vena femorale che l' atrio destro. Il sangue per
caduta va alla maccchina. Naturalmente questo sangue viene drenato dalla macchina, viene

ossigenato, e quindi, divenuto sangue arterioso, viene reimmesso nel paziente, incannulando, in
genere, l'aorta ascendente che è il più grosso vaso, nonchè il più prossimale, da cui il sangue può
raggiungere tutti gli altri distretti arteriosi. In alcuni particolari casi può essere incannulata l'
arteria femorale. Riepiloghiamo i siti di di incannulazione più frequenti: atrio destro e cava
inferiore ( in linea di massima la portata di questo drenaggio venoso è tale da consentire l'
esecuzione di un intervento con circolazione extra corporea, però qualora dovessimo eseguire un
intervento sull' atrio destro per cui dobbiamo aprire l'atrio di destra, dobbiamo drenare l'atrio in
questione, utilizziamo un'incannulazione della vena cava superiore e di quella inferiore. In caso
di circolazione extracorporea parziale il sangue, oltre a fluire nelle cannule, passa in parte anche
nel cuore destro. Quindi quando usiamo questo tipo di circolazione andiamo sempre in bypass
parziale, ciò avviene quando non si fanno passare i lacci intorno alle cave. Se invece noi
occludiamo le cave intorno alle cannule con dei lacci tutto il sangue del corpo passerà nella
macchina per cui avremo una condizione di bypass cardiopolmonare totale (utilizzato in apertura
di atrio di destra). L' incannulazione venosa consente di drenare il sangue dal paziente,
sangue che, dopo essere stato ossigenato dalla macchina, deve essere rimpompato nel paziente.
Come? Si incannula l' aorta, in particolare la parte distale dell' aorta ascendente prima
dell'emergenza dei tronchi sovraaortici (tronco anonimo,carotide di sinistra e succlavia di sinistra)
in maniera tale da avere lo spazio per chiudere la parte prossimale (più vicina al cuore) dell'
aorta, applicando un angiostato che va a chiudere l' aorta ascendente prossimalmente all'
impianto della cannula; la circolazione nel resto del corpo è così assicurata dalla cannula e noi
abbiamo lo spazio per operare, quindi escludiamo il cuore e naturalmente i polmoni dalla
circolazione sistemica. Arrivati a questo punto l' anestesista deve staccare il respiratore perchè
altrimenti insuffla i polmoni inutilmente.
Priming: al momento dell' inizio della circolazione extracorporea se io apro gli angiostati e
faccio drenare il sangue dal paziente nella macchina e dico al tecnico di pompare, cosa pompa?
Aria, perche tutto il circuito è riempito di aria, e ciò non è possibile.Per cui si deve riempire il
circuito di qualche liquido. All' inizio si pensava che avendo sottratto sangue al paziente fosse
necessario reinserire sangue dello stesso gruppo omologo. Il riempimento della macchina si
chiama priming, e in tal caso si trattava di priming ematico; il concetto di fondo era che
bisognava aumentare il trasporto di ossigeno al paziente, per cui basandosi sul dato che un
aumento di emoglobina si traduce in un miglioramento del trasporto di ossigeno, si pensava che
aggiungendo sangue aumentasse anche il trasporto di ossigeno. Si vedeva però che questi
pazienti avevano una serie di complicanze: polmone da shock, insufficienza renale, embolia
cerebrale, nonchè infezioni enormi e non si riusciva a capire il perchè.
Negli USA Curey, un altro padre della cardiochirurgia, si trovò a dover operare un testimone di
Geova. Dopo aver fatto firmare al paziente una carta, in cui lo stesso affermava di non volere
sangue, Curey pensò di inserire soluzione fisiologica nella macchina di circolazione
extracorporea. Il paziente non solo sopravvisse, ma non ebbe nemmeno le solite complicanze,
perciò si definì per la prima volta quella che oggi è definita sindrome del sangue omologo
dovuta al fatto che l' aumento dell' ematocrito è vero che determina un aumento netto dei livelli
dell' emoglobina con conseguente aumento della capacità di trasporto dell'ossigeno, ma al

contempo determina aumento della viscosità del sangue per cui, a livello del microcircolo, i
globuli rossi si impilano uno dietro l' altro,e si ha quindi trombosi renale, polmonare e cerebrale,
nonchè il sintomo tipico noto come “shock lungs” o “white lungs” (polmoni da shock o bianchi) e
morte del paziente. Da questo momento in poi cominciarono a cambiare le modalità,
passando dapprima alla emodiluizione parziale, con aggiunta di una parte di soluzione fisiologica
associata ad una parte di sangue, finchè non si convinsero persino i più “conservatori” e si
passò ell'emodiluizione totale, riempendo la macchina solo con soluzione fisiologica( oggi se ne
inseriscono 1,2 litri, in passato 2 litrozzi) . È vero che in questo modo si riducono sia l'
emoglobina che l' ematocrito del 18/20% però al contempo si riduce la viscosità del sangue e
migliora la perfusione del letto capillare. Naturalmente diminuirono anche le infezioni (epatiti,
AIDS). Al giorno d'oggi il priming si fa con soluzione fisiologica con aggiunta di eparina.
Quindi in sunto elenchiamo vantaggi e svantaggi dell'emodiluizione totale.
Vantaggi:
‐risparmio di sangue
‐prevenzione di eventuali reazioni da sangue omologo
‐migliorata microcircolazione per riduzione della viscosità del sangue, mantenimento della
diuresi a valori alti
Svantaggi: ‐ acidosi transitoria
Ovviamente, come è stato anticipato, c'è l' assoluta necessità che il paziente sia anticoagulato
tramite l' inserimento in aorta ascendente (per essere sicuri) di una dose di eparina. In caso
contrario si ha coagulazione intravascolare passiva.
Ho detto all' inizio che è importantissimo monitorizzare la temperatura del paziente. Noi
sfruttiamo il principio che l' attività metabolica raddoppia o si dimezza per ogni 10 gradi in più
o meno di temperatura corporea, perchè naturalmente se riscaldiamo, i processi enzimatici
avvengono più velocemente mentre se raffreddiamo avvengono più lentamente, per cui
raffreddando il paziente il consumo di ossigeno da parte degli organi è minore.
In particolare vediamo che a 33°C si ha perdita di coscienza, a 30°C si ha poichilotermia, a 28 °C
si ha fibrillazione atriale, a 25 °C si ha fibrillazione ventricolare e al di sotto dei 25°C, non si sa
perchè con valori variabili nei diversi individui, si ha perdita di riflessi del tronco encefalico
(perdita dell'attività cerebrale). Come abbiamo detto prima, per regolare la temperatura del
paziente utilizziamo uno scambiatore di calore, o per mantenere la normotermia e per
raffreddare o riscaldare il paziente. Quindi noi definiamo normotermia le temperature tra
36‐37°C, ipotermia moderata tra 32‐28 °C, ipotermia intermedia tra 28‐20°C e ipotermia
profonda una temperatura minore o uguale a 20°C. Ricordiamo che ponendo un angiostato
nell'aorta ascendente noi escludiamo il cuore dalla circolazione, come conseguenza di ciò non
circola più sangue nelle coronarie e il cuore va in arresto anossico, che in passato causava dei

piccoli problemi e nel migliore dei casi permetteva al paziente di sopravvivere con l'aorta
chiusa solo 15 minuti perchè causava alterazioni dei mitocondri e delle cellule cardiache tali
che si avevano dei grossi danni. La cosa più terribile che succedeva era il cosiddetto “cuore di
pietra” . Le cellule cardiache si contraevano in maniera spasmodica ,il cuore diveniva di pietra e
la situazione diveniva irreversibile. Succedeva quello che succede all' impiccato(che va in anossia
e muore). Nel corso degli anni si arrivò al concetto di arresto cardioplegico, ovvero una plegia
coronarica e una plegia cardiaca indotta farmacologicamente. Il componente fondamentale di
questa soluzione farmacologica è il potassio; alte concentrazioni di potassio iniettate
direttamente nelle coronarie danno arresto cardioplegico. Il cuore viene arrestato in diastole,
quindi con un minimo insulto di ossigeno, si ha una abolizione del lavoro elettromeccanico del
cuore, una riduzione enorme della richiesta energetica da parte del cuore. Oggi con l' arresto
cardioplegico si può arrivare a stare col cuore fermo anche per 2‐3 ore e poi il cuore riprende a
funzionare. La soluzione contenente potassio può essere cristalloide o ematica per cui possiamo
avere arresto cardioplegico cristalloide o ematico. Come si somministra questa soluzione? Se non
c'è insufficienza valvolare aortica (perchè in tal caso incannulando il bulbo aortico il sangue non
fluirebbe nelle coronarie ma tornerebbe nel ventricolo) e se noi non dobbiamo aprire l'aorta
ascendente , questa soluzione può essere iniettata per via anterograda, direttamente nel bulbo
dell'aorta( foriamo l'aorta ascendente e iniettiamo questa soluzione che non può andare in
direzione distale perchè c'è l' angiostato e non può andare in direzione prossimale perchè c'è la
valvola aortica e quindi va nelle coronarie, oppure nel caso in cui dobbiamo aprire l' aorta
ascendente si incannulano direttamente le arterie coronariche con degli osti coronarici e la
soluzione fisiologica viene iniettata direttamente negli osti per via anterograda); in altri casi se
noi abbiamouna stenosi della coronaria destra associata ad una stenosi prossimale della
coronaria sinistra, iniettando una soluzione cardioplegica per via anterograda questa non
raggiunge le coronarie o le raggiunge in maniera molto lenta. Quindi noi somministriamo la
cardioplegia per via retrograda, incannulando il seno coronarico.
Invece se dobbiamo andare ad operare sull' arco aortico andiamo in ipotermia profonda
associata ad arresto di circolo ed esanguinamento totale del paziente . Cioè andiamo in
circolazione extracorporea; in questo caso, in genere, viene incannulata l' arteria femorale o l'
arteria ascellare destra. Andiamo in ipotermia profonda, al di sotto dei 26 °C; raggiunta questa
temperatura si ferma la macchina di circolazione extracorporea,tutto il sangue del paziente viene
drenato e messo nella macchina di circolazione extracorporea, quindi si apre l'aorta e si opera
sull'arco aortico. Perche si va in ipotermia profonda? Per quanto detto prima, e cioè che
riducendo di 10°C la temperatura si riduce anche l'attività metabolica nonchè il consumo di
ossigeno e arrivati verso i 20°C si ha anche un arresto dell'attività cerebrale, per cui è
preferibile indurre ipotermia profonda nel paziente ed eseguire molto rapidamente l'intervento
nella speranza che non sopraggiungano danni cerebrali; infatti in genere questo tipo di
protezione è valida per 20‐25 minuti,quando l'elettroencefalogramma è piatto.
[In passato una tecnica che si adoperava per operare i bambini co nsisteva nel metterli in
circolazione extracorporea,ricoprirli di ghiaccio al fine di raggiungere la temperatura desiderata,

per poi riscaldarli nuovamente con delle coperte al termine dell'intervento.]
Come si ottiene la protezione cerebrale? Fino al 1994 si otteneva tramite ipotermia profonda
con arresto di circolo (DHCA) [descritta precedentemente]. Poi è stata inventata la tecnica di
retroperfusione cerebrale, utilizzata fino al 1997 , che consisteva nell'inserire una cannula nella
cava superiore e nel perfondere il cervello per via retrograda attraverso la cava superiore.
Al giorno d' oggi si utilizza la tecnica di perfusione anterograda selettiva, che consiste nell'
indurre ipotermia (non ipotermia profonda ma intorno ai 26°C) , si apre l' aorta e si espongono i
tronchi sopraortici, si mette una cannula nel tronco anonimo e un'altra nella carotide di sinistra e
si perfonde il cervello, naturalmente a un flusso basso perchè se andasse a flussi pieni
scoppierebbe il cervello . Per perfondere gli altri organi addominali si mette una cannula nell'
aorta toracica discendente. Finito l'intervento sull'arco aortico, si tolgono le cannule di
perfusione cerebrale e il perfusionista riimmette sangue nel paziente. Se ho incannulato l'arteria
femorale il perfusionista riperfonde il paziente dal basso, se ho incannulato l'arteria ascellare di
destra posso risparmiare una delle due cannule di perfusione cerebrale. Perchè? Perchè quando
sono andato in arresto, ho esanguinato il paziente e ho aperto l'aorta ascendente, posso
chiudere il tronco anonimo e mettere una sola cannula di perfusione cerebrale nella carotide
di sinistra, perchè se ho incannulato l'arteria ascellare di destra, questa va al tronco anonimo ma
il sangue non può circolare nel tronco anonimo che è chiuso, per cui va sopra alla carotide di
destra.
Durante la circolazione extracorporea noi abbiamo il controllo su diverse variabili dell' organismo,
e possono essere variabili a controllo esterno, variabili a controllo misto (esterno e del paziente)
oppure sono variabili incontrollabili come la reazione infiammatoria sistemica, perchè
naturalmente la circolazione extracorporea è una cosa estremamente antifisiologica, uno stato di
shock perenne. Pensate che cambia persino la curva pressoria, che di norma è pulsatile mentre
in questo caso si annulla. Abbiamo un flusso laminare per cui la pressione è piatta e non c'è più
l'onda pressoria; in più ci sono tutti i materiali che noi insieriamo nel corpo, gli eventuali detriti
della macchina cui l' organismo può reagire con un' eventuale reazione infiammatoria.
variabili a controllo esterno: 1) GITTATA CARDIACA, dato che noi possiamo regolare la portata
cardiaca aumentando o diminuendo il numero di giri o della pompa a rullo o della pompa
centrifuga; 2) LA PRESSIONE VENOSA CENTRALE, il cui controllo ci può, in seguito alla valutazione
di quanto sangue sia presente nel resevoir, consentire di procedere a flussi pieni aumentando il
numero di giri del rotore (finchè c'è sangue nel reservoir) o a flussi progressivamente ridotti
fino a chiudere la linea venosa, quindi quella arteriosa e a far camminare il cuore di per sè; 3) LA
PRESSIONE POLMONARE; 4) EMATOCRITO( lo possiamo variare come vogliamo noi, dipende
dall'acqua che ci diamo) E COMPOSIZIONE CHIMICA DEL LIQUIDO DI PERFUSIONE 5) PO2 E PCO2
6) EQUILIBRIO ACIDO‐BASE 7) TEMPERATURA CORPOREA
La difficoltà principale nel controllo di questa macchina consiste proprio nel monitoraggio
attento di tutte queste variabili.

Domanda: “Quando si adopera la via retrograda ?” Il prof risponde: “ La via anterograda si
effettua incannulando il bulbo aortico o direttamente gli osti coronarici (nei casi di insufficienza
valvolare aortica) mentre quella retrograda si effettua incannulando il seno coronarico, da cui il
sangue fluisce nelle vene coronariche, quindi nelle arterie coronariche e nel bulbo dell'aorta.”
Un'altra componente importante sono gli ASPIRATORI, specialmente quando si sta in bypass
cardiopolmonare parziale, condizione nella quale una parte del sangue va al cuore, per cui è
necessario inserire nel cuore delle linee di aspirazione ( in aorta ascendente o in arteria
polmonare, atrio sinistro, atrio destro e così via) che aspirano via il sangue.
Quando studierete i mezzi di assistenza meccanica del circolo, vi renderete conto di come la
macchina di circolazione extracorporea sia il più completo dei mezzi di assistenza meccanica
perchè sostituisce la funzione di cuore e di polmoni, però può essere usata solo per ampi
interventi chirurgici perchè implica che il paziente sia lasciato col torace aperto per tutta la
durata dell'intervento. Per cui v'è tutta una serie di altri mezzi di assistenza meccanica del circolo
che vanno a sostituire alcuni solo la funzione di pompa cardiaca, altri tanto quella di pompa
cardiaca quanto quella polmonare. Quindi possiamo dire che la macchina di circolazione
extracorporea fa parte dei mezzi di assistenza meccanica del circolo temporanei.

CHIRURGIA CARDIACA Prof. Nappi 16/11/2016
Il tronco comune dell'arteria coronarica sinistra origina dall'aorta ascendente in corrispondenza
del seno aortico di Valsalva sinistro, in posizione più craniale rispetto all'origine della arteria
coronarica destra. Presenta un calibro maggiore della coronaria destra (diametro tra 3 e 6 mm) e
può avere una lunghezza di 10‐15 mm. Dopo la sua origine decorre dietro al tronco polmonare
dirigendosi in avanti fino a raggiungere il solco interventricolare anteriore dove, nei 2/3 dei
soggetti si divide in:
a. Ramo interventricolare anteriore o discendente anteriore.
b. Ramo circonflesso.
Raramente il tronco comune è assente : in tal caso l’arteria discendente anteriore e l’arteria
circonflessa originano da osti separati del seno di Valsalva sinistro.
a. L'Arteria Discendente Anteriore (Left Anterior Descending, LAD) discende nel solco
interventricolare anteriore e, in circa l'80% dei pazienti, circonda l'apice del ventricolo
sinistro e risale per un breve tratto nel solco interventricolare posteriore terminando sulla
superficie diaframmatica del ventricolo sinistro.
Nel 20% dei casi l'arteria discendente anteriore non raggiunge, invece, la superficie
diaframmatica e termina a livello dell'apice cardiaco o prima.
In quest'ultima evenienza, l’arteria discendente posteriore (Posterior Descending Artery,
PDA) dell'arteria coronarica destra è più larga e più lunga del normale e rifornisce la
porzione apicale del ventricolo sinistro. Dall'arteria discendente anteriore originano rami
per il versante anteriore dei due ventricoli e per i 2/3 anteriori del setto interventricolare.
In particolare, da essa emergono:
Rami diagonali
Rami settali o perforanti.
I rami diagonali vascolarizzano la parete laterale del ventricolo sinistro ed il muscolo
papillare antero‐mediale della valvola mitrale. Il numero ed il decorso dei rami diagonali è
variabile: nella maggior parte dei casi sono presenti almeno tre rami diagonali.
I rami settali o perforanti vascolarizzano i 2/3 della parte anteriore e mediale del setto
interventricolare ma irrorano anche il nodo atrio‐ventricolare e il fascio atrio‐ventricolare.
Essi nascono ad angolo retto dalla porzione ventricolare dell'arteria discendente anteriore.
Hanno un calibro inferiore rispetto ai rami diagonali e differiscono per dimensioni, numero
e distribuzione: nella maggior parte dei soggetti esistono almeno tre rami perforanti. In
alcuni casi vi e un primo grosso ramo orientato verticalmente, il quale si divide in un certo
numero di rami secondari a ramificazione obliqua che decorrono lungo il setto. In altri casi
è presente un primo grande ramo settale orientato più orizzontalmente che decorre
parallelamente alla stessa arteria discendente anteriore. In altri casi ancora, un certo
numero di arterie settali, paragonabili tra loro per dimensioni, si interdigitano con altre

simili che
una rete d
Il ramo cir
seconda d
sinistra in
del ventric
solco inter
casi fornisc
sinistro, pr
ed il musco
e l’arteria d
originano i
i canali colla
rconflesso
ella domina
rapporto co
colo sinistro
rventricolar
ce un ramo
rosegue fino
olo papillar
discendente
n alto dal
aterali.
più piccolo
anza anato
on la vena c
o e rami ma
re posterior
per il nodo
o alla crux
e postero‐la
e posteriore
ramo disce
o ,ramo int
mica) deco
cardiaca ma
rginali per
re, anastom
o del seno e
e fornisce u
aterale dell
e.
endente po
erventricola
rre postero
agna. Da ess
il margine o
mizzandosi c
e, nel caso i
uno o più ra
a valvola m
steriore de
are anterio
olateralmen
so emergon
ottuso. Term
con l'arteria
n cui la dom
ami postero
mitrale, l'arte
ella coronar
ore, (diamet
nte nel solc
no rami per
mina, per lo
a coronaric
minanza cor
o‐laterali pe
eria per il n
ria destra p
tro tra 3.4
o atrio‐ven
l'atrio sinis
o più, in pro
ca destra. N
ronaria sia d
er il ventric
nodo atrio‐v
producendo
e 4.2 mm
tricolare di
tro, la base
ossimità del
Nel 45% dei
del sistema
olo sinistro
ventricolare
o
m
i
e
l
i
a
o
e

L’ arteria
solco atri
irrorare la
margine a
intervent
Si parla
coronaria
data dalla
irrorare l
sinistro e
destra è d
atrio vent
ARTERIE
Arteria
Interventri
anteriore
discendent
(arteria
sinistra)
Arteria
(arteria
coronarica
ioventricola
a parete lib
acuto con l
ricolare pos
di domina
a di destra (
a circonfles
a parete an
il terzo infe
dominante
tricolare (in
icolare
o Arteria
te anterior
coronaria
Circonflessa
coronaria
a di destra,
are destro
era del ven
l’arteria cor
steriore.
anza destr
(e avviene
sa si parla
nteriore lib
eriore del s
ed irrora il
n caso di dom
PORZIO
a
re
a
i. ii. iii.
iv.
a
a
i. ii. iii.
, invece, or
e dà le art
ntricolo di d
ronarica de
a quando
nel 70% de
invece di d
era del ven
etto interve
muscolo pa
minanza sin
ONI DEL CU
2/3 antPareteMuscomitraliLa pare
PareteMuscoMusco
igina dal se
terie del m
estro. Nell’
estra che ne
l’intervent
ei casi), qua
ominanza s
ntricolo di
entricolare.
apillare post
nistra quest
ORE IRRORA
teriori del s anterolatelo papillarca ete anterior
posteriore lo papillarelo papillare
eno di Valsa
argine acut
aspetto po
ella maggio
tricolare po
ndo l’arter
sinistra.Qui
destra, la p
.Nella magg
tero medial
i rami sono
ATE
setto interverale del vene anterolat
re apicale d
laterale dee anterolatee posterom
alva di dest
to del cuor
osteriore de
or parte dei
osteriore è
ia intervent
indi la coro
parete post
gior parte d
e, il nodo s
o forniti dall
entricolare ntricolo siniterale dell
el ventricol
el ventricoloerale della mmediale dell
tra e si port
re che vann
el cuore si v
i casi dà l’a
è fornita d
tricolare po
onaria di de
teriore del
ei casi la co
eno atriale
a circonfles
stro a valvola
o destro
o sinistro mitralica la valvola
ta nel
no ad
vede il
arteria
dall’arteria
osteriore è
estra va ad
ventricolo
oronaria di
ed il nodo
ssa).

CARDIOPATIA ISCHEMICA
La Ucardiopatia ischemicaU interviene quando viene alterato il rapporto tra apporto e richiesta di
ossigeno.
Quali sono i fattori che a livello coronarico possono alterare l ‘apporto di ossigeno?
Innanzitutto il flusso coronarico è la capacità di trasporto di ossigeno da parte del sangue. Il
flusso coronarico viene naturalmente determinato dalle resistenze vascolari che a loro volta
sono dipendenti da fattori neurologici, da sistemi di autoregolazione e da ostruzione del vaso
stesso. A livello coronarico il flusso di sangue avviene in diastole. L’ altro fattore importante è la
capacità del sangue di trasportare ossigeno con emoglobina.
Quali sono invece i fattori che vanno a determinare la richiesta di ossigeno da parte del
miocardio?
a. La frequenza cardiaca: quanto più aumenta il battito cardiaco tanto più aumenta la
richiesta di ossigeno da parte del cuore;
b. La contrattilità intesa come la velocità con cui il ventricolo si contrae;
c. La pressione sistolica del ventricolo sinistr;, quando è presente un aumento della
pressione telediastolica del ventricolo sinistro si ha una riduzione del flusso coronarico
che avviene in diastole.
MALATTIA ATEROSCLEROTICA
Qual è la definizione di Cardiopatia ischemica aterosclerotica?
È la manifestazione clinica della localizzazione del processo aterosclerotico nella coronarica, con
conseguente ischemia cardiaca; cioè una volta che il processo aterosclerotico si è localizzato nella
coronaria, si ha un aumento della placca che dà una ostruzione emodinamicamente significativa
con riduzione dell’apporto di ossigeno.
sinistra) mitralica (frequentemente)
Arteria coronaria
destra
i. Parete anteriore libera del ventricolo destro ii. Parete posteriore del ventricolo sinistro iii. Terzo inferiore del setto interventricolare
Se la coronaria di destra è dominante (70% dei casi) iv. Nodo seno atriale v. Nodo Atrio ventricolare vi. Muscolo papillare postero mediale

Infatti nella maggior parte dei casi una riduzione dell’apporto di ossigeno, e quindi di sangue nelle
arterie coronariche, è dovuto ad una ostruzione aterosclerotica del vaso.
Quando la placca aterosclerotica è ricoperta da una capsula viene definita stabile: quando
raggiunge determinate dimensioni può portare ad una significativa riduzione del flusso
coronarico. Questo processo può essere accelerato da fenomeni di vasocostrizione che
determinano un’ulteriore riduzione del flusso ematico, come una ulcerazione o fessurazione
della stessa capsula che portano ad una serie di eventi che generano un trombo con completa
ostruzione del lume vasale. Si passa così da una placca aterosclerotica stabile ad una placca
aterosclerotica instabile.

Nella grande maggioranza dei casi la cardiopatia ischemica è dovuta all’ aterosclerosi; esistono
però altri gruppi di coronaropatie non collegate necessariamente a tale patologia, come nel caso
di :
Una sproporzione tra richiesta ed apporto di ossigeno al miocardio per effetto dell’aumento delle richieste metaboliche del miocardio in assenza di una lesione ostruttiva coronarica. Ci sono pazienti con coronarie integre in cui c’è un’aumentata richiesta di ossigeno da parte del miocardio tale che le coronarie pur essendo normali non riescono a soddisfare. Esiste infatti un gruppo di arteriopatie non sclerotiche quali embolie, anomalie coronariche congenite, trombosi.
Malattie ematologiche che possono dare origine a processi trombotici:
a. Sindrome di Kawasaki P0F
1
b. Lupus Eritematoso
c. Spondilite Anchilosante
d. Spondilite Reumatoide
Questo gruppo di arteriti dà occlusioni ma non di tipo aterosclerotico.
Coronaropatie da malattie metaboliche come ad esempio l’omocistinuriaP1F
2P, amiloidosi,
terapia radiante.
Malattie a carico delle coronarie determinate da uno spasmo coronarico; l’esempio
classico è dato dall’ angina di Prinzmetal: questa forma di angina è dovuta allo spasmo
coronarico in assenza di lesioni ostruttive, dissezione aortica, dissezione coronarica.
Cardiopatie da arteriti come quella luetica, granulomatosa, poliartrite, traumi coronarici;
Ischemie cardiache non aterosclerotiche possono essere dovute a endocardite infettiva,
prolasso della valvola mitralica, trombosi atriale sinistra e trombosi ventricolare sinistra;
Anomalie congenite come fistole coronariche o prolasso della mitrale.
Vi è poi un altro gruppo di pazienti in cui le coronarie non sono malate ma vi è un aumentata
richiesta di ossigeno da parte del cuore. Questo succede nella:
a. la stenosi valvolare aortica : il meccanismo di compenso consiste in una Uipertrofia U
UconcentricaU del ventricolo sinistro; la sua parete aumenta di spessore ma il suo volume
rimane invariato, il ventricolo va incontro soltanto ad un sovraccarico di pressione. Se
abbiamo infatti un paziente affetto da stenosi valvolare aortica con pressione periferica
1 La sindrome di Kawasaki o sindrome muco‐cutanea dei linfonodi è una vasculite infantile delle arterie di media e piccola dimensione che colpisce soprattutto le arterie coronarie. L'eziologia è ancora sconosciuta. È caratterizzata da febbre prolungata, esantema, congiuntivite, mucosite, linfoadenopatia cervicale e poliartrite di gravità variabile. Se non diagnosticata in tempo può portare all'infarto del miocardio. 2 L'omocistinuria è una malattia rara, dovuta a un errore congenito del metabolismo. Deve il suo nome al segno principale: la presenza dell'amminoacido omocisteina nelle urine. L'omocistinuria è conosciuta anche come omocisteinemia. Anche tale parola identifica un segno importante di questa malattia: il rilievo patologico dell'omocisteina nel sangue. In questo caso, però, il dato patologico è in realtà l'iperomocisteinemia.

di 120 , tenendo conto che la stenosi valvolare aortica genera un gradiente tra ventricolo
sinistro e aorta di 100, la pressione sistolica massima è 220. Aumenta di conseguenza la
pressione telediastolica con conseguente ischemia subendocardica.
b. Nell’insufficienza valvolare aortica/mitralica il ventricolo sinistro viene sottoposto ad un
aumento di volume e quindi di pressione con Uipertrofia eccentricaU. Si ha cioè un’
ipertrofia per il maggior carico di sangue con un aumento di volume.
c. Avvelenamento da monossido di carbonio: viene ridotta la capacità di trasporto di
ossigeno da parte del sangue, in quanto nell’avvelenamento da anidride carbonica
l’ossiemoglobina viene sostituita da carbossiemoglobina.
d. Tireotossicosi
e. Shock
f. Abuso di cocaina.
DOMANDA FREQUENTE
Quando il cuore si ipertrofizza come ad esempio nella stenosi aortica si ha un aumento di
spessore senza un aumento di volume, si ha un aumento della pressione telediastolica del
ventricolo sinistro. Tenendo presente che la profusione coronarica è una profusione diastolica,
questo aumento di pressione all’interno del ventricolo in diastole, va ad ostruire, per una
compressione esterna, il flusso di sangue alle coronarie. Quindi nella stenosi aortica uno dei
segni principali è l’angina, perché le coronarie pur essendo normali non riescono a soddisfare la
richiesta di ossigeno da parte del miocardio ipertrofico.
FORME CLINICHE
Il dolore è la diretta conseguenza della cascata ischemica, sono infatti le alterazioni chimiche e
mitocondriali che portano prima ad un’alterazione della meccanica cardiaca e poi alla
manifestazione clinica del dolore. La stabilità della cardiopatia ischemica dipende dalla
sintomatologia: se essa rimane costante per almeno tre settimane si parla di angina stabile, se
invece subisce variazioni si parla di angina instabile.
La cardiopatia ischemica aterosclerotica si può manifestare in forma cronica ed acuta.
L’angina stabile e il rimodellamento post‐infartuale del ventricolo sinistro sono forme tipiche di
Ucardiopatia ischemica cronicaU. L’angina instabile e l’infarto acuto del miocardio rappresentano
invece le Umanifestazioni acute della cardiopatia ischemicaU.
Tra le forme acute c’è la sindrome coronarica acuta che comprende le manifestazioni più gravi
di cardiopatie ischemiche come:
L’ angina instabile e l’infarto miocardico acuto, il quale si può suddividere a sua volta in:
a. Infarto miocardico acuto senza elevazione del tratto ST
b. Infarto miocardico acuto con elevazione del tratto ST all’ elettrocardiogramma.

L’introduzione del concetto della sindrome coronarica acuta è abbastanza recente e si è voluto
distinguere la sindrome coronarica clinica in angina instabile o in infarto in base alla elevazione
degli enzimi cardiaci, essenzialmente della troponina e del CK‐MB; perché in effetti
clinicamente l’angina instabile o infarto sono nelle prime fasi praticamente indistinguibili.
L’ angina stabile è la manifestazione più classica della forma cronica della cardiopatia
ischemica, essa in genere si manifesta con un dolore toracico oppressivo o costrittivo. In genere
è provocata da uno sforzo e passa dopo l’eliminazione di quest’ ultimo. E’ necessario chiedere
al paziente da quanto tempo ha questo dolore: se il paziente dice di averlo da più di tre
settimane allora siamo nel concetto di stabilità. La domanda successiva da porre al paziente è
in merito allo sforzo che determina l’angina: se il dolore avviene sempre per lo stesso sforzo
l’angina è stabile, se invece il paziente riferisce che il dolore sopravviene per sforzi anche
inferiori si tratta di angina ingravescente. Il dolore in genere è precordiale con irradiazione alla
parte ulnare del braccio sinistro, ma può anche essere irradiato al braccio destro o può
manifestarsi con un mal di stomaco.
La funzionalità cardiaca ha 2 classificazioni:
La classificazione NYHA che si riferisce alle capacità funzionali del paziente e si basa sull’ attività
che egli riesce a svolgere senza affaticarsi:
Classe I: Non viene compromessa la normale attività
Classe II: La normale attività può provocare fatica, palpitazione e dispnea
Classe III: Si ha una forte riduzione dell’attività ordinaria
Classe IV: Il paziente è fortemente limitato nell’attività giornaliera, alle volte non riesce
neanche a mangiare.
La classificazione della CCS è ,invece, una classificazione funzionale e si riferisce essenzialmente a
angina di classe 1: l’ angine insorge per sforzi fisici molto sostenuti;
angina di classe 2 :riduzione della capacità di compiere attività quotidiane;
angina di classe 3: le attività sono molto ridotte;

angina di classe 4 :inabilità totale del paziente nel compiere qualsiasi attività.
La NYHA si riferisce alle capacità funzionali del paziente essenzialmente per dispnea mentre la
classificazione CCS si riferisce alla capacità funzionale del paziente in relazione all’ insorgenza
dall’angina.
Vediamo adesso la definizione di angina instabile: se un paziente vi riferisce di un dolore toracico
e vi riferisce di averlo da una settimana, quello deve essere classificato come angina instabile
perché è molto difficile vedere l‘ evoluzione a breve termine di quell’ angina. Se successivamente
si vede che il tipo di dolore perdura per più di un mese, lo classificheremo come angina stabile .
Quindi si parla di angina instabile o per recente insorgenza o per aggravamento di una angina
precedentemente stabile. La sintomatologia dell’angina instabile non è associata a segni
dell‘infarto e quindi non si ha un aumento degli enzimi cardiaci. Molte forme di angina instabile
possono simulare una sindrome coronarica acuta e possono presentarsi da un punto di vista
elettrocardiografico con 2 caratteristiche: elevazione del tratto ST con sviluppo dell’ infarto
miocardico, o senza elevazione del tratto ST. In questo caso si tratta di forme di ischemia cardiaca
che raramente evolve verso l’infarto.
INDICAZIONE CHIRURGICA
La cardiopatia ischemica può essere ad indicazione chirurgica in tre possibili occasioni:
1. La fase dell’ischemia (è la fase in cui domina il quadro sintomatologico)
2. L’infarto può essere limitato nei danni che produce se si interviene con
rivascolarizzazione chirurgica nelle prime 4 ore.
3. Il post‐infarto precoce o tardivo:
Rottura di cuore

Insufficienza mitralica
Aneurisma
L’indicazione chirurgica si pone per stenosi maggiore del 75% del vaso coronarico. L’intervento più
eseguito è quello di bypass aorto‐coronarico.Tramite l'intervento di bypass si crea un ponte
artificiale che permette di aggirare l'ostacolo alla circolazione. Questo ponte, chiamato appunto
bypass, è costituito da un tratto di 0T 0T3Tvaso sanguigno 3T0T 0Tsano e ben funzionante, che viene prelevato dal
chirurgo al momento stesso dell'operazione. Quando possibile, si utilizzeranno preferibilmente
alcuni segmenti delle arterie mammarie del paziente (che presentano caratteristiche funzionali
ottimali per espletare al meglio l'azione di bypass); in alternativa si ricorre a tratti della
vena 0T 0T3Tsafena3T ( invertita secondo il senso delle valvole ). Possono essere usate anche la radiale o
l’epigastrica inferiore. Questi segmenti vasali vengono poi innestati a monte e a valle della
coronaria occlusa, creando così il bypass; tale espediente permette di far riaffluire al cuore un
apporto ottimale di sangue ed ossigeno.
Dai primi anni '70, in cui la tecnica del bypass aortocoronarico cominciò a prendere piede, le
tecniche chirurgiche si sono notevolmente evolute. Dall'intervento tradizionale in anestesia
generale e a circolazione extracorporea (il cuore viene fermato e si utilizza una macchina esterna
per far circolare il sangue), si è giunti in epoche più recenti ad interventi eseguibili a cuore
battente ed addirittura in anestesia locale.

COMPLICANZE MECCANICHE POST‐INFARTUALI
L’infarto miocardico significa necrosi delle cellule miocardiche. Esso può incorrere in maniera non
complicata oppure esitare in complicanze acute quali:
Insufficienza mitralica acuta
Rottura del setto interventricolare
Rottura della parete libera del ventricolo sinistro
La valvola mitralica è situata tra l’atrio e il ventricolo sinistro; da un punto di vista anatomo‐
funzionale essa è composta da lembi valvolari, corde tendinee , muscoli papillari. Le corde
tendinee ,ancorate ai muscoli papillari, impediscono il prolasso della mitrale nell’atrio durante la
sistole ventricolare, separando anatomicamente l’atrio dal ventricolo. Un’alterazione di questo
sistema ( spostamento del muscolo papillare, rottura delle corde tendinee..) ,provocato
dall’infarto, può portare all’insufficienza mitralica acuta: la separazione delle due camere sinistre
del cuore viene a mancare, anzi durante la sistole ventricolare parte del sangue passa attraverso la
valvola insufficiente e raggiunge l’atrio generando un soffio apprezzabile in regione interscapolare.
Secondariamente alla necrosi è possibile apprezzare la rottura del setto interventricolare in
diversi punti. Nel 60% dei casi si localizza nel setto antero‐apicale dopo un infarto intramurale che
colpisce il territorio dell’ IVA. Nel 20%‐40% dei casi si localizza nel setto posteriore dopo un infarto
intramurale infero settale che colpisce la coronaria destra dominante o, più raramente, un’arteria
circonflessa dominante. Generalmente la rottura del setto interventricolare si presenta in maschi
di più di 65 anni con una malattia monovasale ed uno scarso circolo collaterale dopo 2‐4 giorni dal
primo infarto. In caso di rottura del setto si verifica una shunt sinistro destro con segni di
insufficienza cardiaca e di iperafflusso polmonare.
La terapia medica mira a ridurre l’entità dello shunt sinistro‐destro con l’utilizzo di vasodilatatori

arteriosi (idralazina, nitroprussiato o altri), che riducono le resistenze vascolari sistemiche; tuttavia
l’efficacia di tali farmaci è spesso modesta o nulla per concomitante azione sulle resistenze
polmonari. Sono controindicati invece i farmaci come la NTG per la loro prevalente azione di
vasodilatazione venosa e conseguente riduzione del precarico. La terapia più efficace è
rappresentata dalla correzione chirurgica del difetto eventualmente associata a rivascolarizzazione
coronaria : la mortalità operatoria è < 25% nei pazienti emodinamicamente stabilizzati e la
sopravvivenza a distanza è nettamente superiore rispetto al trattamento medico. Negli anni più
recenti, in funzione dell’anatomia, della posizione e della dimensione della rottura, è stata
utilizzata anche la riparazione mediante protesi di diversa foggia, inserite per via per cutanea.
Ovviamente il tipo di intervento è decisamente meno traumatico e meglio sopportato anche dai
soggetti più compromessi. L’inserimento viene eseguito con ausilio di strumenti radiologici, ma
l’efficacia della correzione viene verificata mediante ecocardiografia.
L’infarto può infine condurre a rottura parziale o totale della parete libera del ventricolo sinistro.
La rottura di cuore è un’evenienza catastrofica, quasi sempre mortale, che si verifica
generalmente nella prima settimana di infarto acuto. Interessa più frequentemente la parete
anteriore e laterale del ventricolo sinistro ed è dovuta ,in genere, all’occlusione di un solo vaso
coronarico senza circolo collaterale.

L’unica possibilità terapeutica è rappresentata dall’intervento chirurgico, teso alla riparazione della
breccia mediante semplici colle.

Insufficienza mitralica
Prof. De Feo
17/11/16
Oggi nella pratica clinica si vedono molti più pazienti con insufficienza mitralica piuttosto che con
stenosi, quest’ultima è legata soprattutto alla malattia reumatica che nel mondo occidentale è
andata progressivamente scomparendo.
Definizione di IM: Incompleta chiusura dell’ostio mitralico cui segue un reflusso di sangue, in sistole, dal ventricolo all’atrio sinistro. La normale apertura e la perfetta continenza della valvola mitrale dipendono dal corretto e integrato comportamento di 6 componenti fondamentali: • Lembi • Annulus • Commissure • Corde tendinee • Muscoli papillari • Integrità morfologica e funzionale del VS (poiché i muscoli papillari si inseriscono sulla parete libera del VS in caso di infarto possiamo avere un’insufficienza mitralica secondaria, in questo caso definita funzionale). Quindi l’insufficienza mitralica può essere di tipo:
Organico quando c’è la patologia di uno dei componenti della struttura
Funzionale quando è secondaria ad un’alterazione della parete del VS Ricordate che la circonferenza dell’annulus è mediamente 8/10 cm e che l’area mitralica è mediamente 5 cm2. La valvola è formata da:
‐ un lembo anteriore, molto ampio, è il principale responsabile della motilità ‐ un lembo posteriore, più piccolo, è essenzialmente la struttura d’appoggio.
Classificazione chirurgica della valvola mitrale:

I 3 settori lembo posIl prolasso Le corde tesul m.papi
Di I
Di I
Di I La zona dcosiddettaAi fini dellalivello. I mm. Papinfatti nell’VS.
EziologiaIn base alla
o scallops (teriore. di P2 è il pi
endinee cosllare. Le cla
I ordine che
II ordine
III ordine so
i contatto “zona ruvida corretta f
illari sono p’insufficienz
a modalità d
A1, A2, A3)
ù frequente
stituiscono ssifichiamo
e si inserisco
ono le più pi
fra i lembida” dei lemfunzionalità
perfusi dallza mitralica
di insorgenz
) formano il
e ed è anch
l’ apparatoo in:
ono direttam
iccole, sono
i viene defmbi. della valvo
e coronarie funzionale
za l’IM può
l lembo ant
e quello più
sottovalvo
mente sul m
o quelle che
finita punto
ola è fondam
e per cui soe c’è una dis
essere dist
teriore, men
ù facilmente
olare che da
muscolo pap
e sottendon
o di coapta
mentale che
ono particolsfunzione le
inta in: acut
ntre P1,P2,
e riparabile
al lembo po
pillare;
o il lembo d
azione ed a
e i due lem
larmente vuegata all’isch
ta e cronica
P3 sono i 3
.
steriore va
della valvola
avviene a l
bi coaptino
ulnerabili ahemia della
a
3 settori del
ad inserirsi
a.
ivello della
allo stesso
ll’ischemia,a parete del
l
i
a
o
, l

Cause di IM acuta: 1) Alterazione dell’anello mitralico: ‐ trauma (chirurgia valvolare) ‐ endocardite infettiva (formazione di un ascesso), molto frequente. Comune è il reperto di ascessi micotici ad alterare la geometria dell’anello 2) Alterazione dei lembi valvolari: ‐ endocardite infettiva (vegetazione, perforazione). Di solito il processo degenerativo inizia da qui per poi estendersi all’anello ‐ traumi (lesione toracica penetrante; valvulotomia percutanea) ‐ tumori (mixoma atriale) 3) Rottura di corde tendinee: ‐ idiopatica (spontanea) ‐ degenerazione mixomatosa (forma più frequente, anche nota come Floppy valve) ‐ endocardite infettiva 4) Alterazione dei muscoli papillari:
- coronaropatia (rottura o disfunzione per IMA o malattia ischemica) - trauma
Cause di IM cronica: la forma più frequente è la post ischemica, il ventricolo si dilata, dilatandosi il ventricolo si dilata l’anello. Si parla di insufficienza mitralica funzionale 1) Infiammatoria: ‐ cardite reumatica ‐ connettiviti (LES, sclerodermia) 2) Degenerativa: ‐ degenerazione mixomatosa (collagenopatie) ‐ calcificazione dell’annulus 3) Infettiva: ‐ endocardite infettiva ‐ rottura corde tendinee (IMA, trauma, endocardite) 4) Strutturale: ‐ rottura o disfunzione dei muscoli papillari (IMA o ischemia) ‐ dilatazione dell’anello mitralico (cardiomiopatia dilatativa, aneurisma del VS) 5) Congenita: ‐ fessurazione valvolare tra due scallop (Cleft) ‐ prolasso valvolare mitralico Classificazione secondo Carpentier
Tipi di insufficienza mitralica Lesioni anatomiche
I) movimento valvolare normale Dilatazione dell’annulus Perforazione di un lembo
II) prolasso valvolare (più frequente) Rottura o allungamento delle corde (maggior parte dei casi)

III) IIIa in dias IIIb in sist
Sindrome d(malattia d è u più è la
In essa uno La forma mcorde si as In caso di casi, la vaparticolarmvalore è undel soggett Cleft Mitra Molto freqfrequente tra i due sc Fisiopatolo
da ipomotstole ole
del prolassodi Barlow –
na sindrom comune nea causa più
o dei due le
mixomatosasottigliano
insufficienzalvola si premente dilatna guida: leto ma utiliz
alico quente, sopnel lembo callops della
ogia
tilità dei lem
o della mitr– floppy mit
me di frequeelle donne tgrave di ins
embi prolass
a (Floppy ma “chewing
za mitralica esta moltoato, cioè ine dimensionziamo ques
prattutto inposteriore a valvola
mbi (più rara
rale tral valve)
nte riscontrtra i 14 e i 3sufficienza m
sa ovvero e
itral valve) g gum”.
è importan bene ad nferiore ai i del ventricsto valore co
n pediatria, . La riparaz
Rott
a) FusiProc
ro, ma con 30 anni mitralica iso
subera, va a
è la forma
nte interveninterventi d5,5 cm, pecolo vanno ome riferim
è il Cleft Mzione è mol
tura o allun
ione commecesso fibrot
quadro clin
olata
al di sopra d
più frequen
nire (ai fini di riparazioer evitare rconsideran
mento).
Mitralico, uto semplice
gamento d
essurale tico
nico variabil
del piano di
nte incontra
riparativi none) quandrischio di innte anche in
n incisione e, consiste
ei m. papilla
e
i coaptazion
ata. In ques
ella maggiodo il ventricnsufficienzan base a pes
tra gli scallin una sutu
ari
ne.
sta forma le
or parte deicolo non è del VD. (Ilso e altezza
lops, moltoura del cleft
e
i è l a
o t

lo svuotamento sistolico del VS avviene secondo un gradiente pressorio
quando, all’inizio della sistole il ventricolo comincia a contrarsi, il flusso trova meno resistenza in atrio che in aorta: quasi il 30% del volume viene rigurgitato in atrio sx prima dell’apertura della valvola aortica
il volume di flusso retrogrado dipende dalle dimensioni dell’orifizio rigurgitante e dalle resistenze del circolo sistemico (post‐carico)
fase di scompenso
un aumento delle dimensioni del VS aumenta l’orifizio rigurgitante (dilatazione dell’annulus)
l’aumento di volume telediastolico ventricolare aumenta, secondo la legge di Laplace, la tensione di parete che tende a dilatare ulteriormente il ventricolo (circolo vizioso)
infine la contrattilità comincia a ridursi (aumento volume telesistolico) Nell’insufficienza mitralica soffre:
Ventricolo SX: a lungo andare si dilata
Circolo polmonare: il volume rigurgitante causa ipertensione polmonare (che riesce a compensare evitando così ripercussioni sul VD, a differenza di quanto accade nella stenosi in cui si ha tricuspidalizzazione)
L’insufficienza mitralica tende ad essere progressiva: l’apparato valvolare va incontro ad ulteriore deterioramento, il rigurgito aumenta. Sintomi Forme croniche:
- Palpitazioni (frequente extrasistolia, tachicardia) - Astenia (poco frequente) - Ridotta resistenza allo sforzo fisico - Dispnea da sforzo (frequente) - Ortopnea - Dispnea parossistica notturna
Forme acute (per mancato meccanismo di compenso) possono esordire con:
- Edema polmonare - Emottisi - Shock cardiogeno
Segni Clinici • Itto sollevante e diffuso • I tono ridotto o assente (se le cuspidi presentano ridotta flessibilità) • II tono accentuato o sdoppiato (ipertensione polmonare) • Soffio sistolico puntale (rude, irradiato all’ascella) [quello da stenosi aortica si irradia al collo] • Soffio mesodiastolico puntale (da iperafflusso transmitralico) • III tono (da sovraccarico diastolico)

Il soffio sistolico puntale va distinto da: - Difetto del setto interventricolare - Stenosi aortica - Insufficienza tricuspidale
Diagnosi Strumentale ECG RX Torace: Ecocardiogramma - Transtoracico TTE: ci permette di fare diagnosi Ecocardiografia ci dice:
Presenza e grado di insufficienza mitralica
Morfologia della valvola mitrale, e valutazione del meccanismo dell’insufficienza
Dimensioni, spessori, indici di funzione di pompa e contrattilità del VS
Dimensioni atrio sx e valutazione del sovraccarico delle sezioni dx
Follow up nelle IM
Follow up dopo riparazione o sostituzione valvolare - Transesofageo TEE: con ricostruzione tridimensionale. Fornisce i dettagli per la
preparazione chirurgica riparativa. Varie modalità di utilizzo:
Intraoperatoria per stabilire l’anatomia e guidare la riparazione
Valutazione del grado, del meccanismo dell’IM e/o lo stato di funzione VS, quando TTE inadeguata
Follow up quando TTE inadeguata Esame emodinamico - Valutazione eco della gravità. Metodo del color doppler (il più usato): Entità del jet in AS, in
rapporto all’area dell’atrio
Area jet 20% area AS: IM lieve
Area jet 20‐40% area AS: IM moderata
Area jet > 40% area AS: IM impotante - Indicazioni a coronarografia:
IM in pz con angina o precedenti infarti
Ischemia sospettata
Pz con età superiore ai 40 anni che vanno incontro a intervento cardiochirurgico Terapia Medica • Profilassi per la malattia reumatica • Profilassi per endocardite batterica • Digitale (ormai poco usata, per fenomeni aritmici) o anticoagulanti (in pz con Fibrillazione atriale) • ACE‐inibitori per ridurre il post‐carico • Diuretici per controllare l’insufficienza cardiaca e la dispnea N.B il warfarin è un farmaco anticoagulante cumarinico, per i portatori di protesi CARDIACHE. I NAO (nuovi anticoagulanti orali) sono per i portatori di tutti gli altri tipi di protesi, cardiache escluse, inoltre sono indicati nei pz con fibrillazione atriale (solo se non portatori di protesi cardiache). Il limite dei NAO era/è che non hanno un antidoto, ma oggi in commercio è disponibile l’antidoto del Dabigatran (il primo dei NAO).

Terapia chirurgica Tipi di intervento
Sostitutivo (con protesi). Oggi nell’ 80% la terapia è di tipo conservativo (la valvola si ripara), soltanto in alcuni casi è necessario fare una terapia di tipo sostitutivo. Esattamente il contrario della stenosi: l’80% dei casi richiede una terapia sostitutiva con protesi, mentre soltanto qualche raro caso (non capita ormai da anni, la stessa stenosi è rara) si opera con commissurotomia. Quando è necessario sostituirla:
- quando ci sono molte calcificazioni. Se queste sono presenti specie sull’anello è difficile che si possa effettuare una riparazione.
- quando si forma un’endocardite molto estesa. L’endocardite spesso si presenta con delle vegetazioni che non rappresentano un grande problema, perché si può effettuare una vegetectomia (si prende la vegetazione, si pulisce e si toglie), però quasi sempre quando c’è un’endocardite e sono presenti le vegetazioni anche l’anello è interessato: spesso si trovano ascessi. In questi casi non è possibile assolutamente fare una terapia riparativa Svantaggi della sostituzione: anche se di poco, cambia la struttura valvolare, si riduce l’elasticità atriale, si riduce la componente di sostegno dell’apparato sotto‐valvolare, e chiaramente, insieme alla protesi bisogna iniziare il trattamento anticoagulante con il Warfarin (attualmente terapia riconosciuta e utilizzata per le protesi valvolari cardiache, Coumadin nome commerciale). E’ preferibile, per quanto possibile, lasciare l’apparato sotto‐valvolare. Quindi, in caso di un’insufficienza non correggibile, trattabile solo con protesi, si preferisce togliere il lembo anteriore, tagliare poco il posteriore, salvando le corde sottostanti: sembra che sul rimodellamento ventricolare a distanza il cuore si riprende meglio rispetto al taglio completo del lembo posteriore, con conseguente taglio delle corde tendinee e relativo attacco sui muscoli papillari. Come si impianta la protesi? Normalmente viene impiantata, biologica o meccanica che sia, o attraverso punti semplici nell’annulus (più frequenti) o con dei punti complessi. Mediamente servono 25 punti di sutura per inserire la protesi sull’annulus.
Conservativo. Quali sono le indicazioni alla chirurgia: le valvole che più facilmente si riescono a riparare sono quelle che vedono un’eziologia di tipo degenerativo. I prolassi della mitrale sono quelli che nel 90% dei casi si riescono a riparare. In mani molto esperte anche i casi di endocardite si riescono a riparare, molto meno le forma reumatiche e le forme ischemiche. La chirurgia riparativa ha una mortalità che si aggira intorno all’1% (la mortalità è un po' più alta per i pazienti che vanno incontro a sostituzione, ma in genere per l’ammalato più complesso, non tanto per la tecnica di intervento).
Come si effettua un intervento di riparazione o sostituzione della mitrale: essenzialmente attraverso un’atriotomia sinistra. Il paziente viene messo sempre in circolazione extracorporea.
1‐ CANNULE: CONNESSIONE PER IL DRENAGGIO VENOSO:
Sistema delle doppie cannule Quando si cannulano le vene cave? quando si vuole avere un accesso migliore all’atrio. In tal caso si parla di circolazione circolazione aorto‐bicavale
Sistema della monocannula atriale

2‐ CANNULE: SISTEMA DI IMMISSIONE ARTERIOSA: Il sangue ritorna al paziente in aorta oppure in a. femorale 80%, a. ascellare 20‐30%.
3‐ IPODERMIA Questi interventi si effettuano raffreddando il paziente (ipotermia moderata) a 30°. Maggiore è la durata dell’intervento, maggiore è l’importanza dell’ipotermia. Sono due i sistemi per abbassare la temperatura: uno tramite lo scambiatore di calore (circolazione extracorporea), un altro è tramite l’utilizzo di ghiaccio diretto nel mediastino (raffreddamento topico) .
4‐ ARRESTO CARDIACO Quando si cannula il paziente il cuore batte, ma è “vuoto” ( poco sangue all’interno). A 30° il cuore va in fibrillazione. Nella circolazione extracorporea non crea danni ovviamente, ma si vuole operare su un cuore fermo, non un cuore fibrillante. Si interrompere la circolazione nelle coronarie tramite il clampaggio aortico, a quel punto per proteggerlo (altrimenti non ripartirà più) si fa l’iniezione di Potassio (CARDIOPLEGIA) ogni 20‐30 min. Il cuore si ferma in diastole. Il cuore quando è arrestato va protetto altrimenti si rischia lo stone Heart (cuore di pietra) alla fine dell’intervento: il cuore non riparte
5‐ Come si fa ripartire il cuore? Tramite il Declampaggio il cuore pian piano acquista la sua contrattilità. Si può utilizzare, in caso di debole risposta cardiaca, un pacemaker temporaneo in modo da farlo riperfondere più rapidamente (Questo vale in linea di massima per tutti gli interventi cardiochirurgici).
In cosa consiste l’intervento una volta fermato il cuore? Si crea un accesso tramite atriotomia Sx, ottenendo un accesso diretto alla mitralica. Una via alternativa è tramite atriotomia Dx, ma in questo caso bisogna incidere anche il setto interatriale. Si ha una visuale migliore della valvola, però dopo bisogna ricostruire con un patch il setto, è una procedura più lunga. TERAPIA RIPARATIVA, QUELLA Più FREQUENTE L’obiettivo è quello di ripristinare la funzione piuttosto che l’anatomia vera e propria. Talvolta l’anatomia viene leggermente modificata dalle tecniche riparative, specie quelle più sofisticate. il trattamento è relativo ai vari livelli di insufficienza. Ci si rifà quindi alla CLASSIFICAZIONE DI CARPENTIER Tipo 1. - Dilatazione dell’anello: se si dilata l’anello senza prolasso dei lembi si effettua solitamente
un anuloplastica: Si va a restringere l’anello valvolare. Si può effettuare in tanti modi, il più comune utilizza degli anelli sintetici che possono essere rigidi, semirigidi, flessibili. Possono essere completi o incompleti (manca una porzione e l’anello viene messo da un trigono ad un altro). Alcuni chirurghi utilizzano addirittura un pezzo di pericardio al posto degli anelli sintetici.
- In caso di perforazione (99% endocarditi, abbiamo detto però che l’endocardite si presta poco alla riparazione per la presenza di ascessi, quindi queste sono situazioni particolari) se la vegetazione è localizzata solo in una zona di un lembo, senza coinvolgimento dell’anello, si può tentare di ricostruire il lembo con un patch di pericardio.
Tipo 2. Prolasso. Può essere del lembo anteriore, posteriore o bilembo. La più frequente è il prolasso del lembo posteriore, il P2 in particolare che è più centrale (ed è anche più facile da ricostruire). Si può effettuare una resezione di P2 con anuloplastica: a seconda dell’ampiezza si effettua una resezione quadrangolare o triangolare di P2, dopodicchè si suturano le due parti aperte (se si trovano alla stessa altezza). Se non si trovano alla stessa altezza i 2 lembi si devono riportare allo stesso livello: si reseca la porzione più vicina all’annulus e si abbassa l’anello: quest’operazione si chiama SLIDING. L’anello si mette in ogni caso: dopo aver fatto la resezione la valvola può non

aderire perfettamente. Basta però inserire l’anello, e l’eventuale insufficienza residua scompare completamente perché le due zone non sovrapposte completamente vengono a combaciare perfettamente. In alcuni prolassi il P2 non è molto esuberante (il punto di coaptazione è stato ovviamente perso) e non conviene effettuare una resezione. Come si riporta il lembo più in basso? Tramite corde tendinee artificiali: impianto di corde artificiali con anuloplastica (molto spesso il prolasso è causato proprio da corde allungate). Questa tecnica la si può usare sia per il lembo posteriore che per l’anteriore. Ricordate le opzioni disponibili
- lembo posteriore: resezione + anuloplastica; corde + anuloplstica. - lembo anteriore: corde + anuloplastica.
C’è un altro caso: la tecnica Alfieri o “plastica edge to edge” per il prolasso bilembo, ideata dal prof. Alfieri al San Raffaele. Il prolasso bilembo è di solito il più difficile da riparare. In queste situazioni si può mettere un punto tra il margine libero del lembo anteriore e posteriore e chiudere. Quello che si crea è una valvola mitrale a 2 orifici, e dal punto di vista funzionale i risultati sono buoni. Chiaramente viene ridotta, anche se di poco l’area valvolare. Attuamemte si può effettuare anche con chirurgia endovascolare, quindi minimanente invasiva (MitraClip). Viene effettuata tutte quelle volte in cui l’intervento tradizionale viene sconsigliato (malati anziani). Si riduce il grado di insufficienza, la qualità di vita migliora.
TIPO 3. Legato all’ipomotilità dei lembi o in diastole o in sistole. Se c’è una retrazione del
lembo (spesso il posteriore, rare forme di malattia reumatica) molto abbondante, lo si può staccare dall’anello, suturare un pezzo di pericardio e ricomporre il tutto. Questa tecnica è utilizzata molto poco, di solito la valvola si cambia in malattia reumatica con interessamento del lembo posteriore.
Prima di ripristinare la circolazione si effettua la PROVA IDRODINAMICA: alla fine dell’intervento si spruzzano delle siringhe di acqua nel ventricolo attraverso la valvola fino a riempirlo. Una volta pieno si valuta l’eventuale rigurgito. TEE: una volta fatto ripartire il cuore e ripristinata la circolazione, si valuta il risultato dell’operazione.
Stenosi mitralica Definizione: Per stenosi intendiamo un restringimento dell’area valvolare con ostruzione al flusso di sangue dall’atrio al ventricolo sinistro Classificazione: Stenosi mitralica lieve: area valvolare=2‐1,5 cm2, Stenosi mitralica moderata: area valvolare= 1,5‐1,0 cm2, Stenosi mitralica importante: area valvolare= 1‐ 0,5 cm2. Normalmente il lembo posteriore diventa fibrotico – calcifico, si calcificano le commissure. Gia questo lascia pensare che è una valvola che difficilmente si presta a riparazione. La pressione media in atrio sx è normalmente di 7mmHg Eziologia: malattia reumatica, endocardite infettiva, sono le più comuni attualmente che giungono in
sala operatoria. Un altro abbastanza comune è il mixoma atriale sx: il mixoma andando a occupare spazio
rappresenta un occlusione. E’ il tumore più frequente del cuore, un tumore benigno, si presenta essenzialmente in due forme:

forma acinosa, più piccolo ma più pericoloso, sono acini della grandezza di un melograno, estremamente friabili. Questa friabilità è la causa dell’embolia in caso del più piccolo errore nella rimozione.
forma la capsulare, più grandi generalmente occupano tutto l’atrio, hanno una buona sede di impianto, durante la resezione si riesce a prendere l’intera massa facilmente. Perché il mixoma è l’unica causa neoplastica di stenosi? Perché gli altri colpiscono tendenzialmente il cuore dx e sono quasi sempre forme metastatiche di carcinomi uterini, renali.. Il mixoma dell’atrio Dx è raro
Anaotmia Patologica: Possiamo avere fusioni dell’apparato commissurale, delle cuspidi, delle corde oppure un insieme di tutto questo. La valvola si presenta a bocca di pesce o asola e spesso presenta queste calcificazioni. Fisiopatologia: aumento della pressione trans‐valvolare aumento pressione atrio sx. L’atrio sx si dilata per quanto possibile, la dilatazione si riflette sulla circolazione polmonare. Prima aumenta la pressione venosa, successivamente si arriva all’ipertensione arteriosa polmonare. Il ventricolo dx si ipertrofizza in un primo momento, poi inizia a dilatarsi e va incontro a sofferenza. Si arriva alla tricuspidalizzazione mitralica: insufficienza tricuspidale (dilatazione dell’annulus) secondaria a stenosi mitralica. SI ha quindi tutto il quadro clinico dello scompenso destro (edemi declivi, vene giugulari ingrossate…) Sintomi: sono in genere ben tollerati finchè l’aria valvolare non diventa eccessivamente ridotta. Sono dovuti all’aumento delle pressioni sx e alla riduzione della portata cardiaca. Una classica manifestazione è la fibrillazione atriale, campanello di allarme di malattia in fase avanzata. Ad esempio il reperto in una donna giovane con un’area valvolare non troppo ristretta di fibrillazione atriale può anticipare l’intervento chirurgico, considerando che sostituendo la valvola e ripristinando una corretta circolazione si ha una buona probabilità di ripristinare un buon ritmo sinusale, risultati che invece difficilmente si apprezzano quando si interviene su di un “mega‐atrio”, un atrio molto dilatato > 5 – 5,5 cm. In questi casi (mega‐atrio) si può associare come tecnica chirurgica l’ablazione della fibrillazione atriale, ma il più delle volte è inefficace. Il pz rimane quindi fibrillante, e il suo trattamento con Warfarin, che manterrà perché portatore di protesi, lo dovrà forse aumentare leggermente perché avente 2 fattori di rischio: una protesi e la fibrillazione atriale. Aspetto fondamentale della coagulazione è l’international normalized ratio (INR). I soggetti sani hanno un INR = 1. Con paziente portatore di protesi l’obiettivo è aumentare l’INR (“fluidificare” il sangue)per evitare che si formino trombi. Le linee guida dicono che per i portatori di protesi in sede aortica l’INR deve essere tra 2 e 3, in assenza di altri fattori di rischio. Con una protesi in sede mitralica l’INR deve essere tra 2,5 e 3,5. Perché i valori per le due protesi sono diversi? Per il gradiente di pressione. In ambito chirurgico si parla di “lavaggio”: la valvola aortica viene lavata meglio e di più rispetto ad una valvola mitralica dove le pressioni sono molto più basse. Per una tricuspide l’INR si mantiene > di 3 I sintomi sono legati alla congestione polmonare Segni clinici: la facies mitralica non la si vede praticamente più, è difficile che si arrivi a situazioni così gravi; Schiocco d’apertura: ‐ distanza variabile da II tono (tanto più vicino quanto più importante è la stenosi: intervallo < 80 msec espressione di stenosi importante!)

Rullio diastolico: ‐ massima intensità in protodiastole e rinforzo presistolico (in ritmo sinusale): la durata è indice di gravità! Complicanze: aritmie ed embolie Diagnosi: essenzialmente ecocardiografica; il TEE ci dà qualche notizia in più. Terapia chirurgica:
essenzialmente di tipo sostitutivo 90%;
conservativo 10%. In situazioni particolari, senza eccessiva calcificazione, senza coinvolgimento dell’annulus, con un solo processo fibrotico a carico delle commissure si può effettuare una commissurotomia: un incisura a livello delle commissure per aumentare l’ostio valvolare. Anche in queste situazioni si associa sempre l’anuloplastica: può infatti succedere di incidere troppo le commissure e dare origine quindi in un insufficienza mitralica; in età pediatrica, spesso per attendere la crescita del neonato/bambino, si può effettuare una valvuloplastica con palloncino

LEZIONE CHIRURGIA CARDIACA De Feo DEL 1/12/16
VALVULOPATIE AORTICHE
Stenosi valvolare aortica
Anatomia della valvola aortica: è costituita da 3 lembi che si attaccano direttamente sulla parete
ventricolare e separa la porzione finale di efflusso del ventricolo sinistro dall’aorta. Il lembo
valvolari sono: coronarico destro, coronarico sinistro e non coronarico. Si chiamano cosi perché
sottendono i seni di Valsalva delle 2 coronarie, dx e sx. Ciascun lembo è separato dall’altro tramite
una commessura. La commessura tra il lembo non coronarico e coronarico sx è posta lungo la zona
di continuità mitro‐aortica. Il lembo coronarico è in continuità con la porzione posteriore del tratto
di efflusso ventricolare sx e questa è la porzione collegata direttamente alla parete atriale dx. la
commessura tra cuspide coronarica dx e non coronarica è posta direttamente sopra il nodo atrio
ventricolare e il setto membranoso. La commessura tra cuspide coronarica dx e sx è opposta
invece alla commessura della valvola polmonare. La porzione laterale del seno coronarico sx è
l’unica porzione valvolare che non è in continuità con un’altra camera cardiaca ma è direttamente
correlata alla cavità pericardica.
Area della mitrale è di 5 cm2, quello della valvola aortica è di 3 cm2. Questo vuol dire che alti flussi
possono attraversare l’aorta senza che si verifichi in sistole una significativa differenza di pressione
tra ventricolo sx e aorta. Il meccanismo di apertura e chiusura della valvola è passivo ed è legato
alle variazioni di pressione tra camera ventricolare ed aorta durante il ciclo cardiaco.
La stenosi valvolare aortica è estremamente diffusa. Molto frequente nell’anziano
Può essere:
1) congenita (bambino) : Valvola unicuspide (al di sotto di un anno di età).
Valvola bicuspide (fusione delle commessure, è la più
frequente. Compare nel bambino e poi lo riscontriamo in età adulta. Non è una patologia
vera e propria ma è comunque una fragilità come accade per il prolasso della mitrale;
quindi se c’è un infezione è piu facile che attecchisca su questi punti di fragilità )
Poi ci sono la valvola diaframmatica e tricuspidale.
2) acquisita: degenerativa (senile, +65,70 anni)‐‐> è la più frequente. Se si manifesta più
precocemente allora si tratta di quelle forme congenite di valvola aortica bicuspide che poi
va incontro a calcificazioni. È il risultato del processo infiammatorio che determina
deposito di calcio a livello dei lembi (basi dei lembi cioè lungo le linee di flessione dove si
infiltrano i macrofagi e i linfociti T), delle commessure e l’anulus. Talvolta può accadere che
una valvola aortica tricuspide si comporti come bicuspide per chiusura di una commessura
da parte delle calcificazioni. Il processo di calcificazione può espandersi e coinvolgere sia
l'aorta in alto che la valvola mitrale in basso. Il processo si può anche estendere in fasi
avanzate alle carotidi e alle coronarie.

Tac toracica per vedere le calcificazioni valvolare aortica ma soprattutto quelle del tratto
ascendente dell'aorta; è importante per vedere se è possibile fare la circolazione
exstracorporea incannulando l’aorta. Questo si può fare solo nel tratto non calcifico. Stesso
discorso vale per il clampaggio che potrebbe essere ostacolato dalla calcificazione. Quindi è
importante per la strategia da usare per la sostituzione della valvola con aortotomia.
Fisiopatologia: Ostruzione al efflusso, aumento pressione del vsx, aumento della massa del vsx,
quindi anche il consumo con conseguente ipertrofia di tipo concentrica. Ischemia miocardica per
ridotta afflusso nelle coronarie e per ipertrofia miocardica.
Diagnosi: ecocardio transtoracico per la valvola aortica. Mentre per la valvola mitrale molte
informazioni ce le dà l’ecotransesofageo.
L’ostruzione si valuta con 2 parametri:
1) gradiente pressorio tra vsx e aorta: ( max , medio e minimo) gradiente medio > 40 mmHg
vi è indicazione alla chirurgia.
2) Orifizio aortica effettivo (area valvolare) ; stenosi severa quando l’area valvolare è <0,75
cm2 stenosi valvolare moderata :
0.76‐1 cm2
Stenosi valvolare lieve: 1‐2 cm2
Finché il ventricolo compensa il Pz è asintomatico ma dall'altro il rischio è quello della
morte improvvisa (perché il cuore lavora a pressioni intraventricolari molto alte visto che
l’orifizio è molto stretto). Quindi è una malattia un po’ subdola. Molto spesso vengono
operati pz con stenosi aortica severa del tutto asintomatici.
SINTOMI : triade caratteristica della stenosi aortica
‐ Angina: legata alla bassa portata anterograda ( a valle) questo vuol dire che la gittata
è bassa. Nel pz senza coronaropatia l’angina deriva dalla combinazione dell’aumento
delle richieste di ossigeno del miocardio ipertrofico e della riduzione dell’apporto di
ossigeno secondaria a eccessiva compressione dei vasi coronarici.
‐ Sincope: da ipoafflusso cerebrale sotto sforzo. Frequenti sintomi premonitori sono
l’ipotensione da sforzo, obnubilamento visivo e vertigini. Può essere anche una sincope
a riposo da fibrillazione atriale e ventricolare o blocco atrio‐ventricolare.
‐ Dispnea: se il processo patologico a causa di un aumento della pressione telediastolica
ventricolare si estende all'atrio sx e poi secondariamente al polmone con ipertensione
venosa polmonare. (stasi ematica a monte)
Prima si manifesta con dispnea da sforzo, poi con ortopnea, poi con dispnea
parossistica notturna.
Il pz può andare incontro a fibrillazione atriale e scompenso (potremmo rischiare di
perdere l’ammalato).

Focolaio di ascoltazione: sul 2 spazio intercostale dx sulla linea marginosternale. Soffio rude
eiettivo.
Ecg: segno di sovraccarico sistolico del vsx.
‐ Deviazione assiale sx
‐ R aumentato di voltaggio
‐ ST sottoslivellato
‐ T negativa
RX del torace: ipertrofia del vsx e calcificazioni.
Terapia: nell'anziano con valvola estremamente calcifica è un pò più difficile. Nell'infanzia
l'obiettivo è di dilatare la valvola transcatetere con palloncino per poi arrivare a una età tale da
poter fare la valvuloplastica con impianto di una protesi di un calibro adeguato che gli possa
durare per tutta la vita. La chirurgia è SOSTITUTIVA con protesi meccanica, biologica o un
omoinnesto fatto con tessuto di cadavere ( può essere una buona opzione terapeutica solo nei
pazienti con endocardite batterica recidivante).
Quest'ultimo però va facilmente incontro a calcificazione dopo 7‐8 anni così come l'aorta
sovrastante quindi non viene quasi mai usata.
La sostituzione della valvola aortica si fa in circolazione exstracorporea collegando l’ammalato alla
macchina incannulando in alternativa all'aorta la femorale e l'ascellare. Il problema si ha con il
clampaggio dell'aorta che potrebbe far staccare un pezzo di calcificazione. È una tecnica risolutiva.
Ipotermia moderata a 30‐32 gradi. Prima che il cuore fibrilli clampiamo l'aorta per arrestare la
circolazione. Cardioplegia come altro meccanismo di protezione per fermare il cuore in diastole
sotto il tratto dell'aorta clampata. Nell’insufficienza aortica invece dopo aver clampato apro l'aorta
in maniera traversa e vado ad iniettare la cardioplegia direttamente negli osti coronarici. Ci dà il
vantaggio di pulire il tutto dalle calcificazioni. L'unico svantaggio è l'invasività anche se oggi si fa in
sternotomia aprendo fino al 4 spazio intercostale. Oltre gli 85 anni ci sono rischi chirurgici legati
alle comorbidità quindi si fa una TAVI: si va nella valvola nativa tramite la arteria femorale (
procedura endovascolare), poi si gonfia il pallone x dilatare la valvola stenotica che potrebbe
staccare emboli di calcio, poi dopo la dilatazione si mettere la protesi che va ad incarcerare la
valvola nativa. È importante non toccare le pareti calcificate nel passaggio attraverso l'aorta , ma
nella maggior parte dei casi il rischio si ha nella dilatazione con palloncino della valvola. Se la
valvola non è messa bene il paziente potrebbe avere insufficienza valvolare. Potrebbe dare
ostruzione coronarica se l'impianto va ad ostruire il seno coronarico. Può dare anche complicanze
vascolari. La principale complicanza è il distacco della protesi e il distacco di emboli di calcio. TAVI
trans apicale e trans aortico come alternativa alla TAVI con arteria femorale.
È più facile che possa embolizzare un po’ di calcio che sta sulla valvola rispetto a se vai a toglierlo
completamente perché noi andiamo a buttare l’acqua sulla valvola e nel ventricolo per un lavaggio
a fine procedura. La prevenzione dei blocchi: verosimilmente se la protesi non è impiantata
perfettamente nel punto in cui deve stare può dare fenomeni di blocco e le prime casistiche di

incidenza di impianto di pacemaker dopo una TAVI era del 23% (non poco); se non è messa nel
punto giusto ad esempio davanti all’ostio coronarico (la distanza non è tantissima) può dare
occlusione coronarica e difficilmente il paziente sopravvive
L’altra complicanza è quella vasclare periferiche se è vero che al paziente non abbiamo fatto un
intervento tradizionale perche ha l’aorta calcifica probabilmente ha anche le femorali calcifiche
(problemi vascolari periferici)
Se l’EURO score non è alto e il rischio non è alto oggi si fa sempre la sostituzione.
Se c’e rischio proibitivo o comunque delle comorbità che ci impediscono l’intervento tradizionale
sicuramente è indicata la tavi; la forma di utilizzo più frequente per una tavi è la via transfemorale
oppure esistono quelle trans apicale o anche trans aortico per procedure ibride.
Se nella stenosi c’è un restringimento dell’area valvolare, nell’insufficienza abbiamo una mancata
o ridotta coartazione dei lembi valvolari durante la diastole.
Il meccanismo normale di chiusura della valvola aortica è passivo, legata a variazioni di pressione
tra la camera ventricolare e l’aorta durante il regolare ciclo cardiaco.
Esiste una forma congenita poco frequente legata alla valvola bicuspide mentre la forma acquisita
può essere primitiva o secondaria.
Nell’adulto l’insufficienza aortica è legata in linea di massima alla valvola che degenera; finché il
ventricolo compensa, il paziente è paucisintomatico o completamente asintomatico ma
nell’insufficienza l’ipertrofia è di tipo eccentrica, a differenza della stenosi, e quindi avremo
progressiva dilatazione del ventricolo e in un paziente giovane la valvola in questo momento va
sostituita (quando il ventricolo supera i 5,5 cm e va operato senza aspettare)
Nell’ aneurisma dell’aorta la valvola è salva a meno che non interessi anche la radice dell’aorta
ascendente, però è quasi sempre il contrario cioè l’insufficienza porta ad aneurisma.
La forma più frequente di insufficienza aortica acuta è la dissezione dell’aorta ascendente
(slaminamento aorta, formazione di un foro nell’intima che si rompe, intima e avventizia si
slaminano quindi l’intima si stacca dall’aorta portando con se l’anello e la valvola diventa
insufficiente e quindi dobbiamo cambiarla; di per se la valvola è sana ma risulta staccata,se
l’insufficienza è lieve potremmo anche lasciargliela perché si potrebbe riparare da sola dopo aver
riparato le tuniche) [DOMANDA CHE IL PROF NAPPI FA SPESSO]
Forme di dissecazione:
Forma A: interessa aorta ascendete;
forma B: dopo istmo, aorta toracica discendente con terapia endovascolare, si operano con
endoprotesi
Le forme più frequenti di insufficienza acuta della valvola:
La forma calcifica dell’anziano a cui si associa spesso gotto vizio
La malattia reumatica è più rara
Forme degenerative della valvola
steno insufficienza
Endocarditi
In seguito a trauma (rara)
Forme secondarie poco frequenti

Fisiopatologia:
si ha un notevole rigurgito di sangue, quindi una progressiva dilatazione del ventricolo sx che
risponde con ipertrofia eccentrica e poi con la dilatazione, la quale è un campanello d’allarme che
ci fa decidere di operare soprattutto se in diastole supera i 5.5 cm e in sistole 4 cm.
Da un punto di vista clinico il paziente è asintomatico; poi con insufficienza severa il paziente
diventa dispnoico, dispnea da sforzo, ortopnea, dispnea parossistica notturna solo nella fase
tardiva può avere angina e fenomeni aritmici, extrasistolia, tachicardia.
Le manifestazione della forma acuta (trauma o dissecazione) possono esordire anche con edema
polmonare o shock cardiogeno.
Auscultazione: soffio da rigurgito sul secondo spazio intercostale, margine sternale dx, molto più
dolce rispetto a quello della stenosi più rude
La Diagnosi è ecocardiografica; la radiografia può darci solo la dilatazione ventricolare ma nessuna
diagnosi solo sospetto di patologia. L’eco ci dice come sono le cuspidi, come è la radice se è
dilatata o se c’è prolasso della valvola, le misure in sistole e diastole e quindi decidiamo se
operare o no volume e massa .
Con doppler conosciamo anche la quantità di sangue rigurgitata.
La Terapia dipende da eziologia: in endocardite bisogna sterilizzare il paziente con 4 settimane di
antibiotici mirati o almeno che il paziente sfebbri per metterlo in circolazione extracorporea,
discorso a parte ovviamente per casi urgenti in cui rischiamo e operiamo senza sterilizzare.
Chirurgia: si va sempre a sostituire la valvola. Ad esempio però in insufficienza
moderata/moderata severa con prolasso di uno dei lembi ma valvola salva possiamo fare plastica
in centri esperti.
Quando abbiamo un paziente con insufficienza aortica severa con dilatazione della radice aortica e
spesso anche ad aneurisma dell’ascendente, va sostituito l’intero blocco quindi non usiamo solo
valvola ma un tubo valvolato protesico; isoliamo osti coronarici li teniamo in sospeso
momentaneamente, si impianta tubo valvolato e su tubo impiantiamo coronarie (intervento di
bettal).

Protesi:
caratteristiche generali:
1‐ecocompatibile più basso livello di eventi trombotici
2‐sicure e durature (sia biologiche che meccaniche)
3‐buona performance emodinamica, gradiente emodinamico pari circa a 10 (meccaniche più basso
rispetto a quelle biologiche)
Tipologie:
meccaniche:
‐1° generazione, “a palla”: che erano affidabili e abbastanza durature, ma con flusso turbolento
‐2° generazione, “a disco”: unico disco mobile (performance non molto inferiori a quelle bidisco)
‐3° generazione, “bidisco”: oggi sono le uniche in commercio, due dischi semicircolari in carbonio
pirolitico con materiali sintetici che rivestono l’anello sempre di carbonio
Miglior performance emodinamica con apertura disco a 80° 85°
Sono stati svolti dei trial con On‐x: Bidisco a 90°, si pensava di poter evitare terapia anticoagulante
ottimizzando il flusso e che l’antiaggregazione fosse sufficiente ma ci sono stati dei morti e quindi
è stato abbandonata la sperimentazione
Vantaggi: durata illimitata
Svantaggi: deve essere trattata solo con terapia anticoagulante dicumarolica (cumadin);
meccanismo non fisiologico, rischio trombo embolico di solito è basso in sede aortica ma ci sono
persone con bassa compliance alla terapia che potrebbero avere un rischio maggiore
INR: valore di sangue che dobbiamo monitorare per sapere la terapia anticoagulante con protesi
aortica
‐tra 2 e 3 senza altre comorbidità (noi lo teniamo a volte anche sotto al due in sede aortica)
‐tra 2.5 e 3.5 in sede mitralica e tricuspidale (le pressioni diminuiscono)
inr 1.8 1.9: elimini rischi emorragici
inr troppo basso: evento trombo embolico sulla protesi
inr troppo alto: rischio emorragico da epistassi a emorragie cerebrali
Biologiche:
porcine o bovine (usate indifferentemente)
‐stented: con anello rigido in ferro rivestito di tessuto con tre lembi di pericardio bovino o porcino
‐stentless: senza supporto, solo materiale biologico [sono nate prima le stented poi l’anello è stato
rimosso considerando quelle persone con elevata superficie corporea ma anelli valvolari piccoli,
quindi avendo generalmente valvole di misure dispari 19/17 , per misure intermedie o inferiori la
rimozione dell’anello può aiutarci a guadagnare una misura] quando possibile comunque usiamo
sempre le stented.
Vantaggi: più fisiologica e la terapia anticoagulante va fatta solo per i primi tre mesi
Svantaggi: durata limitata, 10 15 anni

Le procedure endovascolari come la tavi si sono portate avanti per dilatare vecchie protesi
degenerate calcificate ad esempio “valv in valv” (dilato inserendoci una nuova valvola dentro ad
esempio per anziani con vecchie protesi senza nuova operazione invasiva)
Endocardite: maggiore causa di rischio per protesi meccaniche e biologiche, va sostituita la protesi
e il paziente per ogni intervento ortopedico o anche pedicure, manicure e qualsiasi procedura
invasiva deve fare profilassi antibiotiche (ampicillina).
Si può avere anche formazione di panno fibrotico o rottura di micro strutture della protesi.
Linee guida europee e americane:
sopra i 70 anni: protesi biologica
sotto i 60 anni: protesi meccanica
tra i 60 e 70 anni: valutare caso per caso in base alle caratteristiche del paziente, comorbidità,
aspettative vita, compliance terapia anticoagulante

LEZIONE CHIRURGIA CARDIACA (Prof. Nappi) 02‐12‐16
CHIRURGIA DELL’AORTA
Le patologie dell’aorta sono particolarmente rilevanti perché danno luogo ad una serie di diagnosi
differenziali e sono spesso oggetto di errori diagnostici; inoltre, l’approccio chirurgico all’aorta non
è semplice.
[Evoluzione delle tecniche chirurgiche per il trattamento delle patologie dell’aorta. Nel ’38:
inserimento di spirali di metallo negli aneurismi dell’aorta per provocare la trombosi
intravascolare e ridurre la possibilità di rottura. Successivamente si passò all’utilizzo di un trapping,
cioè avvolgere l’aorta con materiale sintetico in maniera tale che non si rompesse. Negli anni 50‐
60: sostituzione di un ramo dell’aorta con Homografts (materiale autologo biologico) o con
materiale sintetico (Vinyon). Successivamente utilizzo del Teflon. Nel ’68 ci fu l’introduzione di un
materiale protesico (ancora oggi usato), il Double Velour, ma dati i problemi (era poroso al sangue)
si passò ad impregnarlo con gelatina e collagene (buona tenuta). Nel ’90: la colla biologica. Negli
ultimi anni: utilizzo di endoprotesi].
L’aorta è una struttura vulnerabile perché povera di fibrocellule e ricca di tessuto elastico. Essa è
sede di processi degenerativi (degenerazione cistica o conseguente ad un processo
aterosclerotico).
Classificazione delle patologie dell’aorta: acute e croniche.
Le sindromi aortiche acute (AAS) indicano un insieme di condizioni più o meno interconnesse tra
loro e con sintomatologia clinica e gestione terapeutica simili.
Dissezione dell’aorta.
Ematoma intramurale (IMH).
Ulcera aterosclerotica penetrante (PAU).
Rottura dell’aorta.

Patogenesi. Si può parlare di AAS in caso di:
Lacerazione dell’intima o ulcera penetrante l’intima che consente il passaggio di sangue dal
lume vero, attraverso l’intima, nella parete dell’aorta.
Ematoma intramurale: accumulo di sangue nella parete aortica tra tunica media e l’intima
(a livello della membrana elastica interna). In questo caso non c’è una lacerazione ma la
rottura dei vasa vasorum della parete aortica.
In entrambi i casi l’aorta è dissecata, cioè si crea un doppio lume: lume vero (quello dell’aorta
normale) e lume falso (per separazione dell’intima dalla media a livello della membrana elastica
interna).
Il sangue penetra nella parete aortica e si propaga prossimalmente (verso il cuore) o distalmente
(verso la periferia) ed incontra i rami che originano dall’aorta.
Esempio: Lacerazione dell’aorta ascendente. Il sangue penetra e si propaga distalmente. Il primo
ramo che incontra è il tronco brachiocefalico (tronco comune) dissecandolo circolarmente e
comprimendo il lume vero (primo meccanismo di ipoperfusione nelle aree di distribuzione del
tronco brachiocefalico: cervello e braccio). L’intima si stacca, si invagina su sé stessa, chiude il
flusso di sangue ed il ramo rimane attaccato all’aorta mediante la sola avventizia. L’ematoma
progredisce (se distalmente incontra la carotide sinistra, la succlavia sinistra). L’ematoma può
rompersi all’esterno: se arriva a livello dell’aorta toracica discendente si romperà in pleura; se si
propaga prossimalmente si può rompere nel pericardio causando un emopericardio e
tamponamento cardiaco (incontrerà le arterie coronariche con conseguente malperfusione del
cuore e quindi ischemia cardiaca, infarto). Può andare in diagnosi differenziale con un’angina, un
infarto del miocardio, un ictus cerebrale, un addome acuto, un’ischemia dell’arto inferiore (si può
presentare come una dissezione dell’arteria femorale: arto freddo, ischemico).

Fattori di rischio. Non c’è un’eziologia delle AAS, ma ci sono fattori di rischio (fattori
predisponenti):
Ipertensione
Fumo
Cocaina
Dislipidemia
Sindromi genetiche (s. di Marfan e s. di Turner)
Disordini autoimmuni
Infezioni (spirilli e tubercolosi)
Fattori iatrogeni (cateteri)
Quadro clinico. I pazienti affetti da AAS hanno presentazione clinica più o meno simile
indipendentemente dalla condizione sottostante.
Dolore trafittivo, lancinante, estremamente intenso. Il dolore può essere migrante (perché
l’ematoma può propagarsi). È talmente forte che non cessa con la morfina (a differenza del dolore
dell’ischemia cardiaca). Per la cessazione del dolore è necessario correggere i due fattori che sono
la causa della propagazione dell’ematoma: la pressione arteriosa e la velocità d’eiezione del
ventricolo sinistro. Quindi per far passare il dolore bisogna diminuire la pressione arteriosa e la
frequenza cardiaca (perché la velocità d’eiezione del VS è dovuta ad una differenza di pressione e
una differenza di tempo). La pressione può essere abbassata fino a quando viene garantita la
perfusione degli organi (essenzialmente gli organi addominali). Per la valutazione della perfusione
il parametro essenziale è la diuresi: fino a quando il paziente urina si può abbassare la pressione.
Per abbassare la pressione si utilizzano farmaci (antipertensivi) a rapida azione e di breve tempo.
Per diminuire la frequenza cardiaca si utilizzano i beta bloccanti. È necessario somministrare prima
il beta bloccante e poi l’antipertensivo (perché una diminuzione della pressione può dare di
riflesso un aumento della frequenza cardiaca).
Tutti i pazienti stanno molto male. Stanno in shock cardiogeno: è l’unico shock cardiogeno a
pressione alta (perché per definizione lo shock cardiogeno è a pressione bassa).
Il paziente è sudato freddo, la cute è pallida, la pressione è alta. Può accadere che misurando la
pressione al braccio destro essa sia alta e misurandola al braccio sinistro essa sia bassa;
rimisurandola al braccio destro non c’è più pressione (perché l’ematoma si è spostato e può aver
chiuso il tronco brachiocefalico). Il polso può comparire e scomparire (a seconda di come si muove
l’ematoma). Misurando la pressione essa è alta, ma c’è un caso in cui la pressione è bassa: quando
la dissezione è complicata (per esempio c’è un’emorragia). L’ematoma si è rotto all’esterno: se si
rompe in pleura ci sarà versamento pleuro‐ematico e quindi shock ipovolemico (la pressione è
bassa); se si rompe nel pericardio ci saranno ipovolemia e tamponamento cardiaco da
compressione.

Le AAS hanno delle peculiarità: nella dissezione si può avere sincope; nell’ematoma intramurale:
più dolore (ma meno intenso rispetto alla dissezione aortica); l’ulcera penetrante (non in fase
dissecante) può essere asintomatica.
DISSEZIONE AORTICA
È la più comune manifestazione delle AAS. Più frequente nel sesso maschile rispetto a quello
femminile (ma nella femmina la sintomatologia è più drammatica).
Classificazione della dissezione aortica
1. Classificazione temporale
Acuta: meno di 2 settimane dall’inizio della sintomatologia
Subacuta: tra 2 e 6 settimane
Cronica: oltre 6 settimane
2. Classificazione anatomica (Classificazione di De Backey). Si basa sulla localizzazione
dell’entry tear (porta d’entrata) e sull’estensione della dissezione.
I: lacerazione (porta d’entrata) in aorta ascendente e dissezione che interessa tutta l’aorta.
II: lacerazione in aorta ascendente e dissezione che si ferma prima dell’emergenza del
tronco brachiocefalico.
III: lacerazione in aorta toracica discendente (dopo l’origine della succlavia sinistra) ed
ematoma dissecante che si propaga nell’aorta toracica (se si ferma all’aorta toracica:
sottotipo A; se va oltre il diaframma: sottotipo B).
3. Classificazione di Stanford
A: comprende tutte le dissezioni che coinvolgono l’aorta ascendente. Vengono aggredite
chirurgicamente con una sternotomia mediana.
B: comprende le dissezioni che non coinvolgono l’aorta ascendente. Vengono aggredite
chirurgicamente con una toracotomia laterale.
(I e II De Backey sono incluse in Stanford A; III De Backey fa parte di Stanford B)

4. Classificazione clinica (Classificazione dell’Università della Pennsylvania). Permette di
comparare la gravità dei pazienti in rapporto ai risultati chirurgici. Si basa sulla
presentazione in 4 profili a seconda della presenza/assenza di fenomeni ischemici di vari
organi.
Classe A: paziente senza collasso cardiocircolatorio e senza malperfusione di qualche
branca (paziente che sta relativamente abbastanza bene).
Classe B: paziente con malperfusione di qualche branca (c’è angina, infarto o addome
acuto) ma senza collasso cardiocircolatorio.
Classe C: collasso circolatorio con o senza coinvolgimento cardiaco.
Classe B+C: collasso cardiocircolatorio e malperfusione di qualche branca.
Figura (in basso): Lacerazione intimale attraverso cui passa il sangue. Doppio lume. L’ematoma
può propagarsi (prossimalmente o distalmente), comprimere i vasi e può staccarsi: incontra le
arterie intercostali, le arterie renali (blocco renale), il tripode celiaco (addome acuto).

Figura (De Backey):
I: coinvolgimento di tutta l’aorta
II: si ferma a livello del tronco anonimo
III: interessamento dell’aorta toracica (ed eventualmente di quella addominale)

Figura (Stanford)
A: coinvolgimento aorta ascendente (I e II De Backey)
B: non c’è coinvolgimento dell’aorta ascendente (III De Backey)

Diagnosi e prognosi di dissezione aortica
Come si fa la diagnosi strumentale di dissezione aortica? Si può fare con l’aortografia, che è una tecnica
che ormai non si usa più; molto usato invece è l’angio‐TAC che ha un’alta sensibilità e specificità; la
risonanza magnetica ha anch’essa un’alta specificità e sensibilità ma non tutti gli ospedali ne sono muniti.
L’esame principe che ci dà almeno un’idea è l’ecocardiografia sia trans‐toracica sia, con una ancor
maggiore specificità, quella trans‐esofagea (che comunque ci darà alcune “finestre oscure” come l’arco
dell’aorta). Quello che ci interessa di più con questi esami è vedere la “porta di entrata” (ovvero la prima
lacerazione) e l’estensione della dissezione. Molto praticamente il primo esame da fare è l’eco trans‐
toracica poi, eventualmente, si passa all’eco trans‐esofagea (gold standard). Questo è un esempio storico
di aortografia della dissezione aortica che non si fa più, si può apprezzare il falso lume e la grande
compressione dell’aorta toracica discendente.
Qui è possibile vedere l’immagine intraoperatoria in cui è possibile vedere la lacerazione nell’intima (con
tanto di falso lume) con aspetto generalmente sanguinolento dell’aorta da operare.

Vediamo adesso la prognosi:
Nella dissezione di tipo A la mortalità senza trattamento chirurgico è del 1 o 2% ALL’ORA. Dopo una
settimana la mortalità è del 58%; in questo grafico possiamo vedere la tendenza alla mortalità dei pazienti
con dissezione di tipo A e B, altissima nel caso della A e più bassa nel caso della B. Il tipo A è dunque
un’emergenza chirurgica, il tipo B (NON COMPLICATO) prevede semplicemente un trattamento medico.
Ematoma intramurale, ulcere penetranti e altre sindromi acute
Spendiamo ora qualche parola sull’ematoma intramurale che, ricordiamo, fa parte delle sindromi aortiche
acute. Può essere anche precursore della dissezione aortica perché se si crea una lacerazione nell’intima
causata dall’ematoma si avrà una dissezione aortica. Il sintomo principale è costituito dal dolore dato che la
malperfusione degli organi è un evento raro poiché vi rendete conto che si sposta nel circolo sanguigno
come ematoma dissecante. Dal 30 al 50% dei casi può evolvere in dissezione aortica o, eventualmente, può
rompersi.
Le ulcere penetranti possono essere anche asintomatiche: sono delle placche aterosclerotiche che
penetrano nella parete dell’aorta (preferendo l’aorta toracica discendente) e anch’esse possono
trasformarsi in dissezione aortica o addirittura possono perforarla.
Ripetiamo rapidamente le linee guida per quel che riguarda la dissezione aortica: I tipi I e II di DeBakey (tipo
A) sono emergenze chirurgiche (insieme al tipo III COMPLICATO), differentemente dal tipo III di DeBakey
(senza complicazioni come malperfusione,dolore non controllabile, ovvero il tipo B) che può essere trattato
clinicamente.
L’ematoma intramurale viene trattato esattamente come una dissezione aortica (operare se nell’aorta
ascendente, trattare se nella discendente); per l’ulcera il trattamento è medico o chirurgico se interessa
l’aorta ascendente.
Vi presento adesso un caso clinico molto particolare di un paziente di 19 anni: nato con un piccolo difetto
interventricolare che si è risolto da solo; verso i 4 o 5 anni ebbe la chiusura del dotto di Botallo e poi più
tardi fu operato per un difetto interatriale, chiuso da un Amplatzer, un doppio disco metallico inserito
tramite cateterismo all’altezza della zona interatriale, risolvendo il problema. A un dato momento

sottoponendosi ad un ecocardiogramma di controllo ci si accorse che qualcosa non andava: dopo un’angio‐
TAC si scoprì che questo ragazzo aveva una dissecazione all’aorta ascendente, probabilmente causata
dall’Amplatzer (magari un po’ troppo grande) che, posto sul setto interatriale ad un dato momento
avrebbe dissecato il tetto dell’arco di sinistra dell’aorta.
Tra le varie sindromi acute che abbiamo menzionato sono presenti anche le rotture aortiche fulminanti (il
paziente muore immediatamente) , fissurate (dal sangue) o coperte (da coaguli). La sede più frequente
delle rotture è a livello dell’istmo. Queste rotture possono essere causate da aneurismi. Qual è la
differenza fra aneurisma e pseudoaneurisma? Mentre l’aneurisma vero è costituito dalla dilatazione di
tutti e tre gli strati del vaso, lo pseudoaneurisma non li interesserà tutti a livello istologico: un classico
esempio di pseudoaneurisma è una dilatazione del vaso dovuta ad un trombo posto AL DI FUORI della
parete aortica. L’esattezza della localizzazione e la tempestività della diagnosi sono cruciali per la
sopravvivenza del paziente.
Patologie croniche dell’aorta
Naturalmente tra le patologie croniche dell’aorta ci sarà una dissezione cronica. Gli aneurismi, di qualsiasi
eziologia se cardiogena o da microrganismi, possono causare rottura dell’aorta o dissezioni croniche. Il fatto
che essi siano in grado di causare questa rottura è regolato dalla legge di Laplace che ci dice che la tensione
della parete aortica è direttamente proporzionale alla pressione che esercitano gli aneurismi sulla stessa e
al loro raggio. Le indicazioni chirurgiche prevedono la rimozione di aneurismi con diametro> di 5cm oppure,
criterio più valido, quando il loro tasso di espansione è > di 0.3 cm all’anno, ovviamente il tutto applicato
alla sintomatologia clinica e alla patologia di base. Morfologicamente gli aneurismi possono essere
fusiformi o sacciformi e da questo possiamo dedurre che la sintomatologia varia a seconda del tipo di
aneurisma che andiamo ad analizzare e a seconda della localizzazione: se si trova a ridosso dell’arco aortico
per esempio potremmo riscontrare la presenza di disfagia, tosse e raucedine (a causa della compressione
del nervo laringeo ricorrente) oppure in seguito alla compressione del ramo bronchiale. Chirurgicamente si
procede ad isolare l’arteria a monte e a valle e ad introdurre una protesi. Naturalmente se l’aneurisma
interessa l’aorta ascendente (che non posso clampare) c’è bisogno di ricorrere alla circolazione
extracorporea (a differenza di un ramo o della stessa aorta addominale); se invece interessa l’arco
dell’aorta c’è bisogno di desanguinare completamente il paziente procedendo alla perfusione cerebrale
per preservarlo.
Da qualche tempo sono state introdotte le endoprotesi aortiche (esempio in basso) che sono strutture
metalliche (nitinolo) a memoria di forma, con all’interno un altro materiale (PFE) e dei gancetti alle
estremità per aderire. Questa endoprotesi viene chiusa su un catetere che sotto guida angiografica viene
posizionata nel luogo in cui vogliamo posizionarla (in corrispondenza di una dissezione di tipo B, di un
aneurisma cronico o di un’ulcera penetrante). E’ importante che prossimalmente e distalmente l’aorta dia
abbastanza spazio per far agganciare la protesi da entrambe le parti. Il nitinolo a 37° nell’organismo si apre
e si va a schiacciare contro l’aorta. Ovviamente questo processo prevede una guida preferibilmente trans‐
esofagea.

Questa è una tipica endoprotesi aortica e sotto la sua posizione in relazione alle altre strutture toraciche.
Imaging dell’aorta prima e dopo l’inserimento della protesi

Immagine ecocardiografica di una endoprotesi aperta (molto simile a quella chiusa).

Lezione di Chirurgia Cardiaca del 9.11.16
TRAPIANTO CARDIACO Per parlare di trapianto deve esistere un ricevente ed un donatore, in questo senso daremo delle
indicazioni su che tipo di persona è il ricevente è chi è il donatore, quali sono i criteri di scelta.
Alcuni elementi semplici di fisiologia.
Il cuore è la pompa che ha la funzione di far circolare il sangue nel sistema circolatorio. Il ventricolo
destro che voi sapete regge una circolazione a basse resistenze, il circolo polmonare. Il ventricolo
sinistro regge una circolazione ad alte resistenze.
In medicina il parametro che descrive la contrattilità dei ventricoli è la frazione d’eiezione. La
frazione d’eiezione che descrive la capacità di svuotamento delle camere ventricolari ha un numero
che spesso i pazienti e anche i medici non esperti credono che la normalità sia pari al 100% (il 100%
non esiste). La normalità è 55‐65.
Quando scende sotto il 30% allora cominciano a comparire i problemi per il paziente.
Il paziente che viene sottoposto a trapianto è un paziente che è in scompenso cardiaco.
Lo scompenso cardiaco è un quadro clinico che deriva da ogni danno cardiaco strutturale e
funzionale che riduce la capacità del ventricolo di riempirsi o di pompare sangue nel circolo.
Distinguiamo le forme primitive e secondarie che portano allo scompenso cardiaco.
Le forme primitive sono le cardiomiopatie (ipertrofica, aritmogena, dilatativa, restrittiva).
Forme secondarie come la miocardite (anche una semplice influenza può determinarla),
una cardiomiopatia post‐ischemica, una cardiomiopatia post valvolare (determinata da una
lunga storia naturale di valvulopatia).
Il problema dello scompenso cardiaco, che attraversa vari stadi, è notevole. Negli stati uniti si
contano 5.000.000 di individui affetti da scompenso.
A questo si aggiunge che la mortalità da scompenso cardiaco terminale è elevatissima, ad un anno
si attesta al 25%. (HIV 90%, Leucemia 65%, Cancro al Polmone 42% ad un anno dalla diagnosi).
La causa più comune di trapianto sono le cardiomiopatie primitive (anche se non sono la causa più
frequente di scompenso, bisogna però considerare che queste patologie compaiono in soggetti
giovani e che presentano quindi più facilmente tutte le indicazioni al trapianto come l’età,
l’assenza di comorbilità e infezioni rispetto ad un soggetto anziano che ha uno scompenso ad
esempio post ischemico).
Lo scompenso attraversa varie fasi
1. Tappa asintomatica – ace inibitori, beta‐bloccanti
2. Sintomatica, il sintomo è la dispnea
3. Fase terminale, refrattaria alla terapia

Il trapianto va nella direzione dei soggetti terminali, ovvero che nonostante l’utilizzo di un
approccio farmaceutico massimale non riescono ad avere una vita normale. Sono quei pazienti
classe NYHA 4, ovvero quelli affetti da dispnea a riposo.
Qual è l’obiettivo del trapianto del paziente?
1. Aumentare la sopravvivenza (25% ad un anno per lo scompenso)
2. Ridurre l’incidenza delle complicanze
3. Migliorare la qualità della vita del paziente (aumentare la capacità d’esercizio)
4. Ridurre la sintomatologia
Slide confronto sopravvivenza trapianto scompenso
Il trapianto va selezionato nella maniera più attenta possibile, perché il numero dei cuori è
limitato. Bisogna quindi valutare bene le indicazioni e le controindicazioni del ricevente.
Figura 1; Riportata per approfondimento, il professore non ha indicato tutte queste informazioni ma solo quelle descritte sotto
Le indicazioni:
1. Grave scompenso con rischio di morte al 75% non responsivo a terapia medica
2. VO2 < 10 ml/kg/minuto (questa è sempre un indicazione al trapianto)

Le controindicazioni:
1. Qualsiasi condizione non cardiaca che può ridurre l’aspettativa di vita del paziente
Come:
a. Età – inferiore ai 65 anni (70% in altri centri)
b. Assenza di patologie a carico di altri organi o apparati
c. Buona compliance alla terapia medica
d. Stabilità psico‐sociale – è fondamentale perché il paziente andrà incontro a numerosi
controlli e una lunga terapia
Le controindicazioni assolute:
1. Ipertensione polmonare severa e irreversibile – il ventricolo destro del donatore andrebbe
subito in scompenso dato le pressioni notevoli del piccolo circolo
2. Infezioni sistemiche in fase attiva – dato che il ricevente va incontro a terapia
immunosoppressiva
3. Insufficienza renale irreversibile o epatica irreversibile – a meno di trapianto combinato
Controindicazioni relative:
1. Età
2. Infezioni come Epatite,HIV
3. Diabete Mellito scompensato (insulino dipendente)
4. Abuso di alcol e droghe
La storia ha inizio nei primi anni del 1900, il primo trapianto di cuore fu fatto nel 1965 da Barnard a
città del capo, in Sudafrica diventando una delle più grandi celebrità del mondo.
In Italia è stato fatto nel 1985, a Napoli nel 1988.
L’attività cardiochirurgica in Italia inizia con il dottore Fabrizio De Vivo. A Napoli venne compiuto
dal Dottor Cotrufo, l’espianto del cuore fu fatto a Barcellona. Oggi i voli extranazionali non
esistono più, c’è un centro di coordinazione che organizza gli espianti.

Figura 2; La storia di Barnard è molto controversa
Il numero di trapianti in ogni centro è dai 20 ai 30. Il Monaldi è al secondo posto, segue il centro di
Trapianti di Bologna.
Trapiantare un cuore considerando le sue connessioni vascolari significa riconnettere le due cave
nelle sezione destre, connettere l’aorta e la polmonare e le vene polmonari. Questo è abbastanza
logico. Questa soluzione però chiedeva un tempo notevole perciò si è cercato di trovare altre
soluzioni.
In questo senso oggi si usa (quando possibile) la tecnica delle cuffie atriali dove vengono
mantenute le connessioni con le vene non rimuovendo la parte posteriore degli atrii (ci sono
controindicazioni a questo intervento, in particolare patologie a carico degli atrii).

Nel ricevente quindi si rimuove il cuore lasciando aorta e polmonare, si sezioneranno i due atri
lasciando le due cuffie.
Come si fa a proteggere il cuore dal momento in cui viene espiantato?
Lo si fa con una tecnica molto simile agli altri interventi cardiaci, cioè con cardioplegia, che in
questo caso si chiama Celsior, iniettata nelle coronarie prima dell’espianto. La Celsior è
leggermente diversa da quella utilizzata nella CEC perché permette un tempo di trasporto di 4 ore
senza dover essere ri‐iniettata rispetto alla classica che deve essere somministrata ogni 20 minuti
circa. L’organo espiantato si trasporta poi in ghiaccio.
Figura 3; riportata per approfondimenti, il professore non ha mostrato questa immagine a lezione
Riguardo il donatore:
1. La donazione rappresenta uno dei problemi più grandi dei trapianti
Il numero di donazioni non riesce mai a soddisfare le richieste di organo i motivi sono diversi:
a. Il 31% delle famiglie non accettano il trapianto d’organo (77% Bolzano, prima in assoluto,
Napoli è al 44%)
b. I politraumatizzati sono spesso i migliori candidati per il trapianto, le politiche atte alla
sicurezza stradale ha ridotto notevolmente il numero di potenziali donatori! (il professore
chiarisce che questa è una cosa positiva, ci mancherebbe)
c. La mancata conoscenza del significato di morte cerebrale; frequentemente le famiglie non
comprendono che la morte cerebrale è uno stato irreversibile (sotto si spiegherà che la
morte cerebrale è una condizione necessaria per il trapianto) ma confidano in un recupero
del parente.
Del donatore interessano due parametri fondamentali di compatibilità (imparateli sono semplici
e chiesti)
1. Stesso gruppo sanguigno (per motivi immunitari)
2. Superficie corporea simile
Il paziente che dona il cuore è un paziente di morte cerebrale

Stato irreversibile caratterizzato dalla totale e definitiva perdita delle funzioni cerebrali:
a. Stato d’incoscienza
b. Assenza di riflessi
c. Assenza di respiro spontaneo
d. Assenza di attività elettrica cerebrale (elettroencefalogramma piatto da almeno 6 ore negli
adulti, 24 ore nei bambini)
e. Evidente riduzione della temperatura corporea
f. Arresto del flusso cerebrale
Tutto questo viene accertato da una triade di medici che sono: medico legale, anestesista
rianimatore e neurologo.
Dal punto di vista organizzativo il centro trapianto provvede al trasporto, l’equipe parte dal
proprio ospedale e va a prendere il cuore. I centri trapianti sono 3:
1. Uno nord italia
2. Uno nel centro
3. Uno del sud, OCST, di cui fa parte il Monaldi.
Questa divisione non è così netta, alcune regioni del sud fanno parte di centri del nord.
L’equipe prende i dati del donatore, controlla se è presente un paziente compatibile e se questo si
verifica l’equipe parte mentre il ricevente viene portato in camera operatoria e preparato.
Problematica per il ricevente che riceve il trapianto è il rigetto d’organo.
1. Rigetto d’organo acuto
2. Rigetto d’organo cronico
La ciclosporina1 ha rivoluzionato il mondo della cardiochirurgia avendo dato la possibilità
dell’immunosoppressione farmacologica. Ad oggi sono stati trovati nuovi farmaci e si usano
combinazioni di questi.
La terapia deve essere adeguata, perché un’eccessiva immunosoppressione predispone alle
infezioni, una ridotta immunosoppressione favorisce la storia naturale del rigetto (che è
inevitabile, i tempi possono essere fortunatamente molto lunghi, ma è inevitabile).
Come si fa a valutare un rigetto?
1. La clinica come l’ecocardio, se si osserva una riduzione della funzione di pompa si può
sospettare il rigetto
2. Mediante biopsia, inizialmente ogni 7 giorni successivamente ogni 15 il paziente viene
sottoposto a biopsia endomiocardica. Attraverso la giugulare viene inserito un miotomo
che portato al setto interventricolare destro permette l'acquisizione di tessuto da studiare
in anatomia patologica.
1 The immunosuppressive effect of the natural product cyclosporin was discovered in December 1971 in a screening test on immune suppression designed and implemented by Hartmann F. Stähelin at Sandoz

Se ci sono segni di rigetto la terapia immunosoppressiva verrà
aumentata.
Col tempo nonostante l’ottimizzazione della terapia, il rigetto cronico
colpirà inevitabilmente il paziente. Il cuore trapiantato ha una durata
media di 15‐20 anni. Il paziente andrà incontro ad un altro trapianto.
Il problema del rigetto cronico è che non colpisce tanto il muscolo
cardiaco (almeno inizialmente) ma piuttosto le coronarie. Lo stato
d’infiammazione cronico legata al rigetto determina un ispessimento
della parete che comporta con il tempo un occlusione del lume del vaso.
Questo tipo di occlusione è impossibile da trattare chirurgicamente perché interessa tutto il vaso,
non è possibile fare quindi un by‐pass il cui razionale è appunto superare a mo’ di ponte il tratto
stenotico.
La terapia immunosoppressiva può dare altre complicanze le cui più temibili sono sicuramente i
tumori.
A 20 anni il 50% dei pazienti trapiantati sono morti. Ciò non di meno se si considera la condizione
di partenza (25% sopravvivenza ad un anno) una sopravvivenza di 15 anni in più è un ottimo
risultato.
Ad oggi l’impianto di cuori artificiali sembra essere una strada percorribile per ovviare ai soggetti
che non possono avere un trapianto.