Lez 15 Sistematica Inorganica 7 8 Chimica Solidi.ppt [modalità … · 2017-06-09 · per...
Transcript of Lez 15 Sistematica Inorganica 7 8 Chimica Solidi.ppt [modalità … · 2017-06-09 · per...
Lezione 15 01/06/2017
1
Sono non-metalli. A causa della loro reattività non sono mai presenti in natura nella
loro forma elementare. Il F è l’ossidante più energico tra gli elementi (E = +2.87V).
L’At è radioattivo.
Nicola Margiotta 2016/2017
L’At è radioattivo.
Nicola Margiotta 2016/2017
Lezione 15 01/06/2017
2
Il F2 si ottiene per elettrolisi di KF fuso o sciolto in HF anidro. HF si usa per produrre UF6 (vedi radioattività), SF6 e sostanze come il Teflon ed il Freon. Il Cl2 (fortemente ossidante) si ottiene per elettrolisi di NaCl fuso o delle salamoie (vedi) e si usa in molti processi industriali e come sbiancante e disinfettante dell’acqua.
Nicola Margiotta 2016/2017
Il Br2 è un liquido corrosivo, rosso, bruno e fumante. Lo I2 solido si ricavava dalle alghe marine e dalle salamoie dei pozzi di petrolio (sublima facilmente ed è un oligoelemento essenziale per l’uomo). L’At è radioattivo.
Nicola Margiotta 2016/2017
Lezione 15 01/06/2017
3
Il F2 reagisce con H2 in maniera esplosiva. Il Cl2 esplode con H2 in presenza di luce. Tutti gli HXsono gas incolori e di odore pungente (solo HF è liquido sotto i 20 °C a causa dei legami ad H). In acqua formano soluzioni acide (HF è in grado di sciogliere anche il vetro).Ca(ClO)2 si usa per purificare le piscine private. KClO3 si usa nei fuochi d’artificio e nei fiammiferi. HClO4 è l’acido più forte fra quelli di impiego comune. I perclorati sono forti ossidanti ed esplosivi.
Gli ossiacidi del cloro sono tutti agenti ossidanti.
L’acidità e il potere ossidante degli ossiacidi
aumentano con l’aumentare del numero di ossidazione dell’alogeno.
Nicola Margiotta 2016/2017
Il primo composto di un gas nobile è stato preparato nel 1962: XePtF6
Successivamente fu preparato il XeF4.
Nicola Margiotta 2016/2017
Lezione 15 01/06/2017
4
Sono tutti presenti nell’atmosfera come gas monoatomici e si ottengono per distillazione dell’aria liquida (tranne He e Rn). L’He è il secondo elemento nell’universo (dopo l’H) ma sulla terra è raro perché sfugge dall’atm. Si accumula (es. giacimenti rocciosi) dove il Rn resta intrappolato sotto terra (vedi radioattività). Non è infiammabile e si adopera per gonfiare dirigibili, palloni. Si usa come fluido criogenico. Ar si usa anche come atmosfera nella saldatura. Il Rn è un gas radioattivo che esce dal terreno: vedi radioattività).
Ar
Ne
Kr
Xe
Nicola Margiotta 2016/2017
Nicola Margiotta 2016/2017
Capitolo 13 Kotz
Lezione 15 01/06/2017
6
Nicola Margiotta 2016/2017
Nicola Margiotta 2016/2017
Le strutture dei solidi possono essere descritte come reticoli 3D di atomi, ioni,molecole.
Per un solido cristallino si definisce come CELLA ELEMENTAREla più piccola unità che si ripete e che possiede in sé tutte le caratteristiche disimmetria della disposizione degli atomi, degli ioni o delle molecole delsolido.
La cella elementare deveriflettere la stechiometriadel solido
Lezione 15 01/06/2017
7
RETICOLI DI
BRAVAIS
In natura esistono sette tipi dicelle elementari tridimensionaliche costituiscono i reticolicristallini.
Lezione 15 01/06/2017
8
Nicola Margiotta 2016/2017
Nel definire una cella elementare si cerca si posizionare gli atomi o gli ioni nei
PUNTI RETICOLARI cioè ai vertici del cubo o dell’oggetto
geometrico che costituisce la cella elementare.
Assemblaggio 3D del RETICOLO CRISTALLINO
Nicola Margiotta 2016/2017
Simmetrie delle CELLE CUBICHE
cp bcc fccAttenzione: sebbene indicato con colore differente l’atomo/ione alcentro può essere dello stesso tipo di quello ai vertici.
Lezione 15 01/06/2017
9
Nicola Margiotta 2016/2017
Nicola Margiotta 2016/2017
Reticolo cubico primitivo (cp)
Un atomo/ione in ogni cella elementare!
Lezione 15 01/06/2017
10
Nicola Margiotta 2016/2017
Reticolo cubico a corpo centrato (bcc)
Due atomi/ioni in ogni cella elementare!
Reticolo cubico a facce centrate (fcc)
Quattro atomi/ioni in ogni cella elementare!
Nicola Margiotta 2016/2017
Lezione 15 01/06/2017
11
Diffrazione della luce (o di una radiazione elettromagnetica)
Propagazione delle onde dopo che questeincontrano un oggetto o passano attraverso unpiccolo foro o una fenditura.
Nicola Margiotta 2016/2017
Diffrazione della luce attraverso una fenditura
Nicola Margiotta 2016/2017
Lezione 15 01/06/2017
12
Reticoli di diffrazione con più fenditure.
Nicola Margiotta 2016/2017
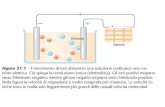
DIFFRAZIONE DI RIMBALZO SU RETICOLI
il cd riflette la luce incidente comportandosi come un reticolo di diffrazione che opera per riflessione, con passo d (distanza tra due solchi successivi) pari a d =1,6 ×10–6 m.
Nicola Margiotta 2016/2017
Lezione 15 01/06/2017
13
Nicola Margiotta 2016/2017
Determinazione della struttura cristallina: CRISTALLOGRAFIA AI RAGGI-X
Su cristallo singolo e su polvere.
Dalla struttura ai raggi-X si ricavano parametri come ad esempio ilraggio atomico (vedi esercitazioni).
Nicola Margiotta 2016/2017
Strutture (e formule) dei solidi ionici CsCl
Cella elementare cp di ioni cloruro con ioni cesioche riempiono le cavità (o viceversa!)
Ricavare formula
Lezione 15 01/06/2017
14
Nicola Margiotta 2016/2017
Strutture dei solidi ionici NaCl
Cella elementare fcc di ioni cloruro e ioni sodiodisposti regolarmente tra questi ioni.Calcolo formula:4 Cl− per ogni cella fcc + [(1Na+ centro cella) + (1/4Na+ per spigolo X 12 spigoli)]4 Cl− + 4 Na+ per ogni cella elementare.
Nicola Margiotta 2016/2017
Strutture dei solidi ionici ZnS
Cella elementare fcc di ioni solfuro e ioni zinco adoccupare metà delle 8 cavità tetraedriche(circondati da 4 ioni di carica opposta).Calcolo formula:4 S2− per ogni cella fcc + 4 Zn2+ = 4 S2− + 4 Zn2+ per ogni cella elementare.
Lezione 15 01/06/2017
15
htt
ps:/
/ww
w.f
ace
bo
ok.c
om
/ne
rdo
sita
Per sostenere l’esame si deve effettuare la prenotazione solo ed
esclusivamente on-line dal sito Esse3
Non si accettano prenotazioni per email
NO DOMANDE SU DATE/AULE/ORARIO-ESAMI per EMAIL!!!!
Si consiglia di controllare periodicamente la prenotazione on line per verificare eventuali modifiche dell’aula o dell’orario dell’esame.