InterazioniProteinaProteina. Consiglio... · 2014-07-10 · Unapremessanecessaria:*il*clonaggio*...
Transcript of InterazioniProteinaProteina. Consiglio... · 2014-07-10 · Unapremessanecessaria:*il*clonaggio*...

Interazioni Proteina-‐Proteina
Giorgia Batelli Federica Consiglio 25 Marzo 2014
Corso di Formazione Genhort

Interazioni proteina-‐proteina
Associazioni tra proteine: servono per la regolazione, espressione e organizzazione di ogni processo cellulare: Replicazione del DNA, Trascrizione, Traduzione, Splicing Controllo del ciclo cellulare, Trasduzione del segnale etc. etc.
Inizialmente lo studio delle interazioni era dominio esclusivo dei biochimici, oggi data la centralità in ogni processo cellulare, anche geneBsB, biologi cellulari, dello sviluppo, molecolari si trovano, per necessità, ad interessarsene

Interazioni proteina-‐proteina I conta> fisici tra proteine sono cruciali per il funzionamento della cellula
Si verificano in:
Complessi stabili: piruvato deidrogenasi, a-‐chetoglutarato deidrogenasi. Vantaggi di un oligomero rispeEo a un grande monomero: Possibilità di combinazioni diverse, Riduzione degli errori di trascrizione e traduzione; ComparBmentalizzazione della funzione.
Complessi transienB tra proteine che sono stabili anche indipendentemente: interazioni di chinasi, fosfatasi, glicosil trasferasi, acil trasferasi etc. etc. Vantaggi Alterazione anche momentanea e mirata delle caraEerisBche della singola proteina: affinità con un ligando, catalisi etc.

Interazioni proteina-‐proteina Perché ci interessano in studi di forward e reverse geneBcs????? • Analisi funzionale: Conoscere l’idenBtà delle proteine con cui la proteina oggeEo di
studio interagisce può dare indicazioni sulla funzione. Ad esempio, se la mia proteina X, di cui non conosco la funzione, interagisce con proteine note coinvolte nella risposta a stress, posso ipoBzzare che la proteina X sia in qualche modo coinvolta nella risposta a stress.
• Strategia di isolamento geni: Viceversa, se la mia proteina X è una proteina nota coinvolta nella risposta a stress, l’idenBficazione di proteina che interagiscono con essa può aiutarmi ad idenBficare proteine a funzione sconosciuta da studiare per quanto riguarda il loro coinvolgimento nella risposta a stress

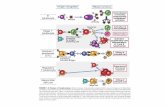
Metodi di invesBgazione di interazioni proteina-‐proteina
Co-‐immunoprecipitaCon
Bimolecular Fluorescence ComplementaCon (BiFC)
Yeast 2 hybrid screen
Tandem Affinity PurificaCon(TAP)
Pull down
Esercitazione

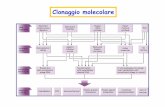
Una premessa necessaria: il clonaggio
Clonare significa produrre copie idenBche: CLONI.
Il CLONAGGIO consiste nella molBplicazione di un segmento di DNA
appartenente ad un dato genoma.
Ciò si oXene unendo tale frammento a una piccola molecola di DNA che serve da
trasportatore
(VETTORE DI CLONAGGIO).
Successivamente si avrà la replicazione di questo DNA modificato (RICOMBINANTE)
migliaia o milioni di volte fornendo un gran numero di copie del clone stesso.
Il risultato è l’amplificazione sele5va di quel determinato frammento di
DNA.

Il clonaggio uBlizza diversi strumenB: • Uno strumento (enzimi) per tagliare il DNA in punB precisi: le
ENDONUCLEASI DI RESTRIZIONE
• Uno strumento (enzima) per unire covalentemente due frammenB di DNA:
DNA LIGASI
• Una piccola molecola di DNA capace di autoreplicarsi:
PLASMIDE.
• Il frammento di DNA che si vuole replicare
• Una CELLULA OSPITE che fornisce l’apparato enzimaBco
necessario per la replicazione del DNA ricombinante.
• Un metodo per la SELEZIONE delle cellule ospiB che contengano il DNA
ricombinante.

TAPPE CARATTERISTICHE DI UN CLONAGGIO
• 1-‐ DIGESTIONE (Taglio del DNA da clonare e del plasmide)
• 2-‐ LIGAZIONE (Unione del DNA da clonare e del plasmide)
• 3-‐ TRASFORMAZIONE (inserimento clone in cellula ospite)
• 4-‐ PIASTRAMENTO (replicazione dei cloni in terreno nutriBvo)
• 5-‐ SELEZIONE ( riconoscimento dei ricombinanB).

I plasmidi • I plasmidi sono degli elemenB geneBci extracromosomali che si replicano
autonomamente in baEeri grazie ad una origine di replicazione.
• Nella maggior parte dei casi sono molecole di DNA circolari libere.
• In biologia molecolare, si uBlizzano plasmidi ingegnerizzaB, che contengono
un marcatore selezionabile (resistenza ad un anBbioBco)
• Diversi siB unici di taglio per enzimi di restrizione, di solito vicini e raggruppaB
in un MulAple Cloning Site

COME E’ POSSIBILE CLONARE UN FRAMMENTO DI DNA ?

Perché copiare (clonare) un frammento di DNA
• Un parBcolare gene può essere isolato e la sua sequenza nucleoBdica può essere determinata
• Le sequenze di controllo del dna possono essere idenBficate e analizzate
• Organismi possono essere “ingegnerizzaB”per scopi specifici, es.produzione di insulina, resistenza agli inseX, etc.
• La funzione di proteine/enzimi/rna può essere valutata

Yeast 2 Hybrid (Y2H) screen
• Inventato da Fields and Song (1989) l’ Y2H cosBtuisce a tuE’ oggi il metodo di screening più rapido, semplice ed uBlizzato per l’ idenBficazione di interazioni proteina-‐proteina; si basa sulla modularità del faEore di trascrizione Gal4
• Osservazioni degli anni '80 portarono a concludere che i faEori di trascrizione sono proteine modulari (composte di più domini separaB) e sono quindi scomponibili;
• Il faEore GAL4 di lievito può essere diviso in due componenB: un dominio di legame al DNA (BD: binding domain) e l'altro di aXvazione della trascrizione (AD: acBvaBon domain);
• I due domini, anche divisi dal resto della proteina saranno capaci l’ uno di legame al DNA (BD)e l’ altro (AD) di aXvazione della trascrizione (posto che venga portato in vicinanza del DNA, ad esempio tramite fusione con un altro dominio che lega il DNA). DNA Binding Domain
(BD) TranscripBon AcBvaBon
Domain (AD)

Principi del Y2H
• Immaginiamo di avere due proteine, X e Y che normalmente formano un complesso;
• Se costruiamo a) una proteina di fusione Gal4(BD)-‐ X e b) una proteina di fusione Y -‐Gal4(AD), possiamo ricosBtuire un aXvatore della trascrizione Gal4 funzionale (cioè la regione di aXvazione di Gal4 si complessa con la regione di legame al DNA)
• Ques to comp le s so ag i s ce da aXvatore della trascrizione per gli enzimi metabolici del galaEosio
L’ interazione X-‐Y riprisBna l’ unità funzionale del faEore di trascrizione GAL4;

Questo principio è stato abbinato all’ uBlizzo di geni reporter facilmente screenabili soEo il controllo di una sequenza di regolazione (UAS) riconosciuta dal BD. Screening visibile e quanBtaBvo delle interazioni.
Proteina X
Proteina Y
Selezione nutrizionale
Selezione “visiva” Sceening Bianco/Blu;
Il ceppo di lievito uBlizzato per il doppio ibrido (AH109) non è capace di crescere su mezzi privi di Leu, Trp,His, Ade.

Costruzione dell’ esca e della/delle prede:
a. Clonaggio in E.coli della nostra proteina esca in veEori «bait»: la proteina esca verrà espressa in fusione con il BD.
Gal4 DNA
Binding Domain
Proteina di fusione X-‐BD
La presenza del plasmide conferisce capacità al lievito di crescere in assenza di Triptofano

b1. Clonaggio in E.coli della nostra proteina preda in veEori «prey»: la proteina preda verrà espressa in fusione con l’ AD. Nel caso il cui abbiamo già un candidato all’ interazione con l’esca.
b2. Costruzione di una AD fusion library: Preparazione di una libreria cDNA in un veEore contenente l’ AD. Bisogna costruire una libreria rappresentaBva e con inserB a lunghezza variabile tanto meglio se oEenuta da mRNA di tessuB in cui la proteina bait viene espressa abbondantemente.
Gal4 AcBvaBon
Domain
Proteina di fusione Y-‐AD
La presenza del plasmide conferisce capacità al lievito di crescere in assenza di Leucina

UBlizzo di AD libraries già disponibili

Trasformazione di lievito
Cotrasformazione: i due costruX vengono trasformaB assieme, preferibile per evitare fenomeni di tossicità in lievito di uno dei 2 costruX. Piastriamo in assenza di Triptofano e di Leucina
Dopo la trasformazione, le cellule vengono piastrate su mezzo seleXvo –TRP, -‐LEU, -‐HIS, -‐ADE, (Selezione nutrizionale della interazione) + X-‐a-‐GAL (Selezione visiva dell’ interazione: blue/white)
-‐His/-‐Ade
Solo le cellule trasformate con entrambi i veEori saranno in grado di crescere
Verifica dell’ interazione
Il saggio del doppio ibrido di lievito sarà oggeEo delle esercitazioni del 01/04 (trasformazione) e 04/04/14 (test per selezione nutrizionale)

Controlli possibili:
Si riclona la sequenza del prey
Switch di bait con prey
Uso di tecniche alternaBve (pull-‐down, co-‐IP) per la conferma
Verifica delle interazioni

Un esempio
TuEe le 6000 ORFs di lievito sono state saggiate per l’interazione due a due: Questo ha permesso di individuare 957 interazioni proteina-‐proteina

Svantaggi del Y2H
Il bait potrebbe avere BD propri: delezione
Alcune proteine potrebbero non essere stabili in lievito
La presenza di AD e BD potrebbe “mascherare” i domini di interazione
Possibilità di folding non correEo o assenza di modificazioni post-‐trascrizionali

Pull down E’ uno dei metodi più facili per un rapido screening di proteine interagenB con la proteina di interesse (deEa “esca”, bait). Può essere uBlizzato anche per la conferma di una interazione già ipoBzzata.
Gli steps:
Espressione e purificazione della proteina esca in baEeri (aggiunta di una TAG) o purificazione da un lisato cellulare;
Legame del bait a una resina
Aggiunta del lisato cellulare
Eluizione del bait (con eventuali proteine associate) dalla resina
Corsa su SDS-‐PAGE; Rilevazione o sequenziamento

AnBcorpo contro la proteina bait
immobilizzato alla resina
Bait riconosciuto dall’ anBcorpo
Proteine interagenB con il
bait
Eluizione
Corsa su SDS PAGE e digesBone
con tripsina
SpeErometria di massa
Validazione con western bloXng
Co-‐Immuno Purificazione
1.
2.
3.
4.
5.
6.
Simile al pull-‐down. Differenza: la proteina esca non è cosBtuita da una proteina ricombinante purificata da E.coli, ma è co-‐purificata da pianta insieme alle prede

BiFC (Bi-‐molecular Fluorescence ComplementaCon): Saggio di complementazione della fluorescenza
Espressione transiente in protoplasB o piante di tabacco: Co-‐trasformazione di esca e preda.
Costruzione dei veEori: Clonaggio delle proteine A e B in veEori contenenB i frammenB della YFP
Visualizzazione al microscopio confocale: la YFP si è ricosBtuita????
Gli steps:
The BiFC assay is based on reconsBtuBon of an intact fluorescent protein when two complementary non-‐fluorescent fragments are brought together by a pair of interacBng proteins.
514 nm
8 possibili combinazioni!

Vantaggi: • E’ un metodo veloce per verificare l’interazione tra due proteine; • E’ un metodo “in vivo”; • Localizza anche il comparBmento intracellulare in cui avviene l’interazione.
Svantaggi: • Il rumore di fondo e’ alto; Possibilita’ di falsi posiBvi. • Viceversa, non sempre interazioni note possono essere confermate. L’orientamento dei frammenB della YFP potrebbe essere importante: bisogna testare molte combinazioni diverse

Tandem Affinity PurificaCon
Sviluppata per la prima volta da Rigaut et al. (1999) per la purificazione di complessi proteici da lievito
La TAP prevede l’ uso di 2 Tags invece di una (x es. pull-‐down): maggiore seleXvità
La TAP è stata uBlizzata con successo in lievito, sistemi animali, baEerici, piante e cellule di inseEo.

Gli step:
1. Clonaggio del gene di interesse in veEore contenente due Tag in tandem
2. Trasformazione stabile di piante
3. Doppia immuno-‐purificazione
4. Separazione delle proteine purificate mediante SDS-‐PAGE e sequenziamento mediante LC/MS-‐MS.

4. Separazione delle proteine purificate mediante SDS-‐PAGE e sequenziamento mediante LC/MS-‐MS.
Dopo il sequenziamento, si fa una ricerca in banca daB (MASCOT) alla ricerca delle proteine idenBficate


Svantaggi della TAP:
• Costa un sacco di soldi!!! Proteasi, anBcorpi, sequenziamento….
• Ci vuole parecchio tempo
• Difficile idenBficare interazioni deboli.
• Complementare all’ Y2H