Cellula deve mantenere omeostasi Relazione struttura – attività biologica di proteine ed enzimi...
-
Upload
benedetto-paoli -
Category
Documents
-
view
216 -
download
0
Transcript of Cellula deve mantenere omeostasi Relazione struttura – attività biologica di proteine ed enzimi...

Cellula deve mantenere
omeostasi
Relazione
struttura – attività biologica di proteine ed enzimi
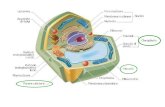
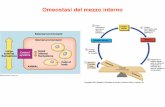
Cellula: ambiente separato
dall’ambiente esterno ma
in comunicazione con esso

H He
Li Be B C N O F Ne
Na Mg Al Si P S Cl Ar
K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr
Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe
Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn
Elementi essenziali
La loro assenza non consente una normale attività cellulare

morte morte
Effetti tossici
Sintomi da deficienza
Stato di “salute”
Concentrazione dell’elemento essenziale
Risposta fisiologica
negativa
positiva
La concentrazione di un elemento essenziale è un parametro importante

Elemento deficitario Tipici sintomi da deficit
Ca Ritardo crescita scheletrica
Mg Crampi muscolari
Fe Anemia
F Carie dentale
I Disfunzioni della tiroide
Mn Infertilità
Zn Ritardo maturazione sessuale
Tabella 1

Funzioni biologiche svolte dagli elementi inorganici.
funzione strutturale (es. Ca2+ e Mg2+ per il polianione DNA)
portatori di carica per il trasferimento veloce di informazioni (es. Na+, K+, per gli impulsi elettrici nei nervi, Ca2+ per la contrazione muscolare)
formazione, metabolismo e degradazione di composti organici. Queste funzioni richiedono catalisi acido/base secondo Lewis (es. Zn2+)
processi di trasferimento elettronico. Questa funzione richiede elementi con attività redox (es. FeII/FeIII/FeIV, CuI/CuII, CoI/CoII)

La reazione tra uno ione metallico e una o più molecole di legante dà un complesso.complesso.
[Co(NH[Co(NH33))66]]3+ 3+ ione Co3+ è circondato da 6 molecole di NH3
La reazione di formazione di un complesso è una reazione tra un acido di Lewis (lo ione metallico centrale) e una base di Lewis (il legante). L’atomo del legante che forma il legame con lo ione metallico si chiama atomo donatore, mentre lo ione metallico è l’atomo accettore
I complessi possono essere carichi o neutri:
Es. [Cu(NH3)4]2+, Ni(CO)4, [Fe(CN)6]3-
i leganti si distinguono in monodentati e polidentati
Il numero di coordinazionenumero di coordinazione dello ione è il numero di atomi del/dei leganti che si coordinano al centro metallico. Esso non sempre coincide al numero di molecole di legante in un complesso. Es. [Cu(NH3)4]2+, Ca(EDTA)2-. Dipende dalle dimensioni dello ione metallico, dall’ingombro dei leganti e dalle interazioni elettroniche tra i due.

formula Nome come legante
formula Nome come legante
formula Nome come legante
Molecole neutre
Anioni Anioni
H2O aquo F- Fluoro SO42- Solfato
NH3 ammino Cl- Cloro NO2- Nitro (atomo
N lega)
CO carbonile Br- Bromo ONO- Nitrito (atomo O lega)
NO nitrosile I- Iodo SCN- Tiocianato (atomo S lega)
C5H5N piridina O2- Osso NCS- Isotiocianato (atomo N lega)
OH- Idrossi
CN- ciano
Tabella 2: leganti monodentati

leganti multidentati
H2N NH2
NNH
N HN
N N

Numero di coordinazione 4:
Geometria tetraedrica: favorita se atomo centrale è piccolo o se i leganti sono grandi
Geometria piano quadrata: si osserva per i metalli con configurazione d8 (es cis platino)
Numero di coordinazione 5:
Poco comune, piramide a base quadrata (eme + istidina) o bipiramide a base triangolare
Numero di coordinazione 6:
Geometria ottaedrica: molto diffusa, spesso è il punto di partenza per geometrie di simmetria inferiore


Nei complessi ci sono vari tipi di isomerie
[PtCl2(NH3)2]
Esistono due isomeri di tipo geometrico
NH3 Cl
ciscis transtrans

Teoria del campo cristallinoTeoria del campo cristallino
Descrive i composti di coordinazione, ne spiega le proprietà spettroscopiche (es. il colore) e quelle magnetiche
La teoria prevede che l’interazione tra metallo e leganti sia puramente elettrostatica
Metallo è costituito da un nucleo carico positivamente circondato da elettroni degli orbitali d
Leganti che circondano lo ione metallico sono visti come cariche negative puntiformi
Quando i leganti si avvicinano allo ione metallico interagiscono con gli elettroni d del metallo

lungo gli assi cartesianifra gli assi cartesiani a 45°


Ione metallico libero
dxy dxz dyz
dx2-y2 dz2
eg
t2g
o
dxy dxz dyz dx2-y2 dz2
Ione metallico in un campo cristallino sferico Ione metallico in un
campo cristallino ottaedrico
energia
Il baricentro resta inalterato

dx2-y2 dz2
eg
t2g
o
energia
dx2-y2 dz2
eg
t2g
o
O dipende dalla forza del legante:
Legante a campo debole
Legante a campo forte
I- < Br- < SCN- < Cl- < F- < OH- < H2O < NH3 < en < phen< CN-< CO
Forza del legante
dxy dxz dyz
dxy dxz dyz

Il valore di o dipende anche dall’identità dello ione metallico
Mn2+< Ni2+< Co2+< Fe2+< V2+< Fe3+< Co3+< Mo3+< Rh3+< Ru3+< Pd4+< Ir3+
o :
aumenta con lo stato di ossidazione del metallo (es. Fe e Co). Fe3+ è più piccolo e le distanze metallo-legante sono minori e quindi le interazioni sono più forti
aumenta scendendo lungo un gruppo (es Co, Rh, Ir). A parità di carica, le dimensioni dei 4d e dei 5 d sono maggiori di quelle dei 3d e quindi anche le interazioni con i leganti sono maggiori.

Basso spin
Alto spin
d1 d2 d3 d4 d5 d6 d7 d8 d9 d10
Ti3+ Ti2+ V2+ Cr2+ Fe3+ Fe2+ Co2+ Ni2+ Cu2+ Zn2+
Configurazioni elettroniche di un complesso allo stato fondamentale non è più così ovvia

[Cr(H2O)6]2+
O< P
[Cr(CN)6]4-
O > P
Configurazione d4
S = 2 S = 1

Ione Fe2+: configurazione d6
o elevato
Basso spin
S=0
o basso
Alto spin
S=2

energia
dx2-y2 dz2
eg
t2g
o
dx2-y2 dz2
eg
t2g
dxy dxz dyz
dxy dxz dyz
o= E = hhc/
Uno ione metallico di transizione non complessato ha orbitali d degeneri.
In un complesso gli orbitali d sono separati in energia e sono possibili transizioni d-d a seguito dell’assorbimento di energia pari a o.
Le energie richieste cadono nella regione
del visibile e i complessi dei metalli di
transizione sono colorati.

Complessi a geometria tetraedrica

Poiché i leganti sono solo 4 e nessuno di loro punta direttamente sugli orbitali d
T < O
I complessi tetraedrici sono ad alto spin

Geometria piano quadrata
Lo splitting degli orbitali d vede il dx2-y2 più in alto in energia rispetto agli altri. Ciò favorisce complessi di metalli d8 a basso spin o di metalli di 4a o 5a serie di transizione (es. cis-platino)

LEGANTI DI INTERESSE BIOLOGICO
peptidi e/o proteine attraverso residui aminoacidici
leganti chelanti macrociclici
basi azotate degli acidi nucleici

CH2 OHN
NCH2
histidine
CH2CH2SCH3methionine
CH2SHcysteine
Aminoacid R
tyrosine
CH2COO-aspartate
CH2CH2COO-glutamate
Aminoacid R
H
1) residui aminoacidici di proteine

I complessi di coordinazione tra ioni metallici e residui aminoacidici presenti nei sistemi biologici possono presentare coordinazione completa o incompleta attorno allo ione metallico in relazione all’attività biologica (es. se il substrato si deve legare al metallo, se deve avvenire solo un trasferimento elettronico…ecc.)
Con ioni tipo Fe2+ le proteine formano complessi stabili termodinamicamente ma labili dal punto di vista cinetico
La stabilità cinetica è garantita da un’altra classe di leganti

2a) leganti macrociclici tetradentati
Eme, clorofilla, cobalamine
NN
N NH
H
porphyrin chlorin (2,3 dihydroporphyrin)
NN
N NH
H
NN
NHN
corrin
NN
N NM
metalloporphyrin complex
sp3
Manca un ponte metinico
Tutti C sp2
Orbitale p non ibrido
per coniugazion
e doppi legami
planare

PRINCIPALI PROPRIETA’ DEI LEGANTI TETRAPIRROLICIPRINCIPALI PROPRIETA’ DEI LEGANTI TETRAPIRROLICI
anello planare, nessuno stress geometrico (lunghezze ed angoli di legame)
assicurano stabilità cinetica al complesso chelato
data la rigidità dell’anello sono selettivi sulle dimensioni dello ione e accolgono ioni metallici di raggio 60-70 pm. Fe2+ basso spin ha raggio di 61 pm, Fe2+ alto spin ha raggio di 78 pm.
il sistema coniugato è responsabile del colore intenso di questi leganti e dei relativi complessi. Sono i pigmenti della vita.
il metallo tetracoordinato può fare altri due legami sfruttando le posizioni assiali (es. eme dell’emoglobina)
M
N N
NN
X
Y

2b) Ionofori, leganti macrociclici multidentati
good for coordination of Na+, K+, Mg2+, Ca2+
Multiple heteroatoms are strategically positioned for bonding metal ions
ring size is tailored to fit metal ionic radius
Dissociation is possible but very unlikely
Inner cavity is polar, outside is lipophile. So these complexes can be transported through biological membranes.
Complessi macrociclici
tridimensionali

Etere corona che coordina uno ione K+

EFFETTO CHELATOEFFETTO CHELATO
[Co(NH3)6]3+ + 3en [Co(en)3]3+ + 6 NH3
K = [[Co(en)3]3+] [NH3]6
[[Co(NH3)6]3+] [en]3
G° = - RT lnK
G° = H° -TS°
La sostituzione di leganti monodentati da parte di leganti chelanti è accompagnata da un forte guadagno di stabilità termodinamica

[Cd(H2O)6]2+ + en [Cd(en)(H2O)4]2+ + 2 H2O
H° = -29.4 kJmol-1 S° = +13.0 JK-1mol-1
G favorevole Kf elevata
[Cd(H2O)6]2+ + 2NH3 [Cd(NH3)2(H2O)4]2+ + 2 H2O
H° = -29.8 kJmol-1 S° = -5.2 JK-1mol-1
G meno favorevole, Kf più bassa
G° = - RT lnK G° = H° -TS°
Reazione con legante chelante
Reazione con legante NON chelante
Il vantaggio entropico è tanto maggiore quanto maggiori sono le proprietà chelanti del legante

3) Basi azotate
imine
amino amido
oxohydroxo
N
N
NH2
N
NR
adenine
RN
NN
N
H
O
H2N
guanine
N
N
NH2
R
O
cytosine
O
R
N
N
H
O
R'
R' = CH3 thymine
R' = H uracil
N
N
R
O
NH
HN
N
R
NH
H
N
N
NH2
R
O O
R = ribose or deoxyribose
Coordinano ioni metallici utili a neutralizzare la carica negativa del DNA. Offrono diversi siti per la coordinazione.

Metalli (acidi Lewis) Leganti (basi Lewis)
Hard
H+ Mn2+ Cr3+ Ca2+
Na+ Al3+ Co3+
K+ Fe3+ Mg2+
Hard
H2O CO32- NH3 OH-
NO3- RNH2 CH3CO2
-
ROH PO43- RO- Cl-
Borderline
Fe2+ Ni2+ Zn2+
Co2+ Cu2+
Borderline
NO2- SO3
2- Br-
Imidazole
Soft
Cu+ Pt2+ Pt4+ Au+
Hg2+ Cd2+ Pb2+
Soft
R2S RS- R3P RSH
RNC CN- SCN- CO
CONCETTO HARD-SOFTCONCETTO HARD-SOFT
Es. criptati e ferro-porfirine

“un metallo hard lega facilmente ed in modo stabile un legante hard un metallo soft legafacilmente ed in modo stabile un legante soft”

Metallotioneine
Basano la loro attività biologica esclusivamente sul concetto hard-soft
30-35% of aminoacid are cysteins with soft –SH groups
repetitive distribution of Cys-X-Cys etc…
coordination of soft heavy metal ions such as Cd2+, Hg2+, Pb2+, Zn2+.
biological function of metallothioneins is to protect cells from toxic heavy metals